eeb15dbf55caf0f4e3960d6a1b2bb2c5.ppt
- Количество слайдов: 70
 Основы молекулярной физики Конспект лекции Елисеев В. А.
Основы молекулярной физики Конспект лекции Елисеев В. А.
 Содержание: 1. Основные понятия молекулярной физики. 2. Статистический и термодинамический методы исследования. 3. Основные положения молекулярно-кинетической теории. 4. Молекулярно-кинетическая теория идеального газа. 5. Основное уравнение молекулярно-кинетической теории идеального газа. 6. Уравнение Клапейрона - Менделеева. 7. Изопроцессы в газах – изотермический , изобарический, изохорный. 8. Барометрическая формула. 9. Распределение Больцмана. 10. Распределение Максвелла молекул по скоростям. 11. Явления переноса: диффузия, теплопроводность и вязкость. 12. Адиабатический процесс. 13. Работа газа в изопроцессах. 14. Теплоемкости газа. 15. Первое начало термодинамики. 16. Цикл Карно. 17. Энтропия. 18. Второе начало термодинамики. 19. Циклические процессы. Тепловые двигатели. 20. Реальные газы. Уравнение Ван-дер-Ваальса 21. Самостоятельное изучение. Свойства разреженных газов. Эффект Кнудсена.
Содержание: 1. Основные понятия молекулярной физики. 2. Статистический и термодинамический методы исследования. 3. Основные положения молекулярно-кинетической теории. 4. Молекулярно-кинетическая теория идеального газа. 5. Основное уравнение молекулярно-кинетической теории идеального газа. 6. Уравнение Клапейрона - Менделеева. 7. Изопроцессы в газах – изотермический , изобарический, изохорный. 8. Барометрическая формула. 9. Распределение Больцмана. 10. Распределение Максвелла молекул по скоростям. 11. Явления переноса: диффузия, теплопроводность и вязкость. 12. Адиабатический процесс. 13. Работа газа в изопроцессах. 14. Теплоемкости газа. 15. Первое начало термодинамики. 16. Цикл Карно. 17. Энтропия. 18. Второе начало термодинамики. 19. Циклические процессы. Тепловые двигатели. 20. Реальные газы. Уравнение Ван-дер-Ваальса 21. Самостоятельное изучение. Свойства разреженных газов. Эффект Кнудсена.
 Теплота и энергия Для той физической величины, которую мы теперь называем энергией, долгое время употреблялся термин «живая сила» , введенный И. Ньютоном (1643– 1727). Но поскольку «живую силу» можно было спутать с обычной силой, последнюю приходилось для ясности называть «мертвой силой» , что нельзя признать удачным. Специальный термин «энергия» был введен в 1807 Т. Юнгом (1773– 1829). Одним из видов энергии является работа, которая совершается, когда тело движется, преодолевая действие некой силы. Примером может служить подача насосом воды в водонапорную башню. О воде в башне говорят, что она имеет потенциальную энергию. Благодаря гравитационному притяжению Земли существует возможность обратного преобразования этой энергии в кинетическую, т. е. в энергию движения воды, текущей по трубам. Когда вода в трубе в конце концов останавливается из-за внутреннего трения, или вязкости, эта энергия оказывается превратившейся в теплоту, т. е. тепловую энергию, которая рассеивается в окружающей среде. Еще в 1620 Ф. Бэкон высказал предположение, что теплота есть просто другая форма движения, но лишь в 1789 это с несомненностью установил Б. Томпсон (Румфорд), наблюдая за выделением теплоты при рассверливании ствола пушки. Дополнительным подтверждением явились опыты Х. Дэви 1799. Эти опыты и наблюдения говорили о том, что тепловая и механическая энергия – одно и то же и что, вероятно, можно найти экспериментально механический эквивалент теплоты, т. е. количество работы в механических единицах, эквивалентное данному количеству теплоты в тепловых единицах.
Теплота и энергия Для той физической величины, которую мы теперь называем энергией, долгое время употреблялся термин «живая сила» , введенный И. Ньютоном (1643– 1727). Но поскольку «живую силу» можно было спутать с обычной силой, последнюю приходилось для ясности называть «мертвой силой» , что нельзя признать удачным. Специальный термин «энергия» был введен в 1807 Т. Юнгом (1773– 1829). Одним из видов энергии является работа, которая совершается, когда тело движется, преодолевая действие некой силы. Примером может служить подача насосом воды в водонапорную башню. О воде в башне говорят, что она имеет потенциальную энергию. Благодаря гравитационному притяжению Земли существует возможность обратного преобразования этой энергии в кинетическую, т. е. в энергию движения воды, текущей по трубам. Когда вода в трубе в конце концов останавливается из-за внутреннего трения, или вязкости, эта энергия оказывается превратившейся в теплоту, т. е. тепловую энергию, которая рассеивается в окружающей среде. Еще в 1620 Ф. Бэкон высказал предположение, что теплота есть просто другая форма движения, но лишь в 1789 это с несомненностью установил Б. Томпсон (Румфорд), наблюдая за выделением теплоты при рассверливании ствола пушки. Дополнительным подтверждением явились опыты Х. Дэви 1799. Эти опыты и наблюдения говорили о том, что тепловая и механическая энергия – одно и то же и что, вероятно, можно найти экспериментально механический эквивалент теплоты, т. е. количество работы в механических единицах, эквивалентное данному количеству теплоты в тепловых единицах.
 Основные понятия молекулярной физики Молекула - наименьшая устойчивая частица вещества, обладающая его основными химическими и физическими свойствами. Состоит молекула из атомов, связанных друг с другом за счет валентных электронов. Размеры молекул зависят от числа атомов в молекуле, которое составляет от двух (H 2 , O 2) до сотен и тысяч (молекулы белков). Моль - единица количества вещества в системе СИ. В одном моле вещества содержатся такое число атомов или молекул, которое равно числу атомов в 12 граммах изотопа углерода С 12. Число Авогадро – NA - число частиц, содержащихся в одном моле. NA = 6, 022∙ 1023 моль-1. Относительная атомная масса, или атомная масса химического элемента - это отношение массы атома этого элемента к 1/12 массы атома С 12. Относительные атомные массы химических элементов приводятся в таблице Менделеева. Относительная молекулярная масса вещества - это отношение массы молекулы этого вещества к 1/12 массы атома углерода С 12. Зная химическую формулу вещества можно найти молекулярную массу как сумму атомных масс элементов, составляющих данное вещество. Например, молекулярная масса воды равна 18. Это безразмерное число. Молярная масса - μ - это масса одного моля вещества, выраженная в кг/моль (система СИ). Из определения моля следует, что молярная масса, выраженная в граммах, численно равна относительной молекулярной массе. Так масса одного моля воды равна 18 г. Атомная единица массы (а. е. м. ) - это 1/12 массы атома углерода С 12. 1 а. е. м. =1, 6605655· 10 -27 кг.
Основные понятия молекулярной физики Молекула - наименьшая устойчивая частица вещества, обладающая его основными химическими и физическими свойствами. Состоит молекула из атомов, связанных друг с другом за счет валентных электронов. Размеры молекул зависят от числа атомов в молекуле, которое составляет от двух (H 2 , O 2) до сотен и тысяч (молекулы белков). Моль - единица количества вещества в системе СИ. В одном моле вещества содержатся такое число атомов или молекул, которое равно числу атомов в 12 граммах изотопа углерода С 12. Число Авогадро – NA - число частиц, содержащихся в одном моле. NA = 6, 022∙ 1023 моль-1. Относительная атомная масса, или атомная масса химического элемента - это отношение массы атома этого элемента к 1/12 массы атома С 12. Относительные атомные массы химических элементов приводятся в таблице Менделеева. Относительная молекулярная масса вещества - это отношение массы молекулы этого вещества к 1/12 массы атома углерода С 12. Зная химическую формулу вещества можно найти молекулярную массу как сумму атомных масс элементов, составляющих данное вещество. Например, молекулярная масса воды равна 18. Это безразмерное число. Молярная масса - μ - это масса одного моля вещества, выраженная в кг/моль (система СИ). Из определения моля следует, что молярная масса, выраженная в граммах, численно равна относительной молекулярной массе. Так масса одного моля воды равна 18 г. Атомная единица массы (а. е. м. ) - это 1/12 массы атома углерода С 12. 1 а. е. м. =1, 6605655· 10 -27 кг.
 Методы исследования Число атомов и молекул в любом теле огромно. Например, в 1 м 3 газа при обычных условиях содержится 1025 молекул, а в жидких и твердых телах 1028 молекул. Если считать, что движение каждого атома или молекулы подчиняется законам классической механики, то практически даже невозможно написать систему дифференциальных уравнений движения такого множества молекул и решить эту систему. Поэтому поведение отдельной молекулы или атома тела не может быть изучено методами классической механики, тем более, что характеристики движения молекулы изменяются со временем случайным образом. Физические свойства макроскопических систем, состоящих из большого числа частиц, изучаются двумя взаимно дополняющими методами: статистическим и термодинамическим. Статистический метод основан на использовании теории вероятностей и определенных моделей строения изучаемых систем. В совокупном поведении большого числа частиц, координаты и импульсы которых случайны в любой момент времени, проявляются особые статистические закономерности. При этом молекулярно-кинетическая теория не интересуется движением каждой отдельной молекулы, а только такими средними величинами, которые характеризуют движение огромного числа молекул. Эти средние величины связаны с параметрами, характеризующими состояние макроскопического тела. Например, в газах можно определить средние значения скоростей молекул и их энергий, однозначно связанных с температурой. Раздел физики, в котором с помощью статистического метода изучаются физические свойства макроскопических систем, называется статистической физикой. В термодинамическом методе исследования поведения большого числа молекул не рассматривается внутреннее строения изучаемых тел, а анализируются условия и количественные соотношения при различных превращениях энергии, происходящих в системе. Раздел физики, в котором физические свойства макроскопических систем изучаются с помощью термодинамического метода, называется термодинамикой. Заметим, что статистическая физика и термодинамика при малом числе частиц теряют смысл.
Методы исследования Число атомов и молекул в любом теле огромно. Например, в 1 м 3 газа при обычных условиях содержится 1025 молекул, а в жидких и твердых телах 1028 молекул. Если считать, что движение каждого атома или молекулы подчиняется законам классической механики, то практически даже невозможно написать систему дифференциальных уравнений движения такого множества молекул и решить эту систему. Поэтому поведение отдельной молекулы или атома тела не может быть изучено методами классической механики, тем более, что характеристики движения молекулы изменяются со временем случайным образом. Физические свойства макроскопических систем, состоящих из большого числа частиц, изучаются двумя взаимно дополняющими методами: статистическим и термодинамическим. Статистический метод основан на использовании теории вероятностей и определенных моделей строения изучаемых систем. В совокупном поведении большого числа частиц, координаты и импульсы которых случайны в любой момент времени, проявляются особые статистические закономерности. При этом молекулярно-кинетическая теория не интересуется движением каждой отдельной молекулы, а только такими средними величинами, которые характеризуют движение огромного числа молекул. Эти средние величины связаны с параметрами, характеризующими состояние макроскопического тела. Например, в газах можно определить средние значения скоростей молекул и их энергий, однозначно связанных с температурой. Раздел физики, в котором с помощью статистического метода изучаются физические свойства макроскопических систем, называется статистической физикой. В термодинамическом методе исследования поведения большого числа молекул не рассматривается внутреннее строения изучаемых тел, а анализируются условия и количественные соотношения при различных превращениях энергии, происходящих в системе. Раздел физики, в котором физические свойства макроскопических систем изучаются с помощью термодинамического метода, называется термодинамикой. Заметим, что статистическая физика и термодинамика при малом числе частиц теряют смысл.
 Термодинамический метод Задачей термодинамического метода изучения состояний макроскопических систем является установление связей между непосредственно наблюдаемыми величинами, такими, как давление, объем, температура, концентрация раствора, напряженность электрического или магнитного поля, световой поток и т. д. Никакие величины, связанные с атомно-молекулярной структурой вещества ( размеры атома или молекулы, их масса, количество и т. д. ), не входят в рассмотрение при термодинамическом подходе к решению задач. Термодинамический метод, не связанный с модельными представлениями, обладает большей общностью, отличается простотой и ведет, после ряда простых математических процедур, к решению целого ряда конкретных задач, не требуя никаких сведений о свойствах атомов или молекул. Однако при термодинамическом рассмотрении остается нераскрытым внутренний (атомно-молекулярный) механизм явлений. По этой причине в термодинамике, как правило, бессмысленны вопросы "почему? " Например, почему при быстром растяжении медная проволока охлаждается, а резиновый жгут нагревается? Мы должны удовлетворить этим результатам, а механизм, ведущий к нему, остается скрытым от нас. В основе термодинамики лежат принципы, являющиеся обобщением опытных данных: принцип температуры (часто называемый нулевым началом термодинамики), принцип энергии (I начало), принцип энтропии (II начало) и постулат Нернста (III начало термодинамики).
Термодинамический метод Задачей термодинамического метода изучения состояний макроскопических систем является установление связей между непосредственно наблюдаемыми величинами, такими, как давление, объем, температура, концентрация раствора, напряженность электрического или магнитного поля, световой поток и т. д. Никакие величины, связанные с атомно-молекулярной структурой вещества ( размеры атома или молекулы, их масса, количество и т. д. ), не входят в рассмотрение при термодинамическом подходе к решению задач. Термодинамический метод, не связанный с модельными представлениями, обладает большей общностью, отличается простотой и ведет, после ряда простых математических процедур, к решению целого ряда конкретных задач, не требуя никаких сведений о свойствах атомов или молекул. Однако при термодинамическом рассмотрении остается нераскрытым внутренний (атомно-молекулярный) механизм явлений. По этой причине в термодинамике, как правило, бессмысленны вопросы "почему? " Например, почему при быстром растяжении медная проволока охлаждается, а резиновый жгут нагревается? Мы должны удовлетворить этим результатам, а механизм, ведущий к нему, остается скрытым от нас. В основе термодинамики лежат принципы, являющиеся обобщением опытных данных: принцип температуры (часто называемый нулевым началом термодинамики), принцип энергии (I начало), принцип энтропии (II начало) и постулат Нернста (III начало термодинамики).
 Термодинамические системы Нулевое начало термодинамики Будем называть термодинамической системой любое макроскопическое тело, находящееся в равновесном или близком к равновесному состоянию. Для каждой термодинамической системы существует состояние термодинамического равновесия, которое она при фиксированных внешних условиях достигает. Например, чайник, снятый с плиты, сам остывает до комнатной температуры. Сформулированный признак термодинамических систем настолько важен, что он получил название нулевого начала термодинамики. Это начало имеет такой странный номер потому, что лишь после того как были открыты первое и второе начала термодинамики, ученые осознали, что этот практически очевидный постулат нужно поставить впереди. По существу, нулевое начало термодинамики постулирует существование температуры.
Термодинамические системы Нулевое начало термодинамики Будем называть термодинамической системой любое макроскопическое тело, находящееся в равновесном или близком к равновесному состоянию. Для каждой термодинамической системы существует состояние термодинамического равновесия, которое она при фиксированных внешних условиях достигает. Например, чайник, снятый с плиты, сам остывает до комнатной температуры. Сформулированный признак термодинамических систем настолько важен, что он получил название нулевого начала термодинамики. Это начало имеет такой странный номер потому, что лишь после того как были открыты первое и второе начала термодинамики, ученые осознали, что этот практически очевидный постулат нужно поставить впереди. По существу, нулевое начало термодинамики постулирует существование температуры.
 Равновесные состояния Состояния любой термодинамической системы могут быть заданы с помощью ряда параметров, например, для газа p, V, T , для жидкости - a (коэффициент поверхностного натяжения), s (поверхность пленки), и. т. д. Следует заметить, что не в любом состоянии системы все ее параметры имеют определенный смысл. Например, представим себе сосуд, разделенный на две половины перегородкой с краном, и пусть вначале в левой половине находится газ, а в правой - вакуум. Если мы откроем кран, то из него вырвется струя газа, и в первые моменты этого процесса объем газа будет неопределенным - плотность газа в правой половине сосуда будет меняться от точки к точке по какому-то сложному закону и указать границы объема, в котором находится газ, невозможно. Можно представить и систему, температура которой меняется от точки к точке, или газ, в разных точках которого давление различно. Такие состояния называются неравновесными. Обычно по прошествии некоторого времени устанавливается состояние, в котором каждый такой параметр имеет одно и то же значение во всех точках системы и остается неизменным сколь угодно долго, если не меняются внешние условия. Такие состояния называются равновесными.
Равновесные состояния Состояния любой термодинамической системы могут быть заданы с помощью ряда параметров, например, для газа p, V, T , для жидкости - a (коэффициент поверхностного натяжения), s (поверхность пленки), и. т. д. Следует заметить, что не в любом состоянии системы все ее параметры имеют определенный смысл. Например, представим себе сосуд, разделенный на две половины перегородкой с краном, и пусть вначале в левой половине находится газ, а в правой - вакуум. Если мы откроем кран, то из него вырвется струя газа, и в первые моменты этого процесса объем газа будет неопределенным - плотность газа в правой половине сосуда будет меняться от точки к точке по какому-то сложному закону и указать границы объема, в котором находится газ, невозможно. Можно представить и систему, температура которой меняется от точки к точке, или газ, в разных точках которого давление различно. Такие состояния называются неравновесными. Обычно по прошествии некоторого времени устанавливается состояние, в котором каждый такой параметр имеет одно и то же значение во всех точках системы и остается неизменным сколь угодно долго, если не меняются внешние условия. Такие состояния называются равновесными.
 Равновесные процессы Процесс перехода термодинамической системы из неравновесного состояния в равновесное называется процессом релаксации, он характеризуется временем релаксации. Представим себе процесс, протекающий в термодинамической системе со скоростью, значительно меньшей скорости релаксации; это значит, что на любом этапе этого процесса значения всех параметров будут успевать выравниваться и такой процесс будет представлять собой последовательность бесконечно близких друг к другу равновесных состояний. Такие достаточно медленные процессы принято называть равновесными или квазистатическими. Ясно, что все реальные процессы являются неравновесными и могут лишь в большей или меньшей степени приближаться к равновесным. Заметим, что равновесный процесс может идти как в прямом, так и в противоположном направлениях. В связи с этим равновесные процессы называют также обратимыми. В дальнейшем мы будет рассматривать только равновесные процессы.
Равновесные процессы Процесс перехода термодинамической системы из неравновесного состояния в равновесное называется процессом релаксации, он характеризуется временем релаксации. Представим себе процесс, протекающий в термодинамической системе со скоростью, значительно меньшей скорости релаксации; это значит, что на любом этапе этого процесса значения всех параметров будут успевать выравниваться и такой процесс будет представлять собой последовательность бесконечно близких друг к другу равновесных состояний. Такие достаточно медленные процессы принято называть равновесными или квазистатическими. Ясно, что все реальные процессы являются неравновесными и могут лишь в большей или меньшей степени приближаться к равновесным. Заметим, что равновесный процесс может идти как в прямом, так и в противоположном направлениях. В связи с этим равновесные процессы называют также обратимыми. В дальнейшем мы будет рассматривать только равновесные процессы.
 Идеальный газ - это физическая модель, в которой: 1) пренебрегают собственными размерами молекул; 2) пренебрегают энергией взаимодействия между молекулами; 3) молекулы ведут себя как абсолютно упругие тела в процессе столкновения между собой и со стенками сосуда. Опыт показывает, что при давлениях, близких к атмосферному, и температурах, близких к комнатной, многие газы (азот, кислород, водород, пары воды и т. д. ) можно считать идеальными. Энергией взаимодействия молекул между собой здесь можно пренебречь потому, что в этих условиях лишь небольшая доля молекул находится в каждый момент времени в состоянии соударения. Молекулярно-кинетическая теория позволяет выразить макроскопические параметры термодинамической системы (давление, температуру и т. д. ) через усредненные микроскопические величины. Давлением p, в случае равномерного распределения сил вдоль поверхности, называется величина р = F/S┴ ; [p] = H/м 2 , где F - сумма приложенных перпендикулярно к участку поверхности сил, S┴ - площадь участка поверхности. Прибор для измерения давления называется манометром. За единицу абсолютной температуры T в системе СИ принят Кельвин (К). Температура в градусах Цельсия (t, o. C) связана с T (К) следующим равенством: T = t + 273, 15 K , причем 1 o. C = 1 К. Прибор для измерения температуры называется термометром.
Идеальный газ - это физическая модель, в которой: 1) пренебрегают собственными размерами молекул; 2) пренебрегают энергией взаимодействия между молекулами; 3) молекулы ведут себя как абсолютно упругие тела в процессе столкновения между собой и со стенками сосуда. Опыт показывает, что при давлениях, близких к атмосферному, и температурах, близких к комнатной, многие газы (азот, кислород, водород, пары воды и т. д. ) можно считать идеальными. Энергией взаимодействия молекул между собой здесь можно пренебречь потому, что в этих условиях лишь небольшая доля молекул находится в каждый момент времени в состоянии соударения. Молекулярно-кинетическая теория позволяет выразить макроскопические параметры термодинамической системы (давление, температуру и т. д. ) через усредненные микроскопические величины. Давлением p, в случае равномерного распределения сил вдоль поверхности, называется величина р = F/S┴ ; [p] = H/м 2 , где F - сумма приложенных перпендикулярно к участку поверхности сил, S┴ - площадь участка поверхности. Прибор для измерения давления называется манометром. За единицу абсолютной температуры T в системе СИ принят Кельвин (К). Температура в градусах Цельсия (t, o. C) связана с T (К) следующим равенством: T = t + 273, 15 K , причем 1 o. C = 1 К. Прибор для измерения температуры называется термометром.
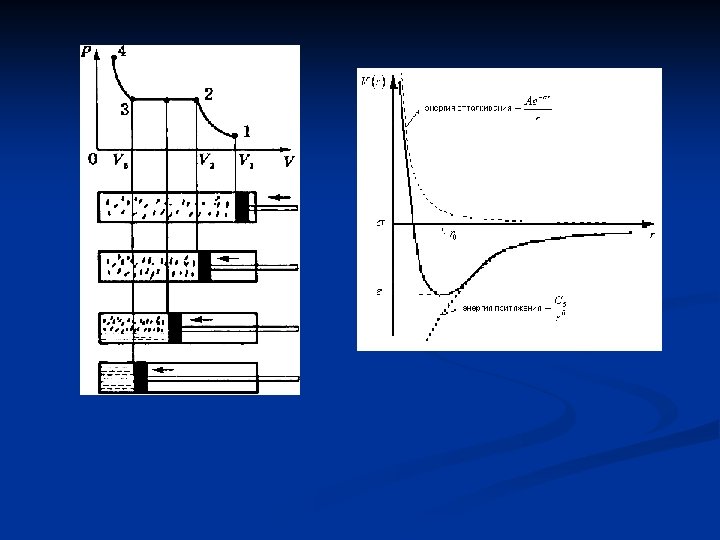
 Основные положения молекулярнокинетической теории 1. Все тела состоят из мельчайших частиц - атомов и молекул. 2. Эти частицы непрерывно и хаотически движутся. 3. Атомы и молекулы взаимодействуют друг с другом - на малых расстояниях отталкиваются, силы отталкивания резко уменьшаются с увеличением расстояния и обращаются на каком-то расстоянии rо в ноль; затем, при дальнейшем увеличении расстояния переходят в силы притяжения. Силы притяжения при увеличении расстояния сначала растут, затем, достигнув максимального значения, убывают до нуля. 4. Средняя кинетическая энергия молекул пропорциональна температуре ½mυ² = 3/2 k. T , где k = 1, 38∙ 10 -23 Дж/K – постоянная Больцмана. Необыкновенную важность основных положений молекулярно-кинетической теории очень образно выразил выдающийся физик современности, лауреат Нобелевской премии Ричард Фейнман: «Если бы в результате какой-то мировой катастрофы все накопленные научные знания оказались бы уничтоженными и к грядущим поколениям живых существ пережила бы только одна фраза, то какое утверждение составленное из наименьшего количества слов, принесло бы наибольшую информацию? Я считаю, что это - атомная гипотеза (можете называть ее не гипотезой, а фактом, но это ничего не меняет: все тела состоят из атомов - маленьких телец, которые находятся в беспрерывном движении, притягиваются на небольшом расстоянии, но отталкиваются, если одно из них прижать плотнее друг к другому. В одной этой фразе содержится невероятное количество информации о мире, стоит лишь приложить к ней немного воображения и чуть соображения» .
Основные положения молекулярнокинетической теории 1. Все тела состоят из мельчайших частиц - атомов и молекул. 2. Эти частицы непрерывно и хаотически движутся. 3. Атомы и молекулы взаимодействуют друг с другом - на малых расстояниях отталкиваются, силы отталкивания резко уменьшаются с увеличением расстояния и обращаются на каком-то расстоянии rо в ноль; затем, при дальнейшем увеличении расстояния переходят в силы притяжения. Силы притяжения при увеличении расстояния сначала растут, затем, достигнув максимального значения, убывают до нуля. 4. Средняя кинетическая энергия молекул пропорциональна температуре ½mυ² = 3/2 k. T , где k = 1, 38∙ 10 -23 Дж/K – постоянная Больцмана. Необыкновенную важность основных положений молекулярно-кинетической теории очень образно выразил выдающийся физик современности, лауреат Нобелевской премии Ричард Фейнман: «Если бы в результате какой-то мировой катастрофы все накопленные научные знания оказались бы уничтоженными и к грядущим поколениям живых существ пережила бы только одна фраза, то какое утверждение составленное из наименьшего количества слов, принесло бы наибольшую информацию? Я считаю, что это - атомная гипотеза (можете называть ее не гипотезой, а фактом, но это ничего не меняет: все тела состоят из атомов - маленьких телец, которые находятся в беспрерывном движении, притягиваются на небольшом расстоянии, но отталкиваются, если одно из них прижать плотнее друг к другому. В одной этой фразе содержится невероятное количество информации о мире, стоит лишь приложить к ней немного воображения и чуть соображения» .
 Основное уравнение молекулярно-кинетической теории идеального газа Пусть число молекул в единице объема сосуда (концентрация молекул) равно n = N/V. Ударяясь о стенку куба, каждая молекула действует на нее с некоторой силой, которая определяется по второму закону Ньютона изменением импульса молекулы F = Δp/Δt. Молекулы внутри сосуда могут двигаться в одном из 6 возможных направлений. Учитывая равноправность этих направлений, будем считать, что параллельно оси Y со скоростью υ к стенке площадью S движется 1/6 часть всех молекул. Предполагая, что происходит абсолютно упругий удар, имеем : |υ1| = |υ2| = υ. За время Δt о стенку площадью S ударятся все те молекулы, которые находились от нее на расстоянии не больше, чем υΔt . Если концентрация молекул равна n , то в этом объеме находится N = n∙V = n. SυΔt молекул, у каждой из которых изменение импульса равно mυ2 –(– mυ1) = 2 mυ. Сила давления, оказываемого на стенку сосуда этими молекулами равна : F = 1/6∙n∙V∙Δp/Δt = 1/6∙n∙S∙υ∙Δt∙ 2 mυ/Δt =1/6∙n∙S∙ 2 mυ2 = ⅓∙n∙S∙mυ2. Давление, определяемое отношением силы к площади, на которую она действует, равно: p = ⅓∙n∙mυ2 = ⅔∙n∙½∙mυ2 или p = ⅔∙n∙<Ек> , где <Ек> = ½∙mυ2 – средняя кинетическая энергия поступательного движения молекул газа. Давление газа на стенки сосуда определяется произведением концентрации молекул n и средней кинетической энергии поступательного движения молекул <Ек>. Определим давление газа на из уравнения Клапейрона – Менделеева для одного моля газа р. V = RT и, учитывая, что R = NA∙k , получаем p = NA/V∙k. T = nk. T = ⅔∙n∙ 3/2∙k. T. Сравнивая предыдущее выражение для давления газа p = ⅔∙n∙½∙mυ² , получаем ½mυ² = 3/2∙k. T : термодинамическая температура T с точностью до постоянного множителя (3/2∙k) равна средней кинетической энергии
Основное уравнение молекулярно-кинетической теории идеального газа Пусть число молекул в единице объема сосуда (концентрация молекул) равно n = N/V. Ударяясь о стенку куба, каждая молекула действует на нее с некоторой силой, которая определяется по второму закону Ньютона изменением импульса молекулы F = Δp/Δt. Молекулы внутри сосуда могут двигаться в одном из 6 возможных направлений. Учитывая равноправность этих направлений, будем считать, что параллельно оси Y со скоростью υ к стенке площадью S движется 1/6 часть всех молекул. Предполагая, что происходит абсолютно упругий удар, имеем : |υ1| = |υ2| = υ. За время Δt о стенку площадью S ударятся все те молекулы, которые находились от нее на расстоянии не больше, чем υΔt . Если концентрация молекул равна n , то в этом объеме находится N = n∙V = n. SυΔt молекул, у каждой из которых изменение импульса равно mυ2 –(– mυ1) = 2 mυ. Сила давления, оказываемого на стенку сосуда этими молекулами равна : F = 1/6∙n∙V∙Δp/Δt = 1/6∙n∙S∙υ∙Δt∙ 2 mυ/Δt =1/6∙n∙S∙ 2 mυ2 = ⅓∙n∙S∙mυ2. Давление, определяемое отношением силы к площади, на которую она действует, равно: p = ⅓∙n∙mυ2 = ⅔∙n∙½∙mυ2 или p = ⅔∙n∙<Ек> , где <Ек> = ½∙mυ2 – средняя кинетическая энергия поступательного движения молекул газа. Давление газа на стенки сосуда определяется произведением концентрации молекул n и средней кинетической энергии поступательного движения молекул <Ек>. Определим давление газа на из уравнения Клапейрона – Менделеева для одного моля газа р. V = RT и, учитывая, что R = NA∙k , получаем p = NA/V∙k. T = nk. T = ⅔∙n∙ 3/2∙k. T. Сравнивая предыдущее выражение для давления газа p = ⅔∙n∙½∙mυ² , получаем ½mυ² = 3/2∙k. T : термодинамическая температура T с точностью до постоянного множителя (3/2∙k) равна средней кинетической энергии
 Уравнение состояния идеального газа Учитывая, что концентрация молекул в объеме V равна n = N/V основное уравнение молекулярно-кинетической теории p = nk. T можно записать в следующем виде: p = N/V∙k. T = М/μV∙NAk. T или p. V = М/μ∙RT, где N = NA∙М/μ – общее число молекул в массе М газа, а М/μ - число молей газа , R = NA·k – универсальная газовая постоянная Значение универсальной газовой постоянной равно : R = NA·k = 6, 022· 1023 моль-1· 1, 38· 10 -23 Дж/К = 8, 31 Дж/(моль·К) Уравнение состояния идеального газа p. V = М/μ∙RT в такой форме записи называется уравнением Клапейрона-Менделеева. При нормальных условиях (НУ), т. е. при давлении ро = 1. 013· 105 Па (что эквивалентно 760 мм ртутного столба или одной физической атмосфере) и температуре То = 273, 15 К (t = 0 о C) многие газы (Н 2, О 2, N 2, воздух и др. ) можно считать с хорошим приближением идеальными. Согласно закону Авогадро при нормальных условиях объем моля любого газа равен Vо = 22, 4 л/моль = 22, 4∙ 10 -3 м 3/моль. Покажем это. Для одного моля газа при НУ po = nk. To = NA /Vo·k. To, откуда Vo = NAk. Tо/ ро. Подставляя сюда численные значения, получаем : Vo = (6, 022· 1023 моль-1· 1, 38∙ 10 -23 Дж ·К-1 · 273, 15 K) /1, 013∙ 105 Па = 22, 4· 10 -3 м 3/моль Авогадро
Уравнение состояния идеального газа Учитывая, что концентрация молекул в объеме V равна n = N/V основное уравнение молекулярно-кинетической теории p = nk. T можно записать в следующем виде: p = N/V∙k. T = М/μV∙NAk. T или p. V = М/μ∙RT, где N = NA∙М/μ – общее число молекул в массе М газа, а М/μ - число молей газа , R = NA·k – универсальная газовая постоянная Значение универсальной газовой постоянной равно : R = NA·k = 6, 022· 1023 моль-1· 1, 38· 10 -23 Дж/К = 8, 31 Дж/(моль·К) Уравнение состояния идеального газа p. V = М/μ∙RT в такой форме записи называется уравнением Клапейрона-Менделеева. При нормальных условиях (НУ), т. е. при давлении ро = 1. 013· 105 Па (что эквивалентно 760 мм ртутного столба или одной физической атмосфере) и температуре То = 273, 15 К (t = 0 о C) многие газы (Н 2, О 2, N 2, воздух и др. ) можно считать с хорошим приближением идеальными. Согласно закону Авогадро при нормальных условиях объем моля любого газа равен Vо = 22, 4 л/моль = 22, 4∙ 10 -3 м 3/моль. Покажем это. Для одного моля газа при НУ po = nk. To = NA /Vo·k. To, откуда Vo = NAk. Tо/ ро. Подставляя сюда численные значения, получаем : Vo = (6, 022· 1023 моль-1· 1, 38∙ 10 -23 Дж ·К-1 · 273, 15 K) /1, 013∙ 105 Па = 22, 4· 10 -3 м 3/моль Авогадро
 Барометрическая формула При выводе основного уравнения молекулярнокинетической теории предполагалось, что на молекулы газа внешние силы не действуют, поэтому молекулы равномерно распределены по объему. Однако молекулы газа находятся в поле тяготения Земли, поэтому их концентрация с высотой уменьшается. Покажем это. Если атмосферное давление на высоте h равно р, то на высоте h+dh оно равно р+dр Разность давлений р и р+dр равна весу газа, заключенного в объеме цилиндра высотой dh с основанием 1 м 2: p - (p+dp) = ∙g∙dh, где = pμ/RT - плотность газа. Поскольку давление с высотой убывает, то при dh>0 dр<0, и dp = - ∙g∙dh = - pμgdh/RT. Тогда dp/p = – μg/RT∙dh. Интегрируя от h = 0 до h , получаем ln(p) = - μgh/RT + С. При h = 0 постоянная С = ln(po) и ln (p) = - μgh/RT + ln(po) или ln(p/po) = - μgh/RT. Проведя потенцирование, получим барометрическую формулу: p = po∙exp( – μgh/RT ) или p = po∙exp( – mgh/k. T ) , где m = μ/NA – масса одной молекулы, k = R/NA = 1, 38∙ 10 -23 Дж/К – постоянная Больцмана.
Барометрическая формула При выводе основного уравнения молекулярнокинетической теории предполагалось, что на молекулы газа внешние силы не действуют, поэтому молекулы равномерно распределены по объему. Однако молекулы газа находятся в поле тяготения Земли, поэтому их концентрация с высотой уменьшается. Покажем это. Если атмосферное давление на высоте h равно р, то на высоте h+dh оно равно р+dр Разность давлений р и р+dр равна весу газа, заключенного в объеме цилиндра высотой dh с основанием 1 м 2: p - (p+dp) = ∙g∙dh, где = pμ/RT - плотность газа. Поскольку давление с высотой убывает, то при dh>0 dр<0, и dp = - ∙g∙dh = - pμgdh/RT. Тогда dp/p = – μg/RT∙dh. Интегрируя от h = 0 до h , получаем ln(p) = - μgh/RT + С. При h = 0 постоянная С = ln(po) и ln (p) = - μgh/RT + ln(po) или ln(p/po) = - μgh/RT. Проведя потенцирование, получим барометрическую формулу: p = po∙exp( – μgh/RT ) или p = po∙exp( – mgh/k. T ) , где m = μ/NA – масса одной молекулы, k = R/NA = 1, 38∙ 10 -23 Дж/К – постоянная Больцмана.
 Распределение Больцмана Анализ барометрической формулы показывает, что чем больше молярная масса μ газа, тем быстрее его давление убывает с высотой. Поэтому атмосфера по мере увеличения высоты все более обогащается легкими газами. Следует иметь в виду, что применимость барометрической формулы к реальной атмосфере несколько ограничена, поскольку атмосфера в действительности не находится в тепловом равновесии и ее температура меняется с высотой. Тем не менее, ее используют, определяя высоту по изменению давления. Барометрическую формулу можно преобразовать, если воспользоваться выражением p = nk. T и независимостью температуры от высоты : nk. T = nok. T∙exp( – m. NAgh/k. NAT ) . Здесь m - масса одной молекулы , NA – число Авогадро, а R = k∙NA – универсальная газовая постоянная, k – постоянная Больцмана. После сокращений получаем : n = no∙exp( – mgh/k. T ). Если учесть, что mgh = Eп - потенциальная энергия молекулы в поле тяготения, то n = no∙exp( – Eп/k. T ) . Больцман доказал, что эта формула справедлива в случае . потенциального поля любой природы (т. е. не только поля тяготения). В связи с этим функцию n/no = exp( – E/k. T ) называют распределением Больцмана молекул по энергии во внешнем силовом поле.
Распределение Больцмана Анализ барометрической формулы показывает, что чем больше молярная масса μ газа, тем быстрее его давление убывает с высотой. Поэтому атмосфера по мере увеличения высоты все более обогащается легкими газами. Следует иметь в виду, что применимость барометрической формулы к реальной атмосфере несколько ограничена, поскольку атмосфера в действительности не находится в тепловом равновесии и ее температура меняется с высотой. Тем не менее, ее используют, определяя высоту по изменению давления. Барометрическую формулу можно преобразовать, если воспользоваться выражением p = nk. T и независимостью температуры от высоты : nk. T = nok. T∙exp( – m. NAgh/k. NAT ) . Здесь m - масса одной молекулы , NA – число Авогадро, а R = k∙NA – универсальная газовая постоянная, k – постоянная Больцмана. После сокращений получаем : n = no∙exp( – mgh/k. T ). Если учесть, что mgh = Eп - потенциальная энергия молекулы в поле тяготения, то n = no∙exp( – Eп/k. T ) . Больцман доказал, что эта формула справедлива в случае . потенциального поля любой природы (т. е. не только поля тяготения). В связи с этим функцию n/no = exp( – E/k. T ) называют распределением Больцмана молекул по энергии во внешнем силовом поле.
 Распределение молекул по компонентам скорости Функция распределения молекул по скоростям ƒ(υ) = n/(dn∙dυ) равна вероятности dn/n встретить молекулу со скоростью в диапазоне от υ до υ+dυ. Следовательно, зная функцию распределения, можно найти число молекул, имеющих скорости в диапазоне от υ до υ+dυ : dn = n∙ƒ(υ)∙dυ. Рассмотрим прохождение молекул через тонкий слой dz , расположенный на высоте z от поверхности земли. Концентрация молекул в этом слое на высоте z равна nz , а z-составляющая скорости равна υz. Вертикально вверх через него пролетают только те молекулы, которые у поверхности земли имели z-составляющую скорости не менее, чем √ 2 gz (из закона сохранения энергии ½mυ² = mgz). За единицу времени через единичную площадку этого слоя снизу вверх (↑) пролетят молекулы, которые находились от него на расстоянии υz. Общее их число равно ∞ nо∙∫ƒо(υz)∙υz∙dυz , √ 2 gz где nо – концентрация молекул у поверхности земли, ƒо(υz) – функция распределения молекул по z-составляющей скорости у поверхности земли. В обратном направлении сверху вниз (↓) через этот слой проходят молекулы, которые на высоте z имеют zкомпоненту скорости υz от нуля до бесконечности. За единицу времени через единичную площадку этого слоя пролетят молекулы, которые находились от него также на расстоянии υz. Общее их число: ∞ nz∙∫ƒz(υz)∙υz∙dυz , 0 где nz – концентрация молекул на высоте z, ƒz(υz) – функция распределения молекул по z-составляющей скорости на высоте z.
Распределение молекул по компонентам скорости Функция распределения молекул по скоростям ƒ(υ) = n/(dn∙dυ) равна вероятности dn/n встретить молекулу со скоростью в диапазоне от υ до υ+dυ. Следовательно, зная функцию распределения, можно найти число молекул, имеющих скорости в диапазоне от υ до υ+dυ : dn = n∙ƒ(υ)∙dυ. Рассмотрим прохождение молекул через тонкий слой dz , расположенный на высоте z от поверхности земли. Концентрация молекул в этом слое на высоте z равна nz , а z-составляющая скорости равна υz. Вертикально вверх через него пролетают только те молекулы, которые у поверхности земли имели z-составляющую скорости не менее, чем √ 2 gz (из закона сохранения энергии ½mυ² = mgz). За единицу времени через единичную площадку этого слоя снизу вверх (↑) пролетят молекулы, которые находились от него на расстоянии υz. Общее их число равно ∞ nо∙∫ƒо(υz)∙υz∙dυz , √ 2 gz где nо – концентрация молекул у поверхности земли, ƒо(υz) – функция распределения молекул по z-составляющей скорости у поверхности земли. В обратном направлении сверху вниз (↓) через этот слой проходят молекулы, которые на высоте z имеют zкомпоненту скорости υz от нуля до бесконечности. За единицу времени через единичную площадку этого слоя пролетят молекулы, которые находились от него также на расстоянии υz. Общее их число: ∞ nz∙∫ƒz(υz)∙υz∙dυz , 0 где nz – концентрация молекул на высоте z, ƒz(υz) – функция распределения молекул по z-составляющей скорости на высоте z.
 Распределение молекул по компонентам скорости В стационарной атмосфере должно наблюдаться равновесие и число молекул, проходящих слой dz в обоих направлениях одинаково: ∞ ↓ nz∙∫ƒz(υz)∙υz∙dυz = nо∙∫ƒo(υz)∙υo∙dυz ↑ 0 √ 2 gz В правой части равенства заменим переменную υo на υz и соответственно и пределы интегрирования. Учтем также и барометрическую формулу для концентрации молекул на высоте z. ∞ ∞ ↓ no∙∫ƒz(υz)∙ exp(- mgz/k. T)∙υz∙dυz = nо∙∫ƒo(υz)∙υz∙dυz ↑ 0 0 Если теперь переменные и пределы интегрирования одинаковы, то подинтегральные выражения тоже равны: no∙exp(- mgz/k. T)∙ƒz(υz)∙υz = nо∙ƒo(υz)∙υz или exp(- mgz/k. T)∙ƒz(υz) = ƒo(υz). С учетом закона сохранения энергии данное выражение справедливо лишь при ƒ(υz) = A∙exp(- ½mυz²/k. T) , то есть exp(-mgz/k. T)∙A∙exp(- ½mυz²/k. T) = A∙exp(- ½mυo²/k. T) или A∙exp(-mgz/k. T-½mυz²/k. T) = A∙exp(-½mυo²/k. T), что подтверждается законом сохранения энергии для молекулы (mgz+½mυz² = ½mυo² ). Следовательно, распределение молекул по z-составляющей скорости определяется как ƒ(υz) = A∙exp(- mυz²/2 k. T). ∞ ∞ Постоянная А найдется из условия нормировки : ∫ƒ(υz)∙dυz) = 1 или ∫A∙exp(- mυz²/2 k. T)∙dυz =1 0 0 ∞ ∞ Приведем интеграл ∫exp(- mυz²/2 k. T)∙dυz к виду ∫exp- x² ∙dx = √π . 0 0 Если mυz²/2 k. T = x² , то υz = x∙√ 2 k. T/m = dx и dυz = dx·√ 2 k. T/m. Подставим это выражение под интеграл, вынесем постоянные за знак интеграла и получим : A∙√ 2 k. T/m∙∫exp(-x²)∙dx = 1 ; A∙√ 2 k. T/m∙√π = 1 , откуда А = √m/2πk. T. Окончательно функция распределения молекул по z-составляющей скорости равна : ƒ(υz) = √m/2πk. T ∙exp(- mυz²/2 k. T).
Распределение молекул по компонентам скорости В стационарной атмосфере должно наблюдаться равновесие и число молекул, проходящих слой dz в обоих направлениях одинаково: ∞ ↓ nz∙∫ƒz(υz)∙υz∙dυz = nо∙∫ƒo(υz)∙υo∙dυz ↑ 0 √ 2 gz В правой части равенства заменим переменную υo на υz и соответственно и пределы интегрирования. Учтем также и барометрическую формулу для концентрации молекул на высоте z. ∞ ∞ ↓ no∙∫ƒz(υz)∙ exp(- mgz/k. T)∙υz∙dυz = nо∙∫ƒo(υz)∙υz∙dυz ↑ 0 0 Если теперь переменные и пределы интегрирования одинаковы, то подинтегральные выражения тоже равны: no∙exp(- mgz/k. T)∙ƒz(υz)∙υz = nо∙ƒo(υz)∙υz или exp(- mgz/k. T)∙ƒz(υz) = ƒo(υz). С учетом закона сохранения энергии данное выражение справедливо лишь при ƒ(υz) = A∙exp(- ½mυz²/k. T) , то есть exp(-mgz/k. T)∙A∙exp(- ½mυz²/k. T) = A∙exp(- ½mυo²/k. T) или A∙exp(-mgz/k. T-½mυz²/k. T) = A∙exp(-½mυo²/k. T), что подтверждается законом сохранения энергии для молекулы (mgz+½mυz² = ½mυo² ). Следовательно, распределение молекул по z-составляющей скорости определяется как ƒ(υz) = A∙exp(- mυz²/2 k. T). ∞ ∞ Постоянная А найдется из условия нормировки : ∫ƒ(υz)∙dυz) = 1 или ∫A∙exp(- mυz²/2 k. T)∙dυz =1 0 0 ∞ ∞ Приведем интеграл ∫exp(- mυz²/2 k. T)∙dυz к виду ∫exp- x² ∙dx = √π . 0 0 Если mυz²/2 k. T = x² , то υz = x∙√ 2 k. T/m = dx и dυz = dx·√ 2 k. T/m. Подставим это выражение под интеграл, вынесем постоянные за знак интеграла и получим : A∙√ 2 k. T/m∙∫exp(-x²)∙dx = 1 ; A∙√ 2 k. T/m∙√π = 1 , откуда А = √m/2πk. T. Окончательно функция распределения молекул по z-составляющей скорости равна : ƒ(υz) = √m/2πk. T ∙exp(- mυz²/2 k. T).
 Распределение молекул по х-составляющей скорости Функция распределения молекул по z-составляющей скорости не является привилегией только направления оси z . Это направление выбрано только потому, что удобно было воспользоваться силой тяжести для выделения одной из составляющих скорости. Такое же распределение имеет место и для других направлений x и y. Обозначим в пространстве скоростей на оси υх диапазон от υх до υх+dυх . Скорости молекул могут быть направлены в разных направлениях. Разместим векторы скоростей на чертеже так, чтобы начала их совпадали с началом отсчета на оси υх. Проекция на ось υх этих векторов будет находиться в диапазоне от υх до υх+dυх , если концы их попадают в обозначенный на чертеже промежуток dυх на оси скоростей υх. Учитывая закон распределения молекул по z‑составляющей скорости, вероятность найти молекулу с данной проекцией скорости в диапазоне от υх до υх+dυх равна: dn/n=√m/2πk. T∙exp(mυx²/2 k. T)∙dυx. При увеличении ширины интервала dυх вероятность найти молекулу с такой составляющей скорости, конечно возрастает.
Распределение молекул по х-составляющей скорости Функция распределения молекул по z-составляющей скорости не является привилегией только направления оси z . Это направление выбрано только потому, что удобно было воспользоваться силой тяжести для выделения одной из составляющих скорости. Такое же распределение имеет место и для других направлений x и y. Обозначим в пространстве скоростей на оси υх диапазон от υх до υх+dυх . Скорости молекул могут быть направлены в разных направлениях. Разместим векторы скоростей на чертеже так, чтобы начала их совпадали с началом отсчета на оси υх. Проекция на ось υх этих векторов будет находиться в диапазоне от υх до υх+dυх , если концы их попадают в обозначенный на чертеже промежуток dυх на оси скоростей υх. Учитывая закон распределения молекул по z‑составляющей скорости, вероятность найти молекулу с данной проекцией скорости в диапазоне от υх до υх+dυх равна: dn/n=√m/2πk. T∙exp(mυx²/2 k. T)∙dυx. При увеличении ширины интервала dυх вероятность найти молекулу с такой составляющей скорости, конечно возрастает.
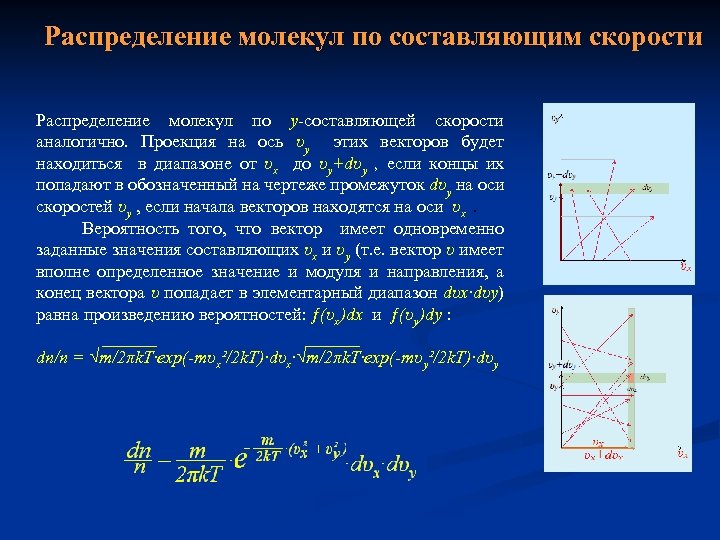 Распределение молекул по составляющим скорости Распределение молекул по y-составляющей скорости аналогично. Проекция на ось υy этих векторов будет находиться в диапазоне от υх до υy+dυy , если концы их попадают в обозначенный на чертеже промежуток dυy на оси скоростей υy , если начала векторов находятся на оси υх . Вероятность того, что вектор имеет одновременно заданные значения составляющих υx и υy (т. е. вектор υ имеет вполне определенное значение и модуля и направления, а конец вектора υ попадает в элементарный диапазон dυx∙dυy) равна произведению вероятностей: ƒ(υx)dx и ƒ(υy)dy : dn/n = √m/2πk. T∙exp(‑mυx²/2 k. T)∙dυx∙√m/2πk. T∙exp(‑mυy²/2 k. T)∙dυy
Распределение молекул по составляющим скорости Распределение молекул по y-составляющей скорости аналогично. Проекция на ось υy этих векторов будет находиться в диапазоне от υх до υy+dυy , если концы их попадают в обозначенный на чертеже промежуток dυy на оси скоростей υy , если начала векторов находятся на оси υх . Вероятность того, что вектор имеет одновременно заданные значения составляющих υx и υy (т. е. вектор υ имеет вполне определенное значение и модуля и направления, а конец вектора υ попадает в элементарный диапазон dυx∙dυy) равна произведению вероятностей: ƒ(υx)dx и ƒ(υy)dy : dn/n = √m/2πk. T∙exp(‑mυx²/2 k. T)∙dυx∙√m/2πk. T∙exp(‑mυy²/2 k. T)∙dυy
 Распределение Максвелла молекул по скорости Функция распределения молекул по z-составляющей скорости не является привилегией только направления оси z . Это направление выбрано только потому, что удобно было воспользоваться силой тяжести для выделения одной из составляющих скорости. Такое же распределение имеет место и для других направлений x и y. Представим вектор скорости υ молекулы в координатах υх , υy , υz как показано на рисунке. Вероятность того, что вектор имеет заданное направление, и конец вектора υ попадает в элементарный объем dυх∙dυy∙dυz равна произведению вероятностей: dn/n=√m/2πk. T∙exp(‑mυx²/2 k. T)∙dυx∙√m/2πk. T∙exp(‑mυy²/2 k. T)∙dυy∙√m/2πk. T∙exp(‑mυz²/2 k. T)∙dυz dn/n=(m/2πk. T)3/2∙exp(‑mυx²/2 k. T‑mυy²/2 k. T‑mυx²/2 k. T) ∙dυх∙dυy∙dυz
Распределение Максвелла молекул по скорости Функция распределения молекул по z-составляющей скорости не является привилегией только направления оси z . Это направление выбрано только потому, что удобно было воспользоваться силой тяжести для выделения одной из составляющих скорости. Такое же распределение имеет место и для других направлений x и y. Представим вектор скорости υ молекулы в координатах υх , υy , υz как показано на рисунке. Вероятность того, что вектор имеет заданное направление, и конец вектора υ попадает в элементарный объем dυх∙dυy∙dυz равна произведению вероятностей: dn/n=√m/2πk. T∙exp(‑mυx²/2 k. T)∙dυx∙√m/2πk. T∙exp(‑mυy²/2 k. T)∙dυy∙√m/2πk. T∙exp(‑mυz²/2 k. T)∙dυz dn/n=(m/2πk. T)3/2∙exp(‑mυx²/2 k. T‑mυy²/2 k. T‑mυx²/2 k. T) ∙dυх∙dυy∙dυz
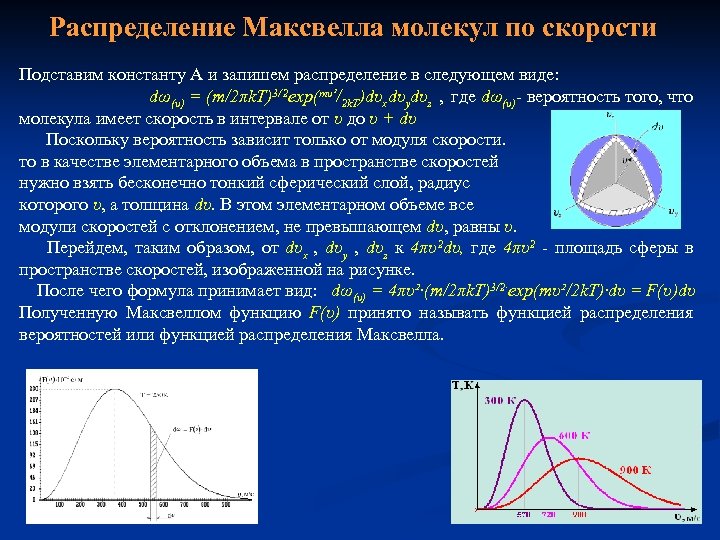 Распределение Максвелла молекул по скорости Подставим константу А и запишем распределение в следующем виде: dω(υ) = (m/2πk. T)3/2 exp(mυ²/2 k. T)dυxdυydυz , где dω(υ)- вероятность того, что молекула имеет скорость в интервале от υ до υ + dυ Поскольку вероятность зависит только от модуля скорости. то в качестве элементарного объема в пространстве скоростей нужно взять бесконечно тонкий сферический слой, радиус которого υ, а толщина dυ. В этом элементарном объеме все модули скоростей с отклонением, не превышающем dυ, равны υ. Перейдем, таким образом, от dυх , dυy , dυz к 4πυ2 dυ, где 4πυ2 - площадь сферы в пространстве скоростей, изображенной на рисунке. После чего формула принимает вид: dω(υ) = 4πυ²∙(m/2πk. T)3/2∙exp(mυ²/2 k. T)∙dυ = F(υ)dυ Полученную Максвеллом функцию F(υ) принято называть функцией распределения вероятностей или функцией распределения Максвелла.
Распределение Максвелла молекул по скорости Подставим константу А и запишем распределение в следующем виде: dω(υ) = (m/2πk. T)3/2 exp(mυ²/2 k. T)dυxdυydυz , где dω(υ)- вероятность того, что молекула имеет скорость в интервале от υ до υ + dυ Поскольку вероятность зависит только от модуля скорости. то в качестве элементарного объема в пространстве скоростей нужно взять бесконечно тонкий сферический слой, радиус которого υ, а толщина dυ. В этом элементарном объеме все модули скоростей с отклонением, не превышающем dυ, равны υ. Перейдем, таким образом, от dυх , dυy , dυz к 4πυ2 dυ, где 4πυ2 - площадь сферы в пространстве скоростей, изображенной на рисунке. После чего формула принимает вид: dω(υ) = 4πυ²∙(m/2πk. T)3/2∙exp(mυ²/2 k. T)∙dυ = F(υ)dυ Полученную Максвеллом функцию F(υ) принято называть функцией распределения вероятностей или функцией распределения Максвелла.
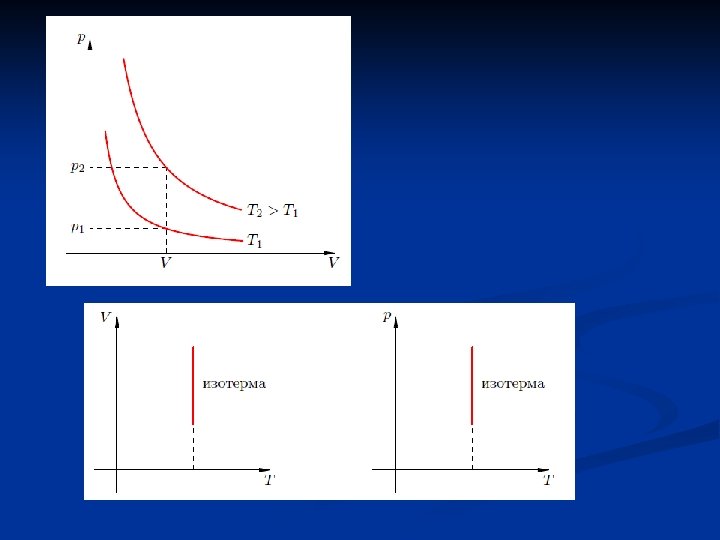
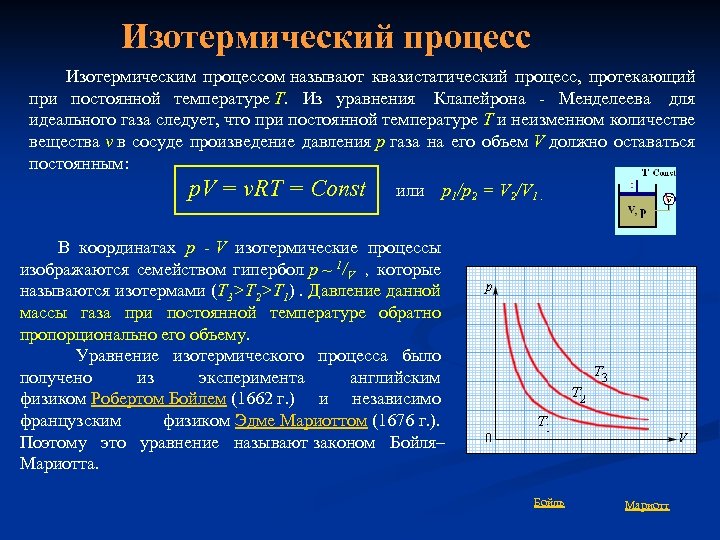 Изотермический процесс Изотермическим процессом называют квазистатический процесс, протекающий при постоянной температуре T. Из уравнения Клапейрона - Менделеева для идеального газа следует, что при постоянной температуре T и неизменном количестве вещества ν в сосуде произведение давления p газа на его объем V должно оставаться постоянным: p. V = νRT = Const или p 1/p 2 = V 2/V 1. В координатах p - V изотермические процессы изображаются семейством гипербол p ~ 1/V , которые называются изотермами (Т 3>Т 2>Т 1). Давление данной массы газа при постоянной температуре обратно пропорционально его объему. Уравнение изотермического процесса было получено из эксперимента английским физиком Робертом Бойлем (1662 г. ) и независимо французским физиком Эдме Мариоттом (1676 г. ). Поэтому это уравнение называют законом Бойля– Мариотта. Бойль Мариотт
Изотермический процесс Изотермическим процессом называют квазистатический процесс, протекающий при постоянной температуре T. Из уравнения Клапейрона - Менделеева для идеального газа следует, что при постоянной температуре T и неизменном количестве вещества ν в сосуде произведение давления p газа на его объем V должно оставаться постоянным: p. V = νRT = Const или p 1/p 2 = V 2/V 1. В координатах p - V изотермические процессы изображаются семейством гипербол p ~ 1/V , которые называются изотермами (Т 3>Т 2>Т 1). Давление данной массы газа при постоянной температуре обратно пропорционально его объему. Уравнение изотермического процесса было получено из эксперимента английским физиком Робертом Бойлем (1662 г. ) и независимо французским физиком Эдме Мариоттом (1676 г. ). Поэтому это уравнение называют законом Бойля– Мариотта. Бойль Мариотт
 Изобарический процесс Изобарным процессом называют квазистатический процесс, протекающий при неизменным давлении p. Практически он осуществляется, например, при нагревании или охлаждении газа, находящегося в цилиндре с подвижным поршнем, на который действует постоянное внешнее давление. Уравнение изобарного процесса для некоторого неизменного количества вещества ν имеет вид: V 1/T 1 = V 2/T 2 = Const или V = Vo∙α∙T , или V = Vо∙(1 + a∙t), где Vо – объем газа при температуре 0°С. Температурный коэффициент объемного расширения газов α = 1/273, 15 К– 1. Зависимость объема газа от температуры при неизменном давлении была экспериментально исследована французским физиком Ж. Гей-Люссаком (1862 г. ). Графически зависимость объема от температуры изображается прямой линией – изобарой (p 1>p 2>p 3). При постоянном давлении объем данной массы газа растет прямо пропорционально его температуре. При очень низких температурах (близких к – 273°С) закон Гей–Люссака не выполняется, поэтому сплошная линия на графике заменена пунктиром. Гей-Люссак
Изобарический процесс Изобарным процессом называют квазистатический процесс, протекающий при неизменным давлении p. Практически он осуществляется, например, при нагревании или охлаждении газа, находящегося в цилиндре с подвижным поршнем, на который действует постоянное внешнее давление. Уравнение изобарного процесса для некоторого неизменного количества вещества ν имеет вид: V 1/T 1 = V 2/T 2 = Const или V = Vo∙α∙T , или V = Vо∙(1 + a∙t), где Vо – объем газа при температуре 0°С. Температурный коэффициент объемного расширения газов α = 1/273, 15 К– 1. Зависимость объема газа от температуры при неизменном давлении была экспериментально исследована французским физиком Ж. Гей-Люссаком (1862 г. ). Графически зависимость объема от температуры изображается прямой линией – изобарой (p 1>p 2>p 3). При постоянном давлении объем данной массы газа растет прямо пропорционально его температуре. При очень низких температурах (близких к – 273°С) закон Гей–Люссака не выполняется, поэтому сплошная линия на графике заменена пунктиром. Гей-Люссак
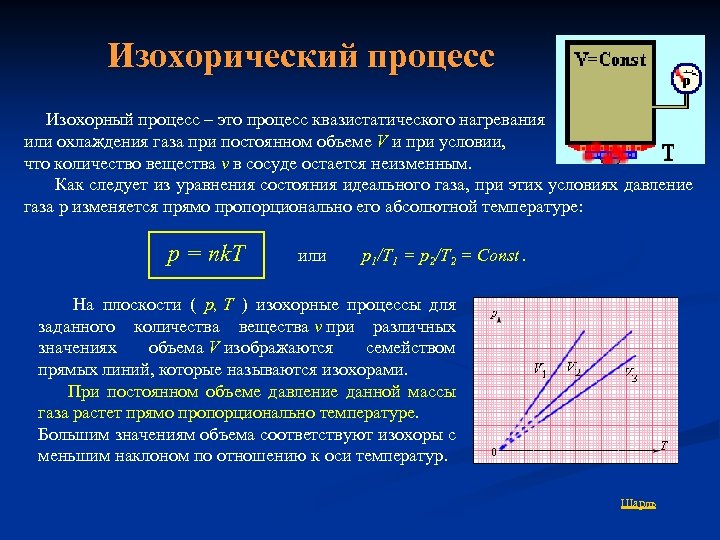 Изохорический процесс Изохорный процесс – это процесс квазистатического нагревания или охлаждения газа при постоянном объеме V и при условии, что количество вещества ν в сосуде остается неизменным. Как следует из уравнения состояния идеального газа, при этих условиях давление газа p изменяется прямо пропорционально его абсолютной температуре: p = nk. T или p 1/T 1 = p 2/T 2 = Const. На плоскости ( p, T ) изохорные процессы для заданного количества вещества ν при различных значениях объема V изображаются семейством прямых линий, которые называются изохорами. При постоянном объеме давление данной массы газа растет прямо пропорционально температуре. Большим значениям объема соответствуют изохоры с меньшим наклоном по отношению к оси температур. Шарль
Изохорический процесс Изохорный процесс – это процесс квазистатического нагревания или охлаждения газа при постоянном объеме V и при условии, что количество вещества ν в сосуде остается неизменным. Как следует из уравнения состояния идеального газа, при этих условиях давление газа p изменяется прямо пропорционально его абсолютной температуре: p = nk. T или p 1/T 1 = p 2/T 2 = Const. На плоскости ( p, T ) изохорные процессы для заданного количества вещества ν при различных значениях объема V изображаются семейством прямых линий, которые называются изохорами. При постоянном объеме давление данной массы газа растет прямо пропорционально температуре. Большим значениям объема соответствуют изохоры с меньшим наклоном по отношению к оси температур. Шарль
 Явления переноса До сих пор мы рассматривали исключительно равновесные системы, характеризующиеся при постоянных внешних условиях, неизменностью параметров (Р, V, T, ) во времени и отсутствием в системе потоков вещества, энергии, импульса. Однако, беспорядочность теплового движения молекул газа, непрерывные столкновения между ними приводят к постоянному перемешиванию частиц и изменению их скоростей и энергий. Если в газе существует пространственная неоднородность плотности, температуры, скорости упорядоченного перемещения отдельных слоев, то происходит самопроизвольное выравнивание этих неоднородностей. В газе возникают потоки вещества, энергии, импульса упорядоченного движения молекул. Эти потоки, характерные для неравновесных состояний газа, являются физической основой особых процессов, объединенных общим названием "явления переноса". К этим явлениям относятся диффузия, теплопроводность и внутреннее трение. Для простоты ограничимся одномерными явлениями переноса. Систему отсчета выберем так, чтобы ось х была ориентирована в направлении переноса.
Явления переноса До сих пор мы рассматривали исключительно равновесные системы, характеризующиеся при постоянных внешних условиях, неизменностью параметров (Р, V, T, ) во времени и отсутствием в системе потоков вещества, энергии, импульса. Однако, беспорядочность теплового движения молекул газа, непрерывные столкновения между ними приводят к постоянному перемешиванию частиц и изменению их скоростей и энергий. Если в газе существует пространственная неоднородность плотности, температуры, скорости упорядоченного перемещения отдельных слоев, то происходит самопроизвольное выравнивание этих неоднородностей. В газе возникают потоки вещества, энергии, импульса упорядоченного движения молекул. Эти потоки, характерные для неравновесных состояний газа, являются физической основой особых процессов, объединенных общим названием "явления переноса". К этим явлениям относятся диффузия, теплопроводность и внутреннее трение. Для простоты ограничимся одномерными явлениями переноса. Систему отсчета выберем так, чтобы ось х была ориентирована в направлении переноса.
 Явления переноса - тепловодность (перенос энергии) Это перенос теплоты (внутренней энергии) от более нагретых мест к менее нагретым. Фурье (1822 г. ) установил, что количество теплоты d. Q , которое переносится вследствие теплопроводности через площадку d. S┴ в перпендикулярном к ней направлении за время dt равно : d. Q = - χ∙(d. T/dx)∙ d. S┴·dt Градиент температуры d. T/dx характеризует скорость изменения температуры Т на единицу длины х , χ - коэффициент теплопроводности. Знак минус указывает, что при теплопроводности перенос внутренней энергии происходит в направлении убывания температуры. Закон Фурье – количество тепла, переносимое через единицу пощади в перпендикулярном к ней направлении за единицу времени пропорционально градиенту температуры. Для газов коэффициент теплопроводности χ равен χ = ⅓∙υср∙λср∙с. V∙ρ , где υср и λср – средняя скорость и средняя длина свободного пробега молекул от одного соударения до другого, с. V - удельная теплоемкость при постоянном объеме газа. Фурье
Явления переноса - тепловодность (перенос энергии) Это перенос теплоты (внутренней энергии) от более нагретых мест к менее нагретым. Фурье (1822 г. ) установил, что количество теплоты d. Q , которое переносится вследствие теплопроводности через площадку d. S┴ в перпендикулярном к ней направлении за время dt равно : d. Q = - χ∙(d. T/dx)∙ d. S┴·dt Градиент температуры d. T/dx характеризует скорость изменения температуры Т на единицу длины х , χ - коэффициент теплопроводности. Знак минус указывает, что при теплопроводности перенос внутренней энергии происходит в направлении убывания температуры. Закон Фурье – количество тепла, переносимое через единицу пощади в перпендикулярном к ней направлении за единицу времени пропорционально градиенту температуры. Для газов коэффициент теплопроводности χ равен χ = ⅓∙υср∙λср∙с. V∙ρ , где υср и λср – средняя скорость и средняя длина свободного пробега молекул от одного соударения до другого, с. V - удельная теплоемкость при постоянном объеме газа. Фурье
 Явления переноса - диффузия (перенос массы) Это перенос массы из мест с большей плотностью к местам с меньшей плотностью. Фик (1855 г) установил, что перенесенная масса dm через расположенную перпендикулярно направлению переноса вещества площадку d. S┴ за время dt равна : dm = - D∙(d /dx)∙d. S┴∙ dt , где d /dx характеризует скорость изменения плотности на единицу длины x , D - коэффициент диффузии. Знак минус указывает, что перенос массы при диффузии происходит в направлении убывании плотности, т. е. вдоль оси х , если 2 > 1 , то d /dx < 0. Для газов коэффициент диффузии равен D = ⅓∙υср∙λср , где υср и λср – средняя скорость и средняя длина свободного пробега молекул от одного соударения до другого.
Явления переноса - диффузия (перенос массы) Это перенос массы из мест с большей плотностью к местам с меньшей плотностью. Фик (1855 г) установил, что перенесенная масса dm через расположенную перпендикулярно направлению переноса вещества площадку d. S┴ за время dt равна : dm = - D∙(d /dx)∙d. S┴∙ dt , где d /dx характеризует скорость изменения плотности на единицу длины x , D - коэффициент диффузии. Знак минус указывает, что перенос массы при диффузии происходит в направлении убывании плотности, т. е. вдоль оси х , если 2 > 1 , то d /dx < 0. Для газов коэффициент диффузии равен D = ⅓∙υср∙λср , где υср и λср – средняя скорость и средняя длина свободного пробега молекул от одного соударения до другого.
 Явления переноса - вязкость жидкостей и газов (перенос импульса) Внутреннее трение (вязкость) возникает между слоями жидкости или газа, движущимися упорядоченно с различными скоростями u . Из за хаотического теплового движения происходит обмен молекулами между слоями, в результате чего импульс слоя, движущегося быстрее, уменьшается, а движущегося медленнее - увеличивается, что приводит к торможению слоя, движущегося быстрее и ускорению слоя, движущегося медленнее. Согласно закону Ньютона (1687 г) сила внутреннего трения между слоями газа или жидкости равна : F = – η ∙ du/dx∙ S┴ , где du/dx характеризует быстроту изменения скорости u на единицу длины x , S┴ - площадь, на которую действует сила (площадка перпендикулярна х ), η = ⅓∙υср∙λср∙ρ – коэффициент внутреннего трения (динамическая вязкость). Знак минус в выражении для силы F указывает, что импульс переносится в направлении убывания скорости слоев u. Анализ формул показывает, что η = ρ∙D и lср/(η∙c. V ) = 1. Используя эти формулы, можно по найденным из опыта одним величинам, определить другие.
Явления переноса - вязкость жидкостей и газов (перенос импульса) Внутреннее трение (вязкость) возникает между слоями жидкости или газа, движущимися упорядоченно с различными скоростями u . Из за хаотического теплового движения происходит обмен молекулами между слоями, в результате чего импульс слоя, движущегося быстрее, уменьшается, а движущегося медленнее - увеличивается, что приводит к торможению слоя, движущегося быстрее и ускорению слоя, движущегося медленнее. Согласно закону Ньютона (1687 г) сила внутреннего трения между слоями газа или жидкости равна : F = – η ∙ du/dx∙ S┴ , где du/dx характеризует быстроту изменения скорости u на единицу длины x , S┴ - площадь, на которую действует сила (площадка перпендикулярна х ), η = ⅓∙υср∙λср∙ρ – коэффициент внутреннего трения (динамическая вязкость). Знак минус в выражении для силы F указывает, что импульс переносится в направлении убывания скорости слоев u. Анализ формул показывает, что η = ρ∙D и lср/(η∙c. V ) = 1. Используя эти формулы, можно по найденным из опыта одним величинам, определить другие.
 Степени свободы молекулы Важной характеристикой термодинамической системы является ее внутренняя энергия U. Это энергия хаотического (теплового) движения микрочастиц системы (молекул, атомов, электронов, ядер и т. д. ) и энергия взаимодействия этих частиц. Число независимых координат, полностью определяющих положение тела (материальной точки, системы материальных точек) в пространстве называется числом степеней свободы i. Так, например, положение материальной точки определяется тремя координатами (x, y, z), следовательно, i = 3. Тонкий стержень имеет 5 степеней свободы (x, y, z, a, b), т. е. 3 поступательные и 2 вращательные, твердое тело имеет 6 степеней свободы (x, y, z, a, b, ), т. е. 3 поступательные и 3 вращательные. С учетом этого для одноатомных молекул газа (He, Ne, Ar) i = 3, для двухатомных молекул газа (H 2, O 2, N 2) с жесткой связью атомов i=5, для трех- и более атомных молекул газа с жесткой связью атомов (CO 2, NH 3) i = 6. Если жесткой связи между атомами не существует - атомы могут совершать колебания - полное число степеней свободы i = iпост+ 2 iколеб. В классической теории рассматривают молекулы с жесткой связью атомов, для них iколеб. = 0. Итак, независимо от числа степеней свободы молекул три степени свободы всегда поступательные. Ни одна из них не имеет преимущества перед другими, поэтому на каждую из них приходится в среднем одинаковая энергия, равная <⅓Ek> = ½k. T. Важнейший закон классической статистической физики - закон равномерного распределения энергии по степеням свободы - утверждает: на каждую степень свободы молекулы в среднем приходится одинаковая кинетическая энергия, равная ½k. Т. Следовательно, средняя кинетическая энергия молекулы, имеющей i степеней свободы,
Степени свободы молекулы Важной характеристикой термодинамической системы является ее внутренняя энергия U. Это энергия хаотического (теплового) движения микрочастиц системы (молекул, атомов, электронов, ядер и т. д. ) и энергия взаимодействия этих частиц. Число независимых координат, полностью определяющих положение тела (материальной точки, системы материальных точек) в пространстве называется числом степеней свободы i. Так, например, положение материальной точки определяется тремя координатами (x, y, z), следовательно, i = 3. Тонкий стержень имеет 5 степеней свободы (x, y, z, a, b), т. е. 3 поступательные и 2 вращательные, твердое тело имеет 6 степеней свободы (x, y, z, a, b, ), т. е. 3 поступательные и 3 вращательные. С учетом этого для одноатомных молекул газа (He, Ne, Ar) i = 3, для двухатомных молекул газа (H 2, O 2, N 2) с жесткой связью атомов i=5, для трех- и более атомных молекул газа с жесткой связью атомов (CO 2, NH 3) i = 6. Если жесткой связи между атомами не существует - атомы могут совершать колебания - полное число степеней свободы i = iпост+ 2 iколеб. В классической теории рассматривают молекулы с жесткой связью атомов, для них iколеб. = 0. Итак, независимо от числа степеней свободы молекул три степени свободы всегда поступательные. Ни одна из них не имеет преимущества перед другими, поэтому на каждую из них приходится в среднем одинаковая энергия, равная <⅓Ek> = ½k. T. Важнейший закон классической статистической физики - закон равномерного распределения энергии по степеням свободы - утверждает: на каждую степень свободы молекулы в среднем приходится одинаковая кинетическая энергия, равная ½k. Т. Следовательно, средняя кинетическая энергия молекулы, имеющей i степеней свободы,
 Внутренняя энергия идеального газа Так как в идеальном газе взаимная потенциальная энергия молекул равна нулю (т. е. молекулы между собой не взаимодействуют), то внутренняя энергия U представляет собой кинетическую энергию его молекул. Для одного моля U =
Внутренняя энергия идеального газа Так как в идеальном газе взаимная потенциальная энергия молекул равна нулю (т. е. молекулы между собой не взаимодействуют), то внутренняя энергия U представляет собой кинетическую энергию его молекул. Для одного моля U =
 Работа и теплота Рассмотрим термодинамическую систему, для которой механическая энергия не изменяется, а изменяется лишь ее внутренняя энергия. Внутренняя энергия закрытой системы (т. е. системы, которая не обменивается веществом с внешней средой) может изменяться качественно различными способами: 1. Путем совершения работы внешними телами над системой, например, при сжатии газа температура его повышается и, следовательно, изменяется (увеличивается) его внутренняя энергия. 2. Путем теплообмена, т. е. процесса обмена внутренними энергиями при контакте тел с различными температурами. Энергию, передаваемую от одних тел к другим в процессе теплообмена, называют теплотой. Таким образом, можно говорить о двух формах передачи энергии от одних тел к другим: работе и теплоте. Энергия механического движения может превращаться в энергию теплового движения и наоборот. При этих превращениях соблюдается закон сохранения и превращения энергии. Применительно к термодинамическим процессам этим законом и является первое начало термодинамики, установленное в результате обобщения многовековых опытных данных.
Работа и теплота Рассмотрим термодинамическую систему, для которой механическая энергия не изменяется, а изменяется лишь ее внутренняя энергия. Внутренняя энергия закрытой системы (т. е. системы, которая не обменивается веществом с внешней средой) может изменяться качественно различными способами: 1. Путем совершения работы внешними телами над системой, например, при сжатии газа температура его повышается и, следовательно, изменяется (увеличивается) его внутренняя энергия. 2. Путем теплообмена, т. е. процесса обмена внутренними энергиями при контакте тел с различными температурами. Энергию, передаваемую от одних тел к другим в процессе теплообмена, называют теплотой. Таким образом, можно говорить о двух формах передачи энергии от одних тел к другим: работе и теплоте. Энергия механического движения может превращаться в энергию теплового движения и наоборот. При этих превращениях соблюдается закон сохранения и превращения энергии. Применительно к термодинамическим процессам этим законом и является первое начало термодинамики, установленное в результате обобщения многовековых опытных данных.
 Работа газа при изменении его объема Найдем работу, совершаемую газом при изменении его объема: δA = F∙dl = p∙S∙dl = p∙d. V , где S - площадь поршня, S∙dl = d. V - изменение объема газа. Следовательно, δA = p∙d. V. Полная работа при расширении газа от объема V 1 до объема V 2 равна A = ∫p∙d. V. Графически она равна площади фигуры, лежащей под кривой p - V. Таким образом, работа не определяется только начальным и конечным состояниями газа, а зависит от всего хода процесса. Криволинейный интеграл зависит от пути интегрирования и поэтому подынтегральное выражение не является полным дифференциалом какой-либо функции состояния газа.
Работа газа при изменении его объема Найдем работу, совершаемую газом при изменении его объема: δA = F∙dl = p∙S∙dl = p∙d. V , где S - площадь поршня, S∙dl = d. V - изменение объема газа. Следовательно, δA = p∙d. V. Полная работа при расширении газа от объема V 1 до объема V 2 равна A = ∫p∙d. V. Графически она равна площади фигуры, лежащей под кривой p - V. Таким образом, работа не определяется только начальным и конечным состояниями газа, а зависит от всего хода процесса. Криволинейный интеграл зависит от пути интегрирования и поэтому подынтегральное выражение не является полным дифференциалом какой-либо функции состояния газа.
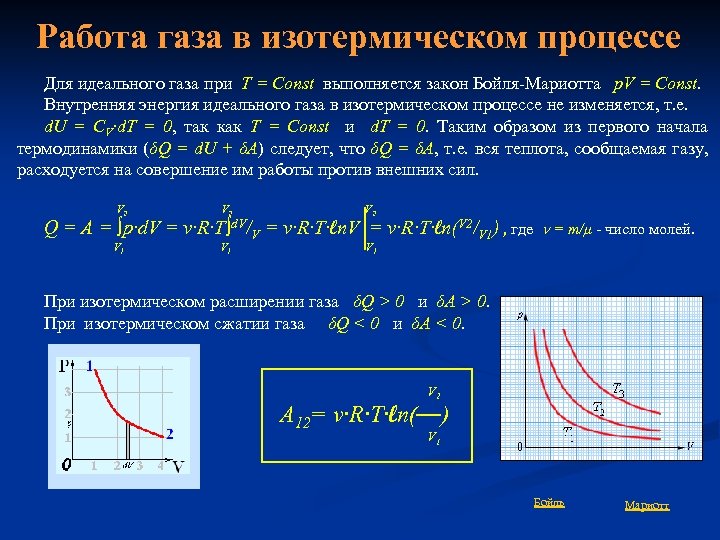 Работа газа в изотермическом процессе Для идеального газа при Т = Const выполняется закон Бойля-Мариотта p. V = Const. Внутренняя энергия идеального газа в изотермическом процессе не изменяется, т. е. d. U = CV∙d. T = 0, так как Т = Const и d. T = 0. Таким образом из первого начала термодинамики (δQ = d. U + δA) следует, что δQ = δA, т. е. вся теплота, сообщаемая газу, расходуется на совершение им работы против внешних сил. V 2 V 2 Q = A = ∫p∙d. V = ν∙R∙T∫d. V/V = ν∙R∙T∙ln(V 2/V 1) , где = m/μ - число молей. V 1 V 1 При изотермическом расширении газа δQ > 0 и δA > 0. При изотермическом сжатии газа δQ < 0 и δA < 0. V 2 А 12= ν∙R∙T∙ln( ) V 1 Бойль Мариотт
Работа газа в изотермическом процессе Для идеального газа при Т = Const выполняется закон Бойля-Мариотта p. V = Const. Внутренняя энергия идеального газа в изотермическом процессе не изменяется, т. е. d. U = CV∙d. T = 0, так как Т = Const и d. T = 0. Таким образом из первого начала термодинамики (δQ = d. U + δA) следует, что δQ = δA, т. е. вся теплота, сообщаемая газу, расходуется на совершение им работы против внешних сил. V 2 V 2 Q = A = ∫p∙d. V = ν∙R∙T∫d. V/V = ν∙R∙T∙ln(V 2/V 1) , где = m/μ - число молей. V 1 V 1 При изотермическом расширении газа δQ > 0 и δA > 0. При изотермическом сжатии газа δQ < 0 и δA < 0. V 2 А 12= ν∙R∙T∙ln( ) V 1 Бойль Мариотт
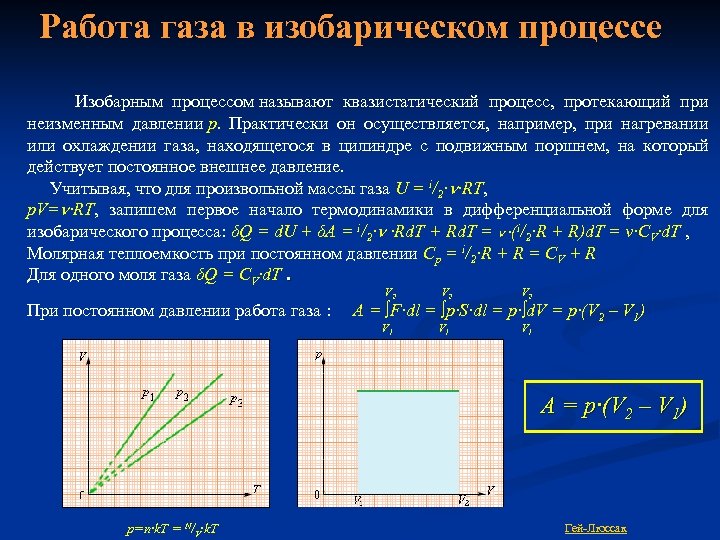 Работа газа в изобарическом процессе Изобарным процессом называют квазистатический процесс, протекающий при неизменным давлении p. Практически он осуществляется, например, при нагревании или охлаждении газа, находящегося в цилиндре с подвижным поршнем, на который действует постоянное внешнее давление. Учитывая, что для произвольной массы газа U = i/2∙ ∙RT, p. V= ∙RT, запишем первое начало термодинамики в дифференциальной форме для изобарического процесса: δQ = d. U + δA = i/2∙ ∙Rd. T + Rd. T = ∙(i/2∙R + R)d. T = ν∙CV∙d. T , Молярная теплоемкость при постоянном давлении Cp = i/2∙R + R = CV + R Для одного моля газа δQ = CV∙d. T. V 2 V 2 При постоянном давлении работа газа : А = ∫F∙dl = ∫p∙S∙dl = p∙∫d. V = p∙(V 2 – V 1) V 1 V 1 A = p∙(V 2 – V 1) p=n∙k. T = N/V∙k. T Гей-Люссак
Работа газа в изобарическом процессе Изобарным процессом называют квазистатический процесс, протекающий при неизменным давлении p. Практически он осуществляется, например, при нагревании или охлаждении газа, находящегося в цилиндре с подвижным поршнем, на который действует постоянное внешнее давление. Учитывая, что для произвольной массы газа U = i/2∙ ∙RT, p. V= ∙RT, запишем первое начало термодинамики в дифференциальной форме для изобарического процесса: δQ = d. U + δA = i/2∙ ∙Rd. T + Rd. T = ∙(i/2∙R + R)d. T = ν∙CV∙d. T , Молярная теплоемкость при постоянном давлении Cp = i/2∙R + R = CV + R Для одного моля газа δQ = CV∙d. T. V 2 V 2 При постоянном давлении работа газа : А = ∫F∙dl = ∫p∙S∙dl = p∙∫d. V = p∙(V 2 – V 1) V 1 V 1 A = p∙(V 2 – V 1) p=n∙k. T = N/V∙k. T Гей-Люссак
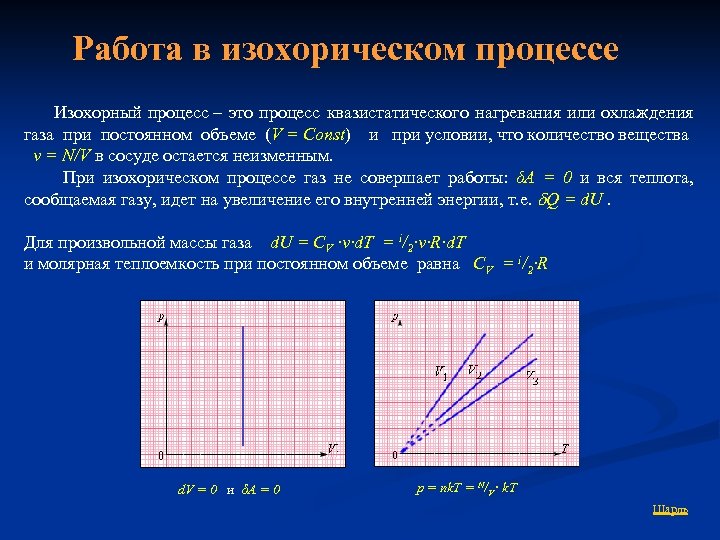 Работа в изохорическом процессе Изохорный процесс – это процесс квазистатического нагревания или охлаждения газа при постоянном объеме (V = Const) и при условии, что количество вещества ν = N/V в сосуде остается неизменным. При изохорическом процессе газ не совершает работы: δA = 0 и вся теплота, сообщаемая газу, идет на увеличение его внутренней энергии, т. е. Q = d. U. Для произвольной массы газа d. U = CV ∙ν∙d. T = i/2∙ν∙R∙d. T и молярная теплоемкость при постоянном объеме равна CV = i/2∙R d. V = 0 и δA = 0 p = nk. T = N/V ∙ k. T Шарль
Работа в изохорическом процессе Изохорный процесс – это процесс квазистатического нагревания или охлаждения газа при постоянном объеме (V = Const) и при условии, что количество вещества ν = N/V в сосуде остается неизменным. При изохорическом процессе газ не совершает работы: δA = 0 и вся теплота, сообщаемая газу, идет на увеличение его внутренней энергии, т. е. Q = d. U. Для произвольной массы газа d. U = CV ∙ν∙d. T = i/2∙ν∙R∙d. T и молярная теплоемкость при постоянном объеме равна CV = i/2∙R d. V = 0 и δA = 0 p = nk. T = N/V ∙ k. T Шарль
 Работа газа в изопроцессах Работа при расширении газа при постоянном давлении от объема V 1 до объема V 2 равна A = p∙∆V = p∙(V 2 – V 1)
Работа газа в изопроцессах Работа при расширении газа при постоянном давлении от объема V 1 до объема V 2 равна A = p∙∆V = p∙(V 2 – V 1)
 Теплоемкости газа Количество тепла, необходимое для нагревания тела рассчитывается по формуле : Q = c∙m∙(T 2 -T 1) = c∙m∙ΔT , где с = Q/m∙ΔT - удельная теплоемкость вещества - величина, равная количеству теплоты, необходимому для нагревания 1 кг вещества на 1 К, m – масса тела, ΔТ = Т 2 - Т 1 – разность температур. В общем случае Q = C∙ ∙ T , где C = μ∙c - молярная теплоемкость, величина, равная количеству теплоты, необходимому для нагревания 1 моля вещества на 1 К , а = m/μ - количество молей вещества. Для равновесных процессов δQ = C∙ν∙d. T
Теплоемкости газа Количество тепла, необходимое для нагревания тела рассчитывается по формуле : Q = c∙m∙(T 2 -T 1) = c∙m∙ΔT , где с = Q/m∙ΔT - удельная теплоемкость вещества - величина, равная количеству теплоты, необходимому для нагревания 1 кг вещества на 1 К, m – масса тела, ΔТ = Т 2 - Т 1 – разность температур. В общем случае Q = C∙ ∙ T , где C = μ∙c - молярная теплоемкость, величина, равная количеству теплоты, необходимому для нагревания 1 моля вещества на 1 К , а = m/μ - количество молей вещества. Для равновесных процессов δQ = C∙ν∙d. T
 Уравнение Майера Внутренняя энергия одного моля идеального газа равна сумме кинетических энергий всех его молекул: U = NA. i/2. mυ2 = NA. 3/2. k. T = i/2. νNAk. T = i/2. νRT и d. U = i/2. νRd. T При малом изменении объема (когда давление можно считать постоянным) работа, совершаемая газом, равна d. A = pd. V. Если p. V = νRT , то d. A = pd. V = νRd. T. Запишем первое начало термодинамики для одного моля газа: d. Q = Cd. T = d. U + d. A = i/2. Rd. T + Rd. T , где C = i/2. R + R (С –молярная теплоемкость газа) Если V = Const , то газ не совершает работу, поскольку d. A = pd. V = 0. Следовательно, при постоянном объеме CV = i/2. R. При постоянном давлении Cp = i/2. R + R = CV + R. Выражение Cp = CV + R называется уравнением Майера. CP всегда больше CV на величину универсальной газовой постоянной R. Это объясняется тем, что для нагревания газа при постоянном давлении требуется еще дополнительное количество теплоты на совершение работы расширения газа. Физический смысл универсальной газовой постоянной R : она численно равна работе, совершаемой одним молем идеального газа при его изобарическом нагревании на 1 К.
Уравнение Майера Внутренняя энергия одного моля идеального газа равна сумме кинетических энергий всех его молекул: U = NA. i/2. mυ2 = NA. 3/2. k. T = i/2. νNAk. T = i/2. νRT и d. U = i/2. νRd. T При малом изменении объема (когда давление можно считать постоянным) работа, совершаемая газом, равна d. A = pd. V. Если p. V = νRT , то d. A = pd. V = νRd. T. Запишем первое начало термодинамики для одного моля газа: d. Q = Cd. T = d. U + d. A = i/2. Rd. T + Rd. T , где C = i/2. R + R (С –молярная теплоемкость газа) Если V = Const , то газ не совершает работу, поскольку d. A = pd. V = 0. Следовательно, при постоянном объеме CV = i/2. R. При постоянном давлении Cp = i/2. R + R = CV + R. Выражение Cp = CV + R называется уравнением Майера. CP всегда больше CV на величину универсальной газовой постоянной R. Это объясняется тем, что для нагревания газа при постоянном давлении требуется еще дополнительное количество теплоты на совершение работы расширения газа. Физический смысл универсальной газовой постоянной R : она численно равна работе, совершаемой одним молем идеального газа при его изобарическом нагревании на 1 К.
 Первое начало термодинамики Допустим, что некоторая термодинамическая система (например, газ, заключенный в цилиндр под поршнем), обладая внутренней энергией U 1, получила некоторое количество теплоты ΔQ, перейдя в новое состояние, характеризующееся внутренней энергией U 2 , и кроме того, совершила работу А над внешней средой, т. е. против внешних сил. В этом случае ΔQ = U 2 - U 1 + A или ΔQ = ΔU + A . Уравнение выражает первое начало термодинамики: теплота, сообщаемая системе, расходуется на изменение ее внутренней энергии и на совершение ею работы против внешних сил. Для бесконечно малых процессов выражение это записывают в дифференциальной форме d. Q = d. U + d. A или в более корректной форме поскольку только d. U является полным дифференциалом, а d. Q и d. А полными дифференциалами не являются. В системе СИ количество теплоты выражается в тех же единицах, что работа и энергия, т. е. в Джоулях (Дж). Если система возвращается в первоначальное состояние, то изменение ее внутренней энергии d. U = 0. Тогда А = Q , т. е. вечный двигатель первого рода, который совершал бы большую работу, чем сообщенная ему извне энергия, невозможен. Это одна из формулировок первого начала термодинамики.
Первое начало термодинамики Допустим, что некоторая термодинамическая система (например, газ, заключенный в цилиндр под поршнем), обладая внутренней энергией U 1, получила некоторое количество теплоты ΔQ, перейдя в новое состояние, характеризующееся внутренней энергией U 2 , и кроме того, совершила работу А над внешней средой, т. е. против внешних сил. В этом случае ΔQ = U 2 - U 1 + A или ΔQ = ΔU + A . Уравнение выражает первое начало термодинамики: теплота, сообщаемая системе, расходуется на изменение ее внутренней энергии и на совершение ею работы против внешних сил. Для бесконечно малых процессов выражение это записывают в дифференциальной форме d. Q = d. U + d. A или в более корректной форме поскольку только d. U является полным дифференциалом, а d. Q и d. А полными дифференциалами не являются. В системе СИ количество теплоты выражается в тех же единицах, что работа и энергия, т. е. в Джоулях (Дж). Если система возвращается в первоначальное состояние, то изменение ее внутренней энергии d. U = 0. Тогда А = Q , т. е. вечный двигатель первого рода, который совершал бы большую работу, чем сообщенная ему извне энергия, невозможен. Это одна из формулировок первого начала термодинамики.
 Адиабатический процесс Это процесс, при котором отсутствует теплообмен (δQ=0) между системой и окружающей средой. К адиабатическим можно отнести все быстропротекающие процессы. Первое начало термодинамики для него имеет вид: d. U+δA = 0 или d. A = -δU , т. е. внешняя работа совершается за счет уменьшения внутренней энергии системы. pd. V = i/2∙ ∙Rd. T = - CV ∙ν∙d. T или для одного моля газа pd. V + CV∙d. T = 0. = Работа адиабатического расширения газа от объема V 1 до V 2 ( при этом температура газа уменьшается от Т 1 до Т 2) равна : T 1 A = ∫ i/ T 2 ∙Rd. T = i/2∙ ∙R∙(T 1 – T 2) = i/2∙ ∙RT 1 - i/2∙ ∙RT 2 = i/2∙ (p. V 2 - p. V 1 ) 2∙ Дифференцируя уравнение Клапейрона – Менделеева p∙V = R∙T , получаем : p∙d. V+V∙dp = R∙d. T и d. T = (p∙d. V + V∙dp)/R. Запишем первое начало термодинамики для адиабатического процесса (pd. V+CV∙d. T = 0 ) : p∙d. V + CV ∙(p∙d. V + V∙dp)/R = 0 или R/CV ∙p∙d. V+ p∙d. V + V∙dp = 0 ; (R/CV +1)∙p∙d. V + V∙dp = 0 = = Разделим уравнение на p. V и получим : (R/CV + 1)∙d. V/V + dp/p = 0. = Обозначим R/CV + 1 = (CV + R)/CV = CP/CV = γ. Тогда γ∙ℓn(V) + ℓn(p) = 0 . γ Интегрируя, имеем: p∙V = Const - уравнение Пуассона. Здесь γ = Cp/CV – отношение молярных теплоемкостей при постоянном давлении и при постоянном объеме. γ = (i+2)/i - показатель адиабаты (коэффициент Пуассона), i - число степеней свободы молекулы газа. Так как >1, то адиабата идет круче, чем изотерма, уравнение которой p∙V = Const.
Адиабатический процесс Это процесс, при котором отсутствует теплообмен (δQ=0) между системой и окружающей средой. К адиабатическим можно отнести все быстропротекающие процессы. Первое начало термодинамики для него имеет вид: d. U+δA = 0 или d. A = -δU , т. е. внешняя работа совершается за счет уменьшения внутренней энергии системы. pd. V = i/2∙ ∙Rd. T = - CV ∙ν∙d. T или для одного моля газа pd. V + CV∙d. T = 0. = Работа адиабатического расширения газа от объема V 1 до V 2 ( при этом температура газа уменьшается от Т 1 до Т 2) равна : T 1 A = ∫ i/ T 2 ∙Rd. T = i/2∙ ∙R∙(T 1 – T 2) = i/2∙ ∙RT 1 - i/2∙ ∙RT 2 = i/2∙ (p. V 2 - p. V 1 ) 2∙ Дифференцируя уравнение Клапейрона – Менделеева p∙V = R∙T , получаем : p∙d. V+V∙dp = R∙d. T и d. T = (p∙d. V + V∙dp)/R. Запишем первое начало термодинамики для адиабатического процесса (pd. V+CV∙d. T = 0 ) : p∙d. V + CV ∙(p∙d. V + V∙dp)/R = 0 или R/CV ∙p∙d. V+ p∙d. V + V∙dp = 0 ; (R/CV +1)∙p∙d. V + V∙dp = 0 = = Разделим уравнение на p. V и получим : (R/CV + 1)∙d. V/V + dp/p = 0. = Обозначим R/CV + 1 = (CV + R)/CV = CP/CV = γ. Тогда γ∙ℓn(V) + ℓn(p) = 0 . γ Интегрируя, имеем: p∙V = Const - уравнение Пуассона. Здесь γ = Cp/CV – отношение молярных теплоемкостей при постоянном давлении и при постоянном объеме. γ = (i+2)/i - показатель адиабаты (коэффициент Пуассона), i - число степеней свободы молекулы газа. Так как >1, то адиабата идет круче, чем изотерма, уравнение которой p∙V = Const.
 Адиабатический процесс Это процесс, при котором отсутствует теплообмен между системой и окружающей средой (d. Q = 0). К адиабатическим можно отнести все быстропротекающие процессы. Из первого начала термодинамики (d. Q = d. U + d. A) для адиабатического процесса следует, что d. A = – d. U , т. е. внешняя работа совершается за счет уменьшения внутренней энергии системы. Учитывая, что d. U = νCv. d. T и d. A = pd. V , первое начало термодинамики для адиабатического процесса имеет вид : pd. V = –νCv. d. T. (1) Из уравнения Менделеева-Клапейрона p. V = νR. T после дифференцирования имеем: pd. V + Vdp = νR. d. T откуда pd. V = νR. d. T – Vdp. Подставим это значение в (1) : νR. d. T – Vdp = –νCv. d. T или ν(R+Cv). d. T = Vdp , где R+Cv = Cp (из уравнения Майера R = Cp – Cv ). Учитывая, что V = νR. T/р , получаем дифференциальное уравнение с разделенными переменными νCp. d. T/T = νR. dp/р или d. T/T = R/Cp. dp/р . В этом уравнении R/Cp = (Cp – Cv)/Cp = 1 – 1/γ = (γ– 1)/γ . Здесь γ = Cp/Cv – отношение молярных теплоемкостей при постоянном давлении и при постоянном объеме. Интегрирование уравнения d. T/T = (γ– 1)/γ. dp/р дает ln(T) = (γ– 1)/γ. ln(p) + Const. После потенцирования получаем зависимость температуры и давления в адиабатическом процессе : T/p (γ– 1)/γ = Const.
Адиабатический процесс Это процесс, при котором отсутствует теплообмен между системой и окружающей средой (d. Q = 0). К адиабатическим можно отнести все быстропротекающие процессы. Из первого начала термодинамики (d. Q = d. U + d. A) для адиабатического процесса следует, что d. A = – d. U , т. е. внешняя работа совершается за счет уменьшения внутренней энергии системы. Учитывая, что d. U = νCv. d. T и d. A = pd. V , первое начало термодинамики для адиабатического процесса имеет вид : pd. V = –νCv. d. T. (1) Из уравнения Менделеева-Клапейрона p. V = νR. T после дифференцирования имеем: pd. V + Vdp = νR. d. T откуда pd. V = νR. d. T – Vdp. Подставим это значение в (1) : νR. d. T – Vdp = –νCv. d. T или ν(R+Cv). d. T = Vdp , где R+Cv = Cp (из уравнения Майера R = Cp – Cv ). Учитывая, что V = νR. T/р , получаем дифференциальное уравнение с разделенными переменными νCp. d. T/T = νR. dp/р или d. T/T = R/Cp. dp/р . В этом уравнении R/Cp = (Cp – Cv)/Cp = 1 – 1/γ = (γ– 1)/γ . Здесь γ = Cp/Cv – отношение молярных теплоемкостей при постоянном давлении и при постоянном объеме. Интегрирование уравнения d. T/T = (γ– 1)/γ. dp/р дает ln(T) = (γ– 1)/γ. ln(p) + Const. После потенцирования получаем зависимость температуры и давления в адиабатическом процессе : T/p (γ– 1)/γ = Const.

 Работа в циклических процессах Общее свойство всех круговых процессов состоит в том, что их невозможно провести, приводя рабочее тело в тепловой контакт только с одним тепловым резервуаром. Их нужно, по крайней мере, два: с более высокой температурой нагреватель (1) и холодильник (2) – с более низкой. Совершая круговой процесс, рабочее тело получает от нагревателя некоторое количество теплоты Q 1 > 0 и отдает холодильнику количество теплоты Q 2 < 0. Полное количество теплоты Q, полученное рабочим телом за цикл, равно Q = Q 1 + Q 2 = Q 1 – |Q 2|. При обходе цикла рабочее тело возвращается в первоначальное состояние, следовательно, изменение его внутренней энергии равно нулю (ΔU = 0). Согласно первому закону термодинамики, ΔU = Q – A = 0. Отсюда следует: A = Q 1 – |Q 2|. Работа A, совершаемая рабочим телом за цикл, равна полученному за цикл количеству теплоты Q. Отношение работы A к количеству теплоты Q 1, полученному рабочим телом за цикл от нагревателя, называется коэффициентом полезного действия η тепловой машины: Коэффициент полезного действия указывает, какая часть тепловой энергии, полученной рабочим телом от «горячего» теплового резервуара, превратилась в полезную работу. Остальная часть (1 – η) была «бесполезно» передана холодильнику. Коэффициент полезного действия тепловой машины всегда меньше единицы (η < 1). В применяемых в технике двигателях используются различные круговые процессы. На рисунке изображены циклы, используемые в бензиновом карбюраторном двигателе (1) и в дизельном двигателе (2). В обоих случаях рабочим телом является смесь паров бензина или дизельного топлива с воздухом. Цикл карбюраторного двигателя внутреннего сгорания состоит из двух изохор (1– 2, 3– 4) и двух адиабат (2– 3, 4– 1). Дизельный двигатель внутреннего сгорания работает по циклу, состоящему из двух адиабат (1– 2, 3– 4), одной изобары (2– 3) и одной изохоры (4– 1). Реальный коэффициент полезного действия у карбюраторного двигателя порядка 30%, у дизельного двигателя – порядка 40 %.
Работа в циклических процессах Общее свойство всех круговых процессов состоит в том, что их невозможно провести, приводя рабочее тело в тепловой контакт только с одним тепловым резервуаром. Их нужно, по крайней мере, два: с более высокой температурой нагреватель (1) и холодильник (2) – с более низкой. Совершая круговой процесс, рабочее тело получает от нагревателя некоторое количество теплоты Q 1 > 0 и отдает холодильнику количество теплоты Q 2 < 0. Полное количество теплоты Q, полученное рабочим телом за цикл, равно Q = Q 1 + Q 2 = Q 1 – |Q 2|. При обходе цикла рабочее тело возвращается в первоначальное состояние, следовательно, изменение его внутренней энергии равно нулю (ΔU = 0). Согласно первому закону термодинамики, ΔU = Q – A = 0. Отсюда следует: A = Q 1 – |Q 2|. Работа A, совершаемая рабочим телом за цикл, равна полученному за цикл количеству теплоты Q. Отношение работы A к количеству теплоты Q 1, полученному рабочим телом за цикл от нагревателя, называется коэффициентом полезного действия η тепловой машины: Коэффициент полезного действия указывает, какая часть тепловой энергии, полученной рабочим телом от «горячего» теплового резервуара, превратилась в полезную работу. Остальная часть (1 – η) была «бесполезно» передана холодильнику. Коэффициент полезного действия тепловой машины всегда меньше единицы (η < 1). В применяемых в технике двигателях используются различные круговые процессы. На рисунке изображены циклы, используемые в бензиновом карбюраторном двигателе (1) и в дизельном двигателе (2). В обоих случаях рабочим телом является смесь паров бензина или дизельного топлива с воздухом. Цикл карбюраторного двигателя внутреннего сгорания состоит из двух изохор (1– 2, 3– 4) и двух адиабат (2– 3, 4– 1). Дизельный двигатель внутреннего сгорания работает по циклу, состоящему из двух адиабат (1– 2, 3– 4), одной изобары (2– 3) и одной изохоры (4– 1). Реальный коэффициент полезного действия у карбюраторного двигателя порядка 30%, у дизельного двигателя – порядка 40 %.
 Тепловые двигатели Тепловым двигателем называется устройство, способное превращать полученное количество теплоты в механическую работу. Механическая работа в тепловых двигателях производится в процессе расширения некоторого вещества, которое называется рабочим телом. В качестве рабочего тела обычно используются газообразные вещества (пары бензина, воздух, водяной пар). Рабочее тело получает (или отдает) тепловую энергию в процессе теплообмена с телами, имеющими большой запас внутренней энергии. Эти тела называются тепловыми резервуарами Как следует из первого закона термодинамики, полученное газом количество теплоты Q полностью превращается в работу A при изотермическом процессе, когда внутренняя энергия остается неизменной (ΔU = 0): A = Q. Но такой однократный акт преобразования теплоты в работу не представляет интереса для техники. Реально существующие тепловые двигатели (паровые машины, двигатели внутреннего сгорания и т. д. ) работают циклически. Процесс теплопередачи и преобразования полученного количества теплоты в работу периодически повторяется. Для этого рабочее тело должно совершать круговой процесс или термодинамический цикл, при котором периодически восстанавливается исходное состояние. Такие процессы изображаются на диаграмме (p, V) газообразного рабочего тела с помощью замкнутых кривых как показано на рисунке. При расширении газ совершает положительную работу A 1, равную площади под кривой abc, при сжатии газ совершает отрицательную работу A 2, равную по модулю площади под кривой cda. Полная работа за цикл A = A 1 + A 2 на диаграмме (p, V) равна площади цикла abcd. Работа A положительна, если цикл обходится по часовой стрелке, и A отрицательна, если цикл обходится в противоположном направлении.
Тепловые двигатели Тепловым двигателем называется устройство, способное превращать полученное количество теплоты в механическую работу. Механическая работа в тепловых двигателях производится в процессе расширения некоторого вещества, которое называется рабочим телом. В качестве рабочего тела обычно используются газообразные вещества (пары бензина, воздух, водяной пар). Рабочее тело получает (или отдает) тепловую энергию в процессе теплообмена с телами, имеющими большой запас внутренней энергии. Эти тела называются тепловыми резервуарами Как следует из первого закона термодинамики, полученное газом количество теплоты Q полностью превращается в работу A при изотермическом процессе, когда внутренняя энергия остается неизменной (ΔU = 0): A = Q. Но такой однократный акт преобразования теплоты в работу не представляет интереса для техники. Реально существующие тепловые двигатели (паровые машины, двигатели внутреннего сгорания и т. д. ) работают циклически. Процесс теплопередачи и преобразования полученного количества теплоты в работу периодически повторяется. Для этого рабочее тело должно совершать круговой процесс или термодинамический цикл, при котором периодически восстанавливается исходное состояние. Такие процессы изображаются на диаграмме (p, V) газообразного рабочего тела с помощью замкнутых кривых как показано на рисунке. При расширении газ совершает положительную работу A 1, равную площади под кривой abc, при сжатии газ совершает отрицательную работу A 2, равную по модулю площади под кривой cda. Полная работа за цикл A = A 1 + A 2 на диаграмме (p, V) равна площади цикла abcd. Работа A положительна, если цикл обходится по часовой стрелке, и A отрицательна, если цикл обходится в противоположном направлении.
 Цикл Карно При работе тепловой машины рабочее тело совершает замкнутый термодинамический цикл. Для любой реальной тепловой машины весь цикл, включая его отдельные процессы, необратим, что вызывает необходимость затрачивать часть произведенной работы для перевода рабочего тела в первоначальное состояние, обеспечивая замыкание кругового процесса. Указанные потери приводят к тому, что не вся произведенная работа становится полезной, а часть её теряется в самой тепловой машине, переходя в теплоту. Максимальным к. п. д. обладает тепловая машина, в которой цикл рабочего тела состоит только из равновесных тепловых процессов, и, следовательно, является обратимым. Однако для осуществления нагревания и охлаждения необходим теплообмен рабочего тела с нагревателем и холодильником тепловой машины, который тем более эффективен, чем заметнее разность температур. Возникающие при этом тепловые потоки нарушают состояние теплового равновесия и делают эти процессы необратимыми. Чтобы избежать этого, необходимо теплообмен осуществлять при очень малой разности температур, в пределе, для достижения равновесного процесса, при бесконечно малой разности. Теплообмен с нагревателем и холодильником в рассматриваемой тепловой машине должен происходить при изотермических процессах, что эквивалентно требованию бесконечной медленности протекания этих процессов. Очевидно, что такое условие может быть выполнено только приближенно. Другой процесс, который может протекать без возникновения тепловых потоков - это адиабатический процесс. Если он протекает бесконечно медленно, то такой процесс является равновесным и обратимым. Указанные два равновесных процесса (изотермический и адиабатический) использованы для составления обратимого цикла. Возможность осуществления такого циклического процесса связана с тем, что с помощью адиабатического процесса всегда возможен переход между любыми изотермами, а с помощью изотермического - между любыми адиабатами.
Цикл Карно При работе тепловой машины рабочее тело совершает замкнутый термодинамический цикл. Для любой реальной тепловой машины весь цикл, включая его отдельные процессы, необратим, что вызывает необходимость затрачивать часть произведенной работы для перевода рабочего тела в первоначальное состояние, обеспечивая замыкание кругового процесса. Указанные потери приводят к тому, что не вся произведенная работа становится полезной, а часть её теряется в самой тепловой машине, переходя в теплоту. Максимальным к. п. д. обладает тепловая машина, в которой цикл рабочего тела состоит только из равновесных тепловых процессов, и, следовательно, является обратимым. Однако для осуществления нагревания и охлаждения необходим теплообмен рабочего тела с нагревателем и холодильником тепловой машины, который тем более эффективен, чем заметнее разность температур. Возникающие при этом тепловые потоки нарушают состояние теплового равновесия и делают эти процессы необратимыми. Чтобы избежать этого, необходимо теплообмен осуществлять при очень малой разности температур, в пределе, для достижения равновесного процесса, при бесконечно малой разности. Теплообмен с нагревателем и холодильником в рассматриваемой тепловой машине должен происходить при изотермических процессах, что эквивалентно требованию бесконечной медленности протекания этих процессов. Очевидно, что такое условие может быть выполнено только приближенно. Другой процесс, который может протекать без возникновения тепловых потоков - это адиабатический процесс. Если он протекает бесконечно медленно, то такой процесс является равновесным и обратимым. Указанные два равновесных процесса (изотермический и адиабатический) использованы для составления обратимого цикла. Возможность осуществления такого циклического процесса связана с тем, что с помощью адиабатического процесса всегда возможен переход между любыми изотермами, а с помощью изотермического - между любыми адиабатами.
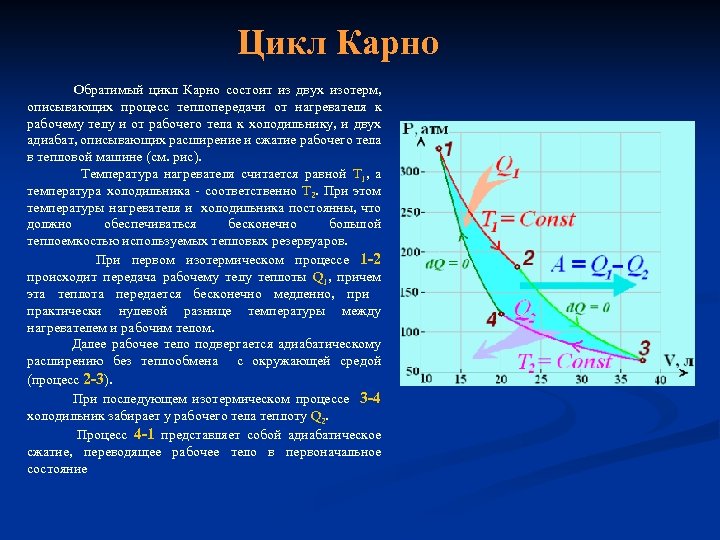 Цикл Карно Обратимый цикл Карно состоит из двух изотерм, описывающих процесс теплопередачи от нагревателя к рабочему телу и от рабочего тела к холодильнику, и двух адиабат, описывающих расширение и сжатие рабочего тела в тепловой машине (см. рис). Температура нагревателя считается равной T 1, а температура холодильника - соответственно T 2. При этом температуры нагревателя и холодильника постоянны, что должно обеспечиваться бесконечно большой теплоемкостью используемых тепловых резервуаров. При первом изотермическом процессе 1 -2 происходит передача рабочему телу теплоты Q 1, причем эта теплота передается бесконечно медленно, при практически нулевой разнице температуры между нагревателем и рабочим телом. Далее рабочее тело подвергается адиабатическому расширению без теплообмена с окружающей средой (процесс 2 -3). При последующем изотермическом процессе 3 -4 холодильник забирает у рабочего тела теплоту Q 2. Процесс 4 -1 представляет собой адиабатическое сжатие, переводящее рабочее тело в первоначальное состояние
Цикл Карно Обратимый цикл Карно состоит из двух изотерм, описывающих процесс теплопередачи от нагревателя к рабочему телу и от рабочего тела к холодильнику, и двух адиабат, описывающих расширение и сжатие рабочего тела в тепловой машине (см. рис). Температура нагревателя считается равной T 1, а температура холодильника - соответственно T 2. При этом температуры нагревателя и холодильника постоянны, что должно обеспечиваться бесконечно большой теплоемкостью используемых тепловых резервуаров. При первом изотермическом процессе 1 -2 происходит передача рабочему телу теплоты Q 1, причем эта теплота передается бесконечно медленно, при практически нулевой разнице температуры между нагревателем и рабочим телом. Далее рабочее тело подвергается адиабатическому расширению без теплообмена с окружающей средой (процесс 2 -3). При последующем изотермическом процессе 3 -4 холодильник забирает у рабочего тела теплоту Q 2. Процесс 4 -1 представляет собой адиабатическое сжатие, переводящее рабочее тело в первоначальное состояние
 Коэффициент полезного действия цикла Карно Коэффициент полезного действия всегда находится как отношение полезно использованной работы ко всей затраченной энергии проведении цикла. В цикле Карно газ совершает работы А 12 при изотермическом расширении на участке 1 -2 и работу А 23 при адиабатическом расширении на участке 2 -3. При изотермическом сжатии на участке 3 -4 работу А 34 над газом совершают внешние силы, также как и работу А 41 при адиабатическом сжатии на участке 4 -1. Таким образом полная работа газа равна : А = А 12 +А 23 + А 34 + А 41. В изотермических процессах А 12 = RT 1 ln. V 2/V 1 и А 34 = RT 2 ln. V 4/V 3 (d. U=0). В адиабатических процессах А 23 = ½∙i∙R∙(Т 2 – Т 1) , А 41 = ½∙i∙R∙(Т 1 – Т 2) и А 23 = -А 41 (d. Q=0). Газ получает энергию только на участке 1 -2 в изотермическом процессе Q 1 = RT 1 ln. V 2/V 1. η = А/Q 1 = (А 12 +А 23 + А 34 + А 41)/Q 1 = [RT 1 ln(V 2/V 1) + RT 2 ln(V 4/V 3)]/ RT 1 ln. V 2/V 1. Запишем законы адиабатических процессов 2 -3: Т 1 V 2γ-1=Т 2 V 3γ-1 и 4 -1: Т 1 V 1γ-1=Т 2 V 4γ-1. Разделив эти соотношения друг на друга, получаем: Т 1 V 2γ-1/T 1 V 1γ-1 = T 2 V 3γ-1/T 2 V 4γ-1 . После сокращений и возведения в степень γ-1 получим V 2/V 1 = V 3/V 4 . Учтем, что ln(V 3/V 4) = - ln(V 4/V 3). Тогда η = [T 1 ln(V 2/V 1) - T 2 ln(V 2/V 1)]/ T 1 ln(V 2/V 1) = (Т 1 – Т 2)/Т 1. Кроме того, с учетом закона сохранения и превращения энергии η = A/Q 1 = (Q 1– Q 2)Q 1. Т 1 -Т 2 Q 1 -Q 2 T 2 Q 2 Окончательно : η = = 1 - = 1 - Т 1 Q 1 T 1 Q 1
Коэффициент полезного действия цикла Карно Коэффициент полезного действия всегда находится как отношение полезно использованной работы ко всей затраченной энергии проведении цикла. В цикле Карно газ совершает работы А 12 при изотермическом расширении на участке 1 -2 и работу А 23 при адиабатическом расширении на участке 2 -3. При изотермическом сжатии на участке 3 -4 работу А 34 над газом совершают внешние силы, также как и работу А 41 при адиабатическом сжатии на участке 4 -1. Таким образом полная работа газа равна : А = А 12 +А 23 + А 34 + А 41. В изотермических процессах А 12 = RT 1 ln. V 2/V 1 и А 34 = RT 2 ln. V 4/V 3 (d. U=0). В адиабатических процессах А 23 = ½∙i∙R∙(Т 2 – Т 1) , А 41 = ½∙i∙R∙(Т 1 – Т 2) и А 23 = -А 41 (d. Q=0). Газ получает энергию только на участке 1 -2 в изотермическом процессе Q 1 = RT 1 ln. V 2/V 1. η = А/Q 1 = (А 12 +А 23 + А 34 + А 41)/Q 1 = [RT 1 ln(V 2/V 1) + RT 2 ln(V 4/V 3)]/ RT 1 ln. V 2/V 1. Запишем законы адиабатических процессов 2 -3: Т 1 V 2γ-1=Т 2 V 3γ-1 и 4 -1: Т 1 V 1γ-1=Т 2 V 4γ-1. Разделив эти соотношения друг на друга, получаем: Т 1 V 2γ-1/T 1 V 1γ-1 = T 2 V 3γ-1/T 2 V 4γ-1 . После сокращений и возведения в степень γ-1 получим V 2/V 1 = V 3/V 4 . Учтем, что ln(V 3/V 4) = - ln(V 4/V 3). Тогда η = [T 1 ln(V 2/V 1) - T 2 ln(V 2/V 1)]/ T 1 ln(V 2/V 1) = (Т 1 – Т 2)/Т 1. Кроме того, с учетом закона сохранения и превращения энергии η = A/Q 1 = (Q 1– Q 2)Q 1. Т 1 -Т 2 Q 1 -Q 2 T 2 Q 2 Окончательно : η = = 1 - = 1 - Т 1 Q 1 T 1 Q 1
 Приведенная теплота и энтропия К макроскопическим параметрам термодинамической системы относятся давление, объём и температура. Однако существует ещё одна важная физическая величина, которую используют для описания состояний и процессов в термодинамических системах. Её называют энтропией. Любой термодинамический процесс, проходящий в системе, состоит из какого-то количества переходов системы из одного состояния в другое. Приведенной теплотой Q' называют отношение количества теплоты в изотермическом процессе Q к температуре T, при которой происходит передача этой теплоты. Q' = Q/T. Для любого незамкнутого термодинамического процесса существует такая функция системы, изменение которой при переходе из одного состояния в другое равно сумме приведенных теплот. Строгий теоретический анализ показывает, что приведенное количество теплоты, сообщаемое телу в любом обратимом круговом процессе, равно нулю. Этой функции Клаузиус дал название «энтропия» и обозначил её буквой S, а отношение общего количества теплоты Q к величине абсолютной температуры Т назвал изменением энтропии. Энтропия есть функция состояния системы, она однозначно характеризует систему и связана (как и все макропараметры) с другими ее характеристиками – давлением, объемом, температурой.
Приведенная теплота и энтропия К макроскопическим параметрам термодинамической системы относятся давление, объём и температура. Однако существует ещё одна важная физическая величина, которую используют для описания состояний и процессов в термодинамических системах. Её называют энтропией. Любой термодинамический процесс, проходящий в системе, состоит из какого-то количества переходов системы из одного состояния в другое. Приведенной теплотой Q' называют отношение количества теплоты в изотермическом процессе Q к температуре T, при которой происходит передача этой теплоты. Q' = Q/T. Для любого незамкнутого термодинамического процесса существует такая функция системы, изменение которой при переходе из одного состояния в другое равно сумме приведенных теплот. Строгий теоретический анализ показывает, что приведенное количество теплоты, сообщаемое телу в любом обратимом круговом процессе, равно нулю. Этой функции Клаузиус дал название «энтропия» и обозначил её буквой S, а отношение общего количества теплоты Q к величине абсолютной температуры Т назвал изменением энтропии. Энтропия есть функция состояния системы, она однозначно характеризует систему и связана (как и все макропараметры) с другими ее характеристиками – давлением, объемом, температурой.
 Энтропия Если в первом начале термодинамики δQ = d. U + d. A заменить d. U = Сvd. T и d. A = рd. V, то с учетом p. V = RT и деления всего уравнения на Т , получим : δQ/T = Cvd. T/Т + Rd. V/V = d. U/T + pd. V/T = d. S. Здесь в правой части имеется полный дифференциал некоторой функции состояния системы, который зависит от изменения всех ее макропараметров, поэтому имеет смысл считать его дифференциалом некоторой функции S , которая также характеризует состояние системы. Эту функцию называют энтропией. После некоторых преобразований ясно, что энтропия возрастает при увеличении температуры и объема : Q/T = d. S = d(Cv. ℓn. Т + R. ℓn. V). Изменение энтропии можно определить как ∆S = ∫d. S , но само значение энтропии в данном состоянии зависит от выбора ее начального значения. Если система совершает циклический процесс и возвращается к первоначальному состоянию, то ∫d. S = 0 , поскольку T 1=Т 2 и V 1=V 2 , и энтропия принимает прежнее значение. Утверждение о существовании энтропии и перечисление её свойств составляют содержание второго и третьего начал термодинамики. Значимость данной величины для физики обусловлена тем, что наряду с температурой её используют для описания термических явлений и термических свойств макроскопических объектов.
Энтропия Если в первом начале термодинамики δQ = d. U + d. A заменить d. U = Сvd. T и d. A = рd. V, то с учетом p. V = RT и деления всего уравнения на Т , получим : δQ/T = Cvd. T/Т + Rd. V/V = d. U/T + pd. V/T = d. S. Здесь в правой части имеется полный дифференциал некоторой функции состояния системы, который зависит от изменения всех ее макропараметров, поэтому имеет смысл считать его дифференциалом некоторой функции S , которая также характеризует состояние системы. Эту функцию называют энтропией. После некоторых преобразований ясно, что энтропия возрастает при увеличении температуры и объема : Q/T = d. S = d(Cv. ℓn. Т + R. ℓn. V). Изменение энтропии можно определить как ∆S = ∫d. S , но само значение энтропии в данном состоянии зависит от выбора ее начального значения. Если система совершает циклический процесс и возвращается к первоначальному состоянию, то ∫d. S = 0 , поскольку T 1=Т 2 и V 1=V 2 , и энтропия принимает прежнее значение. Утверждение о существовании энтропии и перечисление её свойств составляют содержание второго и третьего начал термодинамики. Значимость данной величины для физики обусловлена тем, что наряду с температурой её используют для описания термических явлений и термических свойств макроскопических объектов.
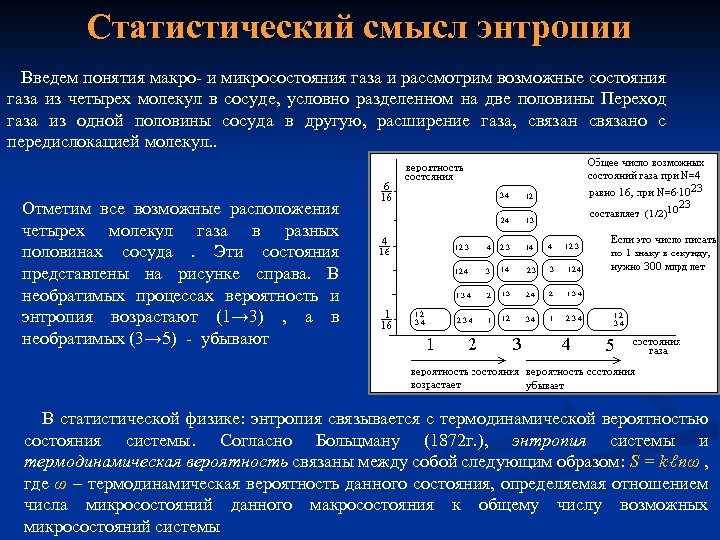 Статистический смысл энтропии Введем понятия макро- и микросостояния газа и рассмотрим возможные состояния газа из четырех молекул в сосуде, условно разделенном на две половины Переход газа из одной половины сосуда в другую, расширение газа, связано с передислокацией молекул. . Отметим все возможные расположения четырех молекул газа в разных половинах сосуда . Эти состояния представлены на рисунке справа. В необратимых процессах вероятность и энтропия возрастают (1→ 3) , а в необратимых (3→ 5) - убывают В статистической физике: энтропия связывается с термодинамической вероятностью состояния системы. Согласно Больцману (1872 г. ), энтропия системы и термодинамическая вероятность связаны между собой следующим образом: S = k. ℓnω , где ω – термодинамическая вероятность данного состояния, определяемая отношением числа микросостояний данного макросостояния к общему числу возможных микросостояний системы
Статистический смысл энтропии Введем понятия макро- и микросостояния газа и рассмотрим возможные состояния газа из четырех молекул в сосуде, условно разделенном на две половины Переход газа из одной половины сосуда в другую, расширение газа, связано с передислокацией молекул. . Отметим все возможные расположения четырех молекул газа в разных половинах сосуда . Эти состояния представлены на рисунке справа. В необратимых процессах вероятность и энтропия возрастают (1→ 3) , а в необратимых (3→ 5) - убывают В статистической физике: энтропия связывается с термодинамической вероятностью состояния системы. Согласно Больцману (1872 г. ), энтропия системы и термодинамическая вероятность связаны между собой следующим образом: S = k. ℓnω , где ω – термодинамическая вероятность данного состояния, определяемая отношением числа микросостояний данного макросостояния к общему числу возможных микросостояний системы
 Второе начало термодинамики Выражая всеобщий закон сохранения и превращения энергии, первое начало термодинамики не позволяет определить направление протекания процессов. Действительно, процесс самопроизвольной передачи теплоты от холодного тела к горячему не противоречит первому началу, если только уменьшение внутренней энергии холодного тела равно энергии, полученной горячим телом. Однако, опыты показывают, что такой процесс не происходит (раскаленный кусок железа, опущенный в воду, не нагревается за счет охлаждения воды). Обобщение огромного экспериментального материала привело к необходимости формулирования второго, третьего и нулевого начал термодинамики. Второе начало термодинамики в отличие от первого не является всеобщим законом природы. Оно справедливо только по отношению к термодинамическим системам. Существует несколько эквивалентных формулировок второго начала термодинамики. 1. Невозможен процесс, единственным результатом которого является передача теплоты от холодного тела к горячему (Клаузиус, 1850 г. ). 2. Невозможен процесс, единственным результатом которого является совершение работы за счет охлаждения одного тела (Томсон, 1851 г. , в 1892 г Томсон получил титул лорда Кельвина). Соответственно этой формулировке была доказана невозможность вечного двигателя второго рода, который целиком превращал бы в работу теплоту, извлекаемую из окружающих тел (океана, атмосферного воздуха и др. ) – для него было бы Q 2 = 0, A = Q 1, h = 1. Заметим, что создание такого двигателя не противоречит первому началу. 3. Энтропия изолированной системы не может убывать при любых происходящих в ней процессах, т. е. d. S ³ 0 (Клаузиус, 1865 г. ). Знак равенства относится к обратимым процессам, а знак больше - к необратимым процессам. В 1876 г. Клаузиус дал наиболее общую формулировку второго начала термодинамики: при реальных (необратимых) адиабатических процессах d. S>0, т. е. энтропия возрастает, достигая максимального значения в состоянии равновесия. Формула Больцмана S = k. lnω позволяет дать статистическое истолкование третьей формулировки второго начала: термодинамическая вероятность состояния изолированной системы при всех происходящих в ней процессах не может убывать. Второе начало термодинамики является статистическим законом. Оно выражает необходимые закономерности хаотического движения большого числа частиц, входящих в состав изолированной системы.
Второе начало термодинамики Выражая всеобщий закон сохранения и превращения энергии, первое начало термодинамики не позволяет определить направление протекания процессов. Действительно, процесс самопроизвольной передачи теплоты от холодного тела к горячему не противоречит первому началу, если только уменьшение внутренней энергии холодного тела равно энергии, полученной горячим телом. Однако, опыты показывают, что такой процесс не происходит (раскаленный кусок железа, опущенный в воду, не нагревается за счет охлаждения воды). Обобщение огромного экспериментального материала привело к необходимости формулирования второго, третьего и нулевого начал термодинамики. Второе начало термодинамики в отличие от первого не является всеобщим законом природы. Оно справедливо только по отношению к термодинамическим системам. Существует несколько эквивалентных формулировок второго начала термодинамики. 1. Невозможен процесс, единственным результатом которого является передача теплоты от холодного тела к горячему (Клаузиус, 1850 г. ). 2. Невозможен процесс, единственным результатом которого является совершение работы за счет охлаждения одного тела (Томсон, 1851 г. , в 1892 г Томсон получил титул лорда Кельвина). Соответственно этой формулировке была доказана невозможность вечного двигателя второго рода, который целиком превращал бы в работу теплоту, извлекаемую из окружающих тел (океана, атмосферного воздуха и др. ) – для него было бы Q 2 = 0, A = Q 1, h = 1. Заметим, что создание такого двигателя не противоречит первому началу. 3. Энтропия изолированной системы не может убывать при любых происходящих в ней процессах, т. е. d. S ³ 0 (Клаузиус, 1865 г. ). Знак равенства относится к обратимым процессам, а знак больше - к необратимым процессам. В 1876 г. Клаузиус дал наиболее общую формулировку второго начала термодинамики: при реальных (необратимых) адиабатических процессах d. S>0, т. е. энтропия возрастает, достигая максимального значения в состоянии равновесия. Формула Больцмана S = k. lnω позволяет дать статистическое истолкование третьей формулировки второго начала: термодинамическая вероятность состояния изолированной системы при всех происходящих в ней процессах не может убывать. Второе начало термодинамики является статистическим законом. Оно выражает необходимые закономерности хаотического движения большого числа частиц, входящих в состав изолированной системы.
 Проблема тепловой смерти Вселенной Вывод о тепловой смерти Вселенной был сформулирован Р. Клаузиусом в 1865 году на основе второго начала термодинамики. Согласно второму началу, любая физическая система, не обменивающаяся энергией с другими системами, стремится к наиболее вероятному равновесному состоянию — к так называемому состоянию с максимумом энтропии. Такое состояние соответствовало бы тепловой смерти Вселенной. Ещё до создания современной космологии были сделаны многочисленные попытки опровергнуть вывод о тепловой смерти Вселенной. Наиболее известна из них флуктуационная гипотеза Л. Больцмана (1872 год), согласно которой Вселенная извечно пребывает в равновесном изотермическом состоянии, но по закону случая то в одном, то в другом её месте иногда происходят отклонения от этого состояния; они происходят тем реже, чем большую область захватывают и чем значительнее степень отклонения. На самом деле ни Клаузиус, ни Больцман не были правы, так как их модели не учитывали важный фактор. Вселенную необходимо рассматривать как гравитирующую систему. В то время как для идеального газа наиболее вероятно равномерное распределение частиц в пространстве, в системе гравитирующих частиц однородное распределение не соответствует максимальной энтропии. Ошибочность вывода о тепловой смерти заключается в том, что бессмысленно применять второе начало термодинамики к незамкнутым системам, например к такой безграничной и бесконечно развивающейся системе, как Вселенная.
Проблема тепловой смерти Вселенной Вывод о тепловой смерти Вселенной был сформулирован Р. Клаузиусом в 1865 году на основе второго начала термодинамики. Согласно второму началу, любая физическая система, не обменивающаяся энергией с другими системами, стремится к наиболее вероятному равновесному состоянию — к так называемому состоянию с максимумом энтропии. Такое состояние соответствовало бы тепловой смерти Вселенной. Ещё до создания современной космологии были сделаны многочисленные попытки опровергнуть вывод о тепловой смерти Вселенной. Наиболее известна из них флуктуационная гипотеза Л. Больцмана (1872 год), согласно которой Вселенная извечно пребывает в равновесном изотермическом состоянии, но по закону случая то в одном, то в другом её месте иногда происходят отклонения от этого состояния; они происходят тем реже, чем большую область захватывают и чем значительнее степень отклонения. На самом деле ни Клаузиус, ни Больцман не были правы, так как их модели не учитывали важный фактор. Вселенную необходимо рассматривать как гравитирующую систему. В то время как для идеального газа наиболее вероятно равномерное распределение частиц в пространстве, в системе гравитирующих частиц однородное распределение не соответствует максимальной энтропии. Ошибочность вывода о тепловой смерти заключается в том, что бессмысленно применять второе начало термодинамики к незамкнутым системам, например к такой безграничной и бесконечно развивающейся системе, как Вселенная.
 Третье начало термодинамики Первый и второй законы термодинамики не позволяют определить значение Sо энтропии системы при абсолютном нyлe температуры. В связи с этим оказывается невозможным теоретический расчет абсолютных значений энтропии. На основании обобщения экспериментальных исследований свойств различных веществ при сверхнизких температурах был установлен закон, устранивший указанную трудность и получивший название третьего законом термодинамики, или теоремы Нернста-Планка - энтропия всех тeл в состоянии равновесия стремится к нулю пo мере приближения температуры к нулю Keльвинa. Этот вывод сделан на основании того, что при Т = 0 К система обладает наименее возможной энергией и не может больше отдавать энергию окружающим телам. Ее внутренняя энергия распределена между составляющими ее частицами однимединственным определенным способом. Все электроны в атомах находятся в наинизших энергетических состояниях, а атомы располагаются в пространстве определенным образом (в узлах кристаллической решетки твердого тела). Благодаря полной упорядоченности этого единственного состояния его термодинамическая вероятность ω = 1. Таким образом, оказывается, что ST→ 0 = k∙ln 1 = 0 т. е. при абсолютном нуле энтропия обращается в нуль. Третье начало термодинамики утверждает невозможность процессов, приводящих к достижению абсолютного нуля температуры, то есть накладывает ограничение на протекание термодинамических процессов, в результате которых тело охладилось бы до 0 К.
Третье начало термодинамики Первый и второй законы термодинамики не позволяют определить значение Sо энтропии системы при абсолютном нyлe температуры. В связи с этим оказывается невозможным теоретический расчет абсолютных значений энтропии. На основании обобщения экспериментальных исследований свойств различных веществ при сверхнизких температурах был установлен закон, устранивший указанную трудность и получивший название третьего законом термодинамики, или теоремы Нернста-Планка - энтропия всех тeл в состоянии равновесия стремится к нулю пo мере приближения температуры к нулю Keльвинa. Этот вывод сделан на основании того, что при Т = 0 К система обладает наименее возможной энергией и не может больше отдавать энергию окружающим телам. Ее внутренняя энергия распределена между составляющими ее частицами однимединственным определенным способом. Все электроны в атомах находятся в наинизших энергетических состояниях, а атомы располагаются в пространстве определенным образом (в узлах кристаллической решетки твердого тела). Благодаря полной упорядоченности этого единственного состояния его термодинамическая вероятность ω = 1. Таким образом, оказывается, что ST→ 0 = k∙ln 1 = 0 т. е. при абсолютном нуле энтропия обращается в нуль. Третье начало термодинамики утверждает невозможность процессов, приводящих к достижению абсолютного нуля температуры, то есть накладывает ограничение на протекание термодинамических процессов, в результате которых тело охладилось бы до 0 К.
 Уравнение Ван-дер-Ваальса Ван-дер-Ваальс внес в уравнение Клапейрона-Менделеева p. V = RT две поправки. Первая поправка связана с действием сил отталкивания между молекулами. Она учитывает собственный объем молекулы Vo и поэтому объем сосуда V заменяют свободным объемом V – b, где b = 4 V 0 NA. Вторая поправка связана с действием сил притяжения между молекулами: в тонком поверхностном слое вблизи стенки сосуда на молекулу, подлетающую к стенке, действует сила притяжения со стороны остальных молекул газа, что приводит к уменьшению силы удара молекулы о стенку сосуда, а, следовательно, и давления на величину p (NA/V)². В результате : (p+a/V 2)(V-b) = RT, которое называют уравнением Ван-дер-Ваальса для одного моля газа. В этом уравнении а и b - постоянные, зависящие только от вида газа. Для произвольной массы газа уравнение Ван-дер-Ваальса имеет вид : (p+a/V 2)(V-ν. b)= ν. RT , где ν = M/μ - число молей газа. Для фиксированных значений p и Т это уравнение третьей степени относительно объема газа V и, следовательно, оно может иметь либо три вещественных корня (V 1, V 2, V 3), либо один вещественных корень (V 1) и два комплексно-сопряженных корня. Поэтому на диаграмме p–V прямая, параллельная оси V может пересекать изотерму либо в трех точках В, F, G либо в одной K. Ван-дер-Ваальс
Уравнение Ван-дер-Ваальса Ван-дер-Ваальс внес в уравнение Клапейрона-Менделеева p. V = RT две поправки. Первая поправка связана с действием сил отталкивания между молекулами. Она учитывает собственный объем молекулы Vo и поэтому объем сосуда V заменяют свободным объемом V – b, где b = 4 V 0 NA. Вторая поправка связана с действием сил притяжения между молекулами: в тонком поверхностном слое вблизи стенки сосуда на молекулу, подлетающую к стенке, действует сила притяжения со стороны остальных молекул газа, что приводит к уменьшению силы удара молекулы о стенку сосуда, а, следовательно, и давления на величину p (NA/V)². В результате : (p+a/V 2)(V-b) = RT, которое называют уравнением Ван-дер-Ваальса для одного моля газа. В этом уравнении а и b - постоянные, зависящие только от вида газа. Для произвольной массы газа уравнение Ван-дер-Ваальса имеет вид : (p+a/V 2)(V-ν. b)= ν. RT , где ν = M/μ - число молей газа. Для фиксированных значений p и Т это уравнение третьей степени относительно объема газа V и, следовательно, оно может иметь либо три вещественных корня (V 1, V 2, V 3), либо один вещественных корень (V 1) и два комплексно-сопряженных корня. Поэтому на диаграмме p–V прямая, параллельная оси V может пересекать изотерму либо в трех точках В, F, G либо в одной K. Ван-дер-Ваальс
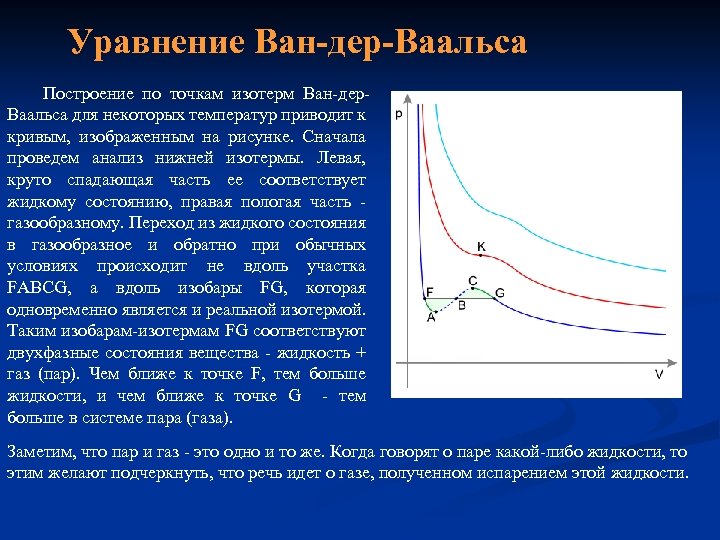 Уравнение Ван-дер-Ваальса Построение по точкам изотерм Ван-дер. Ваальса для некоторых температур приводит к кривым, изображенным на рисунке. Сначала проведем анализ нижней изотермы. Левая, круто спадающая часть ее соответствует жидкому состоянию, правая пологая часть - газообразному. Переход из жидкого состояния в газообразное и обратно при обычных условиях происходит не вдоль участка FAВСG, а вдоль изобары FG, которая одновременно является и реальной изотермой. Таким изобарам-изотермам FG соответствуют двухфазные состояния вещества - жидкость + газ (пар). Чем ближе к точке F, тем больше жидкости, и чем ближе к точке G - тем больше в системе пара (газа). Заметим, что пар и газ - это одно и то же. Когда говорят о паре какой-либо жидкости, то этим желают подчеркнуть, что речь идет о газе, полученном испарением этой жидкости.
Уравнение Ван-дер-Ваальса Построение по точкам изотерм Ван-дер. Ваальса для некоторых температур приводит к кривым, изображенным на рисунке. Сначала проведем анализ нижней изотермы. Левая, круто спадающая часть ее соответствует жидкому состоянию, правая пологая часть - газообразному. Переход из жидкого состояния в газообразное и обратно при обычных условиях происходит не вдоль участка FAВСG, а вдоль изобары FG, которая одновременно является и реальной изотермой. Таким изобарам-изотермам FG соответствуют двухфазные состояния вещества - жидкость + газ (пар). Чем ближе к точке F, тем больше жидкости, и чем ближе к точке G - тем больше в системе пара (газа). Заметим, что пар и газ - это одно и то же. Когда говорят о паре какой-либо жидкости, то этим желают подчеркнуть, что речь идет о газе, полученном испарением этой жидкости.
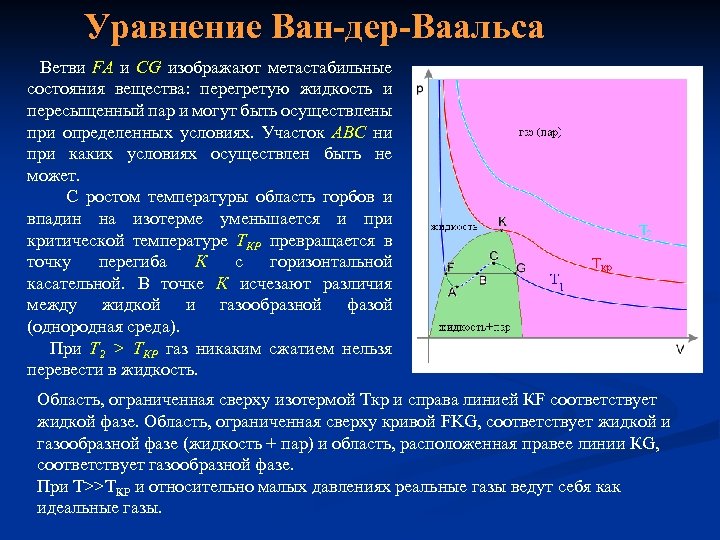 Уравнение Ван-дер-Ваальса Ветви FA и CG изображают метастабильные состояния вещества: перегретую жидкость и пересыщенный пар и могут быть осуществлены при определенных условиях. Участок ABС ни при каких условиях осуществлен быть не может. С ростом температуры область горбов и впадин на изотерме уменьшается и при критической температуре ТКР превращается в точку перегиба К с горизонтальной касательной. В точке К исчезают различия между жидкой и газообразной фазой (однородная среда). При Т 2 > ТКР газ никаким сжатием нельзя перевести в жидкость. Область, ограниченная сверху изотермой Ткр и справа линией КF соответствует жидкой фазе. Область, ограниченная сверху кривой FKG, соответствует жидкой и газообразной фазе (жидкость + пар) и область, расположенная правее линии КG, соответствует газообразной фазе. При Т>>ТКР и относительно малых давлениях реальные газы ведут себя как идеальные газы.
Уравнение Ван-дер-Ваальса Ветви FA и CG изображают метастабильные состояния вещества: перегретую жидкость и пересыщенный пар и могут быть осуществлены при определенных условиях. Участок ABС ни при каких условиях осуществлен быть не может. С ростом температуры область горбов и впадин на изотерме уменьшается и при критической температуре ТКР превращается в точку перегиба К с горизонтальной касательной. В точке К исчезают различия между жидкой и газообразной фазой (однородная среда). При Т 2 > ТКР газ никаким сжатием нельзя перевести в жидкость. Область, ограниченная сверху изотермой Ткр и справа линией КF соответствует жидкой фазе. Область, ограниченная сверху кривой FKG, соответствует жидкой и газообразной фазе (жидкость + пар) и область, расположенная правее линии КG, соответствует газообразной фазе. При Т>>ТКР и относительно малых давлениях реальные газы ведут себя как идеальные газы.
 Лекция окончена. Спасибо за терпение Можно задавать вопросы
Лекция окончена. Спасибо за терпение Можно задавать вопросы
 Амедео Авогадро, граф Куаренья и Черрето Граф Лоренцо Романо Амедео Карло Авогадро (итал. Lorenzo Romano Amedeo Carlo Avogadro di Quaregna e Cerreto; родился 9 августа 1776 года в Турине (Италия) в семье служащего судебного ведомства Филиппо Авогадро. Амедео был третьим из восьми детей. В юношеские годы посещал школу геометрии и экспериментальной физики. По традиции того времени профессии и должности передавались по наследству, поэтому Амедео занялся юриспруденцией. В 20 лет получил степень доктора церковного законоведения. В 25 лет начал самостоятельно изучать физико-математические науки. В 1832 году Туринский университет получил кафедру высшей физики. Авогадро некоторое время занимал должность старшего инспектора Контрольной палаты, а также состоял членом Высшей статистической комиссии, Высшего совета народного образования и председателем Комиссии мер и весов. Несмотря на почтенный возраст, он продолжал публиковать свои исследования в трудах Туринской академии наук. Последняя его работа вышла из печати за три года до смерти, когда Авогадро исполнилось 77 лет. Он умер в Турине 9 июля 1856 года и похоронен в семейном склепе в Верчелли. Авогадро пришел к следующему важному заключению: «число молекул всегда одно и то же в одинаковых объемах любых газов» . В 1814 году появляется статья Авогадро «Очерк об относительных массах молекул простых тел, или предполагаемых плотностях их газа, и о конституции некоторых из их соединений» . Здесь четко формулируется закон Авогадро: «…равные объемы газообразных веществ при одинаковых давлениях и температурах отвечают равному числу молекул, так что плотности различных газов представляют собою меру масс молекул соответствующих газов» . В честь Авогадро назван кратер на Луне, минерал авогадрит, малая планета (12294) Авогадро. ↑
Амедео Авогадро, граф Куаренья и Черрето Граф Лоренцо Романо Амедео Карло Авогадро (итал. Lorenzo Romano Amedeo Carlo Avogadro di Quaregna e Cerreto; родился 9 августа 1776 года в Турине (Италия) в семье служащего судебного ведомства Филиппо Авогадро. Амедео был третьим из восьми детей. В юношеские годы посещал школу геометрии и экспериментальной физики. По традиции того времени профессии и должности передавались по наследству, поэтому Амедео занялся юриспруденцией. В 20 лет получил степень доктора церковного законоведения. В 25 лет начал самостоятельно изучать физико-математические науки. В 1832 году Туринский университет получил кафедру высшей физики. Авогадро некоторое время занимал должность старшего инспектора Контрольной палаты, а также состоял членом Высшей статистической комиссии, Высшего совета народного образования и председателем Комиссии мер и весов. Несмотря на почтенный возраст, он продолжал публиковать свои исследования в трудах Туринской академии наук. Последняя его работа вышла из печати за три года до смерти, когда Авогадро исполнилось 77 лет. Он умер в Турине 9 июля 1856 года и похоронен в семейном склепе в Верчелли. Авогадро пришел к следующему важному заключению: «число молекул всегда одно и то же в одинаковых объемах любых газов» . В 1814 году появляется статья Авогадро «Очерк об относительных массах молекул простых тел, или предполагаемых плотностях их газа, и о конституции некоторых из их соединений» . Здесь четко формулируется закон Авогадро: «…равные объемы газообразных веществ при одинаковых давлениях и температурах отвечают равному числу молекул, так что плотности различных газов представляют собою меру масс молекул соответствующих газов» . В честь Авогадро назван кратер на Луне, минерал авогадрит, малая планета (12294) Авогадро. ↑
 Жан Батист Жозеф Фурье (фр. Jean Baptiste Joseph Fourier; Родился 21 марта 1768, в г. Осер, Франция ; умер 16 мая 1830, в Париже, французский математик и физик Жан Батист Жозеф Фурье был 12 -м из 15 -и детей в семье портного (девятым во втором браке отца). Его отец, Жозеф Фурье, происходил из семьи лавочника из небольшого городка в Лотарингии. Фурье стал сиротой в возрасте восьми лет. В своей первой школе, которой руководил церковный музыкант, Фурье показывал успехи в изучении французского и латыни. К 13 годам Жозеф заинтересовался математикой, а в возрасте 14 лет он освоил шеститомный «Курс математики» Безу. Во время оккупации Египта Фурье работал во французской администрации, руководил археологическими раскопками, а также занимался формированием системы образования. Он принимал участие в создании Каирского института и был одним из 12 членов математического отделения, наряду с Монжем, Малусом и самим Наполеоном. В 1809 году Фурье получил от Наполеона титул барона и был награждён орденом Почётного легиона. Ещё в 1789 году в Париже в Королевской Академии Наук Фурье представил работу о численном решении уравнений любой степени. В своих лекциях в 1796 году он изложил теорему о числе действительных корней алгебраического уравнения, лежащих между данными границами, названную впоследствии его именем. Свои методы (ряды и интегралы Фурье) он использовал в теории распространения тепла. Но вскоре они стали исключительно мощным инструментом математического исследования самых разных задач — особенно там, где есть волны и колебания. А этот круг чрезвычайно широк — астрономия, акустика, теория приливов, радиотехника и др. Его имя внесено в список величайших учёных Франции, помещённый на первом ↑ этаже Эйфелевой башни.
Жан Батист Жозеф Фурье (фр. Jean Baptiste Joseph Fourier; Родился 21 марта 1768, в г. Осер, Франция ; умер 16 мая 1830, в Париже, французский математик и физик Жан Батист Жозеф Фурье был 12 -м из 15 -и детей в семье портного (девятым во втором браке отца). Его отец, Жозеф Фурье, происходил из семьи лавочника из небольшого городка в Лотарингии. Фурье стал сиротой в возрасте восьми лет. В своей первой школе, которой руководил церковный музыкант, Фурье показывал успехи в изучении французского и латыни. К 13 годам Жозеф заинтересовался математикой, а в возрасте 14 лет он освоил шеститомный «Курс математики» Безу. Во время оккупации Египта Фурье работал во французской администрации, руководил археологическими раскопками, а также занимался формированием системы образования. Он принимал участие в создании Каирского института и был одним из 12 членов математического отделения, наряду с Монжем, Малусом и самим Наполеоном. В 1809 году Фурье получил от Наполеона титул барона и был награждён орденом Почётного легиона. Ещё в 1789 году в Париже в Королевской Академии Наук Фурье представил работу о численном решении уравнений любой степени. В своих лекциях в 1796 году он изложил теорему о числе действительных корней алгебраического уравнения, лежащих между данными границами, названную впоследствии его именем. Свои методы (ряды и интегралы Фурье) он использовал в теории распространения тепла. Но вскоре они стали исключительно мощным инструментом математического исследования самых разных задач — особенно там, где есть волны и колебания. А этот круг чрезвычайно широк — астрономия, акустика, теория приливов, радиотехника и др. Его имя внесено в список величайших учёных Франции, помещённый на первом ↑ этаже Эйфелевой башни.
 ЖАК АЛЕКСАНДР СЕЗАР ШАРЛЬ, ЖАК АЛЕКСАНДР СЕЗАР (Jacques. Alexandre-César Charles) (1746– 1823), французский физик и изобретатель. Родился 12 ноября 1746 в Божанси. Учился самостоятельно. В молодости переехал в Париж и поступил на должность канцелярского служащего в министерство финансов. Когда стали известны опыты Б. Франклина с молнией, Шарль повторил их с изменениями – настолько интересными, что сам Франклин приехал познакомиться с ним и похвально отозвался о его способностях. Шарль построил воздушный шар из прорезиненной ткани и первым использовал для его наполнения водород. Исследуя процессы расширения газов, в 1787 установил зависимость объема идеального газа от температуры. Шарль изобрел такие приборы, как мегаскоп и термометрический гидрометр. Умер Шарль в Париже 7 апреля 1823. ↑
ЖАК АЛЕКСАНДР СЕЗАР ШАРЛЬ, ЖАК АЛЕКСАНДР СЕЗАР (Jacques. Alexandre-César Charles) (1746– 1823), французский физик и изобретатель. Родился 12 ноября 1746 в Божанси. Учился самостоятельно. В молодости переехал в Париж и поступил на должность канцелярского служащего в министерство финансов. Когда стали известны опыты Б. Франклина с молнией, Шарль повторил их с изменениями – настолько интересными, что сам Франклин приехал познакомиться с ним и похвально отозвался о его способностях. Шарль построил воздушный шар из прорезиненной ткани и первым использовал для его наполнения водород. Исследуя процессы расширения газов, в 1787 установил зависимость объема идеального газа от температуры. Шарль изобрел такие приборы, как мегаскоп и термометрический гидрометр. Умер Шарль в Париже 7 апреля 1823. ↑
 Жозеф Луи ГЕЙ-ЛЮССАК Жозеф Луи (Gay-Lussac Joseph Louis) (6. XII. 1778 - 9. V. 1850) — французский физик и химик, член Парижской АН (1806). Окончил Политехническую школу (1800) , где работал с 1802 (с 1809 — профессор химии), одновременно в 1808 - 1832 — профессор физики Парижского университета. С 1832 — профессор химии Парижского ботанического сада. Физические работы в области молекулярной физики и теплоты. Исследовал расширение и свойства газов. В 1802 независимо от Дальтона открыл один из газовых законов (закон Гей-Люссака), доказал, что коэффициент расширения всех газов одинаков, и вычислил его (0, 00375 град -1 ). В 1804 дважды осуществил полеты на воздушном шаре (на высоту 7 км), во время которых выполнил ряд научных исследований, в частности, изучал температуру и влажность воздуха. В 1807 установил понижение температуры воздуха при его расширении и повышение — при сжатии (без теплообмена), обнаружил независимость теплоемкости газа от его объема. ↑
Жозеф Луи ГЕЙ-ЛЮССАК Жозеф Луи (Gay-Lussac Joseph Louis) (6. XII. 1778 - 9. V. 1850) — французский физик и химик, член Парижской АН (1806). Окончил Политехническую школу (1800) , где работал с 1802 (с 1809 — профессор химии), одновременно в 1808 - 1832 — профессор физики Парижского университета. С 1832 — профессор химии Парижского ботанического сада. Физические работы в области молекулярной физики и теплоты. Исследовал расширение и свойства газов. В 1802 независимо от Дальтона открыл один из газовых законов (закон Гей-Люссака), доказал, что коэффициент расширения всех газов одинаков, и вычислил его (0, 00375 град -1 ). В 1804 дважды осуществил полеты на воздушном шаре (на высоту 7 км), во время которых выполнил ряд научных исследований, в частности, изучал температуру и влажность воздуха. В 1807 установил понижение температуры воздуха при его расширении и повышение — при сжатии (без теплообмена), обнаружил независимость теплоемкости газа от его объема. ↑
 Роберт Бойль (англ. Robert Boyle; 25 января 1627 года — 30 декабря 1691 года) — физик, химик и богослов, седьмой сын Ричарда Бойля, графа Коркского, вельможи времён Елизаветы Английской. Первоначальное воспитание и обучение получил дома и в коллегии в Итоне, а на двенадцатом году был послан отцом в Женеву, где учился несколько лет, а потом завершил свое образование путешествием в Италию и Францию. Все свое состояние и все свои силы он употребил на изучение природы и на распространение религиозных христианских понятий. По завещанию (1661) Бойль оставил капитал для финансирования ежегодных чтений о Боге и религии, знаменитых «Лекций Бойля» . Целью лекций Бойль определил защиту христианской религии от «печально известных неверных, а именно атеистов, деистов, язычников, иудеев и мусульман» . «Лекции Бойля» продолжались регулярно вплоть до 1905 г. С 2004 г. их возобновили в Лондоне, в церкви St. Mary Le Bow. Они проходят ежегодно, в феврале. Весьма важный физически закон сжатия газов, который носит теперь его имя (Бойля-Мариотта закон), остался бы может быть незамеченным Бойлем, если б не первоначальное указание его ученика Richard'a Townley на правильность сжатая газов с увеличением давления в опытах Бойля. Он подробно развил свои взгляды на строение вещества в нескольких сочинениях: "Sceptical Chemist" (1662 и 1669); "The origin of forms and qualities according to the corpuscular. Philosophy" (1666 и 1667); "Physiological Essays and other Tracts"(1661). ↑
Роберт Бойль (англ. Robert Boyle; 25 января 1627 года — 30 декабря 1691 года) — физик, химик и богослов, седьмой сын Ричарда Бойля, графа Коркского, вельможи времён Елизаветы Английской. Первоначальное воспитание и обучение получил дома и в коллегии в Итоне, а на двенадцатом году был послан отцом в Женеву, где учился несколько лет, а потом завершил свое образование путешествием в Италию и Францию. Все свое состояние и все свои силы он употребил на изучение природы и на распространение религиозных христианских понятий. По завещанию (1661) Бойль оставил капитал для финансирования ежегодных чтений о Боге и религии, знаменитых «Лекций Бойля» . Целью лекций Бойль определил защиту христианской религии от «печально известных неверных, а именно атеистов, деистов, язычников, иудеев и мусульман» . «Лекции Бойля» продолжались регулярно вплоть до 1905 г. С 2004 г. их возобновили в Лондоне, в церкви St. Mary Le Bow. Они проходят ежегодно, в феврале. Весьма важный физически закон сжатия газов, который носит теперь его имя (Бойля-Мариотта закон), остался бы может быть незамеченным Бойлем, если б не первоначальное указание его ученика Richard'a Townley на правильность сжатая газов с увеличением давления в опытах Бойля. Он подробно развил свои взгляды на строение вещества в нескольких сочинениях: "Sceptical Chemist" (1662 и 1669); "The origin of forms and qualities according to the corpuscular. Philosophy" (1666 и 1667); "Physiological Essays and other Tracts"(1661). ↑
 Эдм Мариотт Эдме МАРИОТТ (Edme Mariotte) - французский физик, физиолог и священник, известный тем, что он самостоятельно в 1676 году открыл закон, согласно которому при постоянной температуре объем газа обратно пропорционален давлению, во Франции известен как закон Мариотта, в России же он называется законом Бойля-Мариотта. Родился 1620 в Дижоне. Проживал вблизи Дижона и был приором в городке Сан-Мартан. Мариотт был одним из основателей (1666) и первых членов Академии наук, основанной в Париже. Умер в Париже в 1684 г. , Мариотт также сделал выводы о том, что растения синтезируют материалы путем химических процессов, и эта теория была доказана после его смерти. Научные работы относятся к механике, теплоте, оптике. Описал многочисленные опыты п о изучению течения жидкостей по трубам; экспериментально подтвердил формулу Э. Торричелли относительно скорости истечения жидкости. Исследовал высоту подъёма фонтанов и составил таблицы зависимости высоты подъёма от диаметра отверстия. Изучал столкновение упругих тел, колебания маятника. В «Трактате об ударе или соударении тел» (1678) обобщил исследования в этой области. Доказал увеличение объёма воды при замерзании. Обнаружил в 1666 г. слепое пятно в глазу, исследовал цвета, в частности цветные кольца вокруг Солнца и Луны, изучал радугу, дифракцию света, лучистую теплоту, показал различие между тепловыми и световыми лучами. Изготовил ряд различных физических приборов. ↑
Эдм Мариотт Эдме МАРИОТТ (Edme Mariotte) - французский физик, физиолог и священник, известный тем, что он самостоятельно в 1676 году открыл закон, согласно которому при постоянной температуре объем газа обратно пропорционален давлению, во Франции известен как закон Мариотта, в России же он называется законом Бойля-Мариотта. Родился 1620 в Дижоне. Проживал вблизи Дижона и был приором в городке Сан-Мартан. Мариотт был одним из основателей (1666) и первых членов Академии наук, основанной в Париже. Умер в Париже в 1684 г. , Мариотт также сделал выводы о том, что растения синтезируют материалы путем химических процессов, и эта теория была доказана после его смерти. Научные работы относятся к механике, теплоте, оптике. Описал многочисленные опыты п о изучению течения жидкостей по трубам; экспериментально подтвердил формулу Э. Торричелли относительно скорости истечения жидкости. Исследовал высоту подъёма фонтанов и составил таблицы зависимости высоты подъёма от диаметра отверстия. Изучал столкновение упругих тел, колебания маятника. В «Трактате об ударе или соударении тел» (1678) обобщил исследования в этой области. Доказал увеличение объёма воды при замерзании. Обнаружил в 1666 г. слепое пятно в глазу, исследовал цвета, в частности цветные кольца вокруг Солнца и Луны, изучал радугу, дифракцию света, лучистую теплоту, показал различие между тепловыми и световыми лучами. Изготовил ряд различных физических приборов. ↑
 Ян-Дидерик ВАН-ДЕР-ВААЛЬС (Van der Waals), Ян Дидерик, родился в Лейдене, в семье Якобуса Ван-дер-Ваальса, плотника 23 ноября 1837 г. – умер в Амстердаме 8 марта 1923 г. Нобелевская премия по физике, 1910 г. Окончив начальную и среднюю школу в Лейдене, Ян стал учителем начальной школы. С 1862 по 1865 г. он посещал Лейденский университет как вольнослушатель. В 1864 г. он получил удостоверение учителя средней школы по математике и физике и преподавал физику сначала в Девентере в 1864 г. , а затем в Гааге, где стал в 1866 г. директором школы. Его докторская диссертация, посвященная непрерывности газообразного и жидкого состояний, получила горячее одобрение со стороны Джеймса. Клерка Максвелла, одного из величайших физиков XIX в. , который сказал о работе Ван-дер-Ваальса : "Она сразу поставила его имя в один ряд с самыми (23. XI. 1837 - 8. III. 1923) выдающимися именами в науке". Идеи Ван-дер-Ваальса возникли под влиянием написанной в 1857 г. статьи Рудольфа-Юлиуса. Эмануэля Клаузиуса, немецкого физика, внесшего большой вклад в кинетическую теорию газов. Согласно этой теории, молекулы газа быстро движутся в разных направлениях. Их удары о стенки содержащего их сосуда определяют давление газа, а средняя скорость. Уравнение Ван-дер-Ваальса значительно прояснило обнаруженное ранее существование критической температуры, различной для разных газов, выше которой газ, независимо от величины давления, нельзя было перевести в жидкое состояние. Критическая температура связана с критическим объемом и критическим давлением, которые вместе определяют критическую точку, совокупность специальных значений температуры, давления и объема, при которых нет видимой грани между газом и жидкостью: при этих условиях оба состояния примерно одинаковы, резкого перехода между ними нет. ↑
Ян-Дидерик ВАН-ДЕР-ВААЛЬС (Van der Waals), Ян Дидерик, родился в Лейдене, в семье Якобуса Ван-дер-Ваальса, плотника 23 ноября 1837 г. – умер в Амстердаме 8 марта 1923 г. Нобелевская премия по физике, 1910 г. Окончив начальную и среднюю школу в Лейдене, Ян стал учителем начальной школы. С 1862 по 1865 г. он посещал Лейденский университет как вольнослушатель. В 1864 г. он получил удостоверение учителя средней школы по математике и физике и преподавал физику сначала в Девентере в 1864 г. , а затем в Гааге, где стал в 1866 г. директором школы. Его докторская диссертация, посвященная непрерывности газообразного и жидкого состояний, получила горячее одобрение со стороны Джеймса. Клерка Максвелла, одного из величайших физиков XIX в. , который сказал о работе Ван-дер-Ваальса : "Она сразу поставила его имя в один ряд с самыми (23. XI. 1837 - 8. III. 1923) выдающимися именами в науке". Идеи Ван-дер-Ваальса возникли под влиянием написанной в 1857 г. статьи Рудольфа-Юлиуса. Эмануэля Клаузиуса, немецкого физика, внесшего большой вклад в кинетическую теорию газов. Согласно этой теории, молекулы газа быстро движутся в разных направлениях. Их удары о стенки содержащего их сосуда определяют давление газа, а средняя скорость. Уравнение Ван-дер-Ваальса значительно прояснило обнаруженное ранее существование критической температуры, различной для разных газов, выше которой газ, независимо от величины давления, нельзя было перевести в жидкое состояние. Критическая температура связана с критическим объемом и критическим давлением, которые вместе определяют критическую точку, совокупность специальных значений температуры, давления и объема, при которых нет видимой грани между газом и жидкостью: при этих условиях оба состояния примерно одинаковы, резкого перехода между ними нет. ↑