МКТ_версия ЭД1_20140402.ppt
- Количество слайдов: 34
 Основы МКТ
Основы МКТ
 Молекулярная физика •
Молекулярная физика •
 Количество вещества
Количество вещества
 Уравнение состояния идеального газа Состояние системы – совокупность физических величин (параметров системы), характеризующих состояние системы (температура, давление, объем и т. д. ) Неравновесное состояние – состояние системы, при которой какой-либо параметр системы не имеет определенного значения. Равновесное состояние – состояние системы, при котором все параметры системы имеют определенные значения, которые остаются постоянными сколь угодно долго при неименных внешних условиях. Процесс релаксации – процесс перехода системы из неравновесного состояния в равновесное. Равновесный (квазистатический) процесс – процесс перехода системы из одного состояния в другое, состоящий из непрерывной последовательности равновесных состояний. Круговой процесс (цикл) – процесс, при котором система после ряда изменений возвращается в исходное состояние.
Уравнение состояния идеального газа Состояние системы – совокупность физических величин (параметров системы), характеризующих состояние системы (температура, давление, объем и т. д. ) Неравновесное состояние – состояние системы, при которой какой-либо параметр системы не имеет определенного значения. Равновесное состояние – состояние системы, при котором все параметры системы имеют определенные значения, которые остаются постоянными сколь угодно долго при неименных внешних условиях. Процесс релаксации – процесс перехода системы из неравновесного состояния в равновесное. Равновесный (квазистатический) процесс – процесс перехода системы из одного состояния в другое, состоящий из непрерывной последовательности равновесных состояний. Круговой процесс (цикл) – процесс, при котором система после ряда изменений возвращается в исходное состояние.


 Температура – величина, характеризующая состояние термодинамического равновесия макросистемы. Макросистема – система, состоящая из очень большого числа частиц (атомов, молекул, электронов и т. д. ) Любой метод измерения температуры требует установления температурной шкалы. Реперные точки – точки, на которых основывается шкала измерений. Международная практическая шкала температур (шкала Цельсия): реперные точки – температура замерзания (0°С) и кипения воды (100°С) на уровне моря. Единица измерения международной практической температуры – градус Цельсия (°С)
Температура – величина, характеризующая состояние термодинамического равновесия макросистемы. Макросистема – система, состоящая из очень большого числа частиц (атомов, молекул, электронов и т. д. ) Любой метод измерения температуры требует установления температурной шкалы. Реперные точки – точки, на которых основывается шкала измерений. Международная практическая шкала температур (шкала Цельсия): реперные точки – температура замерзания (0°С) и кипения воды (100°С) на уровне моря. Единица измерения международной практической температуры – градус Цельсия (°С)
 Термодинамическая (абсолютная) шкала температур (шкала Кельвина): Реперная точка – тройная точка воды (Tтр) Tтр=273, 16 К Единица абсолютной температуры – кельвин (К) Значения кельвина и градуса Цельсия одинаковы 1°С=1 К Температура t по шкале Цельсия связана с температурой T по шкале Кельвина T=t+273, 15 Абсолютный нуль температур Т=0 по шкале Цельсия ему соответствует t= – 273, 15°С Шкала Фаренгейта: реперные точки – точка таяния льда равна +32 °F, а точка кипения воды +212 °F, один градус Фаренгейта равен 1/180 разности этих температур Из шкалы Цельсия в шкалу Фаренгейта: Из шкалы Фаренгейта в шкалу Цельсия:
Термодинамическая (абсолютная) шкала температур (шкала Кельвина): Реперная точка – тройная точка воды (Tтр) Tтр=273, 16 К Единица абсолютной температуры – кельвин (К) Значения кельвина и градуса Цельсия одинаковы 1°С=1 К Температура t по шкале Цельсия связана с температурой T по шкале Кельвина T=t+273, 15 Абсолютный нуль температур Т=0 по шкале Цельсия ему соответствует t= – 273, 15°С Шкала Фаренгейта: реперные точки – точка таяния льда равна +32 °F, а точка кипения воды +212 °F, один градус Фаренгейта равен 1/180 разности этих температур Из шкалы Цельсия в шкалу Фаренгейта: Из шкалы Фаренгейта в шкалу Цельсия:
 Внутренняя энергия системы Внутренняя энергия тела – энергия тела за вычетом кинетической энергии тела как целого и потенциальной энергии тела во внешнем поле. Внутренняя энергия состоит из: 1). кинетической энергии хаотического движения частиц, 2). потенциальной энергии взаимодействия частиц , 3). внутренней энергии самих частиц. Внутренняя энергия является функцией состояния системы: - не зависит от того, каким путем систему привели в данное состояние, - когда система оказывается в данном состоянии, её внутренняя энергия принимает присущее этому состоянию значение, независимо от предыстории системы, - изменение внутренней энергии при переходе из одного состояния в другое равно разности между ее значениями в конечном и начальном состояниях.
Внутренняя энергия системы Внутренняя энергия тела – энергия тела за вычетом кинетической энергии тела как целого и потенциальной энергии тела во внешнем поле. Внутренняя энергия состоит из: 1). кинетической энергии хаотического движения частиц, 2). потенциальной энергии взаимодействия частиц , 3). внутренней энергии самих частиц. Внутренняя энергия является функцией состояния системы: - не зависит от того, каким путем систему привели в данное состояние, - когда система оказывается в данном состоянии, её внутренняя энергия принимает присущее этому состоянию значение, независимо от предыстории системы, - изменение внутренней энергии при переходе из одного состояния в другое равно разности между ее значениями в конечном и начальном состояниях.
 Первое начало термодинамики Изменить внутреннюю энергию системы можно, совершив над системой работу внешними силами или путем теплопередачи. Количество теплоты, сообщенное системе, идет на приращение внутренней энергии системы и на совершение системой работы над внешними телами
Первое начало термодинамики Изменить внутреннюю энергию системы можно, совершив над системой работу внешними силами или путем теплопередачи. Количество теплоты, сообщенное системе, идет на приращение внутренней энергии системы и на совершение системой работы над внешними телами
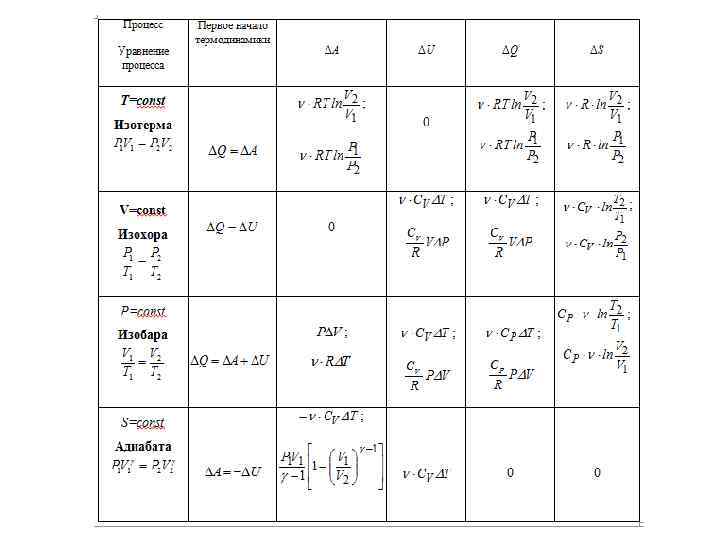
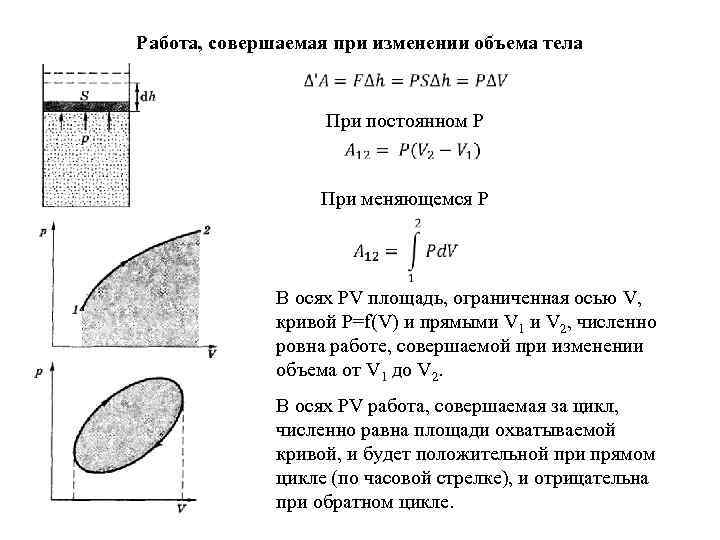 Работа, совершаемая при изменении объема тела При постоянном P При меняющемся P В осях PV площадь, ограниченная осью V, кривой P=f(V) и прямыми V 1 и V 2, численно ровна работе, совершаемой при изменении объема от V 1 до V 2. В осях PV работа, совершаемая за цикл, численно равна площади охватываемой кривой, и будет положительной при прямом цикле (по часовой стрелке), и отрицательна при обратном цикле.
Работа, совершаемая при изменении объема тела При постоянном P При меняющемся P В осях PV площадь, ограниченная осью V, кривой P=f(V) и прямыми V 1 и V 2, численно ровна работе, совершаемой при изменении объема от V 1 до V 2. В осях PV работа, совершаемая за цикл, численно равна площади охватываемой кривой, и будет положительной при прямом цикле (по часовой стрелке), и отрицательна при обратном цикле.
 Внутренняя энергия и теплоемкость Теплоемкость – это физическая величина, равная количеству тепла, которое необходимо сообщить телу, чтобы увеличить его температуру на 1 кельвин Теплоемкость измеряется в Дж/К (джоуль на кельвин) Молярная теплоемкость C – теплоемкость моля вещества, измеряется в Дж/(моль·К) (джоуль на моль-кельвин) Удельная теплоемкость (с) – теплоемкость единицы массы вещества где M – молярная масса. Удельная теплоемкость измеряется в Дж/(кг·К) Теплоемкость при постоянном объеме (СV), теплоемкость при постоянном давлении (Сp).
Внутренняя энергия и теплоемкость Теплоемкость – это физическая величина, равная количеству тепла, которое необходимо сообщить телу, чтобы увеличить его температуру на 1 кельвин Теплоемкость измеряется в Дж/К (джоуль на кельвин) Молярная теплоемкость C – теплоемкость моля вещества, измеряется в Дж/(моль·К) (джоуль на моль-кельвин) Удельная теплоемкость (с) – теплоемкость единицы массы вещества где M – молярная масса. Удельная теплоемкость измеряется в Дж/(кг·К) Теплоемкость при постоянном объеме (СV), теплоемкость при постоянном давлении (Сp).
 Уравнение первого начала термодинамики при V=const Так как CV не зависит от температуры в широком диапазоне, то внутренняя энергия для одного моля Внутренняя энергия для массы газа m
Уравнение первого начала термодинамики при V=const Так как CV не зависит от температуры в широком диапазоне, то внутренняя энергия для одного моля Внутренняя энергия для массы газа m
 Уравнение первого начала термодинамики при P=const Соотношение между теплоемкостями при постоянном объеме и постоянном давлении
Уравнение первого начала термодинамики при P=const Соотношение между теплоемкостями при постоянном объеме и постоянном давлении
 Работа, которую совершает моль идеального газа при повышении его температуры на 1 К при постоянном давлении, равна газовой постоянной R. Внутренняя энергия
Работа, которую совершает моль идеального газа при повышении его температуры на 1 К при постоянном давлении, равна газовой постоянной R. Внутренняя энергия
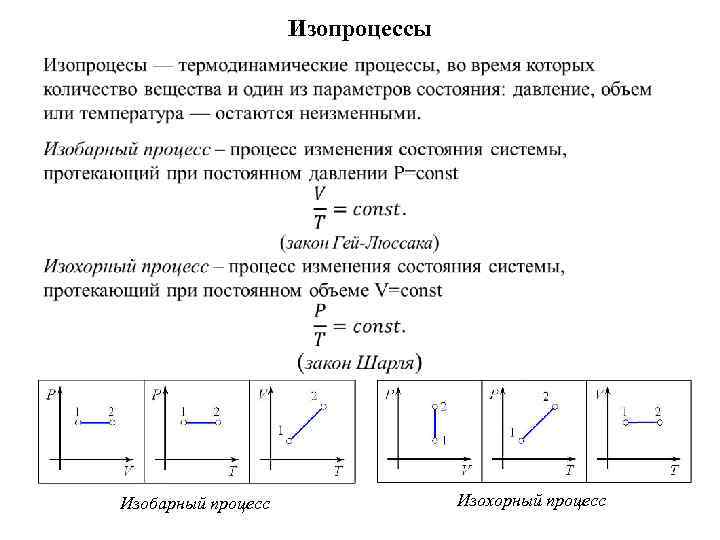 Изопроцессы Изобарный процесс Изохорный процесс
Изопроцессы Изобарный процесс Изохорный процесс
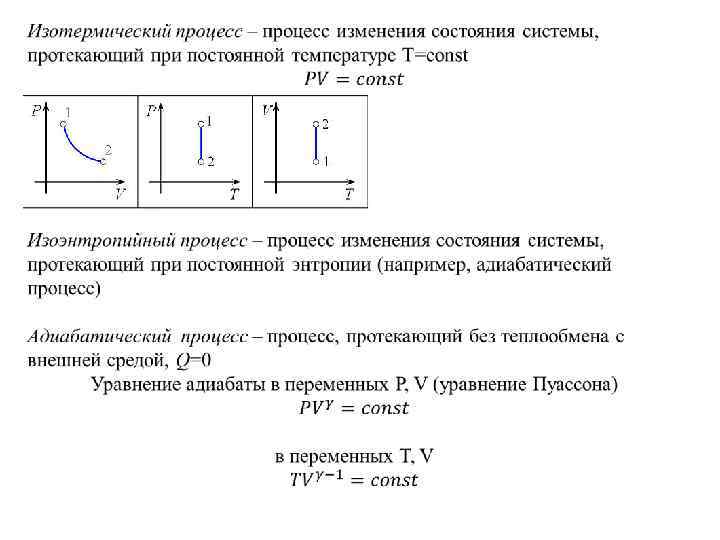
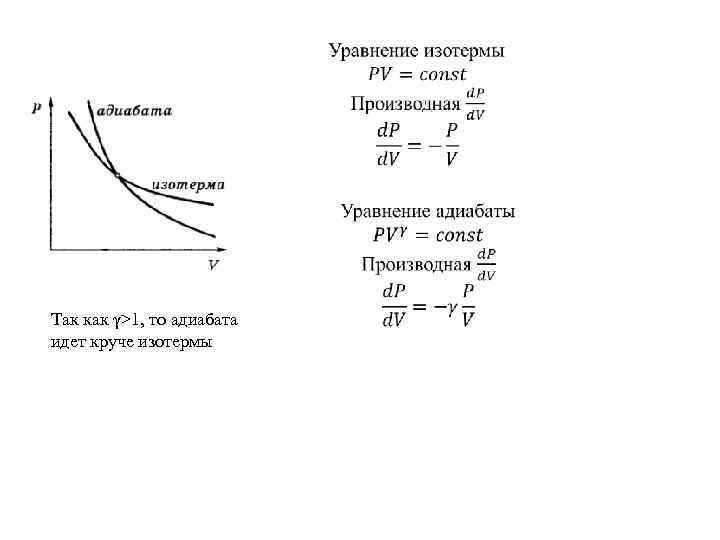 Так как γ>1, то адиабата идет круче изотермы
Так как γ>1, то адиабата идет круче изотермы
 Температура и средняя кинетическая энергия теплового движения молекул и атомов газа Идеальный газ 1). Молекулы газа настолько малы, что их суммарным объемом можно пренебречь по сравнению с объемом всего сосуда. 2). Молекулы практически не взаимодействуют друг с другом. 3). В равновесном состоянии молекулы движутся полностью хаотично (в каждом направлении X, Y, Z движется 1/3 молекул, или 1/6 в одну сторону). 4). Молекулы претерпевают упругие соударения со стенками сосуда и друг с другом.
Температура и средняя кинетическая энергия теплового движения молекул и атомов газа Идеальный газ 1). Молекулы газа настолько малы, что их суммарным объемом можно пренебречь по сравнению с объемом всего сосуда. 2). Молекулы практически не взаимодействуют друг с другом. 3). В равновесном состоянии молекулы движутся полностью хаотично (в каждом направлении X, Y, Z движется 1/3 молекул, или 1/6 в одну сторону). 4). Молекулы претерпевают упругие соударения со стенками сосуда и друг с другом.
 Давление газа на стенку сосуда где <ԑпоступ >=
Давление газа на стенку сосуда где <ԑпоступ >=
 На одну степень свободы поступательного движения приходится энергия ½k. T Число степеней свободы механической системы – количество независимых величин, с помощью которых может быть задано положение системы. Степени свободы молекулы: поступательные, вращательные, колебательные Закон равнораспределения: на каждую степень свободы молекулы приходится в среднем одинаковая кинетическая энергия, равная ½k. T Средняя энергия молекулы где i – суммарное число степеней свободы молекулы
На одну степень свободы поступательного движения приходится энергия ½k. T Число степеней свободы механической системы – количество независимых величин, с помощью которых может быть задано положение системы. Степени свободы молекулы: поступательные, вращательные, колебательные Закон равнораспределения: на каждую степень свободы молекулы приходится в среднем одинаковая кинетическая энергия, равная ½k. T Средняя энергия молекулы где i – суммарное число степеней свободы молекулы
 Так как молекулы идеального газа не взаимодействуют между собой, можно представить внутреннюю энергию одного моля идеального газа, умножив среднюю энергию одной молекулы на число молекул Величина отношения теплоемкостей определяется числом и характером степеней свободы молекулы
Так как молекулы идеального газа не взаимодействуют между собой, можно представить внутреннюю энергию одного моля идеального газа, умножив среднюю энергию одной молекулы на число молекул Величина отношения теплоемкостей определяется числом и характером степеней свободы молекулы
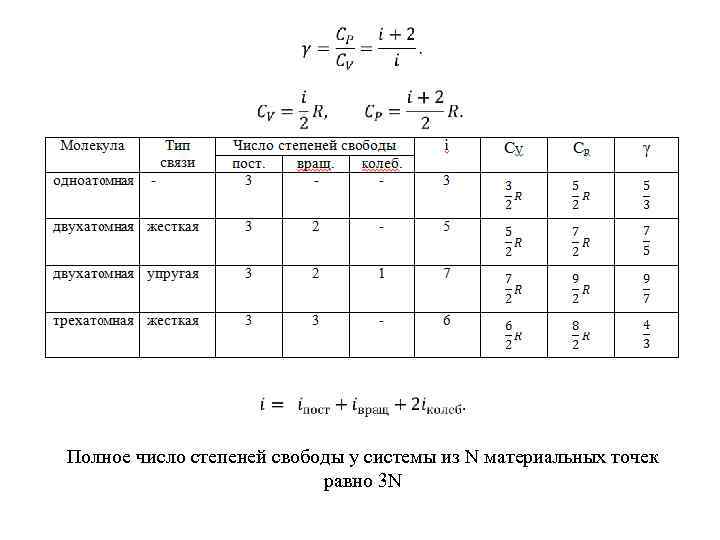 Полное число степеней свободы у системы из N материальных точек равно 3 N
Полное число степеней свободы у системы из N материальных точек равно 3 N
 Первое начало термодинамики Количество теплоты, сообщенное системе, идет на приращение внутренней энергии системы и на совершение системой работы над внешними телами Невозможен вечный двигатель первого рода, т. е. такой периодически действующий двигатель, которой совершал бы работу в большем количестве, чем получаемая им извне энергия. Второе начало термодинамики Клаузиус: невозможен самопроизвольный переход тепла от менее нагретого тела к более нагретому, или невозможны процессы, единственным результатом которых был бы переход тепла от менее нагретого тела к более нагретому. Кельвин: невозможны процессы, единственным результатом которых было бы превращение тепла целиком в работу. Невозможно создать тепловой двигатель с КПД=1.
Первое начало термодинамики Количество теплоты, сообщенное системе, идет на приращение внутренней энергии системы и на совершение системой работы над внешними телами Невозможен вечный двигатель первого рода, т. е. такой периодически действующий двигатель, которой совершал бы работу в большем количестве, чем получаемая им извне энергия. Второе начало термодинамики Клаузиус: невозможен самопроизвольный переход тепла от менее нагретого тела к более нагретому, или невозможны процессы, единственным результатом которых был бы переход тепла от менее нагретого тела к более нагретому. Кельвин: невозможны процессы, единственным результатом которых было бы превращение тепла целиком в работу. Невозможно создать тепловой двигатель с КПД=1.
 Периодически действующий двигатель, совершающий работу за счет получаемого извне тепла, называется тепловой машиной. Q 1 – поглощенное тепло, Q 2 – отдаваемое тепло. Коэффициент полезного действия (КПД) – отношение совершаемой за цикл работы к получаемому за цикл теплу Невозможен вечный двигатель второго рода, т. е. такой периодически действующий двигатель, которой получал бы тепло от одного резервуара и превращал бы это тепло полностью в работу. Тепловой резервуар – тело с бесконечно большой теплоемкостью (это означает, что передача или получение тепла от резервуара не изменяет его температуру).
Периодически действующий двигатель, совершающий работу за счет получаемого извне тепла, называется тепловой машиной. Q 1 – поглощенное тепло, Q 2 – отдаваемое тепло. Коэффициент полезного действия (КПД) – отношение совершаемой за цикл работы к получаемому за цикл теплу Невозможен вечный двигатель второго рода, т. е. такой периодически действующий двигатель, которой получал бы тепло от одного резервуара и превращал бы это тепло полностью в работу. Тепловой резервуар – тело с бесконечно большой теплоемкостью (это означает, что передача или получение тепла от резервуара не изменяет его температуру).
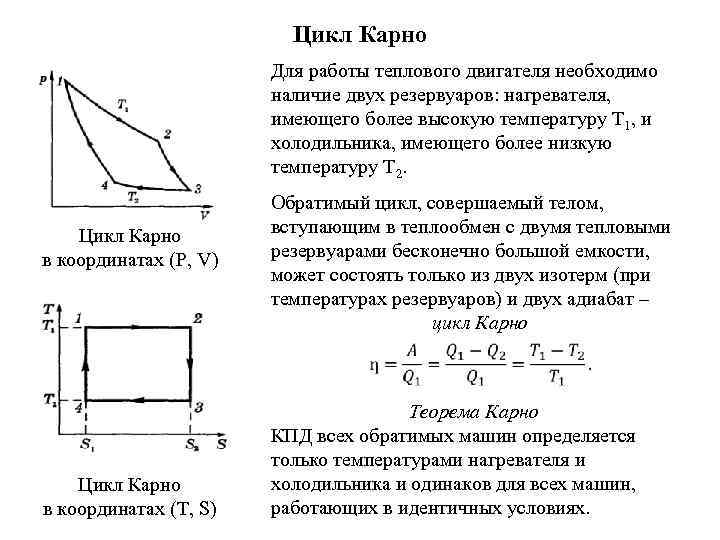 Цикл Карно Для работы теплового двигателя необходимо наличие двух резервуаров: нагревателя, имеющего более высокую температуру T 1, и холодильника, имеющего более низкую температуру T 2. Цикл Карно в координатах (P, V) Обратимый цикл, совершаемый телом, вступающим в теплообмен с двумя тепловыми резервуарами бесконечно большой емкости, может состоять только из двух изотерм (при температурах резервуаров) и двух адиабат – цикл Карно Цикл Карно в координатах (T, S) Теорема Карно КПД всех обратимых машин определяется только температурами нагревателя и холодильника и одинаков для всех машин, работающих в идентичных условиях.
Цикл Карно Для работы теплового двигателя необходимо наличие двух резервуаров: нагревателя, имеющего более высокую температуру T 1, и холодильника, имеющего более низкую температуру T 2. Цикл Карно в координатах (P, V) Обратимый цикл, совершаемый телом, вступающим в теплообмен с двумя тепловыми резервуарами бесконечно большой емкости, может состоять только из двух изотерм (при температурах резервуаров) и двух адиабат – цикл Карно Цикл Карно в координатах (T, S) Теорема Карно КПД всех обратимых машин определяется только температурами нагревателя и холодильника и одинаков для всех машин, работающих в идентичных условиях.
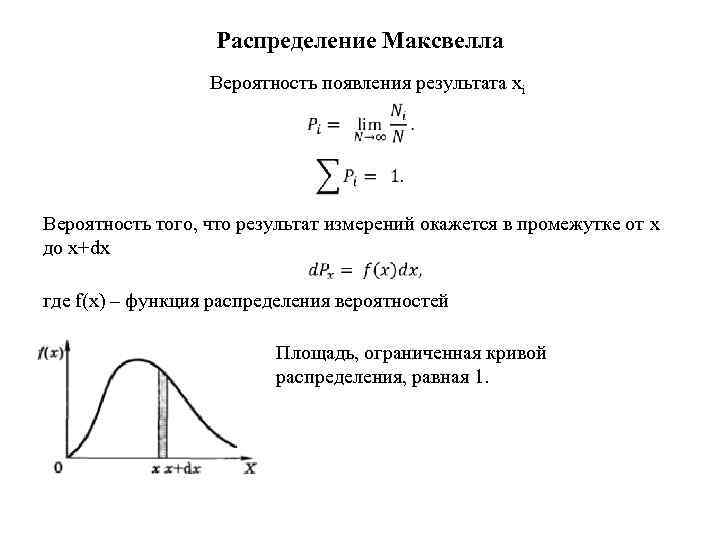 Распределение Максвелла Вероятность появления результата xi Вероятность того, что результат измерений окажется в промежутке от x до x+dx где f(x) – функция распределения вероятностей Площадь, ограниченная кривой распределения, равная 1.
Распределение Максвелла Вероятность появления результата xi Вероятность того, что результат измерений окажется в промежутке от x до x+dx где f(x) – функция распределения вероятностей Площадь, ограниченная кривой распределения, равная 1.
 Распределение Максвелла – закон распределения молекул по значениям скорости (модулям скорости) Площадь, ограниченная кривой, равна единице. Наиболее вероятная скорость (vвер) соответствует максимуму функции F(v) Средняя скорость Среднеквадратичная скорость
Распределение Максвелла – закон распределения молекул по значениям скорости (модулям скорости) Площадь, ограниченная кривой, равна единице. Наиболее вероятная скорость (vвер) соответствует максимуму функции F(v) Средняя скорость Среднеквадратичная скорость
 Зависимость распределения от температуры T 1
Зависимость распределения от температуры T 1
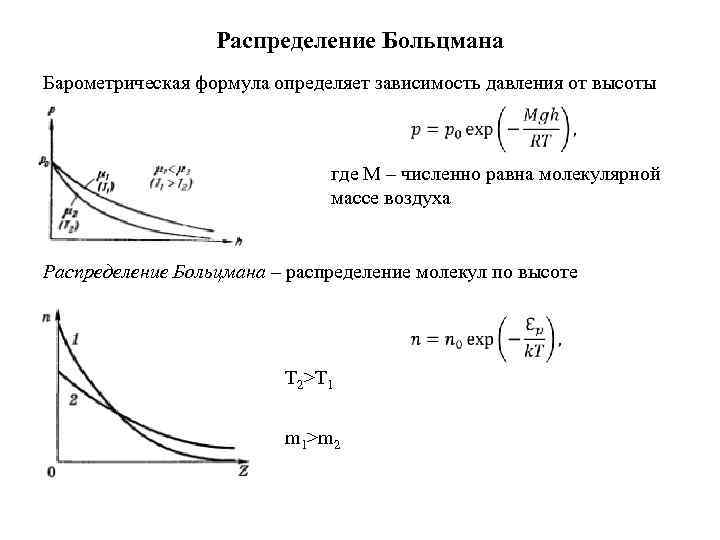 Распределение Больцмана Барометрическая формула определяет зависимость давления от высоты где M – численно равна молекулярной массе воздуха Распределение Больцмана – распределение молекул по высоте T 2>T 1 m 1>m 2
Распределение Больцмана Барометрическая формула определяет зависимость давления от высоты где M – численно равна молекулярной массе воздуха Распределение Больцмана – распределение молекул по высоте T 2>T 1 m 1>m 2
 Энтропия есть отношение элементарного количества тепла, сообщаемого системе, к температуре системы. Цикл Карно в координатах (T, S) Цикл Карно в координатах (P, V)
Энтропия есть отношение элементарного количества тепла, сообщаемого системе, к температуре системы. Цикл Карно в координатах (T, S) Цикл Карно в координатах (P, V)
 1. Энтропия – функция состояния. Адиабатический процесс (нет теплообмена с внешней средой) является изоэнтропным (S=const). 2. Энтропия аддитивна (энтропия макросистемы равна сумме энтропий ее частей). 3. Энтропия замкнутой (теплоизолированной системы) не уменьшается, т. е. либо увеличивается, либо остается постоянной. В состоянии равновесия энтропия принимает максимальное значение. 4. Если система не замкнута, то ее энтропия может как возрастать, так и убывать. 5. Теорема Нернста: приближении температуры к абсолютному нулю энтропия макросистемы также стремится к нулю. 6. Если система частиц совершает обратимый процесс и получает тепло dˈQ>0, то ее энтропия, увеличивается d. S>0. 7. Если система совершает обратимый процесс и при этом отдает тепло dˈQ<0, то ее энтропия уменьшается d. S<0. 8. Если система замкнута, т. е. не обменивается с внешней средой энергией ни в форме тепла, ни в форме работы, то энтропия такой замкнутой системы также остается постоянной при любых совершающихся в ней обратимых процессах. 9. Физический смысл имеет разность ΔS энтропии в двух состояниях системы. Чтобы определить изменение энтропии в случае необратимого перехода системы из одного состояния в другое, нужно придумать какой-нибудь обратимый процесс, связывающий начальное и конечное состояния, и найти приведенное тепло, полученное системой при таком переходе. 10. В замкнутой системе в обратимом процессе, когда система возвращается в исходное состояние, полное изменения энтропии равно нулю
1. Энтропия – функция состояния. Адиабатический процесс (нет теплообмена с внешней средой) является изоэнтропным (S=const). 2. Энтропия аддитивна (энтропия макросистемы равна сумме энтропий ее частей). 3. Энтропия замкнутой (теплоизолированной системы) не уменьшается, т. е. либо увеличивается, либо остается постоянной. В состоянии равновесия энтропия принимает максимальное значение. 4. Если система не замкнута, то ее энтропия может как возрастать, так и убывать. 5. Теорема Нернста: приближении температуры к абсолютному нулю энтропия макросистемы также стремится к нулю. 6. Если система частиц совершает обратимый процесс и получает тепло dˈQ>0, то ее энтропия, увеличивается d. S>0. 7. Если система совершает обратимый процесс и при этом отдает тепло dˈQ<0, то ее энтропия уменьшается d. S<0. 8. Если система замкнута, т. е. не обменивается с внешней средой энергией ни в форме тепла, ни в форме работы, то энтропия такой замкнутой системы также остается постоянной при любых совершающихся в ней обратимых процессах. 9. Физический смысл имеет разность ΔS энтропии в двух состояниях системы. Чтобы определить изменение энтропии в случае необратимого перехода системы из одного состояния в другое, нужно придумать какой-нибудь обратимый процесс, связывающий начальное и конечное состояния, и найти приведенное тепло, полученное системой при таком переходе. 10. В замкнутой системе в обратимом процессе, когда система возвращается в исходное состояние, полное изменения энтропии равно нулю



