Основы метаболизма.ppt
- Количество слайдов: 36

Основы метаболизма. Катаболизм углеводов. Вопросы: 1. Функции метаболизма. 2. Основные участники метаболических процессов. 3. Стадии катаболизма в клетке. 4. Переваривание углеводов. 5. Гликолиз. Основные стадии гликолиза. Энергетический выход гликолиза. 6. ЦТК( ц. Кребса). 7. Глюконеогенез. 8. Переваривание белков в процессе пищеварения. 9. Основные пути распада аминокислот. 10. Орнитиновый цикл образования мочевины.

Функции метаболизма: Ø 1. снабжение химической энергией (хемотрофы, фототрофы) Ø 2. превращение пищевых веществ в строительные блоки для построения макромолекул; Ø 3. сборка из строительных блоков белков, НК, липидов, полисахаридов; Ø 4. синтез и разрушение биомолекул, которые необходимы для выполнения специфических функций данной клетки;
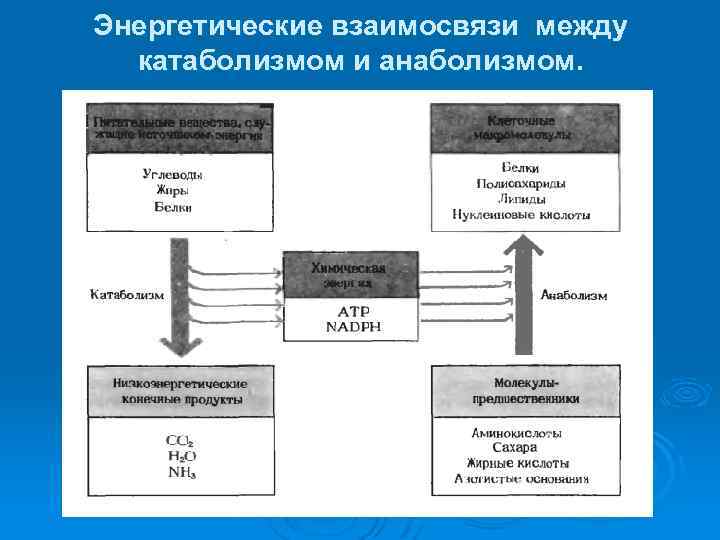
Энергетические взаимосвязи между катаболизмом и анаболизмом.

Формы передачи химической энергии Ø 1) в форме энергии фосфатных связей Ø Ø АТФ - это перемещающийся источник энергии, т. е. система АТФ АДФ - действует как одна из форм передачи химической энергии от катаболических к реакциям анаболизма, которые сопровождаются потреблением энергии. В обычной клетке АТФ расходуется в течение 1 мин после синтеза. В покое человек расходует 40 кг АТФ за сутки 0, 5 кг/мин при интенсивных физических нагрузках При гидролизе АТФ при условиях, существующих в клетке выделяется -12 ккал/моль. Ø 2) в форме энергетически богатых электронов Ø При синтезе некоторых биологических молекул, богатых водородом, например, таких как жирные кислоты, холестерин, для восстановления “=” связей требуются электроны и водород. В клетке электроны отнимаются при катаболизме в реакциях окисления, например при окислении жирных кислот. Эти электроны передаются группам, которые восстанавливаются (например, С=С, С=О), с помощью коферментов. Коферменты играют роль переносчиков электронов. Наиболее важным коферментом для переноса электронов является НАДФ, который превращается в НАДФН (или НАД в НАДН). У всех аэробных организмов существует эффективная система, обеспечивающая фосфорилирование АДФ, сопряженная с окислением НАДН молекулярным кислородом, известная как цепь переноса электронов. Ø Ø

АТФ - носитель свободной энергии в биологических системах Ø Свободная Е необходима для : 1. преобразования механической работы в мышечное сокращение и др. виды клеточного движения; Ø 2. активного транспорта молекул и ионов; Ø 3. для синтеза макромолекул из предшественников; Ø
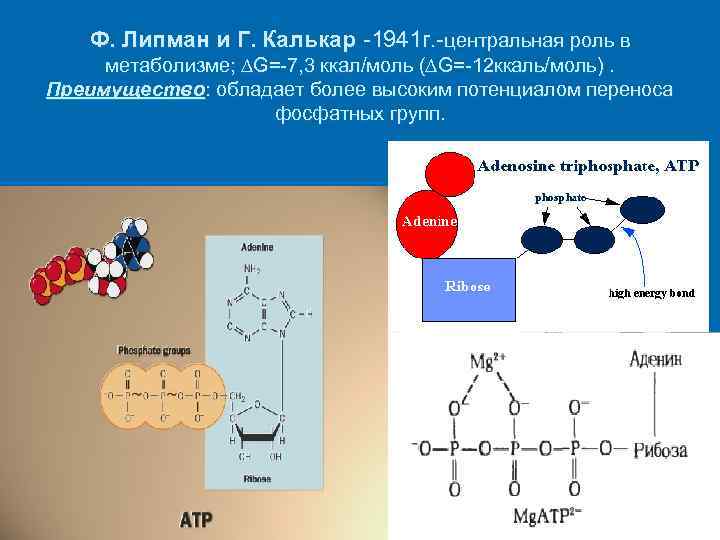
Ф. Липман и Г. Калькар -1941 г. -центральная роль в метаболизме; ∆G=-7, 3 ккал/моль (∆G=-12 ккаль/моль). Преимущество: обладает более высоким потенциалом переноса фосфатных групп.

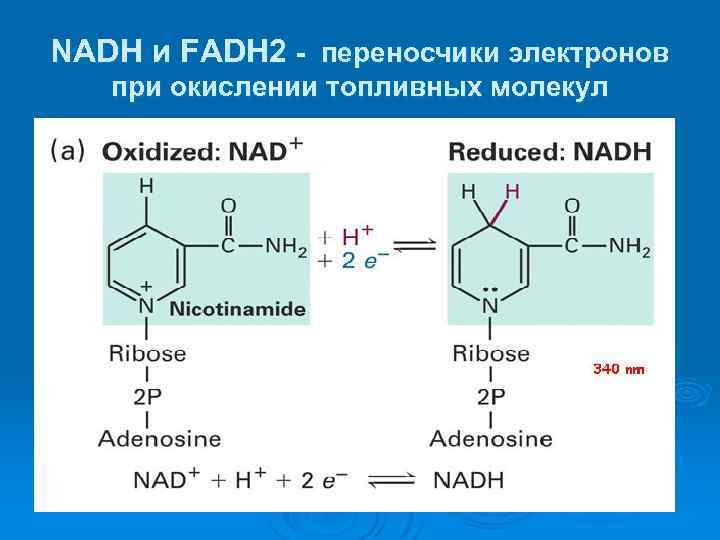
NADH и FADH 2 - переносчики электронов при окислении топливных молекул
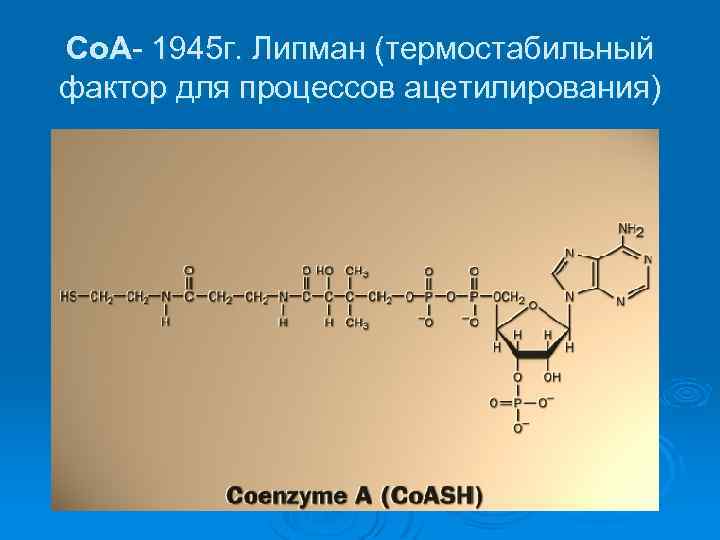
Со. А- 1945 г. Липман (термостабильный фактор для процессов ацетилирования)
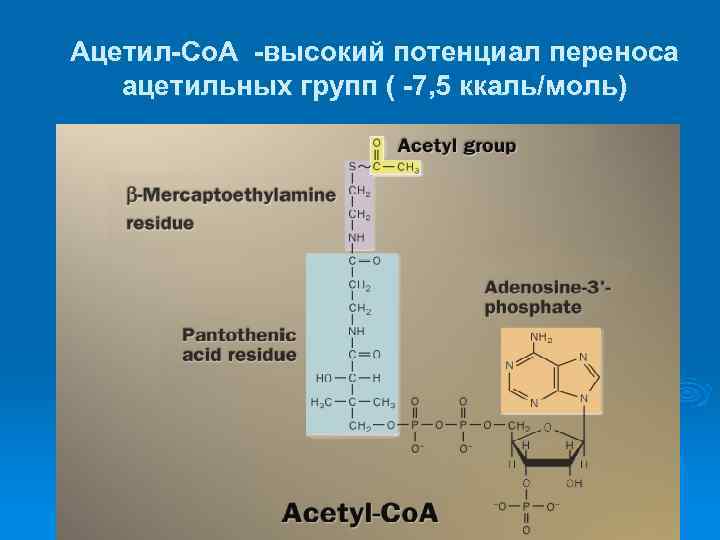
Ацетил-Со. А -высокий потенциал переноса ацетильных групп ( -7, 5 ккаль/моль)
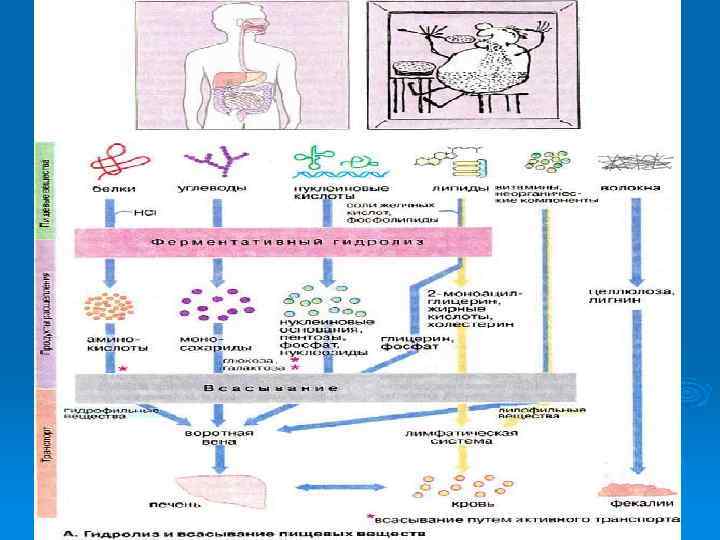
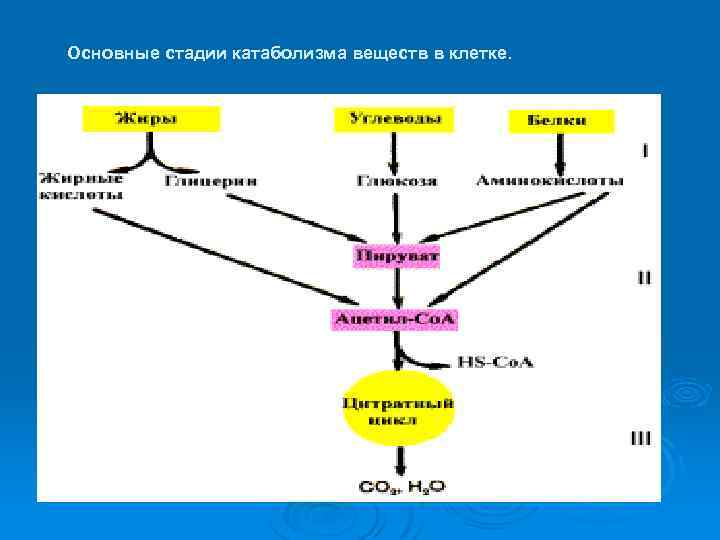
Основные стадии катаболизма веществ в клетке.
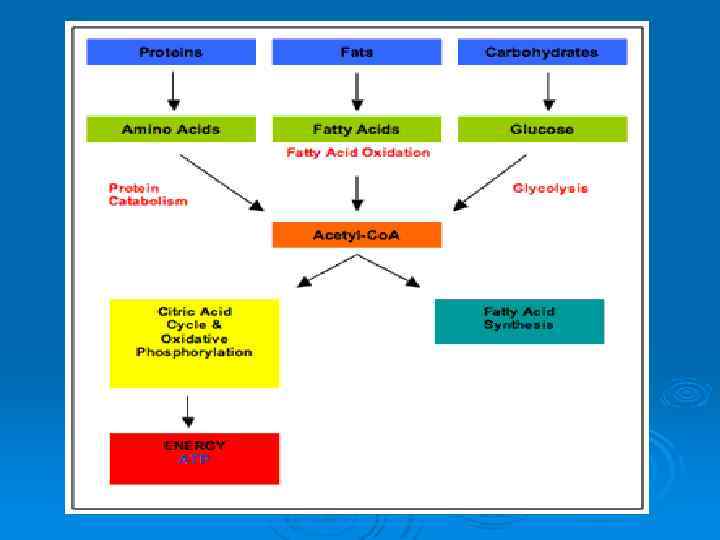
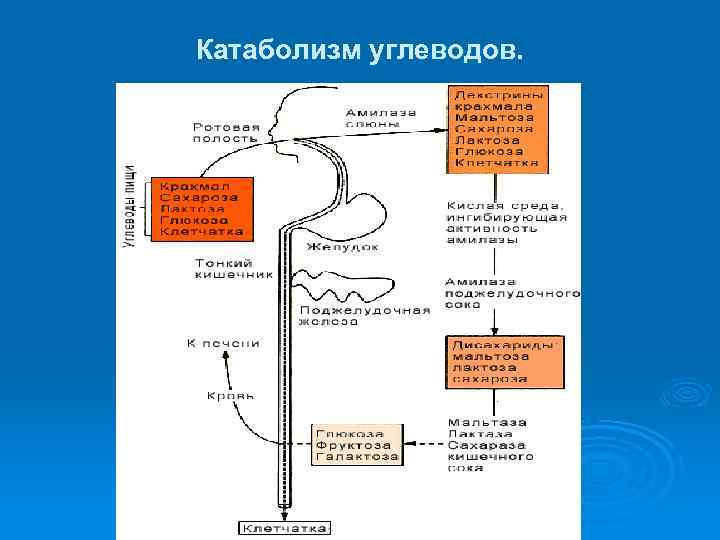
Катаболизм углеводов.

Центральная роль глюкозы объясняется: 1. высокая растворимость; Ø 2. доступная для реагирования карбонильная группа (защищена изза образования полуацеталя) Ø 3. оптимальная стабильность шестичленного пиранозного цикла. Ø Уровень глюкозы в крови 70 -80 мг/мл (через 8 -10 часов после приема пищи) Ø Концентрация глюкозы в крови определяется: Ø 1. скоростями образования глюкозы из гликогена, аминокислот ит. д. ; Ø 2. всасыванием глюкозы из кишечного тракта; Ø 3. утилизацией глюкозы; Ø 4. потерей глюкозы с мочой.

Постоянство содержания глюкозы в крови При нормальном смешанном питании: Ø 3 -5% глюкозы превращается в гликоген; Ø 30% - идет на образование жиров Ø 60 -70% окисляется до СО 2 и Н 20 Ø При обильном углеводном питании: Ø 10% глюкозы откладывается в печени в форме гликогена; Ø 40%- превращается в жиры; Ø 50%- окисляется. Ø

ГЛИКОЛИЗ Гликолиз - последовательность реакций, приводящих к превращению глюкозы с образованием 2 молекул ПИРУВАТА. Ø Локализация в клетке: цитоплазма Ø Выделяют 2 стадии гликолиза: Ø 1. подготовительная (собирательная)- вовлечение инертных гексоз в гликолиз за счет фосфорилирования; Ø 2. окислительная – энергия окисления накапливается в форме АТФ; Ø
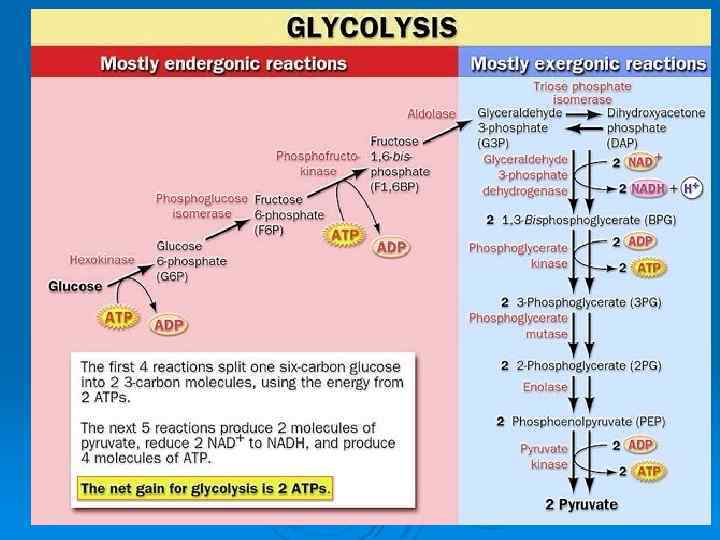
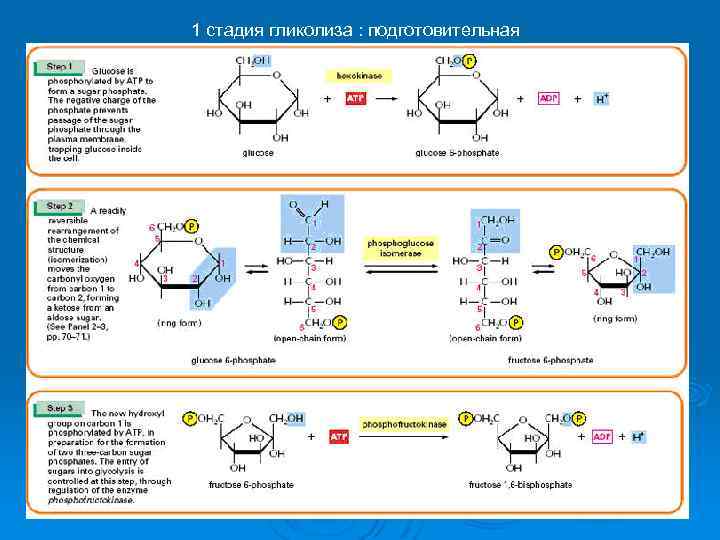
1 стадия гликолиза : подготовительная
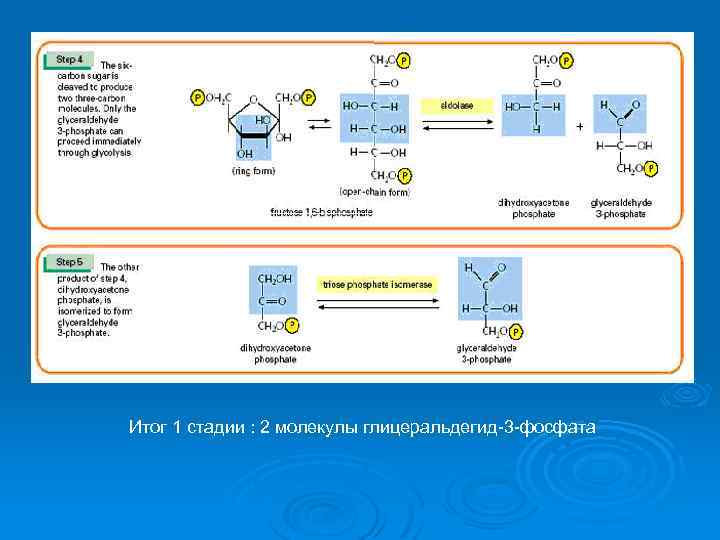
Итог 1 стадии : 2 молекулы глицеральдегид-3 -фосфата
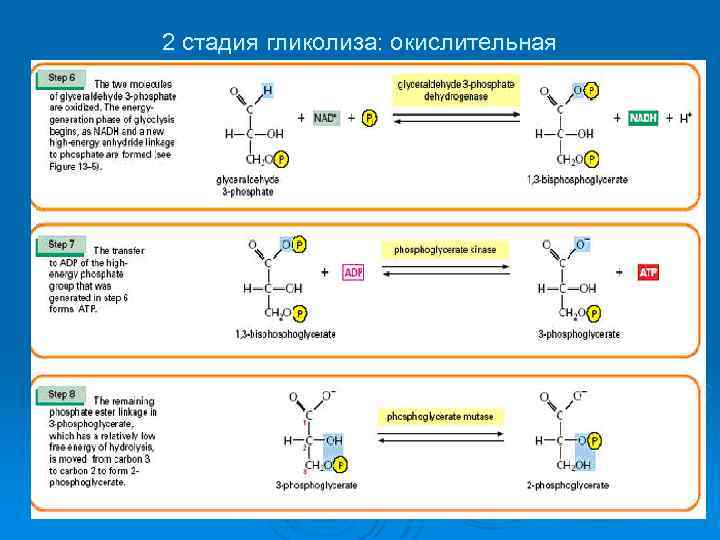
2 стадия гликолиза: окислительная
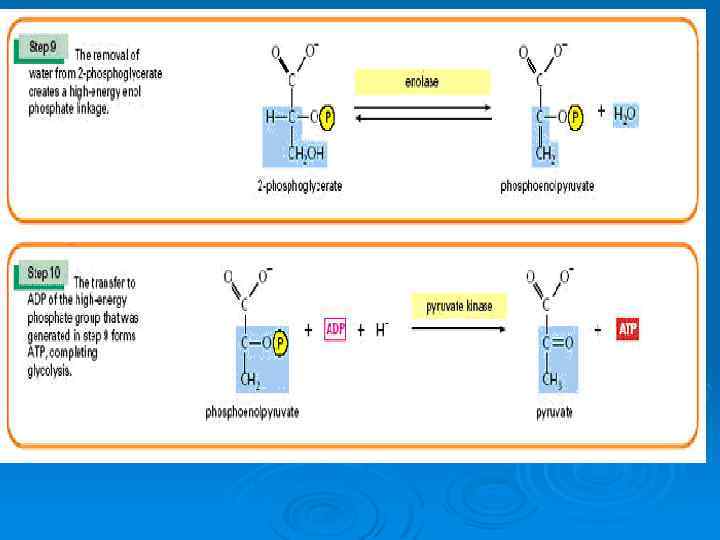
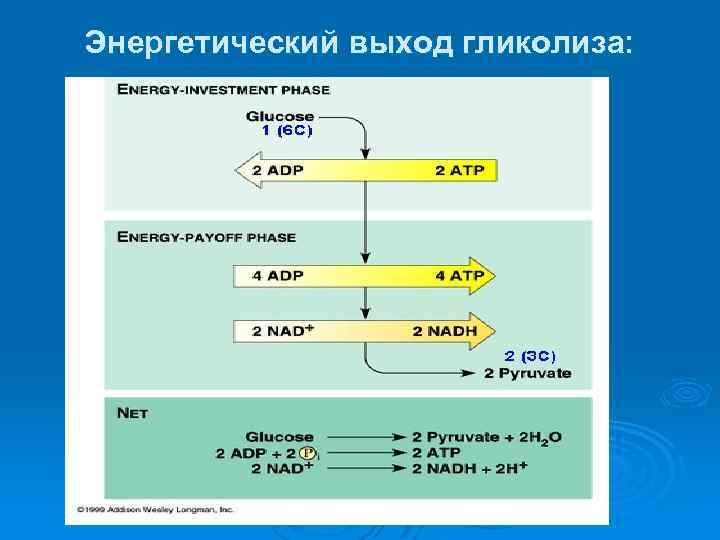
Энергетический выход гликолиза:
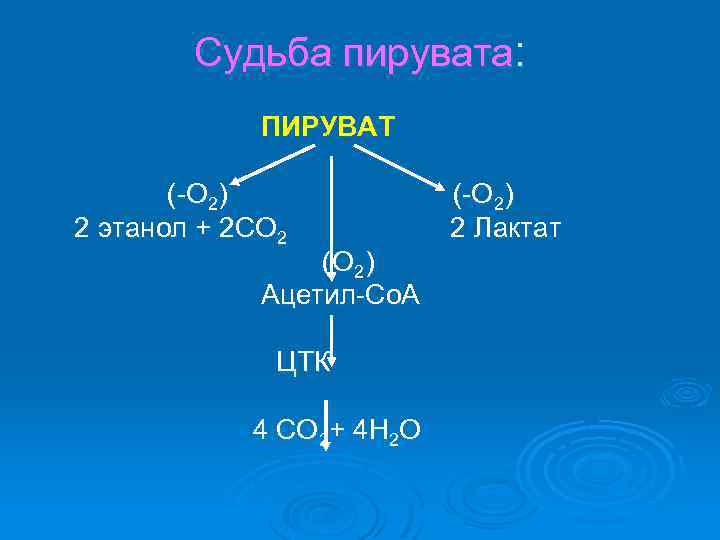
Судьба пирувата: ПИРУВАТ (-О 2) 2 этанол + 2 СО 2 2 Лактат (О 2) Ацетил-Со. А ЦТК 4 СО 2+ 4 Н 2 О
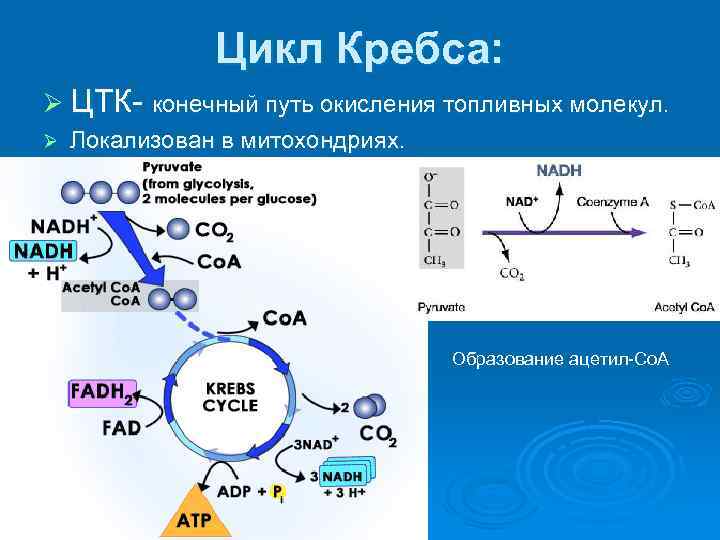
Цикл Кребса: Ø ЦТК- конечный путь окисления топливных молекул. Ø Локализован в митохондриях. Образование ацетил-Со. А
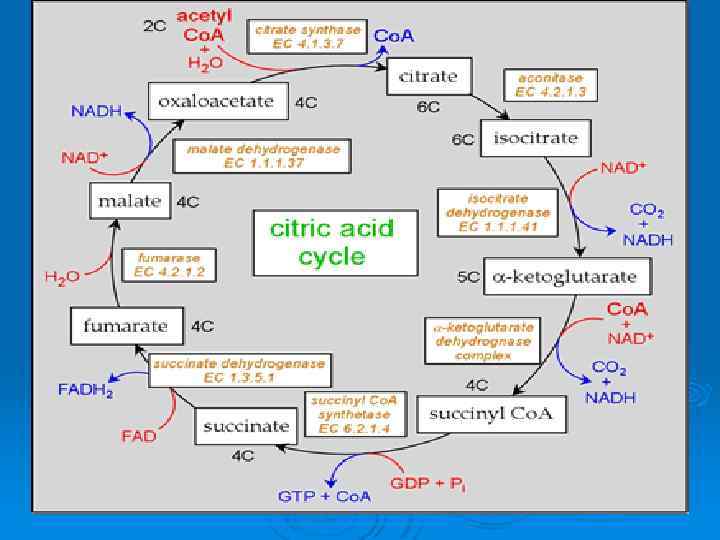
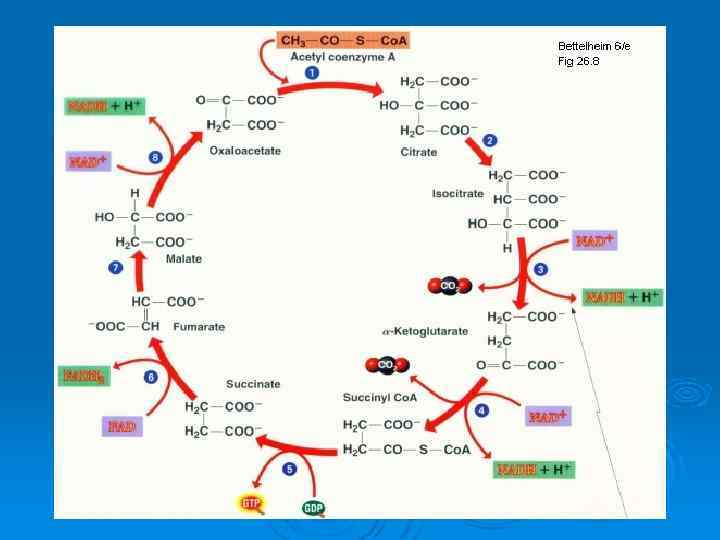
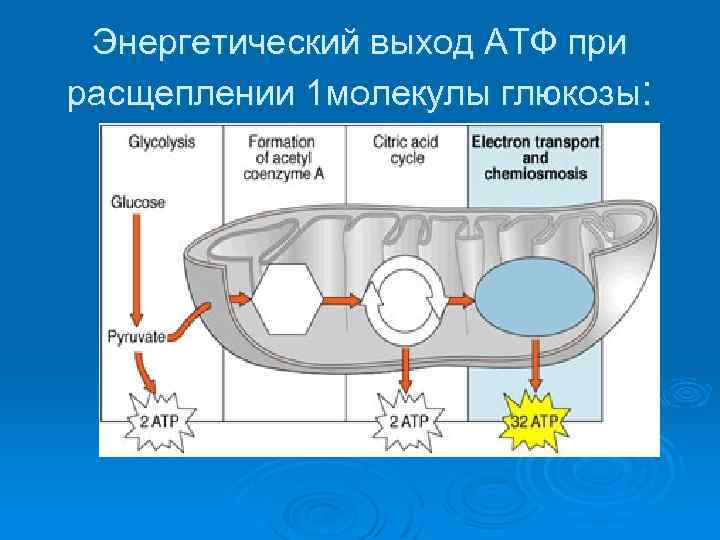
Энергетический выход АТФ при расщеплении 1 молекулы глюкозы:
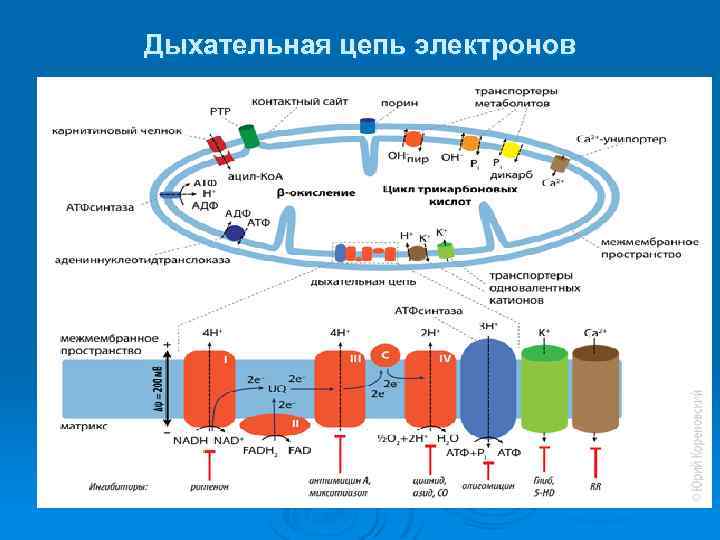
Дыхательная цепь электронов

Характеристика дыхательной цепи Дыхательная электронтранспортная цепь -система структурно и функционально связанных трансмембранных белков и переносчиков электронов. Ø ЭТЦ позволяет запасти энергию, выделяющуюся в ходе окисления НАД∙Н и ФАДН 2 молекулярным кислородом (в случае аэробного дыхания) или иными веществами (в случае анаэробного) за счёт последовательного переноса электрона по цепи, сопряжённого с перекачкой протонов через мембрану. Ø У прокариот ЭТЦ локализована в ЦПМ, у эукариот — на внутренней мембране митохондрий. Переносчики расположены по своему окислительно-восстановительному потенциалу, транспорт электрона на всём протяжении цепи протекает самопроизвольно. Ø Протонный потенциал преобразуется АТФ-синтазой в энергию химических связей АТФ. Сопряжённая работа ЭТЦ и АТФ-синтазы носит название окислительное фосфорилирование. Ø

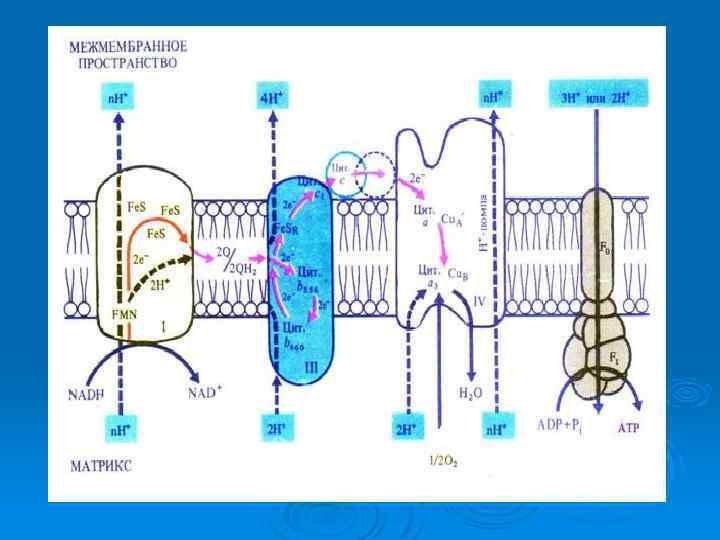
Компоненты дыхательной цепи Ø Ø Комплекс I (НАДН дегидрогеназа) окисляет НАД-Н, отбирая у него два электрона и перенося их на убихинон, который внутри мембраны диффундирует к комплексу III. Вместе с этим, комплекс I перекачивает 4 протона из матрикса в межмембранное пространство митохондрии. Комплекс II (Сукцинат дегидрогеназа) не перекачивает протоны, но обеспечивает вход в цепь дополнительных электронов за счёт окисления сукцината. Комплекс III (Цитохром bc 1 комплекс) переносит электроны с убихинола на два водорастворимых цитохрома с, расположенных на внутренней мембране митохондрии. Убихинол передаёт 2 электрона, а цитохромы за один цикл переносят по одному электрону. При этом туда также переходят 2 протона убихинола и 2 перекачиваются комплексом. Комплекс IV (Цитохром c оксидаза) катализирует перенос 4 электронов с 4 молекул цитохрома на O 2 и перекачивает при этом 4 протона в межмембранное пространство. Комплекс состоит из цитохромов a и a 3, которые, помимо гема, содержат ионы меди.
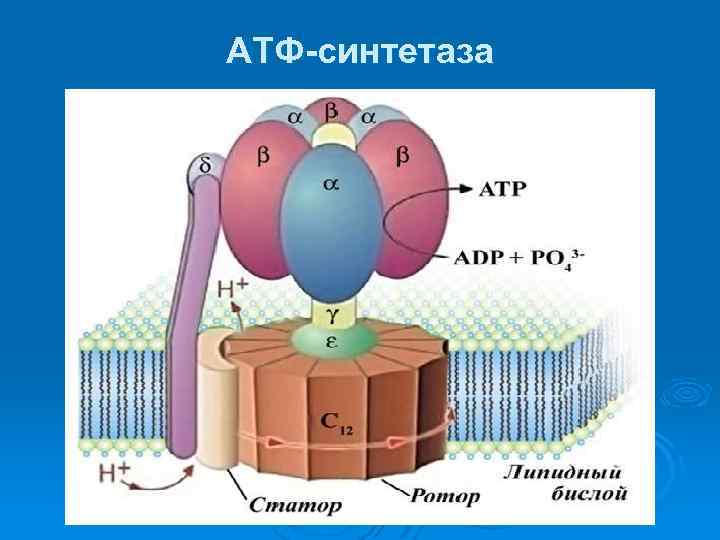
АТФ-синтетаза
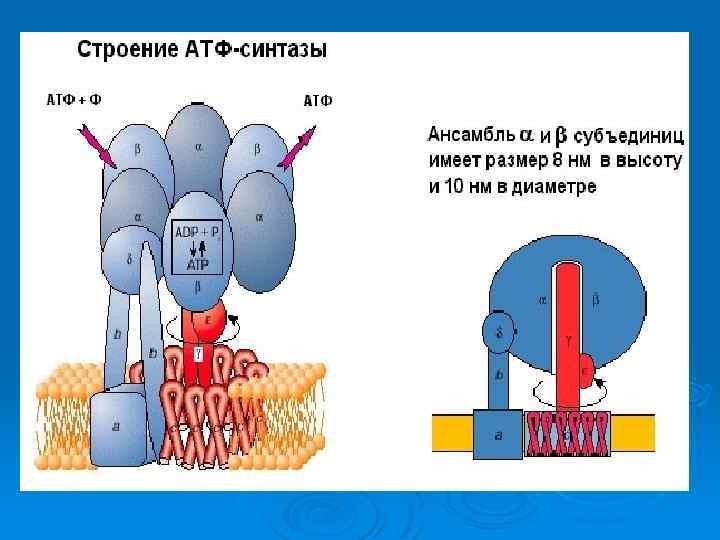

Особенности строения АТФ-азы Ø Ø Ø Фермент, который синтезирует аденозинтрифосфат (АТФ) из аденозиндифосфата (АДФ) и неорганических фосфатов. Энергию для синтеза АТФ-синтаза часто получает от протонов, проходящих по электрохимическому градиенту, например из просвета хлоропласта в его строму, или же из межмембранного пространства в матрикс митохондрии. Реакция синтеза такова: АДФ + Фн → АТФ + H 2 O АТФ-синтазы очень важны для жизнедеятельности почти всех организмов, так как АТФ — основная внутриклеточная «энергетическая валюта» . Имеющаяся в митохондриях АТФ-синтаза F 1 FO очень хорошо исследована. компонент FO — трасмембранный домен, компонент F 1 находится вне мембраны, в матриксе. АТФ-синтазный комплекс FOF 1 по форме напоминает плодовое тело гриба, у которого компонент F 1 — это шляпка, ножка — это γ-субъединица компонента F 1, а «корни» гриба — компонент FO, заякоренный в мембране. Номенклатура фермента имеет традиционное происхождение, поэтому довольно непоследовательна. Обозначение компонента F 1 является сокращением от «Fraction 1» (часть 1), а символом FO (в индексе записана буква O, а не ноль) обозначался участок связывания олигомицина. Некоторые субъединицы фермента имеют также буквенные обозначения: Греческие: α, β, γ, δ, ε Латинские: a, b, c, d, e, f, g, h
Основы метаболизма.ppt