генетика лекции.ppt
- Количество слайдов: 168

ОСНОВЫ МЕДИЦИНСКОЙ ГЕНЕТИКИ Проф. каф. мед. генетики СПб. ГПМА д. б. н. В. Н. Горбунова

Фундаментальными свойствами живой природы, отличающими ее от неживой материи, являются способность к размножению и наследственность

При этом каждый вид характеризуется определенным уровнем изменчивости, и даже братья и сестры никогда не являются точными копиями друга и своих родителей

Генетика это наука о наследственности и изменчивости. Генетические исследования можно проводить на всех уровнях организации жизни от межвидового до молекулярного

Генетика популяций занимается изучением частот мутаций и генотипов в различных популяциях, а также факторов, влияющих на их динамику

Предметом генетики развития является генетический контроль эмбриогенеза, начиная с проэмбриональных стадий созревания половых клеток до завершения дифференцировки различных тканей и органов

Цитогенетика занимается изучением структуры и морфологии отдельных хромосом и их наборов в клетках, а также построением цитогенетических карт различных элементов генома

Биохимическая генетика исследует связи между генами и органическими соединениями, присутствующими в живых организмах

Целью молекулярной генетики является исследование материальной природы генов и генома в целом, а также тех процессов, которые происходят с нуклеиновыми кислотами в клетках

Как любая другая биологическая наука генетика состоит из общих и частных разделов. В частных разделах генетики исследуются особенности проявления общих закономерностей у разных видов организмов

Среди них ведущее положение занимает генетика человека, которая включает такие же разделы, как и общая генетика. Те ее направления, которые посвящены патологии человека, являются предметом медицинской генетики

Те разделы медицинской генетики, которые используются в клинической практике или имеют потенциальное значение для такого использования называются клинической генетикой

Основными методами изучения наследования признаков у экспериментальных объектов является гибридологический анализ (система скрещиваний, позволяющая анализировать гибриды), а у человека – генеалогический анализ или анализ родословных

Основополагающие законы наследования были открыты во второй половине XIX века Грегором Менделем в опытах по скрещиванию различных сортов гороха, различающихся по форме или окраске семян и цветков

Наблюдаемые закономерности позволили Менделю высказать гипотезу о существовании двух дискретных наследственных факторов, ответственных за каждый из исследуемых признаков: доминантного – А и рецессивного – а

Рецессивный фактор не проявляется в присутствии доминантного, но он и не исчезает, и только один из этих факторов с равной вероятностью попадает в гаметы. В результате образуются растения трех типов: АА, Аа и аа в соотношении 1: 2: 1
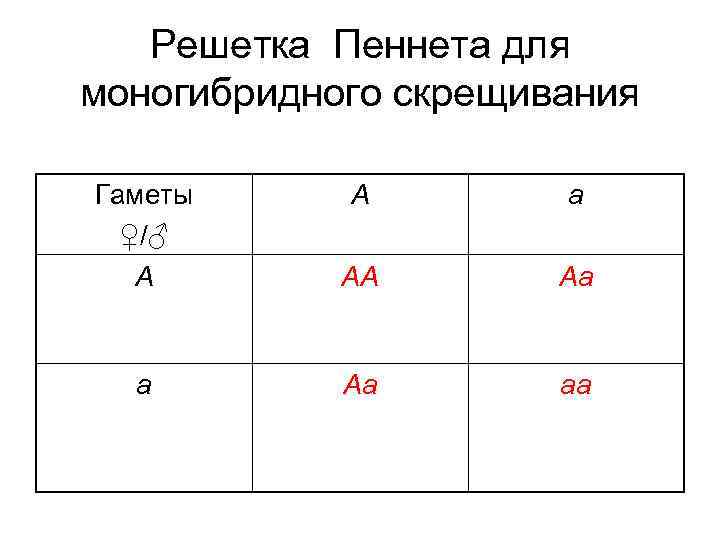
Решетка Пеннета для моногибридного скрещивания Гаметы ♀/♂ А А а АА Аа аа

В. Иогансен предложил назвать постулированные Менделем наследственные факторы генами, совокупность генов – генотипом, а совокупность признаков организма – фенотипом

Варианты наследственных факторов или альтернативные состояния генов (А, а) носят названия аллелей Аллели влияют на характер развития признаков, что и служит основой для фенотипической изменчивости

Генотип может быть гомозиготным при наличии двух одинаковых аллелей (АА или аа) или гетерозиготным, если аллели разные (Аа)


Если фенотипическая изменчивость не выходит за пределы нормы, то аллели называют нормальными. Если частоты аллелей в популяции превышают определенный уровень, их называют полиморфными или полиморфизмами

Аллели, приводящие к патологическому развитию признака, называют мутантными аллелями или мутациями.

Сочетания нормальных и мутантных аллелей всех генов человека определяют его индивидуальную наследственную конституцию. Таким образом, люди отличаются между собой не по наборам генов, а по их состояниям, то есть по наследственной конституции

Анализ родословных человека дает нам возможность судить о том, является признак наследственным и подчиняется ли он законам Менделя

Ключевая роль при делении клеток принадлежит хромосомам – таким структурам в ядрах клеток, которые в метафазе отчетливо видны при световой микроскопии и использовании специфических методов окрашивания

В соматических клетках каждая хромосома представлена двумя копиями, то есть диплоидным набором В половых клетках набор хромосом одинарный или гаплоидный Это обеспечивается за счет особой формы деления половых клеток – мейоза


Набор хромосом и их морфология являются видовыми признаками. У человека 46 хромосом, состоящих из 23 пар. 22 из них – аутосомы и 1 – половые хромосомы – X и Y. Нормальный кариотип женщины (46, XX), а мужчины - (46, XY)


В процессе мейоза происходит обмен между участками гомологичных хромосом – кроссинговер или гомологичная рекомбинация. В результате появляются гаметы, в которых хромосомы составлены из фрагментов родительских хромосом и могут иметь необычные сочетания аллелей разных генов
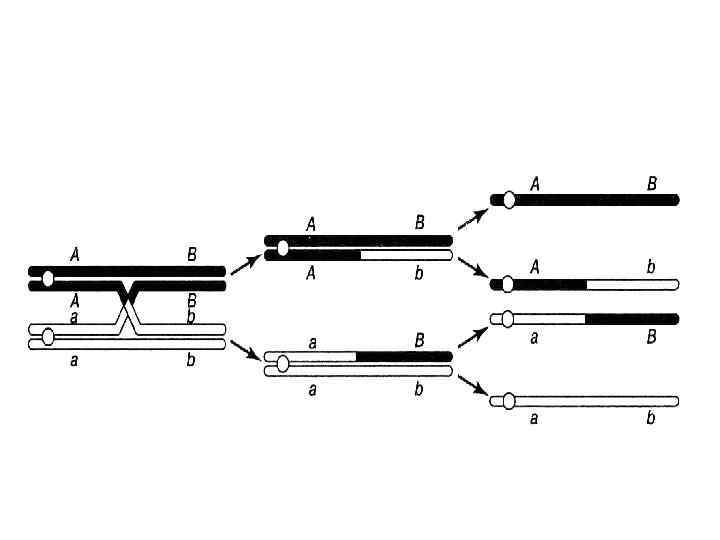

В начале XX века были получены доказательства локализации генов в хромосомах, так как их поведение соответствует поведению постулированных Менделем наследственных факторов

Появилось представление о гене, как об участке хромосомы или хромосомном локусе, который отвечает за один признак и одновременно является единицей рекомбинации и мутации, ведущей к изменению фенотипа

Хромосомы всех исследованных видов состоят из молекул ДНК и белков, большая часть из которых– до 80% – относится к специфическому классу гистонов

В середине 40 -х годов были получены доказательства того, что именно ДНК являются носителями генов или веществом наследственности

Определение пространственной организации ДНК явилось самым ярким открытием ХХ века. В 1953 г. Уотсон и Крик предложили модель, в соответствии с которой ДНК состоит из двух полимерных цепей, образующих форму двойной спирали


В основании каждой из полимерных цепей лежат последовательности из одинаковых сахаров – дезоксирибозы – соединенных между собой остатками фосфорной кислоты или фосфодиэфирной связью
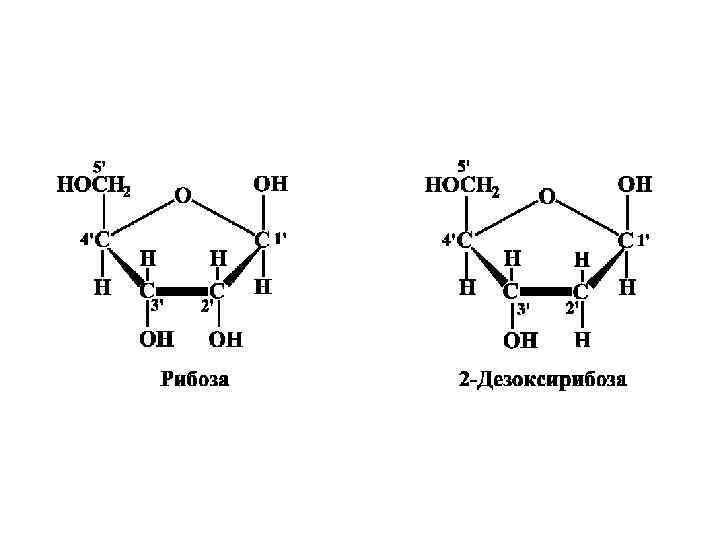

Каждый сахар, в свою очередь, соединен гликозидной связью с одним из четырех азотистых оснований: двух пуринов – аденина (A) и гуанина (G), и двух пиримидинов – цитозина (C) и тимина (T)
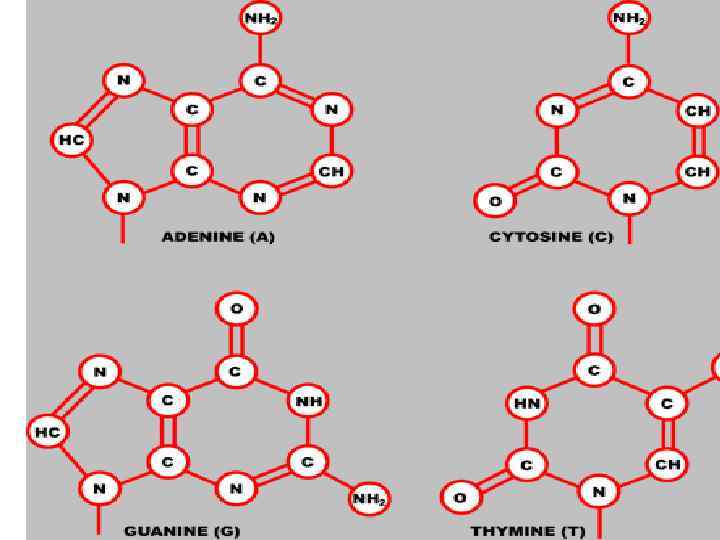

Азотистое основание, сахар и остаток фосфорной кислоты вместе составляют нуклеотид. Таким образом, цепь ДНК представляет собой последовательность нуклеотидов
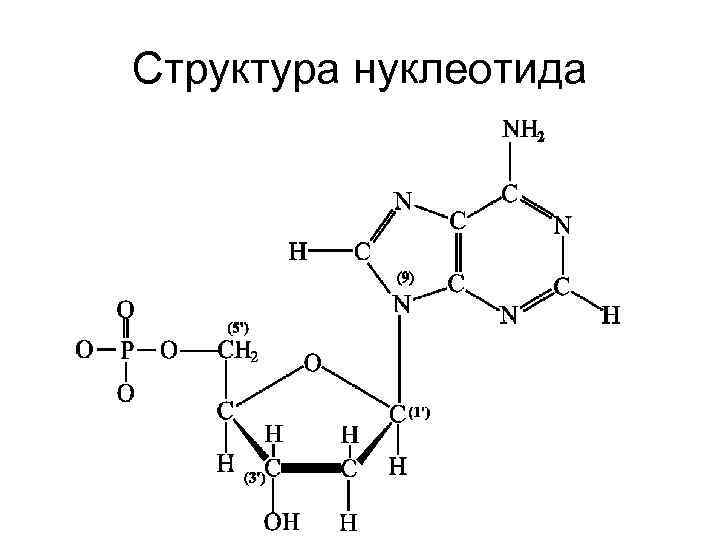
Структура нуклеотида

Две цепи ДНК удерживаются вместе за счет водородных связей между нуклеотидами. Аденин связывается с тимином, а гуанин с цитозином. Это правило – A-T, G-C называется правилом комплементарности
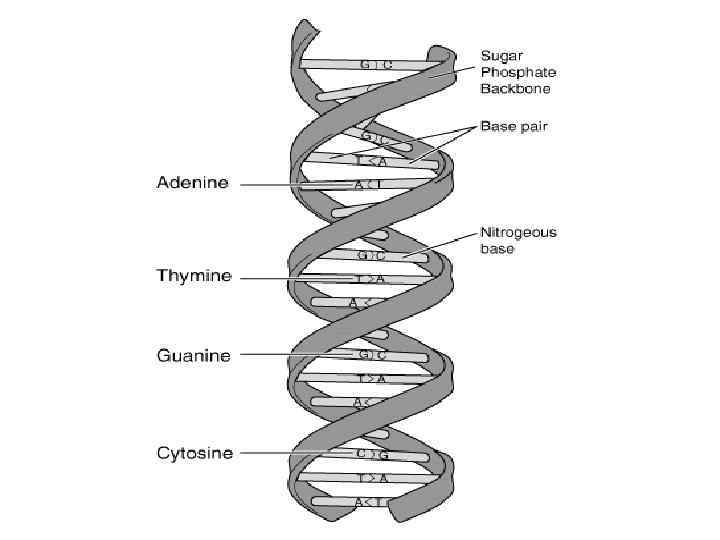

Длина молекул ДНК измеряется в нуклеотидах или в парах оснований (п. о. ). Суммарная длина молекулы ДНК человека составляет 3, 2 миллиарда п. о.

Основная масса ДНК находится в ядрах клеток в составе хромосом в суперскрученном состоянии за счет взаимодействия с гистонами. Около 1% ДНК находится в митохондриях

Хромосома – это форма упаковки ДНК в клетке. В процессе клеточного цикла длина хромосом меняется в 10 000 раз

Плотная упаковка хромосомы обеспечивается за счет образования хроматина. На этой основе формируются три универсальных уровня пространственной организации хроматина: нуклеосомный, нуклеомерный и хромомерный

Четыре пары гистонов образуют нуклеосому – основную структурную единицу хроматина, которая связывает ДНК длиной в 147 нуклеотидов. Затем нуклеосомы организуются в нуклеомеры

Три свойства отличают ДНК от всех других биологических молекул. Это способность к самовоспроизводству (репликация), кодирующая способность и изменчивость. Таким образом, ДНК – это молекулы жизни, так как они определяют ее фундаментальные свойства

Большинство генов человека кодируют белки, точнее полипептидные цепи. При экспрессии генов в клетке происходит направленный перенос генетической информации: ДНК – РНК – белок. В дифференцированных клетках одновременно экспрессируются не более 20% генов

Наборы экспрессирующихся генов в разных специализированных клетках различны. Некоторые гены работают во всех типах клеток, обеспечивая их энергетику, дыхание и другие жизненно важные процессы. Это – гены «домашнего хозяйства»
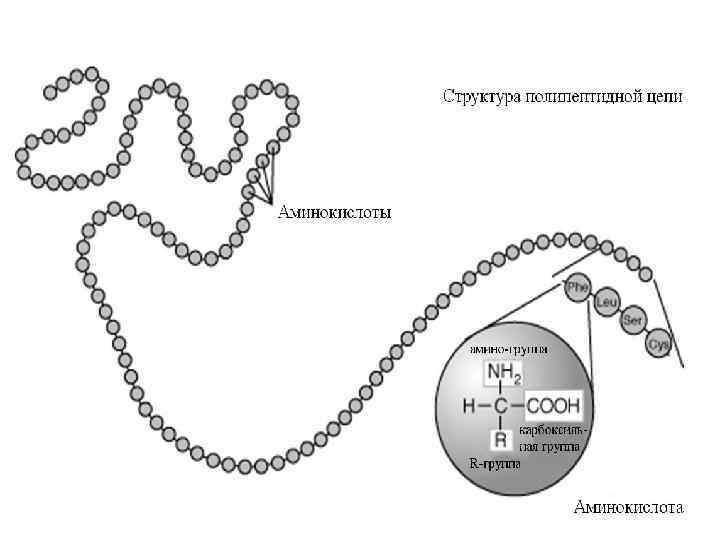

Первым шагом на пути перехода от гена к полипептидной цепи является транскрипция – синтез с помощью фермента РНК-полимеразы молекул пре. РНК, комплементарных генам

Серия модификаций превращает пре. РНК в информационную или матричную РНК – м. РНК. При этом происходят изменения на концах молекулы, обеспечивающие стабилизацию м. РНК

Главной смысловой модификацией при процессинге м. РНК является сплайсинг, то есть избирательное вырезание интронов и сшивка экзонов с образованием м. РНК
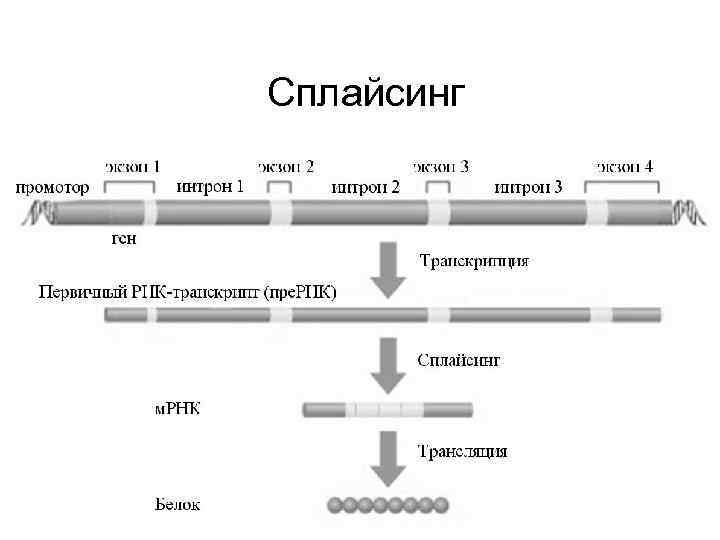
Сплайсинг

Поскольку интроны, в среднем, значительно длиннее экзонов, молекулы м. РНК могут быть в десятки раз короче молекул пре. РНК

Зрелая м. РНК переходит в цитоплазму клетки и транслируется. Трансляция – это синтез полипептидной цепи по молекуле м. РНК. Трансляция происходит на рибосомах с помощью транспортных РНК (т. РНК)

Структура т. РНК
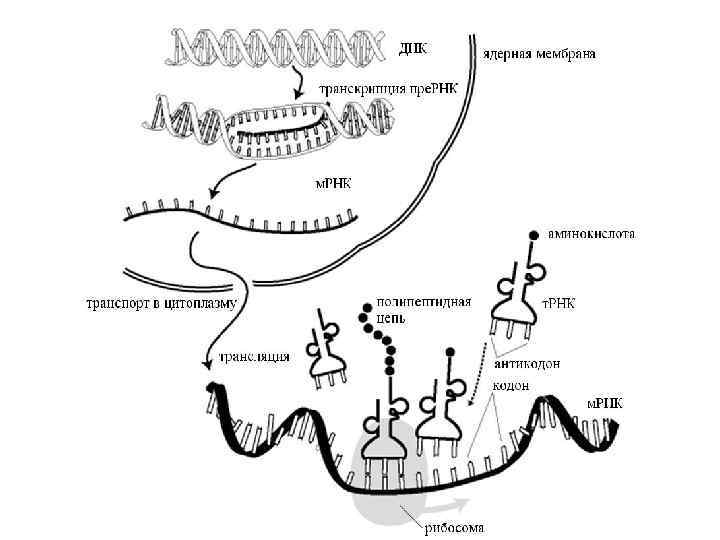

Разные типы т. РНК транспортируют разные аминокислоты в зависимости от структуры антикодона – последовательности из трех нуклеотидов, которая определяет специфичность присоединяемой аминокислоты

В месте контакта м. РНК с рибосомой, располагается кодирующий триплет или кодон. Рибосома продвигается по м. РНК постепенно – «шажками» , продвигая м. РНК сквозь себя ровно на один триплет

Таким образом, происходит специфический отбор аминокислот и их сшивка на рибосоме с образованием полипептидной цепи. Окончание синтеза кодируется любым из трех стоп- или нонсенс-кодонов

Итак, м. РНК – это последовательность нуклеотидов, полипептидная цепь – это последовательность аминокислот. По какому правилу происходит этот переход? Как называется этот центральный закон жизни?

Это генетический код – соответствие последовательности из трех нуклеотидов в м. РНК (кодона) определенной аминокислоте в полипептидной цепи, а значит и в белке
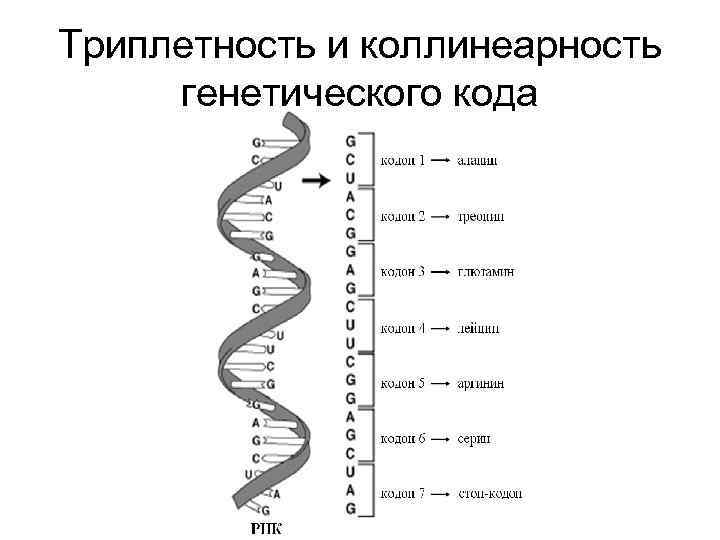
Триплетность и коллинеарность генетического кода

Свойства генетического кода • Триплетность – три нуклеотида соответствуют одной аминокислоте • Линейность – определяется линейным расположением кодонов в м. РНК • Неперекрываемость – каждый нуклеотид входит в состав своего кодона • Вырожденность – способность кодировать одну аминокислоту несколькими вариантами триплетов • Универсальность - генетический код одинаков для всего живого на Земле

Генетический код триплетен и составлен из четырех нуклеотидов. Число возможных сочетаний из четырех нуклеотидов по три в кодоне равно 64. Из них 3 соответствуют нонсенс-кодонам. Остальные варианты триплетов (61) кодируют 20 аминокислот

Это значит, что каждая аминокислота, за исключением метионина кодируется не одним, а несколькими вариантами триплетов – вырожденность генетического кода

Универсальность генетического кода является бесспорным доказательством родственности всего живого на Земле.

Конечными продуктами примерно четверти генов человека являются не белки, а рибонуклеиновые кислоты, которые не транслируются и, возможно, участвуют в регуляции работы других генов

В основе хранения и наследственной передачи информации лежит матричный принцип.

К матричным процессам наряду с транскрипцией и рекомбинацией относятся репликация, которая осуществляется с помощью фермента ДНК-полимеразы, а также репарация – исправление ошибок, возникающих при репликации ДНК

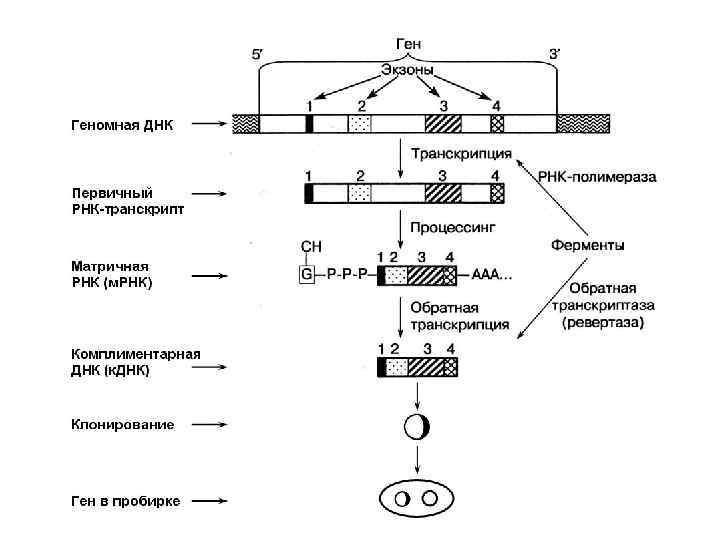
Идентификация любого гена предполагает его изоляцию и последующее клонирование кодирующей области гена, так называемой, молекулы комплементарной ДНК – к. ДНК

к. ДНК образуется путем обратной транскрипции РНК с помощью фермента обратной транскриптазы. При использовании в качестве матрицы м. РНК получают к. ДНК, состоящую только из экзонов, то есть представляющий собой кодирующую часть гена

При клонировании этой к. ДНК получают «ген в пробирке» . Клонирование – это встраивание чужеродной ДНК в векторную молекулу и введение этой конструкции в клетки-хозяина, чаще всего в бактериальные клетки

Клонирование – это основной метод генной инженерии, в частности гено-инженерного производства лекарственных препаратов, таких как инсулин, интерферон и др. ДНК, составленные из фрагментов разного происхождения, называются рекомбинантными ДНК

«Ген в пробирке» - это удобная система, которая дает возможность определять нуклеотидную последовательность кодирующей части гена, производить искусственный синтез в системе in vitro кодируемого геном белка, получать антитела к этому белку и осуществлять переход на белковый уровень анализа

Открытие гена означает не только получение «гена в пробирке» , но идентификацию первичного биохимического дефекта и первичной патологической метаболической цепи, а затем создание на этой базе предпосылок для разработки патогенетических методов лечения

Мутациями называются любые изменения последовательности нуклеотидов в молекуле ДНК. Применительно к наследственным заболеваниям мутациями называются такие нарушения в структуре ДНК, которые приводят к патологическому развитию соответствующих признаков

Мутации спонтанно возникают в любых популяциях с частотами 10 -8– 10 -9 на один ген за одно поколение. Причины их возникновения, чаще всего, остаются неизвестными

Ионизирующее облучение и некоторые химические соединения увеличивают частоту возникновения мутаций. При повторном облучении мутагенный эффект суммируется. Химический мутагенез прямо зависит от дозы и продолжительности обработки

Мутации, возникающие de novo: (1) в гаметах приводят к гонадному мозаицизму, (2) в клетках зародыша – к соматическому мозаицизму, (3) в соматических клетках в специфических генах – к канцерогенезу
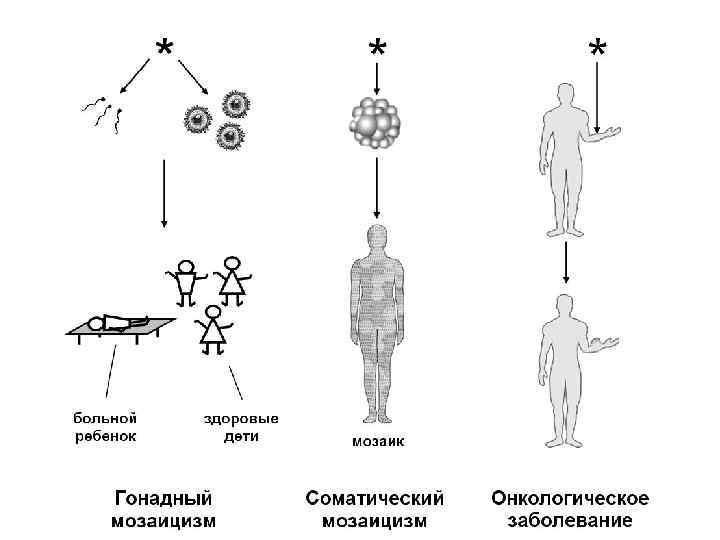

Мутации могут быть геномными, хромосомными и генными. Числовые хромосомные мутации затрагивают целые хромосомы. К ним относятся полиплоидии – изменения гаплоидного набора хромосом и анеуплоидии – моносомии, трисомии, полисомии

Структурные хромосомные перестройки затрагивают не целые хромосомы, а их фрагменты. Они связаны с возникновением одной или нескольких точек разрыва хромосом, которые приводят к потере или перегруппировке генетического материала

Потери участка хромосом называют делециями, вставки – инсерциями, удвоения – дупликациями, поворот участка хромосомы – инверсиями, а перенос фрагмента одной хромосомы на другую – транслокациями

Транслокации могут быть сбалансированными, при которых не происходит утраты генетического материала, и несбалансированными, когда часть генетического материала при переносе фрагментов хромосом теряется
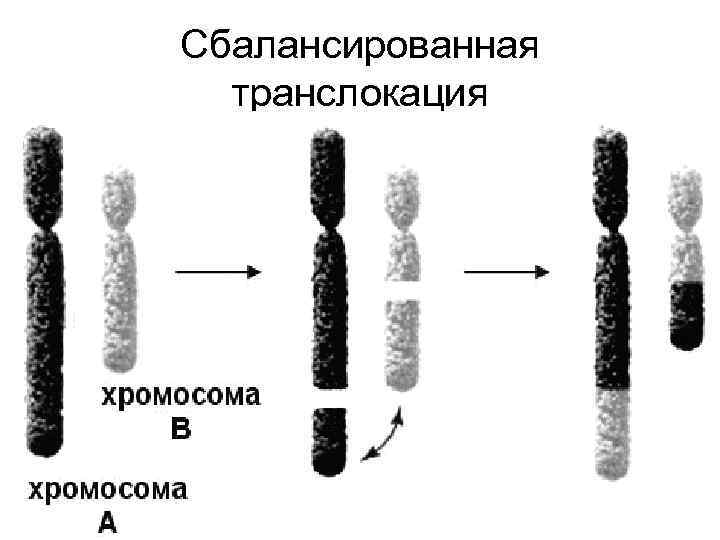
Сбалансированная транслокация

Присутствие сбалансированных транслокаций обычно не влияют на жизнеспособность их носителей. Однако в этом случае велика вероятность бесплодия, спонтанного прерывания беременности, мертворождений и рождения ребенка с хромосомной болезнью

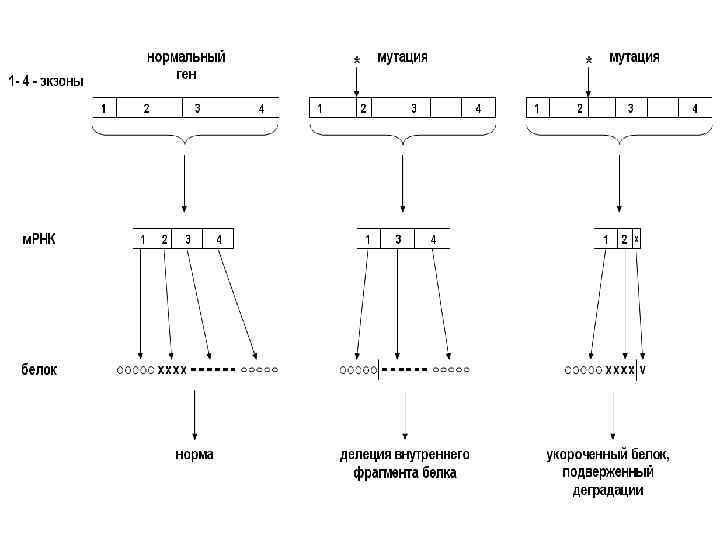
К генным мутациям относятся любые изменения последовательности нуклеотидов в пределах гена, включая структурные перестройки, затрагивающие от одного до нескольких нуклеотидов или экзонов (структурные мутации), а также замены нуклеотидов

Наиболее тяжелыми по последствиям являются структурные мутации со сдвигом рамки считывания, при которых велика вероятность преждевременного прекращения трансляции и деградация мутантного белка
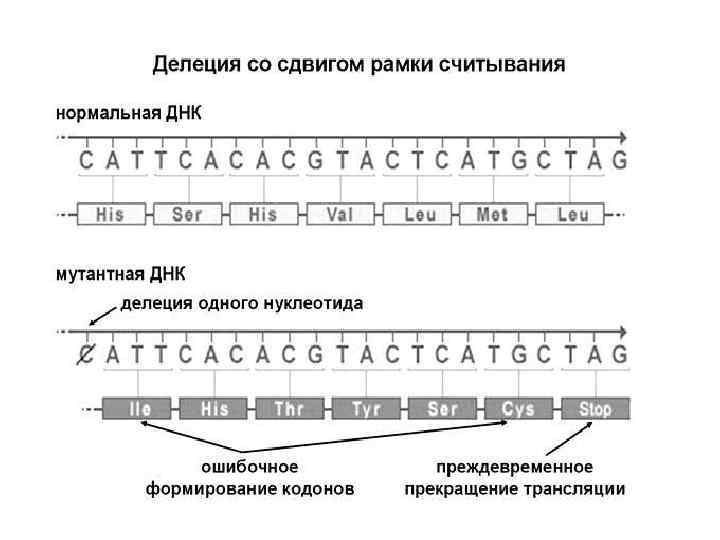

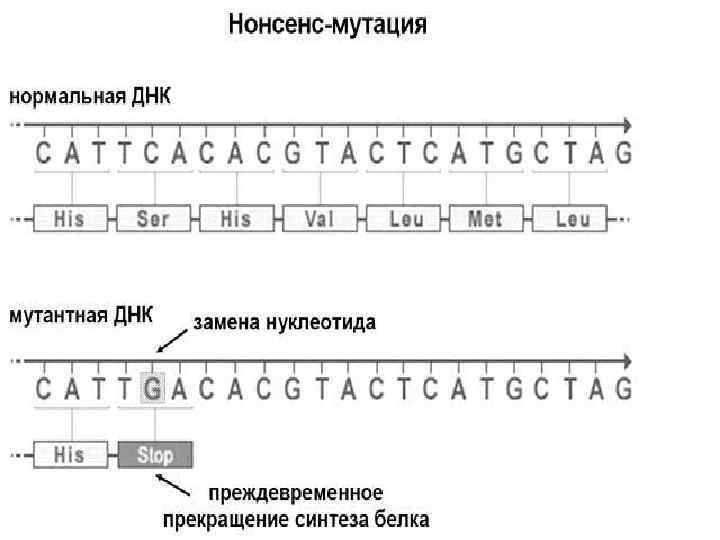
Замены нуклеотидов относятся к точковым мутациям. Они могут быть нейтральными без изменения структуры белка, нонсенс-типа с образованием преждевременного стоп-кодона и миссенс-типа с заменой аминокислоты в белке

Нейтральные замены относятся к классу нормальных аллелей, и они могут с высокими частотами встречаться в популяциях. Последствия нонсенс-мутаций сопоставимы с теми, которые происходят при мутациях со сдвигом рамки считывания – преждевременное прекращение синтеза белка и его деградация
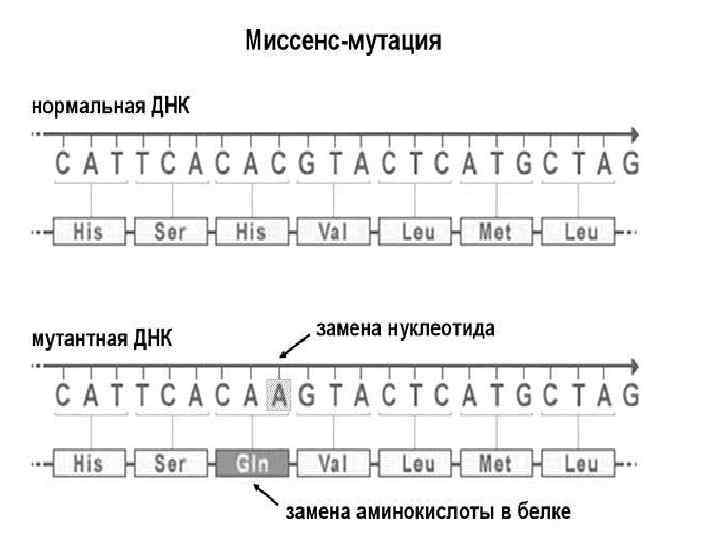

Последствия миссенсмутаций могут быть очень разными в зависимости от места расположения подобной замены и функциональной значимости соответствующего участка белка

Мутации в регуляторных областях гена приводят лишь к количественным нарушениям, при этом структура белка сохраняется нормальной. Поэтому регуляторные полиморфные замены чаще ассоциированы не с моногенной, а с многофакторной патологией

Широкое распространение имеют сплайсинговые мутации. Они могут приводить либо к ошибочному вырезанию экзона, либо к сохранению в составе м. РНК интрона, содержащего стоп -кодоны. Сплайсинговые мутации часто ассоциированы с тяжелыми патологическими состояниями

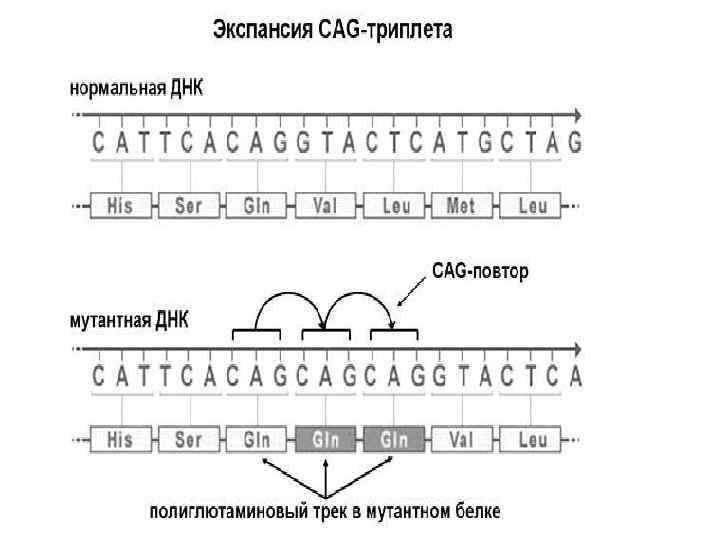
К новому типу относятся динамические мутации – увеличение (или экспансия) выше допустимого предела числа повторов, расположенных в функционально значимых областях генов. Заболевания, обусловленные динамическими мутациями, называются болезнями экспансии

В конце ХХ века молекулярные технологии развивались настолько интенсивно, что были созданы предпосылки для планомерного изучения нуклеотидных последовательностей ДНК разных видов живых существ, включая человека

Таким образом, родилась новая наука – геномика. Начало нового тысячелетия ознаменовалось крупнейшим открытием в области геномики – расшифрована структура генома человека, то есть определена нуклеотидная последовательность молекулы ДНК человека

Под геномом понимается полная генетическая система, обеспечивающая функционирование клетки и наследственную передачу в ряду поколений всех ее свойств. В молекулярной генетике геном и ДНК часто используют как синонимы

Главным итогом завершения международного проекта «Геном человека» является идентификация всех генов человека и определение аминокислотных последовательностей кодируемых ими белков

В настоящее время интенсивно изучается ассоциация этих генов с различными патологическими состояниями человека и, в первую очередь, с наследственными болезнями


Расшифровка структуры генома человека привела к сенсационному открытию. Оказалось, что в геноме человека только 32 000 генов, что в несколько раз меньше количества белков. При этом белок-кодирующих генов только 20 -22 000, продуктами остальных генов являются молекулы РНК

Процент сходства по нуклеотидным последовательностям ДНК между разными индивидуумами, этническими группами и расами составляет 99, 9%. Это сходство и делает нас людьми – Homo sapiens!

Процент сходства по нуклеотидным последовательностям ДНК между разными индивидуумами, этническими группами и расами составляет 99, 9%. Это сходство и делает нас людьми – Homo sapiens!

Но, посмотрим друг на друга – мы все разные. Около 100 000 мутаций в кодирующей части генома определяют изменчивость человека. В среднем 3 -4 мутации на ген

Подавляющее большинство этих мутаций, около 70%, определяет нашу индивидуальную непатологическую изменчивость, то, что нас отличает, но не делает хуже по отношению друг к другу

Около 5% мутаций ассоциированы с моногенными заболеваниями, количество нозологических форм которых достигает 5000. Эти болезни могут затрагивать любые системы, ткани и органы человека, но объединены они потому, что в основе каждого из них лежат мутации в одном гене

Около четверти оставшихся мутаций относятся к классу функциональных полиморфизмов. Они участвуют в формировании наследственной предрасположенности к широко распространенной многофакторной патологии

Молекулярно-генетические методы основаны на анализе нуклеиновых кислот. Их основной целью является диагностика мутаций, исследование их ассоциации с наследственными заболеваниями, а также выявление гетерозиготных и гомозиготных носителей мутации

Преимуществом ДНКдиагностики является использование унифицированного набора методов, практически, не зависящих от целей исследования. Главными из них являются выделение ДНК, полимеразная цепная реакция и электрофорез

ДНК можно выделять из любых типов клеток, содержащих ядра. У человека геномную ДНК чаще всего выделяют из лейкоцитов, для чего производят забор из вены от 1 до 5 мл крови в присутствии антикоагулянтов

Дальнейшие этапы заключаются в выделении ядер, протеолитическом разрушении белков и разделении высокомолекулярных фракций ДНК и низкомолекулярных фракций, содержащих фрагменты белков, липиды, углеводы и другие компоненты ядер

Более современными являются сорбентные методы изоляции ДНК. Клетки подвергают лизису с детергентами, а затем добавляют в эту смесь сорбент, (силикагель), на который осаждается ДНК. После отмывки сорбента ДНК смывают в малом объеме водного раствора

Внедрению молекулярной генетики в медицину способствовала разработка более 20 лет тому назад Керри Мулисом метода полимеразной цепной реакции (ПЦР) или специфической амплификации ДНК

ПЦР позволяет тестировать состояния генов у отдельных индивидуумов. Его суть заключается в избирательном копировании in vitro небольшого фрагмента ДНК, в котором может быть локализована мутация, с использованием в качестве матрицы геномной ДНК обследуемого

Небольшие размеры копируемого (или амплифицируемого) фрагмента гена в сочетании с их огромным числом позволяют в дальнейшем использовать простые методы анализа этого участка ДНК и выявления его особенностей у больного

ПЦР проводится в одноразовых пробирках в маленьком объеме, не превышающем 10 -50 мкл. Для проведения реакции необходимо искусственно синтезировать небольшие (от 15 до 30 п. о. ) однонитевые молекулы ДНК – праймеры, комплементарные концам амплифицируемого фрагмента ДНК

Праймеры служат «затравкой» для синтеза ДНК и потому определяют его специфичность. Синтез проводят с помощью термофильной ДНК-полимеразы в присутствии четырех типов дезоксинуклеотидтрифосфатов (d. NTP)

На первом этапе матричную ДНК переводят в однонитевую форму путем нагревания раствора выше 95 градусов в течение нескольких минут

Затем начинают циклически чередовать три кратковременные процедуры, длящиеся несколько десятков секунд: (1) гибридизация (отжиг) исследуемой ДНК с праймерами (2) синтез ДНК и (3) денатурация синтезированной ДНК. Затем все повторяют, начиная с процедуры (1)

Гибридизация ДНК с праймерами происходит при охлаждении раствора до 30 -50 градусов. Синтез ДНК, начиная с праймера, происходит при повышении температуры раствора до значений, оптимальных для работы термофильной ДНК-полимеразы – 55 -70 градусов

Денатурация синтезированной ДНК достигается повышением температуры раствора свыше 90 градусов. После проведения 25 -30 подобных циклов количество вновь синтезированных фрагментов ДНК достигает или даже превышает миллион копий
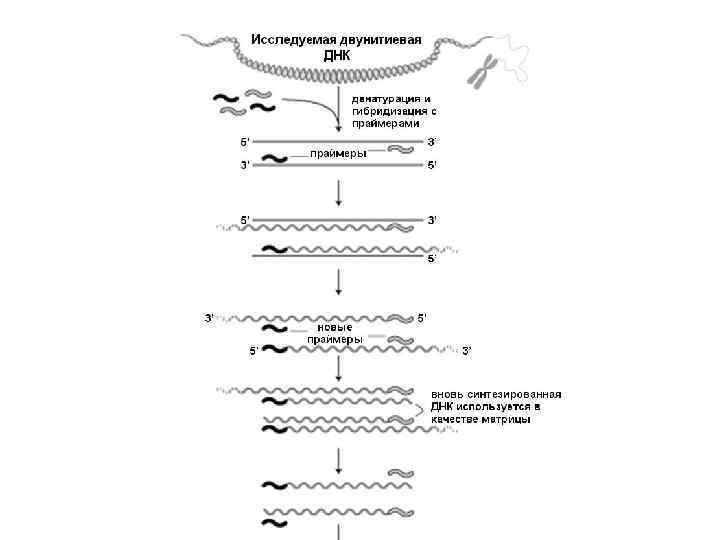

Циклическая смена температур производится автоматически в приборе, который называется амплификатор ДНК или термоциклер

Молекулярная диагностика мутаций зависит от характера повреждения гена. Наиболее просто диагностируются делеции и инсерции, так как они изменяют длину, а значит, и электрофоретическую подвижность амплифицируемого фрагмента ДНК

Для диагностики таких мутаций достаточно провести ПЦР с использованием специфических праймеров и электрофорез, а затем сопоставить длину амплифицированного фрагмента ДНК в норме и у больного

Количества ДНК, синтезируемой в процессе ПЦР, достаточно для ее визуальной оценки после помещения геля в раствор со специфическим красителем, каковым является этидиум бромид

После окрашивания ДНК начинает светиться красным цветом при просмотре геля под ультрафиолетовой лампой. Обычно гели с окрашенной ДНК фотографируют, и соответствующие негативы подвергают более тщательному анализу для идентификации всех полос ДНК
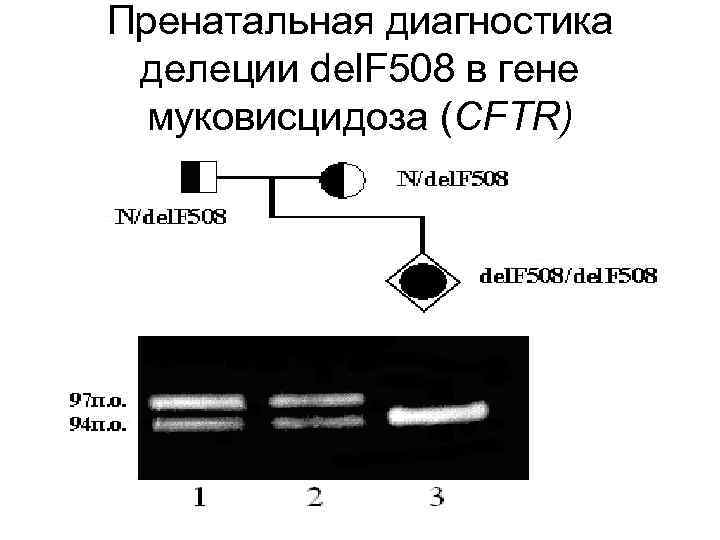
Пренатальная диагностика делеции del. F 508 в гене муковисцидоза (CFTR)

Для молекулярной диагностики точковых мутаций миссенс- или нонсенс-типа используются более сложные методы, такие как, рестрикционный анализ или метод аллель-специфических олигонуклеотидов (АСО)

Рестриктазы или эндонуклеазы – это бактериальные ферменты, катализирующие разрезание двунитевых ДНК в местах локализации специфических последовательностей из 4 -12 нуклеотидов, которые называются сайтами узнавания или сайтами рестрикции

В настоящее время идентифицировано более 500 рестриктаз, каждая из которых характеризуется своим сайтом узнавания

Огромное количество сайтов рестрикции, достаточно равномерно распределенных по всему геному, позволяет во многих случаях осуществлять ДНК диагностику заболеваний, связанных с однонуклеотидными заменами

Если мутация случайным образом изменяет естественный сайт узнавания для определённой рестриктазы, фермент утрачивает способность разрезания ДНК в данном месте

В этом случае мутантный и нормальный ПЦР-продукты, обработанные выбранной рестриктазой, дадут разные по длине фрагменты рестрикции, что можно легко обнаружить при проведении электрофореза

Разработаны компьютерные программы, позволяющие проводить идентификацию сайтов рестрикции в области локализации мутации. При успешном поиске, клиническая диагностика мутации проводится методом рестрикционного анализа

Он включает три последовательные процедуры: (1) ПЦР, (2) рестрикцию амплифицированного фрагмента ДНК с использованием специфической эндонуклеазы и (3) электрофорез
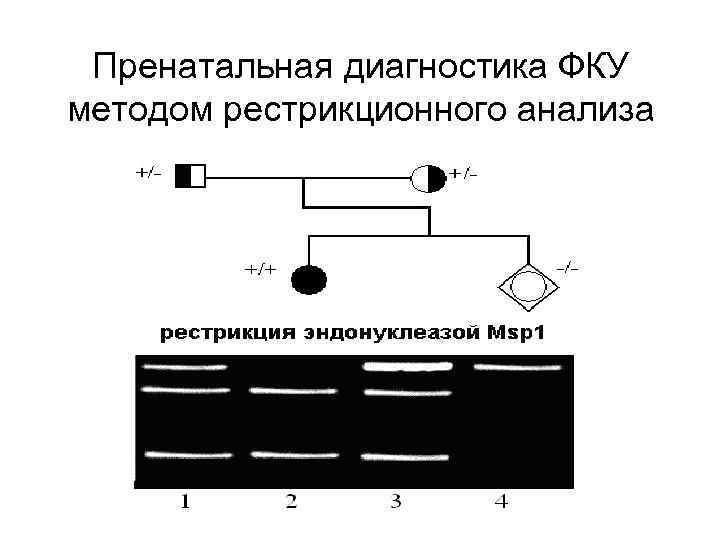
Пренатальная диагностика ФКУ методом рестрикционного анализа

Последний метод требует ДНК-зондов – олигонуклеотидных ДНК, используемых для поиска комплементарных последовательностей

Метод АСО более трудоемкий и требует использования ДНКзондов, но он универсальный и поддается автоматизации. На его базе разработаны технологии, позволяющие одновременно тестировать десятки или даже сотни мутаций

При этом используются микрочиповые нанатехнологии, то есть меченные олигонуклеотидные ДНК-зонды в небольшом количестве наносятся на твердые носители (биочипы), а затем проводится их гибридизация с исследуемыми образцами ДНК

ПЦР лежит в основе ДНКдиагностики любых наследственных заболеваний. Данный подход широко используется и для анализа генетических факторов риска, предрасполагающих к развитию широко распространенных многофакторных заболеваний

При молекулярной диагностике инфекций амплифицируется фрагмент ДНК, специфичный для определенного возбудителя, а затем с помощью электрофореза тестируется наличие этого фрагмента, а значит и самого возбудителя, в том биологическом образце, который был взят для анализа

ПЦР широко используется в молекулярной онкологии для диагностики мутаций в онкогенах и супрессорах опухолей в нормальных и патологических тканях больного

Использование ПЦР в судебной медицине основано на амплификации высоко изменчивых областей генома, позволяющих проводить идентификацию личности – метод геномной дактилоскопии
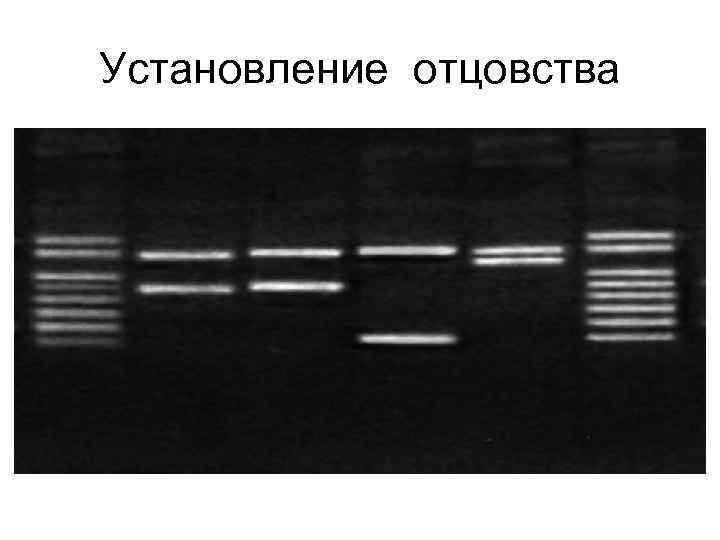
Установление отцовства

Методология молекулярногенетического анализа Широко используется в фармакогенетике с целью изучения влияния наследственной конституции на метаболизм различных лекарственных препаратов

Методология молекулярногенетического анализа лежит в основе генной терапии – лечения путем введения смысловых последовательностей ДНК

В настоящее время традиционные методы молекулярно-генетического анализа все больше вытесняются исследованиями по сканированию состояния и экспрессии всего генома

Разработаны высокотехнологичные методы нового поколения, позволяющие одновременно проводить идентификацию до миллиона генетических маркеров (SNPs) – методология GWAS (Genome. Wide Association Scan)

Такие исследования проводятся на больших выборках больных в различных этнических и возрастных группах. Они позволяет более эффективно отбирать генетические факторы риска, ассоциированные с определенными многофакторными заболеваниями

Полногеномные исследования позволяют оценивать не только структурные особенности молекул ДНК при различных патологических состояниях, но и одновременно определять характер экспрессии десятков тысяч генов, то есть получать экспрессионные профили генов

Подобные исследования проводятся при сердечнососудистых, онкологических, аутоиммунных и многих других заболеваниях. Сопоставляются профили экспрессии генов на разных этапах онтогенеза, в различных специализированных тканях, в различные возрастные периоды жизни человека

Таким образом, полногеномные исследования расширяют возможности дифференциальной диагностики больных и разработки методов персонифицированной терапии

Области использования генетических методов в медицине • Клинико-генеалогическмй анализ и медикогенетическое консультирование семей больных • Цитогенетический анализ и диагностика хромосомных болезней • Диагностика и профилактика моногенных болезней • Молекулярная идентификация мутаций и пренатальная диагностика • Определение генетических факторов риска многофакторной патологии

Области использования генетических методов в медицине • Идентификация личности в судебной медицине • Молекулярная диагностика инфекций • Анализ онкогенов и супрессоров опухолей в онкологии • Определение индивидуальной чувствительности к лекарственным препаратам в фармакогенетике • Разработка патогенетических методов лечения, включая генную терапию
генетика лекции.ppt