электронный учебник.pptx
- Количество слайдов: 27
 Основы материаловедения Журавлёва Л. А.
Основы материаловедения Журавлёва Л. А.
 СОДЕРЖАНИЕ Глава 1. Общие свойства металлов § 1. Свойства и классификация металлов и сплавов. Лабораторная работа № 1 «Изучение микроструктур сплавов» § 2. Деформация металла. § 3. Химическая и термическая обработка металлов. Глава 2. Черные металлы § 4. Железо. Сплавы, классификация, свойства, состав. Лабораторная работа № 2 « Свойства железа и его сплавов» . § 5. Маркировка, применение, требование к качеству. Практическая работа № 1 «Марки черных сплавов» . Глава 1. Цветные металлы. § 6. Медь и её сплавы. Лабораторная работа № 3 « Свойства цветных металлов и сплавов» . § 7. Группы цветных металлов: Zn, Sn, Pb, Ni свойства, применение. § 8. Группы цветных металлов: Аl, Cd, Hg свойства, применение. Практическая работа № 2 «Цветные металлы» Глава 3. Благородные металлы § 9. Благородные металлы. § 10. Au, Ag, Pt: свойства, применение, месторождение. § 11. Pd , Rh, Ru, Ir, Os: свойства, применение, месторождение. § 12. Сплавы драгоценных металлов. Лабораторная работа № 4 « Свойства благородных металлов и сплавов» . § 13. Маркировка, проба, требование. § 14. Художественные материалы, назначение, виды. Практическая работа № 3 «Визуальное определение физических свойств» . Практическая работа № 4 «Пробы драгоценных металлов» . . Лабораторная работа № 5 «Подбор материалов для выполнения ювелирных и художественных работ» Глава 4. Ювелирные камни § 15. Свойства ювелирных камней. § 16. Классификация ювелирных камней. § 17. Самоцветы. § 18. Цветные камни. § 19. Органические камни. § 20. Искусственные камни. § 21. Стекло. Пластические массы. § 22. Кость, рог, кожа, дерево. § 23. Текстиль, резина, фарфор. Глава 5. Вспомогательные материалы § 24. Кислоты. § 25. Щелочи, соли. § 26. Пробирные реактивы. § 27. Огнеупорные материалы. § 28. Клеи. Флюсы. § 29. Припои, отбелы. Лабораторная работа № 6 « Подбор проб на основании характеристик золотых и серебряных припоев» Практическая работа № 5 «Вычисление проб и лигатур» , Практическая работа № 6 «Подбор солей используемых в качестве пробирного вещества» . с о д е р ж а н и е
СОДЕРЖАНИЕ Глава 1. Общие свойства металлов § 1. Свойства и классификация металлов и сплавов. Лабораторная работа № 1 «Изучение микроструктур сплавов» § 2. Деформация металла. § 3. Химическая и термическая обработка металлов. Глава 2. Черные металлы § 4. Железо. Сплавы, классификация, свойства, состав. Лабораторная работа № 2 « Свойства железа и его сплавов» . § 5. Маркировка, применение, требование к качеству. Практическая работа № 1 «Марки черных сплавов» . Глава 1. Цветные металлы. § 6. Медь и её сплавы. Лабораторная работа № 3 « Свойства цветных металлов и сплавов» . § 7. Группы цветных металлов: Zn, Sn, Pb, Ni свойства, применение. § 8. Группы цветных металлов: Аl, Cd, Hg свойства, применение. Практическая работа № 2 «Цветные металлы» Глава 3. Благородные металлы § 9. Благородные металлы. § 10. Au, Ag, Pt: свойства, применение, месторождение. § 11. Pd , Rh, Ru, Ir, Os: свойства, применение, месторождение. § 12. Сплавы драгоценных металлов. Лабораторная работа № 4 « Свойства благородных металлов и сплавов» . § 13. Маркировка, проба, требование. § 14. Художественные материалы, назначение, виды. Практическая работа № 3 «Визуальное определение физических свойств» . Практическая работа № 4 «Пробы драгоценных металлов» . . Лабораторная работа № 5 «Подбор материалов для выполнения ювелирных и художественных работ» Глава 4. Ювелирные камни § 15. Свойства ювелирных камней. § 16. Классификация ювелирных камней. § 17. Самоцветы. § 18. Цветные камни. § 19. Органические камни. § 20. Искусственные камни. § 21. Стекло. Пластические массы. § 22. Кость, рог, кожа, дерево. § 23. Текстиль, резина, фарфор. Глава 5. Вспомогательные материалы § 24. Кислоты. § 25. Щелочи, соли. § 26. Пробирные реактивы. § 27. Огнеупорные материалы. § 28. Клеи. Флюсы. § 29. Припои, отбелы. Лабораторная работа № 6 « Подбор проб на основании характеристик золотых и серебряных припоев» Практическая работа № 5 «Вычисление проб и лигатур» , Практическая работа № 6 «Подбор солей используемых в качестве пробирного вещества» . с о д е р ж а н и е
 § 1. Свойства и классификация металлов и сплавов. Детальное изучение свойств и характеристик материалов, с которыми должен работать ювелир, необходимо для правильной и качественной их обработки. В производстве ювелирных изделий необходимо в первую очередь учитывать физические свойства металлов и сплавов, плотность, температуру плавления, тепловое расширение, теплопроводность, отражательную способность. Знание этих свойств позволяет правильно выбрать термические режимы литья, ковки, прокатки, пайки и других видов горячей обработки металлов. Важное значение при различных методах изготовления металлических деталей ювелирных украшений, оправ драгоценных камней, столовых приборов и посуды из сплавов благородных металлов имеют их основные механические свойства. К ним относятся: прочность, твердость, упругость, пластичность. Твердость способность металла оказывать сопротивление проникновению в него другого, более твердого тела. Наиболее распространены два способа определения твердости: Бринелля и Роквелла. Прочность способность металла сопротивляться разрушению под действием внешних сил. Для определения прочности образец металла установленной формы и размера испытывают на наибольшее разрушающее напряжение при растяжении, которое называют пределом прочности (временное сопротивление) и обозначают Σв (сигма). Пластичность способность металла, не разрушаясь, изменять форму под нагрузкой и сохранять ее после прекращения действия нагрузки. При испытании на растяжение пластичность характеризуется относительным удлинением Δ (дельта), которое соответствует отношению приращения длины образца после разрыва к его первоначальной длине в процентах. Сплав представляет собой смесь двух или нескольких металлов или металла и неметаллов. Сплав образуется посредством совместного сплавления компонентов, а также взаимодействия жидкого металла с жидкими и газообразными веществами.
§ 1. Свойства и классификация металлов и сплавов. Детальное изучение свойств и характеристик материалов, с которыми должен работать ювелир, необходимо для правильной и качественной их обработки. В производстве ювелирных изделий необходимо в первую очередь учитывать физические свойства металлов и сплавов, плотность, температуру плавления, тепловое расширение, теплопроводность, отражательную способность. Знание этих свойств позволяет правильно выбрать термические режимы литья, ковки, прокатки, пайки и других видов горячей обработки металлов. Важное значение при различных методах изготовления металлических деталей ювелирных украшений, оправ драгоценных камней, столовых приборов и посуды из сплавов благородных металлов имеют их основные механические свойства. К ним относятся: прочность, твердость, упругость, пластичность. Твердость способность металла оказывать сопротивление проникновению в него другого, более твердого тела. Наиболее распространены два способа определения твердости: Бринелля и Роквелла. Прочность способность металла сопротивляться разрушению под действием внешних сил. Для определения прочности образец металла установленной формы и размера испытывают на наибольшее разрушающее напряжение при растяжении, которое называют пределом прочности (временное сопротивление) и обозначают Σв (сигма). Пластичность способность металла, не разрушаясь, изменять форму под нагрузкой и сохранять ее после прекращения действия нагрузки. При испытании на растяжение пластичность характеризуется относительным удлинением Δ (дельта), которое соответствует отношению приращения длины образца после разрыва к его первоначальной длине в процентах. Сплав представляет собой смесь двух или нескольких металлов или металла и неметаллов. Сплав образуется посредством совместного сплавления компонентов, а также взаимодействия жидкого металла с жидкими и газообразными веществами.
 § 2. Деформация металла.
§ 2. Деформация металла.
 § 3. Химическая и термическая обработка металлов.
§ 3. Химическая и термическая обработка металлов.
 Черные металлы. Железо (Fe) § 4. Железо. Сплавы, классификация, свойства, состав. Железо голубовато белого цвета. Из за наличия во влажном воздухе паров воды и кислорода железо покрывается коричневым слоем ржавчины состоящим из водосодержащего окисла железа. Железо растворяется в соляной кислоте до хлорида; в концентрированной серной и азотной кислотах оно покрывается защитным слоем, который предохраняет его от дальнейшего разъедания. Вследствие высокой температуры плавления и легкой окисляемости железо редко используется в ювелирном деле. Железоуглеродистые сплавы с примесями марганца, кремния, серы, фосфора и некоторых других элементов принято называть черными металлами. В зависимости от содержания углерода они делятся на две группы: чугуны и стали. Сплавы железа с углеродом, содержащие свыше 2% С, а также примеси кремния, марганца, фосфора и серы относятся к чугунам (Серый чугун мягок и хрупок, он является исходным продуктом для получения чугунного литья. Белый чугун тверд и хрупок, он является исходным продуктом для получения стали. Высокопрочный чугун получают прибавлением к расплавленному чугуну присадок магния Такой чугун обладает повышенной прочностью и пластичностью. Ковкий чугун получают длительным отжигом отливок из белого чугуна. Обладает повышенной прочностью и пластичностью. Высокопрочные и ковкие чугуны маркируются буквами и цифрами: ВЧ высокопрочный чугун, КЧ ковкий чугун; первые две цифры предел прочности при растяжении в кгс/мм 2 (1 кгс/мм 2 = 9, 608 МПа ? 10 МПа). Сталь это сплав железа с углеродом, содержащий до 1, 8% углерода. Стали относятся к пластичным металлам, которым деформированием можно придать необходимую форму. По химическому составу они делятся на углеродистые и легированные; по назначению на конструкционные, инструментальные, особого назначения (нержавеющие, жаропрочные и др. ).
Черные металлы. Железо (Fe) § 4. Железо. Сплавы, классификация, свойства, состав. Железо голубовато белого цвета. Из за наличия во влажном воздухе паров воды и кислорода железо покрывается коричневым слоем ржавчины состоящим из водосодержащего окисла железа. Железо растворяется в соляной кислоте до хлорида; в концентрированной серной и азотной кислотах оно покрывается защитным слоем, который предохраняет его от дальнейшего разъедания. Вследствие высокой температуры плавления и легкой окисляемости железо редко используется в ювелирном деле. Железоуглеродистые сплавы с примесями марганца, кремния, серы, фосфора и некоторых других элементов принято называть черными металлами. В зависимости от содержания углерода они делятся на две группы: чугуны и стали. Сплавы железа с углеродом, содержащие свыше 2% С, а также примеси кремния, марганца, фосфора и серы относятся к чугунам (Серый чугун мягок и хрупок, он является исходным продуктом для получения чугунного литья. Белый чугун тверд и хрупок, он является исходным продуктом для получения стали. Высокопрочный чугун получают прибавлением к расплавленному чугуну присадок магния Такой чугун обладает повышенной прочностью и пластичностью. Ковкий чугун получают длительным отжигом отливок из белого чугуна. Обладает повышенной прочностью и пластичностью. Высокопрочные и ковкие чугуны маркируются буквами и цифрами: ВЧ высокопрочный чугун, КЧ ковкий чугун; первые две цифры предел прочности при растяжении в кгс/мм 2 (1 кгс/мм 2 = 9, 608 МПа ? 10 МПа). Сталь это сплав железа с углеродом, содержащий до 1, 8% углерода. Стали относятся к пластичным металлам, которым деформированием можно придать необходимую форму. По химическому составу они делятся на углеродистые и легированные; по назначению на конструкционные, инструментальные, особого назначения (нержавеющие, жаропрочные и др. ).
 § 5. Маркировка, применение, требование к качеству. Марки серого чугуна обозначаются буквами СЧ и числами, соответствующими его пределу прочности при растяжении в кгс/мм 2. Высокопрочные и ковкие чугуны маркируются буквами и цифрами: ВЧ высокопрочный чугун, КЧ ковкий чугун; первые две цифры предел прочности при растяжении в кгс/мм 2 (1 кгс/мм 2 = 9, 608 МПа ? 10 МПа). Углеродистые конструкционные стали подразделяются на обыкновенного качества, качественные и автоматные. Стали обыкновенного качества обозначаются буквами Ст и цифрами о 0 до 7. Качественные имеют меньше посторонних примесей. Они маркируются цифрами 08, 10, 15, 20 и так далее до 60, указывающие содержание углерода в сотых долях процента. Выпускаются две группы таких сталей: I с нормальным и II с повышенным содержанием марганца. Последние в конце маркировки имеют букву Г марганец. Качественные стали группы II обладают повышенной прочностью и упругостью. обозначают буквами и цифрами. Первые две цифры указывает среднее Марки легированных сталей содержание углерода в сотых долях процента; затем следуют цифры, обозначающие легирующий элемент; цифры после букв примерное содержание легирующего элемента в процентах. Если содержание элемента близко к 1%, цифра после буквы не ставится. В маркировке приняты следующие буквенные обозначения элементов: Г - марганец, С - кремний, Х - хром, Н - никель, М - молибден, В - вольфрам, Ф - ванадий, К кобальт, Ю - алюминий, Т - титан, Д - медь. Буква А в конце марки означает, что сталь высококачественная. Марки этих сталей обозначают буквой У углеродистая, а цифры после нее указывают среднее содержание углерода в десятых долях процента. У высококачественных сталей в конце маркировки указывается буква А. Быстрорежущие стали маркируются буквами и цифрами. Первая буква Р означает, что сталь быстрорежущая. Цифры после нее указывают среднее содержание вольфрама в процентах. Остальные буквы и цифры означают то же, что и в марках легированных сталей. Например 18 Н 4 ВА марки стали содержит (%): углерода – 1, 8, хрома 1, никеля – 4 и вольфрама – 1.
§ 5. Маркировка, применение, требование к качеству. Марки серого чугуна обозначаются буквами СЧ и числами, соответствующими его пределу прочности при растяжении в кгс/мм 2. Высокопрочные и ковкие чугуны маркируются буквами и цифрами: ВЧ высокопрочный чугун, КЧ ковкий чугун; первые две цифры предел прочности при растяжении в кгс/мм 2 (1 кгс/мм 2 = 9, 608 МПа ? 10 МПа). Углеродистые конструкционные стали подразделяются на обыкновенного качества, качественные и автоматные. Стали обыкновенного качества обозначаются буквами Ст и цифрами о 0 до 7. Качественные имеют меньше посторонних примесей. Они маркируются цифрами 08, 10, 15, 20 и так далее до 60, указывающие содержание углерода в сотых долях процента. Выпускаются две группы таких сталей: I с нормальным и II с повышенным содержанием марганца. Последние в конце маркировки имеют букву Г марганец. Качественные стали группы II обладают повышенной прочностью и упругостью. обозначают буквами и цифрами. Первые две цифры указывает среднее Марки легированных сталей содержание углерода в сотых долях процента; затем следуют цифры, обозначающие легирующий элемент; цифры после букв примерное содержание легирующего элемента в процентах. Если содержание элемента близко к 1%, цифра после буквы не ставится. В маркировке приняты следующие буквенные обозначения элементов: Г - марганец, С - кремний, Х - хром, Н - никель, М - молибден, В - вольфрам, Ф - ванадий, К кобальт, Ю - алюминий, Т - титан, Д - медь. Буква А в конце марки означает, что сталь высококачественная. Марки этих сталей обозначают буквой У углеродистая, а цифры после нее указывают среднее содержание углерода в десятых долях процента. У высококачественных сталей в конце маркировки указывается буква А. Быстрорежущие стали маркируются буквами и цифрами. Первая буква Р означает, что сталь быстрорежущая. Цифры после нее указывают среднее содержание вольфрама в процентах. Остальные буквы и цифры означают то же, что и в марках легированных сталей. Например 18 Н 4 ВА марки стали содержит (%): углерода – 1, 8, хрома 1, никеля – 4 и вольфрама – 1.
 Цветные металлы. § 6. Медь и её сплавы. Медь металл красновато розового цвета, плотностью 8, 94, температура плавления 1083°С, обладает высокой тепло и электропроводностью, пластичностью и тягучестью. Твердость по Моосу 2, 5 3. Медь хорошо полируется, но плохо подвергается обработке режущим инструментом из за свое мягкости. Во влажной среде покрывается зеленоватым налетом закиси меди, в сухой атмосфере тончайшей пленкой оксида меди. Образуя защитный слой, медь предохраняется от дальнейшего разрушения. Она легко растворяется в азотной кислоте и в Медь (Cu) концентрированной серной кислоте при нагревании. В соляной кислоте растворяется только в присутствии кислорода. Медные сплавы обозначают начальными буквами их названия ( Бр или Л), после чего следуют первые буквы названий основных элементов, образующих сплав, и цифры, указывающие кол во элемента в процентах. Приняты следующие обозначения компонентов сплавов: А – алюминий Мц марганец С свинец Б бериллий Мг – магний Ср – серебро Ж железо Мш мышьяк Су – сурьма К – кремний Н – никель Т – титан Кд – кадмий О – олово Ф – фосфор Х – хром Ц цинк Примеры: Бр. А 9 Мц2 Л бронза, содержащая 9% алюминия, 2% Mn, остальное Cu ("Л"' указывает, что сплав литейный); ЛЦ 40 Мц3 Ж латунь, содержащая 40% Zn, 3% Mn, ~ l% Fe, остальное Cu; Бр0 Ф 8, 0 0, 3 бронза на ряду с медью содержащая 8% олова и 0, 3% фосфора; Латуни сплавы меди с цинком (до 50% Zn) и небольшими добавками алюминия, кремния, свинца, никеля, марганца. Бронзы - медно оловяные сплавы, содержащие от 3 до 12% олова. В сплав могут входить цинк, свинец, фосфор, никель. Кроме оловяных бывают и другие виды бронзы алюминиевые, кремнистые, бериллиевые, кадмиевые. Мельхиор медно никелевый сплав с содержанием никеля от 18 до 20%, серебристого цвета, отличается устойчивостью к коррозиям. Нейзильбер сплав из трех компонентов на основе меди. Кроме нее в его состав входят 13, 5 16, 5% никеля и 18 22% цинка.
Цветные металлы. § 6. Медь и её сплавы. Медь металл красновато розового цвета, плотностью 8, 94, температура плавления 1083°С, обладает высокой тепло и электропроводностью, пластичностью и тягучестью. Твердость по Моосу 2, 5 3. Медь хорошо полируется, но плохо подвергается обработке режущим инструментом из за свое мягкости. Во влажной среде покрывается зеленоватым налетом закиси меди, в сухой атмосфере тончайшей пленкой оксида меди. Образуя защитный слой, медь предохраняется от дальнейшего разрушения. Она легко растворяется в азотной кислоте и в Медь (Cu) концентрированной серной кислоте при нагревании. В соляной кислоте растворяется только в присутствии кислорода. Медные сплавы обозначают начальными буквами их названия ( Бр или Л), после чего следуют первые буквы названий основных элементов, образующих сплав, и цифры, указывающие кол во элемента в процентах. Приняты следующие обозначения компонентов сплавов: А – алюминий Мц марганец С свинец Б бериллий Мг – магний Ср – серебро Ж железо Мш мышьяк Су – сурьма К – кремний Н – никель Т – титан Кд – кадмий О – олово Ф – фосфор Х – хром Ц цинк Примеры: Бр. А 9 Мц2 Л бронза, содержащая 9% алюминия, 2% Mn, остальное Cu ("Л"' указывает, что сплав литейный); ЛЦ 40 Мц3 Ж латунь, содержащая 40% Zn, 3% Mn, ~ l% Fe, остальное Cu; Бр0 Ф 8, 0 0, 3 бронза на ряду с медью содержащая 8% олова и 0, 3% фосфора; Латуни сплавы меди с цинком (до 50% Zn) и небольшими добавками алюминия, кремния, свинца, никеля, марганца. Бронзы - медно оловяные сплавы, содержащие от 3 до 12% олова. В сплав могут входить цинк, свинец, фосфор, никель. Кроме оловяных бывают и другие виды бронзы алюминиевые, кремнистые, бериллиевые, кадмиевые. Мельхиор медно никелевый сплав с содержанием никеля от 18 до 20%, серебристого цвета, отличается устойчивостью к коррозиям. Нейзильбер сплав из трех компонентов на основе меди. Кроме нее в его состав входят 13, 5 16, 5% никеля и 18 22% цинка.
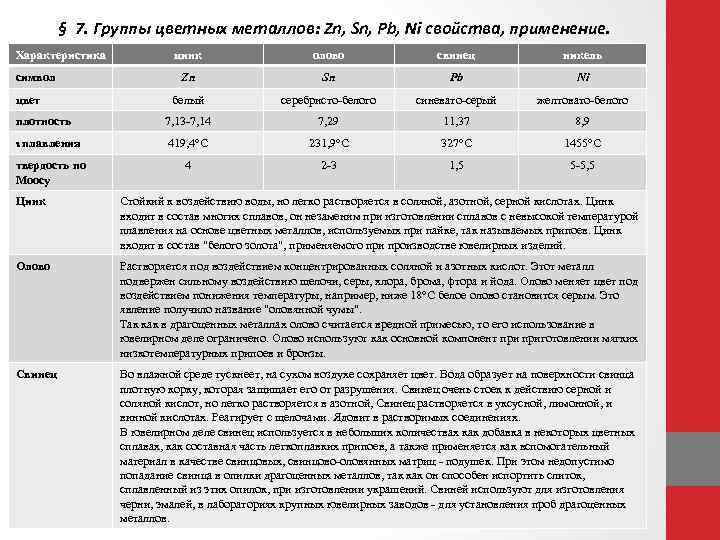 § 7. Группы цветных металлов: Zn, Sn, Pb, Ni свойства, применение. Характеристика цинк олово свинец никель Zn Sn Pb Ni белый серебристо белого синевато серый желтовато белого плотность 7, 13 7, 14 7, 29 11, 37 8, 9 ᵼ плавления 419, 4°С 231, 9°С 327°С 1455°С твердость по Моосу 4 2 3 1, 5 5 5, 5 символ цвет Цинк Стойкий к воздействию воды, но легко растворяется в соляной, азотной, серной кислотах. Цинк входит в состав многих сплавов, он незаменим при изготовлении сплавов с невысокой температурой плавления на основе цветных металлов, используемых при пайке, так называемых припоев. Цинк входит в состав "белого золота", применяемого при производстве ювелирных изделий. Олово Растворяется под воздействием концентрированных соляной и азотных кислот. Этот металл подвержен сильному воздействию щелочи, серы, хлора, брома, фтора и йода. Олово меняет цвет под воздействием понижения температуры, например, ниже 18°С белое олово становится серым. Это явление получило название "оловянной чумы". Так как в драгоценных металлах олово считается вредной примесью, то его использование в ювелирном деле ограничено. Олово используют как основной компонент приготовлении мягких низкотемпературных припоев и бронзы. Свинец Во влажной среде тускнеет, на сухом воздухе сохраняет цвет. Вода образует на поверхности свинца плотную корку, которая защищает его от разрушения. Свинец очень стоек к действию серной и соляной кислот, но легко растворяется в азотной, Свинец растворяется в уксусной, лимонной, и винной кислотах. Реагирует с щелочами. Ядовит в растворимых соединениях. В ювелирном деле свинец используется в небольших количествах как добавка в некоторых цветных сплавах, как составная часть легкоплавких припоев, а также применяется как вспомогательный материал в качестве свинцовых, свинцово оловянных матриц подушек. При этом недопустимо попадание свинца в опилки драгоценных металлов, так как он способен испортить слиток, сплавленный из этих опилок, при изготовлении украшений. Свиней используют для изготовления черни, эмалей, в лабораториях крупных ювелирных заводов для установления проб драгоценных металлов.
§ 7. Группы цветных металлов: Zn, Sn, Pb, Ni свойства, применение. Характеристика цинк олово свинец никель Zn Sn Pb Ni белый серебристо белого синевато серый желтовато белого плотность 7, 13 7, 14 7, 29 11, 37 8, 9 ᵼ плавления 419, 4°С 231, 9°С 327°С 1455°С твердость по Моосу 4 2 3 1, 5 5 5, 5 символ цвет Цинк Стойкий к воздействию воды, но легко растворяется в соляной, азотной, серной кислотах. Цинк входит в состав многих сплавов, он незаменим при изготовлении сплавов с невысокой температурой плавления на основе цветных металлов, используемых при пайке, так называемых припоев. Цинк входит в состав "белого золота", применяемого при производстве ювелирных изделий. Олово Растворяется под воздействием концентрированных соляной и азотных кислот. Этот металл подвержен сильному воздействию щелочи, серы, хлора, брома, фтора и йода. Олово меняет цвет под воздействием понижения температуры, например, ниже 18°С белое олово становится серым. Это явление получило название "оловянной чумы". Так как в драгоценных металлах олово считается вредной примесью, то его использование в ювелирном деле ограничено. Олово используют как основной компонент приготовлении мягких низкотемпературных припоев и бронзы. Свинец Во влажной среде тускнеет, на сухом воздухе сохраняет цвет. Вода образует на поверхности свинца плотную корку, которая защищает его от разрушения. Свинец очень стоек к действию серной и соляной кислот, но легко растворяется в азотной, Свинец растворяется в уксусной, лимонной, и винной кислотах. Реагирует с щелочами. Ядовит в растворимых соединениях. В ювелирном деле свинец используется в небольших количествах как добавка в некоторых цветных сплавах, как составная часть легкоплавких припоев, а также применяется как вспомогательный материал в качестве свинцовых, свинцово оловянных матриц подушек. При этом недопустимо попадание свинца в опилки драгоценных металлов, так как он способен испортить слиток, сплавленный из этих опилок, при изготовлении украшений. Свиней используют для изготовления черни, эмалей, в лабораториях крупных ювелирных заводов для установления проб драгоценных металлов.
 § 8. Группы цветных металлов: Аl, Cd, Hg свойства, применение. Алюминий Аl легкий металл, обладающий высокими тепло и электропроводностью, стойкий к коррозии. В зависимости от степени чистоты первичный алюминий согласно ГОСТ 11069 74 бывает особой (А 999), высокой (А 995, А 95) и технической чистоты (А 85, А 7 Е, АО и др. ). Алюминий маркируют буквой А и цифрами, обозначающими доли процента свыше 99, 0% Al; буква "Е" обозначает повышенное содержание железа и пониженное кремния. А 999 алюминий особой чистоты, в котором содержится не менее 99, 999% Al; А 5 алюминий технической чистоты в котором 99, 5% алюминия. Алюминиевые сплавы разделяют на деформируемые и литейные. Те и другие могут быть не упрочняемые и упрочняемые термической обработкой. Кадмий Cd металл белого цвета, ковкий, вязкий, мягче цинка. Плотность 8, 64; температура плавления 321°С; твердость по Моосу 3 3, 5. В сухом воздухе он не окисляется, при увлажнении покрывается пленкой коричневого цвета, предохраняющий его от разрушения. Кадмий легко растворяется в азотной кислоте, а также несколько хуже в соляной и серной. При накаливании кадмий сгорает, выделяя бурый оксид. Пары и соли кадмия ядовиты. Кадмий применяется в зубопротезной, химической промышленности. В ювелирном деле кадмий входит в состав многих ювелирных припоев, требующих относительно невысокой температуры плавления. Ртуть Нg - Ртуть — металл светло серебристого цвета, находящийся в жидком состоянии при нормальной температуре, стойкий на воздухе и обладающий сильным блеском. плотность 13, 55 г/см 3, температуру плавления 38, 83° С, температуру кипения 356, 950 С. При нагревании металла образуется окись ртути, дислоцирующая при температуре свыше 400° С. Так как ртуть при комнатной температуре выделяет ядовитые пары, то хранить ее необходимо только в закрытых емкостях. Ртуть взаимодействует со слабо разбавленной азотной кислотой с образованием нитрата и с концентрированной серной кислотой с образованием сульфата. С соляной кислотой ртуть не взаимодействует. Для повышения температуры плавления в нее добавляют золото, серебро и другие металлы. Полученные таким образом амальгамы при комнатной температуре тверды. Ювелиры используют ртуть для получения золотой и серебряной амальгам при горячем золочении и серебрении.
§ 8. Группы цветных металлов: Аl, Cd, Hg свойства, применение. Алюминий Аl легкий металл, обладающий высокими тепло и электропроводностью, стойкий к коррозии. В зависимости от степени чистоты первичный алюминий согласно ГОСТ 11069 74 бывает особой (А 999), высокой (А 995, А 95) и технической чистоты (А 85, А 7 Е, АО и др. ). Алюминий маркируют буквой А и цифрами, обозначающими доли процента свыше 99, 0% Al; буква "Е" обозначает повышенное содержание железа и пониженное кремния. А 999 алюминий особой чистоты, в котором содержится не менее 99, 999% Al; А 5 алюминий технической чистоты в котором 99, 5% алюминия. Алюминиевые сплавы разделяют на деформируемые и литейные. Те и другие могут быть не упрочняемые и упрочняемые термической обработкой. Кадмий Cd металл белого цвета, ковкий, вязкий, мягче цинка. Плотность 8, 64; температура плавления 321°С; твердость по Моосу 3 3, 5. В сухом воздухе он не окисляется, при увлажнении покрывается пленкой коричневого цвета, предохраняющий его от разрушения. Кадмий легко растворяется в азотной кислоте, а также несколько хуже в соляной и серной. При накаливании кадмий сгорает, выделяя бурый оксид. Пары и соли кадмия ядовиты. Кадмий применяется в зубопротезной, химической промышленности. В ювелирном деле кадмий входит в состав многих ювелирных припоев, требующих относительно невысокой температуры плавления. Ртуть Нg - Ртуть — металл светло серебристого цвета, находящийся в жидком состоянии при нормальной температуре, стойкий на воздухе и обладающий сильным блеском. плотность 13, 55 г/см 3, температуру плавления 38, 83° С, температуру кипения 356, 950 С. При нагревании металла образуется окись ртути, дислоцирующая при температуре свыше 400° С. Так как ртуть при комнатной температуре выделяет ядовитые пары, то хранить ее необходимо только в закрытых емкостях. Ртуть взаимодействует со слабо разбавленной азотной кислотой с образованием нитрата и с концентрированной серной кислотой с образованием сульфата. С соляной кислотой ртуть не взаимодействует. Для повышения температуры плавления в нее добавляют золото, серебро и другие металлы. Полученные таким образом амальгамы при комнатной температуре тверды. Ювелиры используют ртуть для получения золотой и серебряной амальгам при горячем золочении и серебрении.
 Практическая работа № 2 «Цветные металлы» Цель: Изучить состав и свойства цветных металлов их классификацию, применение, пробы и маркировку. Определить марки цветных сплавов по образцам, используя дополнительные буквенные и цифровые обозначения. Оборудование: Виды сплавов цветных металлов. Таблицы. Ход работы: 1) Рассмотреть виды сплавов цветных металлов: Бр. А 9 Мц2 Л, ЛЦ 40 Мц3 Ж, Бр0 Ф 8, 0 0, 3, АК 4 МЦ 6, Используя таблицу определить состав сплавов, описать его свойства и применение. Отчет оформить в виде таблицы. № марки ровка состав назначение 2) Ответьте на вопросы: • Какие существуют сплавы на основе меди. • Какими свойствами обладает сплав мельхиор. • Какие металлы являются легирующими для сплавов алюминия.
Практическая работа № 2 «Цветные металлы» Цель: Изучить состав и свойства цветных металлов их классификацию, применение, пробы и маркировку. Определить марки цветных сплавов по образцам, используя дополнительные буквенные и цифровые обозначения. Оборудование: Виды сплавов цветных металлов. Таблицы. Ход работы: 1) Рассмотреть виды сплавов цветных металлов: Бр. А 9 Мц2 Л, ЛЦ 40 Мц3 Ж, Бр0 Ф 8, 0 0, 3, АК 4 МЦ 6, Используя таблицу определить состав сплавов, описать его свойства и применение. Отчет оформить в виде таблицы. № марки ровка состав назначение 2) Ответьте на вопросы: • Какие существуют сплавы на основе меди. • Какими свойствами обладает сплав мельхиор. • Какие металлы являются легирующими для сплавов алюминия.
 § 9 Благородные металлы.
§ 9 Благородные металлы.
 § 10. Au, Ag, Pt: свойства, применение, месторождение. Золото. Химический элемент, символ Аи, плотность 19, 3 г/см 3, температуру плавления 10630 С, температуру кипения 2970° С, твердость по Бринелю в отожженном состоянии 18— 20 ктс/мм 2. Золото — металл красивого желтого цвета, тонколистовое (сусальное) золото имеет зеленоватый оттенок. Золото с трудом образует химические соединения, оно химически устойчиво на воздухе, в воде и в кислотах, за исключением царской водки. Золото имеет высокую отражательную способность и хорошо полируется; оно обладает высокой пластичностью и прокатывается в листы толщиной до 0, 0001 мм. Из за невысокой твердости и прочности золото используют в ювелирном деле в виде сплавов с другими металлами и в очень редких случаях в чистом виде. Серебро. Химический элемент, символ Ag, плотность 10, 5 г/см 3, температуру правления 960, 5° С, кипения 2210° С, твердость по Бринелю в отожженном состоянии 25 кгс/мм 2. Металл белого цвета, практически не изменяющийся под действием кислорода воздуха при комнатной температуре, однако из за наличия в воздухе сероводорода со временем покрывается темным налетом сульфида серебра Ag 2 S. Серебро устойчиво в воде, но растворяется в азотной и горячей концентрированной серной кислоте. С царской водкой оно образует нерастворимый хлорид серебра Ag. Cl. Как и золото, серебро взаимодействует щелочными растворами цианидов. Серебро хорошо полируется, имеет высокую отражательную способность; оно обладает хорошей ковкостью и самой высокой из всех металлов тепло и электропроводностью Чтобы повысить твердость и прочность серебра, его используют в сплавах с другими металлами. При изготовлении ювелирных украшении серебро в чистом виде применяют сравнительно редко. Платина. Химический элемент, символ Pt, имеет порядковый номер 78, атомный вес 195, 23, валентность II, IV, плотность 21. 45 г/см 3, температуру плавления 1773. 5° С, температуру кипения 4410° С, твердость по Бринелю в отожженном состоянии около 50 кгс/мм 3. Металл имеет бело серую окраску, схожую по цвету со cталыю, и практически нерастворим ни в воде, ни в кислотах, за исключением горячей царской водки. Платина весьма пластична, хорошо полируется и обладает большой отражательной способностью. Наряду с палладием и иридием она имеет очень низкую тепло и электропроводность, низкую удельную теплоемкость и с трудом вступает в химические соединении. Платина в чистом виде очень мягка, поэтому ее легируют иридием, родием и другими металлами. Для изготовления ювелирных изделий в сплав, кроме этих компонентов, добавляют еще и медь.
§ 10. Au, Ag, Pt: свойства, применение, месторождение. Золото. Химический элемент, символ Аи, плотность 19, 3 г/см 3, температуру плавления 10630 С, температуру кипения 2970° С, твердость по Бринелю в отожженном состоянии 18— 20 ктс/мм 2. Золото — металл красивого желтого цвета, тонколистовое (сусальное) золото имеет зеленоватый оттенок. Золото с трудом образует химические соединения, оно химически устойчиво на воздухе, в воде и в кислотах, за исключением царской водки. Золото имеет высокую отражательную способность и хорошо полируется; оно обладает высокой пластичностью и прокатывается в листы толщиной до 0, 0001 мм. Из за невысокой твердости и прочности золото используют в ювелирном деле в виде сплавов с другими металлами и в очень редких случаях в чистом виде. Серебро. Химический элемент, символ Ag, плотность 10, 5 г/см 3, температуру правления 960, 5° С, кипения 2210° С, твердость по Бринелю в отожженном состоянии 25 кгс/мм 2. Металл белого цвета, практически не изменяющийся под действием кислорода воздуха при комнатной температуре, однако из за наличия в воздухе сероводорода со временем покрывается темным налетом сульфида серебра Ag 2 S. Серебро устойчиво в воде, но растворяется в азотной и горячей концентрированной серной кислоте. С царской водкой оно образует нерастворимый хлорид серебра Ag. Cl. Как и золото, серебро взаимодействует щелочными растворами цианидов. Серебро хорошо полируется, имеет высокую отражательную способность; оно обладает хорошей ковкостью и самой высокой из всех металлов тепло и электропроводностью Чтобы повысить твердость и прочность серебра, его используют в сплавах с другими металлами. При изготовлении ювелирных украшении серебро в чистом виде применяют сравнительно редко. Платина. Химический элемент, символ Pt, имеет порядковый номер 78, атомный вес 195, 23, валентность II, IV, плотность 21. 45 г/см 3, температуру плавления 1773. 5° С, температуру кипения 4410° С, твердость по Бринелю в отожженном состоянии около 50 кгс/мм 3. Металл имеет бело серую окраску, схожую по цвету со cталыю, и практически нерастворим ни в воде, ни в кислотах, за исключением горячей царской водки. Платина весьма пластична, хорошо полируется и обладает большой отражательной способностью. Наряду с палладием и иридием она имеет очень низкую тепло и электропроводность, низкую удельную теплоемкость и с трудом вступает в химические соединении. Платина в чистом виде очень мягка, поэтому ее легируют иридием, родием и другими металлами. Для изготовления ювелирных изделий в сплав, кроме этих компонентов, добавляют еще и медь.
 § 11. Pd , Rh, Ru, Ir, Os: свойства, применение, месторождение. Иридий. Химический элемент, символ Ir, имеет порядковый номер 77, атомный вес 193, 1, плотность 22, 5 г/см 3, температуру плавления 2454° С, температуру кипения 53000 С, твердость по Бринелю в отожженном состоянии 172 кгс/мм 2. Из за большой твердости и высокой температуры плавления иридий с трудом поддается обработке. Относительное удлинение при растяжении составляет лишь 2%. При высоких температурах металл можно обрабатывать давлением. При небольшой добавке иридия к платине значительно повышается ее твердость. Палладий. Химический элемент, символ Pd, имеет порядковый номер 46, атомный вес 106, 4, плотность 12, 0 г/см 3, температуру плавления 1554, 5° С, температуру кипения 40000 С, твердость по Бринелю в отожженном состоянии 52 кгс/мм 2. Палладий имеет более светлую окраску, чем платина, он химически устойчив на воздухе и в воде, растворяется в горячей, слегка разбавленной азотной кислоте с образованием нитрата палладия. При температурах от 400 до 850° С палладий покрывается светло фиолетовым окисным слоем, который исчезает при более высоких температурах. Благодаря хорошей обрабатываемости, низкой температуре плавления и относительной дешевизне, он чаще других метал нов платиновой группы используется в ювелирных изделиях. Как тегирующий металл палладий улучшает свойства платины, осветляет ее окраску, а также способствует отбеливанию сплава при получении так называемого белого золота. Родий. Химический элемент, символ Rh, имеет порядковый номер 45, атомный вес 102, 91, плотность 12, 4 г/см 3, температуру плавления 1966° С, температуру кипения 45000 С, твердость по Бринелю 101 кгс/мм 2. По цвету родий сходен с платиной, не вступает во взаимодействие с кипящими кислотами и смесями кислот, но растворяется в щелочных растворах цианидов; абсолютно не окисляется на воздухе и в воде, хорошо поддается горячей обработке давлением. Осмий 1870 s. Его стоимость составляет 200 тысяч долларов за грамм. Этот металл является самым плотным в таблице Менделеева (22, 61 г/см 3). Данный химический элемент имеет порядковый номер 76 в таблице Менделеева. Чаще всего этот химический элемент встречается в виде порошка. При обычных условиях осмий имеет серебристый цвет и обладает резким запахом, схожим с озоном. Осмий впервые был открыт ученым из Англии, который получил его путем растворения платины в смеси из азотной и соляной кислот, так называемой "царской водке". Применяют изотоп осмия при производстве ядерного оружия, в аэрокосмической сфере, фармацевтике, при изготовлении некоторых измерительных приборов, реже в ювелирных изделиях.
§ 11. Pd , Rh, Ru, Ir, Os: свойства, применение, месторождение. Иридий. Химический элемент, символ Ir, имеет порядковый номер 77, атомный вес 193, 1, плотность 22, 5 г/см 3, температуру плавления 2454° С, температуру кипения 53000 С, твердость по Бринелю в отожженном состоянии 172 кгс/мм 2. Из за большой твердости и высокой температуры плавления иридий с трудом поддается обработке. Относительное удлинение при растяжении составляет лишь 2%. При высоких температурах металл можно обрабатывать давлением. При небольшой добавке иридия к платине значительно повышается ее твердость. Палладий. Химический элемент, символ Pd, имеет порядковый номер 46, атомный вес 106, 4, плотность 12, 0 г/см 3, температуру плавления 1554, 5° С, температуру кипения 40000 С, твердость по Бринелю в отожженном состоянии 52 кгс/мм 2. Палладий имеет более светлую окраску, чем платина, он химически устойчив на воздухе и в воде, растворяется в горячей, слегка разбавленной азотной кислоте с образованием нитрата палладия. При температурах от 400 до 850° С палладий покрывается светло фиолетовым окисным слоем, который исчезает при более высоких температурах. Благодаря хорошей обрабатываемости, низкой температуре плавления и относительной дешевизне, он чаще других метал нов платиновой группы используется в ювелирных изделиях. Как тегирующий металл палладий улучшает свойства платины, осветляет ее окраску, а также способствует отбеливанию сплава при получении так называемого белого золота. Родий. Химический элемент, символ Rh, имеет порядковый номер 45, атомный вес 102, 91, плотность 12, 4 г/см 3, температуру плавления 1966° С, температуру кипения 45000 С, твердость по Бринелю 101 кгс/мм 2. По цвету родий сходен с платиной, не вступает во взаимодействие с кипящими кислотами и смесями кислот, но растворяется в щелочных растворах цианидов; абсолютно не окисляется на воздухе и в воде, хорошо поддается горячей обработке давлением. Осмий 1870 s. Его стоимость составляет 200 тысяч долларов за грамм. Этот металл является самым плотным в таблице Менделеева (22, 61 г/см 3). Данный химический элемент имеет порядковый номер 76 в таблице Менделеева. Чаще всего этот химический элемент встречается в виде порошка. При обычных условиях осмий имеет серебристый цвет и обладает резким запахом, схожим с озоном. Осмий впервые был открыт ученым из Англии, который получил его путем растворения платины в смеси из азотной и соляной кислот, так называемой "царской водке". Применяют изотоп осмия при производстве ядерного оружия, в аэрокосмической сфере, фармацевтике, при изготовлении некоторых измерительных приборов, реже в ювелирных изделиях.
 § 12. Сплавы драгоценных металлов. Для изготовления ювелирных изделий используют обычно не чистые металлы, а сплавы, добавляя в первые в определенных соотношениях другие металлы. Эти металлы называются легирующими или лигатурой. Легирующими могут быть и драгоценные и недрагоценные металлы, но полученные сплавы называются драгоценными. В ювелирном деле обычно используются три вида сплавов: сплавы золота, сплавы серебра, сплавы платины. Сплавы золота формируются с добавками следующих легирующих компонентов: серебра, меди, палладия, никеля, платины, кадмия и цинка. Участие каждого компонента в золотом сплаве определяется в зависимости от свойств, которыми должен обладать сплав. Серебро повышает мягкость, ковкость сплава золота, понижает температуру плавления и изменяет цвет золота. По мере добавления серебра цвет золота зеленеет и становится желто зеленый. Если содержание серебра в сплаве золота более 30%, то цвет его становится желто белым и бледнеет. При содержании серебра более 65% желтый цвет полностью исчезает. Медь повышает твердость, ковкость сплава золота, сохраняя ковкость и тягучесть. Сплав приобретает красноватый цвет. Если содержание меди в сплаве золота более 14, 6%, то цвет его становится ярко красного цвета, медь понижает антикоррозионные свойства золота, при большом его содержании поверхность сплава темнеет. Палладий повышает температуру плавления сплава, сохраняет пластичность и ковкость, изменяет его цвет при содержании палладия в сплаве до 10% до белого. Никель изменяет цвет сплава золота в бледно желтый, сохраняет ковкость металла, придает ему твердость и повышает литейные свойства. При добавлении никеля сплав золота приобретает магнитные свойства, что не всегда является необходимым. Платина придает золоту белый цвет, желтизна теряется при содержании платины в сплаве 8, 4% до белого. Она также повышает температуру плавления сплава. При содержании платины в сплаве до 20% увеличивается упругость сплава. Кадмий понижает температуру плавления сплава, но сохраняет пластичность и ковкость. Сплавы серебра, используемые для изготовления ювелирных украшений, имеют в своем составе всего один легирующий материал медь. Она повышает твердость сплавов, сохраняя достаточную пластичность, ковкость, тягучесть. Все серебряные сплавы одинаковы по цвету и отличаются друг от друга процентным содержанием серебра. Согласно ГОСТам для изготовления ювелирных изделий в четырех сплавах серебра должно присутствовать 91, 6%; 87, 5%; 80%; 50%. Однако в практике обычно используют сплавы серебра 916 й и 875 й пробы. Сплавы платины, используемые в ювелирном деле, составляются в двух вариантах, причем содержание платины и в том и в другом 95%. Легирующие компоненты платиновых сплавов медь и иридий. Оба сплава двухкомпонентные. Цвет обоих сплавов остается характерным для платины. При содержании в платиново медном сплаве 5% меди понижается температура плавления, сохраняется мягкость, тягучесть, пластичность сплава. При содержании в платиново медном сплаве 5% иридия повышается температура плавления, кислотостойкость и твердость сплава, что делает изделия из него износостойкими.
§ 12. Сплавы драгоценных металлов. Для изготовления ювелирных изделий используют обычно не чистые металлы, а сплавы, добавляя в первые в определенных соотношениях другие металлы. Эти металлы называются легирующими или лигатурой. Легирующими могут быть и драгоценные и недрагоценные металлы, но полученные сплавы называются драгоценными. В ювелирном деле обычно используются три вида сплавов: сплавы золота, сплавы серебра, сплавы платины. Сплавы золота формируются с добавками следующих легирующих компонентов: серебра, меди, палладия, никеля, платины, кадмия и цинка. Участие каждого компонента в золотом сплаве определяется в зависимости от свойств, которыми должен обладать сплав. Серебро повышает мягкость, ковкость сплава золота, понижает температуру плавления и изменяет цвет золота. По мере добавления серебра цвет золота зеленеет и становится желто зеленый. Если содержание серебра в сплаве золота более 30%, то цвет его становится желто белым и бледнеет. При содержании серебра более 65% желтый цвет полностью исчезает. Медь повышает твердость, ковкость сплава золота, сохраняя ковкость и тягучесть. Сплав приобретает красноватый цвет. Если содержание меди в сплаве золота более 14, 6%, то цвет его становится ярко красного цвета, медь понижает антикоррозионные свойства золота, при большом его содержании поверхность сплава темнеет. Палладий повышает температуру плавления сплава, сохраняет пластичность и ковкость, изменяет его цвет при содержании палладия в сплаве до 10% до белого. Никель изменяет цвет сплава золота в бледно желтый, сохраняет ковкость металла, придает ему твердость и повышает литейные свойства. При добавлении никеля сплав золота приобретает магнитные свойства, что не всегда является необходимым. Платина придает золоту белый цвет, желтизна теряется при содержании платины в сплаве 8, 4% до белого. Она также повышает температуру плавления сплава. При содержании платины в сплаве до 20% увеличивается упругость сплава. Кадмий понижает температуру плавления сплава, но сохраняет пластичность и ковкость. Сплавы серебра, используемые для изготовления ювелирных украшений, имеют в своем составе всего один легирующий материал медь. Она повышает твердость сплавов, сохраняя достаточную пластичность, ковкость, тягучесть. Все серебряные сплавы одинаковы по цвету и отличаются друг от друга процентным содержанием серебра. Согласно ГОСТам для изготовления ювелирных изделий в четырех сплавах серебра должно присутствовать 91, 6%; 87, 5%; 80%; 50%. Однако в практике обычно используют сплавы серебра 916 й и 875 й пробы. Сплавы платины, используемые в ювелирном деле, составляются в двух вариантах, причем содержание платины и в том и в другом 95%. Легирующие компоненты платиновых сплавов медь и иридий. Оба сплава двухкомпонентные. Цвет обоих сплавов остается характерным для платины. При содержании в платиново медном сплаве 5% меди понижается температура плавления, сохраняется мягкость, тягучесть, пластичность сплава. При содержании в платиново медном сплаве 5% иридия повышается температура плавления, кислотостойкость и твердость сплава, что делает изделия из него износостойкими.
 § 13. Маркировка, проба, требование. Общепринято выражать количество золота в сплаве пробой. До введения метрической системы количество золота в сплаве измеряли, в каратах, а серебро в лотах, имелись и другие меры проб. Чистые металлы в расчетах обозначаются общепринятыми символами золото Au, серебро Ag, палладий Pd, платина Pt, медь Cu, цинк Zn и т. д. в соответствии с таблицей Менделеева. Если сплав двух , трех , или четырехкомпонентный, в наименовании указывается сокращенное наименование компонентов сплава, а по количественному составу указываются тысячные части только одного, двух или трех компонентов, последний компонент составляет оставшиеся части. Например сплав например Зл. Ср. М 585 80 (красное золото) означает сплав состоящий из золота 585 частей, серебра 80 частей и меди оставшиеся (1000 585 80=335) частей, соответственно в слитке сплава этой марки весом 100 грамм содержится золота 58, 5 г, серебра 8 г, меди 33, 5 г. Для благородных металлов в России установлены следующие пробы: золото— 375, 500, 585, 750, 958, 999 серебро — 800, 830, 875, 925, 960, 999 платина — 850, 900, 950 палладий — 500, 850 Каратная проба
§ 13. Маркировка, проба, требование. Общепринято выражать количество золота в сплаве пробой. До введения метрической системы количество золота в сплаве измеряли, в каратах, а серебро в лотах, имелись и другие меры проб. Чистые металлы в расчетах обозначаются общепринятыми символами золото Au, серебро Ag, палладий Pd, платина Pt, медь Cu, цинк Zn и т. д. в соответствии с таблицей Менделеева. Если сплав двух , трех , или четырехкомпонентный, в наименовании указывается сокращенное наименование компонентов сплава, а по количественному составу указываются тысячные части только одного, двух или трех компонентов, последний компонент составляет оставшиеся части. Например сплав например Зл. Ср. М 585 80 (красное золото) означает сплав состоящий из золота 585 частей, серебра 80 частей и меди оставшиеся (1000 585 80=335) частей, соответственно в слитке сплава этой марки весом 100 грамм содержится золота 58, 5 г, серебра 8 г, меди 33, 5 г. Для благородных металлов в России установлены следующие пробы: золото— 375, 500, 585, 750, 958, 999 серебро — 800, 830, 875, 925, 960, 999 платина — 850, 900, 950 палладий — 500, 850 Каратная проба
 § 14. Художественные материалы, назначение, виды.
§ 14. Художественные материалы, назначение, виды.
 Практическая работа № 3 «Визуальное определение физических свойств» .
Практическая работа № 3 «Визуальное определение физических свойств» .
 § 15. Свойства ювелирных камней. Твердость важнейшее диагностическое свойство минералов. Для определения твердости используют шкалу Мооса набор стандартных минералов. В шкале минералы рас положены в порядке возрастания твердости. Шкала твердости: Тальк -1, Гипс 2 , Кальцит – 3, Флюорит – 4, Апатит – 5, Ортоклаз – 6, Кварц – 7, Топаз – 8, Корунд 9, Алмаз 10 Удельный вес (плотность) земных минералов колеблется от значений, менее единицы (природные газы) до 23 (минералы группы осмистого иридия). Цвет минералов и цвет черты. Цвет минералов является важнейшим диагно стическим свойством. Названия многих минералов связаны с их цветом: хлорит — зеленый, родонит — розовый, рубин – красный и т. д. Для перечисленных мине ралов цвет всегда постоянен. Однако есть минералы, у которых окраска непостоянна и может меняться в зависимости от условий образования, примесей и т. д. Ряд минералов оставляет на фарфоровой пластинке (бисквите) черту характер ной окраски. Цвет черты минерала это его цвет в тонком порошке. Например, халькопирит дает на фарфоровой пластинке черную черту с зеленоватым оттенком, хотя в куске он латунно желтый, аурипигмент дает желтую черту и т. д. Блеск минералов. Интенсивность отраженного света от поверхности минералов известна под названием блеска. Минералы подразделяют по блеску на три груп пы с металлическим, полуметаллическим, и : неметаллическим блеском. Спайность и излом. Спайность способность минералов кристаллического строения раскалываться по определенным кристаллографическим направлениям с образованием ровных блестящих поверхностей. Выделяют четыре типа спайности по степени совершенства: Весьма совершенная минерал легко расщепляется на тонкие зеркальные пла стинки. Совершенная минерал раскалывается на равные поверхности при легком уда ре. Несовершенная ровные поверхности обнаруживаются с трудом. Весьма несовершенная минералы при расколе образуют неровные, ракови стые поверхности, плоскости спайности наблюдаются очень редко. Излом — поверхность, получающаяся при расколе или разломе минерала. У ми нералов с совершенной и весьма совершенной спайностью ровный или ступенчатый излом, у волокнистых минералов занозистый излом. Особые свойства минералов. Некоторые минералы хорошо распознаются по особым свойствам: двойному лучепреломлению (исландский шпат), магнитности (магнетит, пирротин), растворимости (галит растворяется в воде, кальцит в раз бавленной соляной кислоте), запаху (при трении кусочков фосфорита ощущается запах жженой кости, а кусочков арсенопирита запах чеснока), упругости и гибко сти (у слюды листочки гибкие, упругие, а листочки гипса ломаются) и т. д.
§ 15. Свойства ювелирных камней. Твердость важнейшее диагностическое свойство минералов. Для определения твердости используют шкалу Мооса набор стандартных минералов. В шкале минералы рас положены в порядке возрастания твердости. Шкала твердости: Тальк -1, Гипс 2 , Кальцит – 3, Флюорит – 4, Апатит – 5, Ортоклаз – 6, Кварц – 7, Топаз – 8, Корунд 9, Алмаз 10 Удельный вес (плотность) земных минералов колеблется от значений, менее единицы (природные газы) до 23 (минералы группы осмистого иридия). Цвет минералов и цвет черты. Цвет минералов является важнейшим диагно стическим свойством. Названия многих минералов связаны с их цветом: хлорит — зеленый, родонит — розовый, рубин – красный и т. д. Для перечисленных мине ралов цвет всегда постоянен. Однако есть минералы, у которых окраска непостоянна и может меняться в зависимости от условий образования, примесей и т. д. Ряд минералов оставляет на фарфоровой пластинке (бисквите) черту характер ной окраски. Цвет черты минерала это его цвет в тонком порошке. Например, халькопирит дает на фарфоровой пластинке черную черту с зеленоватым оттенком, хотя в куске он латунно желтый, аурипигмент дает желтую черту и т. д. Блеск минералов. Интенсивность отраженного света от поверхности минералов известна под названием блеска. Минералы подразделяют по блеску на три груп пы с металлическим, полуметаллическим, и : неметаллическим блеском. Спайность и излом. Спайность способность минералов кристаллического строения раскалываться по определенным кристаллографическим направлениям с образованием ровных блестящих поверхностей. Выделяют четыре типа спайности по степени совершенства: Весьма совершенная минерал легко расщепляется на тонкие зеркальные пла стинки. Совершенная минерал раскалывается на равные поверхности при легком уда ре. Несовершенная ровные поверхности обнаруживаются с трудом. Весьма несовершенная минералы при расколе образуют неровные, ракови стые поверхности, плоскости спайности наблюдаются очень редко. Излом — поверхность, получающаяся при расколе или разломе минерала. У ми нералов с совершенной и весьма совершенной спайностью ровный или ступенчатый излом, у волокнистых минералов занозистый излом. Особые свойства минералов. Некоторые минералы хорошо распознаются по особым свойствам: двойному лучепреломлению (исландский шпат), магнитности (магнетит, пирротин), растворимости (галит растворяется в воде, кальцит в раз бавленной соляной кислоте), запаху (при трении кусочков фосфорита ощущается запах жженой кости, а кусочков арсенопирита запах чеснока), упругости и гибко сти (у слюды листочки гибкие, упругие, а листочки гипса ломаются) и т. д.
 § 16. Классификация ювелирных камней.
§ 16. Классификация ювелирных камней.
 § 17. Самоцветы.
§ 17. Самоцветы.
 § 18. Цветные камни.
§ 18. Цветные камни.
 § 19. Органические камни.
§ 19. Органические камни.
 § 20. Искусственные камни.
§ 20. Искусственные камни.
 § 21. Стекло. Пластические массы.
§ 21. Стекло. Пластические массы.
 § 22.
§ 22.



