2013-03-29_Glazer2.ppt
- Количество слайдов: 51
 ОСНОВЫ ИММУНОГЕНЕТИКИ
ОСНОВЫ ИММУНОГЕНЕТИКИ
 У животных различают два основных типа неспецифический и приобретенный специфический. иммунитета: врожденный Способностью к приобретенному иммунитету обладают только позвоночные. В приобретенном иммунном ответе ключевую роль играют лимфоидные В- и Тклетки, синтезирующие белки-рецепторы, специфически связывающие антигены. Приобретенный иммунитет бывает гуморальным и клеточно-опосредованным. Гуморальный иммунитет связан с вырабатываемыми В-лимфоцитами разнообразными антителами (иммуноглобулинами). Чтобы начать продуцировать антитела, В-клетка должна получить сигнал от особого Т-лимфоцита – Т-хелпера. Антитела образуют комплексы со специфическими антигенами. Формирование комплекса антиген-антитело инициирует процесс уничтожения антигена, привлекая систему комплемента и макрофаги. Клеточно-опосредованный иммунитет осуществляет лимфоцитов – цитотоксические Т-клетки (Т-киллеры). особый класс Т- Клеточно-опосредованный иммунитет вызывается внутриклеточными паразитами, например, вирусами. В результате вирусной инфекции фрагменты вирусных антигенов экспонируются на поверхности инфицированной клетки с помощью одного из белков – представителей главного комплекса гистосовместмости (MHC). В таком виде антиген может распознаваться и связываться с рецептором Тлимфоцита. Оба типа Т-лимфоцитов, и Т-хелперы, и Т-киллеры, для распознавания антигенов синтезируют на своей поверхности специфические рецепторы Т-клеток (T Cell Receptor – TCR), являющиеся Т-клеточными эквивалентами антител, продуцируемых В-лимфоцитами.
У животных различают два основных типа неспецифический и приобретенный специфический. иммунитета: врожденный Способностью к приобретенному иммунитету обладают только позвоночные. В приобретенном иммунном ответе ключевую роль играют лимфоидные В- и Тклетки, синтезирующие белки-рецепторы, специфически связывающие антигены. Приобретенный иммунитет бывает гуморальным и клеточно-опосредованным. Гуморальный иммунитет связан с вырабатываемыми В-лимфоцитами разнообразными антителами (иммуноглобулинами). Чтобы начать продуцировать антитела, В-клетка должна получить сигнал от особого Т-лимфоцита – Т-хелпера. Антитела образуют комплексы со специфическими антигенами. Формирование комплекса антиген-антитело инициирует процесс уничтожения антигена, привлекая систему комплемента и макрофаги. Клеточно-опосредованный иммунитет осуществляет лимфоцитов – цитотоксические Т-клетки (Т-киллеры). особый класс Т- Клеточно-опосредованный иммунитет вызывается внутриклеточными паразитами, например, вирусами. В результате вирусной инфекции фрагменты вирусных антигенов экспонируются на поверхности инфицированной клетки с помощью одного из белков – представителей главного комплекса гистосовместмости (MHC). В таком виде антиген может распознаваться и связываться с рецептором Тлимфоцита. Оба типа Т-лимфоцитов, и Т-хелперы, и Т-киллеры, для распознавания антигенов синтезируют на своей поверхности специфические рецепторы Т-клеток (T Cell Receptor – TCR), являющиеся Т-клеточными эквивалентами антител, продуцируемых В-лимфоцитами.
 Разнообразие антител-иммуноглобулинов и рецепторов Т-лимфоцитов обеспечивается разнообразием генов, кодирующих эти белки. В геномах генеративных и всех соматических клеток, кроме В-лимфоцитов, гены иммуноглобулинов отсутствуют. В них представлены только наборы сегментов V, D и J, из которых на строго определенных стадиях дифференцировки этих клеток формируются гены иммуноглобулинов, прежде всего, их вариабельные домены. Формирование генов Т-клеточных происходит по той же схеме. рецепторов
Разнообразие антител-иммуноглобулинов и рецепторов Т-лимфоцитов обеспечивается разнообразием генов, кодирующих эти белки. В геномах генеративных и всех соматических клеток, кроме В-лимфоцитов, гены иммуноглобулинов отсутствуют. В них представлены только наборы сегментов V, D и J, из которых на строго определенных стадиях дифференцировки этих клеток формируются гены иммуноглобулинов, прежде всего, их вариабельные домены. Формирование генов Т-клеточных происходит по той же схеме. рецепторов
 Строение антител на примере Ig. G Молекула антитела состоит из двух тяжелых (Н) и двух легких (L) цепей. L-цепь – легкая κ- или λцепь: VL – вариабельный домен СL – единственный константный домен Н-цепь – тяжелая цепь: VH – вариабельный домен СH – константные домены
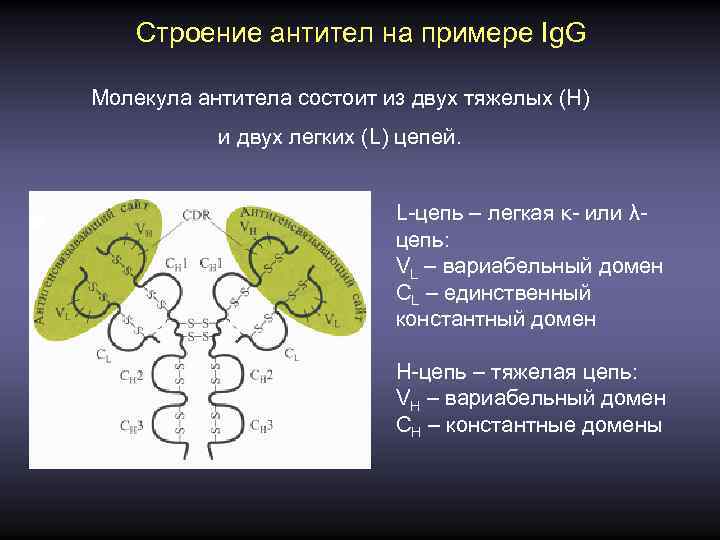
Строение антител на примере Ig. G Молекула антитела состоит из двух тяжелых (Н) и двух легких (L) цепей. L-цепь – легкая κ- или λцепь: VL – вариабельный домен СL – единственный константный домен Н-цепь – тяжелая цепь: VH – вариабельный домен СH – константные домены
 Вариабельный домен тяжелой цепи включает по одному из кодирующих сегментов V, D и J, вариабельный домен легкой цепи состоит из сегментов V и J. Каждый вариабельный домен содержит около 110 а. о. и имеет в определенных положениях несколько гипервариабельных участков из 5 -10 а. о. (complementary-determining regions – CDRs). Произвольное комбинирование множественных сегментов V, D и J обеспечивает так называемое первичное разнообразие антител. В молекуле иммуноглобулина гипервариабельные домены двух идентичных тяжелых цепей и двух идентичных легких цепей формируют активный антиген-связывающий сайт, который по своей конформации комплементарен структуре антигена или какой-либо части антигена (эпитопу), что обеспечивает распознавание и связывание между антигеном и антителом.
Вариабельный домен тяжелой цепи включает по одному из кодирующих сегментов V, D и J, вариабельный домен легкой цепи состоит из сегментов V и J. Каждый вариабельный домен содержит около 110 а. о. и имеет в определенных положениях несколько гипервариабельных участков из 5 -10 а. о. (complementary-determining regions – CDRs). Произвольное комбинирование множественных сегментов V, D и J обеспечивает так называемое первичное разнообразие антител. В молекуле иммуноглобулина гипервариабельные домены двух идентичных тяжелых цепей и двух идентичных легких цепей формируют активный антиген-связывающий сайт, который по своей конформации комплементарен структуре антигена или какой-либо части антигена (эпитопу), что обеспечивает распознавание и связывание между антигеном и антителом.
 В состав иммуноглобулинов входят также константные домены, кодируемые С-сегментами, локализованными в хромосоме по соседству с кодирующими V, D и J-сегментами. Легкие цепи содержат единственный константный домен, либо , и по этому критерию подразделяются на два типа: и . Наборы кодирующих сегментов, необходимых для сборки генов легких цепей двух различных типов, расположены в разных хромосомах. Тяжелые цепи содержат один из нескольких СH-доменов, кодируемых С-сегментами α, , d, e и m. В соответствии с ними у млекопитающих известны 5 классов (изотипов) иммуноглобулинов: Ig. А, Ig. G, Ig. D, Ig. E и Ig. M. Принадлежность к тому или иному классу определяет эффекторные функции В-лимфоцитов. «Наивные» * зрелые В-лимфоциты синтезируют два типа иммуноглобулинов, Ig. M и Ig. D, которым соответствуют два кодирующих Ссегмента – μ и δ, ближайшие к кластеру V, D и J-сегментов в хромосоме. После контакта (активации) с антигеном эти клетки пролиферируют. *Наивные В-лимфоциты – клетки, еще не контактировашие с антигеном.
В состав иммуноглобулинов входят также константные домены, кодируемые С-сегментами, локализованными в хромосоме по соседству с кодирующими V, D и J-сегментами. Легкие цепи содержат единственный константный домен, либо , и по этому критерию подразделяются на два типа: и . Наборы кодирующих сегментов, необходимых для сборки генов легких цепей двух различных типов, расположены в разных хромосомах. Тяжелые цепи содержат один из нескольких СH-доменов, кодируемых С-сегментами α, , d, e и m. В соответствии с ними у млекопитающих известны 5 классов (изотипов) иммуноглобулинов: Ig. А, Ig. G, Ig. D, Ig. E и Ig. M. Принадлежность к тому или иному классу определяет эффекторные функции В-лимфоцитов. «Наивные» * зрелые В-лимфоциты синтезируют два типа иммуноглобулинов, Ig. M и Ig. D, которым соответствуют два кодирующих Ссегмента – μ и δ, ближайшие к кластеру V, D и J-сегментов в хромосоме. После контакта (активации) с антигеном эти клетки пролиферируют. *Наивные В-лимфоциты – клетки, еще не контактировашие с антигеном.
 Ig. A Классы иммуноглобулинов 360 -720 к. Да Ig. M 935 к. Да Ig. D 172 к. Да Ig. E 196 к. Да Ig. G 150 к. Да Ig. A – главный класс иммуноглобулинов серозно-слизистых секретов Ig. D – обильно представлен на мембране многих В-клеток Ig. E – наблюдается на повышенном уровне при аллергических реакциях и паразитарных инфекциях Ig. G – главный изотип Ig нормальной сыворотки человека; на его долю приходится 70 общего количества сывороточных иммуноглобулинов Ig. M – локализован на мембране В-клеток; образуется первым при контакте с чужеродным антигеном Антитела Ig. M особенно активны против бактерий. ©
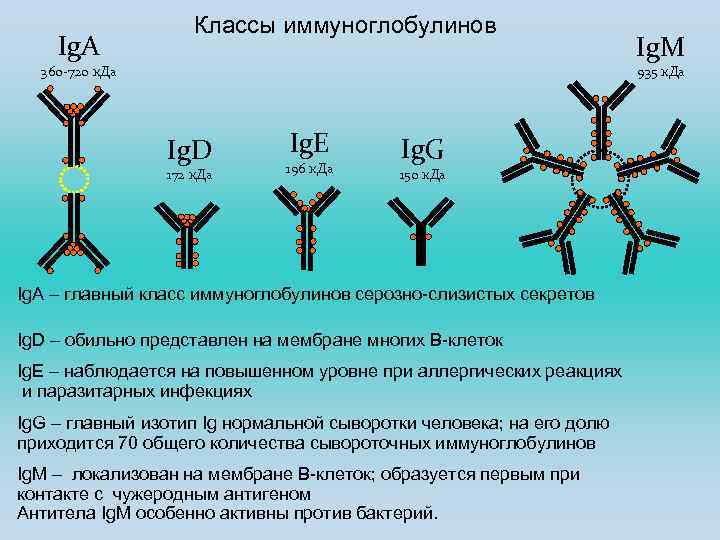
Ig. A Классы иммуноглобулинов 360 -720 к. Да Ig. M 935 к. Да Ig. D 172 к. Да Ig. E 196 к. Да Ig. G 150 к. Да Ig. A – главный класс иммуноглобулинов серозно-слизистых секретов Ig. D – обильно представлен на мембране многих В-клеток Ig. E – наблюдается на повышенном уровне при аллергических реакциях и паразитарных инфекциях Ig. G – главный изотип Ig нормальной сыворотки человека; на его долю приходится 70 общего количества сывороточных иммуноглобулинов Ig. M – локализован на мембране В-клеток; образуется первым при контакте с чужеродным антигеном Антитела Ig. M особенно активны против бактерий. ©
 После того, как эти активированные В-лимфоциты получат через свои CD 40 - и цитокиновые рецепторы специфический сигнал (при участии Тлимфоцитов), они приступят к переключению классов антител (Class Switch Recombination – CSR) для синтеза одного из белков: Ig. G, Ig. A или Ig. E. В процессе переключения один константный кодирующий сегмент заменяется на другой, но вариабельный район не затрагивается, то есть антигенная специфичность не изменяется. Позднее мы рассмотрим процесс переключения классов иммуноглобулинов более подробно, а сейчас вернемся к формированию вариабельных доменов иммуноглобулиновых генов.
После того, как эти активированные В-лимфоциты получат через свои CD 40 - и цитокиновые рецепторы специфический сигнал (при участии Тлимфоцитов), они приступят к переключению классов антител (Class Switch Recombination – CSR) для синтеза одного из белков: Ig. G, Ig. A или Ig. E. В процессе переключения один константный кодирующий сегмент заменяется на другой, но вариабельный район не затрагивается, то есть антигенная специфичность не изменяется. Позднее мы рассмотрим процесс переключения классов иммуноглобулинов более подробно, а сейчас вернемся к формированию вариабельных доменов иммуноглобулиновых генов.
 Гены, кодирующие тяжелые и легкие цепи иммуноглобулинов, формируются в незрелых В-лимфоцитах путем cлучайных рекомбинационных состыковок кодирующих сегментов V, (D) и J. Аналогичным способом формируются гены рецепторов Т-лимфоцитов. Рассмотрим схемы формирования генов легких k-цепей и тяжелых цепей иммуноглобулинов по отдельности.
Гены, кодирующие тяжелые и легкие цепи иммуноглобулинов, формируются в незрелых В-лимфоцитах путем cлучайных рекомбинационных состыковок кодирующих сегментов V, (D) и J. Аналогичным способом формируются гены рецепторов Т-лимфоцитов. Рассмотрим схемы формирования генов легких k-цепей и тяжелых цепей иммуноглобулинов по отдельности.
 Формирование генов легких k-цепей иммуноглобулинов Локус легких -цепей зародышевой линии включает ~40 различных Vkcегментов, каждый с собственной лидерной (L) последовательностью (на рисунке не показаны) и 5 Jk-сегментов. Протяженный (2 -3 т. п. н. ) интрон отделяет единственный Сk-сегмент константной области от сегментов Jk. Наличие лидерной последовательности – характерное свойство Vсегментов, кодирующих все типы цепей. Лидерные последовательности отщепляются (уже на уровне белкового продукта) в шероховатом эндоплазматическом ретикулуме. Vk-сегмент может соединиться с любым из сегментов Jk, вместе они образуют вариабельный экзон формируемого гена. Все остальные Jсегменты слева от присоединенного J-сегмента вырезаются и удаляются, а все J-сегменты справа воспринимаются как часть интрона между вариабельным (на рисунке это J 4) и константным экзонами и вырезаются в составе этого интрона при сплайсинге в ходе созревания первичного транскрипта. Таким образом состыковку вариабельного и константного доменов обеспечивает сплайсинг. На этом и на следующих слайдах интроны представлены в виде тонких линий между экзонами.
Формирование генов легких k-цепей иммуноглобулинов Локус легких -цепей зародышевой линии включает ~40 различных Vkcегментов, каждый с собственной лидерной (L) последовательностью (на рисунке не показаны) и 5 Jk-сегментов. Протяженный (2 -3 т. п. н. ) интрон отделяет единственный Сk-сегмент константной области от сегментов Jk. Наличие лидерной последовательности – характерное свойство Vсегментов, кодирующих все типы цепей. Лидерные последовательности отщепляются (уже на уровне белкового продукта) в шероховатом эндоплазматическом ретикулуме. Vk-сегмент может соединиться с любым из сегментов Jk, вместе они образуют вариабельный экзон формируемого гена. Все остальные Jсегменты слева от присоединенного J-сегмента вырезаются и удаляются, а все J-сегменты справа воспринимаются как часть интрона между вариабельным (на рисунке это J 4) и константным экзонами и вырезаются в составе этого интрона при сплайсинге в ходе созревания первичного транскрипта. Таким образом состыковку вариабельного и константного доменов обеспечивает сплайсинг. На этом и на следующих слайдах интроны представлены в виде тонких линий между экзонами.
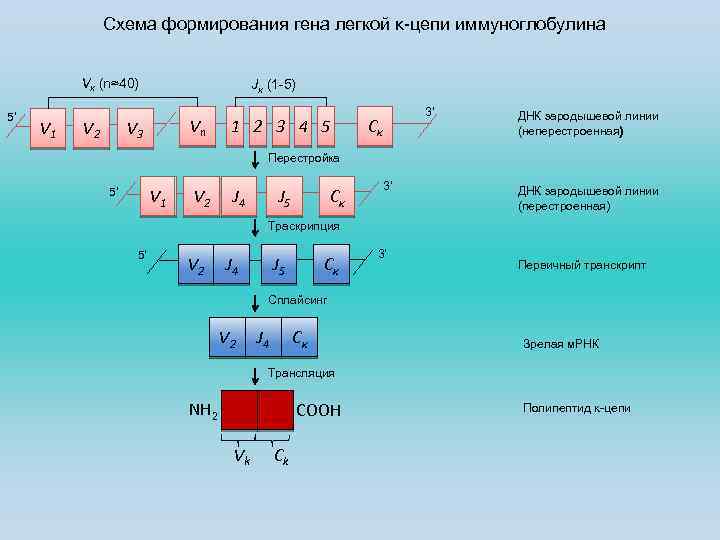 Схема формирования гена легкой κ-цепи иммуноглобулина Vκ (n≈40) 5’ V 1 V 2 Jκ (1 -5) Vn V 3 1 2 3 4 5 3’ Cκ ДНК зародышевой линии (неперестроенная) Перестройка V 1 5’ V 2 J 4 J 5 Cκ 3’ ДНК зародышевой линии (перестроенная) Траскрипция 5’ V 2 J 4 J 5 Cκ 3’ Первичный транскрипт Сплайсинг V 2 J 4 Cκ Зрелая м. РНК Трансляция NH 2 COOH Vk Ck Полипептид κ-цепи
Схема формирования гена легкой κ-цепи иммуноглобулина Vκ (n≈40) 5’ V 1 V 2 Jκ (1 -5) Vn V 3 1 2 3 4 5 3’ Cκ ДНК зародышевой линии (неперестроенная) Перестройка V 1 5’ V 2 J 4 J 5 Cκ 3’ ДНК зародышевой линии (перестроенная) Траскрипция 5’ V 2 J 4 J 5 Cκ 3’ Первичный транскрипт Сплайсинг V 2 J 4 Cκ Зрелая м. РНК Трансляция NH 2 COOH Vk Ck Полипептид κ-цепи
 Формирование генов тяжелых цепей иммуноглобулинов Для образования генов тяжелых цепей используются сегменты V, D и сегмент J-C. Первый раунд рекомбинации состыковывает сегменты D и J-C. Второй раунд объединяет сегменты V и D-J-C. Для локуса тяжелых цепей характерно наличие большого количества С-сегментов, каждый из них окружен с обеих сторон интронами. Кроме того, область константных сегментов отделена от вариабельных сегментов длинным интроном. Ближе всего к области вариабельных сегментов находятся С-сегменты m и d, которые в процессе развития В-лимфоцитов транскрибируются первыми. Перестроенная ДНК (первичный ген иммуноглобулина) транскрибируется вместе с С-сегментами m и d. Образовавшийся первичный транскрипт подвергается альтернативному сплайсингу с формированием двух м. РНК: VDJ-m и VDJ-d, трансляция которых приведет к синтезу соответствующих полипептидов. Таким образом, одна покоящаяся В-клетка может одновременно синтезировать как m-, так и d-тяжелые цепи, имеющие одинаковую антигенную специфичность. Кроме того, на 3’-конце каждого С-сегмента находятся два дополнительных экзона (на рисунке не представлены), один из которых кодирует трансмембранный и концевой цитоплазматический домены мембранной формы иммуноглобулина, в то время как другой – С-концевую часть секреторной формы молекулы иммуноглобулина. Оба экзона транскрибируются, но альтернативный сплайсинг первичного транскрипта приводит к синтезу либо мембранной, либо секреторной формы полипептида тяжелой цепи.
Формирование генов тяжелых цепей иммуноглобулинов Для образования генов тяжелых цепей используются сегменты V, D и сегмент J-C. Первый раунд рекомбинации состыковывает сегменты D и J-C. Второй раунд объединяет сегменты V и D-J-C. Для локуса тяжелых цепей характерно наличие большого количества С-сегментов, каждый из них окружен с обеих сторон интронами. Кроме того, область константных сегментов отделена от вариабельных сегментов длинным интроном. Ближе всего к области вариабельных сегментов находятся С-сегменты m и d, которые в процессе развития В-лимфоцитов транскрибируются первыми. Перестроенная ДНК (первичный ген иммуноглобулина) транскрибируется вместе с С-сегментами m и d. Образовавшийся первичный транскрипт подвергается альтернативному сплайсингу с формированием двух м. РНК: VDJ-m и VDJ-d, трансляция которых приведет к синтезу соответствующих полипептидов. Таким образом, одна покоящаяся В-клетка может одновременно синтезировать как m-, так и d-тяжелые цепи, имеющие одинаковую антигенную специфичность. Кроме того, на 3’-конце каждого С-сегмента находятся два дополнительных экзона (на рисунке не представлены), один из которых кодирует трансмембранный и концевой цитоплазматический домены мембранной формы иммуноглобулина, в то время как другой – С-концевую часть секреторной формы молекулы иммуноглобулина. Оба экзона транскрибируются, но альтернативный сплайсинг первичного транскрипта приводит к синтезу либо мембранной, либо секреторной формы полипептида тяжелой цепи.
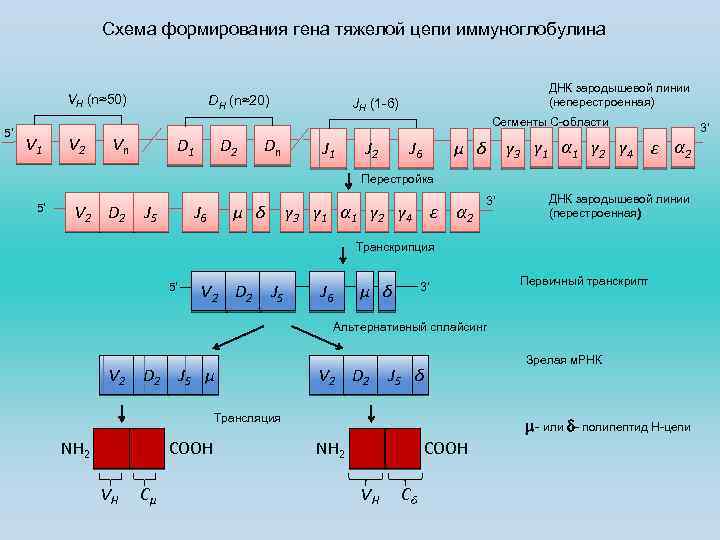 Схема формирования гена тяжелой цепи иммуноглобулина VH (n≈50) 5’ DH (n≈20) ДНК зародышевой линии (неперестроенная) JH (1 -6) Сегменты С-области V 1 V 2 Vn D 1 D 2 Dn J 1 J 2 J 6 μ δ γ 3 γ 1 α 1 γ 2 γ 4 ε α 2 Перестройка 5’ V 2 D 2 J 5 J 6 μ δ γ 3 γ 1 α 1 γ 2 γ 4 ε α 2 3’ ДНК зародышевой линии (перестроенная) Транскрипция 5’ V 2 D 2 J 5 J 6 3’ μ δ Первичный транскрипт Альтернативный сплайсинг V 2 D 2 J 5 μ V 2 D 2 J 5 δ Трансляция NH 2 COOH VH Cμ Зрелая м. РНК m- или d- полипептид Н-цепи NH 2 COOH VH Cδ 3’
Схема формирования гена тяжелой цепи иммуноглобулина VH (n≈50) 5’ DH (n≈20) ДНК зародышевой линии (неперестроенная) JH (1 -6) Сегменты С-области V 1 V 2 Vn D 1 D 2 Dn J 1 J 2 J 6 μ δ γ 3 γ 1 α 1 γ 2 γ 4 ε α 2 Перестройка 5’ V 2 D 2 J 5 J 6 μ δ γ 3 γ 1 α 1 γ 2 γ 4 ε α 2 3’ ДНК зародышевой линии (перестроенная) Транскрипция 5’ V 2 D 2 J 5 J 6 3’ μ δ Первичный транскрипт Альтернативный сплайсинг V 2 D 2 J 5 μ V 2 D 2 J 5 δ Трансляция NH 2 COOH VH Cμ Зрелая м. РНК m- или d- полипептид Н-цепи NH 2 COOH VH Cδ 3’
 Последовательность стадий формирования генов иммуноглобулинов строго запрограммирована. Сначала должен сформироваться функциональный ген тяжелой цепи. Кластер, из сегментов которого формируется ген тяжелой цепи, у человека, расположен на хромосоме 14. В диплоидной клетке имеются две гомологичных хромосомы, но ген может сформироваться только в одной, поэтому формирование идет поочередно, и если функциональный ген в одном гомологе сформировался сразу, то перестройка во втором гомологе не происходит (аллельное исключение). В случае если ген тяжелой цепи в первом гомологе не сформировался, клетка приступает к формированию гена во втором гомологе. Если и эта попытка оказалась неудачной, клетка уходит в апоптоз. Если функциональный ген тяжелой цепи в одном из гомологов сформировался, клетка приступает к формированию гена легкой цепи. Формирование функциональных генов легкой цепи идет по сходному пути, но у гена легкой цепи существует две изоформы – κ и λ, кластеры которых расположены в разных хромосомах (κ в хромосоме 2, λ – в 22). Таким образом, для формирования гена легкой цепи у клетки есть четыре попытки после чего, в случаи неудачи она уходит в апоптоз, а если ген сформировался, клетка продолжает развитие.
Последовательность стадий формирования генов иммуноглобулинов строго запрограммирована. Сначала должен сформироваться функциональный ген тяжелой цепи. Кластер, из сегментов которого формируется ген тяжелой цепи, у человека, расположен на хромосоме 14. В диплоидной клетке имеются две гомологичных хромосомы, но ген может сформироваться только в одной, поэтому формирование идет поочередно, и если функциональный ген в одном гомологе сформировался сразу, то перестройка во втором гомологе не происходит (аллельное исключение). В случае если ген тяжелой цепи в первом гомологе не сформировался, клетка приступает к формированию гена во втором гомологе. Если и эта попытка оказалась неудачной, клетка уходит в апоптоз. Если функциональный ген тяжелой цепи в одном из гомологов сформировался, клетка приступает к формированию гена легкой цепи. Формирование функциональных генов легкой цепи идет по сходному пути, но у гена легкой цепи существует две изоформы – κ и λ, кластеры которых расположены в разных хромосомах (κ в хромосоме 2, λ – в 22). Таким образом, для формирования гена легкой цепи у клетки есть четыре попытки после чего, в случаи неудачи она уходит в апоптоз, а если ген сформировался, клетка продолжает развитие.
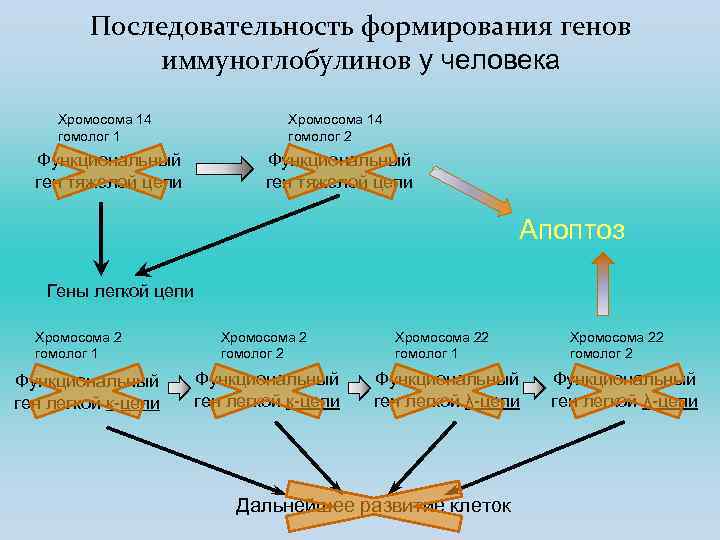 Последовательность формирования генов иммуноглобулинов у человека Хромосома 14 гомолог 1 Хромосома 14 гомолог 2 Функциональный ген тяжелой цепи Апоптоз Гены легкой цепи Хромосома 2 гомолог 1 Функциональный ген легкой к-цепи Хромосома 2 гомолог 2 Функциональный ген легкой к-цепи Хромосома 22 гомолог 1 Функциональный ген легкой λ-цепи Хромосома 22 гомолог 2 Функциональный ген легкой λ-цепи Дальнейшее развитие клеток ©
Последовательность формирования генов иммуноглобулинов у человека Хромосома 14 гомолог 1 Хромосома 14 гомолог 2 Функциональный ген тяжелой цепи Апоптоз Гены легкой цепи Хромосома 2 гомолог 1 Функциональный ген легкой к-цепи Хромосома 2 гомолог 2 Функциональный ген легкой к-цепи Хромосома 22 гомолог 1 Функциональный ген легкой λ-цепи Хромосома 22 гомолог 2 Функциональный ген легкой λ-цепи Дальнейшее развитие клеток ©
 МОЛЕКУЛЯРНЫЙ МЕХАНИЗМ V(D)J-РЕКОМБИНАЦИИ
МОЛЕКУЛЯРНЫЙ МЕХАНИЗМ V(D)J-РЕКОМБИНАЦИИ
 МОЛЕКУЛЯРНЫЙ МЕХАНИЗМ V(D)J-РЕКОМБИНАЦИИ – РАННИЕ ЭТАПЫ
МОЛЕКУЛЯРНЫЙ МЕХАНИЗМ V(D)J-РЕКОМБИНАЦИИ – РАННИЕ ЭТАПЫ
 Молекулярный механизм V(D)J-рекомбинации – ранние этапы. Рекомбинация между генными сегментами – это ключевой момент формирования функциональных генов легких и тяжелых цепей. В настоящее время известен механизм этих генных перестроек и идентифицированы специфические нуклеотидные последовательности, действующие в этом процессе в качестве сигнальных (RSS, от англ. recombination signal sequences). Сигнальная последовательность, расположенная на 5’-концах кодирующих V- , D- , и J-сегментов состоит из палиндромного гептамера CACAGTG и наномера АСАААААСС. Между ними расположен спейсер длиной 23 п. н. Сигнальная последовательность, расположенная на 3’-концах кодирующих сегментов, состоит из тех же наномера и гептамера, но длина спейсера между ними составляет 12 п. н. Гептамеры примыкают к концам сегментов, наномеры расположены дистальнее. Последовательности наномера и гептамера консенсусные, и в них есть так называемые критические нуклеотиды, от которых зависит эффективность рекомбинации. Рекомбинация может происходить только при условии, если длина спейсера с одной стороны кодирующего сегмента будет 12, а с другой стороны – 23 п. н. ( «правило 12/23» ).
Молекулярный механизм V(D)J-рекомбинации – ранние этапы. Рекомбинация между генными сегментами – это ключевой момент формирования функциональных генов легких и тяжелых цепей. В настоящее время известен механизм этих генных перестроек и идентифицированы специфические нуклеотидные последовательности, действующие в этом процессе в качестве сигнальных (RSS, от англ. recombination signal sequences). Сигнальная последовательность, расположенная на 5’-концах кодирующих V- , D- , и J-сегментов состоит из палиндромного гептамера CACAGTG и наномера АСАААААСС. Между ними расположен спейсер длиной 23 п. н. Сигнальная последовательность, расположенная на 3’-концах кодирующих сегментов, состоит из тех же наномера и гептамера, но длина спейсера между ними составляет 12 п. н. Гептамеры примыкают к концам сегментов, наномеры расположены дистальнее. Последовательности наномера и гептамера консенсусные, и в них есть так называемые критические нуклеотиды, от которых зависит эффективность рекомбинации. Рекомбинация может происходить только при условии, если длина спейсера с одной стороны кодирующего сегмента будет 12, а с другой стороны – 23 п. н. ( «правило 12/23» ).
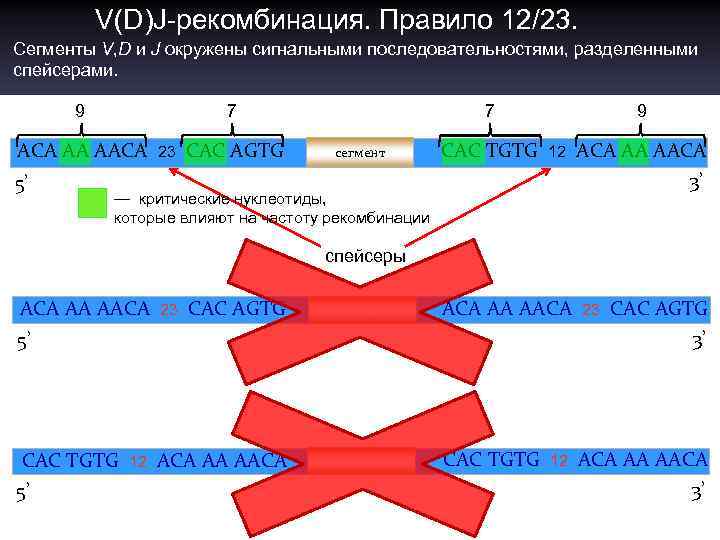 V(D)J-рекомбинация. Правило 12/23. Сегменты V, D и J окружены сигнальными последовательностями, разделенными спейсерами. 9 7 ACA AA AACA 5’ 23 CAC AGTG 7 сегмент CAC TGTG 9 12 — критические нуклеотиды, которые влияют на частоту рекомбинации ACA AA AACA 3’ спейсеры ACA AA AACA CAC AGTG сегмент ACA AA AACA 23 ACA AA AACA сегмент CAC TGTG ACA AA AACA 3’ 23 5’ CAC TGTG 5’ 12 12 CAC AGTG 3’
V(D)J-рекомбинация. Правило 12/23. Сегменты V, D и J окружены сигнальными последовательностями, разделенными спейсерами. 9 7 ACA AA AACA 5’ 23 CAC AGTG 7 сегмент CAC TGTG 9 12 — критические нуклеотиды, которые влияют на частоту рекомбинации ACA AA AACA 3’ спейсеры ACA AA AACA CAC AGTG сегмент ACA AA AACA 23 ACA AA AACA сегмент CAC TGTG ACA AA AACA 3’ 23 5’ CAC TGTG 5’ 12 12 CAC AGTG 3’
 Рекомбинация начинается с образования ДНР ДНК, которые формируются комплексом лимфоид-специфических белков Rag 1 и Rag 2, кодируемых генами RAG 1 и RAG 2 (recombination-activating genes). В системе in vitro этих белков достаточно для реакции разрезания ДНК в RSS. В условиях in vivo высокая эффективность реакции обеспечивается участием других вспомогательных белков, в том числе ДНК-связывающего белка HMG 1.
Рекомбинация начинается с образования ДНР ДНК, которые формируются комплексом лимфоид-специфических белков Rag 1 и Rag 2, кодируемых генами RAG 1 и RAG 2 (recombination-activating genes). В системе in vitro этих белков достаточно для реакции разрезания ДНК в RSS. В условиях in vivo высокая эффективность реакции обеспечивается участием других вспомогательных белков, в том числе ДНК-связывающего белка HMG 1.
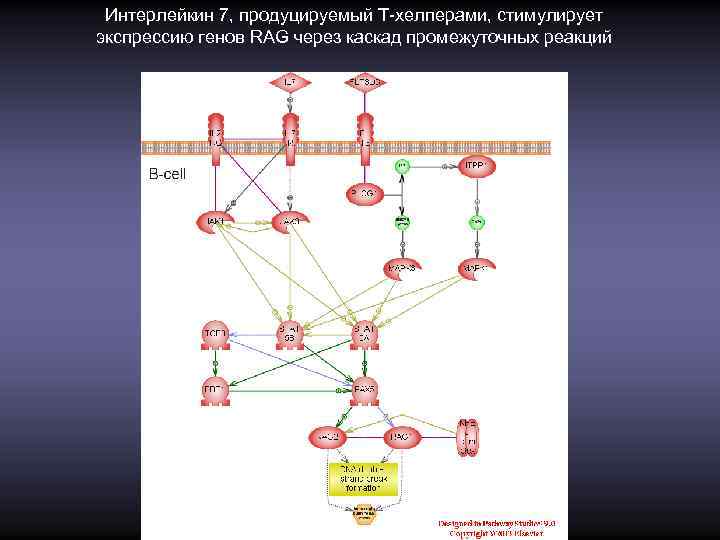 Интерлейкин 7, продуцируемый Т-хелперами, стимулирует экспрессию генов RAG через каскад промежуточных реакций
Интерлейкин 7, продуцируемый Т-хелперами, стимулирует экспрессию генов RAG через каскад промежуточных реакций
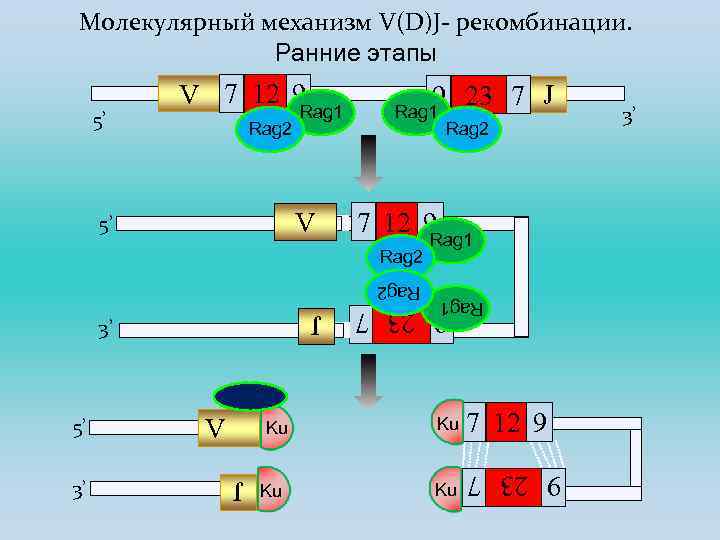
 Белки RAG 1 и RAG 2, воздействуя на синтетические фрагменты ДНК, содержащие сигнальные последовательности RSS в качестве субстрата, способны формировать синаптический комплекс из двух RSS. Сначала белок RAG 1 связывается с наномером, а белок RAG 2, неспособный непосредственно связаться с ДНК, присоединяется к комплексу RAG 1 -ДНК рядом со спейсером из 12 п. н. После этого между спейсерами из 12 и 23 п. н. возникает синапсис, повидимому, как результат взаимодействия между комплексами RAG 1 -Rag 2 наномер-спейсер (23) и RAG 1 -RAG 2 -наномер-спейсер (12). После связывания происходит направляемое гептамерами расщепление ДНК до ДНР на границах между ними и сегментами V-, (D-), и J.
Белки RAG 1 и RAG 2, воздействуя на синтетические фрагменты ДНК, содержащие сигнальные последовательности RSS в качестве субстрата, способны формировать синаптический комплекс из двух RSS. Сначала белок RAG 1 связывается с наномером, а белок RAG 2, неспособный непосредственно связаться с ДНК, присоединяется к комплексу RAG 1 -ДНК рядом со спейсером из 12 п. н. После этого между спейсерами из 12 и 23 п. н. возникает синапсис, повидимому, как результат взаимодействия между комплексами RAG 1 -Rag 2 наномер-спейсер (23) и RAG 1 -RAG 2 -наномер-спейсер (12). После связывания происходит направляемое гептамерами расщепление ДНК до ДНР на границах между ними и сегментами V-, (D-), и J.
 В результате разрывов на конце 12 п. н. -спейсера и 23 п. н. спейсера образуются 4 конца ДНК, два из которых, называемые сигнальными концами, при последующем соединении формируют сигнальную связь. Два других – кодирующих конца впоследствии сомкнутся с образованием кодирующей связи, то есть связи между кодирующими сегментами. Реакция формирования ДНР ДНК происходит в два этапа. Сначала белки RAG делают разрыв в одной цепи гептамера RSS. Возникающая при этом 3’-OH-группа атакует фосфодиэфирную связь в антипараллельной цепи, разрывет ее и ковалентно связывается с возникающим при этом 5’-P-концом (реакция трансэстерификации), результатом которой будут шпильки на обоих кодирующих концах и два «тупых» сигнальных конца – то есть образуется ДНР ДНК. Эта реакция, также катализируемая белками RAG, сходна с таковой, осуществляемой транспозазой при перемещении некоторых мобильных элементов. После формирования ДНР комплекс RAG 1 -RAG 2 -ДНК распадается.
В результате разрывов на конце 12 п. н. -спейсера и 23 п. н. спейсера образуются 4 конца ДНК, два из которых, называемые сигнальными концами, при последующем соединении формируют сигнальную связь. Два других – кодирующих конца впоследствии сомкнутся с образованием кодирующей связи, то есть связи между кодирующими сегментами. Реакция формирования ДНР ДНК происходит в два этапа. Сначала белки RAG делают разрыв в одной цепи гептамера RSS. Возникающая при этом 3’-OH-группа атакует фосфодиэфирную связь в антипараллельной цепи, разрывет ее и ковалентно связывается с возникающим при этом 5’-P-концом (реакция трансэстерификации), результатом которой будут шпильки на обоих кодирующих концах и два «тупых» сигнальных конца – то есть образуется ДНР ДНК. Эта реакция, также катализируемая белками RAG, сходна с таковой, осуществляемой транспозазой при перемещении некоторых мобильных элементов. После формирования ДНР комплекс RAG 1 -RAG 2 -ДНК распадается.
 Молекулярный механизм V(D)J- рекомбинации. Ранние этапы V 5’ 7 12 9 Rag 2 J 3’ V Ku J 5’ Ku Rag 1 9 23 7 3’ Rag 2 Ku 7 12 9 Ku 9 23 7 Rag 2 9 23 7 J Rag 1 5’ V 7 12 9 Rag 1 3’
Молекулярный механизм V(D)J- рекомбинации. Ранние этапы V 5’ 7 12 9 Rag 2 J 3’ V Ku J 5’ Ku Rag 1 9 23 7 3’ Rag 2 Ku 7 12 9 Ku 9 23 7 Rag 2 9 23 7 J Rag 1 5’ V 7 12 9 Rag 1 3’
 В спейсерах нуклеотиды, между которыми происходит рекомбинация, не являются постоянными, поэтому сама рекомбинация при последующем соединении сегментов окажется неточной: от 0 до 10 нуклеотидов либо утрачиваются на концах, либо добавляются к ним. Это приводит к т. н. разнообразию межсегментных соединений. После образования ДНР в RSS шпильки на кодирующих концах должны расщепиться, чтобы могли произойти процессинг и связывание концов. Шпильки надрезаются нуклеазой Artemis в комплексе с ДНК-зависимой протеинкиназой, причем сайт надрезания не фиксмрован (варьирует в пределах нескольких нуклеотидов), при этом высвобождающийся 3’-конец ДНК может подвергаться удалению/удалению отдельных нуклеотидов различными ДНК-полимеразами/экзонуклеазами. Процессинг подразумевает также добавление к концам дополнительных N-нуклеотидов, катализируемое лимфоид-специфичной терминальной дезоксинуклеотдилтрансферазой (Td. T), и удаление лишних однонитевых хвостов ДНК в точке их ответвления (могут возникать при состыковке концов). Кандидатом на эту роль является эндонуклеаза FEN-1 (flap endonuclease). Перечисленные процессы дополнительно повышают разнообразие межсегментных соединений.
В спейсерах нуклеотиды, между которыми происходит рекомбинация, не являются постоянными, поэтому сама рекомбинация при последующем соединении сегментов окажется неточной: от 0 до 10 нуклеотидов либо утрачиваются на концах, либо добавляются к ним. Это приводит к т. н. разнообразию межсегментных соединений. После образования ДНР в RSS шпильки на кодирующих концах должны расщепиться, чтобы могли произойти процессинг и связывание концов. Шпильки надрезаются нуклеазой Artemis в комплексе с ДНК-зависимой протеинкиназой, причем сайт надрезания не фиксмрован (варьирует в пределах нескольких нуклеотидов), при этом высвобождающийся 3’-конец ДНК может подвергаться удалению/удалению отдельных нуклеотидов различными ДНК-полимеразами/экзонуклеазами. Процессинг подразумевает также добавление к концам дополнительных N-нуклеотидов, катализируемое лимфоид-специфичной терминальной дезоксинуклеотдилтрансферазой (Td. T), и удаление лишних однонитевых хвостов ДНК в точке их ответвления (могут возникать при состыковке концов). Кандидатом на эту роль является эндонуклеаза FEN-1 (flap endonuclease). Перечисленные процессы дополнительно повышают разнообразие межсегментных соединений.
 МОЛЕКУЛЯРНЫЙ МЕХАНИЗМ V(D)J -РЕКОМБИНАЦИИ – ПОЗДНИЕ ЭТАПЫ (СОЕДИНЕНИЕ КОДИРУЮЩИХ КОНЦОВ ДНК)
МОЛЕКУЛЯРНЫЙ МЕХАНИЗМ V(D)J -РЕКОМБИНАЦИИ – ПОЗДНИЕ ЭТАПЫ (СОЕДИНЕНИЕ КОДИРУЮЩИХ КОНЦОВ ДНК)
 Далее подключается система негомологичной рекомбинации – NHEJ. На шпильки садятся Ku-белки, Ku 70 и Ku 86, образующие гетеродимер. К образовавшемуся комплексу присоединяется каталитическая субъединица DNA-PKCS (которая вместе с белками Ku 70 и Ku 86 входит в состав ДНК-зависимой протеинкиназы), и затем формируется весь комлекс белков NHEJ. Нуклеаза Артемида (Artemis) в комплексе с ДНК-зависимой протеинкиназой надрезает шпильки, причем сайт надрезания нефиксирован (варьирует в пределах нескольких нуклеотидов). Такие раскрытые структуры распознает терминальная дезоксинуклеотидилтрансфераза, которая внематрично добавляет дополнительные нуклеотиды (N-нуклеотиды) на одну цепочку каждой шпильки, что вносит дополнительное разнообразие в набор генов иммуноглобулинов. В результате происходит частичное перекрывание двух цепей. Для выстраивания кодирующих концов перед замыканием с помощью лимфоид-специфической NHEJ, в отличие от обычной NHEJ, необходима гомология между ними на коротком участке, т. н. микрогомология. Кроме того, при репарации последовательности ДНК в участке шпильки некоторые нуклеотиды могут быть удалены нуклеазой Artemis или другой экзонуклеазой, а некоторые (Р-нуклеотиды) вставлены ДНК-полимеразой. Это еще более повышает разнообразие генов иммуноглобулинов и их продуктов. Процессинг также подразумевает удаление лишних однонитевых хвостов ДНК в точке их ответвления (могут возникать при состыковке концов). Кандидатом на эту роль является эндонуклеаза FEN-1 (flap endonuclease).
Далее подключается система негомологичной рекомбинации – NHEJ. На шпильки садятся Ku-белки, Ku 70 и Ku 86, образующие гетеродимер. К образовавшемуся комплексу присоединяется каталитическая субъединица DNA-PKCS (которая вместе с белками Ku 70 и Ku 86 входит в состав ДНК-зависимой протеинкиназы), и затем формируется весь комлекс белков NHEJ. Нуклеаза Артемида (Artemis) в комплексе с ДНК-зависимой протеинкиназой надрезает шпильки, причем сайт надрезания нефиксирован (варьирует в пределах нескольких нуклеотидов). Такие раскрытые структуры распознает терминальная дезоксинуклеотидилтрансфераза, которая внематрично добавляет дополнительные нуклеотиды (N-нуклеотиды) на одну цепочку каждой шпильки, что вносит дополнительное разнообразие в набор генов иммуноглобулинов. В результате происходит частичное перекрывание двух цепей. Для выстраивания кодирующих концов перед замыканием с помощью лимфоид-специфической NHEJ, в отличие от обычной NHEJ, необходима гомология между ними на коротком участке, т. н. микрогомология. Кроме того, при репарации последовательности ДНК в участке шпильки некоторые нуклеотиды могут быть удалены нуклеазой Artemis или другой экзонуклеазой, а некоторые (Р-нуклеотиды) вставлены ДНК-полимеразой. Это еще более повышает разнообразие генов иммуноглобулинов и их продуктов. Процессинг также подразумевает удаление лишних однонитевых хвостов ДНК в точке их ответвления (могут возникать при состыковке концов). Кандидатом на эту роль является эндонуклеаза FEN-1 (flap endonuclease).
 Механизм рекомбинации NHEJ (non-homologous end-joining) Ku Ku DNA-PKCS – каталитическая субъединица ДНК-зависимой протеинкиназы (DNA-PK) Artemis – нуклеаза, разрезающая шпильки и осуществляющая процессинг концов ДНК Ku Ku XFL/Cernunnos Лигирование ДНК-лигаза IV XRCC 4 Участвует в сборке и стимулирует лигирование комплексом XRCC 4 ДНК-лигаза IV
Механизм рекомбинации NHEJ (non-homologous end-joining) Ku Ku DNA-PKCS – каталитическая субъединица ДНК-зависимой протеинкиназы (DNA-PK) Artemis – нуклеаза, разрезающая шпильки и осуществляющая процессинг концов ДНК Ku Ku XFL/Cernunnos Лигирование ДНК-лигаза IV XRCC 4 Участвует в сборке и стимулирует лигирование комплексом XRCC 4 ДНК-лигаза IV
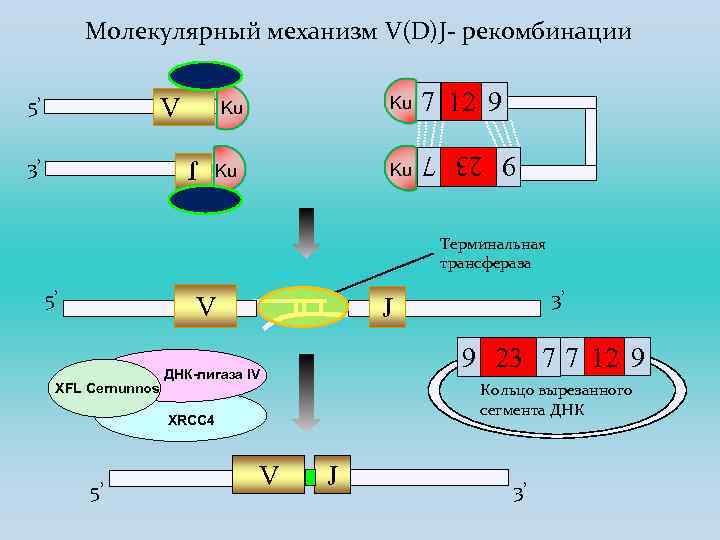 Молекулярный механизм V(D)J- рекомбинации J 3’ Ku Ku 7 12 9 Ku Ku 9 23 7 V 5’ Терминальная трансфераза 5’ V XFL/Cernunnos 9 23 7 7 12 9 ДНК-лигаза IV Кольцо вырезанного сегмента ДНК XRCC 4 5’ 3’ J V J 3’
Молекулярный механизм V(D)J- рекомбинации J 3’ Ku Ku 7 12 9 Ku Ku 9 23 7 V 5’ Терминальная трансфераза 5’ V XFL/Cernunnos 9 23 7 7 12 9 ДНК-лигаза IV Кольцо вырезанного сегмента ДНК XRCC 4 5’ 3’ J V J 3’
 Затем концы сшиваются комплексом ДНК-лигаза 4 -белок XRCC 4. Некомплементарные нуклеотиды удаляются, а оставшиеся бреши заполняются ДНК-полимеразой, предположительно ДНК-полимеразой β (другие кандидаты на эту роль – ДНК-полимеразы δ и ε). Таким образом, происходит состыковка кодирующих сегментов и формируется вариабельный V(D)J-экзон гена иммуноглобулина. В конечном итоге, после присоединения к нему константного экзона, образуется функциональный ген иммуноглобулина. Тупые сигнальные концы просто соединяются комплексом ДНК-лигаза 4 белок XRCC 4, формируя кольцевую структуру. В эту структуру включены вырезанные из хромосомы последовательности, промежуточные между состыкованными сегментами.
Затем концы сшиваются комплексом ДНК-лигаза 4 -белок XRCC 4. Некомплементарные нуклеотиды удаляются, а оставшиеся бреши заполняются ДНК-полимеразой, предположительно ДНК-полимеразой β (другие кандидаты на эту роль – ДНК-полимеразы δ и ε). Таким образом, происходит состыковка кодирующих сегментов и формируется вариабельный V(D)J-экзон гена иммуноглобулина. В конечном итоге, после присоединения к нему константного экзона, образуется функциональный ген иммуноглобулина. Тупые сигнальные концы просто соединяются комплексом ДНК-лигаза 4 белок XRCC 4, формируя кольцевую структуру. В эту структуру включены вырезанные из хромосомы последовательности, промежуточные между состыкованными сегментами.
 Таким образом, процесс состыковки сегментов, кодирующих ген иммуноглобулина, включает два разных механизма рекомбинации: 1. ДНР ДНК в RSS формируются с участием белков Rag 1 и Rag 2 по механизму, родственному нерепликативной транспозиции. 2. Состыковка концов разрезанной молекулы ДНК осуществляется с помощью негомологичной рекомбинации NHEJ. Перекомбинация множества кодирующих сегментов V, D и J на ранних стадиях дифференцировки В-лимфоцитов (до контакта с антигеном) обеспечивает первичное разнообразие генов иммуноглобулинов и кодируемых ими антител.
Таким образом, процесс состыковки сегментов, кодирующих ген иммуноглобулина, включает два разных механизма рекомбинации: 1. ДНР ДНК в RSS формируются с участием белков Rag 1 и Rag 2 по механизму, родственному нерепликативной транспозиции. 2. Состыковка концов разрезанной молекулы ДНК осуществляется с помощью негомологичной рекомбинации NHEJ. Перекомбинация множества кодирующих сегментов V, D и J на ранних стадиях дифференцировки В-лимфоцитов (до контакта с антигеном) обеспечивает первичное разнообразие генов иммуноглобулинов и кодируемых ими антител.
 Факторы, повышающие разнообразие генов иммуноглобулинов и кодируемых ими антител
Факторы, повышающие разнообразие генов иммуноглобулинов и кодируемых ими антител
 Выше мы уже говорили о дополнительных факторах, обеспечивающих повышение первичного разнообразия антител: Разнообразие межсегментных соединений, обусловленное неточностью V(D)J-рекомбинации (при процессинге шпильки и репарации этого участка могут быть удалены некоторые нуклеотиды и вставлены дополнительные (Р-нуклеотиды). Терминальная дезоксинуклеотидилтрансфераза (Td. T) внематрично вставляет дополнительные нуклеотиды (Nнуклеотиды) после разрезания шпилек. Далее мы рассмотрим другие процессы, работающие в том же направлении.
Выше мы уже говорили о дополнительных факторах, обеспечивающих повышение первичного разнообразия антител: Разнообразие межсегментных соединений, обусловленное неточностью V(D)J-рекомбинации (при процессинге шпильки и репарации этого участка могут быть удалены некоторые нуклеотиды и вставлены дополнительные (Р-нуклеотиды). Терминальная дезоксинуклеотидилтрансфераза (Td. T) внематрично вставляет дополнительные нуклеотиды (Nнуклеотиды) после разрезания шпилек. Далее мы рассмотрим другие процессы, работающие в том же направлении.
 После завершения V(D)-рекомбинации зрелые В-лимфоциты мигрируют из костного мозга во вторичные лимфоидные ткани (лимфатические узлы и селезенка), где они встречают антигены, которые им презентируют Т-лимфоциты или фолликулярные дендритные клетки. Лимфоциты, связавшиеся с антигеном через свои иммуноглобулиновые рецепторы, получают сигнал к пролиферации, который стимулирует их дальнейшие деления и дифференцировку. Ключевую роль в процессах, происходящих после этого в стимулированных В-лимфоцитах, играет лимфоид-специфический белок AID (Activation Induced Deaminase). AID инициирует три раздельных процесса диверсификации иммуноглобулинов: 1. соматический гипермутагенез; 2. переключение класса (изотипа) иммуноглобулинов (Class Switch Recombination – CSR); 3. соматическая генная конверсия. В соматическом гипермутагенезе задействованы также ДНКполимеразы TLS, переключение классов иммуноглобулинов использует механизм NHEJ, генная конверсия относится к гомологичной рекомбинации. Перечисленные процессы работают на усиление аффиности антител по отношению к антигенам.
После завершения V(D)-рекомбинации зрелые В-лимфоциты мигрируют из костного мозга во вторичные лимфоидные ткани (лимфатические узлы и селезенка), где они встречают антигены, которые им презентируют Т-лимфоциты или фолликулярные дендритные клетки. Лимфоциты, связавшиеся с антигеном через свои иммуноглобулиновые рецепторы, получают сигнал к пролиферации, который стимулирует их дальнейшие деления и дифференцировку. Ключевую роль в процессах, происходящих после этого в стимулированных В-лимфоцитах, играет лимфоид-специфический белок AID (Activation Induced Deaminase). AID инициирует три раздельных процесса диверсификации иммуноглобулинов: 1. соматический гипермутагенез; 2. переключение класса (изотипа) иммуноглобулинов (Class Switch Recombination – CSR); 3. соматическая генная конверсия. В соматическом гипермутагенезе задействованы также ДНКполимеразы TLS, переключение классов иммуноглобулинов использует механизм NHEJ, генная конверсия относится к гомологичной рекомбинации. Перечисленные процессы работают на усиление аффиности антител по отношению к антигенам.
 Процесс соматического гипермутагенеза, связанный с белком AID и TLS-полимеразами рассмотрим подробнее. Соматический гипермутагенез происходит в вариабельных доменах генов иммуноглобулинов при созревании B-лимфоцитов после их стимуляции антигеном. Он проявляется в точечных заменах нуклеотидов (частота замен превышает частоту спонтанного мутирования в 104 -106 раз по сравнению с другими участками ДНК). Главную роль в соматическом гипермутагенезе играют лимфоидспецифический белок AID и TLS-ДНК-полимераза Pol h (эта). Белок AID является инициатором и главным регулятором соматического гипермутагенеза. Он дезаминирует цитозин, превращая его в урацил, то есть превращает пару G-C в пару неспаренных оснований G·U, которая распознается аппаратом репликации как G·T и при последующей репликации превратится в пару Т-А.
Процесс соматического гипермутагенеза, связанный с белком AID и TLS-полимеразами рассмотрим подробнее. Соматический гипермутагенез происходит в вариабельных доменах генов иммуноглобулинов при созревании B-лимфоцитов после их стимуляции антигеном. Он проявляется в точечных заменах нуклеотидов (частота замен превышает частоту спонтанного мутирования в 104 -106 раз по сравнению с другими участками ДНК). Главную роль в соматическом гипермутагенезе играют лимфоидспецифический белок AID и TLS-ДНК-полимераза Pol h (эта). Белок AID является инициатором и главным регулятором соматического гипермутагенеза. Он дезаминирует цитозин, превращая его в урацил, то есть превращает пару G-C в пару неспаренных оснований G·U, которая распознается аппаратом репликации как G·T и при последующей репликации превратится в пару Т-А.
 ДНК с возникшими в результате дезаминирования цитозина неспариваниями U·G может далее подвергаться различным превращениям: 1. Репликация такой ДНК даст две дочерних молекулы: исходного типа и мутантную, с транзицией А-Т. 2. Неспаренный урацил может быть вырезан урацил-ДНК-гликозилазой (UDG), что приведет к возникновению апиримидинового (АР) сайта. ДНК с АР-сайтом может реплицироваться с участием TLS-полимеразы с включением на месте сайте любого случайного нуклеотида. Это – мутация. Альтернативно, ДНК с АР-сайтом может быть надрезана АР-эндонуклеазой и подвергнуться эксцизионной репарации оснований (BER), в которой репаративную застройку бреши осуществит мутагенная TLS-полимераза. В этой связи важно отметить следующее: в обычной BER застройку брешей осуществляет точная ДНК-полимераза b. Однако в В-лимфоцитах активность этой полимеразы подавлена, в результате чего в репарацию урацил-содержащей ДНК могут быть вовлечены TLS-полимеразы семейства Y. Если два АР-сайта расположены рядом друг с другом, что в этой системе случается достаточно часто, бреши, возникающие при их репарации, могут перекрыться и привести к ДНР ДНК. Попутно отметим, что ДНР, возникшие при осуществлении BER в сайте переключения изотипов или в вариабельном домене иммуноглобулина, могут индуцировать CSR или генную конверсию, соответственно. Продолжение через один слайд.
ДНК с возникшими в результате дезаминирования цитозина неспариваниями U·G может далее подвергаться различным превращениям: 1. Репликация такой ДНК даст две дочерних молекулы: исходного типа и мутантную, с транзицией А-Т. 2. Неспаренный урацил может быть вырезан урацил-ДНК-гликозилазой (UDG), что приведет к возникновению апиримидинового (АР) сайта. ДНК с АР-сайтом может реплицироваться с участием TLS-полимеразы с включением на месте сайте любого случайного нуклеотида. Это – мутация. Альтернативно, ДНК с АР-сайтом может быть надрезана АР-эндонуклеазой и подвергнуться эксцизионной репарации оснований (BER), в которой репаративную застройку бреши осуществит мутагенная TLS-полимераза. В этой связи важно отметить следующее: в обычной BER застройку брешей осуществляет точная ДНК-полимераза b. Однако в В-лимфоцитах активность этой полимеразы подавлена, в результате чего в репарацию урацил-содержащей ДНК могут быть вовлечены TLS-полимеразы семейства Y. Если два АР-сайта расположены рядом друг с другом, что в этой системе случается достаточно часто, бреши, возникающие при их репарации, могут перекрыться и привести к ДНР ДНК. Попутно отметим, что ДНР, возникшие при осуществлении BER в сайте переключения изотипов или в вариабельном домене иммуноглобулина, могут индуцировать CSR или генную конверсию, соответственно. Продолжение через один слайд.
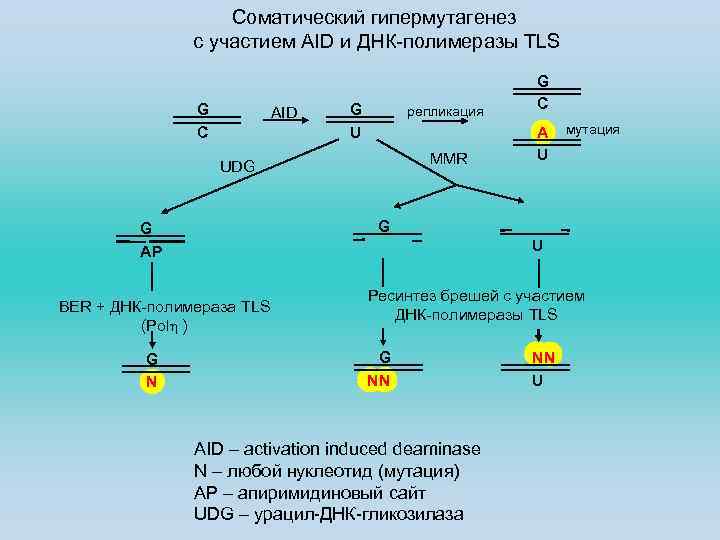 Соматический гипермутагенез с участием AID и ДНК-полимеразы TLS G C AID репликация MMR G U UDG A U мутация G G AP U BER + ДНК-полимераза TLS (Polη ) G N G C Ресинтез брешей с участием ДНК-полимеразы TLS G NN AID – activation induced deaminase N – любой нуклеотид (мутация) AP – апиримидиновый сайт UDG – урацил-ДНК-гликозилаза NN U
Соматический гипермутагенез с участием AID и ДНК-полимеразы TLS G C AID репликация MMR G U UDG A U мутация G G AP U BER + ДНК-полимераза TLS (Polη ) G N G C Ресинтез брешей с участием ДНК-полимеразы TLS G NN AID – activation induced deaminase N – любой нуклеотид (мутация) AP – апиримидиновый сайт UDG – урацил-ДНК-гликозилаза NN U
 3. Неспаренные U·G могут быть репарированы системой MMR, в которой репаративный синтез бреши осуществит мутагенная ДНК-полимераза TLS. У мышей, дефектных по различным компонентам системы MMR, наблюдается снижение уровня соматического мутагенеза и повышение соотношения частот мутаций в парах G-C над А-Т. Бреши, возникающие при осуществлении MMR, могут перекрываться и формировать ДНР, как и в случае BER, и так же индуцировать CSR и генную конверсию. ДНК-полимеразы TLS характеризуются большим количеством ошибок, которые они допускают при репаративной репликации в гипервариабельных районах иммуноглобулиновых генов.
3. Неспаренные U·G могут быть репарированы системой MMR, в которой репаративный синтез бреши осуществит мутагенная ДНК-полимераза TLS. У мышей, дефектных по различным компонентам системы MMR, наблюдается снижение уровня соматического мутагенеза и повышение соотношения частот мутаций в парах G-C над А-Т. Бреши, возникающие при осуществлении MMR, могут перекрываться и формировать ДНР, как и в случае BER, и так же индуцировать CSR и генную конверсию. ДНК-полимеразы TLS характеризуются большим количеством ошибок, которые они допускают при репаративной репликации в гипервариабельных районах иммуноглобулиновых генов.
 У генов, кодирующих Т-клеточные рецепторы, соматический гипермутагенез не обнаружен. Если разнообразие сочетаний кодирующих сегментов и случайные сочетания различных тяжелых и легких цепей в молекулах антител обеспечивают диапазон вариабельности порядка 106, то перечисленные выше факторы повышают потенциально возможное количество иммуноглобулинов до 1012 и более.
У генов, кодирующих Т-клеточные рецепторы, соматический гипермутагенез не обнаружен. Если разнообразие сочетаний кодирующих сегментов и случайные сочетания различных тяжелых и легких цепей в молекулах антител обеспечивают диапазон вариабельности порядка 106, то перечисленные выше факторы повышают потенциально возможное количество иммуноглобулинов до 1012 и более.
 Переключение класса иммуноглобулинов
Переключение класса иммуноглобулинов
 Ранее мы рассмотрели, как один и тот же В-лимфоцит в результате альтернативного сплайсинга может синтезировать Ig. M и Ig. D c одинаковой антигенной специфичностью. Далее мы покажем, как В-лимфоцит может переключаться на синтез антител одного из остальных классов (изотипов): Ig. A, Ig. E или Ig. G. Этот процесс носит название переключение класса (или изотипа) – СSR. В основе переключения класса лежат перестройки уже сформированных генов, кодирующих тяжелые цепи иммуноглобулинов. Они происходят в стимулированных антигеном зрелых В-клетках, синтезирующих Ig. M и Ig. D, и зависят от цитокинов, высвобождаемых Т-клетками. В результате каждая В-клетка, имеющая уникальную антигенную специфичность, способна синтезировать антитела всех возможных классов в зависимости от переключений в ДНК, кодирующих тяжелые цепи. Рассмотрим молекулярный механизм процесса переключения.
Ранее мы рассмотрели, как один и тот же В-лимфоцит в результате альтернативного сплайсинга может синтезировать Ig. M и Ig. D c одинаковой антигенной специфичностью. Далее мы покажем, как В-лимфоцит может переключаться на синтез антител одного из остальных классов (изотипов): Ig. A, Ig. E или Ig. G. Этот процесс носит название переключение класса (или изотипа) – СSR. В основе переключения класса лежат перестройки уже сформированных генов, кодирующих тяжелые цепи иммуноглобулинов. Они происходят в стимулированных антигеном зрелых В-клетках, синтезирующих Ig. M и Ig. D, и зависят от цитокинов, высвобождаемых Т-клетками. В результате каждая В-клетка, имеющая уникальную антигенную специфичность, способна синтезировать антитела всех возможных классов в зависимости от переключений в ДНК, кодирующих тяжелые цепи. Рассмотрим молекулярный механизм процесса переключения.
 Молекулярный механизм процесса переключения класса иммуноглобулинов – CSR Переключение происходит после контакта В-лимфоцита с антигеном. В стимуляции процесса также участвуют цитокины, высвобождаемые Тклетками. В ходе переключения из хромосомы удаляется участок между вариабельным сегментом и нужным константным сегментом и происходит их состыковка с формированием нового варианта гена, в котором один константный сегмент заменен на другой. В хромосоме перед каждым С-сегментом, кроме сегмента Сd, имеется консервативная нуклеотидная последовательность, называемая S (switch region). На рисунке на следующем слайде она отмечена ромбом. В двух определенных сайтах S возникают ДНР ДНК. Инициирующую роль в формировании ДНР играет белок AID, вслед за которым по схеме, описанной выше, действуют белки BER – UDG, AP-эндонуклеаза и т. д. Свободные концы в сайтах ДНР соединяются с помощью системы NHEJ. В-лимфоциты, претерпевшие CSR, будут синтезировать иммуноглобулин только одного класса.
Молекулярный механизм процесса переключения класса иммуноглобулинов – CSR Переключение происходит после контакта В-лимфоцита с антигеном. В стимуляции процесса также участвуют цитокины, высвобождаемые Тклетками. В ходе переключения из хромосомы удаляется участок между вариабельным сегментом и нужным константным сегментом и происходит их состыковка с формированием нового варианта гена, в котором один константный сегмент заменен на другой. В хромосоме перед каждым С-сегментом, кроме сегмента Сd, имеется консервативная нуклеотидная последовательность, называемая S (switch region). На рисунке на следующем слайде она отмечена ромбом. В двух определенных сайтах S возникают ДНР ДНК. Инициирующую роль в формировании ДНР играет белок AID, вслед за которым по схеме, описанной выше, действуют белки BER – UDG, AP-эндонуклеаза и т. д. Свободные концы в сайтах ДНР соединяются с помощью системы NHEJ. В-лимфоциты, претерпевшие CSR, будут синтезировать иммуноглобулин только одного класса.
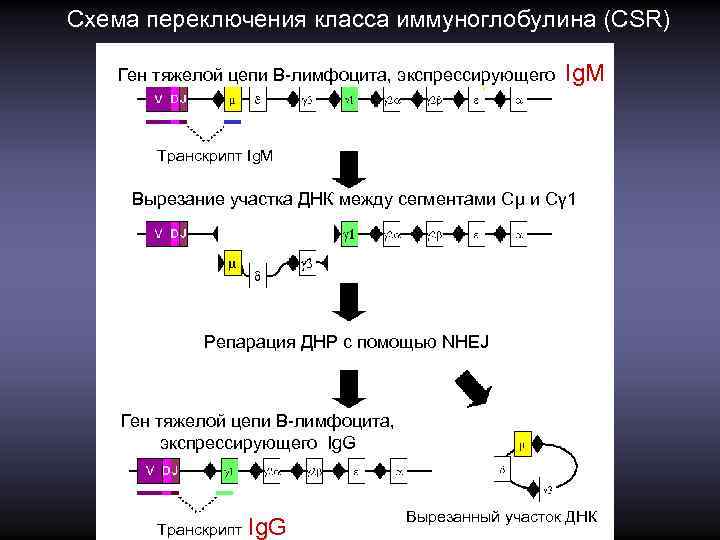 Схема переключения класса иммуноглобулина (CSR) Ген тяжелой цепи B-лимфоцита, экспрессирующего Ig. M Транскрипт Ig. M Вырезание участка ДНК между сегментами Сµ и Сγ 1 Репарация ДНР с помощью NHEJ Ген тяжелой цепи B-лимфоцита, экспрессирующего Ig. G Транскрипт Ig. G Вырезанный участок ДНК
Схема переключения класса иммуноглобулина (CSR) Ген тяжелой цепи B-лимфоцита, экспрессирующего Ig. M Транскрипт Ig. M Вырезание участка ДНК между сегментами Сµ и Сγ 1 Репарация ДНР с помощью NHEJ Ген тяжелой цепи B-лимфоцита, экспрессирующего Ig. G Транскрипт Ig. G Вырезанный участок ДНК
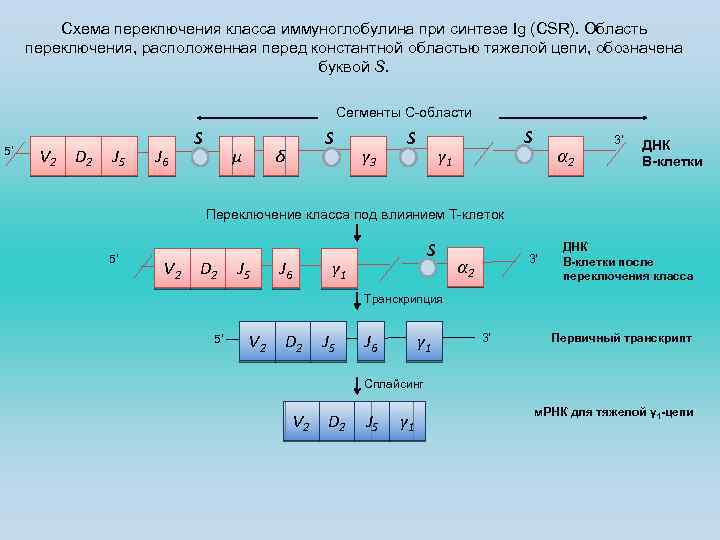 Схема переключения класса иммуноглобулина при синтезе Ig (CSR). Область переключения, расположенная перед константной областью тяжелой цепи, обозначена буквой S. Сегменты С-области 5’ V 2 D 2 J 5 J 6 S μ S δ γ 3 S S γ 1 α 2 3’ ДНК В-клетки Переключение класса под влиянием Т-клеток 5’ V 2 D 2 J 5 J 6 S γ 1 3’ α 2 ДНК В-клетки после переключения класса Транскрипция 5’ V 2 D 2 J 5 J 6 γ 1 3’ Первичный транскрипт Сплайсинг V 2 D 2 J 5 γ 1 м. РНК для тяжелой γ 1 -цепи
Схема переключения класса иммуноглобулина при синтезе Ig (CSR). Область переключения, расположенная перед константной областью тяжелой цепи, обозначена буквой S. Сегменты С-области 5’ V 2 D 2 J 5 J 6 S μ S δ γ 3 S S γ 1 α 2 3’ ДНК В-клетки Переключение класса под влиянием Т-клеток 5’ V 2 D 2 J 5 J 6 S γ 1 3’ α 2 ДНК В-клетки после переключения класса Транскрипция 5’ V 2 D 2 J 5 J 6 γ 1 3’ Первичный транскрипт Сплайсинг V 2 D 2 J 5 γ 1 м. РНК для тяжелой γ 1 -цепи
 Участие генной конверсии в формировании генов иммуноглобулинов Способ формирования генов иммуноглобулинов, в основе которого лежит произвольная состыковка разнообразных кодирующих V-, (D-) и Jсегментов, случайно выбираемых из геномной ДНК, обнаружен в исследованиях на клетках мыши и человека. Однако в последующих исследованиях на многих других видах животных (сначала курица, а затем кролик, свинья, овца, крупный рогатый скот, лошадь) было показано, что в основе разнообразия иммуноглобулинов у них лежит механизм соматической генной конверсии.
Участие генной конверсии в формировании генов иммуноглобулинов Способ формирования генов иммуноглобулинов, в основе которого лежит произвольная состыковка разнообразных кодирующих V-, (D-) и Jсегментов, случайно выбираемых из геномной ДНК, обнаружен в исследованиях на клетках мыши и человека. Однако в последующих исследованиях на многих других видах животных (сначала курица, а затем кролик, свинья, овца, крупный рогатый скот, лошадь) было показано, что в основе разнообразия иммуноглобулинов у них лежит механизм соматической генной конверсии.
 Оказалось, что, в отличие от человека и мыши, локусы L- и Н-цепей у курицы содержат по единственному функциональному V-сегменту, снабженному сигнальной рекомбинационной последовательностью (RSS) для белков RAG. В этих случаях в В-лимфоцитах первоначально формируется по одному гену (реже очень ограниченному количеству генов) для тяжелой и легкой цепей, а их последующее разнообразие обеспечивается за счет конверсии уже сформированных генов, использующей в качестве доноров генетической информации короткие нуклеотидные последовательности, случайно выбираемые из набора V-сегментов-псевдогенов (в случае курицы 25 для L-цепей и 80 для Н-цепей). Последние не участвуют в перестройках, а участвуют только в конверсии. При этом один ген может акцептировать информацию от нескольких псевдогенов, но только из той же хромосомы, то есть конверсия всегда внутрихромосомная. Разнообразие иммуноглобулинов и здесь дополняется соматическим гипермутагенезом. Разные виды животных отличаются по относительному вкладу конверсии и гипермутагенеза в разнообразие иммуноглобулинов.
Оказалось, что, в отличие от человека и мыши, локусы L- и Н-цепей у курицы содержат по единственному функциональному V-сегменту, снабженному сигнальной рекомбинационной последовательностью (RSS) для белков RAG. В этих случаях в В-лимфоцитах первоначально формируется по одному гену (реже очень ограниченному количеству генов) для тяжелой и легкой цепей, а их последующее разнообразие обеспечивается за счет конверсии уже сформированных генов, использующей в качестве доноров генетической информации короткие нуклеотидные последовательности, случайно выбираемые из набора V-сегментов-псевдогенов (в случае курицы 25 для L-цепей и 80 для Н-цепей). Последние не участвуют в перестройках, а участвуют только в конверсии. При этом один ген может акцептировать информацию от нескольких псевдогенов, но только из той же хромосомы, то есть конверсия всегда внутрихромосомная. Разнообразие иммуноглобулинов и здесь дополняется соматическим гипермутагенезом. Разные виды животных отличаются по относительному вкладу конверсии и гипермутагенеза в разнообразие иммуноглобулинов.
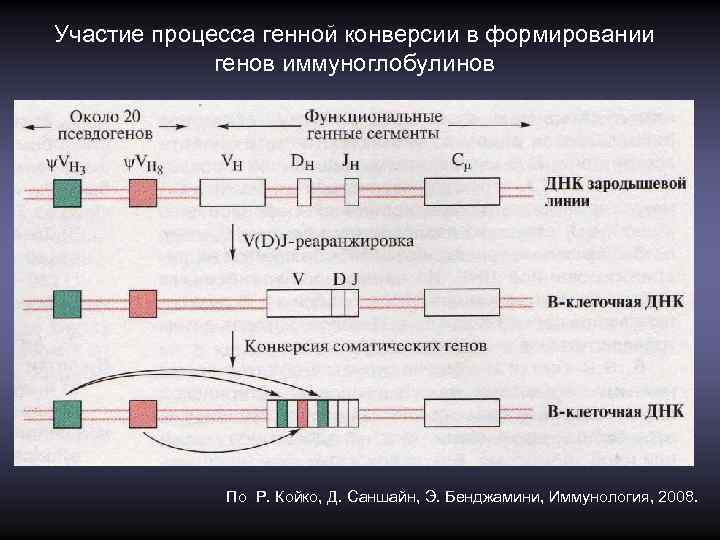 Участие процесса генной конверсии в формировании генов иммуноглобулинов По Р. Койко, Д. Саншайн, Э. Бенджамини, Иммунология, 2008.
Участие процесса генной конверсии в формировании генов иммуноглобулинов По Р. Койко, Д. Саншайн, Э. Бенджамини, Иммунология, 2008.
 Таким образом, процессы формирования генов иммуноглобулинов и генов Т-клеточных рецепторов у позвоночных представляют самый яркий и наиболее изученный пример запрограммированных геномных перестроек, происходящих в особых районах хромосом. Эти процессы включают формирование ДНР ДНК с участием белков, родственных транспозазам мобильных генетических элементов, залечивание разрывов с помощью негомологичной рекомбинации NHEJ, нематричное включение нуклеотидов в ДНК, генную конверсию (нереципрокная гомологичная рекомбинация) и соматический гипермутагенез. Все перечисленные процессы строго запрограммированы в отношении их последовательности и времени осуществления в ходе дифференцировки лимфоцитов. Отдельный интерес представляют генетическая регуляция формирования этих генов (и дифференцировки лимфоцитов), с одной стороны, и их экспрессии, с другой.
Таким образом, процессы формирования генов иммуноглобулинов и генов Т-клеточных рецепторов у позвоночных представляют самый яркий и наиболее изученный пример запрограммированных геномных перестроек, происходящих в особых районах хромосом. Эти процессы включают формирование ДНР ДНК с участием белков, родственных транспозазам мобильных генетических элементов, залечивание разрывов с помощью негомологичной рекомбинации NHEJ, нематричное включение нуклеотидов в ДНК, генную конверсию (нереципрокная гомологичная рекомбинация) и соматический гипермутагенез. Все перечисленные процессы строго запрограммированы в отношении их последовательности и времени осуществления в ходе дифференцировки лимфоцитов. Отдельный интерес представляют генетическая регуляция формирования этих генов (и дифференцировки лимфоцитов), с одной стороны, и их экспрессии, с другой.
 Адаптивный иммунитет у миног и миксин (бесчелюстные)
Адаптивный иммунитет у миног и миксин (бесчелюстные)
 Миноги и миксины имеют лимфоциты и способны развивать гуморальный иммунный ответ. Однако у них отсутствуют гены RAG, а их лимфоциты не синтезируют иммуноглобулины. Функции иммуноглобулинов у бесчелюстных выполняют так называемые VLR (Variable Lymphocyte Receptors). В геномах зародышевых и соматических клеток бесчелюстных содержатся различные кодирующие сегменты, из которых при созревании лимфоцитов собираются гены VLR. Среди них ключевыми являются сегменты, кодирующие N- и С-концевые части будущего VLR и набор вариабельных богатых лейцином повторов LRR (Leucine Rich Repeats), формирующих в гене VLR центральный вариабельный район. Предполагается, что последовательная сборка VLR происходит по схеме, сходной переключением классов иммуноглобулинов (CSR) у челюстноротых. В геноме миноги выявлены два лимфоид-специфических ортолога гена AID. Вероятно, как и в случае переключения классов иммуноглобулинов (CSR) в В-лимфоцитах, дезаминирование цитозина ортологами AID сопровождается возникновением ДНР, репарация которого участием NHEJ приведет к встраиванию (состыковке) произвольного LRR в формирующийся ген VLR.
Миноги и миксины имеют лимфоциты и способны развивать гуморальный иммунный ответ. Однако у них отсутствуют гены RAG, а их лимфоциты не синтезируют иммуноглобулины. Функции иммуноглобулинов у бесчелюстных выполняют так называемые VLR (Variable Lymphocyte Receptors). В геномах зародышевых и соматических клеток бесчелюстных содержатся различные кодирующие сегменты, из которых при созревании лимфоцитов собираются гены VLR. Среди них ключевыми являются сегменты, кодирующие N- и С-концевые части будущего VLR и набор вариабельных богатых лейцином повторов LRR (Leucine Rich Repeats), формирующих в гене VLR центральный вариабельный район. Предполагается, что последовательная сборка VLR происходит по схеме, сходной переключением классов иммуноглобулинов (CSR) у челюстноротых. В геноме миноги выявлены два лимфоид-специфических ортолога гена AID. Вероятно, как и в случае переключения классов иммуноглобулинов (CSR) в В-лимфоцитах, дезаминирование цитозина ортологами AID сопровождается возникновением ДНР, репарация которого участием NHEJ приведет к встраиванию (состыковке) произвольного LRR в формирующийся ген VLR.
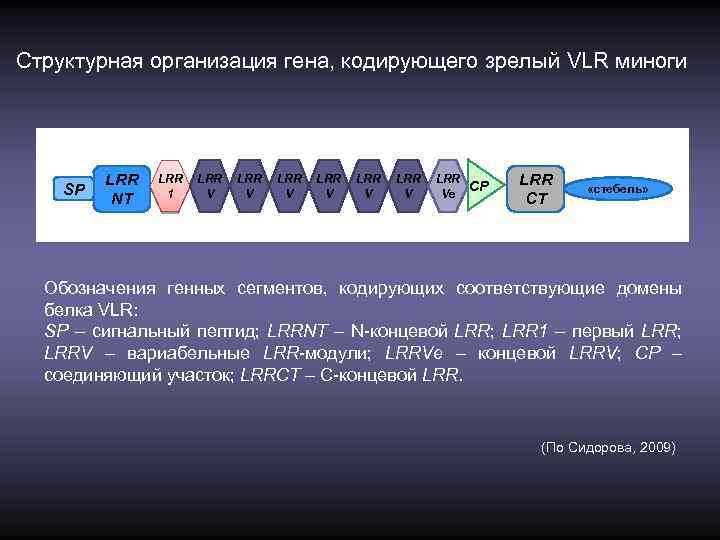 Структурная организация гена, кодирующего зрелый VLR миноги SP LRR NT LRR 1 LRR V LRR V LRR СР Ve LRR CT «стебель» Обозначения генных сегментов, кодирующих соответствующие домены белка VLR: SP – сигнальный пептид; LRRNT – N-концевой LRR; LRR 1 – первый LRR; LRRV – вариабельные LRR-модули; LRRVe – концевой LRRV; CP – соединяющий участок; LRRCT – C-концевой LRR. (По Сидорова, 2009)
Структурная организация гена, кодирующего зрелый VLR миноги SP LRR NT LRR 1 LRR V LRR V LRR СР Ve LRR CT «стебель» Обозначения генных сегментов, кодирующих соответствующие домены белка VLR: SP – сигнальный пептид; LRRNT – N-концевой LRR; LRR 1 – первый LRR; LRRV – вариабельные LRR-модули; LRRVe – концевой LRRV; CP – соединяющий участок; LRRCT – C-концевой LRR. (По Сидорова, 2009)


