2Нормальная микрофлора организма человека. ОЗ..ppt
- Количество слайдов: 92

Основы экологической микробиологии. Микрофлора тела здорового человека. Дисбактериоз


ОСНОВНЫЕ ПОНЯТИЯ ПО МИКРОЭКОЛОГИИ Экология микроорганизмов - наука о взаимоотношениях микробов друг с другом и с окружающей средой. В медицинской микробиологии объектом изучения служит комплекс взаимоотношений микроорганизмов с человеком. Популяция – совокупность особей одного вида, обитающих в пределах определенного биотопа. Биотоп – территориально ограниченный участок биосферы с относительно однородными условиями жизни. Микробиоценоз – сообщество популяций микроорганизмов, обитающих в определенном биотопе.

Микроколонии бактерий - биопленки, в разных биотопах.

Типы взаимоотношений микробов в биоценозах Симбиоз - совместное длительное существование микроорганизмов в долгоживущих сообществах. При этом обе популяции извлекают для себя пользу. Коменсализм - разновидность симбиоза, при которой выгоду извлекает только один партнер, не принося видимого вреда другому

Паразитизм Антагонистический симбиоз - симбиотические отношения, наносящие хозяину более или менее выраженный вред; его крайнее проявление паразитизм. Паразитические виды живут за счет живых тканей растений и животных. Проникая в организм хозяина, они могут вызывать у него заболевание, поэтому их обозначают как патогенные микроорганизмы. Факультативные паразиты в зависимости от внешних условий могут вести себя как паразиты, либо как сапрофиты. К ним относятся большинство условно-патогенных бактерий.

Облигатные паразиты в естественных условия размножаются только в организме хозяина, вне организма они могут сохраняться лишь некоторое время, не размножаясь. В организме они размножаются внеклеточно или внутриклеточно. Факультативно внутриклеточные паразиты лучше размножаются в цитоплазме или ядре клеток, но могут размножаться и вне клетки (менингококки, гонококки, микобактерии туберкулеза и др. ). Облигатно внутриклеточные паразиты размножаются только в клетках организмахозяина (риккетсии, хламидии, вирусы).

При антагонизме (конкуренции) происходит подавление жизнедеятельности одной популяции другой. Формы истребления могут быть вариабельными - от банального поглощения более мелких видов до выделения высокоспецифичных продуктов, токсичных для конкурента (бактериоцины, антибиотики, фитонциды, интерферон, органические и жирные кислоты и др. )

МИКРОФЛОРА ТЕЛА ЗДОРОВОГО ЧЕЛОВЕКА Организм человека в норме содержит сотни видов микроорганизмов; среди них доминируют бактерии. Вирусы и простейшие представлены значительно меньшим числом видов. Термин «нормальная микрофлора» объединяет микроорганизмы, более или менее часто выделяемые из организма здорового человека. Провести четкую границу между сапрофитами и патогенными микробами, входящими в состав нормальной микрофлоры, часто невозможно. Кровь и внутренние органы здорового человека и животных практически стерильны. Не содержат микробов и некоторые полости, соприкасающиеся с внешней средой - матка, мочевой пузырь. Быстро уничтожаются микробы в легких. Но в ротовой полости, в носу, в кишечнике, во влагалище имеется постоянная нормальная микрофлора, характерная для каждой области тела (аутохтонная).

При этом человек служит источником поступления в окружающую среду множества микроорганизмов. В течение внутриутробного периода организм развивается в стерильных условиях полости матки, и его первичное обсеменение происходит при прохождении через родовые пути и в первые сутки при контакте с окружающей средой. Затем в течение ряда лет после рождения формируется характерный для определенных биотопов его организма микробный «пейзаж» . Среди нормальной микрофлоры выделяют резидентную (постоянную) облигатную микрофлору и транзиторную (непостоянную) микрофлору, не способную к длительному существованию в организме.

Основные микробные биотопы Кожа На кожных покровах микроорганизмы подвержены действию бактерицидных факторов сального секрета, повышающих кислотность. В подобных условиях живут преимущественно Staphylococcus epidermidis, микрококки, сарцины, аэробные и анаэробные дифтероиды. Соблюдение элементарных правил гигиены может уменьшить число бактерий на 90%.

Дыхательная система В верхние дыхательные пути попадают пылевые частицы, нагружен-ные микроорганизмами, большая часть которых задерживается в носо- и ротоглотке. Здесь растут бактероиды, коринеморфные бактерии, гемофильные палочки, пептококки, лактобактерии, стафило-кокки, стрептококки, непатогенные нейссерии и др. Трахеи и бронхи обычно стерильны.

Мочеполовая система Микробный биоценоз органов мочеполовой системы более скудны. Верхние отделы мочевыводящих путей обычно стерильны; в нижних отделах доминируют. Staphylococcus epidermidis, негемолитические стрептококки, дифтероиды; часто выделяют грибы родов Candida. В наружных отделах доминируют Mycobacterium smegmatis. В микробиоценоз влагалища включены молочнокислые бактерии, энтерококки, стрептококки, стафилококки, коринебактерии, палочки Додерлайна.
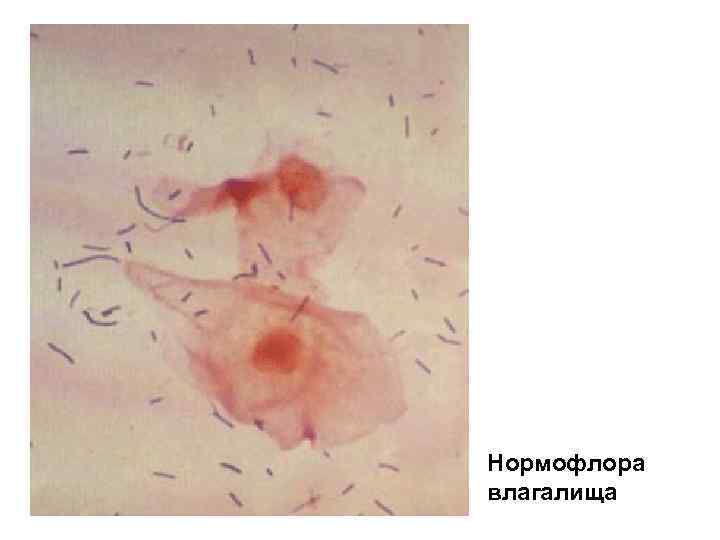
Нормофлора влагалища

Полость рта Ротовая полость является удобным местом для развития микроорганизмов. Влажность, обилие питательных веществ, оптимальная температура, слабо щелочная реакция среды являются благоприятными факторами для развития микроорганизмов. Поэтому микрофлора полости рта чрезвычайно обильна и разнообразна. Среди бактерий доминируют стрептококки, составляющие 30 -60% всей микрофлоры ротоглотки. Менее аэрируемые участки колонизируют анаэробы - актиномицеты, бактероиды, фузобактерии и вейлонеллы. В полости рта также обитают спирохеты, микоплазмы, грибы рода Candida и разнообразные простейшие.

Нормальная микрофлора ротовой полости может быть причиной воспалительных процессов и кариеса зубов, однако, при огромном количестве микробов в полости рта воспалительные процессы возникают сравнительно редко. Защитное значение имеют барьерная функция слизистой оболочки и эмали зубов, фагоцитоз.
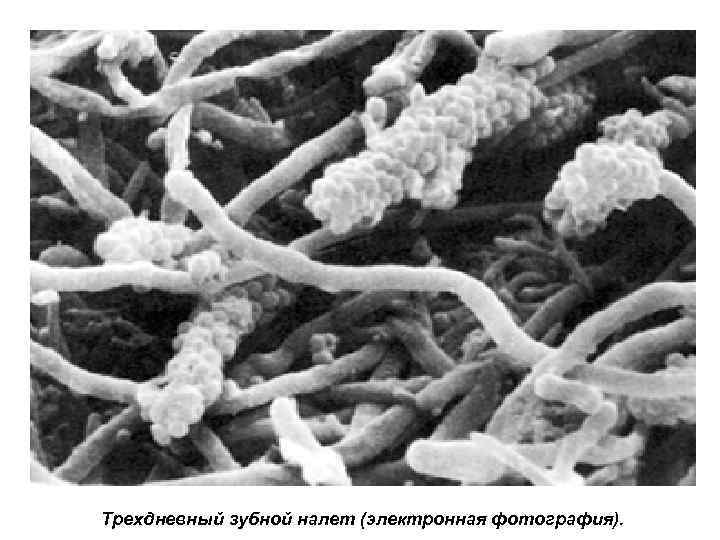
Трехдневный зубной налет (электронная фотография).

Желудочно-кишечный тракт (ЖКТ) Наиболее активно бактерии заселяют ЖКТ; при этом колонизация осуществляется «по этажам» . В желудке здорового человека микробов практически нет, что вызвано действием желудочного сока. Тем не менее отдельные виды (например, Helicobacter pylori) адаптировались к обитанию на слизистой оболочке желудка.
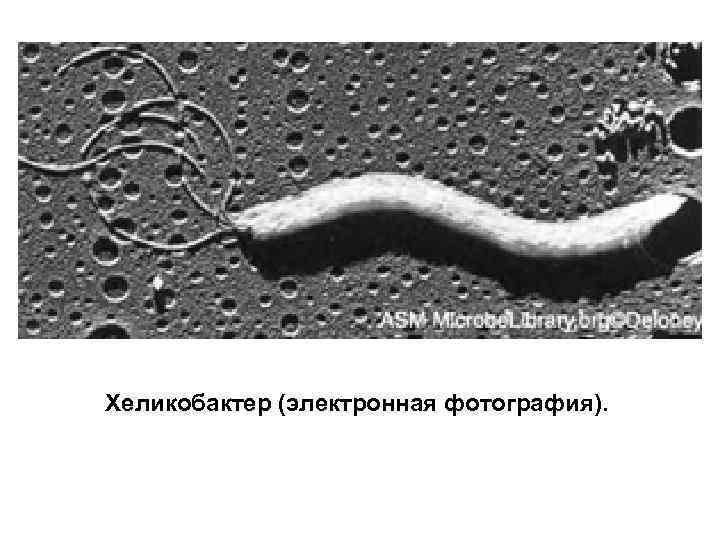
Хеликобактер (электронная фотография).

Верхние отделы тонкой кишки также относительно свободны от бактерий, что связано с неблагоприятным действием щелочного р. Н и пищеварительных ферментов. Тем не менее в этих отделах можно обнаружить кандиды, стрептококки и лактобациллы. Нижние отделы тонкой и, особенно, толстая кишка - огромный резервуар бактерий; их содержание может достигать 1012 в 1 г фекалий (30% сухой массы кала). Микрофлора кишечника представлена тремя основными группами. К 1 -й группе относятся грамположительные бесспоровые анаэробы - бифидобактерии и грамотрицательные бактероиды, составляющие 95% микробиоценоза.

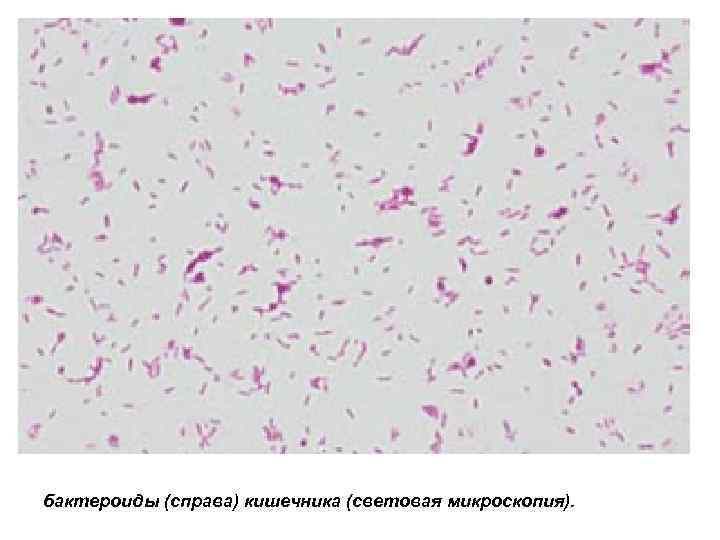
бактероиды (справа) кишечника (световая микроскопия).
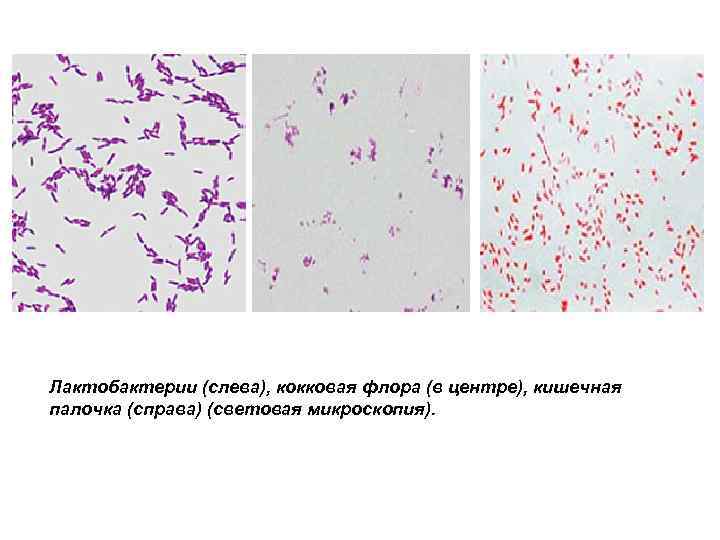
Лактобактерии (слева), кокковая флора (в центре), кишечная палочка (справа) (световая микроскопия).

Значение микрофлоры тела для человека 1. Барьер. Пристеночная микрофлора кишечника колонизирует слизистую оболочку в виде микроколоний, образуя своеобразную биологическую пленку. При этом бактерии препятствуют проникновению внутрь организма и вредных микробов, и продуктов их жизнедеятельности.

2. Защита. Нормальная микрофлора является одним из важнейших факторов естественной резистентности (устойчивости) организма, так как проявляет высоко антагонистическое действие по отношению к другим, в том числе патогенным бактериям, препятствуя их размножению в организме.

3. Метаболизм. Микрофлора, особенно толстого кишечника, участвует в процессах пищеварения, в том числе в обмене холестерина и желчных кислот. Важная роль микрофлоры заключается также в том, что она обеспечивает организм человека различными витаминами, которые синтезируются ее представителями (витамин В 1, В 2, В 6, В 12, К, никотиновая, пантотеновая, фолиевая кислоты и др. ) Эти витамины обеспечивают большую часть потребностей в них организма. Микрофлора регулирует водно-солевой обмен и газовый состав кишечника.

4. Детоксикация. Микроорганизмы ингибируют выделение токсина некоторыми микроорганизмами, принимают участие в детоксикации попадающих из внешней среды в организм ксенобиотиков (чужеродные вещества) и образующихся токсичных продуктов метаболизма путем их преобразования в нетоксичные продукты, разрушают концерогенные вещества.

5. Стимуляция иммунной системы. Микрофлора своими антигенными факторами стимулирует развитие лимфоидной ткани организма, образование антител и таким образом способствует поддержанию гомеостаза слизистых оболочек.


Инфекция. Однако представители нормальной микрофлоры не всегда приносят только пользу. При определенных условиях, в частности, при воздействии факторов, снижающих естественную резистентность, особенно в результате ионизирующего облучения, практически все представители нормальной микрофлоры, за исключением бифидобактерий, могут стать виновниками различных эндогенных инфекций, чаще всего гнойно-воспалительных заболеваний с различной локализацией: ангины, менингиты, циститы, отиты, нефриты, аппендициты, абсцессы, флегмоны и т. п.

Дисбактерио з (от греч. — «дис - - приставка, означающая "затруднение", "отклонение от нормы", "нарушение функции"» и «бактерия» ) — качественное изменение нормального видового состава бактерий (микробиоты) кишечника, или кожи.

Дисбактериоз. Состояние эубиоза динамического равновесия микрофлоры и организма человека может нарушаться под влиянием факторов окружающей среды: состава и качества пищи, курения и употребления алкоголя, нормальной перистальтики и своевременного опорожнения кишечника и мочевого пузыря, качества пережевывания пищи и даже характера трудовой деятельности (сидячий или иной), стрессовых воздействий, широкого и бесконтрольного применения антимикробных препаратов, лучевой и химиотерапии. В результате нарушается колонизационная резистентность. Аномально размножившиеся микроорганизмы продуцируют токсичные продукты метаболизма - индол, скатол, аммиак, сероводород. Такое состояние, развивающееся в результате утраты нормальных функций микрофлоры, называется дисбактериозом или дисбиозом (дисбиоценоз).

Качественные и количественные нарушения в кишечной микрофлоре возникают в результате разных причин. Основными являются следующие: • заболевания органов пищеварения; • перенесенные острые кишечные инфекции и глистные инвазии, в том числе иерсиниоз, лямблиоз, описторхоз, клонорхоз и др. ; • длительный прием некоторых лекарственных препаратов (например, антибиотиков); • неполноценные диеты, приводящие к развитию гнилостных и бродильных процессов и другим расстройствам процессов пищеварения и всасывания; • декомпенсированные заболевания внутренних органов и систем.

При дисбактериозе происходят изменения количественного соотношения и состава нормальной микрофлоры организма, главным образом его кишечника, при котором происходит уменьшение количества или исчезновение обычно составляющих ее микроорганизмов и появление в большом количестве редко встречающихся или несвойственных ей микробов, а также изменение сферы их обитания. Наиболее тяжелые формы дисбактериозов - стафилококковый сепсис, системный кандидоз и псевдомембранозный колит; среди всех форм доминируют поражения микрофлоры кишечника.

Стадии дисбактериоза I стадия дисбактериоза характеризуется умеренным уменьшением численности облигатных бактерий в полости кишечника. Патогенная микрофлора, как правило, развита незначительно, а признаки расстройства функции кишечника (симптомы болезни) отсутствуют.

II стадия дисбактериоза характеризуется критическим снижением численности бифидобактерий и актобацилл кишечника (облигатная флора). При этом отмечается стремительное развитие популяции патогенных бактерий. На этой стадии дисбактериоза появляются первые признаки нарушения работы кишечника: понос (зеленоватого цвета), боли в животе, метеоризм.

III стадия дисбактериоза характеризуется воспалительным поражением стенок кишечника под влиянием патогенов. На этом этапе дисбактериоза понос приобретает стойкий хронический характер, а в каловых массах определяются частички непереваренной пищи. У детей может появиться отставание в развитии.

IV стадия дисбактериоза, представляет собой стадию предшествующую острой кишечной инфекции. На этом этапе дисбактериоза облигатная флора кишечника присутствует в очень малых количествах. Основное количество микробов приходится на условно патогенных и патогенных бактерий и грибов. На этой стадии дисбактериоза возникает общее истощение организма, анемия, авитаминоз


Диагностика дисбактериоза Предложены следующие методы диагностики дисбактериоза кишечника: • бактериологический анализ (определение состава фекальной микрофлоры, отражающий микробный состав лишь нижних отделов кишечника — наиболее доступный метод, однако недостаточно точный); • биохимический экспресс-метод определения ферментативной активности надосадочной фракции фекалий;

• высоковольтный электрофорез на бумаге с целью обнаружения бета-аспартилглицина, бета-аспартиллизина, бета-аланина, 5 аминовалериановой и гаммааминомасляной кислот и др. ; • ионная хроматография; • газожидкостная хроматография; • исследование микрофлоры в биоптате тощей кишки, полученном в ходе эндоскопического исследования, — наиболее точный метод, который, однако, из-за технических сложностей не может применяться достаточно широко.

Лабораторная диагностика дисбактериоза чаще всего базируется на микробиологическом анализе кала. Микробиологическими критериями служат снижение бифидолактобактерий, снижение или увеличение эшерихий, появление штаммов с измененными свойствами, повышение количества кокков, обнаружение условнопатогенных грамотрицательных палочек, а также грибов и клостридий более 103 КОЕ/л. В анализах возможны различные сочетания указанных сдвигов.

Для лечения дисбактериоза исполь-зуют длительное время препараты, содержащие представителей нормальной микрофлоры, например, бифидобактерии (бифидумбактерин), лактобактерии (лактобактерин), бифидобактерии и кишечную палочку (бификол) и др. Кроме того необходимо соблюдать определенную диету с преобладанием в рационе молочно-растительной пищи, а также психотерапию с настроем на добрые чувства.

Лечение дисбактериоза В лечении дисбактериоза используются препараты из группы пробиотиков: Наринэ-Форте, Линекс, Хилак форте, Бифидумбактерин, а также препараты из группы пребиотиков, например Дюфалак, Лактусан, Бактисубтил. Также дополнительно для устранения симптомов мальабсорбции и диспепсии - нарушений пищеварения, используют замещающие желудочные и(или) кишечные пищеварительные ферменты препараты - Фестал, Дигестал, Панкреатин, Панзинорм-Форте.

Иногда одновременно с антибактериальной терапией антибиотиками (особенно пенициллинами) или сульфаниламидами назначают антигрибковые антибиотики (напр. Нистатин) с целью профилактики дисбактериоза, а также лече-ния кожного дисбактериоза, особенно при длительной антибактериальной терапии. Вскармливание грудным молоком защищает детей от дисбактериоза.
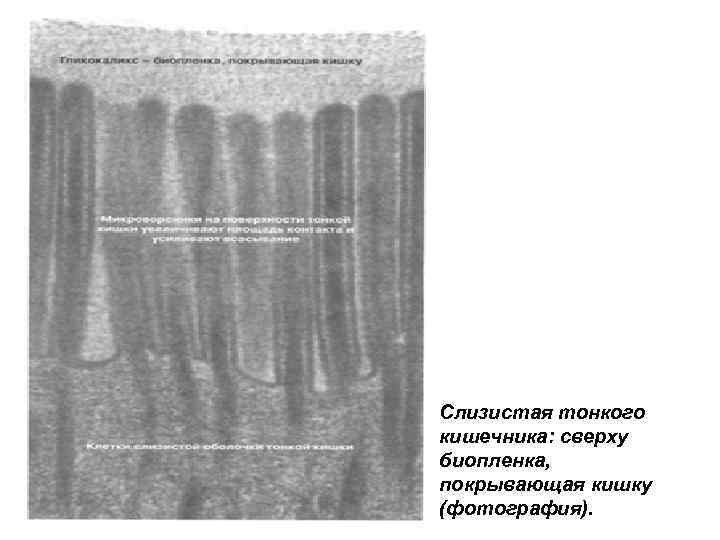
Слизистая тонкого кишечника: сверху биопленка, покрывающая кишку (фотография).

Различают: • Постоянная (резидентная, индигенная или автохтонная) Бывает облигатная – бифидобактерии, лактобактерии, пептострептобактерии, КП и. т. д. Факультативная – стафилококки, стрептококки, клебсиеллы, клостридии , некоторые грибы- их меньше. • Транзиторная ( непостоянная или аллохтонная) Организм человека и нормальная микрофлора- эндоэкологическая система. Количество МО организма взрослого человека около 1014.

Микрофлора организма человека. В организме человека более 500 видов МО 7 Сообщество- микробиоценоз. Эубиоз- в состоянии равновесия. Большинство комменсалы. Заселяют различные органы и системы








Галитоз (Halitosis) дурной запах изо рта. Причиной временного галитоза может быть недавно съеденная пища с сильным запахом (например, лук или чеснок), или прием некоторых лекарственных веществ, таких как паральдегид. Кроме того, галитоз может возникать при дыхании человека через рот, периодонтальной болезни, а также при наличии инфекционных заболеваний носа, горла и легких (особенно в случае бронхоэктатической болезни). Запор, нарушение процесса пищеварения, а также некоторые заболевания печени также могут вносить свой вклад в появление неприятного запаха изо рта человека.

Халитоз - неприятный запах изо рта, который постоянно ощущается в выдыхаемом воздухе или независим от акта дыхания. Указанные жалобы обусловлены метаболической активностью бактерий ротовой полости - выделение сероводорода, метилмеркаптана и др. соединений, которые возникают при бактериальном распаде белков, содержащихся в остатках пищи и отмирающих тканях (десневые каналы, содержимое секрета слюнных желёз). Разложению бактерий препятствует слюна (благодаря наличию в ней кислорода). Поэтому болезни слюнных желёз, голод, дыхание через нос (что постоянно наблюдается в детской практике), лекарства, предменструальный период и множество других причин, вызывающих сухость во рту, в определённой мере способствуют развитию халитоз.


Классификация халитоза: Экзогенные причины: • Табакокурение, алкоголь, пища содержащая ароматические вещества (лук, чеснок, маринад, соусы и пр). • Некоторые отравления( синильная кислота и пр. )

• Эндогенные: Заболевания зубов, дёсен. • Патология носоглотки. • Заболевания желудочно-кишечного тракта (грыжа пищеводного отверстия диафрагмы, ГЭРБ, дивертикулы пищевода, последствия стволовой ваготомии и пр. ) • Опухоли желудка (в стадии распада). • Кишечная непроходимость. • Патология лёгких ( бронхоэктазы, гнойный бронхит и пр.

Эндотоксикоз: Венозная или почечная недостаточность, диабетический ацидоз.


Рекомендации ученых для профилактики халитоза: • Тщательный уход за полостью рта если причины стоматологические (полоскатель для рта, зубная паста, зубной порошок). • 2 раза в день чистить поверхность языка специальными щетками; • использовать антибактериальную зубную паст Эти простые меры профилактики показали высокую эффективность в борьбе с запахом изо рта.

По мнению учёных к халитозу приводит триметиламиноурия–редкая ферментопатия, при дефиците которой нарушается метаболизм холина в толстой кишке (переход холина в триметиламин). Последний выделяется из организма при дыхании, с потом, мочой придавая им своеобразный рыбный запах. Таким образом, проблема ранней установки причины данного явления, его своевременного устранения, являются актуальной проблемой, как у стоматологов, так и у интернистов.





По мнению учёных к халитозу приводит триметиламиноурия–редкая ферментопатия, при дефиците которой нарушается метаболизм холина в толстой кишке (переход холина в триметиламин). Последний выделяется из организма при дыхании, с потом, мочой придавая им своеобразный рыбный запах. Таким образом, проблема ранней установки причины данного явления, его своевременного устранения, являются актуальной проблемой, как у стоматологов, так и у интернистов.

Галитоз — медицинский термин, означающий неприятный запах изо рта у людей и животных. Наиболее часто употребляем в стоматологической области, однако, причины галитоза зачастую кроются не только в патологических развитиях в самой ротовой полости, но и в патологиях внутренних органов.

Причины Галитоз вызывают: • стоматологические заболевания (кариес зубов и его осложнения, а также заболевание слизистых оболочек полости рта, болезни десен, некачественные протезы и ортодонтические конструкции); • плохая или неправильная гигиена полости рта, в результате чего в полости рта скапливается большое количество бактерий, разлагаются остатки пищи. • заболевания верхних дыхательных путей и глотки (например хронический насморк, тонзиллит, фарингит); • системные заболевания внутренних органов (желудка, разных желёз, нарушенное пищеварение)

Часто неприятный запах изо рта появляется у человека в послеобеденное время, если человек ничего не ел на завтрак и/или обед и запахи полупереваренной пищи поднимаются вверх по пустому пищеводу. Это не является патологией, необходимо пообедать и воспользоваться ароматическими жвачками или конфетами с запахом мяты, лимона, клубники и т. п. , выпить напиток.

Антибио тики (от др. -греч. ἀντί — anti — против, βίος — bios — жизнь) — вещества природного или полусинтетического происхождения, подавляющие рост живых клеток, чаще всего прокариотических или простейших.

Классификация Огромное разнообразие антибиотиков и видов их воздействия на организм человека явилось причиной классифицирования и разделения антибиотиков на группы. По характеру воздействия на бактериальную клетку антибиотики можно разделить на три группы: • бактериостатические (бактерии живы, но не в состоянии размножаться), • бактерициды (бактерии умертвляются, но физически продолжают присутствовать в среде), • бактериолитические (бактерии умертвляются, и бактериальные клеточные стенки разрушаются).

Классификация по химической структуре, которую широко используют в медицинской среде, состоит из следующих групп: • Бета-лактамные антибиотики, делящиеся на две подгруппы: Пенициллины — вырабатываются колониями плесневого грибка Penicillium; Цефалоспорины — обладают схожей структурой с пенициллинами. Используются по отношению к пенициллинустойчивым бактериям.

• Макролиды — антибиотики со сложной циклической структурой. Действие — бактериостатическое. • Тетрациклины — используются для лечения инфекций дыхательных и мочевыводящих путей, лечения тяжелых инфекций типа сибирской язвы, туляремии, бруцеллёза. Действие — бактериостатическое. • Аминогликозиды — обладают высокой токсичностью. Используются для лечения тяжелых инфекций типа заражения крови или перитонито

• Левомицетины — Использование ограничено по причине повышенной опасности серьезных осложнений — поражении костного мозга, вырабатывающего клетки крови. Действие — бактерицидное. • Гликопептидные антибиотики нарушают синтез клеточной стенки бактерий. Оказывают бактерицидное действие, однако в отношении энтерококков, некоторых стрептококков и стафилококков действуют бактериостатически.

• Линкозамиды оказывают бактериостатическое действие, которое обусловлено ингибированием синтеза белка рибосомами. В высоких концентрациях в отношении высокочувствительных микроорганизмов могут проявлять бактерицидный эффект. • Противогрибковые — разрушают мембрану клеток грибков и вызывают их гибель. Действие — литическое. Постепенно вытесняются высокоэффективными синтетическими противогрибковыми препаратами.

Действие антибиотиков Антибиотики в отличие от антисептиков обладают антибактериальной активностью не только при наружном применении, но и в биологических средах организма при их системном (перорально, внутримышечно, внутривенно, ректально, вагинально и др. ) применении.

Механизмы биологического действия 1. Нарушение синтеза клеточной стенки посредством ингибирования синтеза пептидогликана (пенициллин, цефалоспорин, монобактамы), образования димеров и их переноса к растущим цепям пептидогликана (ванкомицин, флавомицин) или синтеза хитина (никкомицин, туникамицин). Антибиотики, действующие по подобному механизму обладают бактерицидным действием, не убивают покоящиеся клетки и клетки, лишенные клеточной стенки.

2. Нарушение функционирования мембран: нарушение целостности мембраны, образование ионных каналов, связывание ионов в комплексы, растворимые в липидах, и их транспортировка. Подобным образом действуют нистатин, грамицидины, полимиксины.

3. Подавление синтеза нуклеиновых кислот: связывание с ДНК и препятствование продвижению РНКполимеразы (актидин), сшивание цепей ДНК, что вызывает невозможность её расплетания (рубомицин), ингибирование ферментов. Нарушение синтеза пуринов и пиримидинов (азасерин, саркомицин).

4. Нарушение синтеза пуринов и пиримидинов (азасерин, саркомицин). 5. Нарушение синтеза белка: ингибирование активации и переноса аминокислот, функций рибосом (стрептомицин, тетрациклин, пуромицин). 6. Ингибирование работы дыхательных ферментов (антимицины, олигомицины, Ауровертин

Антибиотикорезистентность Под антибиотикорезистентностью понимают способность микроорганизма противостоять действию антибиотика. Антибиотикорезистентность возникает спонтанно вследствие мутаций и под воздействием антибиотика закрепляется в популя-ции. Сам по себе антибиотик не является причиной появления резистентности.

Механизмы резистентности • У микроорганизма может отсутствовать структура на которую действует антибиотик (например бактерии рода микоплазма (лат. Mycoplasma) нечувствительны к пенициллину, так как не имеют клеточной стенки); • Микроорганизм непроницаем для антибиотика (большинство грамотрицательных бактерий невосприимчивы к пенициллину G, поскольку клеточная стенка защищена дополнительной мембраной);

• Микроорганизм в состоянии переводить антибиотик в неактивную форму (многие стафилококки (лат. Staphylococcus) содержат фермент β-лактамазу, который разрушает βлактамовое кольцо большинства пенициллинов) • Вследствие генных мутаций, обмен веществ микроорганизма может быть изменён таким образом, что блокируемые антибиотиком реакции больше не являются критичными для жизнедеятельности организма; • Микроорганизм в состоянии выкачивать антибиотик из клетки

Для определения чувствительности микробов к антибиотикам существует ряд методов: • метод последовательных разведений в жидкой питательной среде или питательном агаре, • метод диффузии в агар (метод дисков, насыщенных антибиотиками) и ускоренные методы.

Метод дисков прост, широко используется, но дает лишь качественный ответ. Более надежным и точным количественным методом является метод последовательных разведений антибиотиков в питательной среде в стандартных условиях опыта.
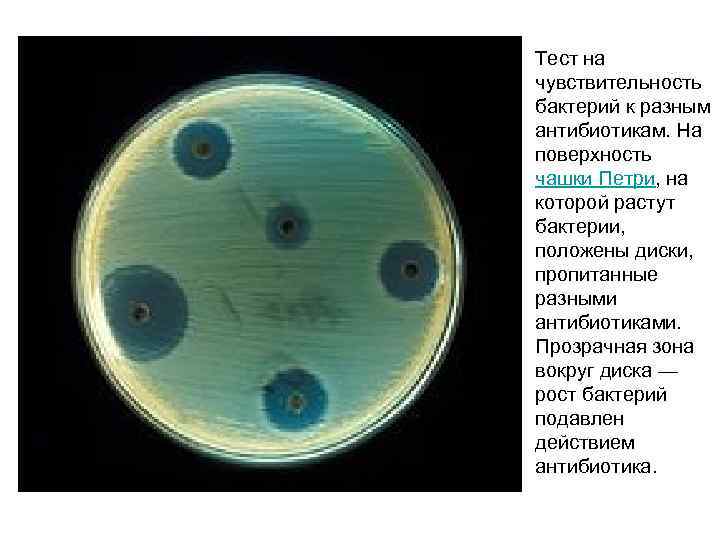
Тест на чувствительность бактерий к разным антибиотикам. На поверхность чашки Петри, на которой растут бактерии, положены диски, пропитанные разными антибиотиками. Прозрачная зона вокруг диска — рост бактерий подавлен действием антибиотика.
2Нормальная микрофлора организма человека. ОЗ..ppt