биоэнергетика-6.ppt
- Количество слайдов: 95

Основы биоэнергетики

Главная энергетическая реакция в организме человека 2 Н 2 + О 2 = 2 Н 2 О+

- Расщепление жиров, углеводов и белков происходит через многочисленные цепочки реакций и в конце всех этих превращений образуется одно и то же вещество – ацетилкоэнзим А. Данное соединение представляет собой активную форму уксусной кислоты (ацетата). - Далее ацетил-Ко. А вступает в цикл трикарбоновых кислот (цикл Кребса). В ходе реакций выделяется углекислый газ (СО 2) и водород.
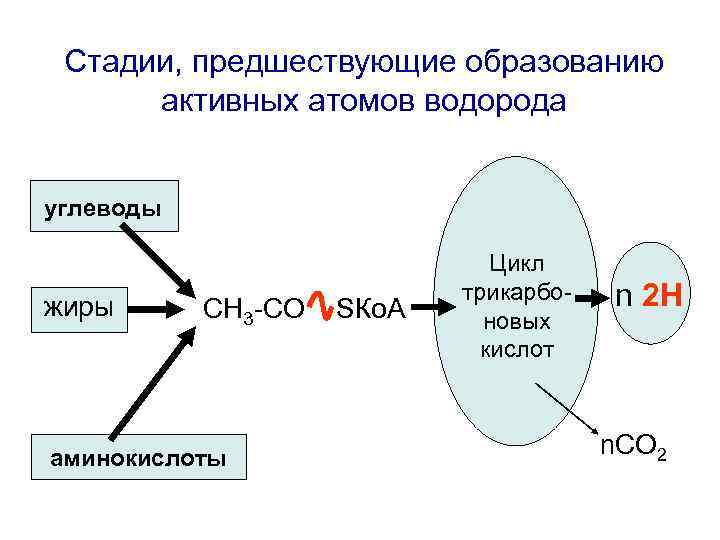
Стадии, предшествующие образованию активных атомов водорода углеводы жиры СН 3 -СО аминокислоты SКо. А Цикл трикарбоновых кислот n 2 Н n. СО 2
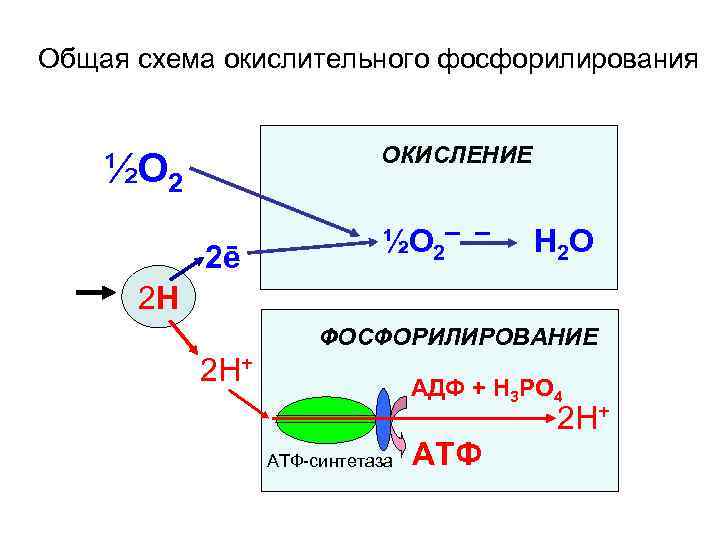
Общая схема окислительного фосфорилирования ОКИСЛЕНИЕ ½О 2 2ē ½О 2– – Н 2 О 2 Н ФОСФОРИЛИРОВАНИЕ 2 Н+ АДФ + Н 3 РО 4 2 Н+ АТФ-синтетаза АТФ

• Весь процесс, упрощенно, можно представить как горение водорода в кислороде: 2 Н 2 + О 2 = 2 Н 2 О. Данная реакция протекает со взрывом, то есть, сопровождается выделением огромной энергии. Однако, в организме человека такая реакция протекает при температуре около 37 о С. Энергия реакции выделяется не в виде тепла, а аккумулируется в молекулы макроэргических соединений. • Наиболее важной такой молекулой для всех живых организмов является аденозин-трифосфорная кислота (АТФ). Она состоит из азотистого основания (аденина), рибозы и трех остатков фосфорной кислоты.
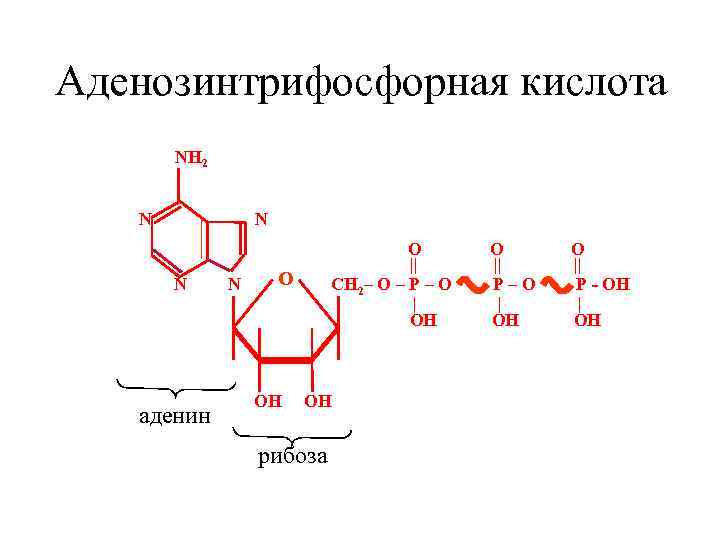
Аденозинтрифосфорная кислота NH 2 N N N аденин N О || CH 2– O – P – O | ОН ОН рибоза О || P–O | ОН О || P - ОН | ОН

Энергия в клетках может запасаться и другой молекулой – креатином. При этом, креатин взаимодействует с избытком АТФ. Остаток фосфата с макроэргической связью присоединяется к креатину и образуется макроэргическое соединение – фосфокреатин. Реакция обратима, при недостатке в клетке АТФ равновесие реакции сдвигается в сторону синтеза АТФ. При этом количество фосфокреатина падает, а креатина увеличивается. Таким образом, в клетке концентрация АТФ сохраняется на постоянном уровне, несмотря на прерывистый характер расходования энергии. Следует заметить, что фосфокреатин не может использоваться в реакциях взамен АТФ. Вначале из фосфокреатина образуется АТФ, а затем АТФ расходуется клеткой на энергозависимые реакции.
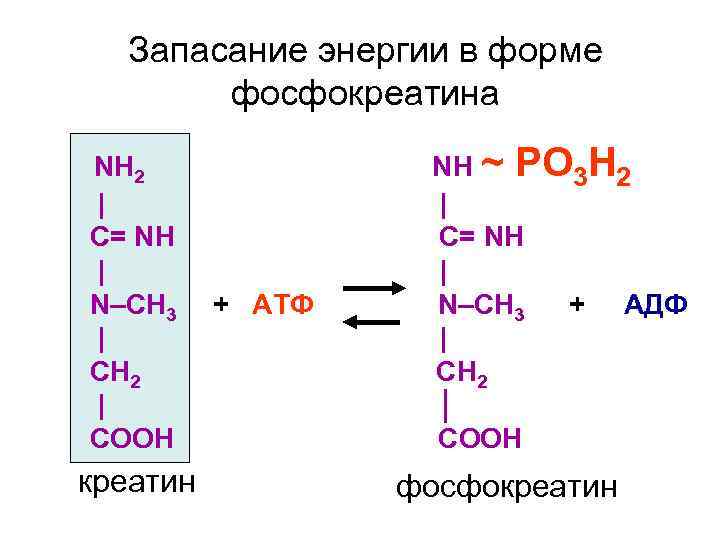
Запасание энергии в форме фосфокреатина NH 2 | C= NH | N–CH 3 | CH 2 | COOH креатин + АТФ NH ~ РО 3 Н 2 | C= NH | N–CH 3 + АДФ | CH 2 COOH фосфокреатин

• Взаимодействие водорода с кислородом (окислительновосстановительная реакция) протекает во внутренней мембране митохондрий клеток. • Катализируют эту реакцию ферменты, образуя при этом дыхательную цепочку.
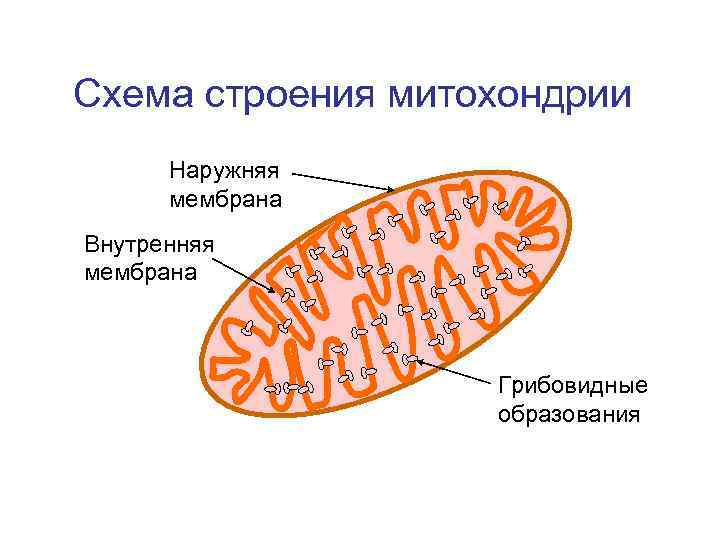
Схема строения митохондрии Наружняя мембрана Внутренняя мембрана Грибовидные образования
Глазами инженера конструкция энергетической машины в клетке
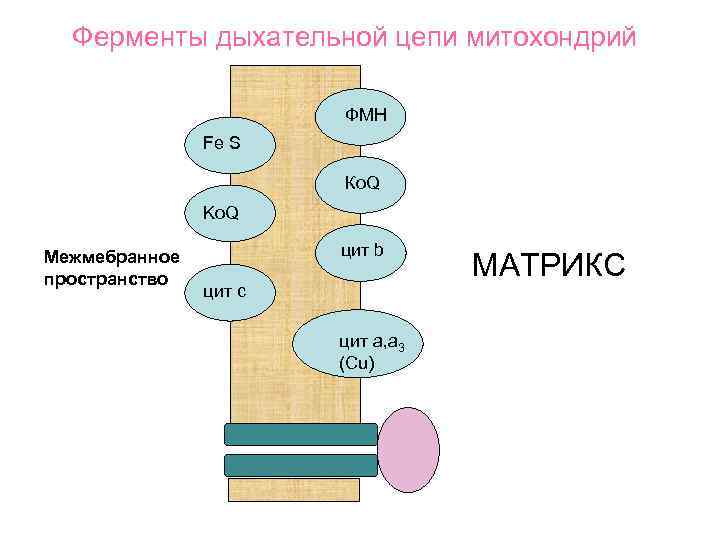
Ферменты дыхательной цепи митохондрий ФМН Fe S Ко. Q Ko. Q Межмебранное пространство цит b цит с цит а, а 3 (Сu) МАТРИКС
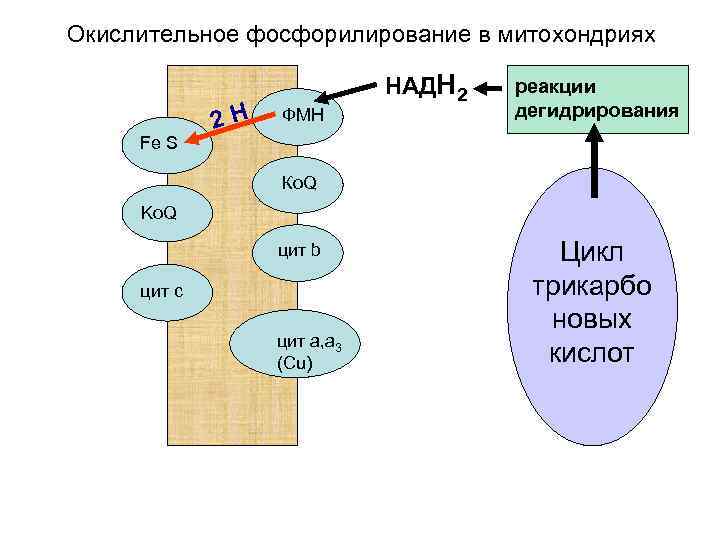
Окислительное фосфорилирование в митохондриях Fe S 2 Н ФМН НАДН 2 реакции дегидрирования Ко. Q Ko. Q цит b цит с цит а, а 3 (Сu) Цикл трикарбо новых кислот

• Атомы водорода принимаются первым ферментным комплексом со стороны матрикса митохондрий и, далее, посылаются к наружной стороне мембраны. В этом месте атомы водорода распадаются на протоны и электроны. Протоны выталкиваются наружу, а электроны направляются в сторону матрикса к следующему комплексу дыхательных ферментов.
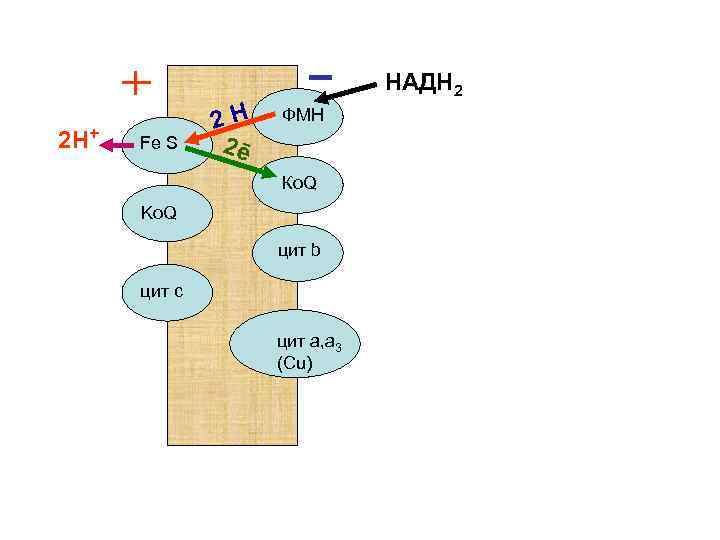
НАДН 2 2 Н+ Fe S 2 Н 2ē ФМН Ко. Q Ko. Q цит b цит с цит а, а 3 (Сu)
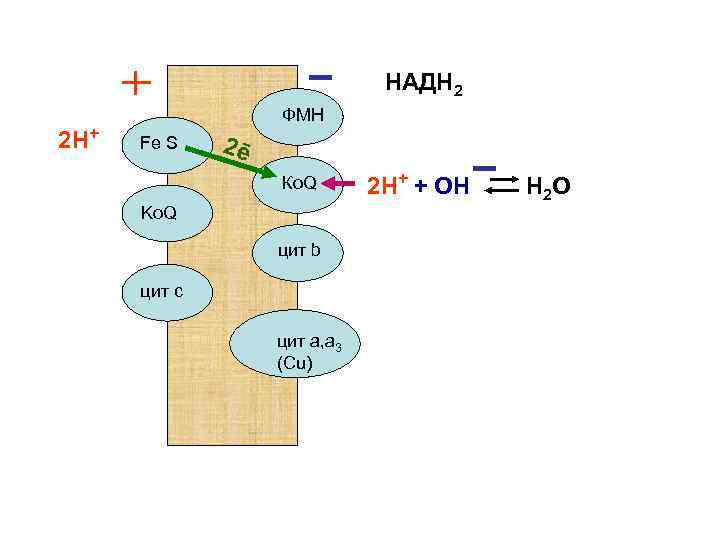
НАДН 2 2 Н+ ФМН Fe S 2ē Ко. Q Ko. Q цит b цит с цит а, а 3 (Сu) 2 Н+ + ОН Н 2 О

На этой стадии электроны присоединяются к протонам воды матрикса. Образуются атомы водорода, которые посылаются ферментами дыхательной цепи наружу. Ко. Q участвует в расщеплении атома водорода на протоны и электроны. Протоны выталкиваются в межмембранное пространство, а электроны вновь посылаются к внутренней стороне мембраны митохондрий – к цитохрому b.
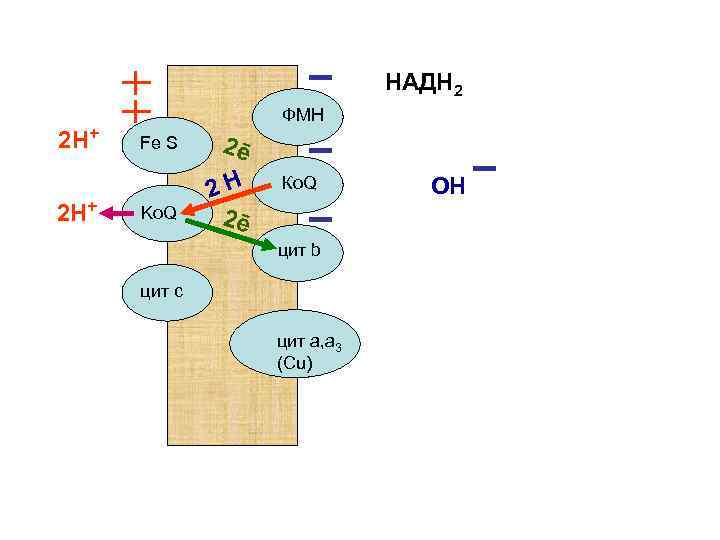
НАДН 2 2 Н+ ФМН Fe S Ko. Q 2ē 2 Н 2ē Ко. Q цит b цит с цит а, а 3 (Сu) ОН

Цитохром b соединяет электроны с протонами воды матрикса. Образующийся водород направляется наружу мембраны. Там с помощью цитохрома С атомы Н распадаются на протоны и электроны.
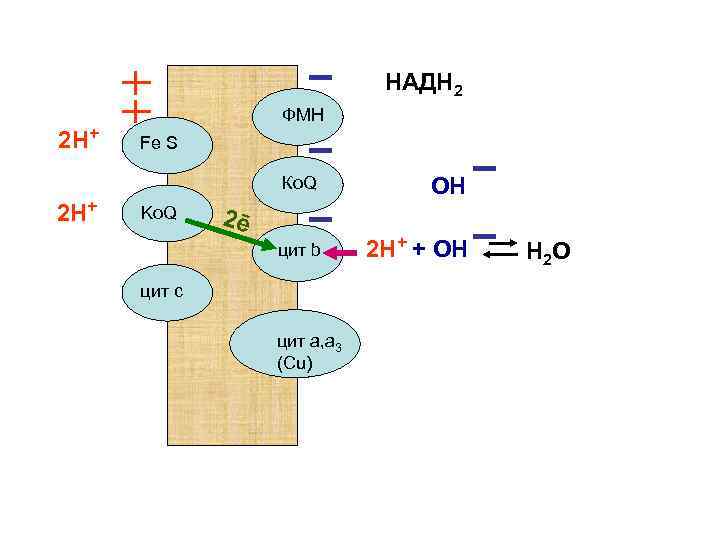
НАДН 2 2 Н+ ФМН Fe S Ко. Q 2 Н+ цит b Ko. Q ОН 2 Н+ + ОН 2ē цит с цит а, а 3 (Сu) Н 2 О
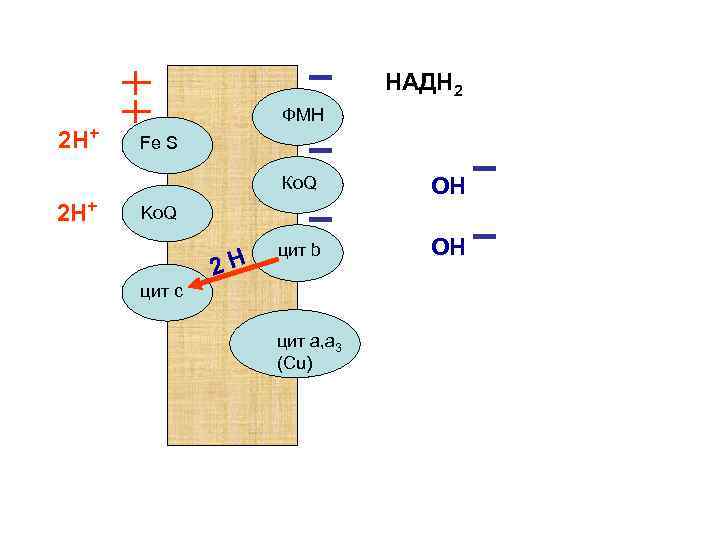
НАДН 2 2 Н+ ФМН Fe S Ко. Q 2 Н+ ОН цит b ОН Ko. Q цит с 2 Н цит а, а 3 (Сu)

Протоны выталкиваются наружу, а электроны посылаются к цитохромоксидазе (цит а. а 3) – заключительному ферменту дыхательной цепи митохондрий.
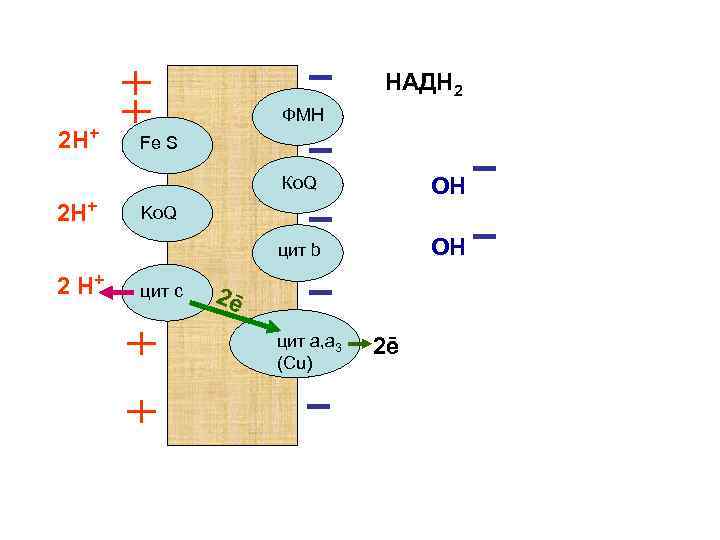
НАДН 2 2 Н+ ФМН Fe S Ко. Q цит b 2 Н+ 2 Н+ ОН ОН Ko. Q цит с 2ē цит а, а 3 (Сu) 2ē

Цитохромоксидаза взаимодействует с кислородом Этому процессу помогают атомы меди, входящие в в состав цитохромоксидазы.
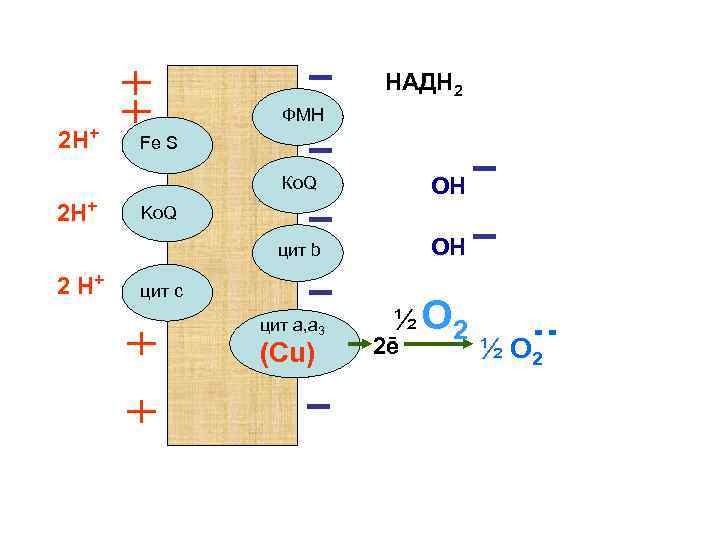
НАДН 2 2 Н+ ФМН Fe S Ко. Q цит b 2 Н+ 2 Н+ ОН ОН цит а, а 3 ½ О 2 Ko. Q цит с (Сu) 2ē ½ О 2

Каждый атом молекулы кислорода (½ О 2) получает по 2 электрона. В результате образуются атомы активного кислорода, которые взаимодействуя с протонами водного пространства матрикса, образуют воду.
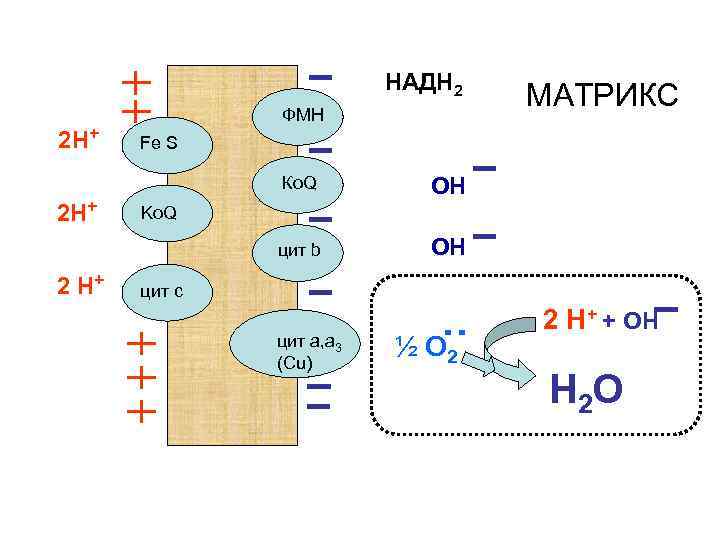
НАДН 2 2 Н+ ФМН Fe S Ко. Q 2 Н+ ОН цит b 2 Н+ МАТРИКС ОН Ko. Q цит с цит а, а 3 (Сu) ½ О 2 2 Н+ + ОН Н 2 О

В результате окислительно-восстановительных реакций на внешней стороне мембраны накапливаются положительно заряженные частицы – протоны (Н+), а с внутренней сто- ионы. роны ОН Возникает мембранный потенциал, который может достигать значения 0, 2 вольт.
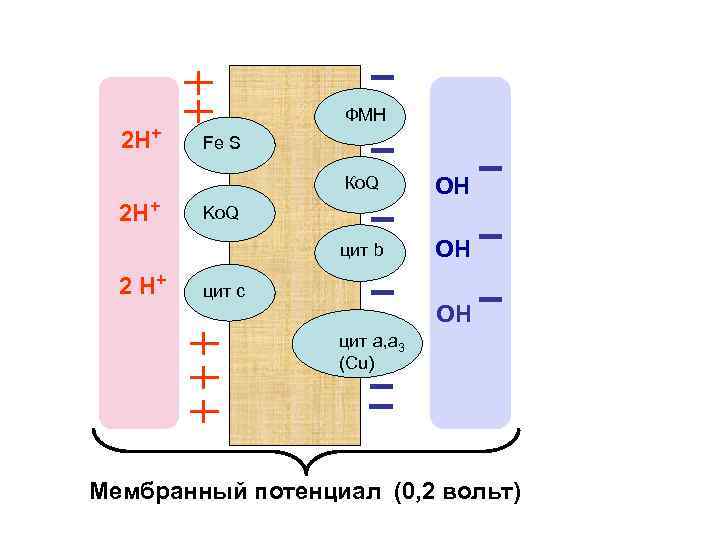
2 Н+ ФМН Fe S Ко. Q цит b 2 Н+ 2 Н+ ОН ОН Ko. Q цит с ОН цит а, а 3 (Сu) Мембранный потенциал (0, 2 вольт)

Энергия мембранного потенциала должна превращаться в энергию макроэргических связей АТФ. Важную роль в этой трансформации энергии играют белки протонного канала и АТФ-синтетаза. На электронно-микроскопических снимках ученые обнаружили грибовидные структуры, которые оказались ферментами, превращающие энергию мембранного потенциала в энергию АТФ.
Фотография грибовидных образований во внутренней мембране митохондрии грибовидные образования
Фотография грибовидных образований во внутренней мембране митохондрии Внутренняя мембрана митохондрии Грибовидные образования
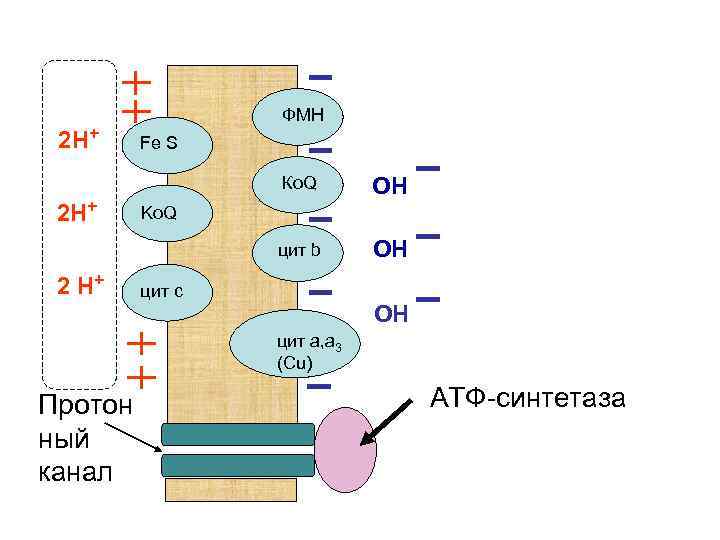
2 Н+ ФМН Fe S Ко. Q цит b 2 Н+ 2 Н+ ОН ОН Ko. Q цит с ОН цит а, а 3 (Сu) Протон ный канал АТФ-синтетаза
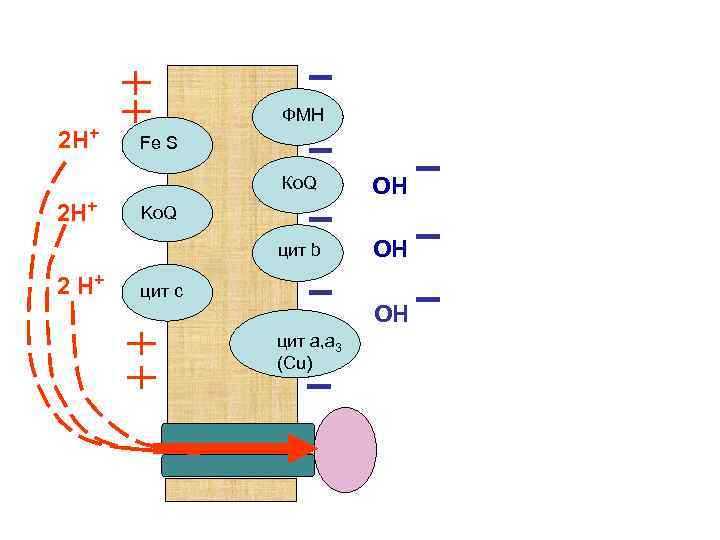
2 Н+ ФМН Fe S Ко. Q цит b 2 Н+ 2 Н+ ОН ОН Ko. Q цит с ОН цит а, а 3 (Сu)

При увеличении концентрации АДФ происходит открытие протонного канала, через которые начинают поступать протоны внутрь митохондрии. Проходя через активный центр АТФ-синтетазы протоны катализируют превращение АДФ в АТФ. В результате концентрация протонов снаружи мембраны начинает падать, что приводит к снижению мембранного потенциала. В свою очередь, это служит толчком для активации ферментов дыхательной цепи митохондрий. Происходит накопление новой порции протонов снаружи внутренней мембраны митохондрий.
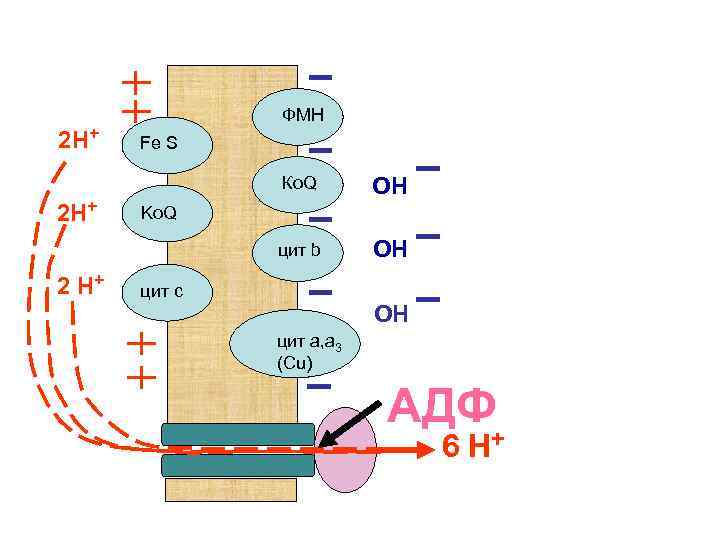
2 Н+ ФМН Fe S Ко. Q цит b 2 Н+ 2 Н+ ОН ОН Ko. Q цит с ОН цит а, а 3 (Сu) АДФ 6 Н+
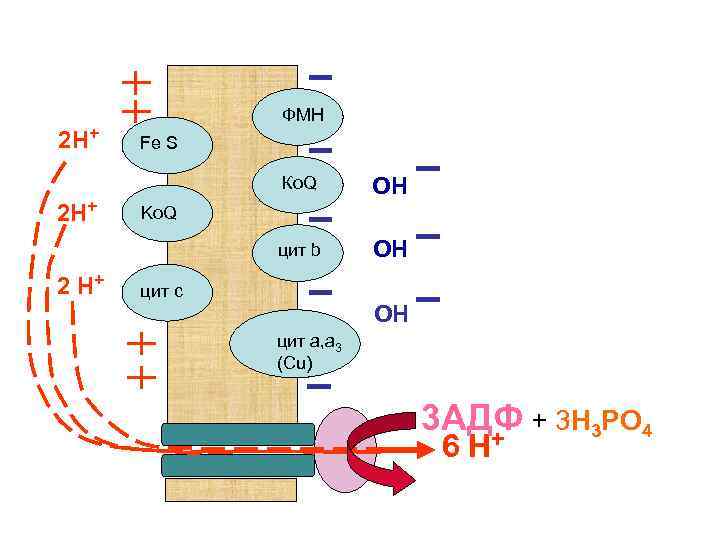
2 Н+ ФМН Fe S Ко. Q цит b 2 Н+ 2 Н+ ОН ОН Ko. Q цит с ОН цит а, а 3 (Сu) 3 АДФ + 3 Н 3 РО 4 + 6 Н
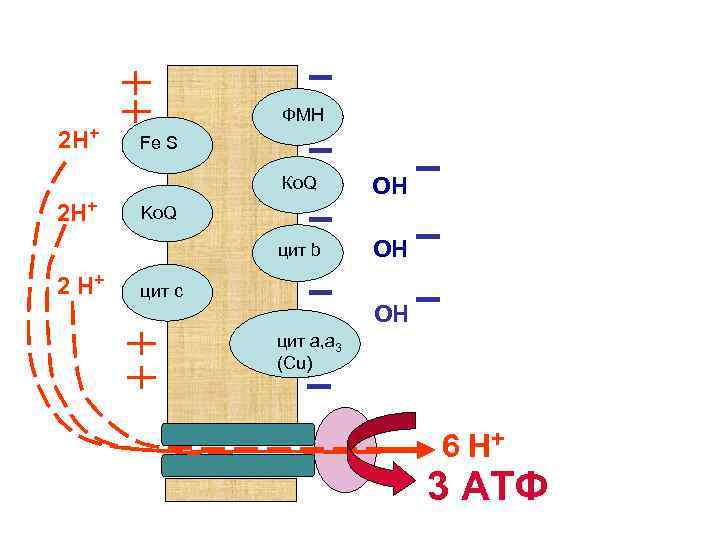
2 Н+ ФМН Fe S Ко. Q цит b 2 Н+ 2 Н+ ОН ОН Ko. Q цит с ОН цит а, а 3 (Сu) 6 Н+ 3 АТФ

Строение АТФ-синтетазы и протонного канала
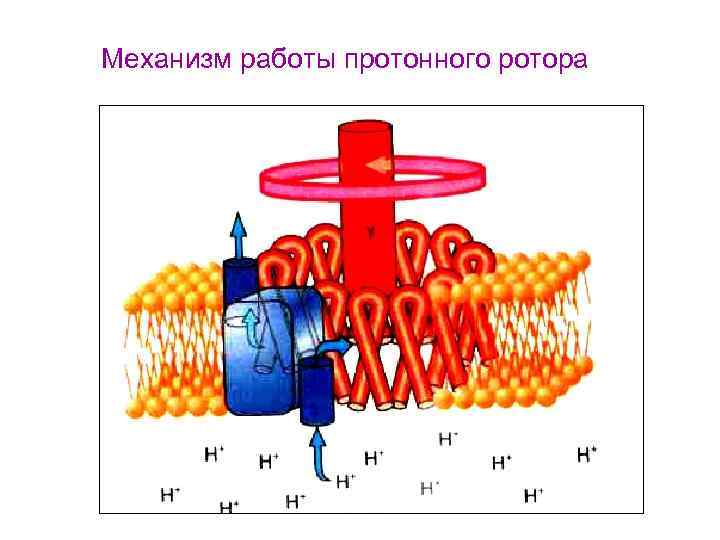
Механизм работы протонного ротора
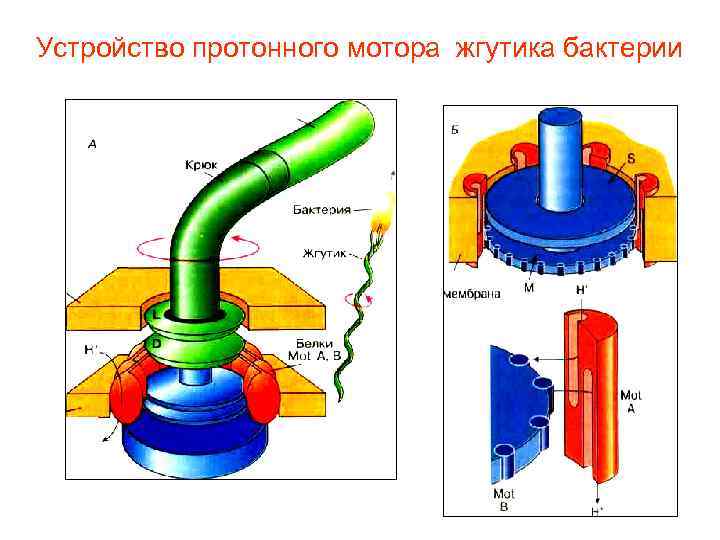
Устройство протонного мотора жгутика бактерии

Понятие о дыхательном контроле

• Скорость движения электронов по дыхательной цепи к кислороду зависит от двух сил, первая – ускоряет движение, а вторая – останавливает перенос электронов. • Известно, что кислород является одним из сильнейших окислителей. При этом молекула О 2 способна принимать 4 электрона, а один атом кислорода, соответственно, присоединяет 2 электрона. • Поэтому кислород является мощной первой силой, заставляющей двигаться электроны по дыхательной цепи. Митохондрии в этом состоянии активно поглощают (расходуют) кислород, в результате у человека возникает одышка.
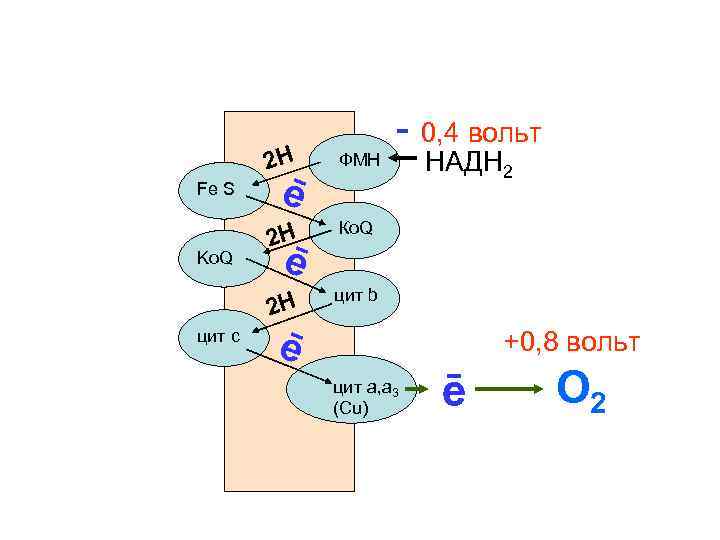
2 Н Ko. Q цит с 2 Н Ко. Q 2 Н Fe S ФМН - 0, 4 вольт цит b ē ē НАДН 2 ē +0, 8 вольт цит а, а 3 (Сu) ē О 2

• Однако, по мере накопления протонов снаружи мембраны возникает мембранный потенциал со знаком (+) на наружной поверхности и (–) внутри митохондрий. • Согласно приведенной схемы видно, что электроны, двигаясь поперек мембраны испытывают влияние этого потенциала. • Электронам приходится преодолевать электрическое поле, которое останавливает их движение.
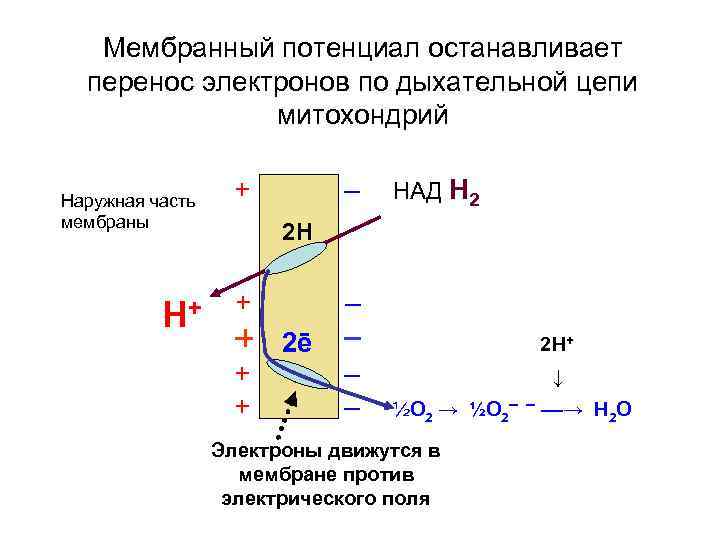
Мембранный потенциал останавливает перенос электронов по дыхательной цепи митохондрий Наружная часть мембраны Н+ + – НАД Н 2 2 Н + + + – 2ē 2 Н+ – – ↓ ½О 2 → ½О 2– Электроны движутся в мембране против электрического поля – ––→ Н 2 О

• Регулятором интенсивности работы дыхательных ферментов и скорости поглощения митохондриями кислорода является аденозиндифосфорная кислота (АДФ). При повышении ее количества внутри клеток происходит активирование АТФ-синтетазы. • Протонный канал начинает пропускать протоны внутрь митохондрий, концентрация протонов снаружи митохондриальной мембраны падает, снижается и величина мембранного потенциала. Низкое значение мембранного потенциала способствует переносу электронов на кислород, расход кислорода при этом возрастает. Таким образом, АДФ осуществляет, так называемый, “дыхательный контроль ”.
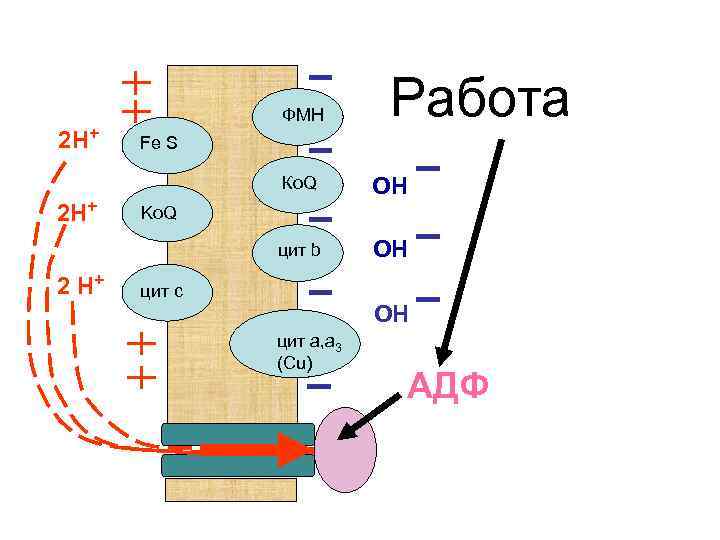
2 Н+ ФМН Работа Fe S Ко. Q цит b 2 Н+ 2 Н+ ОН ОН Ko. Q цит с ОН цит а, а 3 (Сu) АДФ
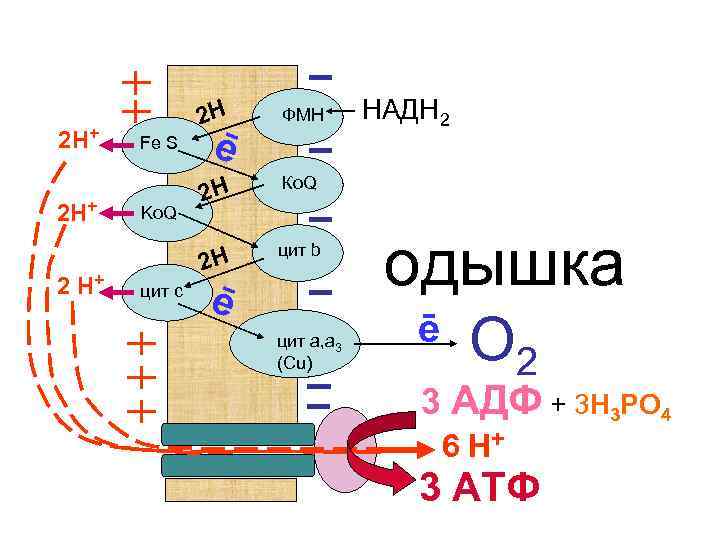
2 Н+ 2 Н Ko. Q цит с 2 Н цит b НАДН 2 Ко. Q 2 Н Fe S ФМН ē ē цит а, а 3 (Сu) одышка ē О 2 3 АДФ + 3 Н 3 РО 4 6 Н+ 3 АТФ
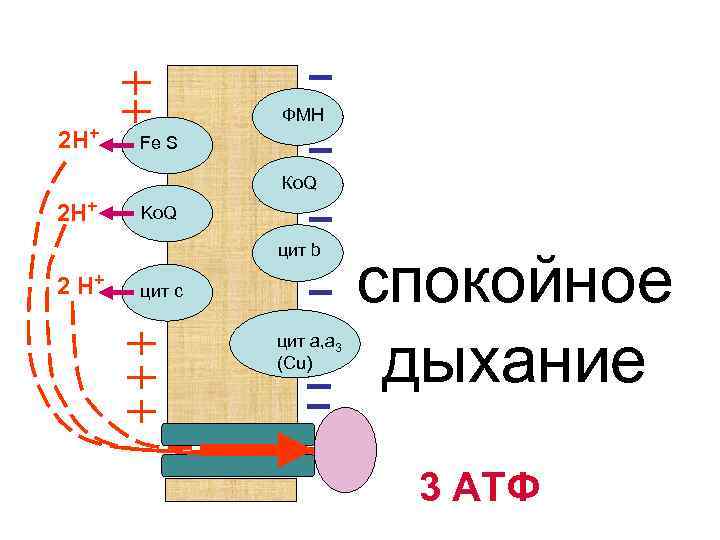
2 Н+ ФМН Fe S Ко. Q 2 Н+ Ko. Q цит b 2 Н+ цит с цит а, а 3 (Сu) спокойное дыхание 3 АТФ

Перенос энергии в клетке

Учитывая значительные размеры внутриклеточного пространства (по сравнению с размерами молекул) возникает вопрос – как энергетический материал так быстро доставляется на место, минуя при этом массу внутриклеточных препятствий – мембранные образования? Существует 2 механизма доставки энергии на расстояние. Первый – с помощью энергии мембранного потенциала и второй – с помощью фосфокреатина.
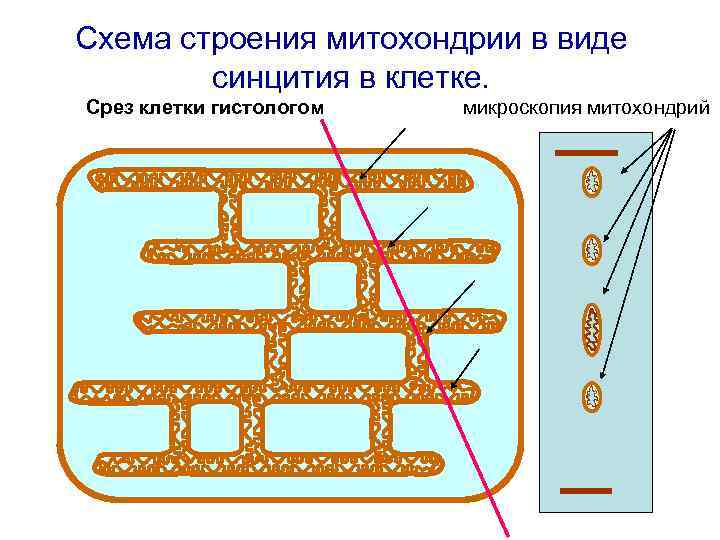
Схема строения митохондрии в виде синцития в клетке. Срез клетки гистологом микроскопия митохондрий

Миокард левого желудочка сердца
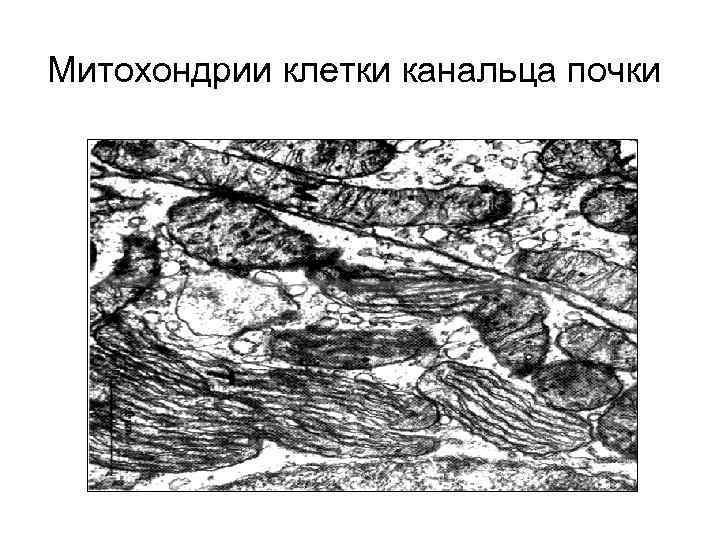
Митохондрии клетки канальца почки
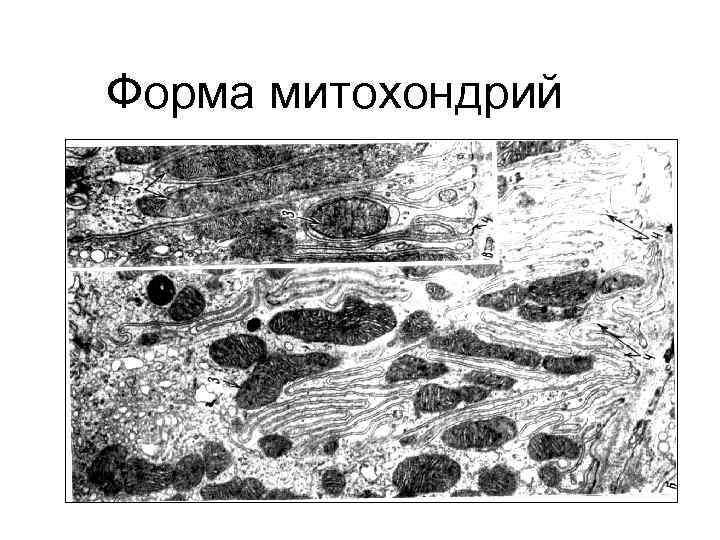
Форма митохондрий
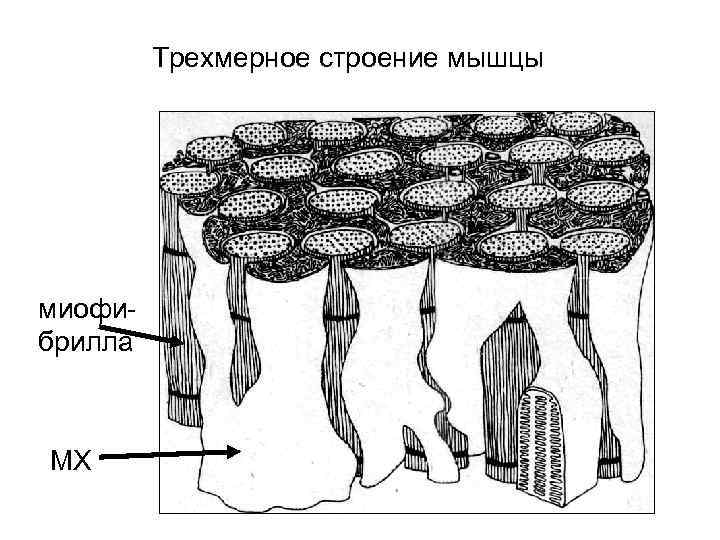
Трехмерное строение мышцы миофибрилла МХ

Реконструкция послойных срезов митохондрии клетки печени
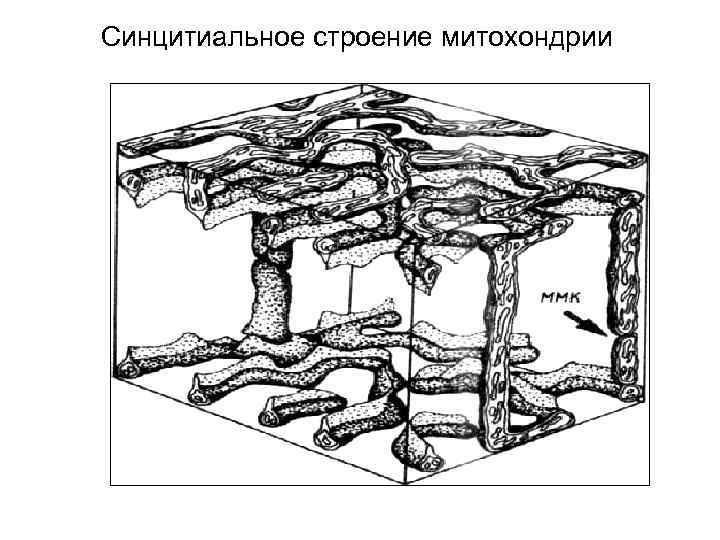
Синцитиальное строение митохондрии

На одной из сторон клетки участок митохондрии лучше снабжается кислородом и субстратами окисления. Возникший мембранный потенциал мгновенно распространяется по всей митохондрии. После этого синтез АТФ может осуществляться в любой точке цитоплазмы клетки за счет энергии мембранного потенциала.
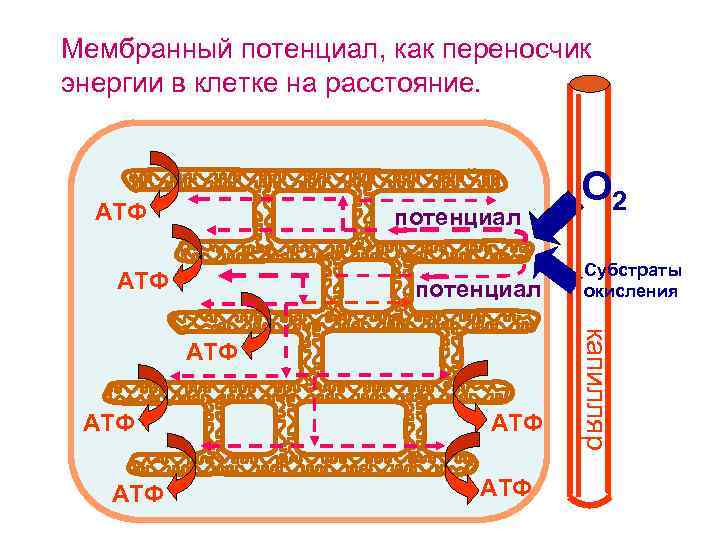
Мембранный потенциал, как переносчик энергии в клетке на расстояние. АТФ потенциал АТФ АТФ Субстраты окисления капилляр АТФ О 2

Перенос энергии в клетке с помощью фосфокреатина (ФКР) АДФ АТФ Потребитель энергии ФКР КР КР АТФ ФКР АДФ Синтез АТФ в митохондрии

Понятие о разобщении дыхания от фосфорилирования
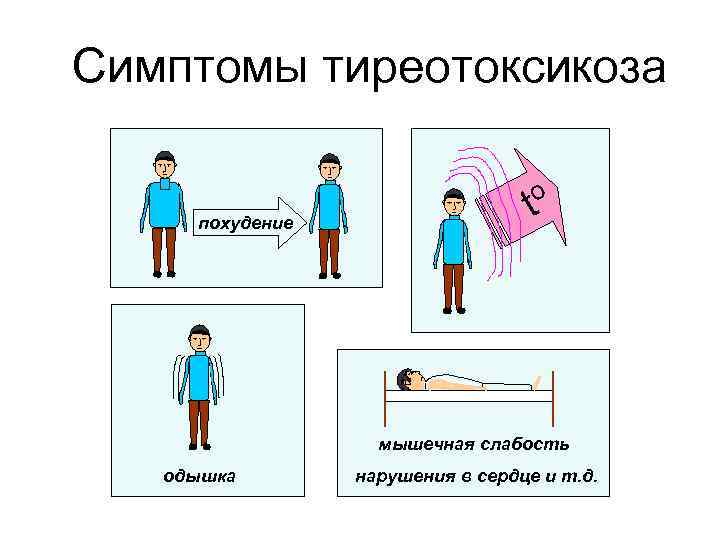
Симптомы тиреотоксикоза o похудение t мышечная слабость одышка нарушения в сердце и т. д.
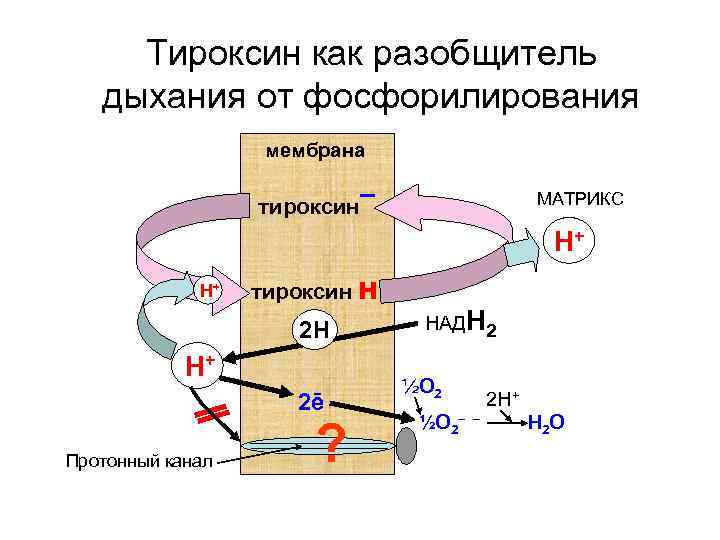
Тироксин как разобщитель дыхания от фосфорилирования мембрана тироксин – МАТРИКС Н+ Н+ тироксин Н 2 Н 2 Н Н+ 2ē Протонный канал ? НАДН 2 ½О 2– 2 Н+ – Н 2 О
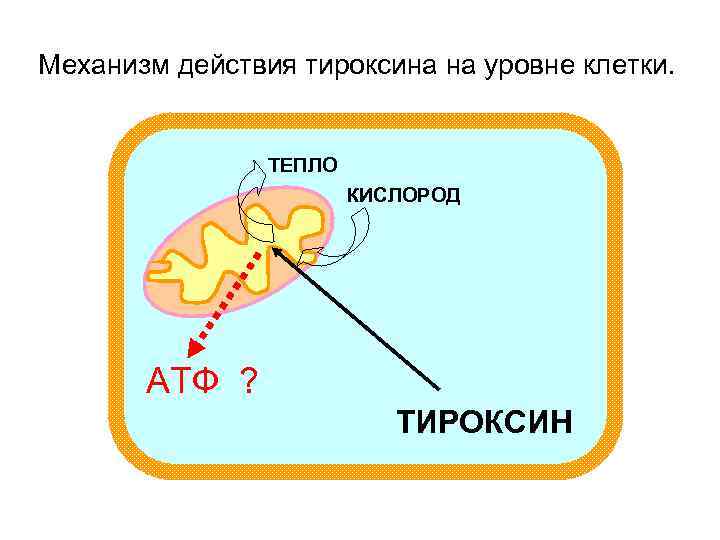
Механизм действия тироксина на уровне клетки. ТЕПЛО КИСЛОРОД АТФ ? ТИРОКСИН
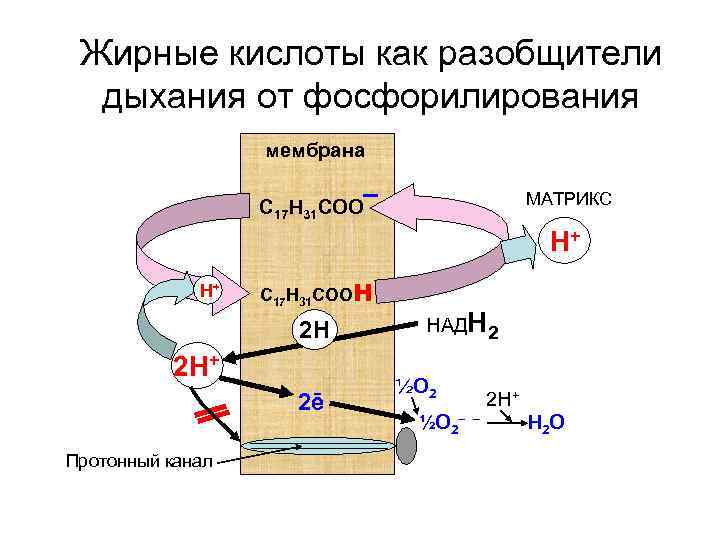
Жирные кислоты как разобщители дыхания от фосфорилирования мембрана С 17 Н 31 СОО – МАТРИКС Н+ Н+ С 17 Н 31 СООН 2 Н 2 Н 2 Н+ 2ē Протонный канал НАДН 2 ½О 2– 2 Н+ – Н 2 О

Локализация «бурого жира» у ребенка.

Полярографический метод измерения показателей дыхания и фосфорилирования в изолированных митохондриях
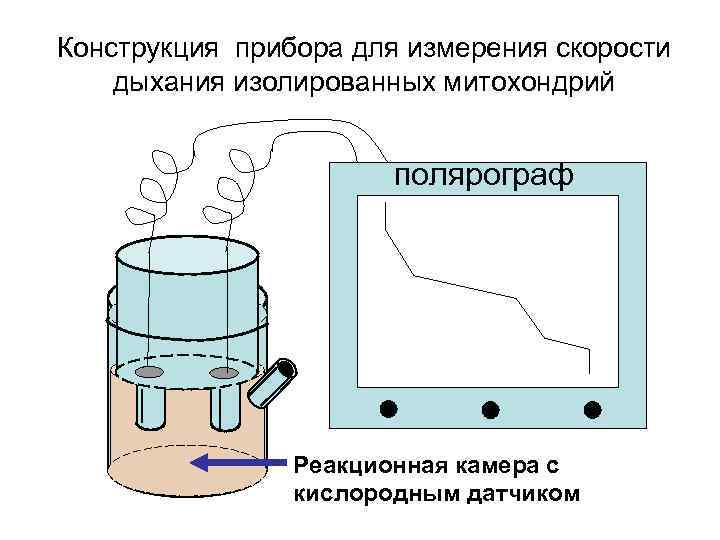
Конструкция прибора для измерения скорости дыхания изолированных митохондрий полярограф Реакционная камера с кислородным датчиком

Полярограммы представляют собой графические изображения динамики убыли кислорода из реакционной среды. На оси ординат показана концен-трация кислорода, которая снижается во время поглощения митохондриями кис-лорода (на графике уменьшается кон-центрация кислорода сверху вниз). По оси абсцисс представлено время, в течение которого происходят окисли-тельновосстановительные реакции.
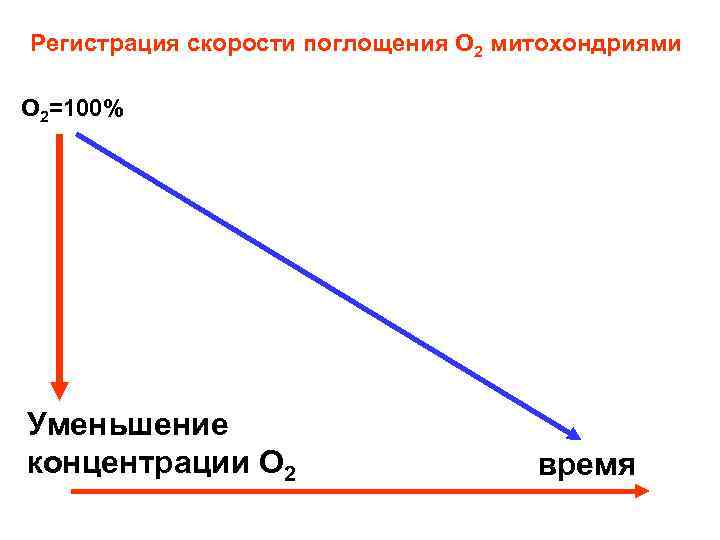
Регистрация скорости поглощения О 2 митохондриями О 2=100% Уменьшение концентрации О 2 время

В начале каждой записи демонстрируется содержание кислорода до добавки в инкубационную среду митохондрий.

Регистрация скорости поглощения О 2 митохондриями О 2=100% запись поглощения О 2 Уменьшение концентрации О 2 время

Регистрация скорости поглощения О 2 митохондриями О 2=100% митохондрии Уменьшение концентрации О 2 время

Субстратами окисления для митохондрий являются атомы водорода, присоединенные к коферменту НАД или ФАД. Субстратами окисления могут также служить различные вещества, способные отдавать атомы водорода на коферменты НАД или ФАД с помощью соответствующих дегидрогеназ.

Регистрация скорости поглощения О 2 митохондриями О 2=100% Митохондрии НАДН 2 (ФАДН 2) (яблочная кислота) Уменьшение концентрации О 2 время

Например, яблочная кислота подвергается дегидрированию с помощью малатдегидрогеназы (дегидрогеназы яблочной кислоты). На полярограмме процесс накопления НАДН 2 в этом случае не приводится. Донорами водорода могут служить промежуточные продукты цикла Кребса, молочная кислота, аскорбиновая кислота и др.

При добавлении НАДН 2, ФАДН 2 или субстратов окисления к митохондриям скорость окисления этих веществ остается невысокой, а следовательно, скорость поглощения митохондриями кислорода небольшая.

Регистрация скорости поглощения О 2 митохондриями О 2=100% Митохондрии НАДН 2 (ФАДН 2) (яблочная кислота) Уменьшение концентрации О 2 время

Скорость дыхания митохондрий резко возрастает при добавлении АДФ.
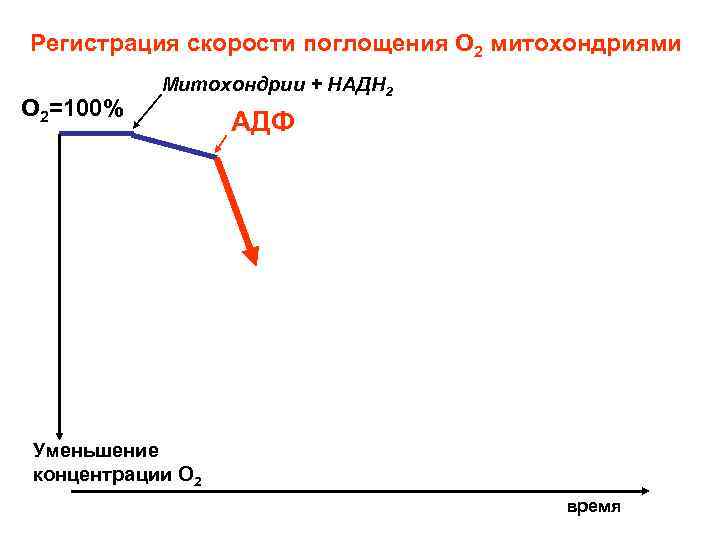
Регистрация скорости поглощения О 2 митохондриями О 2=100% Митохондрии + НАДН 2 АДФ Уменьшение концентрации О 2 время

При этом открывается протонный канал, ускоряется движение протонов внутрь митохондрий – в матрикс. Результатом перемещения протонов через активный центр АТФ-синтетазы митохондрий является синтез АТФ из АДФ и Н 3 РО 4.
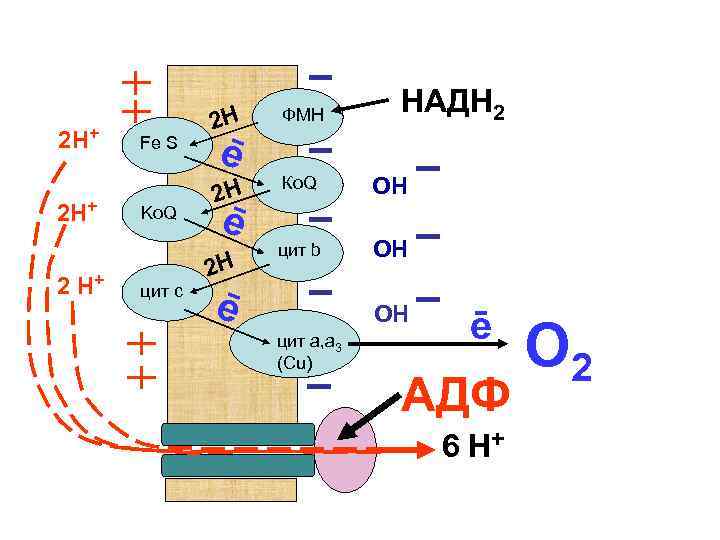
2 Н+ 2 Н+ Fe S Ko. Q цит с НАДН 2 2 Н ФМН 2 Н Ко. Q ОН цит b ОН ē ē 2 Н ē ОН цит а, а 3 (Сu) ē АДФ 6 Н+ О 2
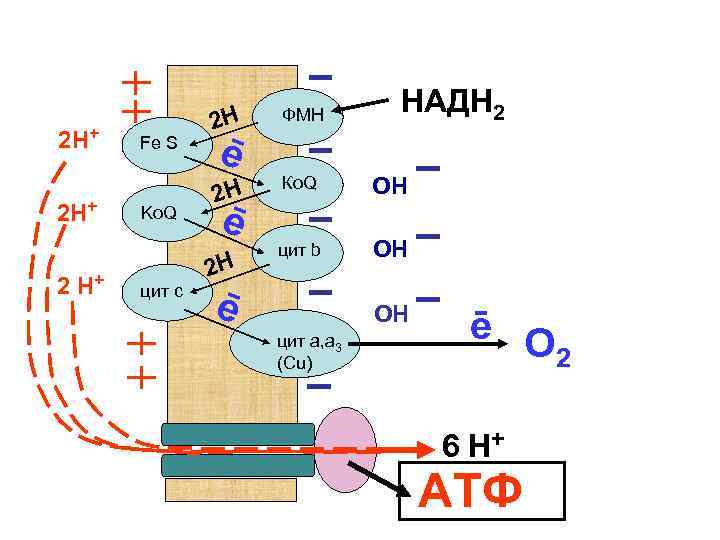
2 Н+ 2 Н+ Fe S Ko. Q цит с НАДН 2 2 Н ФМН 2 Н Ко. Q ОН цит b ОН ē ē 2 Н ē ОН цит а, а 3 (Сu) ē О 2 6 Н+ АТФ
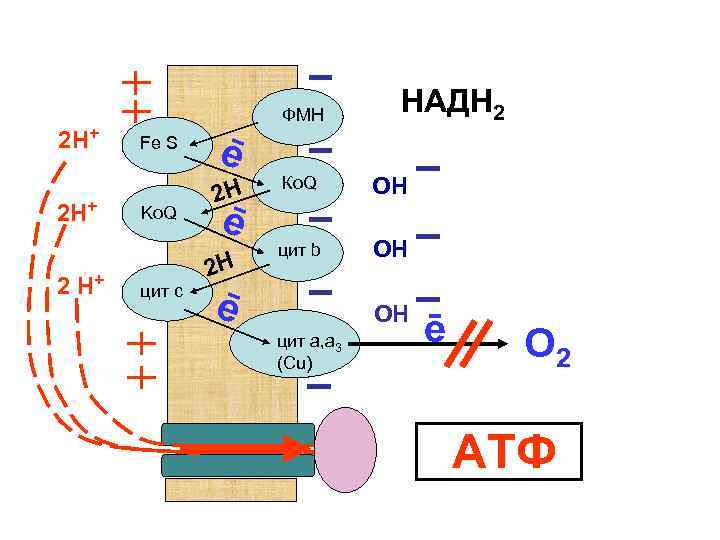
2 Н+ 2 Н+ ФМН Fe S Ko. Q цит с НАДН 2 ē 2 Н Ко. Q ОН цит b ОН ē 2 Н ē ОН цит а, а 3 (Сu) ē О 2 АТФ

Дыхание митохондрий затем замедляется, поскольку концентрация АДФ падает, а количество АТФ возрастает
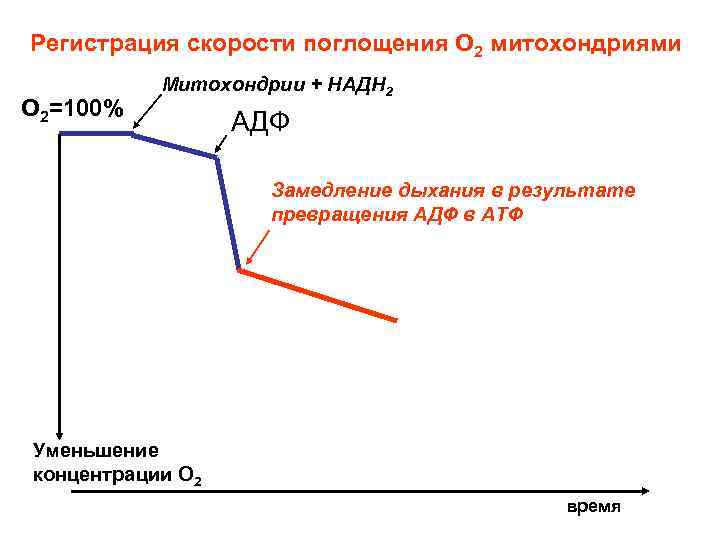
Регистрация скорости поглощения О 2 митохондриями О 2=100% Митохондрии + НАДН 2 АДФ Замедление дыхания в результате превращения АДФ в АТФ Уменьшение концентрации О 2 время

Добавки АТФ не вызывают ускорения дыхания, поскольку протонный канал открывает только АДФ.
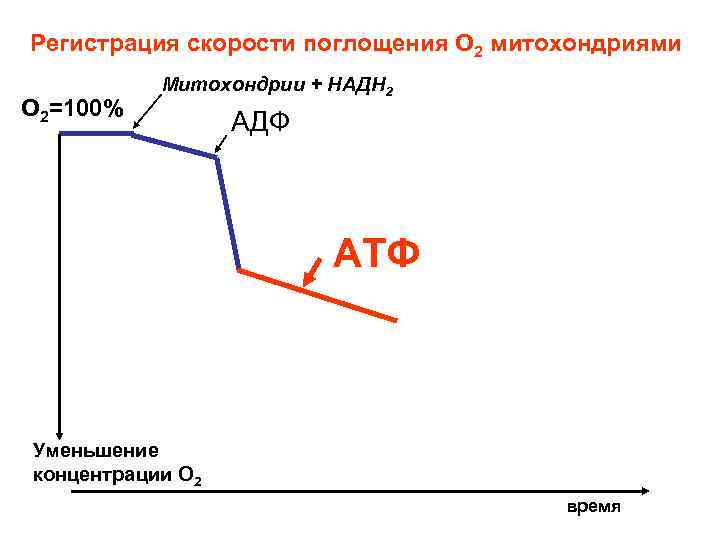
Регистрация скорости поглощения О 2 митохондриями О 2=100% Митохондрии + НАДН 2 АДФ АТФ Уменьшение концентрации О 2 время

Добавки АДФ вновь усиливают интенсивность поглощения кислорода митохондриями.
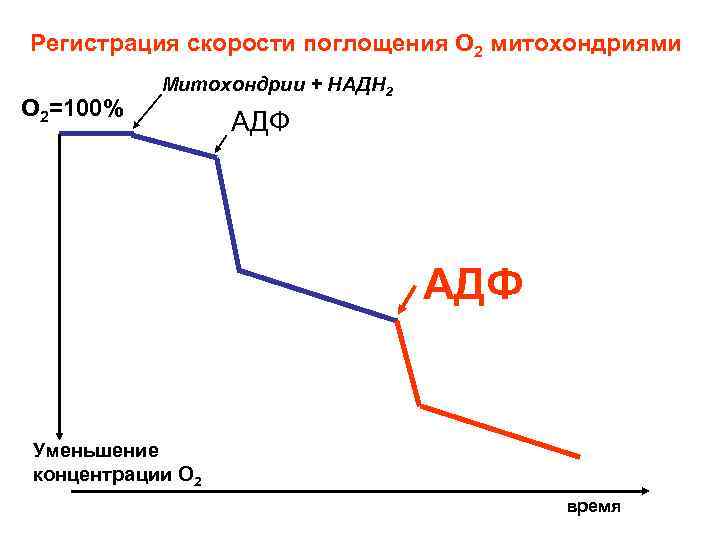
Регистрация скорости поглощения О 2 митохондриями О 2=100% Митохондрии + НАДН 2 АДФ Уменьшение концентрации О 2 время

Регистрация поглощения кислорода митохондриями прекращается, поскольку концентрация кислорода в инкубационной среде падает до нуля.
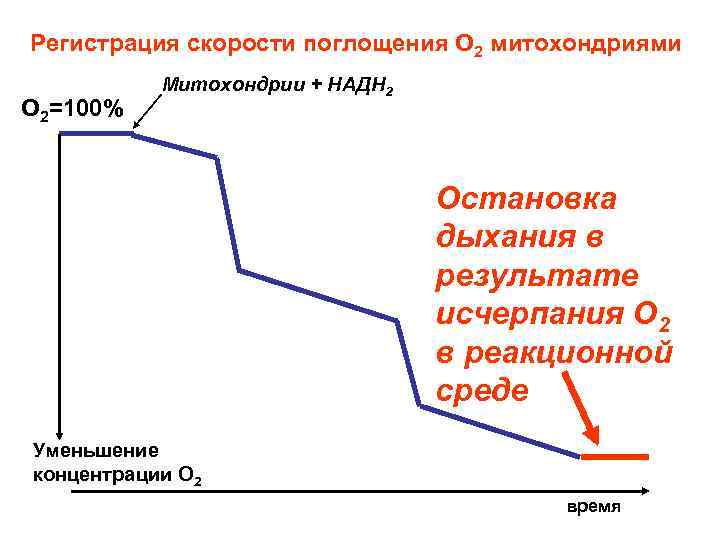
Регистрация скорости поглощения О 2 митохондриями О 2=100% Митохондрии + НАДН 2 Остановка дыхания в результате исчерпания О 2 в реакционной среде Уменьшение концентрации О 2 время
биоэнергетика-6.ppt