Lecture2_110914.ppt
- Количество слайдов: 44
 Основные законы химии Лекция 2 1
Основные законы химии Лекция 2 1
 Закон сохранения массы В ходе химической реакции как общая масса веществ, так и масса отдельных элементов остается постоянной. Ломоносов, 1748 Лавуазье, 1774 Михаил Васильевич Ломоносов (1711 -1765) 2 Антуан Лоран Лавуазье (1743 -1794)
Закон сохранения массы В ходе химической реакции как общая масса веществ, так и масса отдельных элементов остается постоянной. Ломоносов, 1748 Лавуазье, 1774 Михаил Васильевич Ломоносов (1711 -1765) 2 Антуан Лоран Лавуазье (1743 -1794)
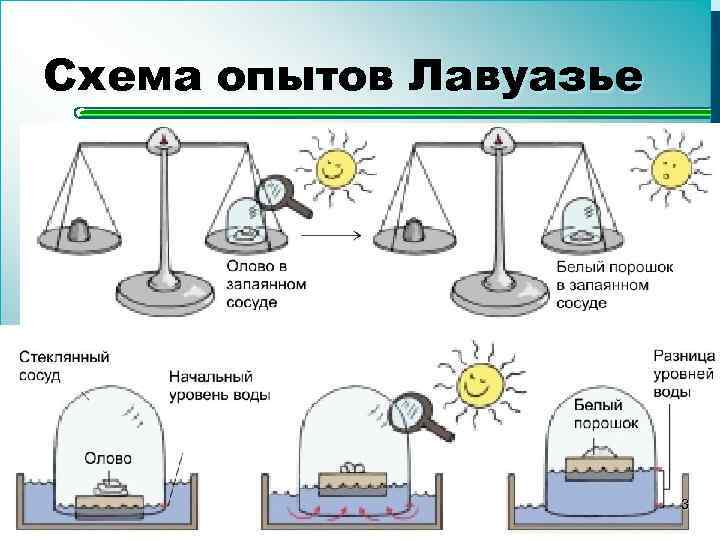 Схема опытов Лавуазье 3
Схема опытов Лавуазье 3
 Закон сохранения массы означает, что в ходе реакции масса не изменяется. Значит сумма масс продуктов реакции всегда равна сумме масс исходных реагентов. 2 H 2 + O 2 = 2 H 2 O 2 г 16 г 18 г (2 + 16 = 18) 4
Закон сохранения массы означает, что в ходе реакции масса не изменяется. Значит сумма масс продуктов реакции всегда равна сумме масс исходных реагентов. 2 H 2 + O 2 = 2 H 2 O 2 г 16 г 18 г (2 + 16 = 18) 4
 Закон постоянства состава Соотношения между массами элементов, входящих в состав данного соединения постоянны и не зависят от способа его получения. Пруст, 1797 Жозеф Луи Пруст (1754 -1826) Закон определенных пропорций Соотношения между массами элементов, входящих в состав соединения могут быть произвольными и меняться непрерывно. Клод Луи Бертолле (1748 -1822) Бертолле, 1803 5
Закон постоянства состава Соотношения между массами элементов, входящих в состав данного соединения постоянны и не зависят от способа его получения. Пруст, 1797 Жозеф Луи Пруст (1754 -1826) Закон определенных пропорций Соотношения между массами элементов, входящих в состав соединения могут быть произвольными и меняться непрерывно. Клод Луи Бертолле (1748 -1822) Бертолле, 1803 5
 Дальтониды и бертоллиды После того, как постоянство состава обычных соединений было подтверждено, в середине-конце 19 -го века было обнаружено, что значительное количество твердых веществ (галогениды, оксиды, карбонаты, гидроксиды, сульфиды, и т. п. ) могут иметь переменный состав в зависимости от условий синтеза и обработки. § Вещества постоянного состава называют дальтонидами. § Вещества переменного состава называют бертоллидами. 6
Дальтониды и бертоллиды После того, как постоянство состава обычных соединений было подтверждено, в середине-конце 19 -го века было обнаружено, что значительное количество твердых веществ (галогениды, оксиды, карбонаты, гидроксиды, сульфиды, и т. п. ) могут иметь переменный состав в зависимости от условий синтеза и обработки. § Вещества постоянного состава называют дальтонидами. § Вещества переменного состава называют бертоллидами. 6
 Закон кратных соотношений Если два элемента образуют друг с другом несколько соединений, то массы одного из элементов, приходящиеся на одну и ту же массу другого, относятся между собой как простые целые числа. Дальтон, 1803 Джон Дальтон (1766 -1844) 7
Закон кратных соотношений Если два элемента образуют друг с другом несколько соединений, то массы одного из элементов, приходящиеся на одну и ту же массу другого, относятся между собой как простые целые числа. Дальтон, 1803 Джон Дальтон (1766 -1844) 7
 Атомная теория Дальтона § Вся материя состоит из мельчайших частиц, называемых атомами, которые являются наименьшими частицами элементов, участвующих в химических реакциях. § Все атомы каждого элемента одинаковы. § Атомы различных элементов различны § Соединения образуются из атомов различных элементов в строго определенных пропорциях. § В ходе химических реакций атомы не разрушаются и не создаются, а только изменяется характер их взаимодействия друг с другом. Дальтон, 1803 8
Атомная теория Дальтона § Вся материя состоит из мельчайших частиц, называемых атомами, которые являются наименьшими частицами элементов, участвующих в химических реакциях. § Все атомы каждого элемента одинаковы. § Атомы различных элементов различны § Соединения образуются из атомов различных элементов в строго определенных пропорциях. § В ходе химических реакций атомы не разрушаются и не создаются, а только изменяется характер их взаимодействия друг с другом. Дальтон, 1803 8
 Атомные единицы массы На основании закона кратных соотношений Дальтон определил атомные массы известных к тому времени элементов, взяв за единицу массу наиболее легкого атома водорода. Абсолютные массы атомов, точно определенные позже, весьма невелики (~ 10 -27 – 10 -25 кг). Поэтому химики обычно пользуются относительными атомными единицами массы (а. е. м. ). С 1961 года в качестве единой а. е. м. используются углеродные единицы – 1/12 массы изотопа 12 С. 1 а. е. м. = 1, 661 * 10 -27 кг 9
Атомные единицы массы На основании закона кратных соотношений Дальтон определил атомные массы известных к тому времени элементов, взяв за единицу массу наиболее легкого атома водорода. Абсолютные массы атомов, точно определенные позже, весьма невелики (~ 10 -27 – 10 -25 кг). Поэтому химики обычно пользуются относительными атомными единицами массы (а. е. м. ). С 1961 года в качестве единой а. е. м. используются углеродные единицы – 1/12 массы изотопа 12 С. 1 а. е. м. = 1, 661 * 10 -27 кг 9
 Изотопы – это различающиеся по массе атомы одного элемента. Большинство элементов представляют собой смесь нескольких изотопов с различным естественным содержанием. Например: природный кремний состоит из 92, 28% 28 Si, 4, 67% 29 Si и 3, 05% 30 Si. 10
Изотопы – это различающиеся по массе атомы одного элемента. Большинство элементов представляют собой смесь нескольких изотопов с различным естественным содержанием. Например: природный кремний состоит из 92, 28% 28 Si, 4, 67% 29 Si и 3, 05% 30 Si. 10
 11
11
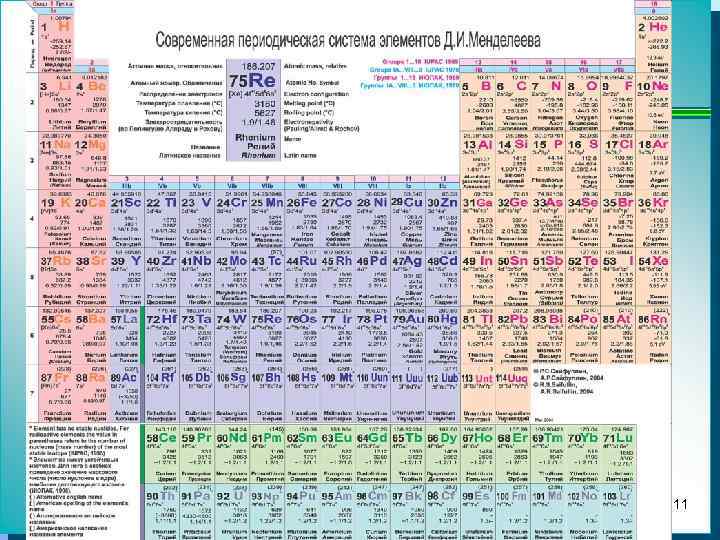
 Средняя атомная масса химического элемента равна среднему арифметическому относительных масс изотопов с учетом их естественного содержания. Средние атомные массы приведены в таблице Менделеева. Пример: Определить среднюю атомную массу хлора по следующим данным: Изотоп Масса изотопа, а. е. м. 35 Cl 34, 97 37 Cl 36, 95 Относительное содержание 0, 7553 0, 2447 Решение: Ar = 34, 97*0, 7553 + 36, 95 * 0, 2447 = 35, 45 а. е. м 12.
Средняя атомная масса химического элемента равна среднему арифметическому относительных масс изотопов с учетом их естественного содержания. Средние атомные массы приведены в таблице Менделеева. Пример: Определить среднюю атомную массу хлора по следующим данным: Изотоп Масса изотопа, а. е. м. 35 Cl 34, 97 37 Cl 36, 95 Относительное содержание 0, 7553 0, 2447 Решение: Ar = 34, 97*0, 7553 + 36, 95 * 0, 2447 = 35, 45 а. е. м 12.
 Молекулярная масса Молекулярной массой вещества называют отношение его массы к 1/12 массы атома углерода. Поскольку масса молекулы равна сумме масс составляющих ее атомов, то молекулярная масса равна сумме соответствующих атомных масс. 13
Молекулярная масса Молекулярной массой вещества называют отношение его массы к 1/12 массы атома углерода. Поскольку масса молекулы равна сумме масс составляющих ее атомов, то молекулярная масса равна сумме соответствующих атомных масс. 13
 Моль – количество вещества, которое содержит такое же число структурных единиц (молекул, атомов, ионов, электронов и т. д. ), как и в 12, 000 г изотопа углерода 12 С. Молярная масса (масса одного моля) вещества в г/моль численно равна его молекулярной массе в а. е. м. Число Авогадро 1 моль любого вещества содержит 6, 022 * 1023 молекул (атомов и т. п. ). 14
Моль – количество вещества, которое содержит такое же число структурных единиц (молекул, атомов, ионов, электронов и т. д. ), как и в 12, 000 г изотопа углерода 12 С. Молярная масса (масса одного моля) вещества в г/моль численно равна его молекулярной массе в а. е. м. Число Авогадро 1 моль любого вещества содержит 6, 022 * 1023 молекул (атомов и т. п. ). 14
 Расчет молярной массы Пример: рассчитать молярную массу CO 2. Решение: Mr (CO 2) = Ar (C) + 2 * Ar (O) = 12, 01 + Молекулярная 2 * 16, 00 = 44, 01 а. е. м масса M (CO 2) = 44, 01 г/моль Молярная масса 15
Расчет молярной массы Пример: рассчитать молярную массу CO 2. Решение: Mr (CO 2) = Ar (C) + 2 * Ar (O) = 12, 01 + Молекулярная 2 * 16, 00 = 44, 01 а. е. м масса M (CO 2) = 44, 01 г/моль Молярная масса 15
 Использование молярной массы Молярная масса (M) устанавливает связь между количеством вещества (n) и его массой (m). M = m/n или m = M * n или n = m/M Пример: Рассчитать количество вещества воды массой 5, 4 г. M (H 2 O) = 2 * 1, 0 + 16, 0 = 18, 0 г/моль n = m/M = 5, 4 г / 18, 0 г/моль = 0, 30 моль 16
Использование молярной массы Молярная масса (M) устанавливает связь между количеством вещества (n) и его массой (m). M = m/n или m = M * n или n = m/M Пример: Рассчитать количество вещества воды массой 5, 4 г. M (H 2 O) = 2 * 1, 0 + 16, 0 = 18, 0 г/моль n = m/M = 5, 4 г / 18, 0 г/моль = 0, 30 моль 16
 Массовая доля элемента Массовую долю элемента в соединении можно рассчитать как произведение атомной массы элемента на число его атомов в молекуле и на 100% поделенное на молекулярную массу соединения. Пример: Найти массовую долю кислорода в H 3 PO 4. Mr (H 3 PO 4) = 97. 99 а. е. м. %O = 4 * 16, 00 / 97, 99 * 100% = 65, 31% 17
Массовая доля элемента Массовую долю элемента в соединении можно рассчитать как произведение атомной массы элемента на число его атомов в молекуле и на 100% поделенное на молекулярную массу соединения. Пример: Найти массовую долю кислорода в H 3 PO 4. Mr (H 3 PO 4) = 97. 99 а. е. м. %O = 4 * 16, 00 / 97, 99 * 100% = 65, 31% 17
 Молекулярная и эмпирическая формулы вещества § Молекулярная формула соединения определяет истинное количество атомов различных элементов в молекуле (H 2 O вода). § Эмпирическая формула соединения - это формула отражающая качественный и количественный состав с использованием наименьших целых чисел. Например: Молекулярная формула бензола C 6 H 6. Его эмпирическая формула CH. 18
Молекулярная и эмпирическая формулы вещества § Молекулярная формула соединения определяет истинное количество атомов различных элементов в молекуле (H 2 O вода). § Эмпирическая формула соединения - это формула отражающая качественный и количественный состав с использованием наименьших целых чисел. Например: Молекулярная формула бензола C 6 H 6. Его эмпирическая формула CH. 18
 Определение формулы вещества Задача: Определить эмпирическую и молекулярную формулы вещества, содержащего 94, 06% O и 5, 93% H, если его молярная масса равна 34 г/моль. Решение: 1. Определяем, что других элементов в веществе нет: %O + %H = 94, 06% + 5, 93% = 99, 99% 100%. 2. Определяем относительное количество атомов каждого типа делением массовой доли на атомную массу каждого элемента: n (H) = 5, 93 г / 1, 01 г/моль = 5, 87 моль n (O) = 94, 06 г / 16, 00 г/моль = 5, 87 моль 3. Определяем наименьшие целые числа соотношения элементов: n (H) / n (O) = 5, 87 / 5, 87 = 1: 1. Эмпирическая формула вещества: HO. 19
Определение формулы вещества Задача: Определить эмпирическую и молекулярную формулы вещества, содержащего 94, 06% O и 5, 93% H, если его молярная масса равна 34 г/моль. Решение: 1. Определяем, что других элементов в веществе нет: %O + %H = 94, 06% + 5, 93% = 99, 99% 100%. 2. Определяем относительное количество атомов каждого типа делением массовой доли на атомную массу каждого элемента: n (H) = 5, 93 г / 1, 01 г/моль = 5, 87 моль n (O) = 94, 06 г / 16, 00 г/моль = 5, 87 моль 3. Определяем наименьшие целые числа соотношения элементов: n (H) / n (O) = 5, 87 / 5, 87 = 1: 1. Эмпирическая формула вещества: HO. 19
 Определение формулы вещества (продолжение) 4. Определяем молярную массу, соответствующую эмпирической формуле: M (OH) = 1, 01 + 16, 00 = 17, 01 г/моль. 5. Делением истинной молярной массы на полученное значение определяем целочисленный коэффициент, на который на умножить эмпирическую формулу: k = 34 / 17, 01 = 2 Молекулярная формула: H 2 O 2 (пероксид водорода). 20
Определение формулы вещества (продолжение) 4. Определяем молярную массу, соответствующую эмпирической формуле: M (OH) = 1, 01 + 16, 00 = 17, 01 г/моль. 5. Делением истинной молярной массы на полученное значение определяем целочисленный коэффициент, на который на умножить эмпирическую формулу: k = 34 / 17, 01 = 2 Молекулярная формула: H 2 O 2 (пероксид водорода). 20
 Закон эквивалентных отношений Весовые количества двух или нескольких веществ, которые порознь вступают в химические реакции с постоянным количеством третьего вещества совпадают с количествами двух первых веществ в их реакции между собой или являются простыми кратными этих Иеремия Вениамин Рихтер количеств. (1762 -1807) 21 Рихтер, 1792
Закон эквивалентных отношений Весовые количества двух или нескольких веществ, которые порознь вступают в химические реакции с постоянным количеством третьего вещества совпадают с количествами двух первых веществ в их реакции между собой или являются простыми кратными этих Иеремия Вениамин Рихтер количеств. (1762 -1807) 21 Рихтер, 1792
 Закон эквивалентов Все вещества реагируют друг с другом в количествах, пропорциональных их эквивалентам. Эквивалент [fэкв (B) – это реальная или условная часть вещества, которая в реакции может присоединять, замещать либо соответствовать одному атому или иону водорода (H, H+) или одному молю водорода (H, H+), а в окислительновосстановительных реакциях - одному электрону или одному молю электронов. 22
Закон эквивалентов Все вещества реагируют друг с другом в количествах, пропорциональных их эквивалентам. Эквивалент [fэкв (B) – это реальная или условная часть вещества, которая в реакции может присоединять, замещать либо соответствовать одному атому или иону водорода (H, H+) или одному молю водорода (H, H+), а в окислительновосстановительных реакциях - одному электрону или одному молю электронов. 22
 Фактор эквивалентности (fэкв) – это число, равное той доле вещества, которая эквивалентна одному атому (иону) водорода или одному молю атомов (ионов) водорода. Фактор эквивалентности может быть равен или меньше единицы. Фактор эквивалентности можно выразить как 1/z, где z – число эквивалентности, равное числу функциональных групп кислот, оснований, участвующих в реакции, или степени окисления элемента в соединении. 23
Фактор эквивалентности (fэкв) – это число, равное той доле вещества, которая эквивалентна одному атому (иону) водорода или одному молю атомов (ионов) водорода. Фактор эквивалентности может быть равен или меньше единицы. Фактор эквивалентности можно выразить как 1/z, где z – число эквивалентности, равное числу функциональных групп кислот, оснований, участвующих в реакции, или степени окисления элемента в соединении. 23
![Молярная масса эквивалента вещества [M(1/z B)] – это масса моля эквивалента вещества, равная произведению Молярная масса эквивалента вещества [M(1/z B)] – это масса моля эквивалента вещества, равная произведению](https://present5.com/presentation/-76557896_347407276/image-24.jpg) Молярная масса эквивалента вещества [M(1/z B)] – это масса моля эквивалента вещества, равная произведению его молярной массы на фактор эквивалетности. [M(1/z B)] = fэкв * M = 1/z * M Молярная масса эквивалента кислоты равна ее молярной массе, деленной на основность кислоты (n H+) или на число катионов водорода, участвующих в обмене. Пример: Определить M(1/z H 2 SO 4) в реакциях полного обмена: z = 2; fэкв = ½; M (H 2 SO 4) = 2 * 1, 01 г/моль + 32, 07 г/моль + 4 * 16, 00 г/моль = 98, 09 г/моль M(1/z H 2 SO 4) = 1/z * M (H 2 SO 4) = ½ * 98, 09 г/моль = 49, 05 г/моль 24
Молярная масса эквивалента вещества [M(1/z B)] – это масса моля эквивалента вещества, равная произведению его молярной массы на фактор эквивалетности. [M(1/z B)] = fэкв * M = 1/z * M Молярная масса эквивалента кислоты равна ее молярной массе, деленной на основность кислоты (n H+) или на число катионов водорода, участвующих в обмене. Пример: Определить M(1/z H 2 SO 4) в реакциях полного обмена: z = 2; fэкв = ½; M (H 2 SO 4) = 2 * 1, 01 г/моль + 32, 07 г/моль + 4 * 16, 00 г/моль = 98, 09 г/моль M(1/z H 2 SO 4) = 1/z * M (H 2 SO 4) = ½ * 98, 09 г/моль = 49, 05 г/моль 24
 Молярная масса эквивалента основания равна его молярной массе, деленной на число гидроксильных групп (n OH-) , участвующих в обмене. Молярная масса эквивалента соли равна ее молярной массе, деленной на произведение заряда катиона металла на число катионов в молекуле соли. Молярная масса эквивалента простого вещества равна его молярной массе, деленной на валентность. Пример: Определить M(1/z Al 2(SO 4)3). M (Al 2(SO 4)3 = 2 * 26, 98 + 3 * (32, 07 + 4 * 16, 00) = 342, 17 г/моль. M(1/z Al 2(SO 4)3) = M (Al 2(SO 4)3 / (ZAl 3+ * n. Al 3+) = 342, 17 г/моль / (3 * 2) = 57, 03 г/моль 25
Молярная масса эквивалента основания равна его молярной массе, деленной на число гидроксильных групп (n OH-) , участвующих в обмене. Молярная масса эквивалента соли равна ее молярной массе, деленной на произведение заряда катиона металла на число катионов в молекуле соли. Молярная масса эквивалента простого вещества равна его молярной массе, деленной на валентность. Пример: Определить M(1/z Al 2(SO 4)3). M (Al 2(SO 4)3 = 2 * 26, 98 + 3 * (32, 07 + 4 * 16, 00) = 342, 17 г/моль. M(1/z Al 2(SO 4)3) = M (Al 2(SO 4)3 / (ZAl 3+ * n. Al 3+) = 342, 17 г/моль / (3 * 2) = 57, 03 г/моль 25
 Применение закона эквивалентов Массы реагирующих без остатка веществ пропорциональны их эквивалентам или молярным массам эквивалентов. m(A) M(1/z. A) = = m(B) M(1/z. B) Если одно из веществ находится в газовом состоянии, закон можно записать иначе: m(A) V 0(газа) = M(1/z. A) Vэкв(газа) Здесь V 0 и Vэкв – объем газа и объем эквивалента газа, соответственно. 26
Применение закона эквивалентов Массы реагирующих без остатка веществ пропорциональны их эквивалентам или молярным массам эквивалентов. m(A) M(1/z. A) = = m(B) M(1/z. B) Если одно из веществ находится в газовом состоянии, закон можно записать иначе: m(A) V 0(газа) = M(1/z. A) Vэкв(газа) Здесь V 0 и Vэкв – объем газа и объем эквивалента газа, соответственно. 26
 Химическое уравнение – это краткая запись химической реакции с использованием химических символов. В уравнениях должны быть показаны: § все реагенты и продукты; § физические состояния всех веществ; § любые дополнительные условия реакции; Количество атомов каждого элемента в реагентах и продуктах должны быть равны. t Ca. CO 3 (тв) = Ca. O (тв) + CO 2 (газ) 27
Химическое уравнение – это краткая запись химической реакции с использованием химических символов. В уравнениях должны быть показаны: § все реагенты и продукты; § физические состояния всех веществ; § любые дополнительные условия реакции; Количество атомов каждого элемента в реагентах и продуктах должны быть равны. t Ca. CO 3 (тв) = Ca. O (тв) + CO 2 (газ) 27
 Стехиометрия – раздел химии, изучающий, в каких количественных и объемных соотношениях вещества взаимодействуют друг с другом. Нужно уравнять уравнение и работать с молями 28
Стехиометрия – раздел химии, изучающий, в каких количественных и объемных соотношениях вещества взаимодействуют друг с другом. Нужно уравнять уравнение и работать с молями 28
 Этапы стехиометрических расчетов 1. 2. 3. Уравняйте химическое уравнение. Рассчитайте молярные массы. Переведите все данные массы (объемы) в моли. 4. Используйте химическое уравнение для получения нужного результата. 5. Переведите моли назад в массы, если нужно. 29
Этапы стехиометрических расчетов 1. 2. 3. Уравняйте химическое уравнение. Рассчитайте молярные массы. Переведите все данные массы (объемы) в моли. 4. Используйте химическое уравнение для получения нужного результата. 5. Переведите моли назад в массы, если нужно. 29
 Стехиометрические расчеты Задача: Сколько кислорода необходимо для окисления 2, 57 г CO в CO 2. Решение: 1. Записываем уравнение реакции: CO + O 2 = CO 2 2. Уравниваем его: 2 CO + O 2 = 2 CO 2 3. Рассчитываем молярные массы всех реагентов: M (CO) = 28, 01 г/моль; M (CO 2) = 44, 01 г/моль; M (O 2) = 32, 00 г/моль. 30
Стехиометрические расчеты Задача: Сколько кислорода необходимо для окисления 2, 57 г CO в CO 2. Решение: 1. Записываем уравнение реакции: CO + O 2 = CO 2 2. Уравниваем его: 2 CO + O 2 = 2 CO 2 3. Рассчитываем молярные массы всех реагентов: M (CO) = 28, 01 г/моль; M (CO 2) = 44, 01 г/моль; M (O 2) = 32, 00 г/моль. 30
 Стехиометрические расчеты 4. Определяем количество молей CO: n (CO) = 2, 57 г / 28, 01 г/моль = 0, 09175 моль. 5. Из уравнения реакции определяем, что 2 моля CO реагирует с 1 молем O 2. n (O 2) = n (CO) / 2 = 0, 09175 / 2 = 0, 04588 моль 6. Рассчитываем массу прореагировавшего O 2: m (O 2) = n (O 2) * M (O 2) = 0, 04588 * 32, 00 = 1, 47 г. 31
Стехиометрические расчеты 4. Определяем количество молей CO: n (CO) = 2, 57 г / 28, 01 г/моль = 0, 09175 моль. 5. Из уравнения реакции определяем, что 2 моля CO реагирует с 1 молем O 2. n (O 2) = n (CO) / 2 = 0, 09175 / 2 = 0, 04588 моль 6. Рассчитываем массу прореагировавшего O 2: m (O 2) = n (O 2) * M (O 2) = 0, 04588 * 32, 00 = 1, 47 г. 31
 Лимитирующие реагенты Реагенты, расходующийся в ходе реакции первым, называют лимитирующим. Реагент, остающийся после расходования лимитирующего реагента и окончания реакции, называют избыточным. Для определения того, какой из реагентов будет лимитировать реакцию, определяют наименьшее из отношений количества вещества реагентов к их стехиометрическим коэффициентам. 32
Лимитирующие реагенты Реагенты, расходующийся в ходе реакции первым, называют лимитирующим. Реагент, остающийся после расходования лимитирующего реагента и окончания реакции, называют избыточным. Для определения того, какой из реагентов будет лимитировать реакцию, определяют наименьшее из отношений количества вещества реагентов к их стехиометрическим коэффициентам. 32
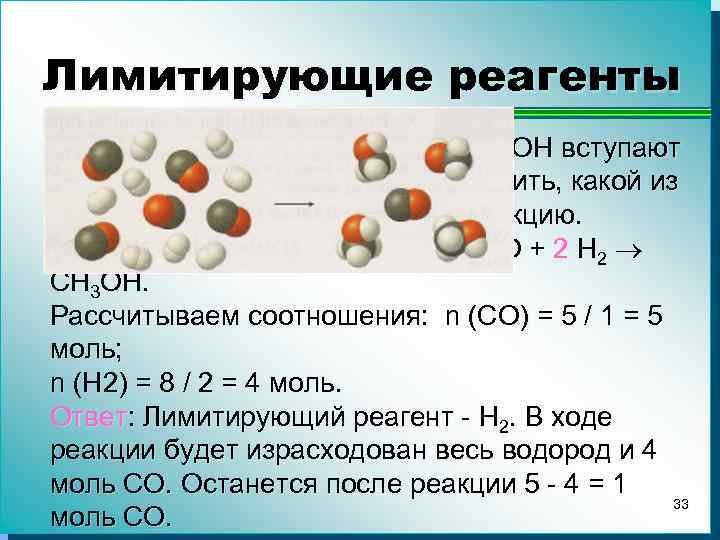 Лимитирующие реагенты Пример: В реакцию CO + H 2 CH 3 OH вступают 5 молей CO и 8 молей H 2. Определить, какой из реагентов будет лимитировать реакцию. Решение: Уравниваем реакцию: CO + 2 H 2 CH 3 OH. Рассчитываем соотношения: n (CO) = 5 / 1 = 5 моль; n (H 2) = 8 / 2 = 4 моль. Ответ: Лимитирующий реагент - H 2. В ходе реакции будет израсходован весь водород и 4 моль СO. Останется после реакции 5 - 4 = 1 33 моль СO.
Лимитирующие реагенты Пример: В реакцию CO + H 2 CH 3 OH вступают 5 молей CO и 8 молей H 2. Определить, какой из реагентов будет лимитировать реакцию. Решение: Уравниваем реакцию: CO + 2 H 2 CH 3 OH. Рассчитываем соотношения: n (CO) = 5 / 1 = 5 моль; n (H 2) = 8 / 2 = 4 моль. Ответ: Лимитирующий реагент - H 2. В ходе реакции будет израсходован весь водород и 4 моль СO. Останется после реакции 5 - 4 = 1 33 моль СO.
 Выход реакции Количество продуктов, которое должно образовываться согласно уравнению реакции называют теоретическим выходом. Теоретический выход подразумевает, что весь лимитирующий реагент полностью превращается в продукт(ы). На практике практический выход практически всегда ниже теоретического. Выход реакции определяют как отношение реального выхода к теоретическому, умноженное на 100%. Y = (практический выход/ теоретический выход) * 34 100%
Выход реакции Количество продуктов, которое должно образовываться согласно уравнению реакции называют теоретическим выходом. Теоретический выход подразумевает, что весь лимитирующий реагент полностью превращается в продукт(ы). На практике практический выход практически всегда ниже теоретического. Выход реакции определяют как отношение реального выхода к теоретическому, умноженное на 100%. Y = (практический выход/ теоретический выход) * 34 100%
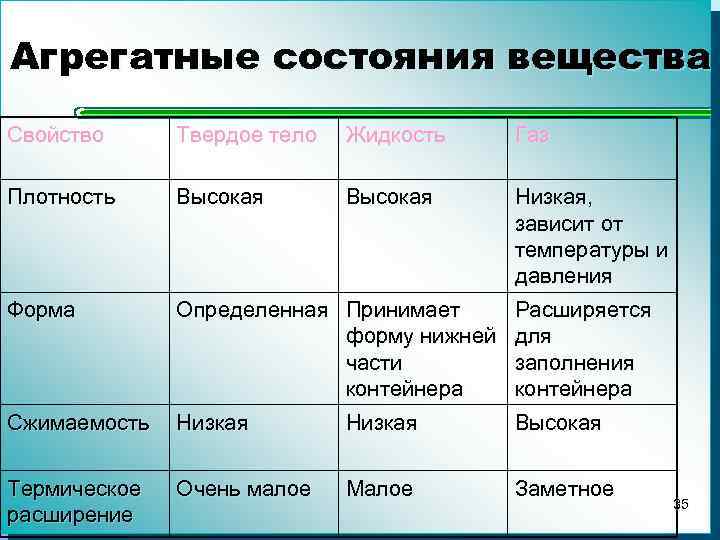 Агрегатные состояния вещества Свойство Твердое тело Жидкость Плотность Высокая Очень малое Малое Форма Сжимаемость Термическое расширение Газ Низкая, зависит от температуры и давления Определенная Принимает Расширяется форму нижней для части заполнения контейнера Низкая Высокая Заметное 35
Агрегатные состояния вещества Свойство Твердое тело Жидкость Плотность Высокая Очень малое Малое Форма Сжимаемость Термическое расширение Газ Низкая, зависит от температуры и давления Определенная Принимает Расширяется форму нижней для части заполнения контейнера Низкая Высокая Заметное 35
 Агрегатные состояния вещества Твердое тело Жидкость Газ 36
Агрегатные состояния вещества Твердое тело Жидкость Газ 36
 Свойства газа § В этом состоянии вещества молекулы обладают достаточной энергией для преодоления сил взаимодействия. § Каждая молекула движется независимо от других. § Это приводит к низкой плотности и заполнению всего объема контейнера газами. 37
Свойства газа § В этом состоянии вещества молекулы обладают достаточной энергией для преодоления сил взаимодействия. § Каждая молекула движется независимо от других. § Это приводит к низкой плотности и заполнению всего объема контейнера газами. 37
 Давление газа Все газы оказывают давление на стенки сосуда, куда они помещены. Его можно измерить барометром. Давление 1 атмосферы газа на уровне моря при нормальном давлении равно 760 мм ртутного столба. 38
Давление газа Все газы оказывают давление на стенки сосуда, куда они помещены. Его можно измерить барометром. Давление 1 атмосферы газа на уровне моря при нормальном давлении равно 760 мм ртутного столба. 38
 Газовые законы § Газовые законы связывают объем, давление, и другие свойства газов между собой: § Закон Бойля-Мариотта § Закон Гей-Люссака § Закон Шарля § Закон Авогадро § Уравнение состояния идеального газа (Менделеева-Клапейрона) связывает все эти законы в одну формулу. 39
Газовые законы § Газовые законы связывают объем, давление, и другие свойства газов между собой: § Закон Бойля-Мариотта § Закон Гей-Люссака § Закон Шарля § Закон Авогадро § Уравнение состояния идеального газа (Менделеева-Клапейрона) связывает все эти законы в одну формулу. 39
 Закон Бойля-Мариотта При постоянной температуре и количестве вещества объем газа обратно пропорционален его давлению. P*V = const или P 1 V 1 = P 2 V 2 Роберт Бойль (1627 -1691) Эдм Мариотт (1620 -1684) На рисунке членов Французской Академии наук 6 -ой справа 40
Закон Бойля-Мариотта При постоянной температуре и количестве вещества объем газа обратно пропорционален его давлению. P*V = const или P 1 V 1 = P 2 V 2 Роберт Бойль (1627 -1691) Эдм Мариотт (1620 -1684) На рисунке членов Французской Академии наук 6 -ой справа 40
 Закон Гей-Люссака При постоянном давлении и количестве вещества объем газа прямо пропорционален абсолютной температуре. V/T = const или V 1/T 1 = V 2/T 2 Абсолютная температура измеряется в Кельвинах. Она равна температуре в °С плюс 273, 15. 0°С = 273, 15 K Жозеф Луи Гей-Люссак (1778 -1850) 41
Закон Гей-Люссака При постоянном давлении и количестве вещества объем газа прямо пропорционален абсолютной температуре. V/T = const или V 1/T 1 = V 2/T 2 Абсолютная температура измеряется в Кельвинах. Она равна температуре в °С плюс 273, 15. 0°С = 273, 15 K Жозеф Луи Гей-Люссак (1778 -1850) 41
 Закон Шарля При постоянном объеме и количестве вещества давление газа прямо пропорционально абсолютной температуре. P/T = const или P 1/T 1 = P 2/T 2 Жак Александр Сезар Шарль (1746 -1823) 42
Закон Шарля При постоянном объеме и количестве вещества давление газа прямо пропорционально абсолютной температуре. P/T = const или P 1/T 1 = P 2/T 2 Жак Александр Сезар Шарль (1746 -1823) 42
 Закон Авогадро Одинаковые объемы газа при одинаковых температуре и давлении содержат одинаковое количество молекул. V = const * n или V 1/n 1 = V 2/n 2 Амедео Авогадро (1776 -1856) 43
Закон Авогадро Одинаковые объемы газа при одинаковых температуре и давлении содержат одинаковое количество молекул. V = const * n или V 1/n 1 = V 2/n 2 Амедео Авогадро (1776 -1856) 43
 Объем газа при стандартных условиях Стандартные условия: Температура: 0°С = 273, 15 K Давление: 1 атм = 1, 013 * 105 Па В этих условиях объем одного моля любого идеального газа равен 22, 4 л. 44
Объем газа при стандартных условиях Стандартные условия: Температура: 0°С = 273, 15 K Давление: 1 атм = 1, 013 * 105 Па В этих условиях объем одного моля любого идеального газа равен 22, 4 л. 44


