modification14-2.pptx
- Количество слайдов: 22

Основные типы посттрансляционной модификации белков 1. Присоединение различных групп к радикалам аминокислот (ацетилирование, метилирование, фосфорилирование, карбоксилирование, гидроксилирование, сульфатирование, иодирование) 2. Изменение химической природы аминокислоты (окисление цистеина, циклизация N-концевого глутамата, амидирование, эпимеризация Lаминокислот, трансформация аргинина в цитруллин) 3. Присоединение кофакторов (пиридоксальфосфат, флавиновые коферменты, гем, биотин, липоевая кислота) 4. Присоединение липидов (изопренильные остатки, миристиновая кта, фосфатидилинозитол) 5. Присоединение пептидов (убиквитинилирование, сумоилирование) 6. Сплайсинг белков 7. Ограниченный протеолиз (удаление N- и С-концевых аминокислот, удаление сигнального пептида, удаление пропептида, созревание белка) 1 8. Присоединение полисахаридов (N- и О-гликозилирование)

Схема созревания белка в ЭР Disulfide bonds S Сигнальная пептидаза, протеазы, ферменты гликозилирования (трансферазы, гликозидазы), протеиндисульфидизомераза, пролилизомераза, шапероны S 2
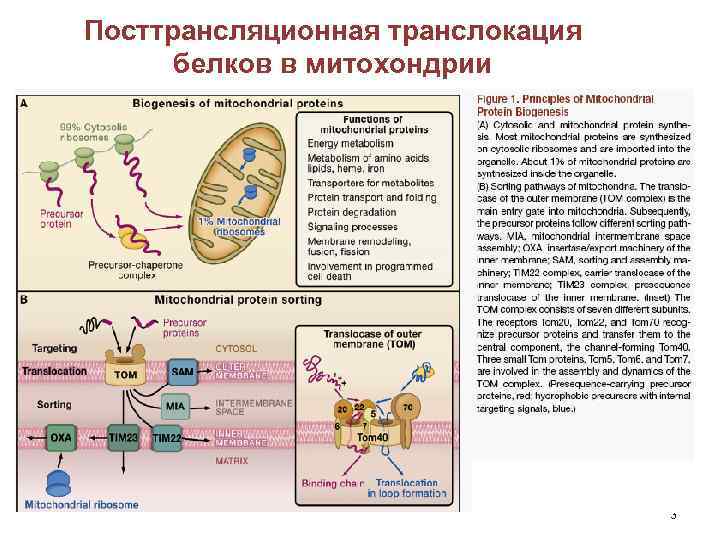
Посттрансляционная транслокация белков в митохондрии 3
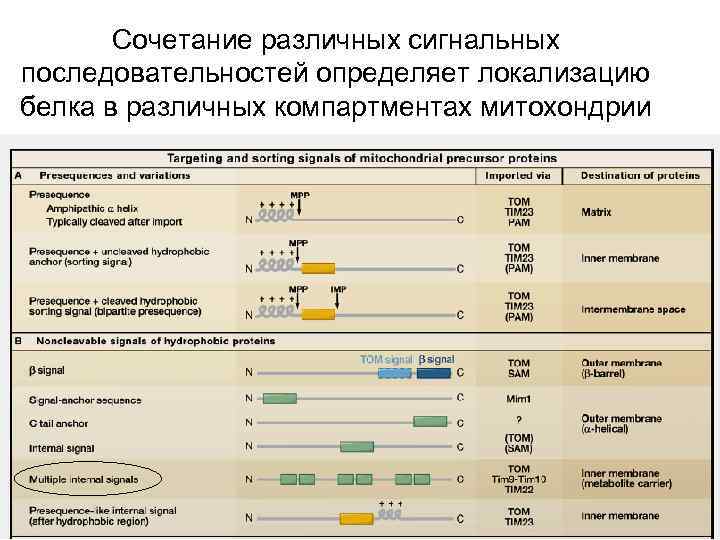
Сочетание различных сигнальных последовательностей определяет локализацию белка в различных компартментах митохондрии 4
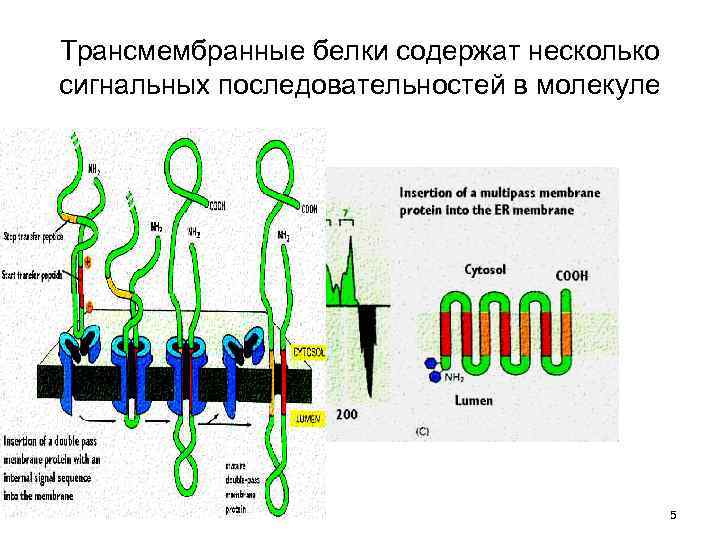
Трансмембранные белки содержат несколько сигнальных последовательностей в молекуле 5
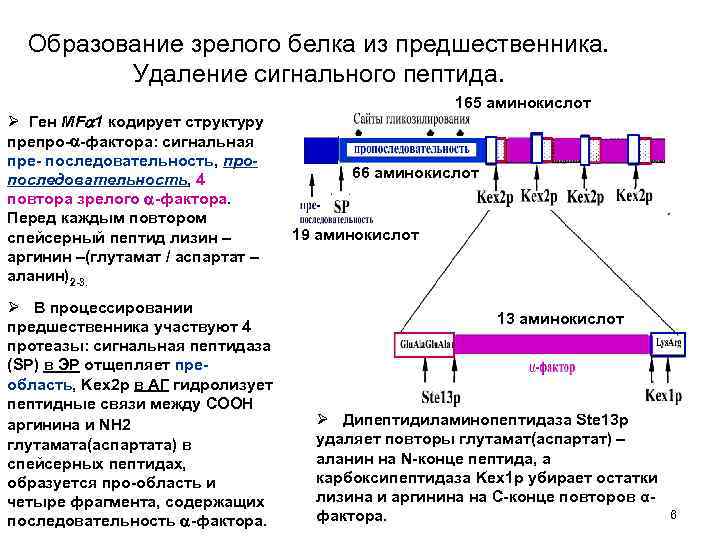
Образование зрелого белка из предшественника. Удаление сигнального пептида. Ø Ген MF 1 кодирует структуру препро- -фактора: сигнальная пре- последовательность, пропоследовательность, 4 повтора зрелого -фактора. Перед каждым повтором спейсерный пептид лизин – аргинин –(глутамат / аспартат – аланин)2 -3. Ø В процессировании предшественника участвуют 4 протеазы: сигнальная пептидаза (SP) в ЭР отщепляет преобласть, Kex 2 p в АГ гидролизует пептидные связи между СООН аргинина и NН 2 глутамата(аспартата) в спейсерных пептидах, образуется про-область и четыре фрагмента, содержащих последовательность -фактора. 165 аминокислот 66 аминокислот 19 аминокислот 13 аминокислот Ø Дипептидиламинопептидаза Ste 13 p удаляет повторы глутамат(аспартат) – аланин на N-конце пептида, а карбоксипептидаза Kex 1 p убирает остатки лизина и аргинина на С-конце повторов αфактора. 6
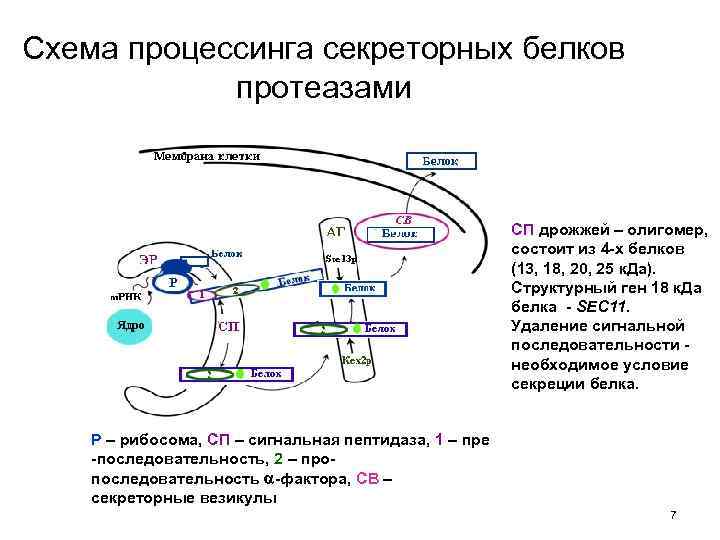
Схема процессинга секреторных белков протеазами СП дрожжей – олигомер, состоит из 4 -х белков (13, 18, 20, 25 к. Да). Структурный ген 18 к. Да белка - SEC 11. Удаление сигнальной последовательности необходимое условие секреции белка. Р – рибосома, СП – сигнальная пептидаза, 1 – пре -последовательность, 2 – пропоследовательность -фактора, СВ – секреторные везикулы 7
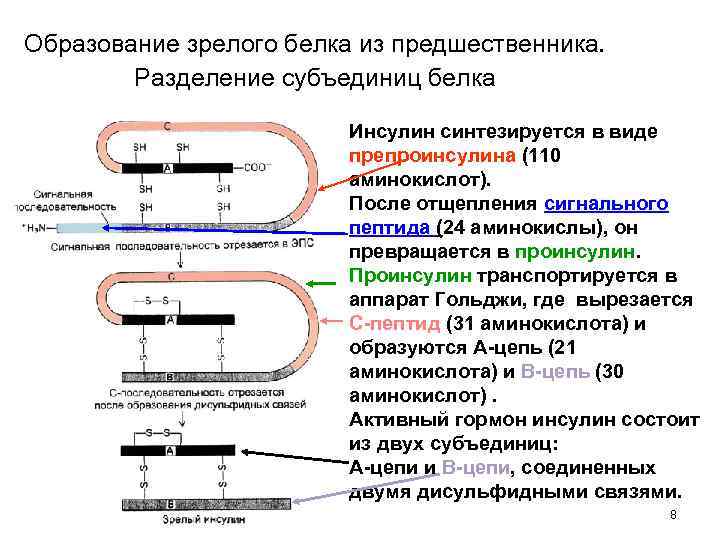
Образование зрелого белка из предшественника. Разделение субъединиц белка Инсулин синтезируется в виде препроинсулина (110 аминокислот). После отщепления сигнального пептида (24 аминокислы), он превращается в проинсулин. Проинсулин транспортируется в аппарат Гольджи, где вырезается С-пептид (31 аминокислота) и образуются A-цепь (21 аминокислота) и B-цепь (30 аминокислот). Активный гормон инсулин состоит из двух субъединиц: A-цепи и B-цепи, соединенных двумя дисульфидными связями. 8
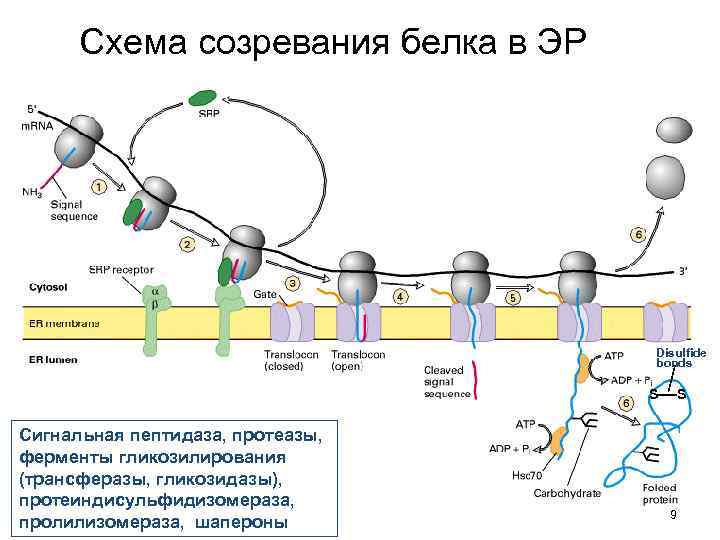
Схема созревания белка в ЭР Disulfide bonds S Сигнальная пептидаза, протеазы, ферменты гликозилирования (трансферазы, гликозидазы), протеиндисульфидизомераза, пролилизомераза, шапероны S 9
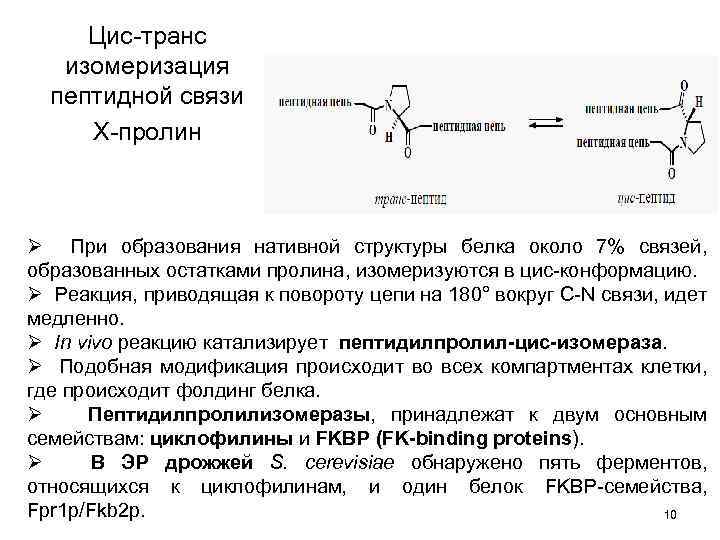
Цис-транс изомеризация пептидной связи Х-пролин Ø При образования нативной структуры белка около 7% связей, образованных остатками пролина, изомеризуются в цис-конформацию. Ø Реакция, приводящая к повороту цепи на 180° вокруг C-N связи, идет медленно. Ø In vivo реакцию катализирует пептидилпролил-цис-изомераза. Ø Подобная модификация происходит во всех компартментах клетки, где происходит фолдинг белка. Ø Пептидилпролилизомеразы, принадлежат к двум основным семействам: циклофилины и FKBP (FK-binding proteins). Ø В ЭР дрожжей S. cerevisiae обнаружено пять ферментов, относящихся к циклофилинам, и один белок FKBP-семейства, Fpr 1 p/Fkb 2 p. 10
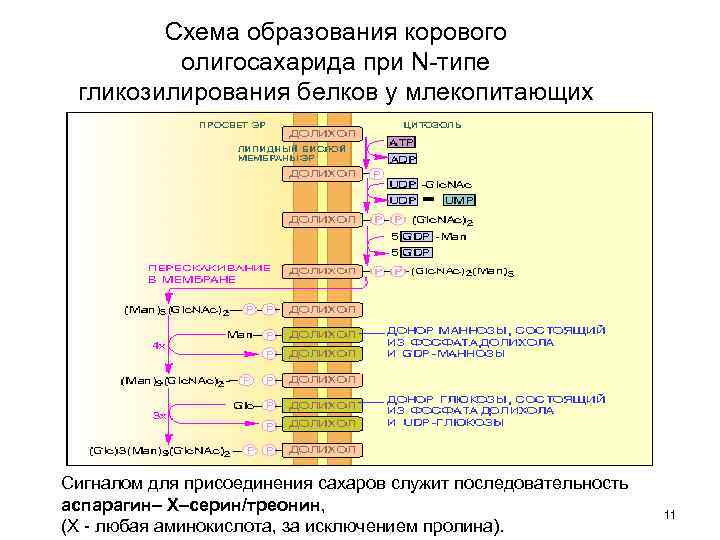
Схема образования корового олигосахарида при N-типе гликозилирования белков у млекопитающих Сигналом для присоединения сахаров служит последовательность аспарагин– Х–серин/треонин, (Х - любая аминокислота, за исключением пролина). 11
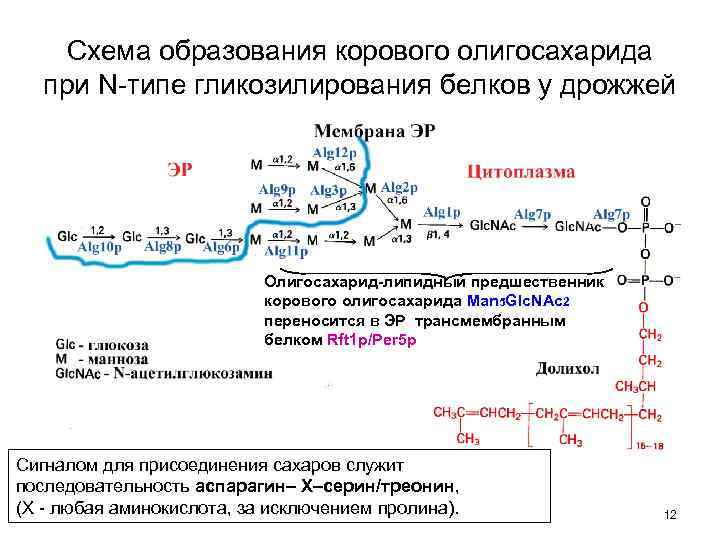
Схема образования корового олигосахарида при N-типе гликозилирования белков у дрожжей Олигосахарид-липидный предшественник корового олигосахарида Man 5 Glc. NAc 2 переносится в ЭР трансмембранным белком Rft 1 p/Per 5 p Сигналом для присоединения сахаров служит последовательность аспарагин– Х–серин/треонин, (Х - любая аминокислота, за исключением пролина). 12
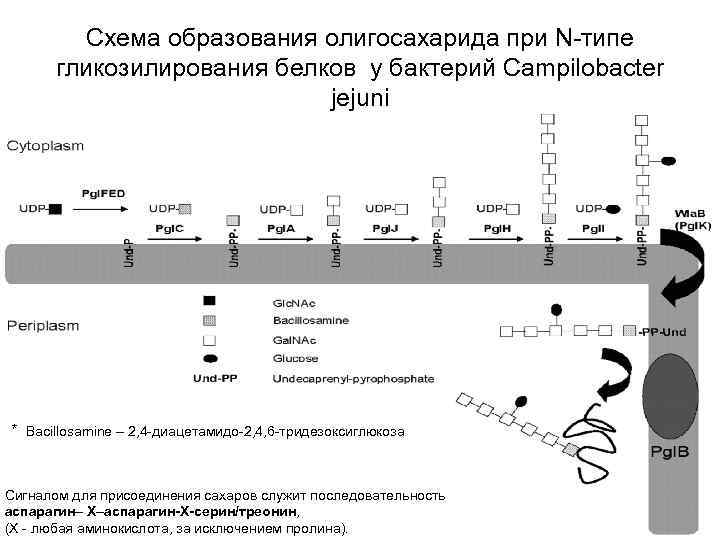
Схема образования олигосахарида при N-типе гликозилирования белков у бактерий Campilobacter jejuni * * Bacillosamine – 2, 4 -диацетамидо-2, 4, 6 -тридезоксиглюкоза Сигналом для присоединения сахаров служит последовательность аспарагин– Х–аспарагин-Х-серин/треонин, (Х - любая аминокислота, за исключением пролина). 13
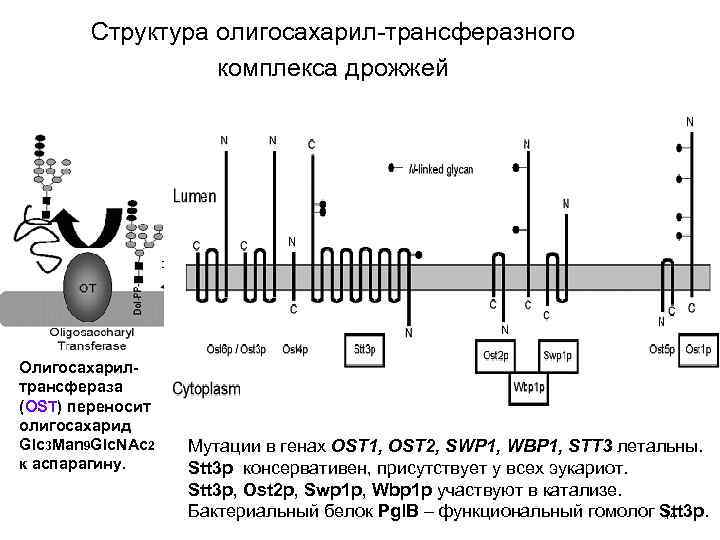
Структура олигосахарил-трансферазного комплекса дрожжей Олигосахарилтрансфераза (OST) переносит олигосахарид Glc 3 Man 9 Glc. NAc 2 к аспарагину. Мутации в генах OST 1, OST 2, SWP 1, WBP 1, STT 3 летальны. Stt 3 p консервативен, присутствует у всех эукариот. Stt 3 p, Ost 2 p, Swp 1 p, Wbp 1 p участвуют в катализе. Бактериальный белок Pgl. B – функциональный гомолог Stt 3 p. 14
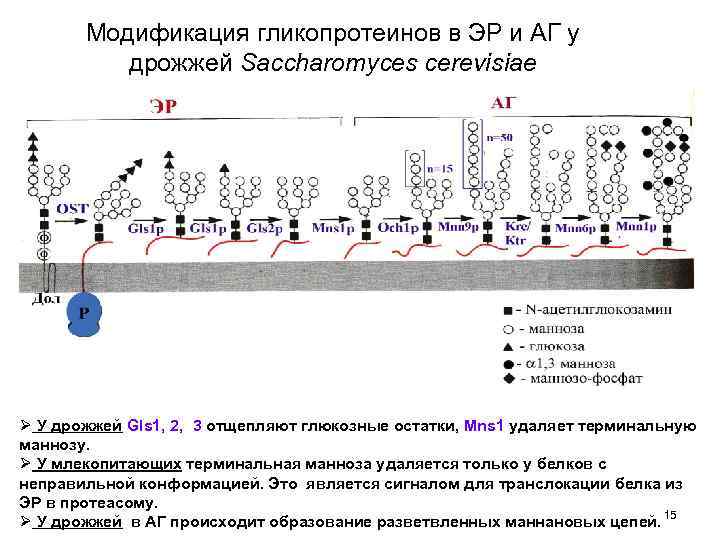
Модификация гликопротеинов в ЭР и АГ у дрожжей Saccharomyces cerevisiae Ø У дрожжей Gls 1, 2, 3 отщепляют глюкозные остатки, Mns 1 удаляет терминальную маннозу. Ø У млекопитающих терминальная манноза удаляется только у белков с неправильной конформацией. Это является сигналом для транслокации белка из ЭР в протеасому. Ø У дрожжей в АГ происходит образование разветвленных маннановых цепей. 15
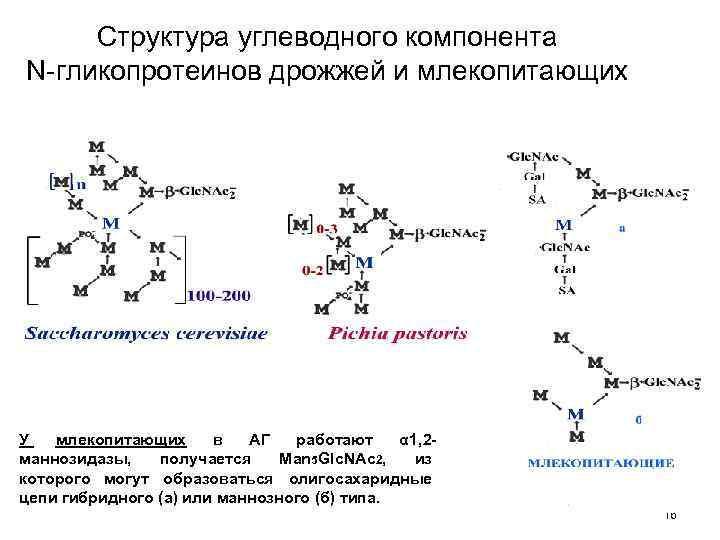
Структура углеводного компонента N-гликопротеинов дрожжей и млекопитающих У млекопитающих в АГ работают α 1, 2 маннозидазы, получается Man 5 Glc. NAc 2, из которого могут образоваться олигосахаридные цепи гибридного (а) или маннозного (б) типа. 16

О-гликозилирование белков N-ацетилгалактозамин Ø У дрожжей синтез олигосахаридной цепи начинается в ЭР. Ø Маннозилтрансфераза переносит маннозу к серину или треонину. Донор маннозодолихолфосфат. Ø Удлинение олигосахаридной цепи происходит в АГ за счет маннозы (1 -6 остатков). Ø Вероятность О-гликозилирования повышается при нахождении лизина перед серином/треонином. Ø В клетках животных синтез олигосахаридной цепи происходит в АГ. Ø Начинается присоединением Nацетилгалактозамина к серину или треонину. Донором углеводного остатка выступает УДФацетилгалактозамин. Ø Удлинение олигосахаридной цепи осуществляется в поздних цистернах АГ за счет ацетилгглюкозамина, галактозы, фукозы и сиаловой кислоты. Ø Вероятность О-гликозилирования повышается при нахождении пролина в +1 и – 1 положении относительно серина/треонина. 17

Фенотипическое проявление мутаций в генах, отвечающих за гликозилирование секреторных белков Ø Мутации, влияющие на активность олигосахарилтрансферазы (ost 2, ost 1, stt 3, swp 1, wbp 1) и мутации pnt, затрагивающие первую стадию О-гликозилирования, летальны. Ø Мутации alg 1, 2, 7, затрагивающие первые этапы синтеза корового олигосахарида, приводят к замедленному росту штаммов. Ø У alg 12 мутантов происходит неправильная транслокация вакуолярной протеиназы А в периплазматическое пространство. Ø Мутации в структурных генах 1, 2 -маннозилтрансфераз (KRE 2, KTR 1, KTR 3) приводят к уменьшению длины внешних полисахаридных цепей маннопротеинов клеточной стенки, что сопровождается нарушением ее структуры. 18
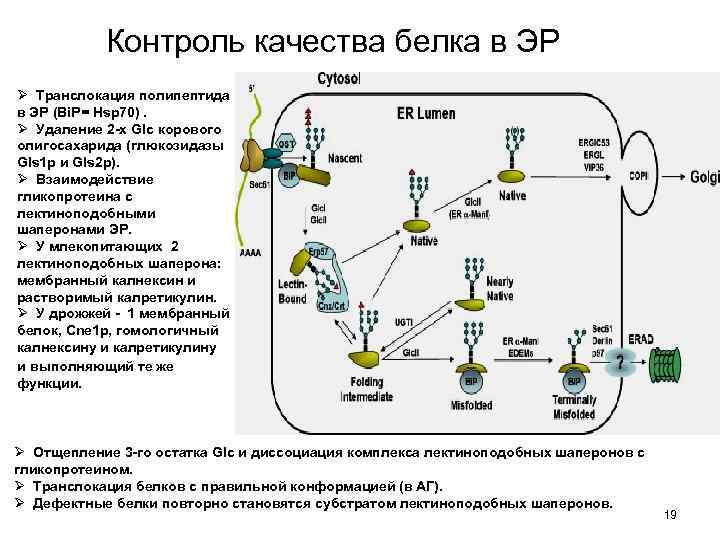
Контроль качества белка в ЭР Ø Транслокация полипептида в ЭР (Bi. P= Hsp 70). Ø Удаление 2 -х Glc корового олигосахарида (глюкозидазы Gls 1 p и Gls 2 p). Ø Взаимодействие гликопротеина с лектиноподобными шаперонами ЭР. Ø У млекопитающих 2 лектиноподобных шаперона: мембранный калнексин и растворимый калретикулин. Ø У дрожжей - 1 мембранный белок, Cne 1 p, гомологичный калнексину и калретикулину и выполняющий те же функции. Ø Отщепление 3 -го остатка Glc и диссоциация комплекса лектиноподобных шаперонов с гликопротеином. Ø Транслокация белков с правильной конформацией (в АГ). Ø Дефектные белки повторно становятся субстратом лектиноподобных шаперонов. 19
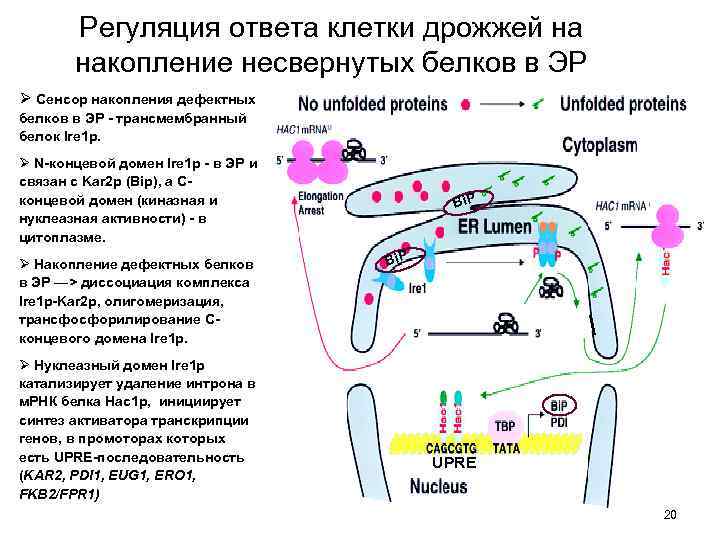
Регуляция ответа клетки дрожжей на накопление несвернутых белков в ЭР Ø Сенсор накопления дефектных белков в ЭР - трансмембранный белок Ire 1 p. Ø N-концевой домен Ire 1 p - в ЭР и связан с Kar 2 p (Bip), а Cконцевой домен (киназная и нуклеазная активности) - в цитоплазме. Ø Накопление дефектных белков в ЭР —> диссоциация комплекса Ire 1 p-Kar 2 p, олигомеризация, трансфосфорилирование Cконцевого домена Ire 1 p. Ø Нуклеазный домен Ire 1 p катализирует удаление интрона в м. РНК белка Hac 1 p, инициирует синтез активатора транскрипции генов, в промоторах которых есть UPRE-последовательность (KAR 2, PDI 1, EUG 1, ERO 1, FKB 2/FPR 1) Bi. Р UPRE 20

Регуляция ответа клеток млекопитающих на накопление несвернутых белков в ЭР (SREBP) SREBP – sterol regulation element binding protein CHOP - C/EBP (CAAT-enhancer binding protein) Atf 4 – ортолог Gcn 4 дрожжей, семейство CREB (c. AMP-response element binding protein) 21
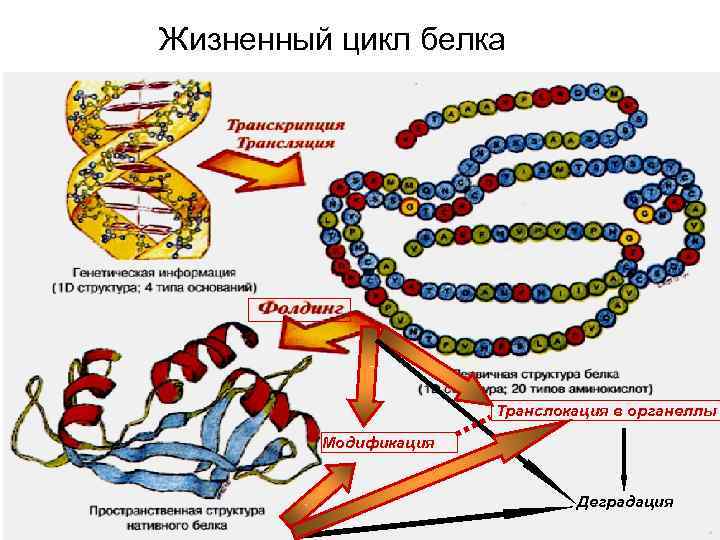
Жизненный цикл белка Транслокация в органеллы Модификация Деградация 22
modification14-2.pptx