Лекция 2,3 ГТУ (горение).ppt
- Количество слайдов: 52
 Основные термодинамические соотношения Интенсивными называют свойства вещества, не зависящие от количества вещества, например температура и давление. Удельные величины, т. е. отнесенные к единице количества вещества, например плотность, теплоемкость, имеют интенсивные свойства. Экстенсивными называют свойства вещества, зависящие от количества вещества, например объем. Температура – это физическая величина, являющаяся мерой отношения одного тела от теплового равновесия другого тела, состояние которого принято за нулевое. В термодинамических расчетах используют шкалу Кельвина, K. Т=t+273, 15 Давление – это сила, действующая по нормали к поверхности тела и отнесенная к единице площади его поверхности. Давление земной атмосферы зависит от высоты над уровнем моря и метеорологических условий данной местности.
Основные термодинамические соотношения Интенсивными называют свойства вещества, не зависящие от количества вещества, например температура и давление. Удельные величины, т. е. отнесенные к единице количества вещества, например плотность, теплоемкость, имеют интенсивные свойства. Экстенсивными называют свойства вещества, зависящие от количества вещества, например объем. Температура – это физическая величина, являющаяся мерой отношения одного тела от теплового равновесия другого тела, состояние которого принято за нулевое. В термодинамических расчетах используют шкалу Кельвина, K. Т=t+273, 15 Давление – это сила, действующая по нормали к поверхности тела и отнесенная к единице площади его поверхности. Давление земной атмосферы зависит от высоты над уровнем моря и метеорологических условий данной местности.
 В среднем на уровне моря давление равно 101325 Па. Эта величина называется нормальным давлением. Термодинамическим параметром является абсолютное давление Ра, Па, рассчитываемое по формулам: при давлении в аппарате больше атмосферного: при давлении в аппарате меньше атмосферного: где Рб – барометрическое (атмосферное) давление; Pм – манометрическое (избыточное) давление; Pв – вакуумметрическое давление. Для замера атмосферного давления используется барометр, для замера избыточного давления – манометр, для замера разряжения - вакуумметр.
В среднем на уровне моря давление равно 101325 Па. Эта величина называется нормальным давлением. Термодинамическим параметром является абсолютное давление Ра, Па, рассчитываемое по формулам: при давлении в аппарате больше атмосферного: при давлении в аппарате меньше атмосферного: где Рб – барометрическое (атмосферное) давление; Pм – манометрическое (избыточное) давление; Pв – вакуумметрическое давление. Для замера атмосферного давления используется барометр, для замера избыточного давления – манометр, для замера разряжения - вакуумметр.
 1 бар = 1, 02 кгс/см 2=750 мм рт. ст. =10, 2 м вод. ст. 1 мм рт. ст. =133 Па=13, 6 мм вод. ст. 1 мм вод. ст. =9, 8 Па=7, 35 х10 -2 мм. рт. ст. Удельным объемом вещества называется объем, занимаемый 1 кг данного вещества: V – объем вещества, м 3; m – масса вещества, кг. Величина, обратная удельному объему, называется плотностью:
1 бар = 1, 02 кгс/см 2=750 мм рт. ст. =10, 2 м вод. ст. 1 мм рт. ст. =133 Па=13, 6 мм вод. ст. 1 мм вод. ст. =9, 8 Па=7, 35 х10 -2 мм. рт. ст. Удельным объемом вещества называется объем, занимаемый 1 кг данного вещества: V – объем вещества, м 3; m – масса вещества, кг. Величина, обратная удельному объему, называется плотностью:
 В природе существуют только реальные газы, однако для каждого Газа есть область состояния, где реальный газ ведет себя как идеальный, например при высокой температуре и низком давлении. Состояние идеального газа описывается уравнением Клайперона: для 1 кг вещества для m кг вещества где Р – абсолютное давление газа, Па; - удельный объем, м 3/кг; 8314 – удельная газовая постоянная, Дж/(кмоль K); М – молярная масса газа, кг/кмоль; Т – абсолютная температура, K; V – объем газа, м 3; m – масса газа, кг.
В природе существуют только реальные газы, однако для каждого Газа есть область состояния, где реальный газ ведет себя как идеальный, например при высокой температуре и низком давлении. Состояние идеального газа описывается уравнением Клайперона: для 1 кг вещества для m кг вещества где Р – абсолютное давление газа, Па; - удельный объем, м 3/кг; 8314 – удельная газовая постоянная, Дж/(кмоль K); М – молярная масса газа, кг/кмоль; Т – абсолютная температура, K; V – объем газа, м 3; m – масса газа, кг.
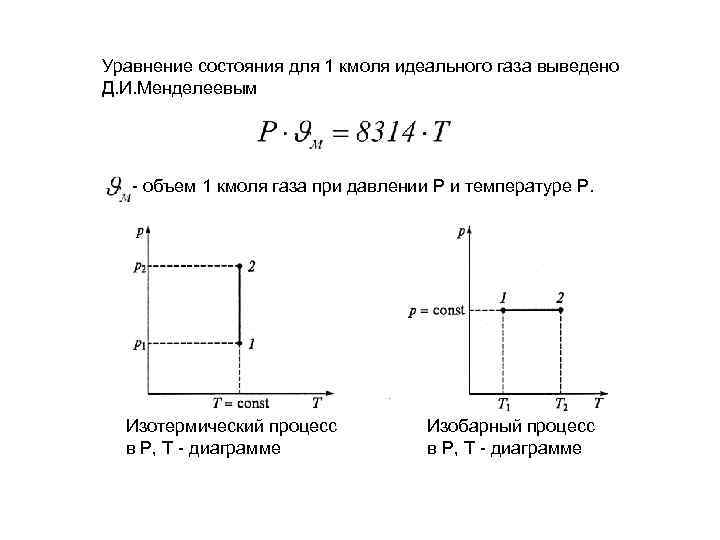 Уравнение состояния для 1 кмоля идеального газа выведено Д. И. Менделеевым - объем 1 кмоля газа при давлении Р и температуре Р. Изотермический процесс в Р, Т - диаграмме Изобарный процесс в Р, Т - диаграмме
Уравнение состояния для 1 кмоля идеального газа выведено Д. И. Менделеевым - объем 1 кмоля газа при давлении Р и температуре Р. Изотермический процесс в Р, Т - диаграмме Изобарный процесс в Р, Т - диаграмме
 Теплота и работа Работа – это энергия, связанная с изменением состояния рабочего тела, с перемещением его во внешнем пространстве или с изменением его положения. Работа является макрофизической формой передачи энергии от одного тела к другому, она характеризуется направленным, упорядоченным движением молекул. Второй способ передачи энергии осуществляется через тепловую энергию (теплоту) Q, Дж. Теплота – часть внутренней энергии тела, которая передается другому телу, имеющему меньшую температуру. Теплота является макрофизической формой передачи энергии от одного тела к другому, Характеризуется хаотическим тепловым движением молекул. Удельная работа газа в изобарном процессе расширения находится из выражения:
Теплота и работа Работа – это энергия, связанная с изменением состояния рабочего тела, с перемещением его во внешнем пространстве или с изменением его положения. Работа является макрофизической формой передачи энергии от одного тела к другому, она характеризуется направленным, упорядоченным движением молекул. Второй способ передачи энергии осуществляется через тепловую энергию (теплоту) Q, Дж. Теплота – часть внутренней энергии тела, которая передается другому телу, имеющему меньшую температуру. Теплота является макрофизической формой передачи энергии от одного тела к другому, Характеризуется хаотическим тепловым движением молекул. Удельная работа газа в изобарном процессе расширения находится из выражения:
 Удельная работа расширения газа в любом термодинамическом процессе рассчитывается по формуле: Энергия термодинамической системы Внутренняя энергия – сумма внутренней кинетической энергии движения молекул и атомов и внутренней потенциальной энергии взаимодействия молекул: Удельная величина внутренней энергии, является параметром состояния рабочего тела: где U – внутренняя энергия, Дж; m – масса тела, кг.
Удельная работа расширения газа в любом термодинамическом процессе рассчитывается по формуле: Энергия термодинамической системы Внутренняя энергия – сумма внутренней кинетической энергии движения молекул и атомов и внутренней потенциальной энергии взаимодействия молекул: Удельная величина внутренней энергии, является параметром состояния рабочего тела: где U – внутренняя энергия, Дж; m – масса тела, кг.
 Энтропия является одним из важнейших параметров состояния тела, который играет большую роль в расчетах термодинамических процессов. Непосредственно измерить энтропию невозможно, она определяется расчетом с помощью дифференциальных уравнений термодинамики по известным параметрам термодинамических свойств. Как правило, при расчете определятся изменение энтропии в процессе: Удельная энтропия s, Дж/(кг K), так же как и внутренняя энергия и удельная энтальпия, является функцией состояния.
Энтропия является одним из важнейших параметров состояния тела, который играет большую роль в расчетах термодинамических процессов. Непосредственно измерить энтропию невозможно, она определяется расчетом с помощью дифференциальных уравнений термодинамики по известным параметрам термодинамических свойств. Как правило, при расчете определятся изменение энтропии в процессе: Удельная энтропия s, Дж/(кг K), так же как и внутренняя энергия и удельная энтальпия, является функцией состояния.
 ВИДЫ ТОПЛИВА И ИХ ОСОБЕННОСТИ
ВИДЫ ТОПЛИВА И ИХ ОСОБЕННОСТИ


 ЭЛЕМЕНТНЫЙ СОСТАВ И ТЕХНИЧЕСКИЕ ХАРАКТЕРИСТИКИ ТОПЛИВА
ЭЛЕМЕНТНЫЙ СОСТАВ И ТЕХНИЧЕСКИЕ ХАРАКТЕРИСТИКИ ТОПЛИВА
 По назначению органическое топливо подразделяется на: - технологическое; - энергетическое. Технологическое - это те виды топлива, которые являются не только источником тепловой энергии, но и используются как компонент технологического процесса. Энергетическое - те виды топлива, которые являются главным образом источником тепловой энергии. Состав топлива Свойства топлива как горючего материала определяются его составом. Чтобы установить состав топлива, производят его технический и химический анализ. При техническом анализе определяют содержание влаги, летучих веществ, золы. Химический (элементный) анализ можно выполнить как по элементному составу, так и определением содержания в топливе определенных химических соединений. Первый метод (по элементному составу) применяют для твердого и жидкого топлива, второй - для газообразного.
По назначению органическое топливо подразделяется на: - технологическое; - энергетическое. Технологическое - это те виды топлива, которые являются не только источником тепловой энергии, но и используются как компонент технологического процесса. Энергетическое - те виды топлива, которые являются главным образом источником тепловой энергии. Состав топлива Свойства топлива как горючего материала определяются его составом. Чтобы установить состав топлива, производят его технический и химический анализ. При техническом анализе определяют содержание влаги, летучих веществ, золы. Химический (элементный) анализ можно выполнить как по элементному составу, так и определением содержания в топливе определенных химических соединений. Первый метод (по элементному составу) применяют для твердого и жидкого топлива, второй - для газообразного.
 СОСТАВ ТВЕРДОГО И ЖИДКОГО ТОПЛИВА Жидкое и твердое топлива принято характеризовать так называемым элементным составом, определяемым в лаборатории. В состав всех видов топлив входят: - углерод (С); - водород (Н); - кислород (О); - азот (N); - сера (S); - минеральная часть – зола (А); - влага (W). В соответствии с анализом различают: - органическую массу (о); горючую массу (г); сухую массу (с); рабочее топливо (р).
СОСТАВ ТВЕРДОГО И ЖИДКОГО ТОПЛИВА Жидкое и твердое топлива принято характеризовать так называемым элементным составом, определяемым в лаборатории. В состав всех видов топлив входят: - углерод (С); - водород (Н); - кислород (О); - азот (N); - сера (S); - минеральная часть – зола (А); - влага (W). В соответствии с анализом различают: - органическую массу (о); горючую массу (г); сухую массу (с); рабочее топливо (р).
 Элементный состав топлива Элементы топлива Индекс С H O N S летучая S орг. А W S колч. о г с р Сера в топливе может находиться в виде различных соединений: органических соединений So, колчедана Sк и сернистых солей в виде сульфатов Ca. SO 4, Fe. SO 4 и др. Органическая и колчеданная сера могут гореть и их объединяют в летучую серу Sк + So = Sл. Сульфаты не горят и являются балластом топлива.
Элементный состав топлива Элементы топлива Индекс С H O N S летучая S орг. А W S колч. о г с р Сера в топливе может находиться в виде различных соединений: органических соединений So, колчедана Sк и сернистых солей в виде сульфатов Ca. SO 4, Fe. SO 4 и др. Органическая и колчеданная сера могут гореть и их объединяют в летучую серу Sк + So = Sл. Сульфаты не горят и являются балластом топлива.
 Минеральная часть в процессе сгорания не участвует и полностью переходит в золу. Она состоит из солей алюминия Al, кремния Si и кальция Ca. Влагу различают : - гигроскопичную (химически связанную); внешнюю (удерживается в топливе механически, при сушке испаряется).
Минеральная часть в процессе сгорания не участвует и полностью переходит в золу. Она состоит из солей алюминия Al, кремния Si и кальция Ca. Влагу различают : - гигроскопичную (химически связанную); внешнюю (удерживается в топливе механически, при сушке испаряется).










 Влага Относится к внешнему балласту, снижает содержание горючих элементов, снижает тепловую ценность топлива. На 1 кг влаги расходуется 2, 51 МДж/кг. Состав газообразного топлива Газообразное топливо представляет собой простую механическую смесь горючих и негорючих газов. Горючими элементами газообразного топлива являются: СH 4, Cm. Hn, H 2 S, CO. Негорючие элементы: O 2, N 2, CO 2, H 2 O. CH 4 + H 2 + Cm. Hn +H 2 S + CO 2 + N 2 = 100 % (по объему)
Влага Относится к внешнему балласту, снижает содержание горючих элементов, снижает тепловую ценность топлива. На 1 кг влаги расходуется 2, 51 МДж/кг. Состав газообразного топлива Газообразное топливо представляет собой простую механическую смесь горючих и негорючих газов. Горючими элементами газообразного топлива являются: СH 4, Cm. Hn, H 2 S, CO. Негорючие элементы: O 2, N 2, CO 2, H 2 O. CH 4 + H 2 + Cm. Hn +H 2 S + CO 2 + N 2 = 100 % (по объему)
 Теплота сгорания топлива (теплотворная способность) Является важнейшей характеристикой топлива. Она определяет тепловую ценность топлива. Теплота сгорания топлива - количество теплоты, которое выделяется при полном сгорании 1 кг твердого или жидкого топлива или 1 м 3 газообразного топлива. Различают: высшую и низшую теплоту сгорания. Так как в топливе содержится водород, то в продуктах сгорания будут присутствовать водяные пары. Если продукты сгорания охладить и сконденсировать водяные пары, то выделившуюся при этом теплоту можно полезно использовать. Высшей теплотой сгорания называется теплота, выделившаяся при полном сгорании топлива, включая теплоту конденсации паров воды, имеющейся в топливе и образующейся в процессе горения (окисления). Низшая теплота сгорания не учитывает теплоты конденсации водяных паров.
Теплота сгорания топлива (теплотворная способность) Является важнейшей характеристикой топлива. Она определяет тепловую ценность топлива. Теплота сгорания топлива - количество теплоты, которое выделяется при полном сгорании 1 кг твердого или жидкого топлива или 1 м 3 газообразного топлива. Различают: высшую и низшую теплоту сгорания. Так как в топливе содержится водород, то в продуктах сгорания будут присутствовать водяные пары. Если продукты сгорания охладить и сконденсировать водяные пары, то выделившуюся при этом теплоту можно полезно использовать. Высшей теплотой сгорания называется теплота, выделившаяся при полном сгорании топлива, включая теплоту конденсации паров воды, имеющейся в топливе и образующейся в процессе горения (окисления). Низшая теплота сгорания не учитывает теплоты конденсации водяных паров.
 Теплота сгорания может быть вычислена по формуле Д. И. Менделеева: - для твердого и жидкого топлива ( % по массе, [к. Дж/кг]) QPH = 339, 5 CP +1256 HP - 25, 8 (9 HP + WP) - 109 ( OP - SPЛ) - для газообразного топлива (% по объему, [к. Дж/м 3] ) QPH = 127 CO + 108 H 2 + 358 CH 4 +234 H 2 S +590 C 2 H 4 + 638 C 2 H 6 + + 913 C 3 H 8 +…+ 1187 C 4 H 10 +1465 C 5 H 12 … Для сравнения тепловой ценности различных топлив используют понятие условного топлива, под которым принимают топливо с теплотой сгорания 7000 ккал/кг = 29350 к. Дж/кг.
Теплота сгорания может быть вычислена по формуле Д. И. Менделеева: - для твердого и жидкого топлива ( % по массе, [к. Дж/кг]) QPH = 339, 5 CP +1256 HP - 25, 8 (9 HP + WP) - 109 ( OP - SPЛ) - для газообразного топлива (% по объему, [к. Дж/м 3] ) QPH = 127 CO + 108 H 2 + 358 CH 4 +234 H 2 S +590 C 2 H 4 + 638 C 2 H 6 + + 913 C 3 H 8 +…+ 1187 C 4 H 10 +1465 C 5 H 12 … Для сравнения тепловой ценности различных топлив используют понятие условного топлива, под которым принимают топливо с теплотой сгорания 7000 ккал/кг = 29350 к. Дж/кг.
 Горение топлива Горение - сложный физико-химический процесс взаимодействия топлива с окислителем, протекающий при высоких температурах и сопровождающийся интенсивным выделением теплоты. Чаще всего в качестве окислителя используется кислород атмосферного воздуха. Для обеспечения непрерывного и устойчивого горения необходимы следующие физические условия: - бесперебойный подвод топлива и окислителя в зону горения; - непрерывное и интенсивное их перемешивание; - подогрев топлива до температуры воспламенения; - подогрев воздуха; - непрерывный отвод продуктов сгорания из зоны горения; - поддержание высокой температуры в зоне горения и т. д.
Горение топлива Горение - сложный физико-химический процесс взаимодействия топлива с окислителем, протекающий при высоких температурах и сопровождающийся интенсивным выделением теплоты. Чаще всего в качестве окислителя используется кислород атмосферного воздуха. Для обеспечения непрерывного и устойчивого горения необходимы следующие физические условия: - бесперебойный подвод топлива и окислителя в зону горения; - непрерывное и интенсивное их перемешивание; - подогрев топлива до температуры воспламенения; - подогрев воздуха; - непрерывный отвод продуктов сгорания из зоны горения; - поддержание высокой температуры в зоне горения и т. д.
 Поэтому горение топлива в технологических устройствах не чисто химический процесс окисления, а сложный физико-химический процесс. В зависимости от агрегатного состояния топлива и окислителя различают: - гомогенное горение; - гетерогенное горение. Если топливо и окислитель находятся в одинаковых фазовых состояниях, то горение называется гомогенным. Если топливо и окислитель находятся в разных фазовых состояниях – горение гетерогенное.
Поэтому горение топлива в технологических устройствах не чисто химический процесс окисления, а сложный физико-химический процесс. В зависимости от агрегатного состояния топлива и окислителя различают: - гомогенное горение; - гетерогенное горение. Если топливо и окислитель находятся в одинаковых фазовых состояниях, то горение называется гомогенным. Если топливо и окислитель находятся в разных фазовых состояниях – горение гетерогенное.
 При полном сгорании выделяется максимальное количество теплоты; при неполном - количество теплоты меньше, т. е. имеют место потери теплоты от химической неполноты сгорания. При полном сгорании углерода (1 кг); С + О 2 = СО 2 + 33600 к. Дж/кг; при неполном сгорании углерода : С +1/2 О 2 = СО + 9900 к. Дж/кг. Расчеты горения топлива Расчеты выполняют с целью определения: - количества необходимого для горения воздуха; - количества и состава продуктов сгорания; - температуры горения. Количество воздуха для горения - теоретическое необходимое количество воздуха; - действительное необходимое количество воздуха.
При полном сгорании выделяется максимальное количество теплоты; при неполном - количество теплоты меньше, т. е. имеют место потери теплоты от химической неполноты сгорания. При полном сгорании углерода (1 кг); С + О 2 = СО 2 + 33600 к. Дж/кг; при неполном сгорании углерода : С +1/2 О 2 = СО + 9900 к. Дж/кг. Расчеты горения топлива Расчеты выполняют с целью определения: - количества необходимого для горения воздуха; - количества и состава продуктов сгорания; - температуры горения. Количество воздуха для горения - теоретическое необходимое количество воздуха; - действительное необходимое количество воздуха.
 Под теоретически необходимым понимают то минимальное количество воздуха, которое требуется для полного окисления всех горючих элементов топлива. Его определяют из стахиометрических реакций окисления горючих элементов топлива. [ l 0 ] = [ кг воздуха/ кг топлива ], [ V 0 ] = [ м 3 воздуха / кг топлива]. Если обозначить G 0 массовое количество О 2, необходимое для окисления всех горючих элементов 1 кг топлива, то l 0 можно определить из выражения: l 0 = G 0 / 0, 232 , где 0, 232 - массовая доля О 2 в воздухе. V 0 = l 0 / 1, 293 , где 1, 293 кг/м 3 - плотность воздуха при нормальных условиях. CP + HP + SPЛ + OP + NP + AP + WP = 100 G 0 = G 0 C + G 0 H + G 0 S - G 00 ,
Под теоретически необходимым понимают то минимальное количество воздуха, которое требуется для полного окисления всех горючих элементов топлива. Его определяют из стахиометрических реакций окисления горючих элементов топлива. [ l 0 ] = [ кг воздуха/ кг топлива ], [ V 0 ] = [ м 3 воздуха / кг топлива]. Если обозначить G 0 массовое количество О 2, необходимое для окисления всех горючих элементов 1 кг топлива, то l 0 можно определить из выражения: l 0 = G 0 / 0, 232 , где 0, 232 - массовая доля О 2 в воздухе. V 0 = l 0 / 1, 293 , где 1, 293 кг/м 3 - плотность воздуха при нормальных условиях. CP + HP + SPЛ + OP + NP + AP + WP = 100 G 0 = G 0 C + G 0 H + G 0 S - G 00 ,
 Обозначим через GO C, H, S массовые количества воздуха, необходимые для окисления соответственно углерода ( C), водорода (Н) , серы ( S ), а через GOO массовое количество кислорода, содержащегося в топливе, то GO = GOC + GOH + GOS - GOO Реакция окисления углерода : С + О 2 = СО 2 1 моль С + 1 моль О 2 = 1 моль СО 2 12 кг С + 32 кг О 2 = 44 кг СО 2 1 кг С + 32/12 кг О 2 = 44/12 кг СО 2 1 кг С + 2, 67 кг О 2 = 3, 67 кг СО 2
Обозначим через GO C, H, S массовые количества воздуха, необходимые для окисления соответственно углерода ( C), водорода (Н) , серы ( S ), а через GOO массовое количество кислорода, содержащегося в топливе, то GO = GOC + GOH + GOS - GOO Реакция окисления углерода : С + О 2 = СО 2 1 моль С + 1 моль О 2 = 1 моль СО 2 12 кг С + 32 кг О 2 = 44 кг СО 2 1 кг С + 32/12 кг О 2 = 44/12 кг СО 2 1 кг С + 2, 67 кг О 2 = 3, 67 кг СО 2
 Реакция окисления водорода Н 2 + 1/2 О 2 = Н 2 О 2 кг Н 2 + 16 кг О 2 = 18 кг Н 2 О 1 кг Н 2 + 8 кг О 2 = 9 кг Н 2 О Реакция окисления серы S + O 2 = SO 2 32 кг S + 32 кг O 2 = 64 кг SO 2 1 кг S + 1 кг O 2 = 2 кг SO 2
Реакция окисления водорода Н 2 + 1/2 О 2 = Н 2 О 2 кг Н 2 + 16 кг О 2 = 18 кг Н 2 О 1 кг Н 2 + 8 кг О 2 = 9 кг Н 2 О Реакция окисления серы S + O 2 = SO 2 32 кг S + 32 кг O 2 = 64 кг SO 2 1 кг S + 1 кг O 2 = 2 кг SO 2
 С учетом того, что l 0 = G 0 / 0, 232 , можно записать l 0 = 0, 115 CP + 0, 345 HP + 0, 043 ( SPЛ - ОР) кг воздуха / кг топлива V 0 = l 0 / 1, 293 = 0, 081 CP + 0, 266 HP + 0, 033 ( SPЛ - ОР) м 3 воздуха / кг топлива Рассуждая аналогично, для газообразного топлива можно получить V 0 = 0, 476 [ 0, 5 (CO + H 2) + 1, 5 H 2 S + (m + n / 4) Cm. Hn - O 2 ] м 3 воздуха / м 3 топлива
С учетом того, что l 0 = G 0 / 0, 232 , можно записать l 0 = 0, 115 CP + 0, 345 HP + 0, 043 ( SPЛ - ОР) кг воздуха / кг топлива V 0 = l 0 / 1, 293 = 0, 081 CP + 0, 266 HP + 0, 033 ( SPЛ - ОР) м 3 воздуха / кг топлива Рассуждая аналогично, для газообразного топлива можно получить V 0 = 0, 476 [ 0, 5 (CO + H 2) + 1, 5 H 2 S + (m + n / 4) Cm. Hn - O 2 ] м 3 воздуха / м 3 топлива
 ДЕЙСТВИТЕЛЬНОЕ КОЛИЧЕСТВО ВОЗДУХА Подача в топки и камеры сгорания воздуха в теоретически необходимом количестве практически не обеспечивает полноты сгорания топлива. Поэтому фактически в камеру сгорания воздуха подают больше, чем это требуется теоретически. Этот избыток воздуха характеризуется коэффициентом избытка воздуха, под которым понимают отношение действительно поданного количества воздуха к теоретически необходимому, т. е. С увеличением коэффициента избытка воздуха происходит увеличение потерь теплоты с продуктами сгорания топлива, т. к. увеличивается их количество. Кроме того, затрачиваетса определенное количество теплоты на нагрев избытка воздуха до температуры горения.
ДЕЙСТВИТЕЛЬНОЕ КОЛИЧЕСТВО ВОЗДУХА Подача в топки и камеры сгорания воздуха в теоретически необходимом количестве практически не обеспечивает полноты сгорания топлива. Поэтому фактически в камеру сгорания воздуха подают больше, чем это требуется теоретически. Этот избыток воздуха характеризуется коэффициентом избытка воздуха, под которым понимают отношение действительно поданного количества воздуха к теоретически необходимому, т. е. С увеличением коэффициента избытка воздуха происходит увеличение потерь теплоты с продуктами сгорания топлива, т. к. увеличивается их количество. Кроме того, затрачиваетса определенное количество теплоты на нагрев избытка воздуха до температуры горения.
 С уменьшением возрастают потери теплоты от химической неполноты сгорания топлива. Поэтому оптимизация является технико - экономической задачей и зависит от вида топлива, типа камеры сгорания, ее объема и т. д. При проектировании топливо-сжигающего устройства коэффициент избытка воздуха принимается согласно установленным нормам. При эксплуатации определяется экспериментально. = 1, 05… 1, 2 - для топок, где сжигается газ или мазут; = 1, 1… 1, 3 - для газовых двигателей; = 0, 8… 1, 1 - для карбюраторных двигателей; = 1, 2… 2, 0 - для дизельных двигателей; = 4… 8 - для газотурбинных установок.
С уменьшением возрастают потери теплоты от химической неполноты сгорания топлива. Поэтому оптимизация является технико - экономической задачей и зависит от вида топлива, типа камеры сгорания, ее объема и т. д. При проектировании топливо-сжигающего устройства коэффициент избытка воздуха принимается согласно установленным нормам. При эксплуатации определяется экспериментально. = 1, 05… 1, 2 - для топок, где сжигается газ или мазут; = 1, 1… 1, 3 - для газовых двигателей; = 0, 8… 1, 1 - для карбюраторных двигателей; = 1, 2… 2, 0 - для дизельных двигателей; = 4… 8 - для газотурбинных установок.
 СОСТАВ И КОЛИЧЕСТВО ПРОДУКТОВ СГОРАНИЯ В топках, камерах сгорания различных устройств практически всегда имеет место неполное сгорание топлива. Причиной этого может быть: недостаток воздуха ( 1); плохое перемешивание топлива с воздухом, даже когда 1; недостаточный объем топочного устройства; низкий температурный уровень в зоне горения. При неполном сгорании могут образовываться следующие продукты: СО, Н 2, H 2 S, Cm. Hn. Состав продуктов неполного сгорания: CO 2 + H 2 O + SO 2 + CO + H 2 S + Cm. Hn + O 2 + N 2 = 100%. Состав продуктов полного сгорания: CO 2 + H 2 O + SO 2 + N 2 = 100%.
СОСТАВ И КОЛИЧЕСТВО ПРОДУКТОВ СГОРАНИЯ В топках, камерах сгорания различных устройств практически всегда имеет место неполное сгорание топлива. Причиной этого может быть: недостаток воздуха ( 1); плохое перемешивание топлива с воздухом, даже когда 1; недостаточный объем топочного устройства; низкий температурный уровень в зоне горения. При неполном сгорании могут образовываться следующие продукты: СО, Н 2, H 2 S, Cm. Hn. Состав продуктов неполного сгорания: CO 2 + H 2 O + SO 2 + CO + H 2 S + Cm. Hn + O 2 + N 2 = 100%. Состав продуктов полного сгорания: CO 2 + H 2 O + SO 2 + N 2 = 100%.
 Массовое количествогазообразных подуктов сгорания выражается суммой сжигаемого топлива и количества воздуха, подаваемого на его сжигание. Mпс = 1 + 0 1 кг продуктов сгорания / 1 кг топлива. Объемное количество продуктов сгорания принято выражать как сумму сухих газов и водяных паров. Vпс = Vсг + Vн 2 о м 3/м 3 продуктов сгорания Vсг = Vco 2 + Vso 2 + Vo N 2 + Vв Vco 2 + Vso 2 = VRO 2 Vпс = VRO 2 + Vo N 2 + Vв + Vн 2 о
Массовое количествогазообразных подуктов сгорания выражается суммой сжигаемого топлива и количества воздуха, подаваемого на его сжигание. Mпс = 1 + 0 1 кг продуктов сгорания / 1 кг топлива. Объемное количество продуктов сгорания принято выражать как сумму сухих газов и водяных паров. Vпс = Vсг + Vн 2 о м 3/м 3 продуктов сгорания Vсг = Vco 2 + Vso 2 + Vo N 2 + Vв Vco 2 + Vso 2 = VRO 2 Vпс = VRO 2 + Vo N 2 + Vв + Vн 2 о
 Составляющие этого уравнения определяются по стехеометрическим реакциям горения аналогично определению теоретически необходимого количества воздуха. Для твердых и жидких топлив VRO 2 = 0, 01866 (Cp + 0, 375 Sp. Л) м 3/кг Vo N 2 = 0, 79 Vo + 0, 008 N 2 p Vн 2 о = 0, 111 Hp + 0, 0124 Wp + 0, 0161 Vo Vв = ( - 1) Vo
Составляющие этого уравнения определяются по стехеометрическим реакциям горения аналогично определению теоретически необходимого количества воздуха. Для твердых и жидких топлив VRO 2 = 0, 01866 (Cp + 0, 375 Sp. Л) м 3/кг Vo N 2 = 0, 79 Vo + 0, 008 N 2 p Vн 2 о = 0, 111 Hp + 0, 0124 Wp + 0, 0161 Vo Vв = ( - 1) Vo
 Для газообразного топлива: VRO 2 = 0, 01 ( СО + + H 2 S + CO 2 м 3/м 3 Vo N 2 = 0, 79 Vo + 0, 01 Np 2 Vн 2 о = 0, 01 ( H 2 + + H 2 S) + 0, 0161 Vo Vв = ( - 1) Vo
Для газообразного топлива: VRO 2 = 0, 01 ( СО + + H 2 S + CO 2 м 3/м 3 Vo N 2 = 0, 79 Vo + 0, 01 Np 2 Vн 2 о = 0, 01 ( H 2 + + H 2 S) + 0, 0161 Vo Vв = ( - 1) Vo
 ОПРЕДЕЛЕНИЕ ЭНТАЛЬПИИ ПРОДУКТОВ СГОРАНИЯ Энтальпию продуктов сгорания определяют всегда на единицу количества топлива и вычисляют по формуле: h пс= Mпс Cpпс toпс = Vпс C’pпс toпс где Mпс - массовое количество продуктов сгорания, кг/кг или кг/м 3; Vпс - объем продуктов сгорания, м 3/кг или м 3/м 3; Cpпс - удельная массовая теплоемкость продуктов сгорания, Дж/(кг град); toпс - температура продуктов сгорания, 0 C; C’pпс - удельная объемная теплоемкость продуктов сгорания, Дж /(кг град); Cpпс = C’p. СО 2 VRO 2/ Vпс +Cp. N 2 Vo N 2/ Vпс + C’p H 2 O VH 2 O/ Vпс +… + C’pв Vв/ Vпс hпс = (C’p. СО 2 VRO 2 +Cp. N 2 Vo N 2 + … + Cp. H 2 O VH 2 O + C’pв Vв) toпс
ОПРЕДЕЛЕНИЕ ЭНТАЛЬПИИ ПРОДУКТОВ СГОРАНИЯ Энтальпию продуктов сгорания определяют всегда на единицу количества топлива и вычисляют по формуле: h пс= Mпс Cpпс toпс = Vпс C’pпс toпс где Mпс - массовое количество продуктов сгорания, кг/кг или кг/м 3; Vпс - объем продуктов сгорания, м 3/кг или м 3/м 3; Cpпс - удельная массовая теплоемкость продуктов сгорания, Дж/(кг град); toпс - температура продуктов сгорания, 0 C; C’pпс - удельная объемная теплоемкость продуктов сгорания, Дж /(кг град); Cpпс = C’p. СО 2 VRO 2/ Vпс +Cp. N 2 Vo N 2/ Vпс + C’p H 2 O VH 2 O/ Vпс +… + C’pв Vв/ Vпс hпс = (C’p. СО 2 VRO 2 +Cp. N 2 Vo N 2 + … + Cp. H 2 O VH 2 O + C’pв Vв) toпс
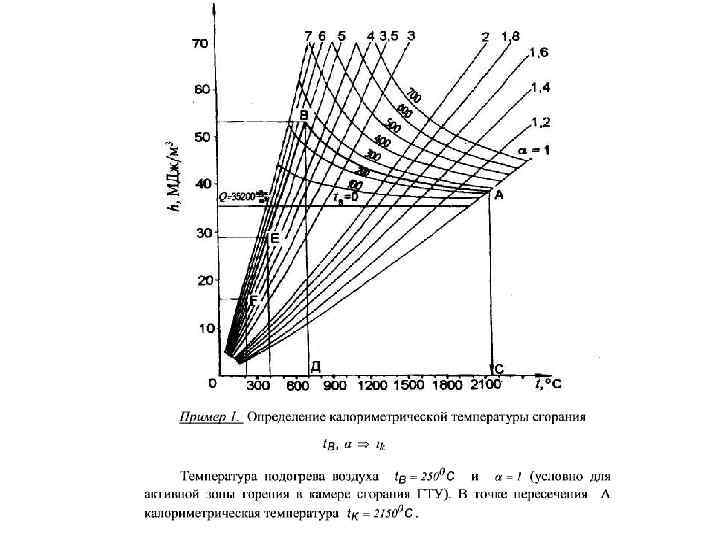
 ОПРЕДЕЛЕНИЕ ТЕМПЕРАТУРЫ СГОРАНИЯ Различают: - калориметрическую; - теоретическую; - действительную температуру сгорания. Калориметрической называют температуру, до которой нагрелись бы продукты полного сгорания, если бы вся теплота топлива и воздуха пошла на нагревание газов. Для этого случая тепловой баланс камеры сгорания: Qp. H + h. T + h. В = Vпс Cpпс tk, h. T - энтальпия топлива.
ОПРЕДЕЛЕНИЕ ТЕМПЕРАТУРЫ СГОРАНИЯ Различают: - калориметрическую; - теоретическую; - действительную температуру сгорания. Калориметрической называют температуру, до которой нагрелись бы продукты полного сгорания, если бы вся теплота топлива и воздуха пошла на нагревание газов. Для этого случая тепловой баланс камеры сгорания: Qp. H + h. T + h. В = Vпс Cpпс tk, h. T - энтальпия топлива.
 h. В - энтальпия воздуха. tk = (Qp. H + h. T + h. В) / (Vпс Cpпс) - калориметрическая температура сгорания. При расчетах калориметрической температуры воздуха ее находят методом последовательного приближения, т. к. входящая в формулу удельная объемная теплоемкость является функцией температуры. Калориметрическая температура может быть определена с помощью h-t – диаграммы продуктов сгорания.
h. В - энтальпия воздуха. tk = (Qp. H + h. T + h. В) / (Vпс Cpпс) - калориметрическая температура сгорания. При расчетах калориметрической температуры воздуха ее находят методом последовательного приближения, т. к. входящая в формулу удельная объемная теплоемкость является функцией температуры. Калориметрическая температура может быть определена с помощью h-t – диаграммы продуктов сгорания.
 Теоретической называют температуру, до которой нагрелись бы продукты сгорания, если на их нагрев пошла бы вся теплота за вычетом физической (qфиз) и химической (qхим) неполноты сгорания топлива и диссоциации продуктов сгорания. Для этого случая тепловой баланс камеры сгорания: где коэффициент тепловыделения равен - потери теплоты от физической неполноты сгорания, %; - потери теплоты от химической неполноты сгорания, %. - теоретическая температура
Теоретической называют температуру, до которой нагрелись бы продукты сгорания, если на их нагрев пошла бы вся теплота за вычетом физической (qфиз) и химической (qхим) неполноты сгорания топлива и диссоциации продуктов сгорания. Для этого случая тепловой баланс камеры сгорания: где коэффициент тепловыделения равен - потери теплоты от физической неполноты сгорания, %; - потери теплоты от химической неполноты сгорания, %. - теоретическая температура
 Действительная температура – температура, учитывающая все потери теплоты (на физическую и химическую неполноту и потери в окружающую среду). Значение действительной температуры может быть определено путем сложных вычислений с учетом теплопередачи. h – t - диаграмма продуктов сгорания При проектировании и эксплуатации теплоиспользующих установок приходится выполнять множество расчетов, связанных с процессом горения топлива в зависимости от коэффициента избытка воздуха, степени подогрева топлива и воздуха, типа форсунки и т. д. Эти расчеты значительно упрощаются при использовании h – t диаграммы продуктов сгорания типичных топлив.
Действительная температура – температура, учитывающая все потери теплоты (на физическую и химическую неполноту и потери в окружающую среду). Значение действительной температуры может быть определено путем сложных вычислений с учетом теплопередачи. h – t - диаграмма продуктов сгорания При проектировании и эксплуатации теплоиспользующих установок приходится выполнять множество расчетов, связанных с процессом горения топлива в зависимости от коэффициента избытка воздуха, степени подогрева топлива и воздуха, типа форсунки и т. д. Эти расчеты значительно упрощаются при использовании h – t диаграммы продуктов сгорания типичных топлив.
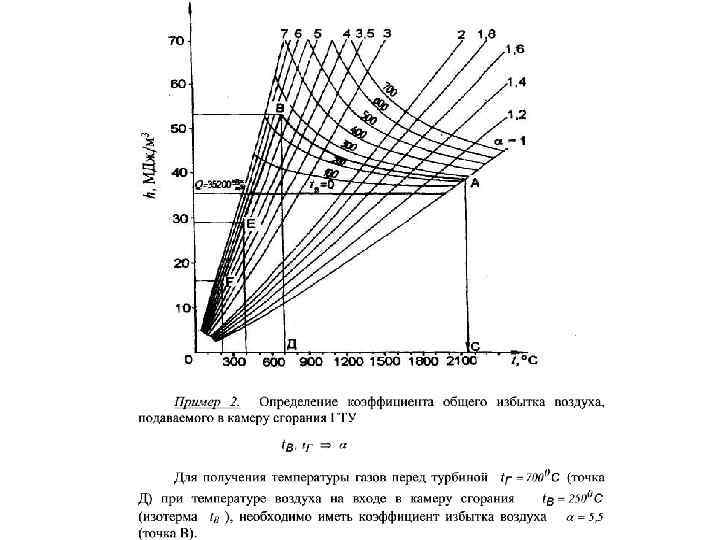
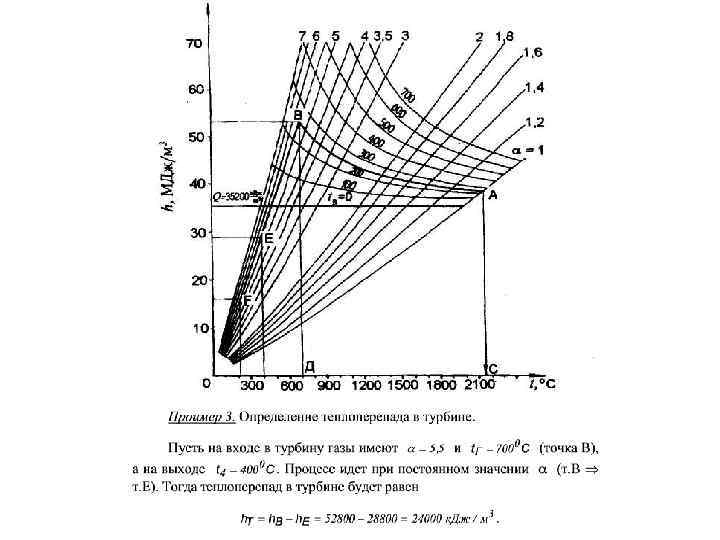
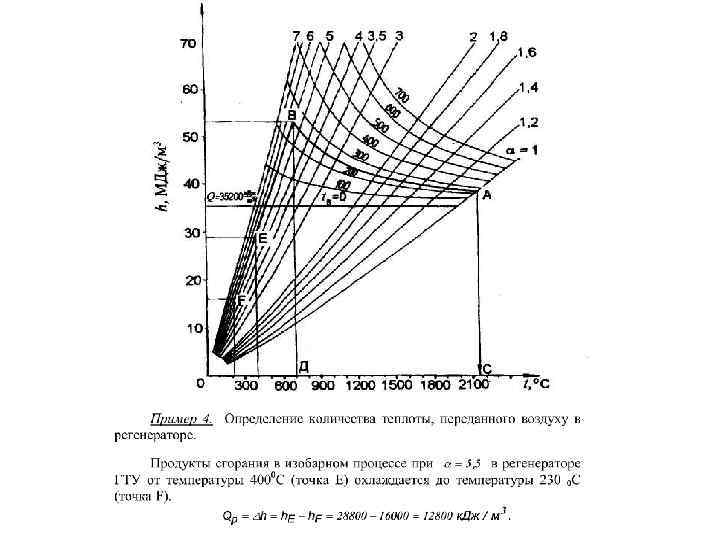
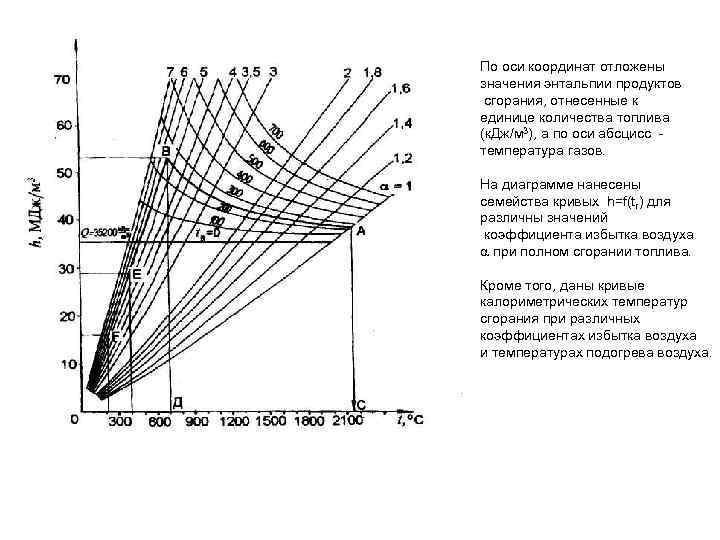 По оси координат отложены значения энтальпии продуктов сгорания, отнесенные к единице количества топлива (к. Дж/м 3), а по оси абсцисс температура газов. На диаграмме нанесены семейства кривых h=f(tг) для различны значений коэффициента избытка воздуха при полном сгорании топлива. Кроме того, даны кривые калориметрических температур сгорания при различных коэффициентах избытка воздуха и температурах подогрева воздуха.
По оси координат отложены значения энтальпии продуктов сгорания, отнесенные к единице количества топлива (к. Дж/м 3), а по оси абсцисс температура газов. На диаграмме нанесены семейства кривых h=f(tг) для различны значений коэффициента избытка воздуха при полном сгорании топлива. Кроме того, даны кривые калориметрических температур сгорания при различных коэффициентах избытка воздуха и температурах подогрева воздуха.