Л2_КИСЛОТЫ.ppt
- Количество слайдов: 32
 Основные термины Химические реакции in vitro in vivo вне организма, в организме в колбе Метаболизм (обмен веществ) – совокупность химических реакций в живом организме. Метаболиты – вещества, образующиеся в процессе метаболизма. Ксенобиотики – чужеродные для организма вещества, вызывающие нарушение биологических процессов.
Основные термины Химические реакции in vitro in vivo вне организма, в организме в колбе Метаболизм (обмен веществ) – совокупность химических реакций в живом организме. Метаболиты – вещества, образующиеся в процессе метаболизма. Ксенобиотики – чужеродные для организма вещества, вызывающие нарушение биологических процессов.
 Метаболизм катаболизм реакции распада веществ анаболизм реакции синтеза веществ Ферменты (энзимы) – это белки-катализаторы Коферменты (коэнзимы) – это низкомолекулярные органические вещества различного строения, связаны с ферментами и необходимы для осуществления каталитической функции ферментов. Коферменты могут быть самостоятельными биокатализаторами.
Метаболизм катаболизм реакции распада веществ анаболизм реакции синтеза веществ Ферменты (энзимы) – это белки-катализаторы Коферменты (коэнзимы) – это низкомолекулярные органические вещества различного строения, связаны с ферментами и необходимы для осуществления каталитической функции ферментов. Коферменты могут быть самостоятельными биокатализаторами.
 КАРБОНОВЫЕ КИСЛОТЫ
КАРБОНОВЫЕ КИСЛОТЫ
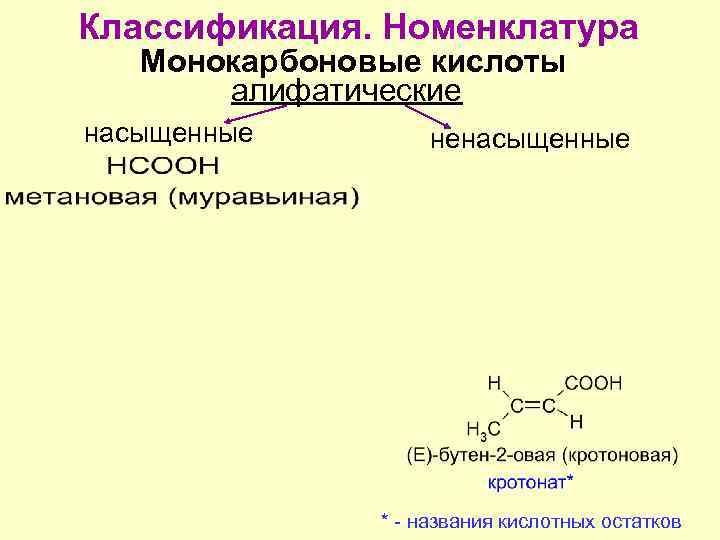 Классификация. Номенклатура Монокарбоновые кислоты алифатические насыщенные ненасыщенные * - названия кислотных остатков
Классификация. Номенклатура Монокарбоновые кислоты алифатические насыщенные ненасыщенные * - названия кислотных остатков
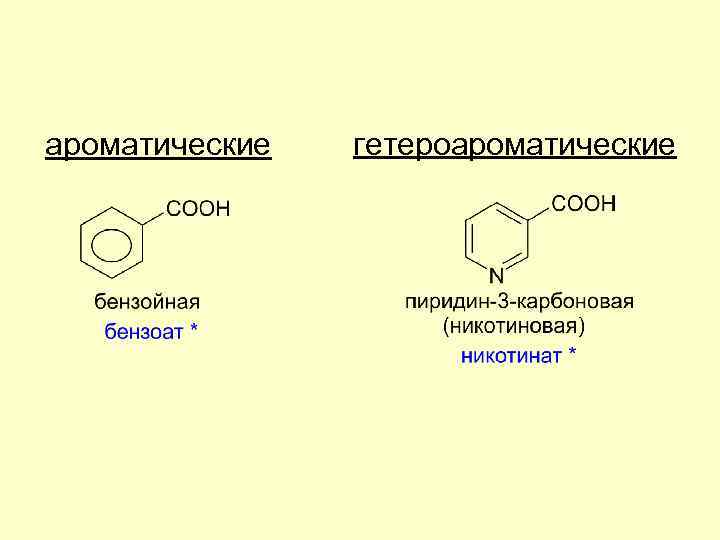 ароматические гетероароматические
ароматические гетероароматические
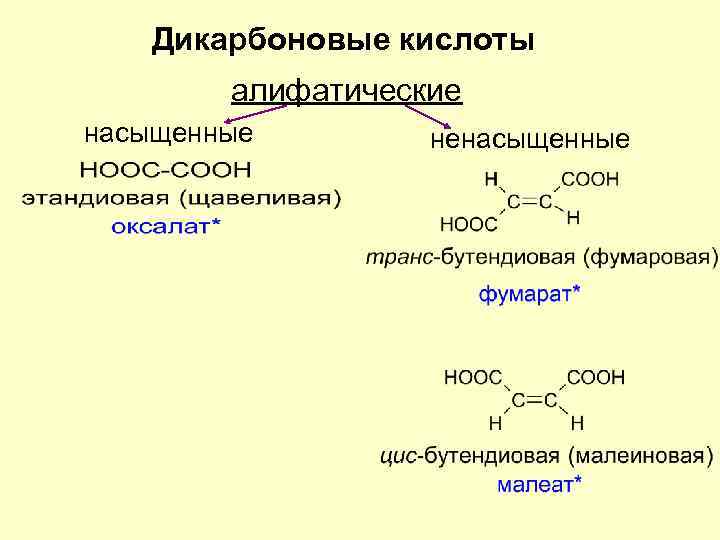 Дикарбоновые кислоты алифатические насыщенные ненасыщенные
Дикарбоновые кислоты алифатические насыщенные ненасыщенные
 Физические свойства Монокарбоновые кислоты (С 1 -С 9) – б/ц жидкости; ароматические, высшие алифатические и почти все дикарбоновые кислоты – твердые в-ва. Муравьиная, уксусная, пропионовая кислоты имеют резкий запах, вызывают химические ожоги слизистых оболочек; кислоты (С 4 и >) имеют специфичный неприятный запах; высшие моно- и дикарбоновые кислоты запаха не имеют.
Физические свойства Монокарбоновые кислоты (С 1 -С 9) – б/ц жидкости; ароматические, высшие алифатические и почти все дикарбоновые кислоты – твердые в-ва. Муравьиная, уксусная, пропионовая кислоты имеют резкий запах, вызывают химические ожоги слизистых оболочек; кислоты (С 4 и >) имеют специфичный неприятный запах; высшие моно- и дикарбоновые кислоты запаха не имеют.
 Ткип. в гомологическом ряду монокарб. алиф. кислот возрастает; Ткип. монокарб. кислот выше Ткип. соответствующих спиртов и альдегидов (за счет образования прочных ассоциатов). Муравьиная, уксусная, пропионовая кислоты смешиваются с водой во всех соотношениях; в гомологическом ряду моно- и дикарб. кислот растворимость в воде уменьшается; аромат. карб. кислоты в воде растворимы плохо, в этаноле – растворимы лучше.
Ткип. в гомологическом ряду монокарб. алиф. кислот возрастает; Ткип. монокарб. кислот выше Ткип. соответствующих спиртов и альдегидов (за счет образования прочных ассоциатов). Муравьиная, уксусная, пропионовая кислоты смешиваются с водой во всех соотношениях; в гомологическом ряду моно- и дикарб. кислот растворимость в воде уменьшается; аромат. карб. кислоты в воде растворимы плохо, в этаноле – растворимы лучше.
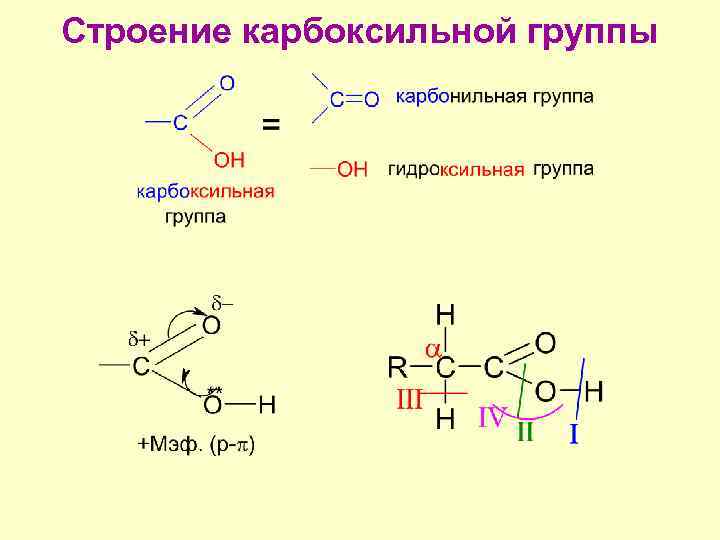 Строение карбоксильной группы
Строение карбоксильной группы
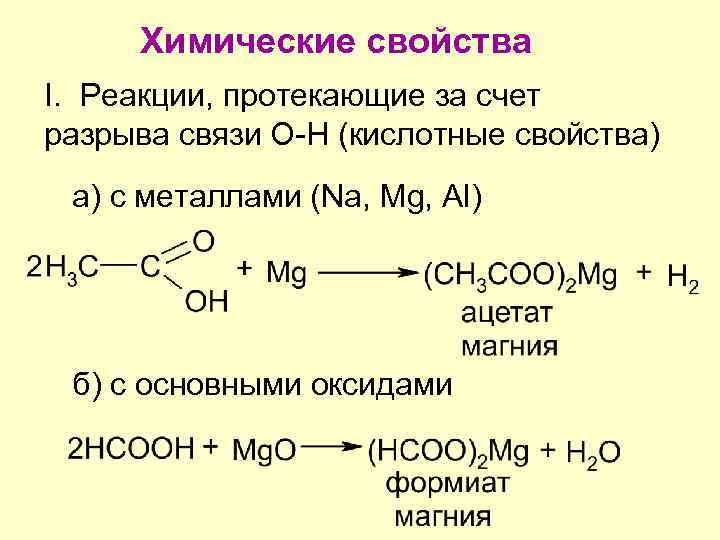 Химические свойства I. Реакции, протекающие за счет разрыва связи О-Н (кислотные свойства) а) с металлами (Na, Mg, Al) б) с основными оксидами
Химические свойства I. Реакции, протекающие за счет разрыва связи О-Н (кислотные свойства) а) с металлами (Na, Mg, Al) б) с основными оксидами
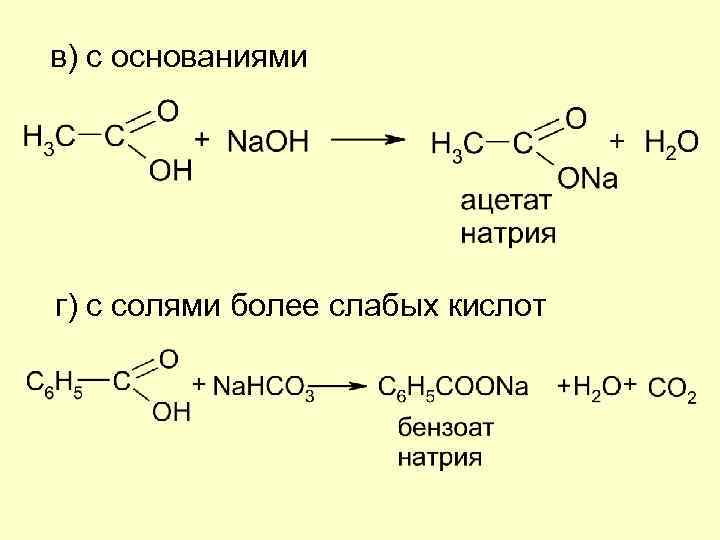 в) с основаниями г) с солями более слабых кислот
в) с основаниями г) с солями более слабых кислот
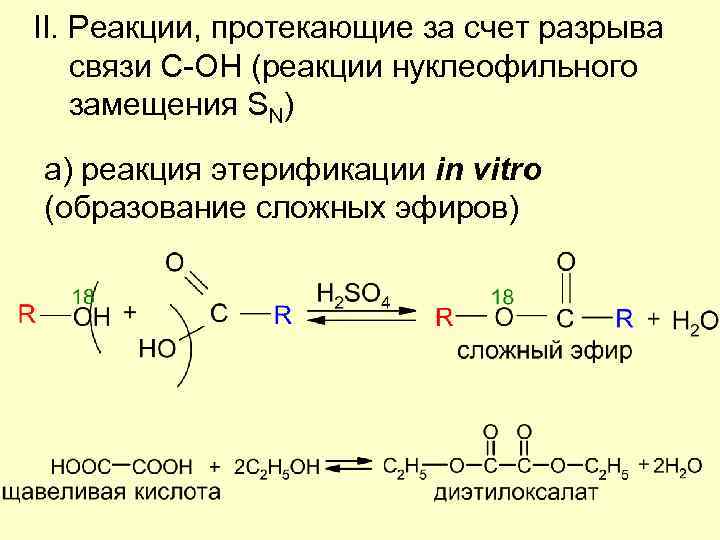 II. Реакции, протекающие за счет разрыва связи С-ОН (реакции нуклеофильного замещения SN) а) реакция этерификации in vitro (образование сложных эфиров)
II. Реакции, протекающие за счет разрыва связи С-ОН (реакции нуклеофильного замещения SN) а) реакция этерификации in vitro (образование сложных эфиров)
 б) образование сложных тиоэфиров (in vivo) Кофермент А (Ко. А-SH) – полифункциональное органическое вещество, которое в организме функционирует в качестве тиоспирта. Ацил-Co. A – это сложные тиоэфиры, содержащие макроэргические связи. - служит переносчиком ацильной группы, т. е. используется для создания новых С, С-связей, что приводит к удлинению углеродной цепи.
б) образование сложных тиоэфиров (in vivo) Кофермент А (Ко. А-SH) – полифункциональное органическое вещество, которое в организме функционирует в качестве тиоспирта. Ацил-Co. A – это сложные тиоэфиры, содержащие макроэргические связи. - служит переносчиком ацильной группы, т. е. используется для создания новых С, С-связей, что приводит к удлинению углеродной цепи.
 в) реакция этерификации in vivo сложные эфиры в организме образуются при взаимодействии спиртов с активированными формами карбоновых кислот - ацилкоферментами А Ацетилхолин – нейромедиатор - посредник при передаче нервного возбуждения в нервных клетках
в) реакция этерификации in vivo сложные эфиры в организме образуются при взаимодействии спиртов с активированными формами карбоновых кислот - ацилкоферментами А Ацетилхолин – нейромедиатор - посредник при передаче нервного возбуждения в нервных клетках
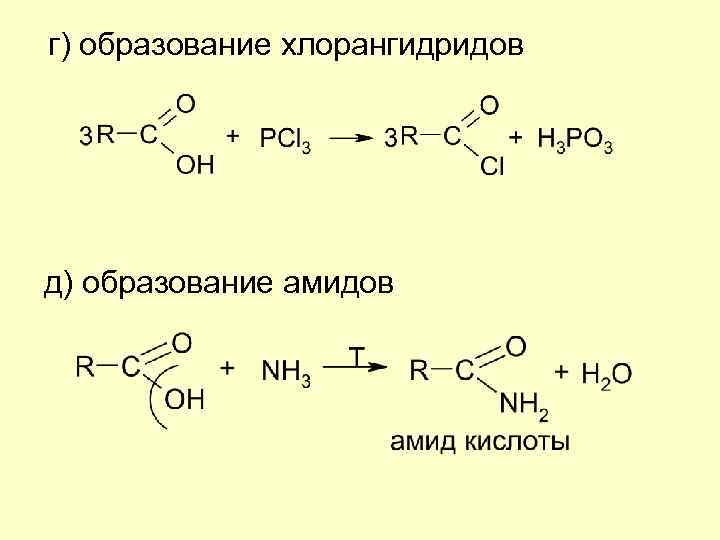 г) образование хлорангидридов д) образование амидов
г) образование хлорангидридов д) образование амидов
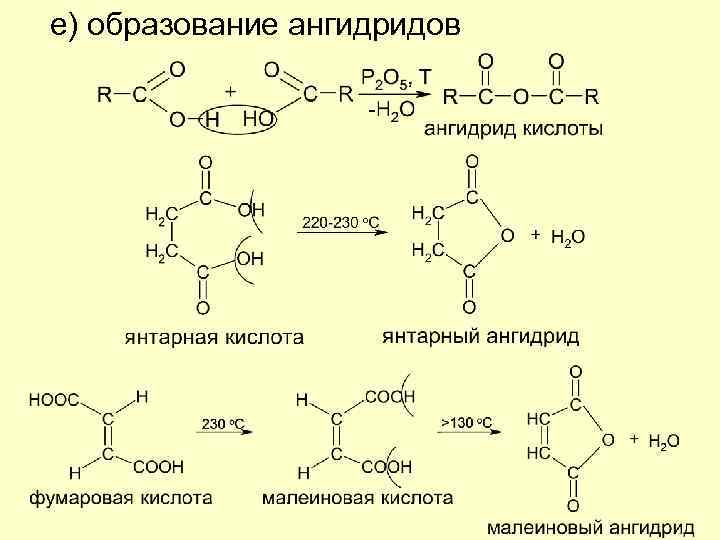 е) образование ангидридов
е) образование ангидридов
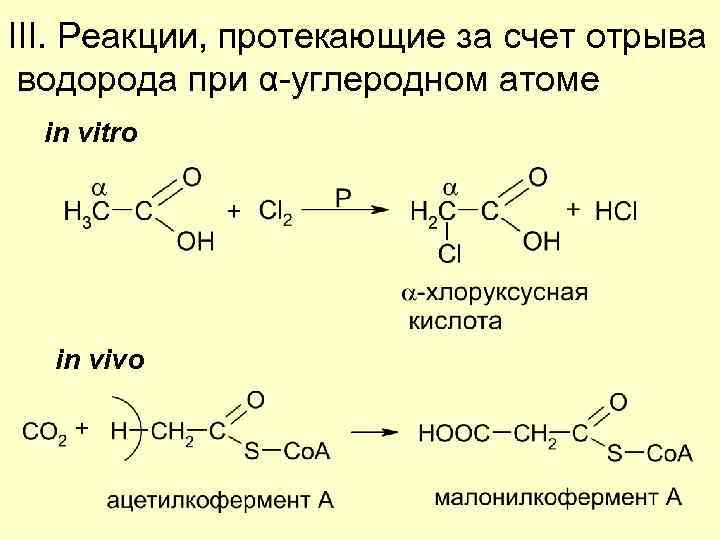 III. Реакции, протекающие за счет отрыва водорода при α-углеродном атоме in vitro in vivo
III. Реакции, протекающие за счет отрыва водорода при α-углеродном атоме in vitro in vivo
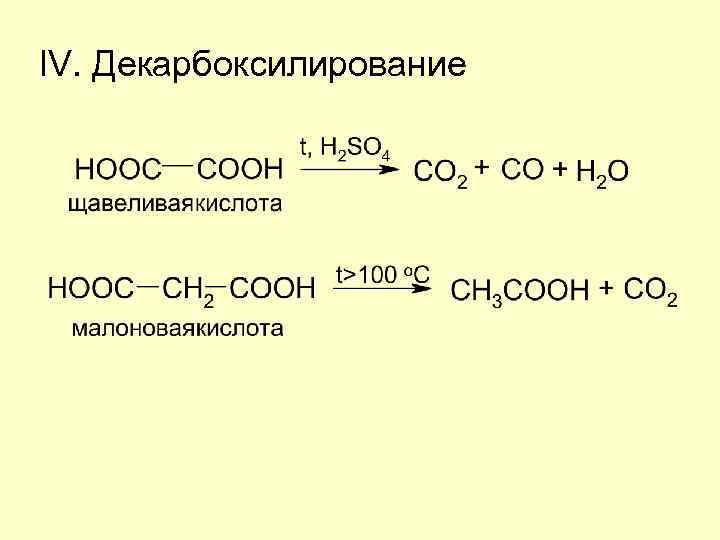 IV. Декарбоксилирование
IV. Декарбоксилирование
 Биологическое значение карбоновых кислот Муравьиную кислоту применяют как консервант, так же для получения лекарств (муравьиный спирт). Уксусную кислоту применяют как консервант и вкусовую приправу. Производные кислоты: эфиры (ацетилсалициловая кислота), амиды (парацетамол) применяют в качестве лекарств. Тиоэфир уксусной кислоты - ацетил-Ко. А центральный клеточный метаболит. Бензойную кислоту применяют как консервант, cоль (бензоат Na) – отхаркивающее средство.
Биологическое значение карбоновых кислот Муравьиную кислоту применяют как консервант, так же для получения лекарств (муравьиный спирт). Уксусную кислоту применяют как консервант и вкусовую приправу. Производные кислоты: эфиры (ацетилсалициловая кислота), амиды (парацетамол) применяют в качестве лекарств. Тиоэфир уксусной кислоты - ацетил-Ко. А центральный клеточный метаболит. Бензойную кислоту применяют как консервант, cоль (бензоат Na) – отхаркивающее средство.
 Валериановая и изовалериановая кислоты содержатся в корнях валерианы. Кислоты применяют для получения лекарств (валидол, валокордин, корвалол). Акриловая, метакриловая кислоты и их эфиры в виде полимеров входят в состав стоматологических материалов. Щавелевая, янтарная и фумаровая кислоты – метаболиты клеток. Щавелевая кислота токсична – вызывает образование оксалатных камней в почках. Янтарная и фумаровая – метаболиты цикла Кребса; входят в состав лекарственных препаратов Малеиновая кислота в природе не найдена.
Валериановая и изовалериановая кислоты содержатся в корнях валерианы. Кислоты применяют для получения лекарств (валидол, валокордин, корвалол). Акриловая, метакриловая кислоты и их эфиры в виде полимеров входят в состав стоматологических материалов. Щавелевая, янтарная и фумаровая кислоты – метаболиты клеток. Щавелевая кислота токсична – вызывает образование оксалатных камней в почках. Янтарная и фумаровая – метаболиты цикла Кребса; входят в состав лекарственных препаратов Малеиновая кислота в природе не найдена.
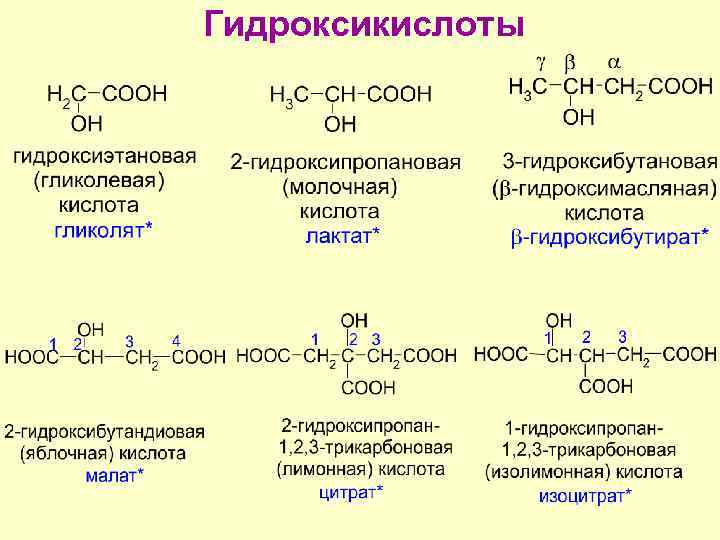 Гидроксикислоты
Гидроксикислоты
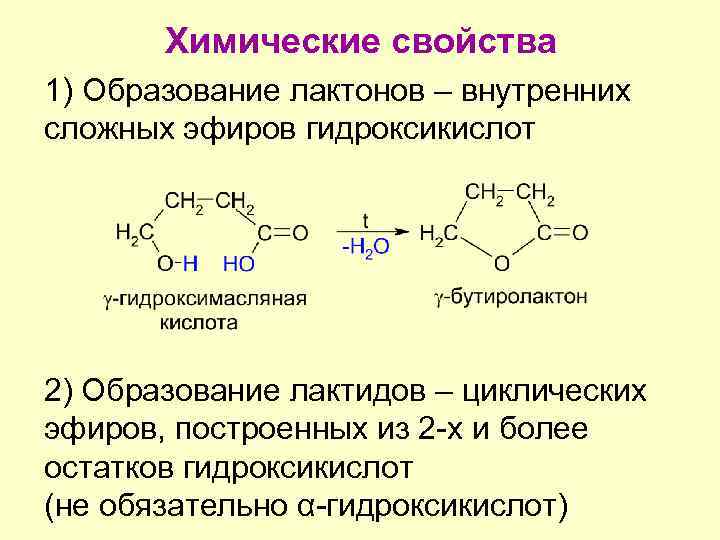 Химические свойства 1) Образование лактонов – внутренних сложных эфиров гидроксикислот 2) Образование лактидов – циклических эфиров, построенных из 2 -х и более остатков гидроксикислот (не обязательно α-гидроксикислот)
Химические свойства 1) Образование лактонов – внутренних сложных эфиров гидроксикислот 2) Образование лактидов – циклических эфиров, построенных из 2 -х и более остатков гидроксикислот (не обязательно α-гидроксикислот)
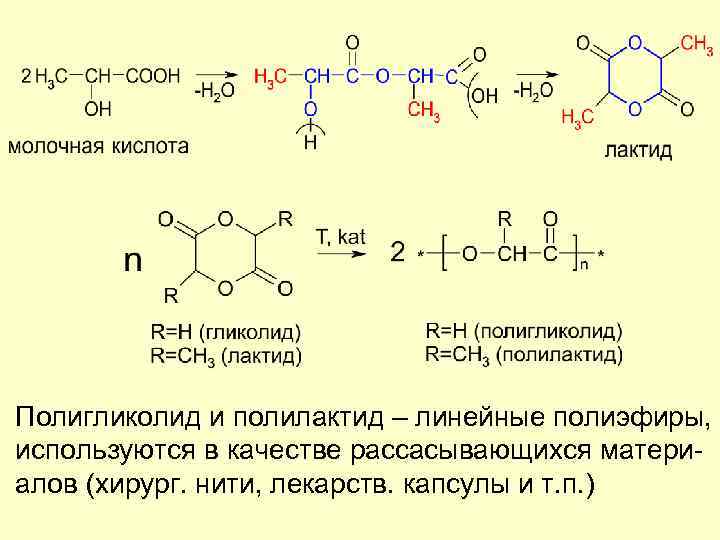 Полигликолид и полилактид – линейные полиэфиры, используются в качестве рассасывающихся материалов (хирург. нити, лекарств. капсулы и т. п. )
Полигликолид и полилактид – линейные полиэфиры, используются в качестве рассасывающихся материалов (хирург. нити, лекарств. капсулы и т. п. )
 3) Реакции элиминирования а) дегидратация (in vitro) б) дегидрирование (in vivo) Биологическое дегидрирование – особый случай окисления, осуществляется при участии кофермента НАД+ (окисленная форма).
3) Реакции элиминирования а) дегидратация (in vitro) б) дегидрирование (in vivo) Биологическое дегидрирование – особый случай окисления, осуществляется при участии кофермента НАД+ (окисленная форма).
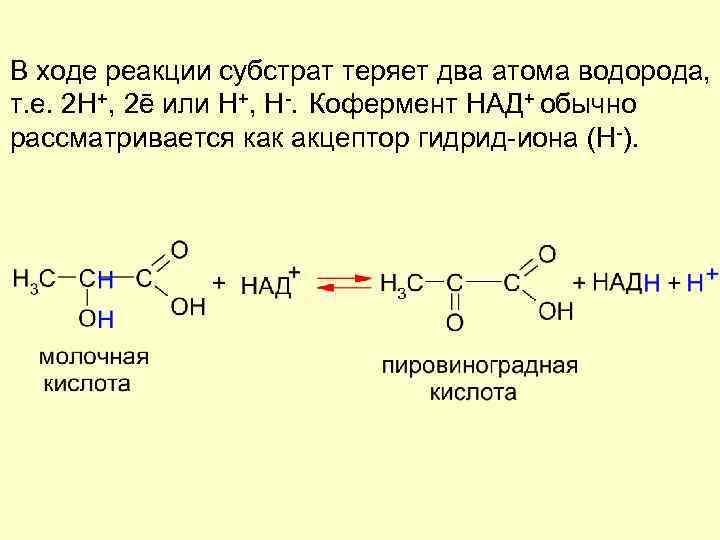 В ходе реакции субстрат теряет два атома водорода, т. е. 2 H+, 2ē или Н+, Н-. Кофермент НАД+ обычно рассматривается как акцептор гидрид-иона (Н-).
В ходе реакции субстрат теряет два атома водорода, т. е. 2 H+, 2ē или Н+, Н-. Кофермент НАД+ обычно рассматривается как акцептор гидрид-иона (Н-).
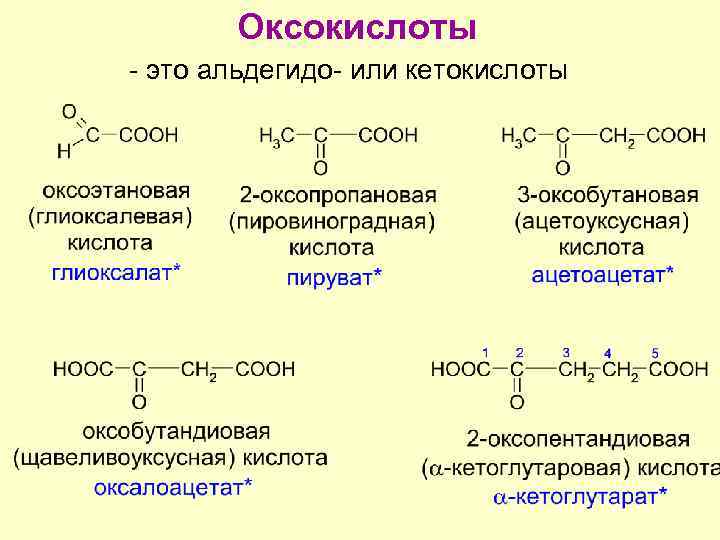 Оксокислоты - это альдегидо- или кетокислоты
Оксокислоты - это альдегидо- или кетокислоты
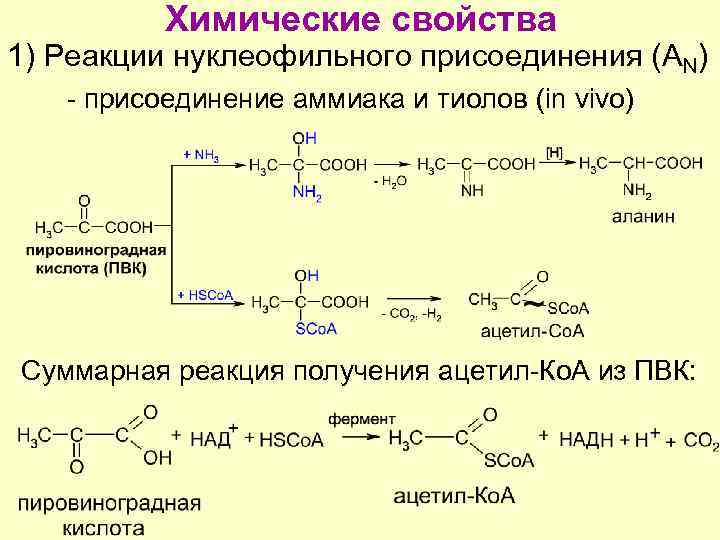 Химические свойства 1) Реакции нуклеофильного присоединения (AN) - присоединение аммиака и тиолов (in vivo) Суммарная реакция получения ацетил-Ко. А из ПВК:
Химические свойства 1) Реакции нуклеофильного присоединения (AN) - присоединение аммиака и тиолов (in vivo) Суммарная реакция получения ацетил-Ко. А из ПВК:
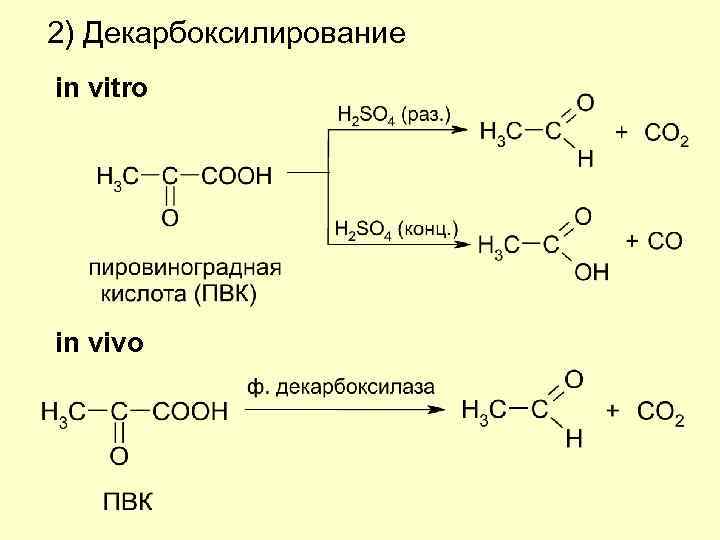 2) Декарбоксилирование in vitro in vivo
2) Декарбоксилирование in vitro in vivo
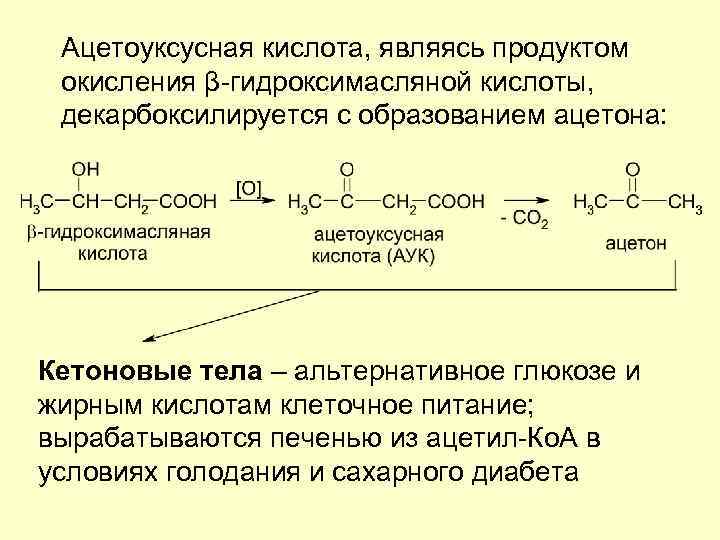 Ацетоуксусная кислота, являясь продуктом окисления β-гидроксимасляной кислоты, декарбоксилируется с образованием ацетона: Кетоновые тела – альтернативное глюкозе и жирным кислотам клеточное питание; вырабатываются печенью из ацетил-Ко. А в условиях голодания и сахарного диабета
Ацетоуксусная кислота, являясь продуктом окисления β-гидроксимасляной кислоты, декарбоксилируется с образованием ацетона: Кетоновые тела – альтернативное глюкозе и жирным кислотам клеточное питание; вырабатываются печенью из ацетил-Ко. А в условиях голодания и сахарного диабета
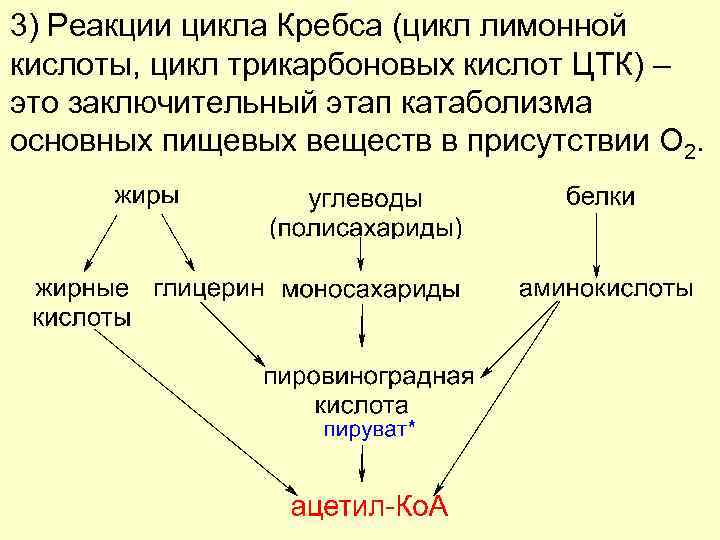 3) Реакции цикла Кребса (цикл лимонной кислоты, цикл трикарбоновых кислот ЦТК) – это заключительный этап катаболизма основных пищевых веществ в присутствии О 2.
3) Реакции цикла Кребса (цикл лимонной кислоты, цикл трикарбоновых кислот ЦТК) – это заключительный этап катаболизма основных пищевых веществ в присутствии О 2.
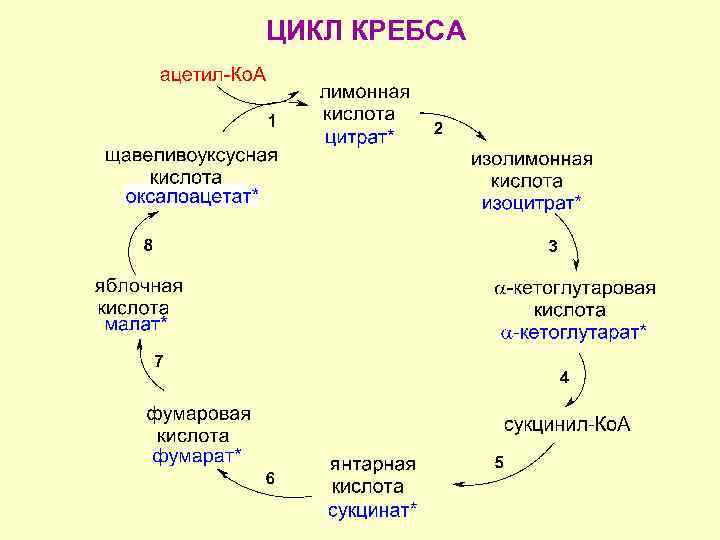 ЦИКЛ КРЕБСА
ЦИКЛ КРЕБСА
 Качественные реакции карбоновых кислот 1. Все растворимые кислоты реагируют с водным Na. HCO 3: RCOOH + Na. HCO 3 → RCOO-Na+ + CO 2 ↑ + H 2 O 2. Щавелевая кислота осаждается ионами кальция; оксалат кальция Са. С 2 О 4 растворяется в сильных кислотах. 3. Молочная и пировиноградная кислоты образуют окрашенные комплексы с солями железа (III)
Качественные реакции карбоновых кислот 1. Все растворимые кислоты реагируют с водным Na. HCO 3: RCOOH + Na. HCO 3 → RCOO-Na+ + CO 2 ↑ + H 2 O 2. Щавелевая кислота осаждается ионами кальция; оксалат кальция Са. С 2 О 4 растворяется в сильных кислотах. 3. Молочная и пировиноградная кислоты образуют окрашенные комплексы с солями железа (III)


