 «Основные соединения серы» Морозова Ольга и Жижневская Татьяна 9 «Д»
«Основные соединения серы» Морозова Ольга и Жижневская Татьяна 9 «Д»
 Основные соединения серы: Ø Н 2 S – сероводород; Ø SO 2 - серный газ; Ø SO 3 -сернистый ангидрид; Ø Н 2 SO 3 - сернистая кислота; Ø Н 2 SO 4 - серная кислота
Основные соединения серы: Ø Н 2 S – сероводород; Ø SO 2 - серный газ; Ø SO 3 -сернистый ангидрид; Ø Н 2 SO 3 - сернистая кислота; Ø Н 2 SO 4 - серная кислота
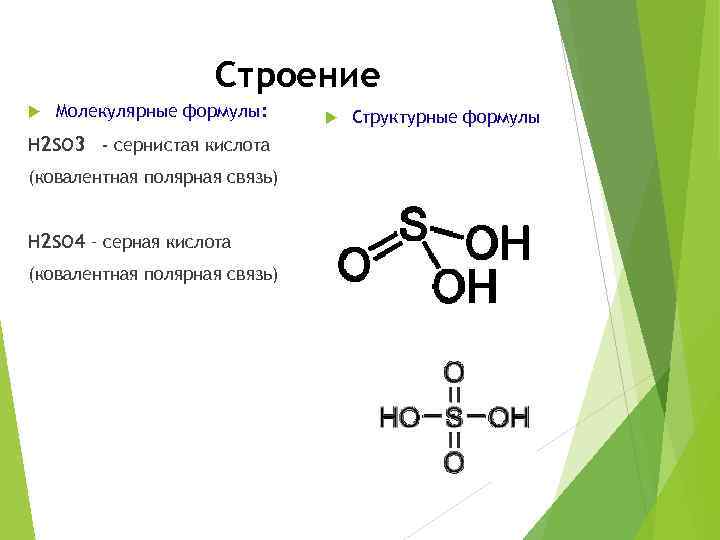 Строение Молекулярные формулы: Н 2 SO 3 - сернистая кислота (ковалентная полярная связь) Н 2 SO 4 – серная кислота (ковалентная полярная связь) Структурные формулы
Строение Молекулярные формулы: Н 2 SO 3 - сернистая кислота (ковалентная полярная связь) Н 2 SO 4 – серная кислота (ковалентная полярная связь) Структурные формулы
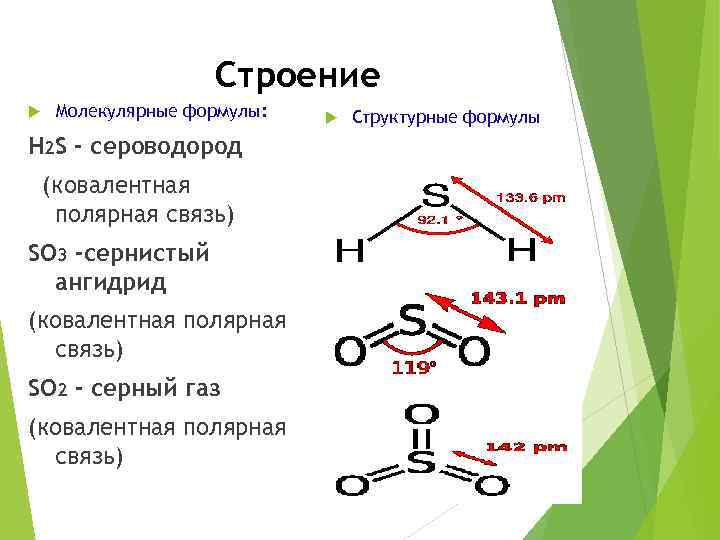 Строение Молекулярные формулы: Н 2 S - сероводород (ковалентная полярная связь) SO 3 -сернистый ангидрид (ковалентная полярная связь) SO 2 - серный газ (ковалентная полярная связь) Структурные формулы
Строение Молекулярные формулы: Н 2 S - сероводород (ковалентная полярная связь) SO 3 -сернистый ангидрид (ковалентная полярная связь) SO 2 - серный газ (ковалентная полярная связь) Структурные формулы
 Гидросульфиды Сульфиды Na. HS- гидросульфид натрия Na 2 S – сульфид натрия Ba(HS)2 - гидросульфид бария Zn. S – сульфид цинка Pb. S- сульфид свинца
Гидросульфиды Сульфиды Na. HS- гидросульфид натрия Na 2 S – сульфид натрия Ba(HS)2 - гидросульфид бария Zn. S – сульфид цинка Pb. S- сульфид свинца
 Серная кислоты – H 2 SO 4 Плотность серной кислоты – 1, 84 г /см 3, Концентрированная серная кислота – это бесцветная маслянистая жидкость, без запаха, примерно в два раза тяжелее воды.
Серная кислоты – H 2 SO 4 Плотность серной кислоты – 1, 84 г /см 3, Концентрированная серная кислота – это бесцветная маслянистая жидкость, без запаха, примерно в два раза тяжелее воды.
 Химические свойства H 2 S является очень слабой кислотой: H 2 S → HS− + H+ Сероводород — сильный восстановитель. На воздухе горит синим пламенем: 2 H 2 S + ЗО 2 = 2 Н 2 О + 2 SO 2 при недостатке кислорода: 2 H 2 S + O 2 = 2 S + 2 H 2 O (на этой реакции основан промышленный способ получения серы).
Химические свойства H 2 S является очень слабой кислотой: H 2 S → HS− + H+ Сероводород — сильный восстановитель. На воздухе горит синим пламенем: 2 H 2 S + ЗО 2 = 2 Н 2 О + 2 SO 2 при недостатке кислорода: 2 H 2 S + O 2 = 2 S + 2 H 2 O (на этой реакции основан промышленный способ получения серы).
 SO 3 — типичный кислотный оксид, ангидрид серной кислоты 1. Кислотно-основные: При взаимодействии с водой образует серную кислоту: SO 3 + H 2 O → H 2 SO 4 Взаимодействует с основаниями: 2 KOH + SO 3 → K 2 SO 4 + H 2 O, основными оксидами: Ca. O + SO 3 → Ca. SO 4, c амфотерными оксидами: 3 SO 3 + Al 2 O 3 → Al 2(SO 4)3
SO 3 — типичный кислотный оксид, ангидрид серной кислоты 1. Кислотно-основные: При взаимодействии с водой образует серную кислоту: SO 3 + H 2 O → H 2 SO 4 Взаимодействует с основаниями: 2 KOH + SO 3 → K 2 SO 4 + H 2 O, основными оксидами: Ca. O + SO 3 → Ca. SO 4, c амфотерными оксидами: 3 SO 3 + Al 2 O 3 → Al 2(SO 4)3
 Нахождение соединений серы в природе Самородная сера Сульфидная сера Сульфатная сера Халькопирит Киноварь Hg. S Cu. Fe. S 2 Галенит Сфалери т Гипс Ca. SO 4 • 2 H 2 O Pb. S Zn. S
Нахождение соединений серы в природе Самородная сера Сульфидная сера Сульфатная сера Халькопирит Киноварь Hg. S Cu. Fe. S 2 Галенит Сфалери т Гипс Ca. SO 4 • 2 H 2 O Pb. S Zn. S
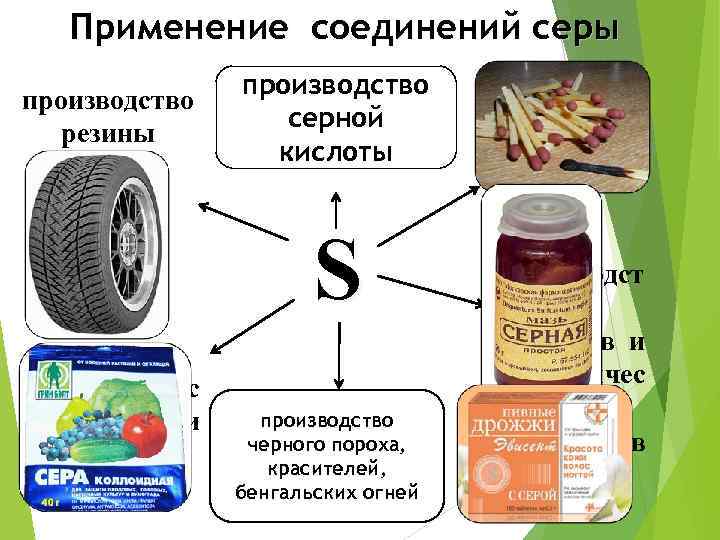 Применение соединений серы производство резины производство серной кислоты S для борьбы с вредителями растений производство черного пороха, красителей, бенгальских огней производст во лекарств и косметичес ких препаратов
Применение соединений серы производство резины производство серной кислоты S для борьбы с вредителями растений производство черного пороха, красителей, бенгальских огней производст во лекарств и косметичес ких препаратов