Гидросфера.ppt
- Количество слайдов: 36
 Основные процессы формирования химического состава природных вод При формировании химического состава природных вод принято выделять прямые и косвенные, а также главные и второстепенные факторы, влияющие на содержание в них растворенных компонентов. По характеру воздействия на формирования состава природных вод все факторы делят на 5 групп: Физико-географические (рельеф, климат и т. п. ); Геологические (вид горных пород, гидрогеологические условия и т. п. ); Биологические (деятельность живых организмов); Антропогенные (состав сточных вод, состав твердых отходов и т. п. ) Физико- химические (химические свойства соединений, кислотноосновные и окислительно-восстановительные условия и др. ).
Основные процессы формирования химического состава природных вод При формировании химического состава природных вод принято выделять прямые и косвенные, а также главные и второстепенные факторы, влияющие на содержание в них растворенных компонентов. По характеру воздействия на формирования состава природных вод все факторы делят на 5 групп: Физико-географические (рельеф, климат и т. п. ); Геологические (вид горных пород, гидрогеологические условия и т. п. ); Биологические (деятельность живых организмов); Антропогенные (состав сточных вод, состав твердых отходов и т. п. ) Физико- химические (химические свойства соединений, кислотноосновные и окислительно-восстановительные условия и др. ).
 Классификация природных вод по величине их минерализации Минерализация, г×л-1 Наименование вод < 0, 2 Ультрапресные 0, 2 - 0, 5 Пресные 0, 5 - 0, 1 С относительно повышенной минерализацией 1, 0 - 3, 0 Солоноватые 3, 0 - 10, 0 Соленые 10, 0 - 35, 0 С повышенной соленостью 35, 0 - 50, 0 Переходные к рассолам 50, 0 - 400 Рассолы
Классификация природных вод по величине их минерализации Минерализация, г×л-1 Наименование вод < 0, 2 Ультрапресные 0, 2 - 0, 5 Пресные 0, 5 - 0, 1 С относительно повышенной минерализацией 1, 0 - 3, 0 Солоноватые 3, 0 - 10, 0 Соленые 10, 0 - 35, 0 С повышенной соленостью 35, 0 - 50, 0 Переходные к рассолам 50, 0 - 400 Рассолы
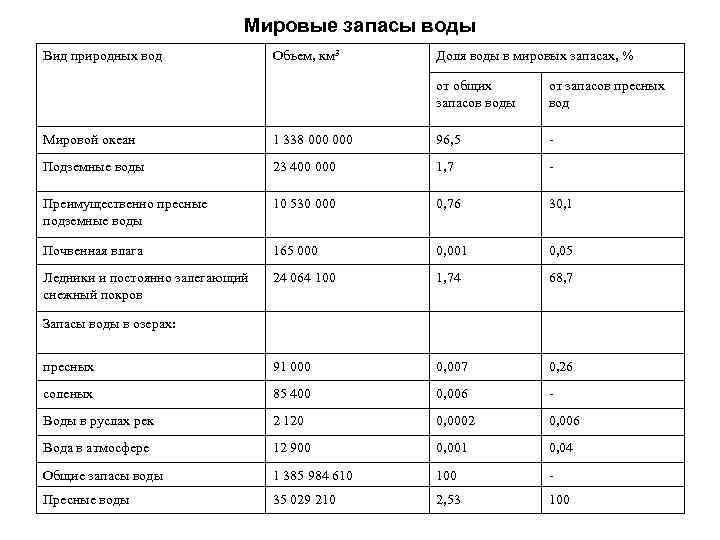 Мировые запасы воды Вид природных вод Объем, км 3 Доля воды в мировых запасах, % от общих запасов воды от запасов пресных вод Мировой океан 1 338 000 96, 5 - Подземные воды 23 400 000 1, 7 - Преимущественно пресные подземные воды 10 530 000 0, 76 30, 1 Почвенная влага 165 000 0, 001 0, 05 Ледники и постоянно залегающий снежный покров 24 064 100 1, 74 68, 7 пресных 91 000 0, 007 0, 26 соленых 85 400 0, 006 - Воды в руслах рек 2 120 0, 0002 0, 006 Вода в атмосфере 12 900 0, 001 0, 04 Общие запасы воды 1 385 984 610 100 - Пресные воды 35 029 210 2, 53 100 Запасы воды в озерах:
Мировые запасы воды Вид природных вод Объем, км 3 Доля воды в мировых запасах, % от общих запасов воды от запасов пресных вод Мировой океан 1 338 000 96, 5 - Подземные воды 23 400 000 1, 7 - Преимущественно пресные подземные воды 10 530 000 0, 76 30, 1 Почвенная влага 165 000 0, 001 0, 05 Ледники и постоянно залегающий снежный покров 24 064 100 1, 74 68, 7 пресных 91 000 0, 007 0, 26 соленых 85 400 0, 006 - Воды в руслах рек 2 120 0, 0002 0, 006 Вода в атмосфере 12 900 0, 001 0, 04 Общие запасы воды 1 385 984 610 100 - Пресные воды 35 029 210 2, 53 100 Запасы воды в озерах:
 • Qиспарения = Qосадки Qиспарения = Qиспарения океан + Qиспарения суша • 520 тыс. км 3 = 449 тыс. км 3 + 71 тыс. км 3 • Qосадки = Qосадки океан + Qосадки суша • 520 тыс. км 3 = 404 тыс. км 3 + 116 тыс. км 3 • Океан -45 тыс. км 3 Суша +45 тыс. км 3
• Qиспарения = Qосадки Qиспарения = Qиспарения океан + Qиспарения суша • 520 тыс. км 3 = 449 тыс. км 3 + 71 тыс. км 3 • Qосадки = Qосадки океан + Qосадки суша • 520 тыс. км 3 = 404 тыс. км 3 + 116 тыс. км 3 • Океан -45 тыс. км 3 Суша +45 тыс. км 3
 • Примерный расход воды в мире • (тыс. км 3) • Сельское хозяйство 7 • Промышленность 1, 7 • Разбавление сточных вод 9 • В быту 0, 6 • Прочие 0, 4 • Подземный сток 13 • Итого 31, 7 • Остаток 13, 3
• Примерный расход воды в мире • (тыс. км 3) • Сельское хозяйство 7 • Промышленность 1, 7 • Разбавление сточных вод 9 • В быту 0, 6 • Прочие 0, 4 • Подземный сток 13 • Итого 31, 7 • Остаток 13, 3
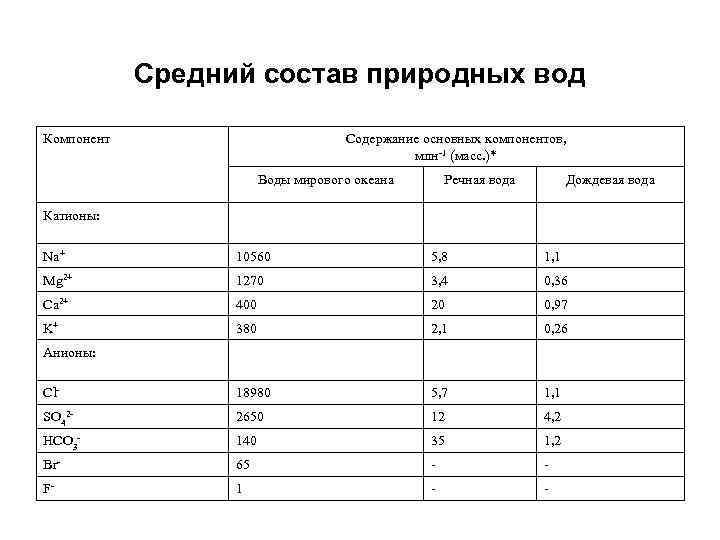 Средний состав природных вод Компонент Содержание основных компонентов, млн-1 (масс. )* Воды мирового океана Речная вода Дождевая вода Катионы: Na+ 10560 5, 8 1, 1 Mg 2+ 1270 3, 4 0, 36 Ca 2+ 400 20 0, 97 K+ 380 2, 1 0, 26 Cl- 18980 5, 7 1, 1 SO 42 - 2650 12 4, 2 HCO 3 - 140 35 1, 2 Br- 65 - - F- 1 - - Анионы:
Средний состав природных вод Компонент Содержание основных компонентов, млн-1 (масс. )* Воды мирового океана Речная вода Дождевая вода Катионы: Na+ 10560 5, 8 1, 1 Mg 2+ 1270 3, 4 0, 36 Ca 2+ 400 20 0, 97 K+ 380 2, 1 0, 26 Cl- 18980 5, 7 1, 1 SO 42 - 2650 12 4, 2 HCO 3 - 140 35 1, 2 Br- 65 - - F- 1 - - Анионы:
 Основные процессы формирования химического состава природных вод При формировании химического состава природных вод принято выделять прямые и косвенные, а также главные и второстепенные факторы, влияющие на содержание в них растворенных компонентов. По характеру воздействия на формирования состава природных вод все факторы делят на 5 групп: Физико-географические (рельеф, климат и т. п. ); Геологические (вид горных пород, гидрогеологические условия и т. п. ); Биологические (деятельность живых организмов); Антропогенные (состав сточных вод, состав твердых отходов и т. п. ) Физико- химические (химические свойства соединений, кислотноосновные и окислительно-восстановительные условия и др. ).
Основные процессы формирования химического состава природных вод При формировании химического состава природных вод принято выделять прямые и косвенные, а также главные и второстепенные факторы, влияющие на содержание в них растворенных компонентов. По характеру воздействия на формирования состава природных вод все факторы делят на 5 групп: Физико-географические (рельеф, климат и т. п. ); Геологические (вид горных пород, гидрогеологические условия и т. п. ); Биологические (деятельность живых организмов); Антропогенные (состав сточных вод, состав твердых отходов и т. п. ) Физико- химические (химические свойства соединений, кислотноосновные и окислительно-восстановительные условия и др. ).
 Жесткость природных вод • Одной из важных характеристик природных вод, во многом определяющих возможности их использования человеком, является жесткость воды. Жесткостью воды называется свойство воды, обусловленное содержанием в ней ионов кальция и магния. Ж = [Са 2+]*f(Ca) /M(Ca) + [Mg 2+]*f(Mg) /M(Mg) Ж = [Са 2+]/ 20, 04 + [Mg 2+]/ 12, 156
Жесткость природных вод • Одной из важных характеристик природных вод, во многом определяющих возможности их использования человеком, является жесткость воды. Жесткостью воды называется свойство воды, обусловленное содержанием в ней ионов кальция и магния. Ж = [Са 2+]*f(Ca) /M(Ca) + [Mg 2+]*f(Mg) /M(Mg) Ж = [Са 2+]/ 20, 04 + [Mg 2+]/ 12, 156
 По величине общей жесткости в моль/куб. м природные воды принято делить на ряд групп: вода очень мягкая Ж < 1, 5 вода мягкая 1, 5 < Ж < 3, 0 вода средней жесткости 3, 0 < Ж < 5, 4; вода жесткая 5, 4 < Ж < 10, 7. вода очень жесткая 10, 7 < Ж.
По величине общей жесткости в моль/куб. м природные воды принято делить на ряд групп: вода очень мягкая Ж < 1, 5 вода мягкая 1, 5 < Ж < 3, 0 вода средней жесткости 3, 0 < Ж < 5, 4; вода жесткая 5, 4 < Ж < 10, 7. вода очень жесткая 10, 7 < Ж.
 Следует отметить, что за рубежом для выражения значений жесткости воды используются различные единицы измерения. Так, например, Немецкий градус жесткости соответствует содержанию в воде 10, 0 мг/л Са. О. Один Французкий градус жесткости соответствует содержанию в воде 10 мг/л Са. СО 3. Один американский градус жесткости соответствует содержанию в воде 1 мг/л Са. СО 3. Соотношение между этими единицами измерения жесткости можно представить равенством: • 1 моль/куб. м = 2, 804 Немецких градуса жесткости; • 1 моль/куб. м = 5, 005 Французских градуса жесткости; • 1 моль/куб. м = 50, 050 Американских градусов жесткости.
Следует отметить, что за рубежом для выражения значений жесткости воды используются различные единицы измерения. Так, например, Немецкий градус жесткости соответствует содержанию в воде 10, 0 мг/л Са. О. Один Французкий градус жесткости соответствует содержанию в воде 10 мг/л Са. СО 3. Один американский градус жесткости соответствует содержанию в воде 1 мг/л Са. СО 3. Соотношение между этими единицами измерения жесткости можно представить равенством: • 1 моль/куб. м = 2, 804 Немецких градуса жесткости; • 1 моль/куб. м = 5, 005 Французских градуса жесткости; • 1 моль/куб. м = 50, 050 Американских градусов жесткости.
 Растворимость карбонатов и р. Н подземных и поверхностных природных вод Процесс непосредственного растворения карбоната кальция по уравнению: Ca. CO 3 = Ca 2+ + CO 32 практически не играет роли при переходе мало растворимых карбонатов в раствор. Соли угольной кислоты в природных водоемах могут переходить в раствор и существовать в нем в заметных количествах только при наличии растворенного диоксида углерода: Ca. CO 3 + CO 2 (р-р) = Ca 2+ + 2 НCO 3 - При равновесии с карбонатными породами р. Н поверхностных вод должен составлять 7, 3 -8, 4.
Растворимость карбонатов и р. Н подземных и поверхностных природных вод Процесс непосредственного растворения карбоната кальция по уравнению: Ca. CO 3 = Ca 2+ + CO 32 практически не играет роли при переходе мало растворимых карбонатов в раствор. Соли угольной кислоты в природных водоемах могут переходить в раствор и существовать в нем в заметных количествах только при наличии растворенного диоксида углерода: Ca. CO 3 + CO 2 (р-р) = Ca 2+ + 2 НCO 3 - При равновесии с карбонатными породами р. Н поверхностных вод должен составлять 7, 3 -8, 4.
 Щелочность природных вод Одной из важнейших особенностей большинства природных вод является способность нейтрализовать ионы водорода. Эта способность называется щелочностью воды и определяется экспериментально при титровании пробы воды сильной кислотой, обычно HCl, в присутствии фенолфталеина (р. Н перехода окраски 8, 3) и затем метилоранжа (р. Н перехода окраски 4, 5 ) Основными компонентами, ответственными за процессы связывания ионов водорода, в большинстве природных вод являются ионы HCO 3 -
Щелочность природных вод Одной из важнейших особенностей большинства природных вод является способность нейтрализовать ионы водорода. Эта способность называется щелочностью воды и определяется экспериментально при титровании пробы воды сильной кислотой, обычно HCl, в присутствии фенолфталеина (р. Н перехода окраски 8, 3) и затем метилоранжа (р. Н перехода окраски 4, 5 ) Основными компонентами, ответственными за процессы связывания ионов водорода, в большинстве природных вод являются ионы HCO 3 -
 Процессы закисления поверхностных водоемов На первом этапе, несмотря на поступление кислых осадков, р. Н практически не меняется. Ионы гидрокарбоната, присутствующие в поверхностных водоемах, успевают полностью нейтрализовать поступающие ионы Н+: НСО 3 - + Н+ = Н 2 О + СО 2 Первый этап. В период наиболее интенсивного поступления кислых вод в водоем (осень - обильные дожди и, особенно, весна - таяние снега) возможны значительные отклонения в величине р. Н поверхностных водоемов. С прекращением интенсивного поступления кислых осадков водоем переходит в обычное состояние, р. Н поднимается до первоначальных значений. На втором этапе закисления водоема р. Н воды обычно не поднимается выше 5, 5 в течение всего года (отсутствует контакт с карбонатными породами); о таких водоемах обычно говорят как об умеренно кислых
Процессы закисления поверхностных водоемов На первом этапе, несмотря на поступление кислых осадков, р. Н практически не меняется. Ионы гидрокарбоната, присутствующие в поверхностных водоемах, успевают полностью нейтрализовать поступающие ионы Н+: НСО 3 - + Н+ = Н 2 О + СО 2 Первый этап. В период наиболее интенсивного поступления кислых вод в водоем (осень - обильные дожди и, особенно, весна - таяние снега) возможны значительные отклонения в величине р. Н поверхностных водоемов. С прекращением интенсивного поступления кислых осадков водоем переходит в обычное состояние, р. Н поднимается до первоначальных значений. На втором этапе закисления водоема р. Н воды обычно не поднимается выше 5, 5 в течение всего года (отсутствует контакт с карбонатными породами); о таких водоемах обычно говорят как об умеренно кислых
 Процессы закисления поверхностных водоемов На третьем этапе закисления р. Н водоемов стабилизируется на значениях р. Н<5 (обычно р. Н=4, 5), даже если атмосферные осадки имеют более высокие значения р. Н. Это связано с присутствием гумусовых веществ и соединений алюминия в водоемах и почвенном слое. Гумусовые соединения в основном представлены в водоемах растворами слабых органических кислот, имеющими р. Н<5. Связывая или выделяя ионы Н+, эти кислоты стабилизируют значение р. Н в водоеме.
Процессы закисления поверхностных водоемов На третьем этапе закисления р. Н водоемов стабилизируется на значениях р. Н<5 (обычно р. Н=4, 5), даже если атмосферные осадки имеют более высокие значения р. Н. Это связано с присутствием гумусовых веществ и соединений алюминия в водоемах и почвенном слое. Гумусовые соединения в основном представлены в водоемах растворами слабых органических кислот, имеющими р. Н<5. Связывая или выделяя ионы Н+, эти кислоты стабилизируют значение р. Н в водоеме.
 Окислительно-восстановительные процессы в гидросфере Окислительно-восстановительные реакции исключительно важную роль в описании процессов протекающих в природных водоемах. Предыстория и качество природных вод в значительной степени зависят от вида окислительно-восстановительных реакций, их кинетических характеристик и величины окислительно-восстановительного потенциала, который соответствовал бы данной системе при установлении равновесия.
Окислительно-восстановительные процессы в гидросфере Окислительно-восстановительные реакции исключительно важную роль в описании процессов протекающих в природных водоемах. Предыстория и качество природных вод в значительной степени зависят от вида окислительно-восстановительных реакций, их кинетических характеристик и величины окислительно-восстановительного потенциала, который соответствовал бы данной системе при установлении равновесия.
 Процесс окисления органического вещества общей формулой {CH 2 О} можно представить следующим уравнением реакции: {CH 2 О} + О 2 = СО 2 + Н 2 О • В связи с отсутствием, по условию примера, дополнительного поступления кислорода, максимальное количество органического вещества, которое может быть окисленно в воде будет определяться содержанием кислорода в воде, которое будет соответствовать условиям равновесия с воздухом, устанавливающимся до начала процесса окисления. При равновесии приземным воздухом это количество составит [С(кисл. )] = КГ(кисл. ) * Р(кисл. )= 8, 3 мг/л
Процесс окисления органического вещества общей формулой {CH 2 О} можно представить следующим уравнением реакции: {CH 2 О} + О 2 = СО 2 + Н 2 О • В связи с отсутствием, по условию примера, дополнительного поступления кислорода, максимальное количество органического вещества, которое может быть окисленно в воде будет определяться содержанием кислорода в воде, которое будет соответствовать условиям равновесия с воздухом, устанавливающимся до начала процесса окисления. При равновесии приземным воздухом это количество составит [С(кисл. )] = КГ(кисл. ) * Р(кисл. )= 8, 3 мг/л
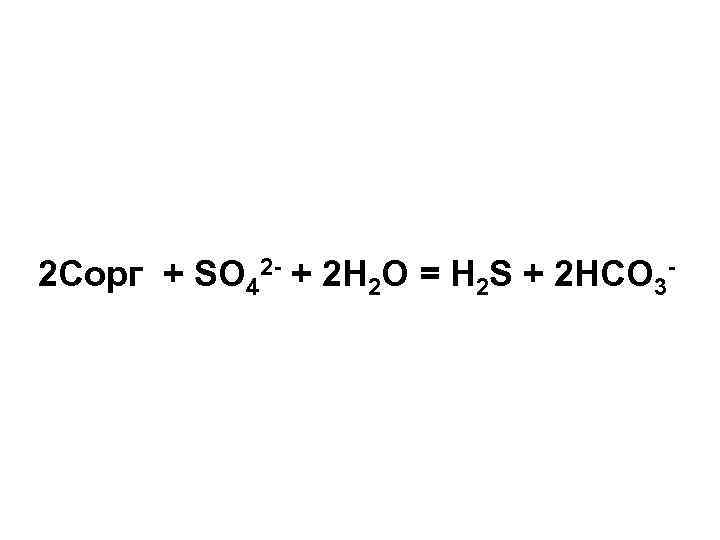 2 Cорг + SO 42 - + 2 H 2 O = H 2 S + 2 HCO 3 -
2 Cорг + SO 42 - + 2 H 2 O = H 2 S + 2 HCO 3 -

 Рациональное использование воды «Вода стоит особняком в истории нашей планеты. Нет природного тела, которое могло бы сравниться с ней по влиянию на ход основных самых грандиозных геологических процессов. Нет земного вещества, минерала, горной породы, живого тела, которое её бы не заключало. Всё земное вещество … ею проникнуто и охвачено» . В. И. Вернадский
Рациональное использование воды «Вода стоит особняком в истории нашей планеты. Нет природного тела, которое могло бы сравниться с ней по влиянию на ход основных самых грандиозных геологических процессов. Нет земного вещества, минерала, горной породы, живого тела, которое её бы не заключало. Всё земное вещество … ею проникнуто и охвачено» . В. И. Вернадский
 Вода является одним из важнейших природных ресурсов, во многом определяющих технический и социальный прогресс тех или иных регионов и стран. Количество потребляемой пресной воды в сотни раз превосходит масштабы потребления всех остальных видов природных ресурсов вместе взятых. Именно круговорот воды составляет основу техногенного круговорота веществ и связанного с ним превращения энергии в эколого-экономических системах. Наша планета богата водными ресурсами, однако на долю пресной воды приходится около 2%, а на долю пригодной (и удобной) для использования - всего 0, 01%. В Антарктиде содержится в три раза больше воды, чем во всех реках мира, а в Байкале находится 10% всей пресной воды мира, причём высшего качества.
Вода является одним из важнейших природных ресурсов, во многом определяющих технический и социальный прогресс тех или иных регионов и стран. Количество потребляемой пресной воды в сотни раз превосходит масштабы потребления всех остальных видов природных ресурсов вместе взятых. Именно круговорот воды составляет основу техногенного круговорота веществ и связанного с ним превращения энергии в эколого-экономических системах. Наша планета богата водными ресурсами, однако на долю пресной воды приходится около 2%, а на долю пригодной (и удобной) для использования - всего 0, 01%. В Антарктиде содержится в три раза больше воды, чем во всех реках мира, а в Байкале находится 10% всей пресной воды мира, причём высшего качества.
 Основой водных ресурсов России является речной сток. В средние по водности годы он составляет 4262 км 3, из которых около 90% приходится на бассейны рек, впадающих в Северный Ледовитый и Тихий океаны. Более 80% населения России и её основной промышленный и сельскохозяйственный потенциал сосредоточены в бассейнах рек, впадающих в Каспийское и Азовское моря. Пять наиболее крупных рек России: Енисей (630 км 3), Лена (532), Обь (404), Амур (344) и Волга (254 км 3). Они обеспечивают 46% всего стока пресных вод с территории нашей страны.
Основой водных ресурсов России является речной сток. В средние по водности годы он составляет 4262 км 3, из которых около 90% приходится на бассейны рек, впадающих в Северный Ледовитый и Тихий океаны. Более 80% населения России и её основной промышленный и сельскохозяйственный потенциал сосредоточены в бассейнах рек, впадающих в Каспийское и Азовское моря. Пять наиболее крупных рек России: Енисей (630 км 3), Лена (532), Обь (404), Амур (344) и Волга (254 км 3). Они обеспечивают 46% всего стока пресных вод с территории нашей страны.
 Физиологическая потребность человека в воде – 23 л. в сутки. Социальная норма потребления воды в Москве – 135 л. в день. Удельный расход воды в жилых домах в Москве в 2005 году составил 357 л/сут. (при нормативе – 135 л. ). Средний уровень потребления воды в Европе составляет, в л/сут. : Германия – 130, Дания – 134, Нидерланды – 158, Англия – 170, Франция – 175, Италия – 230.
Физиологическая потребность человека в воде – 23 л. в сутки. Социальная норма потребления воды в Москве – 135 л. в день. Удельный расход воды в жилых домах в Москве в 2005 году составил 357 л/сут. (при нормативе – 135 л. ). Средний уровень потребления воды в Европе составляет, в л/сут. : Германия – 130, Дания – 134, Нидерланды – 158, Англия – 170, Франция – 175, Италия – 230.
 Основные реки: Волга, Дон, Кубань, Обь, Енисей, Лена, Печора, оцениваются как «загрязнённые» , их крупные притоки: Ока, Кама, Томь, Иртыш, Тобол, Миасс, Висеть, Тура, как “сильнозагрязнённые”. Вода в Москва-реке относится к категории “грязных” и ”чрезвычайно грязных“. Основные загрязняющие вещества: соединения меди, железа, нитратный азот, нефтепродукты. Ниже сбросов Курьяновской и Люберецкой станций аэрации в речной воде обнаруживались аммонийный азот и формальдегид, среднегодовая концентрация которых достигала 8 – 22 ПДК.
Основные реки: Волга, Дон, Кубань, Обь, Енисей, Лена, Печора, оцениваются как «загрязнённые» , их крупные притоки: Ока, Кама, Томь, Иртыш, Тобол, Миасс, Висеть, Тура, как “сильнозагрязнённые”. Вода в Москва-реке относится к категории “грязных” и ”чрезвычайно грязных“. Основные загрязняющие вещества: соединения меди, железа, нитратный азот, нефтепродукты. Ниже сбросов Курьяновской и Люберецкой станций аэрации в речной воде обнаруживались аммонийный азот и формальдегид, среднегодовая концентрация которых достигала 8 – 22 ПДК.
 Создание замкнутых водооборотных систем Годовой сток Волги составляет 254 км 3. Объём сточных вод поступающий в бассейн Волги - порядка 22 км 3. Настоятельная необходимость и целесообразность создания замкнутых систем производственного водоснабжения, являющихся основой рационального водопользования, обусловлены тремя основными факторами: дефицитом пресной воды; исчерпанием обезвреживающей (самоочищающей и разбавляющей) способности водоемов; экономическими преимуществами
Создание замкнутых водооборотных систем Годовой сток Волги составляет 254 км 3. Объём сточных вод поступающий в бассейн Волги - порядка 22 км 3. Настоятельная необходимость и целесообразность создания замкнутых систем производственного водоснабжения, являющихся основой рационального водопользования, обусловлены тремя основными факторами: дефицитом пресной воды; исчерпанием обезвреживающей (самоочищающей и разбавляющей) способности водоемов; экономическими преимуществами
 Если стоимость 90%-ной степени очистки сточных вод принять за единицу, то очистка на 99% обойдется примерно в 10 раз дороже, а очистка на 99, 9%, которая часто и требуется для достижения ПДКрх, будет дороже в 100 раз. В результате локальная очистка сточных вод с целью их повторного использования в производстве в большинстве случаев оказывается значительно дешевле их полной очистки в соответствии с требованиями санитарных норм. В целом, рецикл оказывается более выгоден, чем прямоточная система водоснабжения.
Если стоимость 90%-ной степени очистки сточных вод принять за единицу, то очистка на 99% обойдется примерно в 10 раз дороже, а очистка на 99, 9%, которая часто и требуется для достижения ПДКрх, будет дороже в 100 раз. В результате локальная очистка сточных вод с целью их повторного использования в производстве в большинстве случаев оказывается значительно дешевле их полной очистки в соответствии с требованиями санитарных норм. В целом, рецикл оказывается более выгоден, чем прямоточная система водоснабжения.
 Основные принципы создания замкнутых водооборотных систем Вопросом первостепенной важности при создании замкнутых водооборотных систем является разработка научно-обоснованных требований к качеству воды, используемой во всех технологических процессах и операциях. Поэтому необходимо оценить максимально допустимые пределы основных показателей качества воды, которые, в основном, определяются следующими факторами:
Основные принципы создания замкнутых водооборотных систем Вопросом первостепенной важности при создании замкнутых водооборотных систем является разработка научно-обоснованных требований к качеству воды, используемой во всех технологических процессах и операциях. Поэтому необходимо оценить максимально допустимые пределы основных показателей качества воды, которые, в основном, определяются следующими факторами:
 не должно ухудшаться качество получаемого продукта; • • должна обеспечиваться безаварийная работа оборудования; оно не должно разрушаться вследствие коррозии, на стенках не должны появляться отложения и т. д. ; • не влиять на здоровье обслуживающего персонала за счёт изменения токсикологических или эпидемиологических характеристик воды.
не должно ухудшаться качество получаемого продукта; • • должна обеспечиваться безаварийная работа оборудования; оно не должно разрушаться вследствие коррозии, на стенках не должны появляться отложения и т. д. ; • не влиять на здоровье обслуживающего персонала за счёт изменения токсикологических или эпидемиологических характеристик воды.
 Основные методы переработки (очистки) сточных вод Классификация методов: методы, основанные на выделении примесей без изменения последних, например отстаивание или фильтрация - физические или механические методы; методы, основанные на превращении примесей в другие формы или состояния, физико-химические: – коагуляция; – флотация; –образование малорастворимых соединений; – окисление или восстановление; – мембранные процессы; – ионный обмен; – экстракция и т. д. биохимические методы (аэробные и анаэробные).
Основные методы переработки (очистки) сточных вод Классификация методов: методы, основанные на выделении примесей без изменения последних, например отстаивание или фильтрация - физические или механические методы; методы, основанные на превращении примесей в другие формы или состояния, физико-химические: – коагуляция; – флотация; –образование малорастворимых соединений; – окисление или восстановление; – мембранные процессы; – ионный обмен; – экстракция и т. д. биохимические методы (аэробные и анаэробные).
 Выделение неорганических веществ 1. Дистилляция. 2. Мембранные ( электродиализ и обратный осмос). Электродиализ основан на направленном переносе ионов диссоцированных солей в поле постоянного тока через селективные мембраны из естественных или синтетических материалов Обратный осмос. Процесс разделения водных растворов путем их фильтрации через полупроницаемые мембраны под действием давления, много выше осмотического. 1. Ионный обмен до сих пор остается основным методом приготовления глубокообессоленной воды для АЭС и ТЭС с паровыми котлами высокого, сверхвысокого и критического давления, а также для получения ультрачистой и обессоленной воды для химической, электронной и некоторые других отраслей промышленности.
Выделение неорганических веществ 1. Дистилляция. 2. Мембранные ( электродиализ и обратный осмос). Электродиализ основан на направленном переносе ионов диссоцированных солей в поле постоянного тока через селективные мембраны из естественных или синтетических материалов Обратный осмос. Процесс разделения водных растворов путем их фильтрации через полупроницаемые мембраны под действием давления, много выше осмотического. 1. Ионный обмен до сих пор остается основным методом приготовления глубокообессоленной воды для АЭС и ТЭС с паровыми котлами высокого, сверхвысокого и критического давления, а также для получения ультрачистой и обессоленной воды для химической, электронной и некоторые других отраслей промышленности.
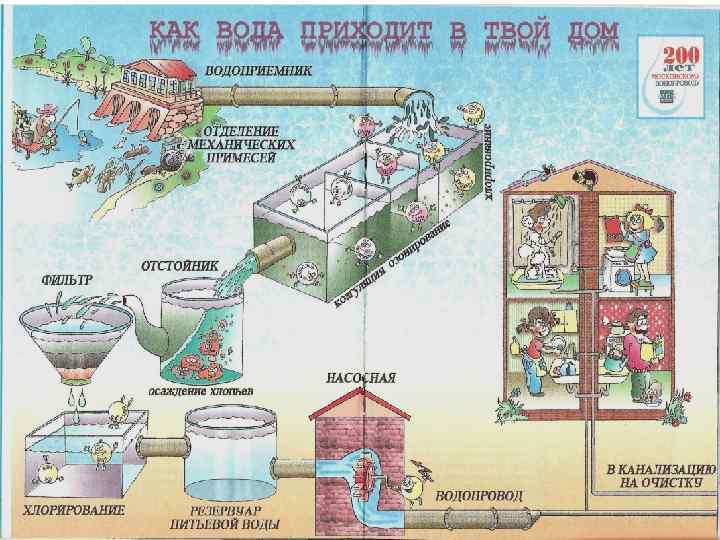
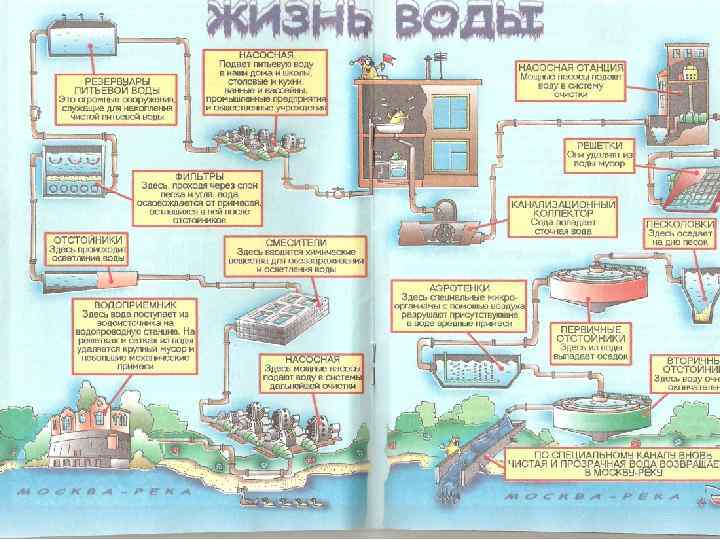
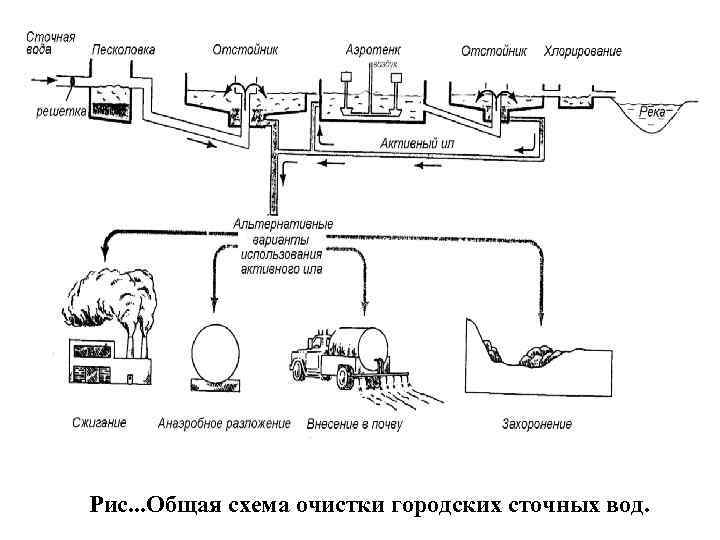 Рис. . . Общая схема очистки городских сточных вод.
Рис. . . Общая схема очистки городских сточных вод.
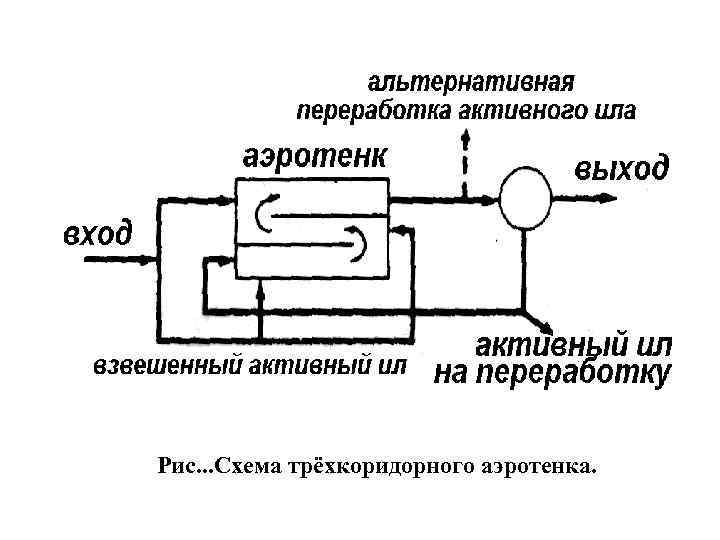 Рис. . . Схема трёхкоридорного аэротенка.
Рис. . . Схема трёхкоридорного аэротенка.
 Очистка от органических веществ Аэробный процесс Для жизнедеятельности живых организмов необходимо поддерживать соответствующие условия: ─ температура процесса 20 -30 0 С; ─ р. Н среды 6, 5 -7, 5; ─ соотношение биогенных элементов БПКп : N : Р не более 100: 5: 1; ─ кислородный режим - не ниже 2 мг. О 2/л; ─ содержание токсичных веществ не выше: тетраэтилсвинца - 0, 001 мг/л, соединений бериллия, титана, шестивалентного хрома и оксида углерода - 0, 01 мг/л, соединений висмута, ванадия, кадмия и никеля - 0, 1 мг/л, сульфата меди - 0, 2 мг/л, цианистого калия - 2 мг/л и т. д.
Очистка от органических веществ Аэробный процесс Для жизнедеятельности живых организмов необходимо поддерживать соответствующие условия: ─ температура процесса 20 -30 0 С; ─ р. Н среды 6, 5 -7, 5; ─ соотношение биогенных элементов БПКп : N : Р не более 100: 5: 1; ─ кислородный режим - не ниже 2 мг. О 2/л; ─ содержание токсичных веществ не выше: тетраэтилсвинца - 0, 001 мг/л, соединений бериллия, титана, шестивалентного хрома и оксида углерода - 0, 01 мг/л, соединений висмута, ванадия, кадмия и никеля - 0, 1 мг/л, сульфата меди - 0, 2 мг/л, цианистого калия - 2 мг/л и т. д.
 Анаэробный процесс В этом случае происходит биологическое окисление органических веществ в отсутствие свободного кислорода за счёт химически связанного в таких соединениях, как SO 42 - , SO 32 - и CO 32 -. Основные технологические параметры процесса: • температура в мезофильных условиях 25 -37 0 С, термофильных - 50 -60 0 С; • р. Н от 6, 7 до 7, 4 (повышение р. Н вызывает снижение скорости процесса брожения, а при р. Н выше 8 оно прекращается); • концентрация органических веществ (по БПК) обычно выше 5000 мг. О 2/л, однако при высокой концентрации микроорганизмов (1 -3%) анаэробный процесс протекает и при более низком содержании органических веществ - вплоть до 1000 мг. О 2/л; • микробы чувствительны к наличию некоторых соединений, особенно пероксидов и хлор- и серосодержащих производных, поэтому в ряде случаев их приходится предварительно удалять.
Анаэробный процесс В этом случае происходит биологическое окисление органических веществ в отсутствие свободного кислорода за счёт химически связанного в таких соединениях, как SO 42 - , SO 32 - и CO 32 -. Основные технологические параметры процесса: • температура в мезофильных условиях 25 -37 0 С, термофильных - 50 -60 0 С; • р. Н от 6, 7 до 7, 4 (повышение р. Н вызывает снижение скорости процесса брожения, а при р. Н выше 8 оно прекращается); • концентрация органических веществ (по БПК) обычно выше 5000 мг. О 2/л, однако при высокой концентрации микроорганизмов (1 -3%) анаэробный процесс протекает и при более низком содержании органических веществ - вплоть до 1000 мг. О 2/л; • микробы чувствительны к наличию некоторых соединений, особенно пероксидов и хлор- и серосодержащих производных, поэтому в ряде случаев их приходится предварительно удалять.


