 ОСНОВНЫЕ ПОНЯТИЯ В ХИМИИ
ОСНОВНЫЕ ПОНЯТИЯ В ХИМИИ
 Химия – это наука о превращениях веществ, связанных с изменением электронного окружения атомных ядер
Химия – это наука о превращениях веществ, связанных с изменением электронного окружения атомных ядер
 Вещество – вид материи, которая обладает массой покоя. Состоит из элементарных частиц: электронов, протонов, нейтронов, мезонов и др. Химия изучает главным образом вещество, организованное в атомы, молекулы, ионы и радикалы. Такие вещества принято подразделять на простые и сложные (хим. соединения).
Вещество – вид материи, которая обладает массой покоя. Состоит из элементарных частиц: электронов, протонов, нейтронов, мезонов и др. Химия изучает главным образом вещество, организованное в атомы, молекулы, ионы и радикалы. Такие вещества принято подразделять на простые и сложные (хим. соединения).
 Простые вещества образованы атомами одного хим. элемента и потому являются формой его существования в свободном состоянии, например, сера, железо, озон, алмаз. Сложные вещества образованы разными элементами и могут иметь состав постоянный (стехиометрические соединения или дальтониды) или меняющийся в некоторых пределах (нестехиометрические соединения или бертоллиды).
Простые вещества образованы атомами одного хим. элемента и потому являются формой его существования в свободном состоянии, например, сера, железо, озон, алмаз. Сложные вещества образованы разными элементами и могут иметь состав постоянный (стехиометрические соединения или дальтониды) или меняющийся в некоторых пределах (нестехиометрические соединения или бертоллиды).
 Атом (от греч. atomos – неделимый), наименьшая частица химического элемента, носитель его свойств. Имеет диаметр несколько десятимиллиардных долей метра (порядка 10– 10 м) и массу порядка 10– 24− 10– 25 кг.
Атом (от греч. atomos – неделимый), наименьшая частица химического элемента, носитель его свойств. Имеет диаметр несколько десятимиллиардных долей метра (порядка 10– 10 м) и массу порядка 10– 24− 10– 25 кг.
 Молекула (новолат. molecula, уменьшит. от лат. moles – масса), микрочастица, образованная из двух или большего числа атомов и способная к самостоятельному существованию.
Молекула (новолат. molecula, уменьшит. от лат. moles – масса), микрочастица, образованная из двух или большего числа атомов и способная к самостоятельному существованию.
 Ионы (от греч. ion – идущий), одноатомные или многоатомные частицы, несущие электрический заряд. Положительные ионы называют катионами (от греч. kation, буквально – идущий вниз), отрицательные – анионами (от греч. anion, буквально идущий вверх).
Ионы (от греч. ion – идущий), одноатомные или многоатомные частицы, несущие электрический заряд. Положительные ионы называют катионами (от греч. kation, буквально – идущий вниз), отрицательные – анионами (от греч. anion, буквально идущий вверх).
 Валентность (от лат. valentia – сила), способность атома присоединять или замещать определенное число других атомов или атомных групп с образованием химической связи.
Валентность (от лат. valentia – сила), способность атома присоединять или замещать определенное число других атомов или атомных групп с образованием химической связи.
 Степень окисления —условный электростатический заряд атома в молекуле исходя из предположения, что все химические связи в соединении только ионные. Степень окисления соответствует заряду иона или формальному заряду атома в молекуле или в химической формальной единице.
Степень окисления —условный электростатический заряд атома в молекуле исходя из предположения, что все химические связи в соединении только ионные. Степень окисления соответствует заряду иона или формальному заряду атома в молекуле или в химической формальной единице.
 Химические элементы - вид атомов с одинаковым числом протонов в ядре называют. Известно 118 химических элементов (92 из них встречаются в природе). Они имеют названия и с 19 века обозначаются символами. Иногда слева от символа пишут 2 индекса: вверху − массовое число (A= число протонов + число нейтронов = Z+N), внизу − заряд ядра, он же порядковый номер элемента (Z= числу протонов). Например, 168 S.
Химические элементы - вид атомов с одинаковым числом протонов в ядре называют. Известно 118 химических элементов (92 из них встречаются в природе). Они имеют названия и с 19 века обозначаются символами. Иногда слева от символа пишут 2 индекса: вверху − массовое число (A= число протонов + число нейтронов = Z+N), внизу − заряд ядра, он же порядковый номер элемента (Z= числу протонов). Например, 168 S.
 Характеристики размеров атомных частиц в веществах: • Ковалентный радиус • Металлический радиус • Ионный радиус • Радиус Ван-дер-Ваальса
Характеристики размеров атомных частиц в веществах: • Ковалентный радиус • Металлический радиус • Ионный радиус • Радиус Ван-дер-Ваальса
 Изотопами называются атомы с одинаковым зарядом ядра и разным числом нейтронов (и поэтому − разной массой). Обычно в природе химические элементы представлены в виде смеси изотопов, поэтому в периодической системе некоторые атомные массы сильно отличаются от целых чисел.
Изотопами называются атомы с одинаковым зарядом ядра и разным числом нейтронов (и поэтому − разной массой). Обычно в природе химические элементы представлены в виде смеси изотопов, поэтому в периодической системе некоторые атомные массы сильно отличаются от целых чисел.
 Поскольку атомы очень маленькие, их чаще всего рассматривают большими наборами. Обычно количество вещества измеряют в молях. Моль − это 6, 022∙ 1023 объектов. Данное число называют ещё числом Авогадро NA. Число молей n называют количеством вещества, n = N/NA , где N − число объктов. 1 моль атомов водорода имеет массу примерно 1 грамм. Удобно то, что масса моля атомов в граммах почти точно равна массовому числу.
Поскольку атомы очень маленькие, их чаще всего рассматривают большими наборами. Обычно количество вещества измеряют в молях. Моль − это 6, 022∙ 1023 объектов. Данное число называют ещё числом Авогадро NA. Число молей n называют количеством вещества, n = N/NA , где N − число объктов. 1 моль атомов водорода имеет массу примерно 1 грамм. Удобно то, что масса моля атомов в граммах почти точно равна массовому числу.
 Относительная атомная масса – это масса атома, выраженная в атомных единицах массы. За атомную единицу массы принята 1/12 часть массы атома углерода: 1 а. е. м. = 1/12 ma(C) = 1, 993. 10 -23/12 = 1, 661. 10 -27 кг Относительная атомная масса – величина безразмерная
Относительная атомная масса – это масса атома, выраженная в атомных единицах массы. За атомную единицу массы принята 1/12 часть массы атома углерода: 1 а. е. м. = 1/12 ma(C) = 1, 993. 10 -23/12 = 1, 661. 10 -27 кг Относительная атомная масса – величина безразмерная
 Относительная молекулярная масса (Mr) вещества – это масса его молекулы, выраженная в а. е. м. Молекулярная масса численно равна сумме атомных масс всех атомов, образующих молекулу вещества. Например, для серной кислоты: Мr (H 2 SO 4) = 2 1, 00797 + 32, 06 + 15, 999 4 = 98, 07194. Молекула серной кислоты в 98, 07194 раз тяжелее 1/12 массы атома углерода-12.
Относительная молекулярная масса (Mr) вещества – это масса его молекулы, выраженная в а. е. м. Молекулярная масса численно равна сумме атомных масс всех атомов, образующих молекулу вещества. Например, для серной кислоты: Мr (H 2 SO 4) = 2 1, 00797 + 32, 06 + 15, 999 4 = 98, 07194. Молекула серной кислоты в 98, 07194 раз тяжелее 1/12 массы атома углерода-12.
 Молярная масса (М) - масса одного моля или масса 6, 02 1023 структурных единиц. Молярная масса измеряется в кг/моль или г/моль. Численно молярная масса равна атомной или молекулярной массе. Например, Аr(О) = 15, 9994 6, 02 1023 атомов кислорода имеют массу 15, 9994 10 -3 кг M(О) =15, 9994 10 -3 кг. Между массой вещества (m), количеством вещества (ν) и молярной массой (M) существует простое соотношение: m = M ν
Молярная масса (М) - масса одного моля или масса 6, 02 1023 структурных единиц. Молярная масса измеряется в кг/моль или г/моль. Численно молярная масса равна атомной или молекулярной массе. Например, Аr(О) = 15, 9994 6, 02 1023 атомов кислорода имеют массу 15, 9994 10 -3 кг M(О) =15, 9994 10 -3 кг. Между массой вещества (m), количеством вещества (ν) и молярной массой (M) существует простое соотношение: m = M ν
 СТЕХИОМЕТРИЯ Стехиометрия - раздел химии, в котором изучаются количественный состав веществ и соотношения между количествами реагентов, вступающих в реакцию, и количествами продуктов, образующихся в результате реакции.
СТЕХИОМЕТРИЯ Стехиометрия - раздел химии, в котором изучаются количественный состав веществ и соотношения между количествами реагентов, вступающих в реакцию, и количествами продуктов, образующихся в результате реакции.
 Стехиометрические коэффициенты – числа, стоящие перед формулами веществ в уравнениях реакций. 4 Cd + 10 HNO 3 = 4 Cd(NO 3)2 +NH 4 NO 3 +3 H 2 O Стехиометрические индексы – это числа, стоящие в химических формулах справа внизу при символах химических элементов. Cd 3 As 2
Стехиометрические коэффициенты – числа, стоящие перед формулами веществ в уравнениях реакций. 4 Cd + 10 HNO 3 = 4 Cd(NO 3)2 +NH 4 NO 3 +3 H 2 O Стехиометрические индексы – это числа, стоящие в химических формулах справа внизу при символах химических элементов. Cd 3 As 2
 ЗАКОНЫ СТЕХИОМЕТРИИ 1. Закон сохранения массы. Открыт в 1760 г. М. В. Ломоносовым, сформулирован в 1789 г. А. Лавуазье: Общая масса веществ, вступающих в химическую реакцию, равна общей массе продуктов реакции. Пример: 130 гр 32 гр 162 гр 2 Zn + O 2 = 2 Zn. O
ЗАКОНЫ СТЕХИОМЕТРИИ 1. Закон сохранения массы. Открыт в 1760 г. М. В. Ломоносовым, сформулирован в 1789 г. А. Лавуазье: Общая масса веществ, вступающих в химическую реакцию, равна общей массе продуктов реакции. Пример: 130 гр 32 гр 162 гр 2 Zn + O 2 = 2 Zn. O
 2. Закон кратных отношений Открыт Д. Дальтоном в 1803 г. Если два элемента образуют между собой более одного соединения, то массы одного элемента, приходящиеся на одну и ту же массу другого элемента, относятся между собой как небольшие целые числа. Рассмотрим на примере оксидов азота.
2. Закон кратных отношений Открыт Д. Дальтоном в 1803 г. Если два элемента образуют между собой более одного соединения, то массы одного элемента, приходящиеся на одну и ту же массу другого элемента, относятся между собой как небольшие целые числа. Рассмотрим на примере оксидов азота.
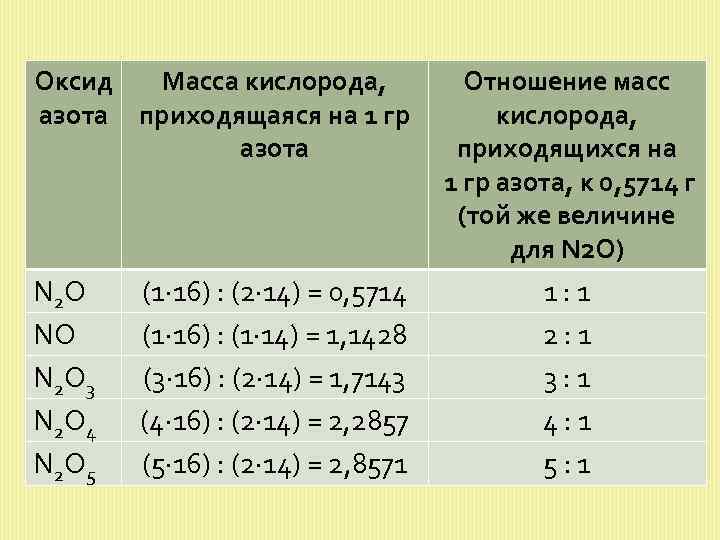 Оксид Масса кислорода, азота приходящаяся на 1 гр азота N 2 O NO N 2 O 3 N 2 O 4 N 2 O 5 (1∙ 16) : (2∙ 14) = 0, 5714 (1∙ 16) : (1∙ 14) = 1, 1428 (3∙ 16) : (2∙ 14) = 1, 7143 (4∙ 16) : (2∙ 14) = 2, 2857 (5∙ 16) : (2∙ 14) = 2, 8571 Отношение масс кислорода, приходящихся на 1 гр азота, к 0, 5714 г (той же величине для N 2 O) 1 : 1 2 : 1 3 : 1 4 : 1 5 : 1
Оксид Масса кислорода, азота приходящаяся на 1 гр азота N 2 O NO N 2 O 3 N 2 O 4 N 2 O 5 (1∙ 16) : (2∙ 14) = 0, 5714 (1∙ 16) : (1∙ 14) = 1, 1428 (3∙ 16) : (2∙ 14) = 1, 7143 (4∙ 16) : (2∙ 14) = 2, 2857 (5∙ 16) : (2∙ 14) = 2, 8571 Отношение масс кислорода, приходящихся на 1 гр азота, к 0, 5714 г (той же величине для N 2 O) 1 : 1 2 : 1 3 : 1 4 : 1 5 : 1
 3. Закон постоянства состава Сформулирован Ж. Прустом в 1808 г. Каждое химическое соединение независимо от способа его получения состоит из одних и тех же элементов, причем отношения их масс постоянны, а относительные количества их атомов выражаются целыми числами.
3. Закон постоянства состава Сформулирован Ж. Прустом в 1808 г. Каждое химическое соединение независимо от способа его получения состоит из одних и тех же элементов, причем отношения их масс постоянны, а относительные количества их атомов выражаются целыми числами.
 4. Закон простых обьемных отношений Открыт Ж. Л. Гей–Люссаком в 1808 году. При неизменных температуре и давлении объемы вступающих в реакцию газов относятся друг к другу, а также к объемам образующихся газообразных продуктов как небольшие целые числа. 2 H 2 + O 2 = 2 H 2 O (пар) V = 44, 8 л V = 22, 4 л V = 44, 8 л V(H 2) : V(O 2) : V(H 2 O пар) = 2 : 1 : 2
4. Закон простых обьемных отношений Открыт Ж. Л. Гей–Люссаком в 1808 году. При неизменных температуре и давлении объемы вступающих в реакцию газов относятся друг к другу, а также к объемам образующихся газообразных продуктов как небольшие целые числа. 2 H 2 + O 2 = 2 H 2 O (пар) V = 44, 8 л V = 22, 4 л V = 44, 8 л V(H 2) : V(O 2) : V(H 2 O пар) = 2 : 1 : 2
 5. Закон Авогадро Открыт в 1811 году А. Авагадро. В равных объемах различных газов при одинаковых условиях (температуре и давлении) содержится равное число молекул. Следствие: массы равных объемов различных газов при одинаковых температуре и давлении относятся друг к другу как молекулярные или молярные массы этих газов.
5. Закон Авогадро Открыт в 1811 году А. Авагадро. В равных объемах различных газов при одинаковых условиях (температуре и давлении) содержится равное число молекул. Следствие: массы равных объемов различных газов при одинаковых температуре и давлении относятся друг к другу как молекулярные или молярные массы этих газов.
 1 моль любого газа при нормальных условиях, т. е. при температуре 0 С (или 273, 15 К) и давлении 101, 325 к. Па занимает объем 22, 4 дм 3. Объем, занимаемый 1 моль газа, называется молярным объемом (Vm). При нормальных условиях Vm = 22, 4 л / моль. Связь между объемом газа и его количеством вещества: V = ν Vm
1 моль любого газа при нормальных условиях, т. е. при температуре 0 С (или 273, 15 К) и давлении 101, 325 к. Па занимает объем 22, 4 дм 3. Объем, занимаемый 1 моль газа, называется молярным объемом (Vm). При нормальных условиях Vm = 22, 4 л / моль. Связь между объемом газа и его количеством вещества: V = ν Vm
 Уравнение состояния идеальных газов, полученное посредством совмещения законов Бойля-Мориотта, Гей-Люссака и Авогадро, имеет следующий вид: P V = (m/M) R T где Р - давление газа, V - его объем, m - масса газа, M - молярная масса, R - универсальная газовая постоянная и Т - абсолютная температура. Уравнение состояния для идеальных газов получило название уравнения Менделеева. Клайперона.
Уравнение состояния идеальных газов, полученное посредством совмещения законов Бойля-Мориотта, Гей-Люссака и Авогадро, имеет следующий вид: P V = (m/M) R T где Р - давление газа, V - его объем, m - масса газа, M - молярная масса, R - универсальная газовая постоянная и Т - абсолютная температура. Уравнение состояния для идеальных газов получило название уравнения Менделеева. Клайперона.
 6. Закон эквивалентов Сформулирован в 1807 году У. Волластаном. Массы реагирующих веществ относятся между собой как молярные массы их эквивалентов.
6. Закон эквивалентов Сформулирован в 1807 году У. Волластаном. Массы реагирующих веществ относятся между собой как молярные массы их эквивалентов.
 Эквивалент - это реальная или условная частица вещества, которая эквивалентна: а) одному иону Н+ или ОН- в данной кислотно -основной реакции; б) одному электрону в данной ОВР (окислительно-восстановительной реакции); в) одной единице заряда в данной реакции обмена, г) количеству монодентатных лигандов, участвующих в реакции образования комплекса.
Эквивалент - это реальная или условная частица вещества, которая эквивалентна: а) одному иону Н+ или ОН- в данной кислотно -основной реакции; б) одному электрону в данной ОВР (окислительно-восстановительной реакции); в) одной единице заряда в данной реакции обмена, г) количеству монодентатных лигандов, участвующих в реакции образования комплекса.
 Фактор эквивалентности (f) – число, обозначающее какая доля реальной частицы вещества эквивалетна одному катиону водорода в данной кислотно-основной реакции или одному электрону в данной окислительно-восстановительной реакции. f – величина безразмерная. Молярная масса эквивалента – масса 1 моль эквивалента.
Фактор эквивалентности (f) – число, обозначающее какая доля реальной частицы вещества эквивалетна одному катиону водорода в данной кислотно-основной реакции или одному электрону в данной окислительно-восстановительной реакции. f – величина безразмерная. Молярная масса эквивалента – масса 1 моль эквивалента.
 Величина Мэкв определяется или экспериментально, или, чаще всего, исходя из химической формулы вещества и его принадлежности к тому или иному классу химических соединений (мы будем рассматривать только неорганические соединения) Мэкв(оксида) = Моксида/(число атомов кислорода∙ 2); Мэкв(основания) = Моснования/кислотность основания; Мэкв(кислоты) = Мкислоты/основность кислоты; Мэкв(соли) = Мсоли/(число атомов металла∙валентность металла).
Величина Мэкв определяется или экспериментально, или, чаще всего, исходя из химической формулы вещества и его принадлежности к тому или иному классу химических соединений (мы будем рассматривать только неорганические соединения) Мэкв(оксида) = Моксида/(число атомов кислорода∙ 2); Мэкв(основания) = Моснования/кислотность основания; Мэкв(кислоты) = Мкислоты/основность кислоты; Мэкв(соли) = Мсоли/(число атомов металла∙валентность металла).
 Для соединений переменного состава вводится понятие формульная масса, вместо молекулярная масса. Так формулу сульфида железа, у которого атомное содержание железа составляет 45% следует писать: Fe 0, 9 S. Формульная масса этого вещества равна: МФ (Fe 0, 9 S) = 0, 9 ∙ 56 + 32 = 82, 4 г/моль. Составы, укладывающиеся внутри граничных значений нарушения стехиометрического состава называется областью нестехиометрии. Так, для соединения Fe 0, 9 -1 S область нестехиометрии Х составляет: 0, 1 - 0 или 0 X < 0, 1.
Для соединений переменного состава вводится понятие формульная масса, вместо молекулярная масса. Так формулу сульфида железа, у которого атомное содержание железа составляет 45% следует писать: Fe 0, 9 S. Формульная масса этого вещества равна: МФ (Fe 0, 9 S) = 0, 9 ∙ 56 + 32 = 82, 4 г/моль. Составы, укладывающиеся внутри граничных значений нарушения стехиометрического состава называется областью нестехиометрии. Так, для соединения Fe 0, 9 -1 S область нестехиометрии Х составляет: 0, 1 - 0 или 0 X < 0, 1.


