Основные понятия и законы химии










Основные понятия и законы химии 2.ppt
- Количество слайдов: 10
 Основные понятия и законы химии Основные газовые законы
Основные понятия и законы химии Основные газовые законы
 Основные газовые законы Закон Дальтона для смеси газов Параметры состояния системы P = p 1 + p 2 + … + pn = Р – давление n – число моль вещества P – общее давление рi – парциальное давление ni – число моль i-го газа n – общее число моль всех газов в смеси
Основные газовые законы Закон Дальтона для смеси газов Параметры состояния системы P = p 1 + p 2 + … + pn = Р – давление n – число моль вещества P – общее давление рi – парциальное давление ni – число моль i-го газа n – общее число моль всех газов в смеси
 Основные газовые законы Закон Бойля и Мариотта (1662) Параметры состояния При постоянной температуре системы (Т = Const) Р – давление V – объём P 1 V 1 = P 2 V 2 или PV = Const
Основные газовые законы Закон Бойля и Мариотта (1662) Параметры состояния При постоянной температуре системы (Т = Const) Р – давление V – объём P 1 V 1 = P 2 V 2 или PV = Const
 Основные газовые законы Закон Шарля и Гей-Люссака (1802) Параметры При постоянном давлении состояния системы (P = Const) V – объём Т – температура
Основные газовые законы Закон Шарля и Гей-Люссака (1802) Параметры При постоянном давлении состояния системы (P = Const) V – объём Т – температура
 Основные газовые законы Объединенный закон газового состояния (Клапейрон) Параметры состояния При нормальных условиях системы или Нормальные условия: Р – давление Р 0=101325 Па = 760 мм рт. ст. Т 0=273 К V – объём V 0(для 1 моль газа)=22, 4 л=22400 мл Т – температура Универсальная газовая постоянная R=8, 31 = 62360
Основные газовые законы Объединенный закон газового состояния (Клапейрон) Параметры состояния При нормальных условиях системы или Нормальные условия: Р – давление Р 0=101325 Па = 760 мм рт. ст. Т 0=273 К V – объём V 0(для 1 моль газа)=22, 4 л=22400 мл Т – температура Универсальная газовая постоянная R=8, 31 = 62360
 Основные газовые законы Закон Авогадро (1811) Параметры состояния В равных объемах разных газов системы при одинаковых условиях (Р, Т) содержится одинаковое число частиц этих газов. n – число моль газа Следствия: m – масса газа I. При нормальных условиях (Т 0, Р 0) 1 моль любого газа занимает объем V 0 М – молярная масса = 22, 4 л II. 1 моль любого вещества состоит из NA = 6. 02*1023 частиц NA – число Авогадро III. Если Х и Y газы, такие, что Vx=Vy, то – относительная плотность газа Х по газу Y.
Основные газовые законы Закон Авогадро (1811) Параметры состояния В равных объемах разных газов системы при одинаковых условиях (Р, Т) содержится одинаковое число частиц этих газов. n – число моль газа Следствия: m – масса газа I. При нормальных условиях (Т 0, Р 0) 1 моль любого газа занимает объем V 0 М – молярная масса = 22, 4 л II. 1 моль любого вещества состоит из NA = 6. 02*1023 частиц NA – число Авогадро III. Если Х и Y газы, такие, что Vx=Vy, то – относительная плотность газа Х по газу Y.
 Основные газовые законы Уравнение Клапейрона-Менделеева (1874) Параметры состояния системы Для n моль газа Т – температура V – объём Р – давление n – число моль газа М – молярная масса m – масса газа
Основные газовые законы Уравнение Клапейрона-Менделеева (1874) Параметры состояния системы Для n моль газа Т – температура V – объём Р – давление n – число моль газа М – молярная масса m – масса газа
 Основные газовые законы Закон объемных отношений газов (Гей-Люссак, 1808) Параметры состояния Объемы газов, участвующих в системы реакции, относятся как стехио- метрические коэффициенты. Если X и Y – газы, участвующие в m – масса реакции V – объём а. А + х. Х в. В + y. Y, то М – молярная масса и
Основные газовые законы Закон объемных отношений газов (Гей-Люссак, 1808) Параметры состояния Объемы газов, участвующих в системы реакции, относятся как стехио- метрические коэффициенты. Если X и Y – газы, участвующие в m – масса реакции V – объём а. А + х. Х в. В + y. Y, то М – молярная масса и
 Основные газовые законы Некоторые понятия и определения Атомная единица массы (а. е. м. ) 1 а. е. м. = =1, 66*10 -24 г Молекулярная масса М Масса молекулы в а. е. м. : для Н 2 М=2 для H 2 SO 4 М=98 Молярная масса Масса моль вещества в г М для Н 2 М=2 г/моль для H 2 SO 4 М=98 г/моль Число моль вещества n
Основные газовые законы Некоторые понятия и определения Атомная единица массы (а. е. м. ) 1 а. е. м. = =1, 66*10 -24 г Молекулярная масса М Масса молекулы в а. е. м. : для Н 2 М=2 для H 2 SO 4 М=98 Молярная масса Масса моль вещества в г М для Н 2 М=2 г/моль для H 2 SO 4 М=98 г/моль Число моль вещества n
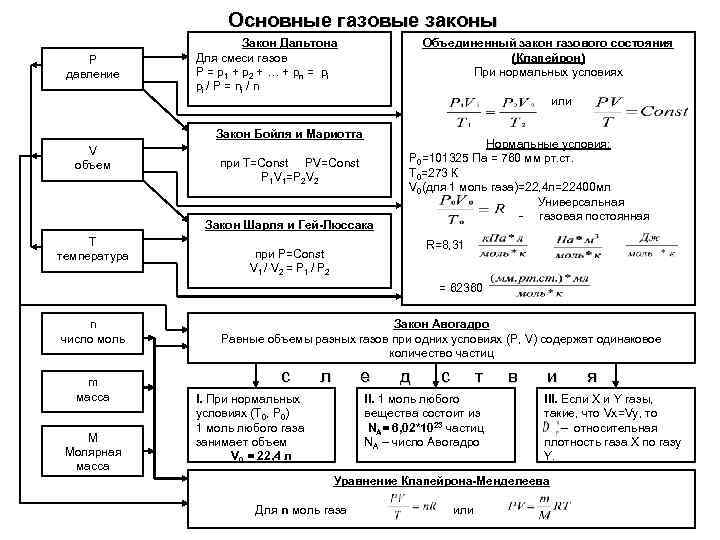
 Основные газовые законы Закон Дальтона Объединенный закон газового состояния Р Для смеси газов (Клапейрон) давление P = p 1 + p 2 + … + pn = pi При нормальных условиях pi / P = ni / n или Закон Бойля и Мариотта Нормальные условия: V при T=Const PV=Const Р 0=101325 Па = 760 мм рт. ст. объем P 1 V 1=P 2 V 2 Т 0=273 К V 0(для 1 моль газа)=22, 4 л=22400 мл Универсальная - газовая постоянная Закон Шарля и Гей-Люссака Т R=8, 31 температура при P=Const V 1 / V 2 = P 1 / P 2 = 62360 n Закон Авогадро число моль Равные объемы разных газов при одних условиях (P, V) содержат одинаковое количество частиц m с л е д с т в и я масса I. При нормальных II. 1 моль любого III. Если Х и Y газы, условиях (Т 0, Р 0) вещества состоит из такие, что Vx=Vy, то 1 моль любого газа NA= 6, 02*1023 частиц – относительная М занимает объем NA – число Авогадро плотность газа Х по газу Молярная V 0 = 22, 4 л Y. масса Уравнение Клапейрона-Менделеева Для n моль газа или
Основные газовые законы Закон Дальтона Объединенный закон газового состояния Р Для смеси газов (Клапейрон) давление P = p 1 + p 2 + … + pn = pi При нормальных условиях pi / P = ni / n или Закон Бойля и Мариотта Нормальные условия: V при T=Const PV=Const Р 0=101325 Па = 760 мм рт. ст. объем P 1 V 1=P 2 V 2 Т 0=273 К V 0(для 1 моль газа)=22, 4 л=22400 мл Универсальная - газовая постоянная Закон Шарля и Гей-Люссака Т R=8, 31 температура при P=Const V 1 / V 2 = P 1 / P 2 = 62360 n Закон Авогадро число моль Равные объемы разных газов при одних условиях (P, V) содержат одинаковое количество частиц m с л е д с т в и я масса I. При нормальных II. 1 моль любого III. Если Х и Y газы, условиях (Т 0, Р 0) вещества состоит из такие, что Vx=Vy, то 1 моль любого газа NA= 6, 02*1023 частиц – относительная М занимает объем NA – число Авогадро плотность газа Х по газу Молярная V 0 = 22, 4 л Y. масса Уравнение Клапейрона-Менделеева Для n моль газа или

