c9248e355bb7d55018b45497891e45bf.ppt
- Количество слайдов: 19

Основные положения метода молекулярных орбиталей. Приближение МО ЛКАО

Электронный гамильтониан N-атомной молекулы в приближении БО • В приближении Борна – Оппенгеймера электронный гамильтониан молекулы, содержащей N ядер и n электронов, имеет вид: • В принципе, такой гамильтониан можно ввести в вариационный интеграл и рассчитать энергии электронных состояний молекул. Необходимо только выяснить, какие идеи следует положить в основу поиска формы волновой функции.

Метод валентных связей (ВС) • В основе метода валентных связей (ВС) лежит предположение, что химическая связь между двумя атомами осуществляется с помощью одной или нескольких электронных пар, которые локализованы преимущественно между ними. • В методе ВС химическая связь всегда двухэлектронная и обязательно двухцентровая. В образовании химической связи принимают участие валентные электроны. Волновая функция, описывающая состояние электронов, образующих связь, называется локализованной орбиталью (ЛО). • Электроны, описываемые ЛО, в соответствии с принципом Паули должны иметь противоположно направленные спины, т. е. в методе ВС все спины спарены, и все молекулы должны быть диамагнитны. Следовательно, метод ВС принципиально не может объяснить магнитные свойства молекул.

Метод молекулярных орбиталей (МО) • В методе МО полная волновая функция молекулы строится из функций, описывающих поведение отдельных электронов в поле, создаваемом остальными электронами и всеми атомными ядрами, которые образуют молекулярный остов. В основе метода МО лежат следующие положения: 1. Молекула рассматривается как целое, а не как совокупность сохраняющих некоторую индивидуальность атомов. Каждый электрон принадлежит молекуле в целом и движется в поле всех её ядер и электронов. 2. Состояние электрона описывается одноэлектронной волновой функцией i, которая называется молекулярной орбиталью (МО). В отличие от одноцентровой АО, молекулярная орбиталь в общем случае многоцентровая, т. к. число ядер в молекуле не менее двух. • В отличие от метода ВС в методе МО простейшая химическая связь может быть как двух-, так и многоцентровой.

Метод молекулярных орбиталей • Исходная идея метода МО примыкает к концепции АО. Значение этой аналогии состоит в возможности перенесения в теорию МО всех основных положений теории и методов описания многоэлектронных атомов. • Подобно АО, МО представляет собой одноэлектронную функцию (т. е. явно зависящую от координат только одного электрона), которая включает пространственную и спиновую части – спин -орбиталь: • Каждая МО характеризуется своим значением энергии, и все электроны молекулы располагаются попарно на МО, заполняя их в порядке повышения энергии.

Метод молекулярных орбиталей • Полная волновая функция молекулы, содержащей 2 n электронов на n попарно заполненных МО, описывается определителем Слейтера, а полная энергия молекулы с волновой функцией такого типа определяется обычным соотношением • Таким образом, аппарат теории многоэлектронного атома легко переносится на случай молекулы в приближении МО, и основная задача метода МО заключается в нахождении пространственных функций i, на основе которых и будет вычисляться полная энергия. • В принципе для нахождения одноэлектронных функций МО можно использовать метод Хартри – Фока и получить таблицы их числовых значений подобно тому, как это делается для атома.

Метод молекулярных орбиталей • Такой путь ведёт к лучшим возможным значениям молекулярных волновых функций и применяется для некоторых двухатомных молекул. Его недостатком кроме отсутствия решения в аналитическом виде являются большие математические трудности, которые в случае атома частично устраняются наличием центральной симметрии системы. • Для молекул соображения симметрии также весьма важны, т. к. очевидно, что МО должна характеризоваться теми же элементами симметрии, какими обладает сама молекула (конфигурация её атомных ядер). • Однако эти соображения лишь ограничивают, но отнюдь не определяют вид волновой функции МО. Из различных приближений, которые можно применить для построения МО, наилучшим является приближение молекулярной орбитали в виде линейной комбинации атомных орбиталей (МО ЛКАО) атомов, образующих молекулу.

Приближение МО ЛКАО • В приближении МО ЛКАО молекулярная орбиталь φi записывается в виде линейной комбинации АО χν: • Здесь M – число базисных функций. • Форма записи волновой функции в виде ЛКАО имеет два существенных достоинства: 1. При «движении» электрона по МО, когда он находится вблизи ядра атома с номером ν, его поведение и его волновая функция должны «совпадать» с соответствующими характеристиками в атоме. Это требование хорошо обеспечивается разложением ЛКАО. 2. Форма записи в виде ЛКАО особенно удачна потому, что для нахождения неизвестных коэффициентов ciν может быть применён вариационный метод Ритца.

Уравнения Рутана • Приближение ЛКАО для поиска вида МО i и представление полной волновой функции молекулы в виде слейтеровского определителя ведёт в рамках метода ХФ с использованием гамильтониана в приближении БО к уравнениям, полученным в 1951 году Рутаном. • Эти уравнения являются приближением к уравнениям Хартри – Фока и лежат в основе почти всех современных неэмпирических методов расчёта сложных молекулярных систем. Они служат также исходными для развития всех основных полуэмпирических теорий метода МО. • Рассмотрим систему с замкнутыми оболочками, а МО представим в виде ЛКАО. Повторяя рассуждения, полностью аналогичные сделанным при выводе уравнений Хартри и применяя вариационный принцип Ритца, придём к уравнением Рутана (Хартри – Фока – Рутана).

Уравнения Рутана • Уравнения Рутана имеют вид ( = 1, 2, …, M ): • Здесь Sµν — матрица интегралов перекрывания, т. к. её элементы говорят о степени пространственного перекрывания АО µ и ν: • Fµν — матрица Фока (фокиан): • Суммирование по j в фокиане ведётся только по занятым МО.

Уравнения Рутана • В фокиан входят матричные элементы Hµν, которые определяют энергии электронов без учёта их взаимодействия друг с другом: • Величины , также входящие в фокиан – это интегралы межэлектронного взаимодействия: • Все волновые функции являются вещественными.

Уравнения Рутана • Уравнения Рутана аналогичны уравнениям в методе Ритца, но здесь матричные элементы фокиана Fµν зависят от коэффициентов ci , поэтому уравнения Рутана являются нелинейными однородными уравнениями относительно неизвестных величин ci. • Введём следующее обозначение: • Матрицу P называют матрицей порядков связей (матрицей плотности) между АО и . При помощи матрицы порядков связей можно переписать фокиан в новом виде: • Систему нелинейных однородных уравнений фокиана можно свести к системе линейных однородных уравнений с помощью процедуры самосогласования.

Самосогласование в методе Рутана • Общая схема самосогласования заключается в следующем. Задаются начальные коэффициенты ciν(0), с помощью которых вычисляют Fµν(0). Считая, что на этом этапе Fµν(0) не зависят от ciν, получим линейную и однородную систему уравнений: • Такая система имеет нетривиальные решения при условии равенства её определителя нулю: • Из векового уравнения находят корни εi(0). Далее подставляют εi(0) в предыдущую систему и вычисляют коэффициенты ciν(1). Затем коэффициенты ciν(1) снова подставляют в фокиан, вычисляют εi(1) и ciν(2) и т. д. • Эту процедуру повторяют до тех пор, пока полная энергия или матрица порядков связей для двух последовательных итераций не будут совпадать с заданной точностью для всех µ и ν.

Занятые и виртуальные орбитали • Количество собственных значений i и соответствующих им собственных функций i равно порядку векового уравнения, т. е. числу базисных функций M в разложении МО ЛКАО. • Определитель Слейтера, определяющий полную волновую функцию системы, строится из n занятых (n < M) электронами МО. • В минимизации полной энергии молекулы участвуют только занятые МО и, поскольку матричные элементы фокиана Fµν зависят только от P , а порядок связей рассчитывается из волновых функций только занятых орбиталей, только они могут рассматриваться как физически определённые. • Незанятые МО, получаемые из уравнений Рутана, не участвуют в минимизации полной энергии, поэтому их соответствие истинным энергетическим уровням молекулы не вполне определено. Такие уровни называют виртуальными.

Ограниченный и неограниченный методы ХФ • Рассмотренный случай системы с замкнутыми оболочками соответствует т. н. ограниченному методу Хартри – Фока (Restricted Hartree – Fock method, RHF). • Уравнения Рутана можно обобщить на случай таких электронных конфигураций, когда одни орбитали заполнены двумя электронами, а другие – одним. Такое приближение называется ограниченным методом Хартри – Фока для незамкнутых оболочек (Restricted Open Shell HF method, ROHF). • Другое обобщение заключается в том, что электроны со спинами и относятся к разным молекулярным орбиталям. В этом случае возникает два набора коэффициентов ciνα и ciνβ, а такое приближение носит название спиннеограниченной конфигурацией, или неограниченным методом Хартри – Фока (Unrestricted HF method, UHF).

Проблема вычисления интегралов в методе Рутана • Введение разложения по базисному набору сыграло большую роль в развитии квантовой химии и превратило математическую задачу численного решения системы связанных дифференциальных уравнений (как в атомных расчётах Хартри) в проблему вычисления трёх- ( ) и шестимерных ( ) интегралов и последующего решения системы алгебраических уравнений Рутана. • Если бы эти интегралы брались аналитически, то модель могла бы оказаться точной в том смысле, что можно было бы достичь хорошей арифметической точности даже в случае, когда основные приближения модели (использование одноконфигурационного детерминанта и конечного базиса) остаются неудовлетворительными.

Проблема вычисления интегралов в методе Рутана • В соответствии с идеями вариационного принципа, чем ближе к полному набору базис разложения МО по АО, т. е. чем больше число базисных функций M, тем более точные решения для МО могут быть получены. С этой точки зрения в наиболее точных расчётах стремятся к увеличению базиса. Однако эта тенденция встречает серьёзные ограничения. • Для того чтобы провести расчёты по схеме Рутана, необходимо вычислить в первую очередь все слагаемые, входящие в матричные элементы фокиана Fµν. • Основная трудность, определяющая требуемое для расчёта время работы компьютера, связана с вычислением интегралов .

Проблема вычисления интегралов в методе Рутана • Подсчитано, что число p одноэлектронных интегралов типа Sµν и Hµν связано с размером базиса M следующим соотношением: • Число q двухэлектронных интегралов типа равно: • Общее число интегралов • Таким образом, с ростом базиса число интегралов резко (при больших значениях M примерно пропорционально M 4) возрастает.
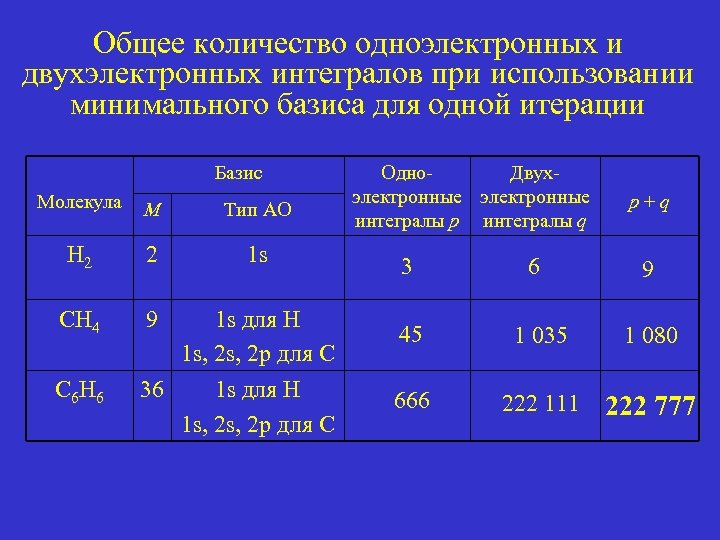
Общее количество одноэлектронных и двухэлектронных интегралов при использовании минимального базиса для одной итерации Базис Молекула M Тип АО H 2 2 1 s CH 4 9 C 6 H 6 1 s для H 1 s, 2 p для С 36 1 s для H 1 s, 2 p для С Одно. Двухэлектронные интегралы p интегралы q p + q 3 6 9 45 1 035 1 080 666 222 111 222 777
c9248e355bb7d55018b45497891e45bf.ppt