Belki_Uglevody.pptx
- Количество слайдов: 31
 ОСНОВНЫЕ ОРГАНИЧЕСКИЕ ВЕЩЕСТВА ПИЩИ ЧАСТЬ 1 Гарафутдинова М. А. 2013 г.
ОСНОВНЫЕ ОРГАНИЧЕСКИЕ ВЕЩЕСТВА ПИЩИ ЧАСТЬ 1 Гарафутдинова М. А. 2013 г.
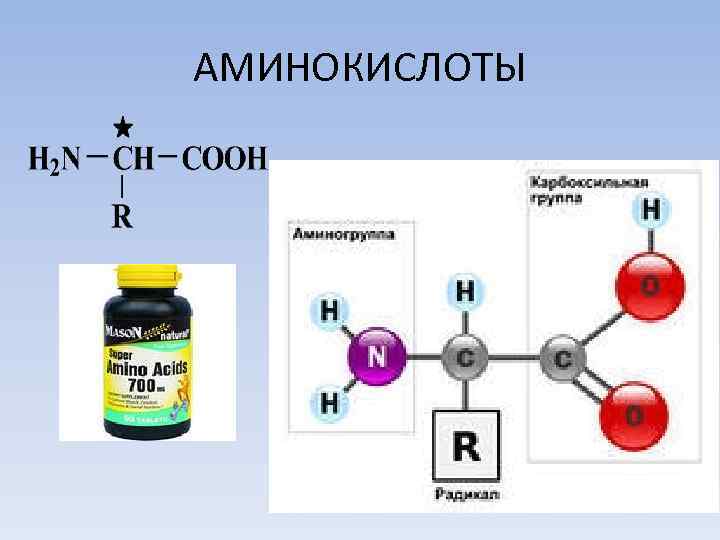 АМИНОКИСЛОТЫ
АМИНОКИСЛОТЫ
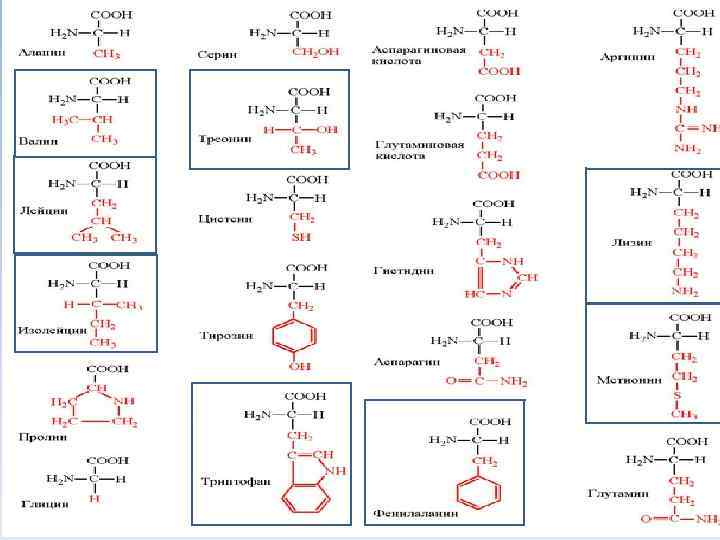
 КЛАССИФИКАЦИЯ АМИНОКИСЛОТ • 1. Незаменимые АК - не могут быть синтезированы организмом из веществ, поступающих с пищей, в количествах, достаточных для того, чтобы удовлетворить физиологические потребности организма. • 2. Заменимые АК В клетках и тканях встречается свыше 170 различных аминокислот. В составе белков обнаруживаются лишь 26 из них; обычными же компонентами белка можно считать лишь 20 аминокислот
КЛАССИФИКАЦИЯ АМИНОКИСЛОТ • 1. Незаменимые АК - не могут быть синтезированы организмом из веществ, поступающих с пищей, в количествах, достаточных для того, чтобы удовлетворить физиологические потребности организма. • 2. Заменимые АК В клетках и тканях встречается свыше 170 различных аминокислот. В составе белков обнаруживаются лишь 26 из них; обычными же компонентами белка можно считать лишь 20 аминокислот
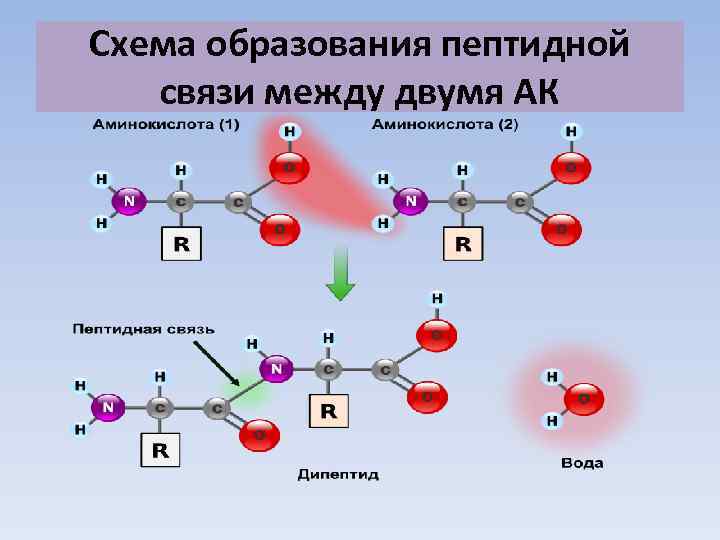 Схема образования пептидной связи между двумя АК
Схема образования пептидной связи между двумя АК
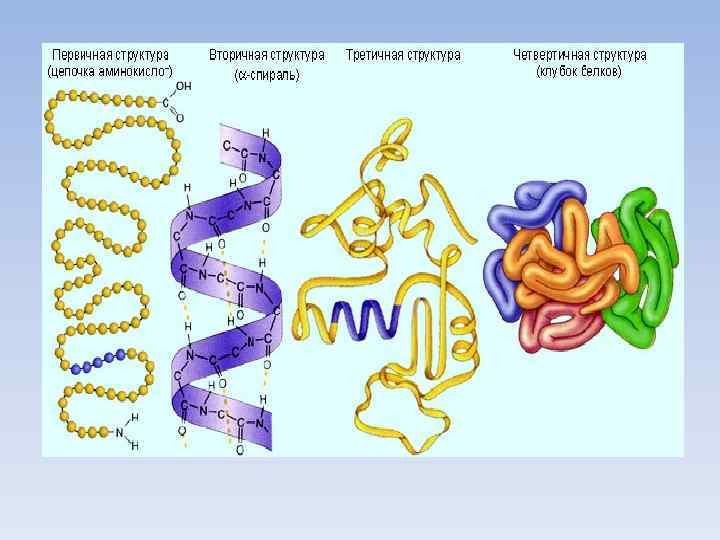
 Структура белков 1. Первичная последовательность соединений аминокислотных остатков в полипептидной цепи
Структура белков 1. Первичная последовательность соединений аминокислотных остатков в полипептидной цепи
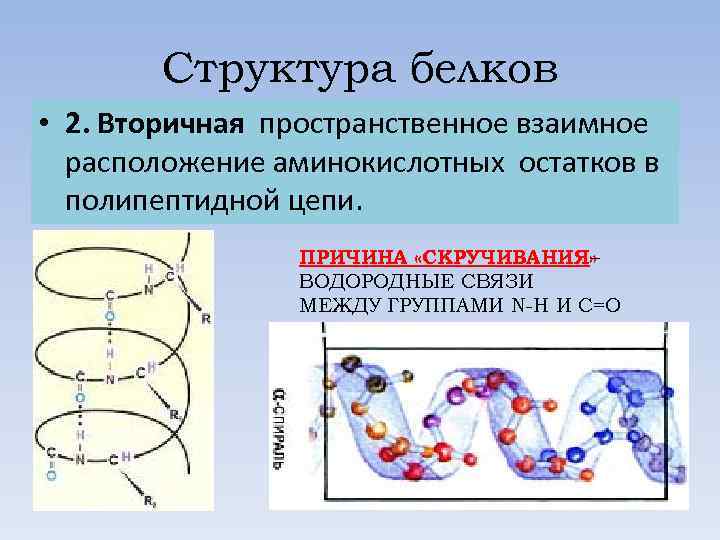 Структура белков • 2. Вторичная пространственное взаимное расположение аминокислотных остатков в полипептидной цепи. ПРИЧИНА «СКРУЧИВАНИЯ» – ВОДОРОДНЫЕ СВЯЗИ МЕЖДУ ГРУППАМИ N-H И С=О
Структура белков • 2. Вторичная пространственное взаимное расположение аминокислотных остатков в полипептидной цепи. ПРИЧИНА «СКРУЧИВАНИЯ» – ВОДОРОДНЫЕ СВЯЗИ МЕЖДУ ГРУППАМИ N-H И С=О
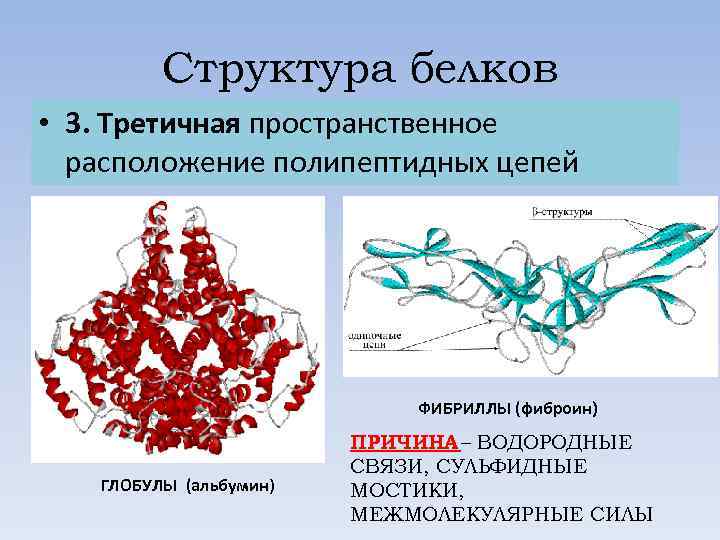 Структура белков • 3. Третичная пространственное расположение полипептидных цепей ФИБРИЛЛЫ (фиброин) ГЛОБУЛЫ (альбумин) ПРИЧИНА – ВОДОРОДНЫЕ СВЯЗИ, СУЛЬФИДНЫЕ МОСТИКИ, МЕЖМОЛЕКУЛЯРНЫЕ СИЛЫ
Структура белков • 3. Третичная пространственное расположение полипептидных цепей ФИБРИЛЛЫ (фиброин) ГЛОБУЛЫ (альбумин) ПРИЧИНА – ВОДОРОДНЫЕ СВЯЗИ, СУЛЬФИДНЫЕ МОСТИКИ, МЕЖМОЛЕКУЛЯРНЫЕ СИЛЫ
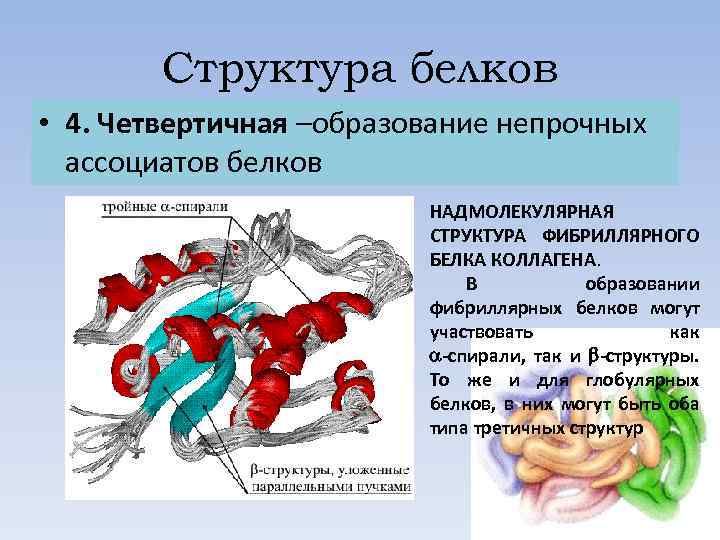 Структура белков • 4. Четвертичная –образование непрочных ассоциатов белков НАДМОЛЕКУЛЯРНАЯ СТРУКТУРА ФИБРИЛЛЯРНОГО БЕЛКА КОЛЛАГЕНА. В образовании фибриллярных белков могут участвовать как a-спирали, так и b-структуры. То же и для глобулярных белков, в них могут быть оба типа третичных структур
Структура белков • 4. Четвертичная –образование непрочных ассоциатов белков НАДМОЛЕКУЛЯРНАЯ СТРУКТУРА ФИБРИЛЛЯРНОГО БЕЛКА КОЛЛАГЕНА. В образовании фибриллярных белков могут участвовать как a-спирали, так и b-структуры. То же и для глобулярных белков, в них могут быть оба типа третичных структур
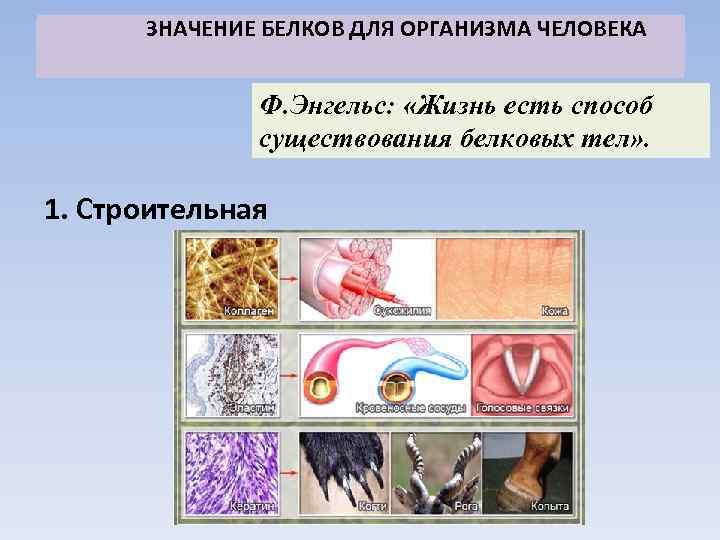 ЗНАЧЕНИЕ БЕЛКОВ ДЛЯ ОРГАНИЗМА ЧЕЛОВЕКА Ф. Энгельс: «Жизнь есть способ существования белковых тел» . 1. Строительная
ЗНАЧЕНИЕ БЕЛКОВ ДЛЯ ОРГАНИЗМА ЧЕЛОВЕКА Ф. Энгельс: «Жизнь есть способ существования белковых тел» . 1. Строительная
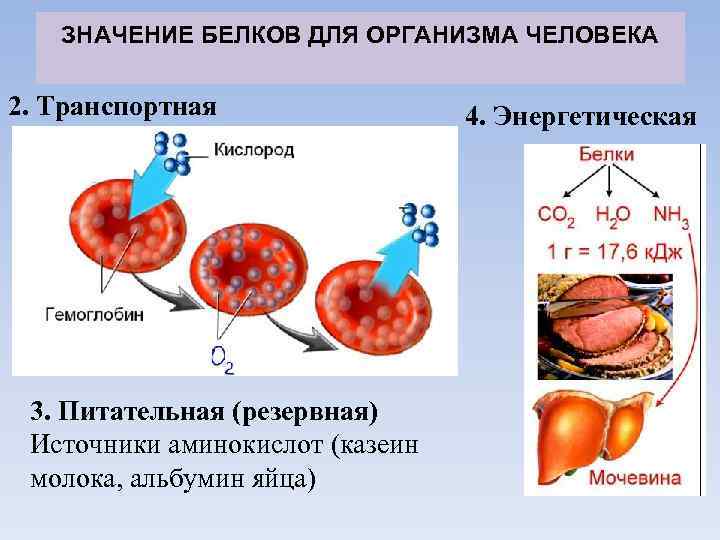 ЗНАЧЕНИЕ БЕЛКОВ ДЛЯ ОРГАНИЗМА ЧЕЛОВЕКА 2. Транспортная 3. Питательная (резервная) Источники аминокислот (казеин молока, альбумин яйца) 4. Энергетическая
ЗНАЧЕНИЕ БЕЛКОВ ДЛЯ ОРГАНИЗМА ЧЕЛОВЕКА 2. Транспортная 3. Питательная (резервная) Источники аминокислот (казеин молока, альбумин яйца) 4. Энергетическая
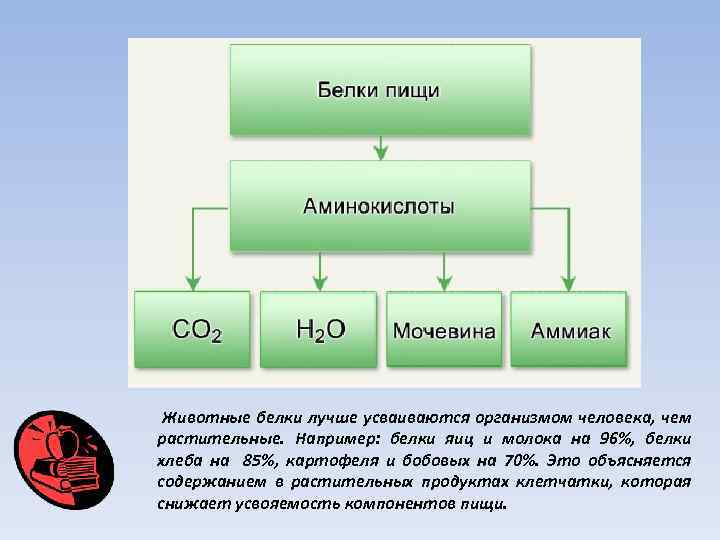 Животные белки лучше усваиваются организмом человека, чем растительные. Например: белки яиц и молока на 96%, белки хлеба на 85%, картофеля и бобовых на 70%. Это объясняется содержанием в растительных продуктах клетчатки, которая снижает усвояемость компонентов пищи.
Животные белки лучше усваиваются организмом человека, чем растительные. Например: белки яиц и молока на 96%, белки хлеба на 85%, картофеля и бобовых на 70%. Это объясняется содержанием в растительных продуктах клетчатки, которая снижает усвояемость компонентов пищи.
 ЗНАЧЕНИЕ БЕЛКОВ ДЛЯ ОРГАНИЗМА ЧЕЛОВЕКА 5. Каталитическая Белки –катализаторы -ферменты 6. Сигнальная и защитная (иммуноглобулины, лизоцим, антитела, лейкоциты) 7. Сократительная или двигательная
ЗНАЧЕНИЕ БЕЛКОВ ДЛЯ ОРГАНИЗМА ЧЕЛОВЕКА 5. Каталитическая Белки –катализаторы -ферменты 6. Сигнальная и защитная (иммуноглобулины, лизоцим, антитела, лейкоциты) 7. Сократительная или двигательная
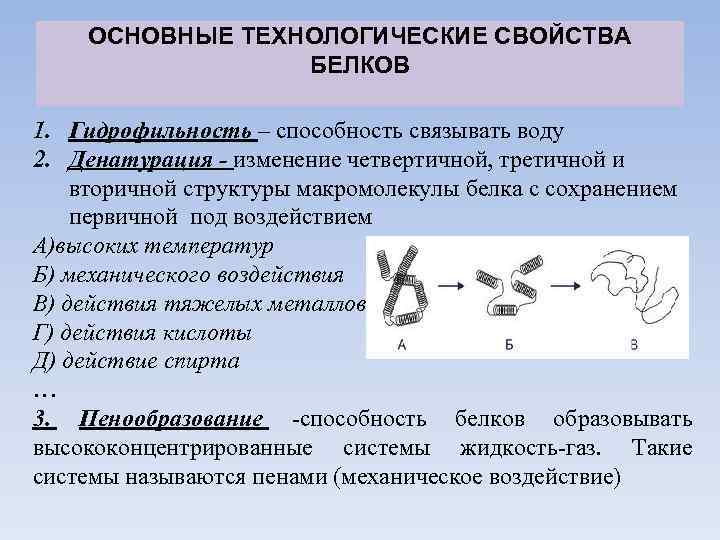 ОСНОВНЫЕ ТЕХНОЛОГИЧЕСКИЕ СВОЙСТВА БЕЛКОВ 1. Гидрофильность – способность связывать воду 2. Денатурация - изменение четвертичной, третичной и вторичной структуры макромолекулы белка с сохранением первичной под воздействием А)высоких температур Б) механического воздействия В) действия тяжелых металлов Г) действия кислоты Д) действие спирта … 3. Пенообразование -способность белков образовывать высококонцентрированные системы жидкость-газ. Такие системы называются пенами (механическое воздействие)
ОСНОВНЫЕ ТЕХНОЛОГИЧЕСКИЕ СВОЙСТВА БЕЛКОВ 1. Гидрофильность – способность связывать воду 2. Денатурация - изменение четвертичной, третичной и вторичной структуры макромолекулы белка с сохранением первичной под воздействием А)высоких температур Б) механического воздействия В) действия тяжелых металлов Г) действия кислоты Д) действие спирта … 3. Пенообразование -способность белков образовывать высококонцентрированные системы жидкость-газ. Такие системы называются пенами (механическое воздействие)
 ОСНОВНЫЕ ТЕХНОЛОГИЧЕСКИЕ СВОЙСТВА БЕЛКОВ 4. Гидролиз белков – распад белков на свободные аминокислоты (разрушение первичной структуры) под действием кислот, щелочей или ферментов
ОСНОВНЫЕ ТЕХНОЛОГИЧЕСКИЕ СВОЙСТВА БЕЛКОВ 4. Гидролиз белков – распад белков на свободные аминокислоты (разрушение первичной структуры) под действием кислот, щелочей или ферментов
 ОСНОВНЫЕ ТЕХНОЛОГИЧЕСКИЕ СВОЙСТВА БЕЛКОВ 5. Реакция Майяра– взаимодействие белков с углеводами с образованием меланоидинов. => «РУМЯНАЯ КОРОЧКА» 6. Ферментативное действие
ОСНОВНЫЕ ТЕХНОЛОГИЧЕСКИЕ СВОЙСТВА БЕЛКОВ 5. Реакция Майяра– взаимодействие белков с углеводами с образованием меланоидинов. => «РУМЯНАЯ КОРОЧКА» 6. Ферментативное действие
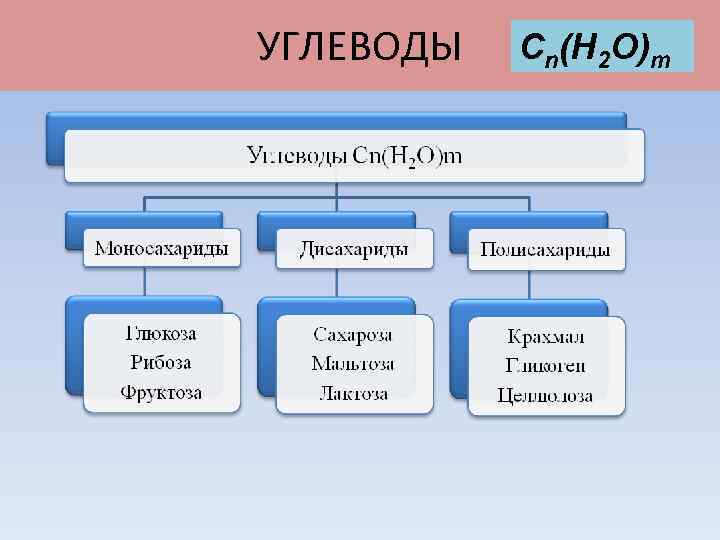 УГЛЕВОДЫ Cn(H 2 O)m
УГЛЕВОДЫ Cn(H 2 O)m
 ГЛЮКОЗА –» ВИНОГРАДНЫЙ САХАР» В свободном виде содержится в ягодах и фруктах. Из молекул глюкозы построены крахмал, гликоген, мальтоза. Глюкоза является составной частью сахарозы и лактозы. Инсулин-гормон надпочечников Углеводы пищи глюкоза гликоген
ГЛЮКОЗА –» ВИНОГРАДНЫЙ САХАР» В свободном виде содержится в ягодах и фруктах. Из молекул глюкозы построены крахмал, гликоген, мальтоза. Глюкоза является составной частью сахарозы и лактозы. Инсулин-гормон надпочечников Углеводы пищи глюкоза гликоген
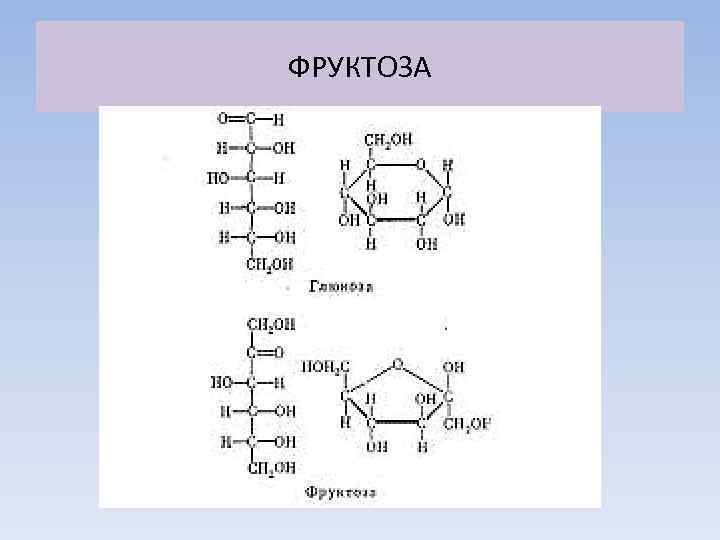 ФРУКТОЗА
ФРУКТОЗА
 Химические свойства глюкозы Реакции альдегидной группы: Реакция «серебряного зеркала» : взаимодействие глюкозы с аммиачным раствором оксида серебра: HOCH 2(CHOH)4 CH=O + Ag 2 O HOCH 2(CHOH)4 COOH + 2 Ag
Химические свойства глюкозы Реакции альдегидной группы: Реакция «серебряного зеркала» : взаимодействие глюкозы с аммиачным раствором оксида серебра: HOCH 2(CHOH)4 CH=O + Ag 2 O HOCH 2(CHOH)4 COOH + 2 Ag
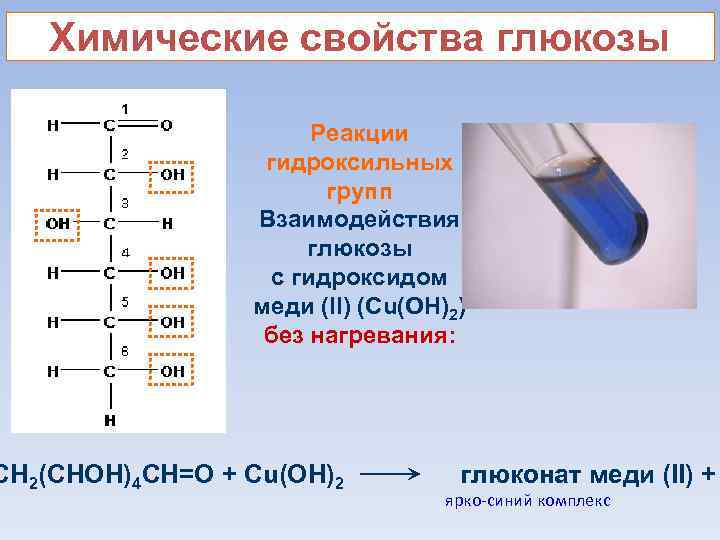 Химические свойства глюкозы Реакции гидроксильных групп Взаимодействия глюкозы с гидроксидом меди (II) (Cu(OH)2) без нагревания: CH 2(CHOH)4 CH=O + Cu(OH)2 глюконат меди (II) + ярко-синий комплекс
Химические свойства глюкозы Реакции гидроксильных групп Взаимодействия глюкозы с гидроксидом меди (II) (Cu(OH)2) без нагревания: CH 2(CHOH)4 CH=O + Cu(OH)2 глюконат меди (II) + ярко-синий комплекс
 Химические свойства глюкозы
Химические свойства глюкозы
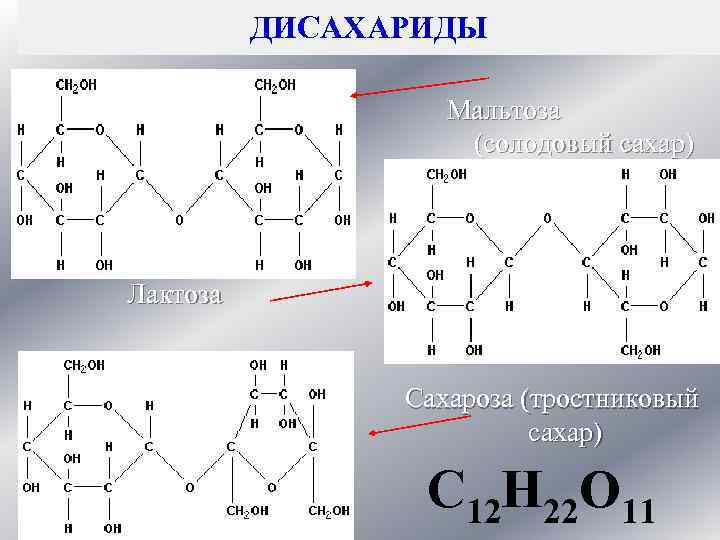 ДИСАХАРИДЫ Мальтоза (солодовый сахар) Лактоза Сахароза (тростниковый сахар) С 12 Н 22 О 11
ДИСАХАРИДЫ Мальтоза (солодовый сахар) Лактоза Сахароза (тростниковый сахар) С 12 Н 22 О 11
 КАКОЙ САХАР САМЫЙ СЛАДКИЙ? Относительная сладость сахаров в условных единицах: Сахароза-100 галактоза-32 Фруктоза-173 мальтоза-32 Глюкоза – 74 лактоза – 16
КАКОЙ САХАР САМЫЙ СЛАДКИЙ? Относительная сладость сахаров в условных единицах: Сахароза-100 галактоза-32 Фруктоза-173 мальтоза-32 Глюкоза – 74 лактоза – 16
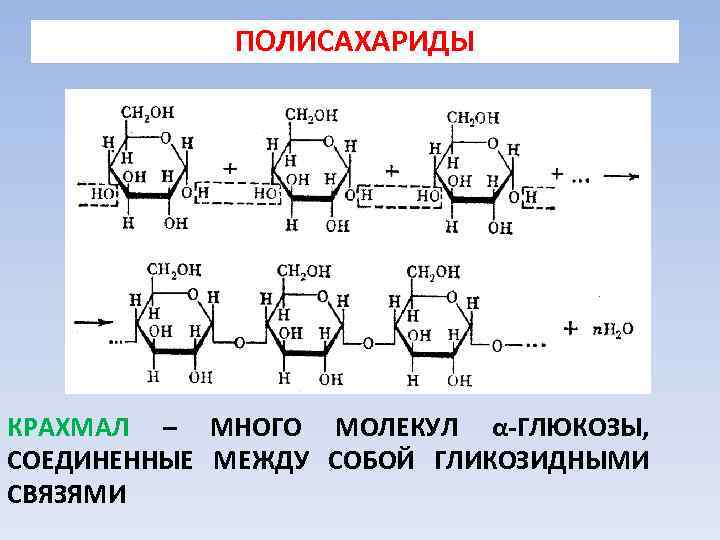 ПОЛИСАХАРИДЫ КРАХМАЛ – МНОГО МОЛЕКУЛ α-ГЛЮКОЗЫ, СОЕДИНЕННЫЕ МЕЖДУ СОБОЙ ГЛИКОЗИДНЫМИ СВЯЗЯМИ
ПОЛИСАХАРИДЫ КРАХМАЛ – МНОГО МОЛЕКУЛ α-ГЛЮКОЗЫ, СОЕДИНЕННЫЕ МЕЖДУ СОБОЙ ГЛИКОЗИДНЫМИ СВЯЗЯМИ
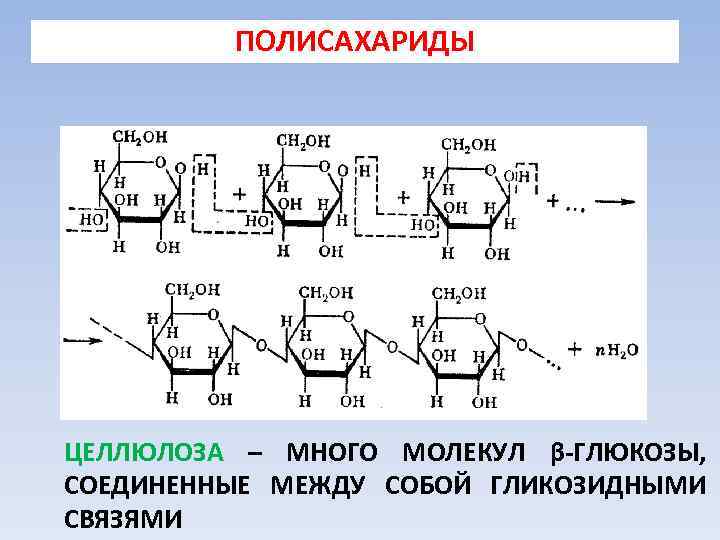 ПОЛИСАХАРИДЫ ЦЕЛЛЮЛОЗА – МНОГО МОЛЕКУЛ β-ГЛЮКОЗЫ, СОЕДИНЕННЫЕ МЕЖДУ СОБОЙ ГЛИКОЗИДНЫМИ СВЯЗЯМИ
ПОЛИСАХАРИДЫ ЦЕЛЛЮЛОЗА – МНОГО МОЛЕКУЛ β-ГЛЮКОЗЫ, СОЕДИНЕННЫЕ МЕЖДУ СОБОЙ ГЛИКОЗИДНЫМИ СВЯЗЯМИ
 ПОЛИСАХАРИДЫ -Это органические полимеры!! n Поликонденсация – это процесс получения полимеров, сопровождающийся образованием побочного продукта (в данном случае – воды). n
ПОЛИСАХАРИДЫ -Это органические полимеры!! n Поликонденсация – это процесс получения полимеров, сопровождающийся образованием побочного продукта (в данном случае – воды). n
 ПОЛИСАХАРИДЫ Качественная реакция на крахмал
ПОЛИСАХАРИДЫ Качественная реакция на крахмал
 ПОЛИСАХАРИДЫ Гидролиз – это реакция разложения, протекающая с участием воды. С 12 Н 22 О 11 + Н 2 О Н+ t Сахароза глюкоза (С 6 Н 10 О 5)n + n. Н 2 О Н+ t Крахмал Целлюлоза С 6 Н 12 О 6 + С 6 Н 12 О 6 фруктоза n. С 6 Н 12 О 6 α-глюкоза n. С 6 Н 12 О 6 β-глюкоза
ПОЛИСАХАРИДЫ Гидролиз – это реакция разложения, протекающая с участием воды. С 12 Н 22 О 11 + Н 2 О Н+ t Сахароза глюкоза (С 6 Н 10 О 5)n + n. Н 2 О Н+ t Крахмал Целлюлоза С 6 Н 12 О 6 + С 6 Н 12 О 6 фруктоза n. С 6 Н 12 О 6 α-глюкоза n. С 6 Н 12 О 6 β-глюкоза
 ПОЛИСАХАРИДЫ Получение спирта из крахмала Крахмал (С 6 Н 10 О 5)n 1 Глюкоза С 6 Н 12 О 6 2 Этанол С 2 Н 5 ОН 1 стадия – гидролиз 2 стадия – спиртовое брожение: С 6 Н 12 О 6 дрожжи 2 С 2 Н 5 ОН + 2 СО 2
ПОЛИСАХАРИДЫ Получение спирта из крахмала Крахмал (С 6 Н 10 О 5)n 1 Глюкоза С 6 Н 12 О 6 2 Этанол С 2 Н 5 ОН 1 стадия – гидролиз 2 стадия – спиртовое брожение: С 6 Н 12 О 6 дрожжи 2 С 2 Н 5 ОН + 2 СО 2


