Основные обратимые термодинамические процессы Исследование термодинамических процессов


Основные обратимые термодинамические процессы

Исследование термодинамических процессов n Устанавливают закономерности изменения состояния рабочего тела. n Выявляют особенности превращения энергии

Изучение изменения состояния рабочего тела n Выводят уравнение процесса и устанавливают соотношение между параметрами состояния рабочего тела; n Определяют количество теплоты, подводимой к рабочему телу, внешнюю работу, совершаемую рабочим телом, и изменение его внутренней энергии.

Классификация термодинамических процессов n Изохорный – при постоянном объеме; n Изобарный – при постоянном давлении; n Изотермический – при постоянной температуре; n Адиабатный – при отсутствии теплообмена между рабочим телом и окружающей средой.

Изохорный процесс v=const n Все тепло, подводимое к системе идет на изменение внутренней энергии системы. Δq= Δu n Уравнение процесса: n Первый закон термодинамики: n Энтропия: Энтальпия: n Работа: внешняя работа удельная располагаемая, полезная работа (работа проталкивания):
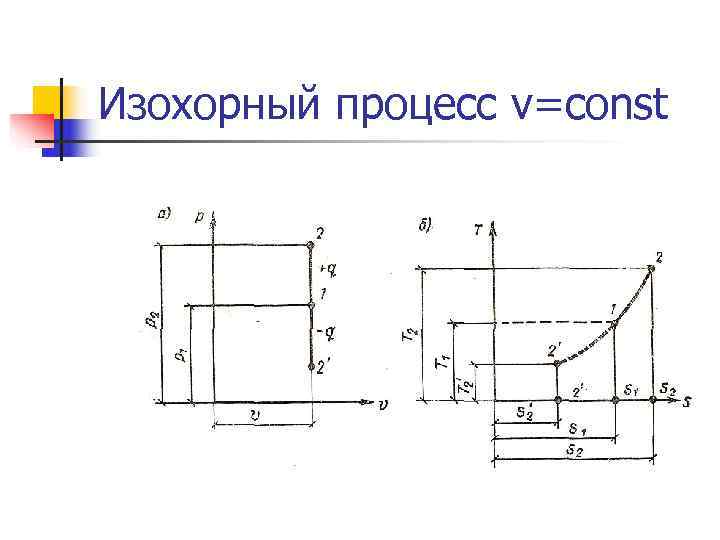
Изохорный процесс v=const

Изобарный процесс p=const n Теплота, сообщаемая системе, увеличивает её энтальпию. Δq= Δi n Уравнение процесса: n Первый закон термодинамики: n Энтропия: Энтальпия: n Работа: т. к. , то n Так как PV=RT , то одновременно n удельная располагаемая (полезная работа)
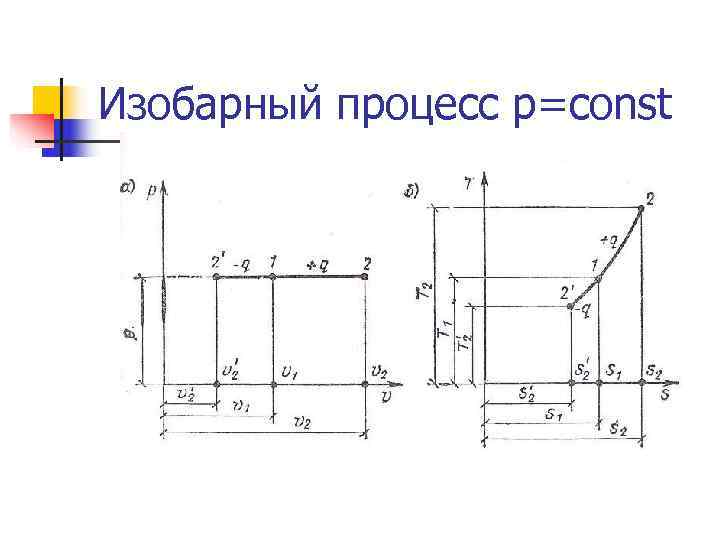
Изобарный процесс p=const

Изотермический процесс T=const n. Теплота, сообщаемая системе, тратится на совершение внешней работы. q=l n Уравнение процесса: n Первый закон термодинамики: n Энтропия: Энтальпия: n Работа: удельная располагаемая (полезная работа)
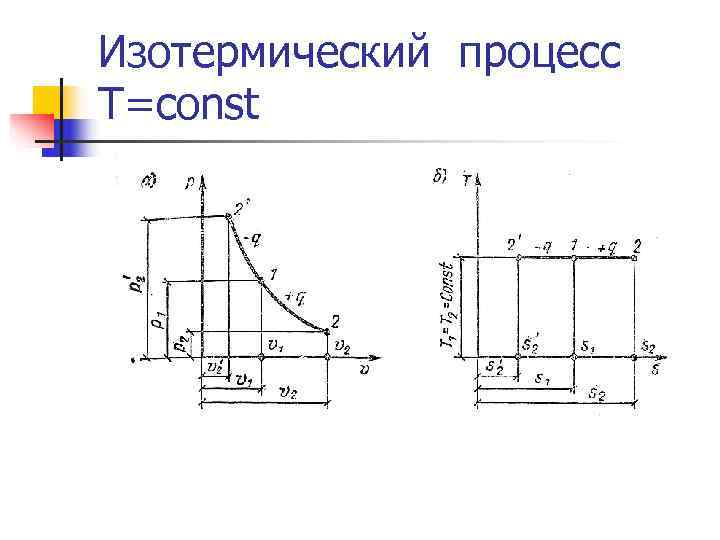
Изотермический процесс T=const

Адиабатный процесс n Внешняя работа совершается рабочим телом за счет изменения его внутренней энергии. n Уравнение процесса: n Первый закон термодинамики: l=-Δu=-cv Δt n Энтропия: ΔS=0; Энтальпия: Δi=v·ΔP n Работа: удельная располагаемая (полезная работа): l’=k·l
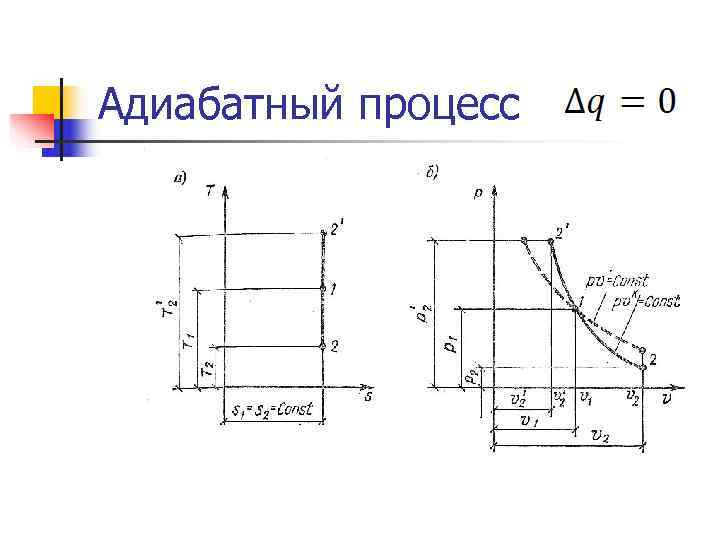
Адиабатный процесс

Политропный процесс n с=const n Все процессы – частный случай политропного. n Изохорный – n Изобарный – n Изотермический – n Адиабатный -

Политропный процесс n Уравнение процесса: n Первый закон термодинамики: q=c·ΔТ n Теплоемкость: n Изменение внутренней энергии: n Энтропия: Энтальпия: n Работа: удельная располагаемая (полезная работа)

Процесс п Изохорный ±∞ Изобарный 0 Изотермический 1 ±∞ Адиабатный k 0
3Основные обратимые термодинамич.процессы.ppt
- Количество слайдов: 15

