Основные классы .pptx
- Количество слайдов: 29
 Основные классы неорганических соединений
Основные классы неорганических соединений
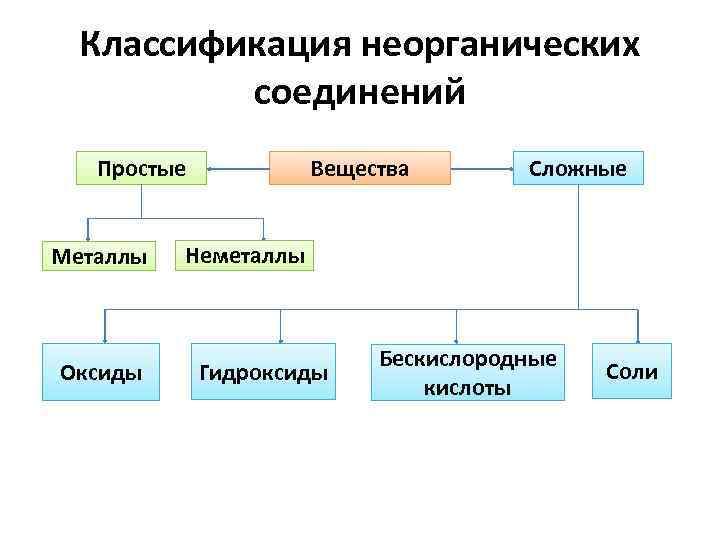 Классификация неорганических соединений Простые Металлы Оксиды Вещества Сложные Неметаллы Гидроксиды Бескислородные кислоты Соли
Классификация неорганических соединений Простые Металлы Оксиды Вещества Сложные Неметаллы Гидроксиды Бескислородные кислоты Соли
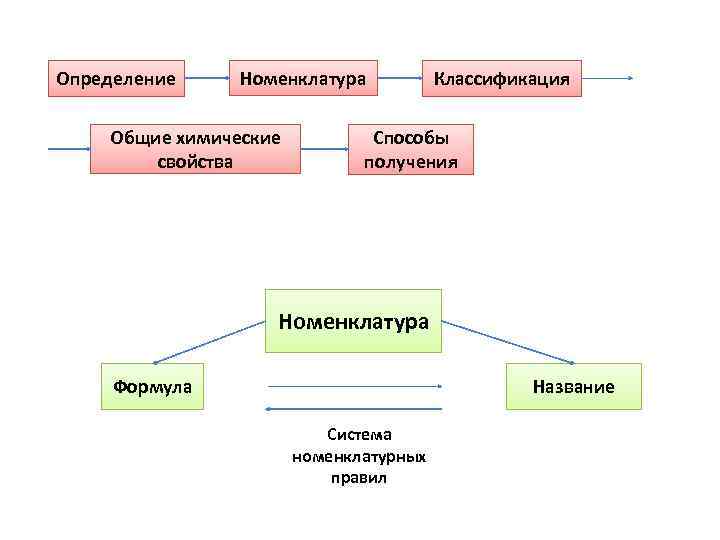 Определение Номенклатура Общие химические свойства Классификация Способы получения Номенклатура Формула Название Система номенклатурных правил
Определение Номенклатура Общие химические свойства Классификация Способы получения Номенклатура Формула Название Система номенклатурных правил
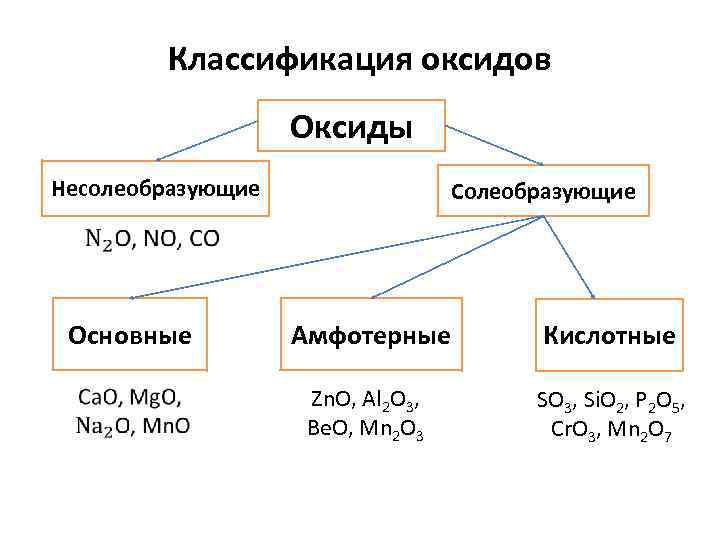 Классификация оксидов Оксиды Несолеобразующие Солеобразующие • Основные Амфотерные Кислотные Zn. O, Al 2 O 3, Be. O, Mn 2 O 3 SO 3, Si. O 2, P 2 O 5, Cr. O 3, Mn 2 O 7
Классификация оксидов Оксиды Несолеобразующие Солеобразующие • Основные Амфотерные Кислотные Zn. O, Al 2 O 3, Be. O, Mn 2 O 3 SO 3, Si. O 2, P 2 O 5, Cr. O 3, Mn 2 O 7
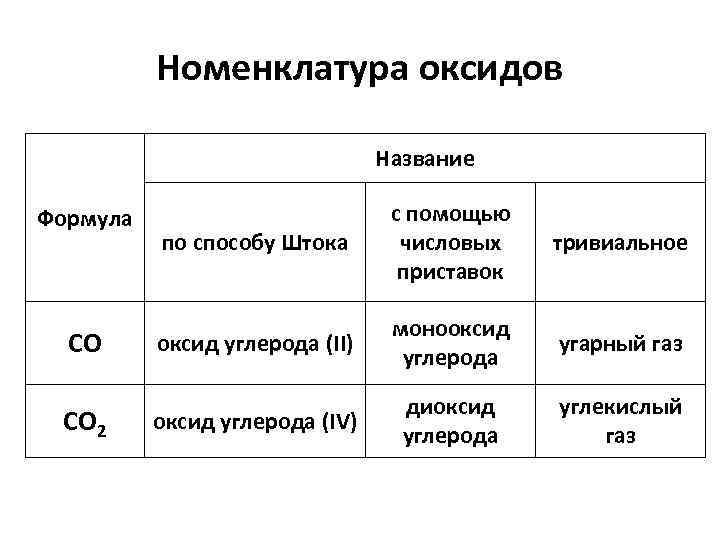 Номенклатура оксидов Название Формула СО СО 2 по способу Штока с помощью числовых приставок тривиальное оксид углерода (II) монооксид углерода угарный газ оксид углерода (IV) диоксид углерода углекислый газ
Номенклатура оксидов Название Формула СО СО 2 по способу Штока с помощью числовых приставок тривиальное оксид углерода (II) монооксид углерода угарный газ оксид углерода (IV) диоксид углерода углекислый газ
 Химические свойства основных оксидов Взаимодействие с водой (только оксиды ЩМ и ЩЗМ) Взаимодействие с кислотами Взаимодействие с кислотными оксидами Na 2 O + H 2 O = 2 Na. OH Cu. O + H 2 SO 4 = Cu. SO 4 + H 2 O Li 2 O + SO 2 = Li 2 SO 3 Mn. O + Si. O 2 = Mn. Si. O 3
Химические свойства основных оксидов Взаимодействие с водой (только оксиды ЩМ и ЩЗМ) Взаимодействие с кислотами Взаимодействие с кислотными оксидами Na 2 O + H 2 O = 2 Na. OH Cu. O + H 2 SO 4 = Cu. SO 4 + H 2 O Li 2 O + SO 2 = Li 2 SO 3 Mn. O + Si. O 2 = Mn. Si. O 3
 Химические свойства кислотных оксидов Взаимодействие с водой (большинство) Взаимодействие со щелочами Взаимодействие с основными оксидами SO 2 + H 2 O = H 2 SO 3 Cr. O 3 + 2 Na. OH = Na 2 Cr. O 4 + H 2 O CO 2 + Ca. O = Ca. CO 3
Химические свойства кислотных оксидов Взаимодействие с водой (большинство) Взаимодействие со щелочами Взаимодействие с основными оксидами SO 2 + H 2 O = H 2 SO 3 Cr. O 3 + 2 Na. OH = Na 2 Cr. O 4 + H 2 O CO 2 + Ca. O = Ca. CO 3
 Химические свойства амфотерных оксидов Взаимодействие с кислотами Zn. O + H 2 SO 4 = Zn. SO 4 +H 2 O Взаимодействие со щелочами а) в растворе б) при сплавлении Zn. O + 2 Na. OH + H 2 O =Na 2[Zn(OH)4] Zn. O + 2 Na. OH = Na 2 Zn. O 2 + H 2 O
Химические свойства амфотерных оксидов Взаимодействие с кислотами Zn. O + H 2 SO 4 = Zn. SO 4 +H 2 O Взаимодействие со щелочами а) в растворе б) при сплавлении Zn. O + 2 Na. OH + H 2 O =Na 2[Zn(OH)4] Zn. O + 2 Na. OH = Na 2 Zn. O 2 + H 2 O
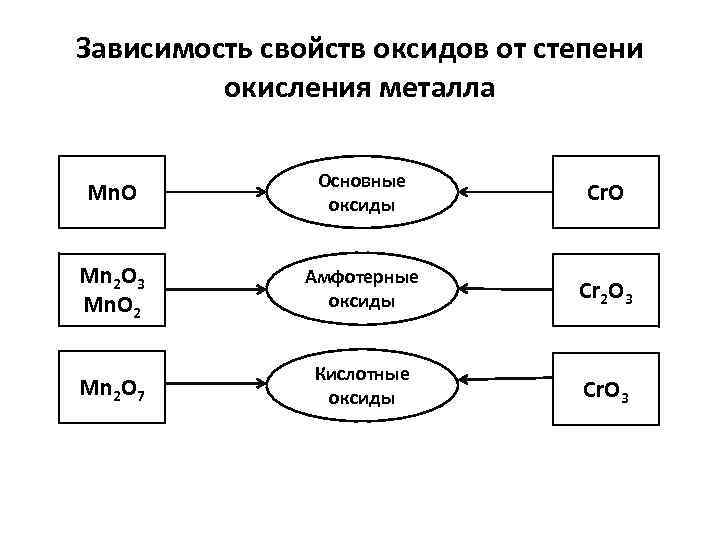 Зависимость свойств оксидов от степени окисления металла Mn. O Основные оксиды Cr. O Mn 2 O 3 Mn. O 2 Амфотерные оксиды Cr 2 O 3 Mn 2 O 7 Кислотные оксиды Cr. O 3
Зависимость свойств оксидов от степени окисления металла Mn. O Основные оксиды Cr. O Mn 2 O 3 Mn. O 2 Амфотерные оксиды Cr 2 O 3 Mn 2 O 7 Кислотные оксиды Cr. O 3
 Способы получения оксидов Взаимодействие простых веществ с кислородом 2 Cu + O 2 = 2 Cu. O Косвенные способы Разложение нерастворимых оснований Cu(OH)2 = Cu. O + H 2 O Разложение оксокислот 4 HNO 3 = 4 NO 2 + 2 H 2 O Разложение солей NH 4 NO 3 = N 2 O + 2 H 2 O 2 Cu(NO 3)2 = 2 Cu. O + 4 NO 2 + O 2 Взаимодействие металлов и неметаллов с кислотамиокислителями C + 2 H 2 SO 4(конц) = СO 2 + 2 SO 2 + 2 H 2 O Cu + 4 HNO 3(конц) = Сu(NO 3)2 +2 NO 2 + +2 H 2 O Горение сложных веществ 2 H 2 S + 3 O 2 = 2 H 2 O + 2 SO 2
Способы получения оксидов Взаимодействие простых веществ с кислородом 2 Cu + O 2 = 2 Cu. O Косвенные способы Разложение нерастворимых оснований Cu(OH)2 = Cu. O + H 2 O Разложение оксокислот 4 HNO 3 = 4 NO 2 + 2 H 2 O Разложение солей NH 4 NO 3 = N 2 O + 2 H 2 O 2 Cu(NO 3)2 = 2 Cu. O + 4 NO 2 + O 2 Взаимодействие металлов и неметаллов с кислотамиокислителями C + 2 H 2 SO 4(конц) = СO 2 + 2 SO 2 + 2 H 2 O Cu + 4 HNO 3(конц) = Сu(NO 3)2 +2 NO 2 + +2 H 2 O Горение сложных веществ 2 H 2 S + 3 O 2 = 2 H 2 O + 2 SO 2
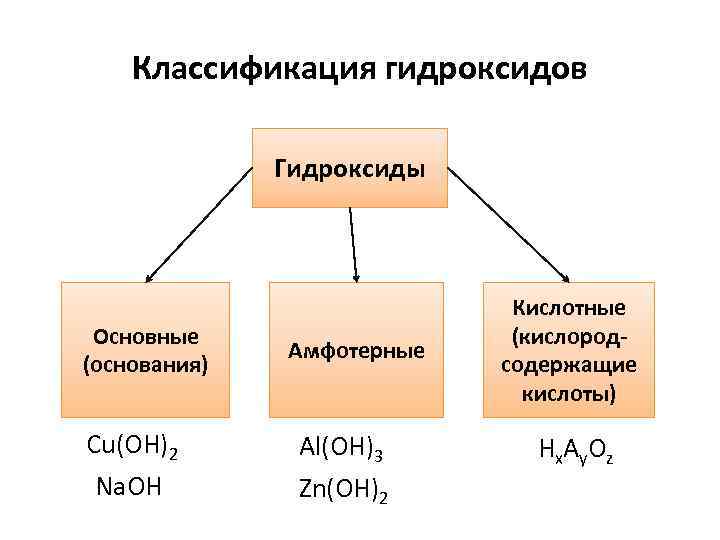 Классификация гидроксидов Гидроксиды Основные (основания) Cu(OH)2 Na. OH Амфотерные Al(OH)3 Zn(OH)2 Кислотные (кислородсодержащие кислоты) Hx A y O z
Классификация гидроксидов Гидроксиды Основные (основания) Cu(OH)2 Na. OH Амфотерные Al(OH)3 Zn(OH)2 Кислотные (кислородсодержащие кислоты) Hx A y O z
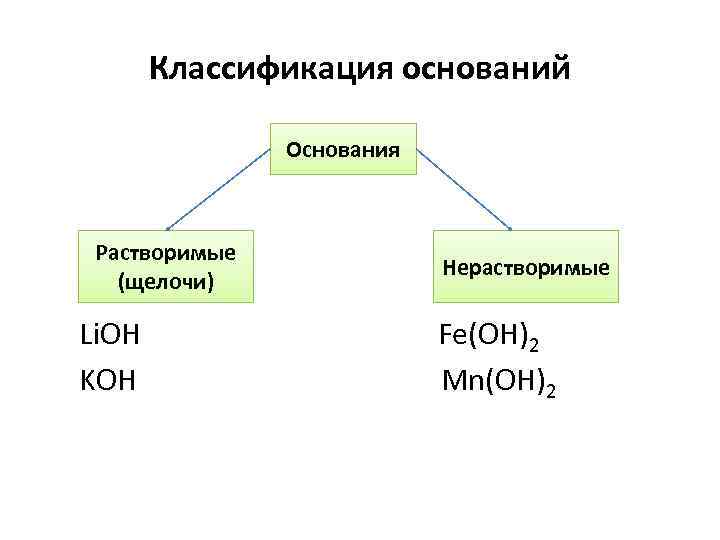 Классификация оснований Основания Растворимые (щелочи) Нерастворимые Li. OH Fe(OH)2 KOH Mn(OH)2
Классификация оснований Основания Растворимые (щелочи) Нерастворимые Li. OH Fe(OH)2 KOH Mn(OH)2
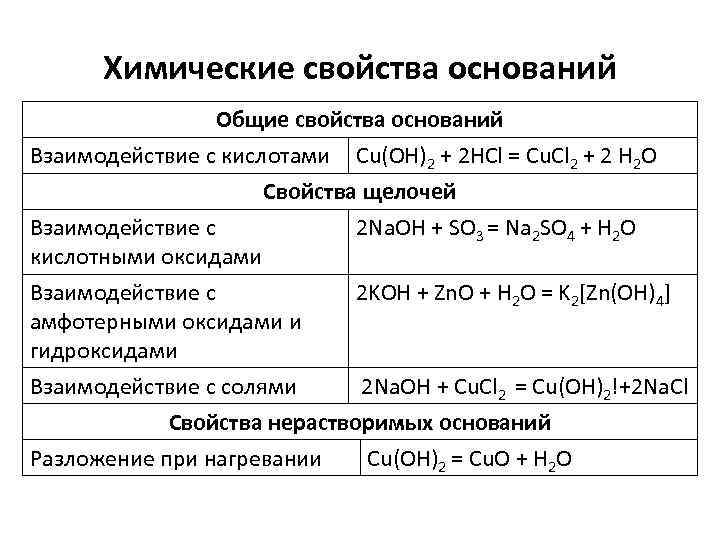 Химические свойства оснований Общие свойства оснований Взаимодействие с кислотами Cu(OH)2 + 2 HCl = Cu. Cl 2 + 2 H 2 O Свойства щелочей Взаимодействие с 2 Na. OH + SO 3 = Na 2 SO 4 + H 2 O кислотными оксидами Взаимодействие с 2 KOH + Zn. O + H 2 O = K 2[Zn(OH)4] амфотерными оксидами и гидроксидами Взаимодействие с солями 2 Na. OH + Cu. Cl 2 = Cu(OH)2!+2 Na. Cl Свойства нерастворимых оснований Разложение при нагревании Cu(OH)2 = Cu. O + H 2 O
Химические свойства оснований Общие свойства оснований Взаимодействие с кислотами Cu(OH)2 + 2 HCl = Cu. Cl 2 + 2 H 2 O Свойства щелочей Взаимодействие с 2 Na. OH + SO 3 = Na 2 SO 4 + H 2 O кислотными оксидами Взаимодействие с 2 KOH + Zn. O + H 2 O = K 2[Zn(OH)4] амфотерными оксидами и гидроксидами Взаимодействие с солями 2 Na. OH + Cu. Cl 2 = Cu(OH)2!+2 Na. Cl Свойства нерастворимых оснований Разложение при нагревании Cu(OH)2 = Cu. O + H 2 O
 Получение оснований Растворимые основания Взаимодействие ЩМ и 2 Na + 2 H 2 O = 2 Na. OH + H 2 ЩЗМ с водой Взаимодействие оксидов Ca. O + H 2 O = Ca(OH)2 ЩМ и ЩЗМ с водой Электролиз 2 Na. Cl +2 H 2 O = 2 Na. OH + Cl 2 + H 2 концентрированных растворов солей Нерастворимые основания Реакции ионного обмена Mn. Cl 2 + 2 Na. OH = Mn(OH)2!+ 2 Na. Cl
Получение оснований Растворимые основания Взаимодействие ЩМ и 2 Na + 2 H 2 O = 2 Na. OH + H 2 ЩЗМ с водой Взаимодействие оксидов Ca. O + H 2 O = Ca(OH)2 ЩМ и ЩЗМ с водой Электролиз 2 Na. Cl +2 H 2 O = 2 Na. OH + Cl 2 + H 2 концентрированных растворов солей Нерастворимые основания Реакции ионного обмена Mn. Cl 2 + 2 Na. OH = Mn(OH)2!+ 2 Na. Cl
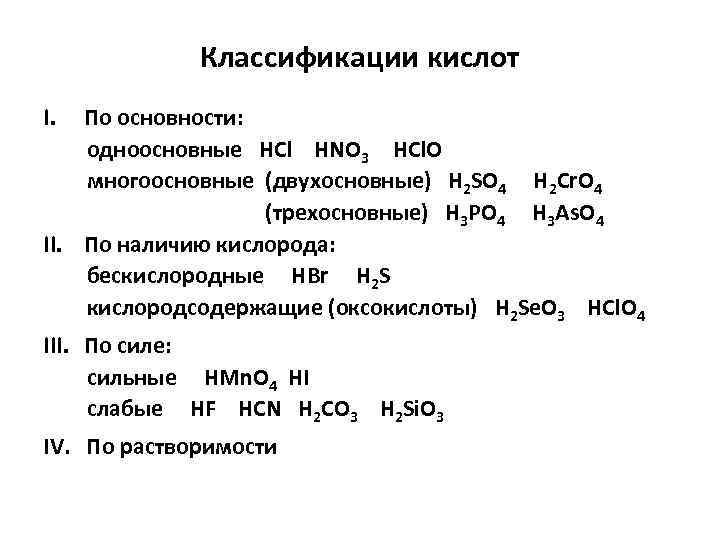 Классификации кислот I. По основности: одноосновные HCl HNO 3 HCl. O многоосновные (двухосновные) H 2 SO 4 H 2 Cr. O 4 (трехосновные) H 3 РO 4 H 3 As. O 4 II. По наличию кислорода: бескислородные HBr H 2 S кислородсодержащие (оксокислоты) H 2 Se. O 3 HCl. O 4 III. По силе: сильные HMn. O 4 HI слабые HF HCN H 2 CO 3 H 2 Si. O 3 IV. По растворимости
Классификации кислот I. По основности: одноосновные HCl HNO 3 HCl. O многоосновные (двухосновные) H 2 SO 4 H 2 Cr. O 4 (трехосновные) H 3 РO 4 H 3 As. O 4 II. По наличию кислорода: бескислородные HBr H 2 S кислородсодержащие (оксокислоты) H 2 Se. O 3 HCl. O 4 III. По силе: сильные HMn. O 4 HI слабые HF HCN H 2 CO 3 H 2 Si. O 3 IV. По растворимости
 Номенклатура кислот НА H x. A y Oz Cтепень окисления элемента А Суффикс Формула Название Высшая или любая единственная -н-, -ов-, -ев- H 2 SO 4 HMn. O 4 H 2 Ge. O 3 серная марганцовая германиевая Промежуточная +5 -новат- HCl. O 3 хлорноватая Промежуточная +4, +3 -(ов)ист- HCl. O 2 H 3 As. O 3 хлористая мышьяковистая Низшая положительная -новатист- HCl. O H 2 N 2 O 2 хлорноватистая азотноватистая HPO 3 метафосфорная H 3 PO 4 ортофосфорная H 4 P 2 O 7 дифосфорная H 2 S 2 O 7 дисерная
Номенклатура кислот НА H x. A y Oz Cтепень окисления элемента А Суффикс Формула Название Высшая или любая единственная -н-, -ов-, -ев- H 2 SO 4 HMn. O 4 H 2 Ge. O 3 серная марганцовая германиевая Промежуточная +5 -новат- HCl. O 3 хлорноватая Промежуточная +4, +3 -(ов)ист- HCl. O 2 H 3 As. O 3 хлористая мышьяковистая Низшая положительная -новатист- HCl. O H 2 N 2 O 2 хлорноватистая азотноватистая HPO 3 метафосфорная H 3 PO 4 ортофосфорная H 4 P 2 O 7 дифосфорная H 2 S 2 O 7 дисерная
 Химические свойства кислот Взаимодействие с металлами, расположенными до Н в ряду напряжений (кислота проявляет окислительные свойства за счет иона Н+) Zn + H 2 SO 4(p-p) = Zn. SO 4 + H 2 Взаимодействие с основаниями и амфотерными гидроксидами HCl + KOH =KCl + H 2 O Взаимодействие с основными и амфотерными оксидами H 2 SO 4 + Mg. O = Mg. SO 4 + H 2 O Взаимодействие с солями (если образуется более слабая или летучая кислота) 2 HCl +Na 2 Si. O 3 = H 2 Si. O 3 +2 Na. Cl Взаимодействие с металлами, расположенными после Н в ряду напряжений (кислота проявляет окислительные свойства за счет аниона ) Cu + 2 H 2 SO 4(конц) = Cu. SO 4 + SO 2 + +2 H 2 O
Химические свойства кислот Взаимодействие с металлами, расположенными до Н в ряду напряжений (кислота проявляет окислительные свойства за счет иона Н+) Zn + H 2 SO 4(p-p) = Zn. SO 4 + H 2 Взаимодействие с основаниями и амфотерными гидроксидами HCl + KOH =KCl + H 2 O Взаимодействие с основными и амфотерными оксидами H 2 SO 4 + Mg. O = Mg. SO 4 + H 2 O Взаимодействие с солями (если образуется более слабая или летучая кислота) 2 HCl +Na 2 Si. O 3 = H 2 Si. O 3 +2 Na. Cl Взаимодействие с металлами, расположенными после Н в ряду напряжений (кислота проявляет окислительные свойства за счет аниона ) Cu + 2 H 2 SO 4(конц) = Cu. SO 4 + SO 2 + +2 H 2 O
 Способы получения кислот Взаимодействие кислотных оксидов с водой SO 3 + H 2 O = H 2 SO 4 2 NO 2 + H 2 O = HNO 2 + HNO 3 Взаимодействие солей с кислотами (используемая кислота должна быть более сильной и менее летучей, чем получаемая) Na. NO 2 + H 2 SO 4 = Na 2 SO 4 + HNO 2 Окисление простых веществ сильными окислителями 3 P + 5 HNO 3 +2 H 2 O = 3 H 3 PO 4 +5 NO Взаимодействие простых веществ (для бескислородных кислот) H 2 + Cl 2 = 2 HCl
Способы получения кислот Взаимодействие кислотных оксидов с водой SO 3 + H 2 O = H 2 SO 4 2 NO 2 + H 2 O = HNO 2 + HNO 3 Взаимодействие солей с кислотами (используемая кислота должна быть более сильной и менее летучей, чем получаемая) Na. NO 2 + H 2 SO 4 = Na 2 SO 4 + HNO 2 Окисление простых веществ сильными окислителями 3 P + 5 HNO 3 +2 H 2 O = 3 H 3 PO 4 +5 NO Взаимодействие простых веществ (для бескислородных кислот) H 2 + Cl 2 = 2 HCl
 Свойства амфотерных гидроксидов Взаимодействие с кислотами Al(OH)3 + 3 HCl = Al. Cl 3 + 3 H 2 O Взаимодействие со щелочами Al(OH)3 + Na. OH = Na[Al(OH)4]
Свойства амфотерных гидроксидов Взаимодействие с кислотами Al(OH)3 + 3 HCl = Al. Cl 3 + 3 H 2 O Взаимодействие со щелочами Al(OH)3 + Na. OH = Na[Al(OH)4]
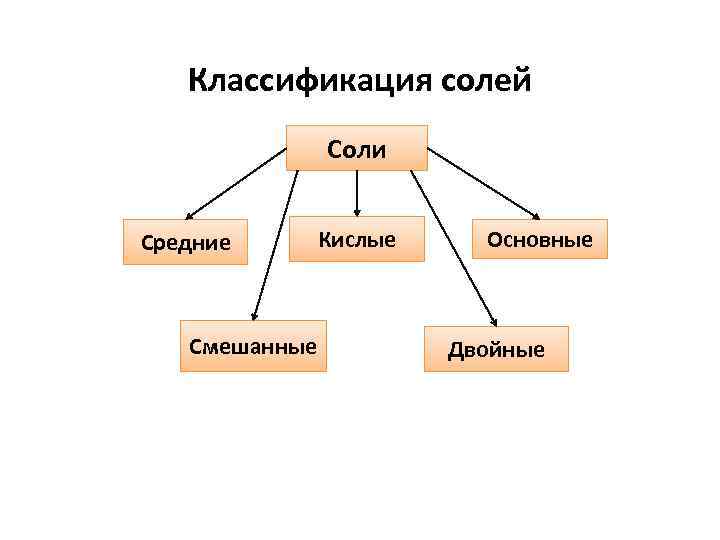 Классификация солей Соли Средние Смешанные Кислые Основные Двойные
Классификация солей Соли Средние Смешанные Кислые Основные Двойные
 Средние соли H 2 SO 4 + 2 Na. OH = Na 2 SO 4 + 2 H 2 O Fe. SO 4 – сульфат железа (II) NH 4 NO 3 – нитрат аммония UO 2 SO 4 – сульфат уранила NONO 3 – нитрат нитрозила Na 2 S – сульфид натрия Cr. Cl 3 – хлорид хрома (III)
Средние соли H 2 SO 4 + 2 Na. OH = Na 2 SO 4 + 2 H 2 O Fe. SO 4 – сульфат железа (II) NH 4 NO 3 – нитрат аммония UO 2 SO 4 – сульфат уранила NONO 3 – нитрат нитрозила Na 2 S – сульфид натрия Cr. Cl 3 – хлорид хрома (III)
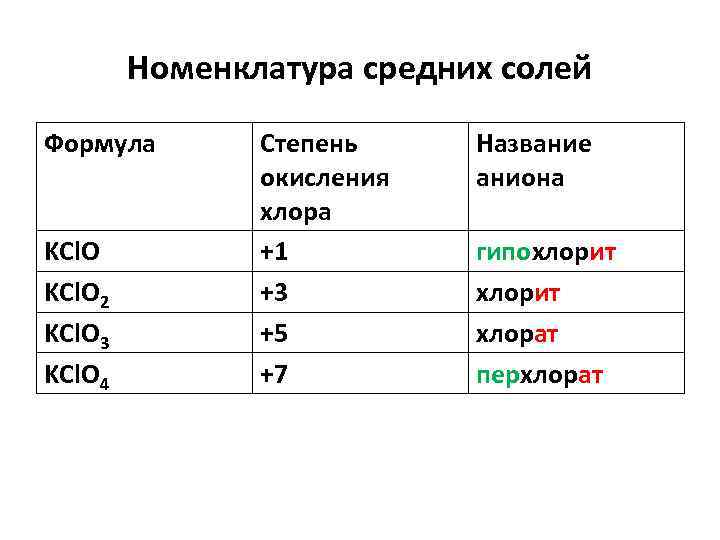 Номенклатура средних солей Формула KCl. O 2 KCl. O 3 KCl. O 4 Степень окисления хлора +1 +3 +5 +7 Название аниона гипохлорит хлорат перхлорат
Номенклатура средних солей Формула KCl. O 2 KCl. O 3 KCl. O 4 Степень окисления хлора +1 +3 +5 +7 Название аниона гипохлорит хлорат перхлорат
 Кислые соли H 2 SO 4 + Na. OH = Na. HSO 4 + H 2 O Ba(HSO 3)2 – гидросульфит бария Ca(H 2 PO 4)2 – дигидроортофосфат кальция Na. HS – гидросульфид натрия Основные соли Fe(OH)3 + 2 HCl = (Fe. OH)Cl 2 + 2 H 2 O (Cu. OH)2 CO 3 – гидроксокарбонат меди(II) Al(OH)Cl 2 – гидроксохлорид алюминия
Кислые соли H 2 SO 4 + Na. OH = Na. HSO 4 + H 2 O Ba(HSO 3)2 – гидросульфит бария Ca(H 2 PO 4)2 – дигидроортофосфат кальция Na. HS – гидросульфид натрия Основные соли Fe(OH)3 + 2 HCl = (Fe. OH)Cl 2 + 2 H 2 O (Cu. OH)2 CO 3 – гидроксокарбонат меди(II) Al(OH)Cl 2 – гидроксохлорид алюминия
 Двойные соли KCr(SO 4)2 – сульфат хрома(III)-калия Na. NH 4 Cl 2 – хлорид аммония-натрия Смешанные соли Ca 5(PO 4)3 F – фторид-ортофосфат кальция
Двойные соли KCr(SO 4)2 – сульфат хрома(III)-калия Na. NH 4 Cl 2 – хлорид аммония-натрия Смешанные соли Ca 5(PO 4)3 F – фторид-ортофосфат кальция
 Свойства солей Взаимодействуют с металлами Взаимодействуют со щелочами Взаимодействуют с кислотами Соли взаимодействуют друг с другом Некоторые соли при нагревании разлагаются Некоторые соли подвергаются гидролизу Zn + Hg(NO 3)2 = Zn(NO 3)2 = Hg Fe. Cl 3 + 3 KOH = Fe(OH)3 + 3 KCl Ca. CO 3 + 2 HCl = Ca. Cl 2 + CO 2 + H 2 O Ca. Cl 2 + Na 2 CO 3 = Ca. CO 3 + 2 Na. Cl (NH 4)2 Cr 2 O 7 = N 2 + Cr 2 O 3 + 4 H 2 O Cu. Cl 2 + H 2 O = Cu. OHCl + HCl
Свойства солей Взаимодействуют с металлами Взаимодействуют со щелочами Взаимодействуют с кислотами Соли взаимодействуют друг с другом Некоторые соли при нагревании разлагаются Некоторые соли подвергаются гидролизу Zn + Hg(NO 3)2 = Zn(NO 3)2 = Hg Fe. Cl 3 + 3 KOH = Fe(OH)3 + 3 KCl Ca. CO 3 + 2 HCl = Ca. Cl 2 + CO 2 + H 2 O Ca. Cl 2 + Na 2 CO 3 = Ca. CO 3 + 2 Na. Cl (NH 4)2 Cr 2 O 7 = N 2 + Cr 2 O 3 + 4 H 2 O Cu. Cl 2 + H 2 O = Cu. OHCl + HCl
 Способы получения солей 1. Взаимодействие оснований с кислотами KOH + HNO 3 = KNO 3 + H 2 O 2. Взаимодействие металлов с кислотами Hg + 4 HNO 3(K)= Hg(NO 3)2 + 2 NO 2+ +2 H 2 O 6 Hg + 8 HNO 3(p)= 3 Hg 2(NO 3)2 + +2 NO + 4 H 2 O 3. Взаимодействие основных или амфотерных Ca. O + 2 HCl = Ca. Cl 2 + H 2 O оксидов с кислотами 4. Взаимодействие 6 Na. OH + P 2 O 5 = 2 Na 3 PO 4 + 3 H 2 O кислотных оксидов с основаниями
Способы получения солей 1. Взаимодействие оснований с кислотами KOH + HNO 3 = KNO 3 + H 2 O 2. Взаимодействие металлов с кислотами Hg + 4 HNO 3(K)= Hg(NO 3)2 + 2 NO 2+ +2 H 2 O 6 Hg + 8 HNO 3(p)= 3 Hg 2(NO 3)2 + +2 NO + 4 H 2 O 3. Взаимодействие основных или амфотерных Ca. O + 2 HCl = Ca. Cl 2 + H 2 O оксидов с кислотами 4. Взаимодействие 6 Na. OH + P 2 O 5 = 2 Na 3 PO 4 + 3 H 2 O кислотных оксидов с основаниями
 5. Взаимодействие основных и кислотных оксидов 6. Взаимодействие солей с кислотами Ca. O +Si. O 2 = Ca. Si. O 3 Mg. CO 3 + 2 HCl = Mg. Cl 2 + CO 2 + H 2 O 7. Взаимодействие солей со Fe(NO 3)2 + 3 Na. OH = 3 Na. NO 3 + щелочами +Fe(OH)3 8. Взаимодействие двух солей 9. Взаимодействие соли с металлом 10. Взаимодействие неметаллов со щелочами Ba. Cl 2 + Na 2 SO 4 = Ba. SO 4 + 2 Na. Cl Cu. SO 4 + Fe = Fe. SO 4 + Cu Cl 2 + 2 KOH = KCl + KCl. O + H 2 O
5. Взаимодействие основных и кислотных оксидов 6. Взаимодействие солей с кислотами Ca. O +Si. O 2 = Ca. Si. O 3 Mg. CO 3 + 2 HCl = Mg. Cl 2 + CO 2 + H 2 O 7. Взаимодействие солей со Fe(NO 3)2 + 3 Na. OH = 3 Na. NO 3 + щелочами +Fe(OH)3 8. Взаимодействие двух солей 9. Взаимодействие соли с металлом 10. Взаимодействие неметаллов со щелочами Ba. Cl 2 + Na 2 SO 4 = Ba. SO 4 + 2 Na. Cl Cu. SO 4 + Fe = Fe. SO 4 + Cu Cl 2 + 2 KOH = KCl + KCl. O + H 2 O
 11. Взаимодействие 2 Fe + 3 Cl 2 =2 Fe. Cl 3 металлов и неметаллов 12. Термическое разложение 2 KNO 3 = 2 KNO 2 + O 2 некоторых солей
11. Взаимодействие 2 Fe + 3 Cl 2 =2 Fe. Cl 3 металлов и неметаллов 12. Термическое разложение 2 KNO 3 = 2 KNO 2 + O 2 некоторых солей
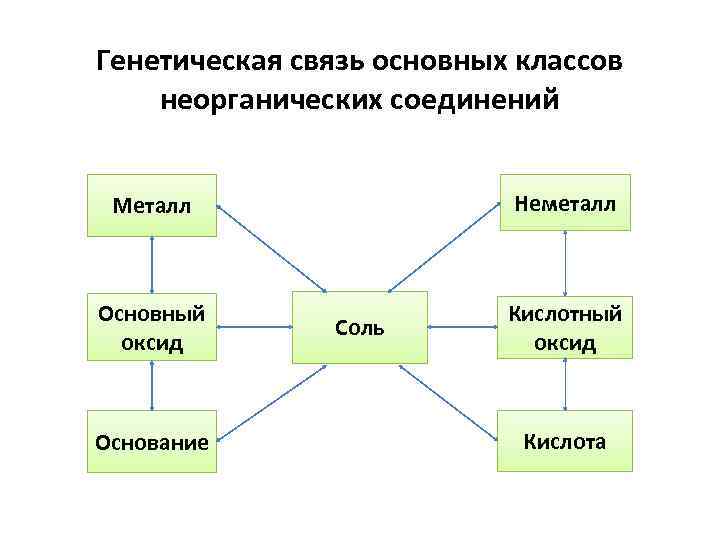 Генетическая связь основных классов неорганических соединений Неметалл Металл Основный оксид Основание Соль Кислотный оксид Кислота
Генетическая связь основных классов неорганических соединений Неметалл Металл Основный оксид Основание Соль Кислотный оксид Кислота


