Компьютерная программа-презентация Основные классы неорганических веществ.ppt
- Количество слайдов: 38
 Основные классы неорганических соединений
Основные классы неорганических соединений
 Информация о программе Дорогие друзья! Вы начали работу с обучающей программой «Основные классы неорганических веществ» . Программа содержит информацию о классификации, общих химических свойствах и способах получения основных классов неорганических веществ. Программа составлена с использованием гиперссылок, позволяющих перейти к странице с нужной информацией. Использование гиперссылок в каждой колонке обобщающей таблицы позволяет изучить каждое химическое свойство веществ: нажатием левой клавиши мышки, вы легко перейдете к странице, где даны необходимые пояснения, приведены примеры уравнений химических реакций. Для проверки, как вы усвоили данную тему, пройдите тестирование. Если вы не верно отвечаете на вопрос теста, программа дает возможность еще раз повторить учебный материал. Успехов! И надеюсь, что эта программа поможет вам в изучении данной темы.
Информация о программе Дорогие друзья! Вы начали работу с обучающей программой «Основные классы неорганических веществ» . Программа содержит информацию о классификации, общих химических свойствах и способах получения основных классов неорганических веществ. Программа составлена с использованием гиперссылок, позволяющих перейти к странице с нужной информацией. Использование гиперссылок в каждой колонке обобщающей таблицы позволяет изучить каждое химическое свойство веществ: нажатием левой клавиши мышки, вы легко перейдете к странице, где даны необходимые пояснения, приведены примеры уравнений химических реакций. Для проверки, как вы усвоили данную тему, пройдите тестирование. Если вы не верно отвечаете на вопрос теста, программа дает возможность еще раз повторить учебный материал. Успехов! И надеюсь, что эта программа поможет вам в изучении данной темы.
 Содержание программы Ш Повторим! Ш Таблица Общие химические свойства и способы получения основных классов неорганических веществ Ш Тест ШПриложение Ряд активности металлов Номенклатура кислот и солей Таблица растворимости солей, кислот и оснований в воде
Содержание программы Ш Повторим! Ш Таблица Общие химические свойства и способы получения основных классов неорганических веществ Ш Тест ШПриложение Ряд активности металлов Номенклатура кислот и солей Таблица растворимости солей, кислот и оснований в воде
 Повторим! Оксиды Основания Кислоты Соли к содержанию
Повторим! Оксиды Основания Кислоты Соли к содержанию
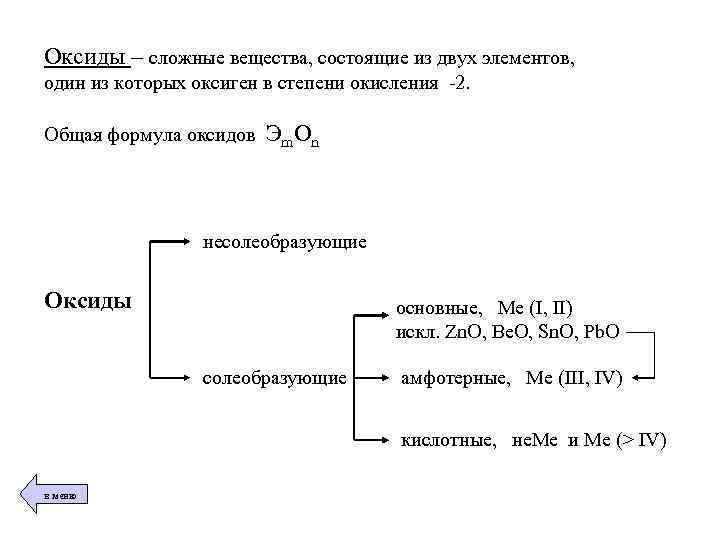 Оксиды – сложные вещества, состоящие из двух элементов, один из которых оксиген в степени окисления -2. Общая формула оксидов Эm Оn несолеобразующие Оксиды основные, Ме (I, II) искл. Zn. O, Be. O, Sn. O, Pb. O солеобразующие амфотерные, Ме (III, IV) кислотные, не. Ме и Ме (> IV) в меню
Оксиды – сложные вещества, состоящие из двух элементов, один из которых оксиген в степени окисления -2. Общая формула оксидов Эm Оn несолеобразующие Оксиды основные, Ме (I, II) искл. Zn. O, Be. O, Sn. O, Pb. O солеобразующие амфотерные, Ме (III, IV) кислотные, не. Ме и Ме (> IV) в меню
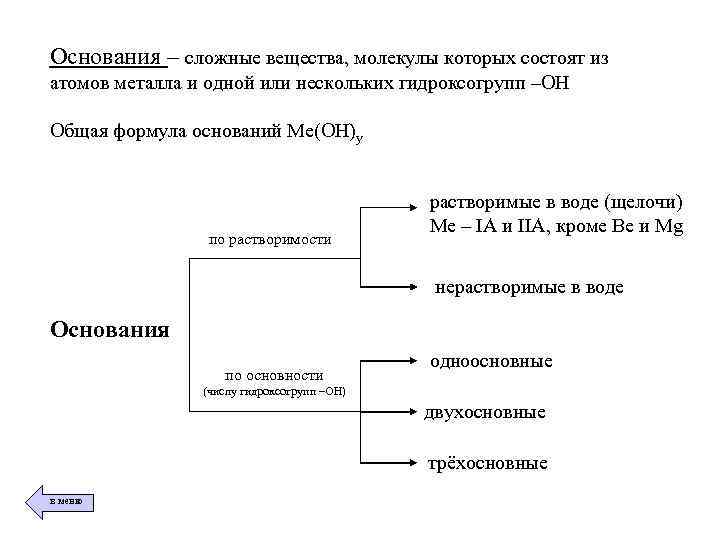 Основания – сложные вещества, молекулы которых состоят из атомов металла и одной или нескольких гидроксогрупп –ОН Общая формула оснований Me(ОН)у по растворимости растворимые в воде (щелочи) Ме – IА и IIА, кроме Be и Mg нерастворимые в воде Основания по основности одноосновные (числу гидроксогрупп –ОН) двухосновные трёхосновные в меню
Основания – сложные вещества, молекулы которых состоят из атомов металла и одной или нескольких гидроксогрупп –ОН Общая формула оснований Me(ОН)у по растворимости растворимые в воде (щелочи) Ме – IА и IIА, кроме Be и Mg нерастворимые в воде Основания по основности одноосновные (числу гидроксогрупп –ОН) двухосновные трёхосновные в меню
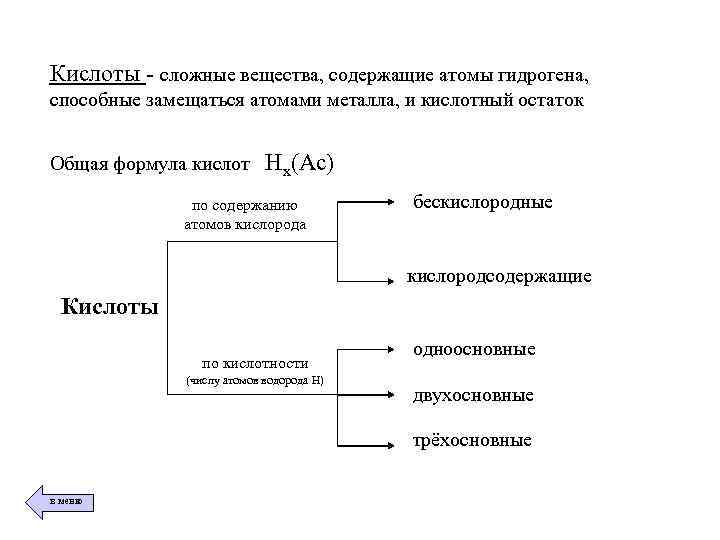 Кислоты - сложные вещества, содержащие атомы гидрогена, способные замещаться атомами металла, и кислотный остаток Общая формула кислот Нx(Ас) по содержанию атомов кислорода бескислородные кислородсодержащие Кислоты по кислотности (числу атомов водорода Н) одноосновные двухосновные трёхосновные в меню
Кислоты - сложные вещества, содержащие атомы гидрогена, способные замещаться атомами металла, и кислотный остаток Общая формула кислот Нx(Ас) по содержанию атомов кислорода бескислородные кислородсодержащие Кислоты по кислотности (числу атомов водорода Н) одноосновные двухосновные трёхосновные в меню
 Соли - сложные вещества, которые являются продуктами замещения атомов гидрогена в молекулах кислот атомами металла или продуктами замещения гидроксогрупп в молекулах оснований кислотными остатками Общая формула солей Mex(Ac)y средние (нормальные) кислые Соли основные двойные комплексные в меню
Соли - сложные вещества, которые являются продуктами замещения атомов гидрогена в молекулах кислот атомами металла или продуктами замещения гидроксогрупп в молекулах оснований кислотными остатками Общая формула солей Mex(Ac)y средние (нормальные) кислые Соли основные двойные комплексные в меню
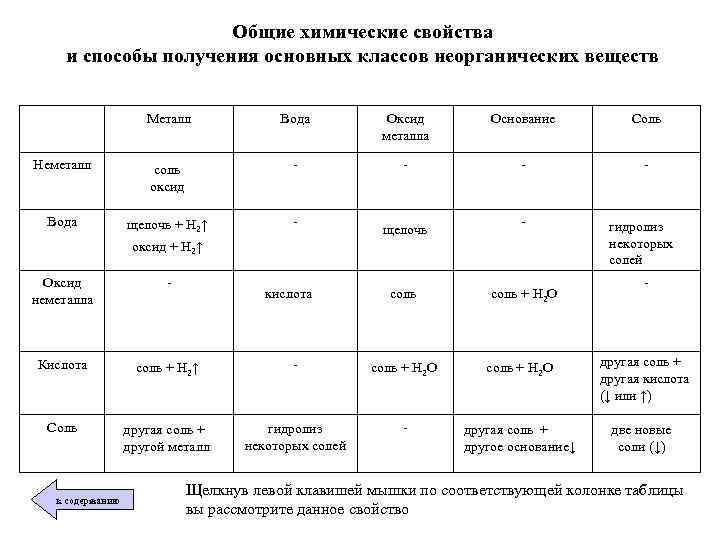 Общие химические свойства и способы получения основных классов неорганических веществ Металл Вода Оксид металла Основание Соль Неметалл соль оксид - - Вода щелочь + Н 2↑ - щелочь - оксид + Н 2↑ гидролиз некоторых солей Оксид неметалла - Кислота соль + Н 2↑ - соль + Н 2 О другая соль + другая кислота (↓ или ↑) Соль другая соль + другой металл гидролиз некоторых солей - другая соль + другое основание↓ две новые соли (↓) к содержанию кислота соль + Н 2 О - Щелкнув левой клавишей мышки по соответствующей колонке таблицы вы рассмотрите данное свойство
Общие химические свойства и способы получения основных классов неорганических веществ Металл Вода Оксид металла Основание Соль Неметалл соль оксид - - Вода щелочь + Н 2↑ - щелочь - оксид + Н 2↑ гидролиз некоторых солей Оксид неметалла - Кислота соль + Н 2↑ - соль + Н 2 О другая соль + другая кислота (↓ или ↑) Соль другая соль + другой металл гидролиз некоторых солей - другая соль + другое основание↓ две новые соли (↓) к содержанию кислота соль + Н 2 О - Щелкнув левой клавишей мышки по соответствующей колонке таблицы вы рассмотрите данное свойство
 1. Me + не. Ме → соль 2 Al + 3 Cl 2→ 3 Al. Cl 3 2. Ме + О 2 → оксид металла 2 Zn + О 2 → 2 Zn. O к таблице к содержанию
1. Me + не. Ме → соль 2 Al + 3 Cl 2→ 3 Al. Cl 3 2. Ме + О 2 → оксид металла 2 Zn + О 2 → 2 Zn. O к таблице к содержанию
 1. Ме + Н 2 О → щелочь + Н 2↑ Обратите внимание! Так взаимодействуют только щелочные (IA) и щелочноземельные металлы (IIA), кроме Be и Mg 2 Na + 2 H 2 O → 2 Na. OH + H 2↑ 2. Ме + Н 2 О → оксид Ме + Н 2↑ Так взаимодействуют менее активные металлы в ряду активности до (Н 2) при нагревании Li K Ba Sr Ca Na Mg Al Mn Zn Cr Fe Co Ni Sn Pb (H 2) Cu Hg Ag Pt Au t 0 Zn + H 2 O → Zn. O +H 2↑ к таблице к содержанию
1. Ме + Н 2 О → щелочь + Н 2↑ Обратите внимание! Так взаимодействуют только щелочные (IA) и щелочноземельные металлы (IIA), кроме Be и Mg 2 Na + 2 H 2 O → 2 Na. OH + H 2↑ 2. Ме + Н 2 О → оксид Ме + Н 2↑ Так взаимодействуют менее активные металлы в ряду активности до (Н 2) при нагревании Li K Ba Sr Ca Na Mg Al Mn Zn Cr Fe Co Ni Sn Pb (H 2) Cu Hg Ag Pt Au t 0 Zn + H 2 O → Zn. O +H 2↑ к таблице к содержанию
 Оксид Ме + Н 2 О → щелочь Обратите внимание! Так взаимодействуют только оксиды щелочные (IA) и щелочноземельные металлы (IIA) Na 2 О + H 2 O → 2 Na. OH Ca. O + H 2 O → Ca(OH)2 к таблице к содержанию
Оксид Ме + Н 2 О → щелочь Обратите внимание! Так взаимодействуют только оксиды щелочные (IA) и щелочноземельные металлы (IIA) Na 2 О + H 2 O → 2 Na. OH Ca. O + H 2 O → Ca(OH)2 к таблице к содержанию
 Возможность и характер протекания гидролиза соли определяется её составом. 1. 2. Соль, образованная сильным основанием и сильной кислотой, гидролизу не подвергается Соль, образованная сильным основанием и слабой кислотой, подвергается гидролизу по аниону Ann- + HOH HAn(n-1)- + OH- 3. Соль, образованная слабым основанием и сильной кислотой, подвергается гидролизу по катиону Katn+ + HOH Kat. OH(n-1)+ + H+ 4. Соль, образованная слабым основанием и слабой кислотой, подвергается гидролизу по катиону и аниону, выбор иона определяется относительной силой кислоты или основания. к таблице к содержанию
Возможность и характер протекания гидролиза соли определяется её составом. 1. 2. Соль, образованная сильным основанием и сильной кислотой, гидролизу не подвергается Соль, образованная сильным основанием и слабой кислотой, подвергается гидролизу по аниону Ann- + HOH HAn(n-1)- + OH- 3. Соль, образованная слабым основанием и сильной кислотой, подвергается гидролизу по катиону Katn+ + HOH Kat. OH(n-1)+ + H+ 4. Соль, образованная слабым основанием и слабой кислотой, подвергается гидролизу по катиону и аниону, выбор иона определяется относительной силой кислоты или основания. к таблице к содержанию
 Оксид не. Ме + Н 2 О → кислота * Исключение кремний (IV) оксид Si. O 2, который с водой не реагирует SO 3 + H 2 O → H 2 SO 4 SO 2 + H 2 O → H 2 SO 3 к таблице к содержанию
Оксид не. Ме + Н 2 О → кислота * Исключение кремний (IV) оксид Si. O 2, который с водой не реагирует SO 3 + H 2 O → H 2 SO 4 SO 2 + H 2 O → H 2 SO 3 к таблице к содержанию
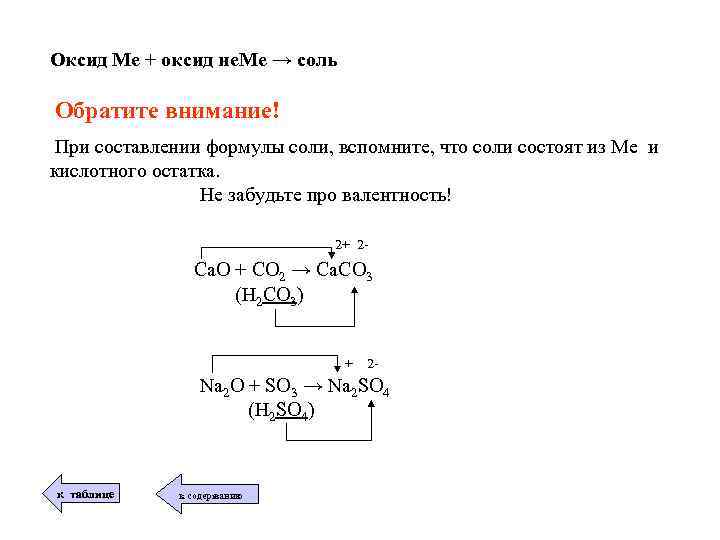 Оксид Ме + оксид не. Ме → соль Обратите внимание! При составлении формулы соли, вспомните, что соли состоят из Ме и кислотного остатка. Не забудьте про валентность! 2+ 2 - Ca. O + CO 2 → Ca. CO 3 (Н 2 СО 3) + 2 - Na 2 O + SO 3 → Na 2 SO 4 (H 2 SO 4) к таблице к содержанию
Оксид Ме + оксид не. Ме → соль Обратите внимание! При составлении формулы соли, вспомните, что соли состоят из Ме и кислотного остатка. Не забудьте про валентность! 2+ 2 - Ca. O + CO 2 → Ca. CO 3 (Н 2 СО 3) + 2 - Na 2 O + SO 3 → Na 2 SO 4 (H 2 SO 4) к таблице к содержанию
 Основание + оксид не. Ме → соль + Н 2 О Обратите внимание! В реакцию вступают только растворимые в воде основания (щелочи) 2 Na. OH + СO 2 → Na 2 CO 3 + H 2 O 6 KOH + P 2 O 5 → 2 K 3 PO 4 + 3 H 2 O к таблице к содержанию
Основание + оксид не. Ме → соль + Н 2 О Обратите внимание! В реакцию вступают только растворимые в воде основания (щелочи) 2 Na. OH + СO 2 → Na 2 CO 3 + H 2 O 6 KOH + P 2 O 5 → 2 K 3 PO 4 + 3 H 2 O к таблице к содержанию
 Кислота + Ме → соль + Н 2↑ Обратите внимание! Для реакции не брать азотную кислоту HNO 3 и конц. серную кислоту H 2 SO 4, а также металлы, стоящие в ряду активности до Н 2, т. к. они реагируют иначе. Zn + 2 HCl → Zn. Cl 2 + H 2↑ Mg + H 2 SO 4 → Mg. SO 4 + H 2↑ к таблице к содержанию
Кислота + Ме → соль + Н 2↑ Обратите внимание! Для реакции не брать азотную кислоту HNO 3 и конц. серную кислоту H 2 SO 4, а также металлы, стоящие в ряду активности до Н 2, т. к. они реагируют иначе. Zn + 2 HCl → Zn. Cl 2 + H 2↑ Mg + H 2 SO 4 → Mg. SO 4 + H 2↑ к таблице к содержанию
 Кислота + оксид Ме → соль + Н 2 О 2 HCl + Ca. O → Ca. Cl 2 + H 2 O t 0 H 2 SO 4 + Cu. O → Cu. SO 4 + H 2 O 6 HNO 3 + Al 2 O 3 → 2 Al(NO 3)3 + 3 H 2 O к таблице к содержанию
Кислота + оксид Ме → соль + Н 2 О 2 HCl + Ca. O → Ca. Cl 2 + H 2 O t 0 H 2 SO 4 + Cu. O → Cu. SO 4 + H 2 O 6 HNO 3 + Al 2 O 3 → 2 Al(NO 3)3 + 3 H 2 O к таблице к содержанию
 Основание + кислота → соль + Н 2 О Na. OH + HCl → Na. Cl + H 2 O 2 KOH + H 2 SO 4 → K 2 SO 4 + 2 H 2 O Cu(OH)2 + 2 HNO 3 → Cu(NO 3)2 + 2 H 2 O к таблице к содержанию (реакция нейтрализации)
Основание + кислота → соль + Н 2 О Na. OH + HCl → Na. Cl + H 2 O 2 KOH + H 2 SO 4 → K 2 SO 4 + 2 H 2 O Cu(OH)2 + 2 HNO 3 → Cu(NO 3)2 + 2 H 2 O к таблице к содержанию (реакция нейтрализации)
 Соль + кислота → др. соль + другая кислота (↑ или ↓) Обратите внимание! Реакция обмена протекает до конца только в том случае, если образуется осадок (↓) или выделяется газ (↑) Ag. NO 3 + HCl → Ag. Cl↓ + HNO 3 Ba. Cl 2 + H 2 SO 4 → Ba. SO 4↓ + 2 HCl Na 2 CO 3 + 2 HCl → 2 Na. Cl + H 2 CO 3 H 2 O CO 2↑ к таблице к содержанию
Соль + кислота → др. соль + другая кислота (↑ или ↓) Обратите внимание! Реакция обмена протекает до конца только в том случае, если образуется осадок (↓) или выделяется газ (↑) Ag. NO 3 + HCl → Ag. Cl↓ + HNO 3 Ba. Cl 2 + H 2 SO 4 → Ba. SO 4↓ + 2 HCl Na 2 CO 3 + 2 HCl → 2 Na. Cl + H 2 CO 3 H 2 O CO 2↑ к таблице к содержанию
 Соль + Ме → др. соль + др. Ме Обратите внимание! * Реакция протекает в соответствии с положением металла в ряду активности: более активный металл вытесняет менее активный из раствора его соли. (см. ряд активности) * Для реакции не следует брать щелочные и щелочноземельные металлы (от Li до Na), т. к. они активно взаимодействуют с водой. Cu. SO 4 + Fe → Fe. SO 4 + Cu Zn. Cl 2 +Mg → Mg. Cl 2 + Zn к таблице к содержанию
Соль + Ме → др. соль + др. Ме Обратите внимание! * Реакция протекает в соответствии с положением металла в ряду активности: более активный металл вытесняет менее активный из раствора его соли. (см. ряд активности) * Для реакции не следует брать щелочные и щелочноземельные металлы (от Li до Na), т. к. они активно взаимодействуют с водой. Cu. SO 4 + Fe → Fe. SO 4 + Cu Zn. Cl 2 +Mg → Mg. Cl 2 + Zn к таблице к содержанию
 Соль + основание → другая соль + другое основание ↓ Обратите внимание! * В реакцию ступают только растворимые соли и щелочи * Реакция протекает до конца, если полученное основание является нерастворимым (выпадает в осадок) Cu. SO 4 + 2 Na. OH → Na 2 SO 4 + Cu(OH)2↓ Fe. Cl 3 +3 KOH → 3 KCl + Fe(OH)3↓ к таблице к содержанию
Соль + основание → другая соль + другое основание ↓ Обратите внимание! * В реакцию ступают только растворимые соли и щелочи * Реакция протекает до конца, если полученное основание является нерастворимым (выпадает в осадок) Cu. SO 4 + 2 Na. OH → Na 2 SO 4 + Cu(OH)2↓ Fe. Cl 3 +3 KOH → 3 KCl + Fe(OH)3↓ к таблице к содержанию
 Соль + соль → две новые соли (↓) Обратите внимание! Реакция обмена протекает до конца, если одна из образующихся солей выпадает в осадок (↓) Ag. NO 3 + Na. Cl → Ag. Cl↓ + Na. NO 3 K 2 CO 3 + Ca(NO 3)2 → 2 KNO 3 + Ca. CO 3↓ к таблице к содержанию
Соль + соль → две новые соли (↓) Обратите внимание! Реакция обмена протекает до конца, если одна из образующихся солей выпадает в осадок (↓) Ag. NO 3 + Na. Cl → Ag. Cl↓ + Na. NO 3 K 2 CO 3 + Ca(NO 3)2 → 2 KNO 3 + Ca. CO 3↓ к таблице к содержанию
 Проверим! Этот тест поможет вам понять насколько вы усвоили химические свойства и способы получения основных классов неорганических веществ. Если во время ответа программа возвращает вас к учебному материалу, значит необходимо ещё раз повторить данное свойство, написать соответствующие уравнения реакций Выберите один правильный вариант ответа 1. Образует щелочь при взаимодействии с водой а) Cu. O б) K 2 O в) Zn. O г) Fe 2 O 3
Проверим! Этот тест поможет вам понять насколько вы усвоили химические свойства и способы получения основных классов неорганических веществ. Если во время ответа программа возвращает вас к учебному материалу, значит необходимо ещё раз повторить данное свойство, написать соответствующие уравнения реакций Выберите один правильный вариант ответа 1. Образует щелочь при взаимодействии с водой а) Cu. O б) K 2 O в) Zn. O г) Fe 2 O 3
 2. При взаимодействии натрия с водой образуются а) водород и натрий оксид б) кислород и натрий оксид в) натрий гидроксид и водород г) натрий гидроксид и кислород
2. При взаимодействии натрия с водой образуются а) водород и натрий оксид б) кислород и натрий оксид в) натрий гидроксид и водород г) натрий гидроксид и кислород
 3. Хлоридная кислота при обычных условиях взаимодействует с а) ртутью б) медью в) магнием г) серебром
3. Хлоридная кислота при обычных условиях взаимодействует с а) ртутью б) медью в) магнием г) серебром
 4. Каким веществом надо подействовать на цинк хлорид Zn. Cl 2, чтобы получить цинк гидроксид Zn(OH)2 а) H 2 O б) HCl в) Fe(OH)2 г) КОН
4. Каким веществом надо подействовать на цинк хлорид Zn. Cl 2, чтобы получить цинк гидроксид Zn(OH)2 а) H 2 O б) HCl в) Fe(OH)2 г) КОН
 5. Реакция нейтрализации протекает при взаимодействии а) Na. Cl + Ag. NO 3 б) Na. OH + HNO 3 в) K 2 O + H 2 O г) CO 2 + H 2 O
5. Реакция нейтрализации протекает при взаимодействии а) Na. Cl + Ag. NO 3 б) Na. OH + HNO 3 в) K 2 O + H 2 O г) CO 2 + H 2 O
 6. Барий хлорид Ba. Cl 2 взаимодействует с а) HNO 3 б) H 2 SO 4 в) HCl г) H 2 О
6. Барий хлорид Ba. Cl 2 взаимодействует с а) HNO 3 б) H 2 SO 4 в) HCl г) H 2 О
 7. Может вытеснить цинк из раствора его соли а) Fe б) Cu в) Al г) Na
7. Может вытеснить цинк из раствора его соли а) Fe б) Cu в) Al г) Na
 8. Реакция обмена протекает до конца между а) барий хлоридом и натрий нитратом б) цинк нитратом и калий сульфатом в) натрий карбонатом и кальций хлоридом г) барий нитратом и натрий хлоридом
8. Реакция обмена протекает до конца между а) барий хлоридом и натрий нитратом б) цинк нитратом и калий сульфатом в) натрий карбонатом и кальций хлоридом г) барий нитратом и натрий хлоридом
 9. Водород выделяется при взаимодействии а) Cu + HNO 3 б) Zn + H 2 SO 4 в) Ag + HCl г) Hg + H 3 PO 4
9. Водород выделяется при взаимодействии а) Cu + HNO 3 б) Zn + H 2 SO 4 в) Ag + HCl г) Hg + H 3 PO 4
 10. Натрий гидроксид при обычных условиях взаимодействует с а) карбон (IV) оксидом б)кальций оксидом в) медью г) водой
10. Натрий гидроксид при обычных условиях взаимодействует с а) карбон (IV) оксидом б)кальций оксидом в) медью г) водой
 Поздравляю! Вы успешно справились с заданием! Желаю вам успехов в освоении химии – одна из интереснейших и практически значимых наук.
Поздравляю! Вы успешно справились с заданием! Желаю вам успехов в освоении химии – одна из интереснейших и практически значимых наук.
 Приложение 1. Ряд активности металлов (электрохимический ряд напряжения металлов Li K Ba Sr Ca Na Mg Al Mn Zn Cr Fe Co Ni Sn Pb (H 2) Cu Hg Ag Pt Au к содержанию
Приложение 1. Ряд активности металлов (электрохимический ряд напряжения металлов Li K Ba Sr Ca Na Mg Al Mn Zn Cr Fe Co Ni Sn Pb (H 2) Cu Hg Ag Pt Au к содержанию
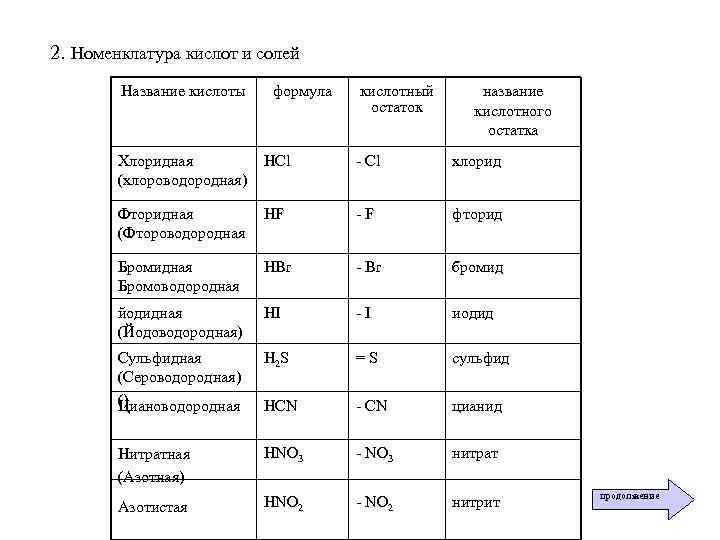 2. Номенклатура кислот и солей Название кислоты формула кислотный остаток название кислотного остатка Хлоридная (хлороводородная) HCl - Cl хлорид Фторидная (Фтороводородная HF -F фторид Бромидная Бромоводородная HBr - Br бромид йодидная (Йодоводородная) HI -I иодид Сульфидная (Сероводородная) () Циановодородная H 2 S =S сульфид HCN - CN цианид Нитратная (Азотная) HNO 3 - NO 3 нитрат Азотистая HNO 2 - NO 2 нитрит продолжение
2. Номенклатура кислот и солей Название кислоты формула кислотный остаток название кислотного остатка Хлоридная (хлороводородная) HCl - Cl хлорид Фторидная (Фтороводородная HF -F фторид Бромидная Бромоводородная HBr - Br бромид йодидная (Йодоводородная) HI -I иодид Сульфидная (Сероводородная) () Циановодородная H 2 S =S сульфид HCN - CN цианид Нитратная (Азотная) HNO 3 - NO 3 нитрат Азотистая HNO 2 - NO 2 нитрит продолжение
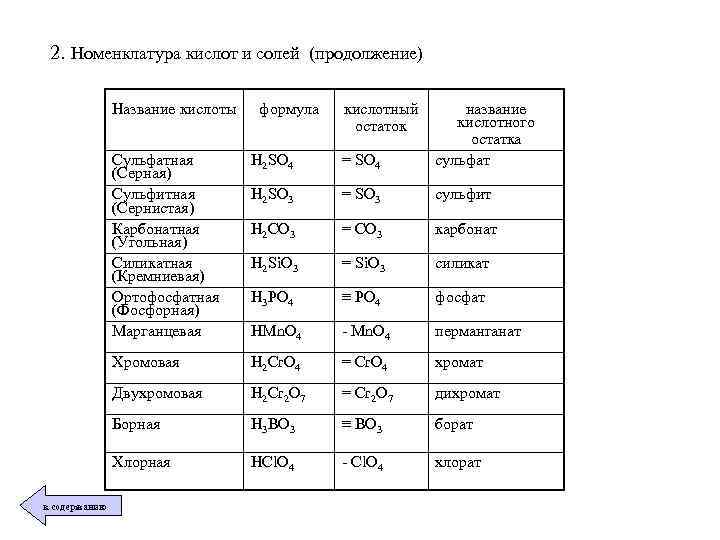 2. Номенклатура кислот и солей (продолжение) Название кислоты Сульфатная (Серная) Сульфитная (Сернистая) Карбонатная (Угольная) Силикатная (Кремниевая) Ортофосфатная (Фосфорная) Марганцевая H 2 SO 4 = SO 4 название кислотного остатка сульфат H 2 SO 3 = SO 3 сульфит H 2 CO 3 = CO 3 карбонат H 2 Si. O 3 = Si. O 3 силикат H 3 PO 4 ≡ PO 4 фосфат HMn. O 4 - Mn. O 4 перманганат Хромовая H 2 Cr. O 4 = Cr. O 4 хромат Двухромовая H 2 Cr 2 O 7 = Cr 2 O 7 дихромат Борная H 3 BO 3 ≡ BO 3 борат Хлорная к содержанию формула кислотный остаток HCl. O 4 - Cl. O 4 хлорат
2. Номенклатура кислот и солей (продолжение) Название кислоты Сульфатная (Серная) Сульфитная (Сернистая) Карбонатная (Угольная) Силикатная (Кремниевая) Ортофосфатная (Фосфорная) Марганцевая H 2 SO 4 = SO 4 название кислотного остатка сульфат H 2 SO 3 = SO 3 сульфит H 2 CO 3 = CO 3 карбонат H 2 Si. O 3 = Si. O 3 силикат H 3 PO 4 ≡ PO 4 фосфат HMn. O 4 - Mn. O 4 перманганат Хромовая H 2 Cr. O 4 = Cr. O 4 хромат Двухромовая H 2 Cr 2 O 7 = Cr 2 O 7 дихромат Борная H 3 BO 3 ≡ BO 3 борат Хлорная к содержанию формула кислотный остаток HCl. O 4 - Cl. O 4 хлорат
 Таблица растворимости солей, кислот и оснований в воде катионы Анионы OH- Cl- Br- I- S 2 - SO 42 - SO 32 - CO 32 - PO 43 - Cr. O 42 - NO 3 - CH 3 COO- Mn. O 4 - Na+ Р Р Р Р K+ Р Р Р Р NH 4+ Р Р Р Р Ag+ - НР НР МР НР НР Р Pb 2+ НР НР НР Р Р Р Hg 2+2 - НР НР МР НР НР Р Ca 2+ МР Р Р МР НР НР НР Р Р Sr 2+ МР Р Р НР НР МР Р Ba 2+ Р Р Р НР НР НР Р Al 3+ НР Р Р - НР НР Р Р Cr 3+ НР Р Р - НР НР НР Р Р - Zn 2+ НР Р - НР НР НР Р Sn 2+ НР Р Р МР НР Р - НР НР МР Р - - Mg 2+ МР Р Р МР НР НР Р Р Mn 2+ НР Р Р - НР НР - Р Р - Fe 2+ НР Р МР НР НР НР Р Р - Fe 3+ НР Р - НР НР НР Р Р - Bi 3+ НР Р - НР НР МР - НР НР НР - Ni 2+ НР Р НР НР НР - Р Р - Cu 2+ НР Р Р НР НР Р - НР НР НР Р Р - к содержанию
Таблица растворимости солей, кислот и оснований в воде катионы Анионы OH- Cl- Br- I- S 2 - SO 42 - SO 32 - CO 32 - PO 43 - Cr. O 42 - NO 3 - CH 3 COO- Mn. O 4 - Na+ Р Р Р Р K+ Р Р Р Р NH 4+ Р Р Р Р Ag+ - НР НР МР НР НР Р Pb 2+ НР НР НР Р Р Р Hg 2+2 - НР НР МР НР НР Р Ca 2+ МР Р Р МР НР НР НР Р Р Sr 2+ МР Р Р НР НР МР Р Ba 2+ Р Р Р НР НР НР Р Al 3+ НР Р Р - НР НР Р Р Cr 3+ НР Р Р - НР НР НР Р Р - Zn 2+ НР Р - НР НР НР Р Sn 2+ НР Р Р МР НР Р - НР НР МР Р - - Mg 2+ МР Р Р МР НР НР Р Р Mn 2+ НР Р Р - НР НР - Р Р - Fe 2+ НР Р МР НР НР НР Р Р - Fe 3+ НР Р - НР НР НР Р Р - Bi 3+ НР Р - НР НР МР - НР НР НР - Ni 2+ НР Р НР НР НР - Р Р - Cu 2+ НР Р Р НР НР Р - НР НР НР Р Р - к содержанию


