1 урок, 9 и 10 кл Осн классы неорг соед.pptx
- Количество слайдов: 30
 Основные классы неорганических соединений игра
Основные классы неорганических соединений игра
 Ход игры: • • • Выбрать жюри (2 человека) В игре участвуют 6 команд Придумать название командам Выбрать спикера команды Подписать название команды на заготовленных листочках (5 шт)
Ход игры: • • • Выбрать жюри (2 человека) В игре участвуют 6 команд Придумать название командам Выбрать спикера команды Подписать название команды на заготовленных листочках (5 шт)
 Жеребьевка • Назовите примеры двух атомов химических элементов с постоянной валентностью
Жеребьевка • Назовите примеры двух атомов химических элементов с постоянной валентностью
 Общие вопросы 100 200 300 400 500 Оксиды 100 200 300 400 500 Основания 100 200 300 400 500 Кислоты 100 200 300 400 500 Соли 100 200 300 400 500 ДЗ
Общие вопросы 100 200 300 400 500 Оксиды 100 200 300 400 500 Основания 100 200 300 400 500 Кислоты 100 200 300 400 500 Соли 100 200 300 400 500 ДЗ
 Общие вопросы 100 Перечислить основные классы неорганических соединений Оксиды Кислоты Соли Основания
Общие вопросы 100 Перечислить основные классы неорганических соединений Оксиды Кислоты Соли Основания
 Общие вопросы 200 • Дать определение оксида. • Оксиды – сложные вещества, состоящие из двух химических элементов один из которых кислород в степени окисления - 2.
Общие вопросы 200 • Дать определение оксида. • Оксиды – сложные вещества, состоящие из двух химических элементов один из которых кислород в степени окисления - 2.
 Общие вопросы 300 • Дать определения основания и щелочи. • Основания – сложные вещества, состоящие из атомов металла и одной или нескольких гидроксогрупп. • Щелочи – это растворимые или малорастворимые основания.
Общие вопросы 300 • Дать определения основания и щелочи. • Основания – сложные вещества, состоящие из атомов металла и одной или нескольких гидроксогрупп. • Щелочи – это растворимые или малорастворимые основания.
 Общие вопросы 400 • Дать определение индикатора. • Перечислить известные вам индикаторы. • Индикаторы – это вещества, меняющие свою окраску в зависимости от среды. • Лакмус • Метилоранж • Фенолфталеин.
Общие вопросы 400 • Дать определение индикатора. • Перечислить известные вам индикаторы. • Индикаторы – это вещества, меняющие свою окраску в зависимости от среды. • Лакмус • Метилоранж • Фенолфталеин.
 Общие вопросы 500 • Дать • Кислоты – сложные вещества, определения состоящие из атомов водорода и кислотных остатков. соли и • Соли – сложные вещества. кислоты. Как Состоящие из атомов металла и составляется кислотных остатков. Степень название Название = кислотного + металла + окисления соли? элемента, остатка в род пад. если она переменна
Общие вопросы 500 • Дать • Кислоты – сложные вещества, определения состоящие из атомов водорода и кислотных остатков. соли и • Соли – сложные вещества. кислоты. Как Состоящие из атомов металла и составляется кислотных остатков. Степень название Название = кислотного + металла + окисления соли? элемента, остатка в род пад. если она переменна
 Оксиды 100 • • степень название окисления оксид + первого + Как дается первого элемента, название оксида? в род. пад. если она Назвать переменна вещества: Na 2 O, N 2 O 5, Cl 2 O 7 • оксид натрия • оксид азота (V) • оксид хлора (VII)
Оксиды 100 • • степень название окисления оксид + первого + Как дается первого элемента, название оксида? в род. пад. если она Назвать переменна вещества: Na 2 O, N 2 O 5, Cl 2 O 7 • оксид натрия • оксид азота (V) • оксид хлора (VII)
 Оксиды 200 • Определение • Валентность < IV основных оксидов. O 2 • Число формул основных оксидов: Na 2 O, Cu. O, HCl, • Na. OH, Cl 2 O 7, CO 2 Основные оксиды – это оксиды металлов со Основный оксид степенью окисления +1, +2. 2
Оксиды 200 • Определение • Валентность < IV основных оксидов. O 2 • Число формул основных оксидов: Na 2 O, Cu. O, HCl, • Na. OH, Cl 2 O 7, CO 2 Основные оксиды – это оксиды металлов со Основный оксид степенью окисления +1, +2. 2
 Оксиды 300 Кислотные оксиды – Кислотный это оксиды 2 оксид неметаллов и оксиды металлов со • Выбрать формулы степенью окисления кислотных оксидов и больше 4. Валентность > IV назвать вещества: Кислотный H 2 SO 4, N 2 O 5, Mn 2 O 7, Zn. O, N 2 O 5 – оксид азота (V) O 2 оксид Na. OH, Fe. O. Mn 2 O 7 – оксид марганца (VII) • Дать определение кислотных оксидов. O
Оксиды 300 Кислотные оксиды – Кислотный это оксиды 2 оксид неметаллов и оксиды металлов со • Выбрать формулы степенью окисления кислотных оксидов и больше 4. Валентность > IV назвать вещества: Кислотный H 2 SO 4, N 2 O 5, Mn 2 O 7, Zn. O, N 2 O 5 – оксид азота (V) O 2 оксид Na. OH, Fe. O. Mn 2 O 7 – оксид марганца (VII) • Дать определение кислотных оксидов. O
 Оксиды 400 Кислотный оксид Амфотерный оксид • Дать определения • Амфотерные амфотерных оксиды – это С основанием и основным оксидов. оксидом – кислотные оксиды металлов свойства со степенью окисления +3, +4. Основный оксид • Исключить лишние вещества: • Ca. O, Al 2 O 3, Mn. O 2, Zn. O, С кислотой и кислотным Mn 2 O 5 оксидом – основные Ca. O, Fe 2 O 3, Mn 2 O 5 свойства
Оксиды 400 Кислотный оксид Амфотерный оксид • Дать определения • Амфотерные амфотерных оксиды – это С основанием и основным оксидов. оксидом – кислотные оксиды металлов свойства со степенью окисления +3, +4. Основный оксид • Исключить лишние вещества: • Ca. O, Al 2 O 3, Mn. O 2, Zn. O, С кислотой и кислотным Mn 2 O 5 оксидом – основные Ca. O, Fe 2 O 3, Mn 2 O 5 свойства
 Оксиды 500 • Исправить ошибки: оксид алюминия- Al 2 O оксид марганца (II) Mn. O 2 оксид кремния Si. O 2 оксид натрия Na 2 O оксид кальция (II) Ca. O Al 2 O 3 оксид марганца (II) Mn. O оксид кремния Si. O 2 оксид натрия Na 2 O оксид кальция Ca. O
Оксиды 500 • Исправить ошибки: оксид алюминия- Al 2 O оксид марганца (II) Mn. O 2 оксид кремния Si. O 2 оксид натрия Na 2 O оксид кальция (II) Ca. O Al 2 O 3 оксид марганца (II) Mn. O оксид кремния Si. O 2 оксид натрия Na 2 O оксид кальция Ca. O
 Основания 100 • Как даются названия основаниям? • Назвать основания: KOH, Fe(OH)3 Название степень гидроксид + металла + окисления в род. пад. металла, если она переменна • гидроксид калия гидроксид железа (III)
Основания 100 • Как даются названия основаниям? • Назвать основания: KOH, Fe(OH)3 Название степень гидроксид + металла + окисления в род. пад. металла, если она переменна • гидроксид калия гидроксид железа (III)
 Основания 200 • Выбрать щелочи и назвать их: • Fe(OH)2, Na. OH, Ca(OH)2, Al(OH)3, Cu(OH)2 • Na. OH гидроксид натрия • Ca(OH)2 гидроксид кальция
Основания 200 • Выбрать щелочи и назвать их: • Fe(OH)2, Na. OH, Ca(OH)2, Al(OH)3, Cu(OH)2 • Na. OH гидроксид натрия • Ca(OH)2 гидроксид кальция
 Основания 300 • Составить формулы: гидроксид кальция гидроксид меди (II) гидроксид цинка • Ca(OH)2, • Cu(OH)2, • Zn(OH)2
Основания 300 • Составить формулы: гидроксид кальция гидроксид меди (II) гидроксид цинка • Ca(OH)2, • Cu(OH)2, • Zn(OH)2
 Основания 400 • С помощью • Фенолфталеин какого (малиновый). индикатора Лакмус (синий). можно отличить щелочи от других Метилоранж (желтый). веществ?
Основания 400 • С помощью • Фенолфталеин какого (малиновый). индикатора Лакмус (синий). можно отличить щелочи от других Метилоранж (желтый). веществ?
 Основания 500 • Для основания Fe(OH)3 составить формулу соответствующего оксида. • Fe 2 O 3
Основания 500 • Для основания Fe(OH)3 составить формулу соответствующего оксида. • Fe 2 O 3
 Кислоты 100 • Как по формуле определить заряд кислотного остатка? • По числу атомов водорода.
Кислоты 100 • Как по формуле определить заряд кислотного остатка? • По числу атомов водорода.
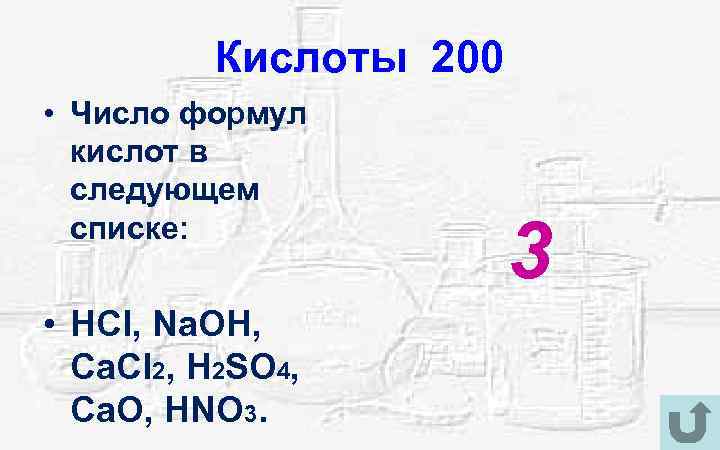 Кислоты 200 • Число формул кислот в следующем списке: • HCl, Na. OH, Ca. Cl 2, H 2 SO 4, Ca. O, HNO 3. 3
Кислоты 200 • Число формул кислот в следующем списке: • HCl, Na. OH, Ca. Cl 2, H 2 SO 4, Ca. O, HNO 3. 3
 Кислоты 300 Назвать кислоты, определить заряды кислотных остатков: HCl H 2 SO 4 HNO 3 H 2 Si. O 3 H 3 PO 4 • соляная (хлороводородная) -1 • серная -2 • азотная -1 • кремниевая -2 • фосфорная -3
Кислоты 300 Назвать кислоты, определить заряды кислотных остатков: HCl H 2 SO 4 HNO 3 H 2 Si. O 3 H 3 PO 4 • соляная (хлороводородная) -1 • серная -2 • азотная -1 • кремниевая -2 • фосфорная -3
 Кислоты 400 • Найти ошибки: H 2 SO 4 – сернистая H 2 PO 4 – фосфорная H 2 CO 3 – угольная H 2 SO 3 – сероводородная H 2 SO 4 – серная H 3 PO 4 – фосфорная H 2 CO 3 – угольная H 2 SO 3 –сернистая
Кислоты 400 • Найти ошибки: H 2 SO 4 – сернистая H 2 PO 4 – фосфорная H 2 CO 3 – угольная H 2 SO 3 – сероводородная H 2 SO 4 – серная H 3 PO 4 – фосфорная H 2 CO 3 – угольная H 2 SO 3 –сернистая
 Кислоты 500 • Составить SO 3 формулы N 2 O 5 оксидов, соответствующих Индикатор лакмус — красный кислотам H 2 SO 4, Кислоту укажет ясно. Индикатор лакмус — синий, HNO 3. Щёлочь здесь — не будь • Как меняется цвет разиней, лакмуса в Когда ж нейтральная среда, кислотах? Он фиолетовый всегда.
Кислоты 500 • Составить SO 3 формулы N 2 O 5 оксидов, соответствующих Индикатор лакмус — красный кислотам H 2 SO 4, Кислоту укажет ясно. Индикатор лакмус — синий, HNO 3. Щёлочь здесь — не будь • Как меняется цвет разиней, лакмуса в Когда ж нейтральная среда, кислотах? Он фиолетовый всегда.
 Соли 100 • Выбрать формулы солей • Ag. NO 3 нитрат и назвать их: серебра Ag. NO 3, Ca(OH)2, • Na. Cl хлорид HCl, Ca. O, Na. Cl. натрия
Соли 100 • Выбрать формулы солей • Ag. NO 3 нитрат и назвать их: серебра Ag. NO 3, Ca(OH)2, • Na. Cl хлорид HCl, Ca. O, Na. Cl. натрия
 Соли 200 • Формула сульфата железа (II): Fe. SO 4 Fe. S, Fe 2(SO 4)3, Fe. SO 4
Соли 200 • Формула сульфата железа (II): Fe. SO 4 Fe. S, Fe 2(SO 4)3, Fe. SO 4
 Соли 300 • Составьте формулы: • хлорид меди (II) • сульфат натрия • карбонат кальция • Cu. Cl 2 • Na 2 SO 4 • Ca. CO 3
Соли 300 • Составьте формулы: • хлорид меди (II) • сульфат натрия • карбонат кальция • Cu. Cl 2 • Na 2 SO 4 • Ca. CO 3
 Соли 400 • Какими основанием и кислотой образована соль Ba. SO 4. Назовите все вещества. • Ba. SO 4 сульфат бария • Ba(OH)2 гидроксид бария • H 2 SO 4 серная кислота
Соли 400 • Какими основанием и кислотой образована соль Ba. SO 4. Назовите все вещества. • Ba. SO 4 сульфат бария • Ba(OH)2 гидроксид бария • H 2 SO 4 серная кислота
 Соли 500 • Напишите формулы соответствую щих оксидов для вещества Al 2(SO 4)3. Назовите все вещества. • Al 2(SO 4)3 сульфат алюминия • Al 2 O 3 оксид алюминия • SO 3 оксид серы (VI)
Соли 500 • Напишите формулы соответствую щих оксидов для вещества Al 2(SO 4)3. Назовите все вещества. • Al 2(SO 4)3 сульфат алюминия • Al 2 O 3 оксид алюминия • SO 3 оксид серы (VI)
 ДЗ Домашнее задание • Выучить § 1 • Письменно: задание 1, стр. 10 (9 класс) • Просмотреть темы «Периодический закон и периодическая система» и «Строение атома» • Обязательно! Иметь при себе таблицу Менделеева
ДЗ Домашнее задание • Выучить § 1 • Письменно: задание 1, стр. 10 (9 класс) • Просмотреть темы «Периодический закон и периодическая система» и «Строение атома» • Обязательно! Иметь при себе таблицу Менделеева


