Osn._klassy_2012-2013_2_semestr_MF.ppt
- Количество слайдов: 25
 Основные классы неорганических соединений
Основные классы неорганических соединений
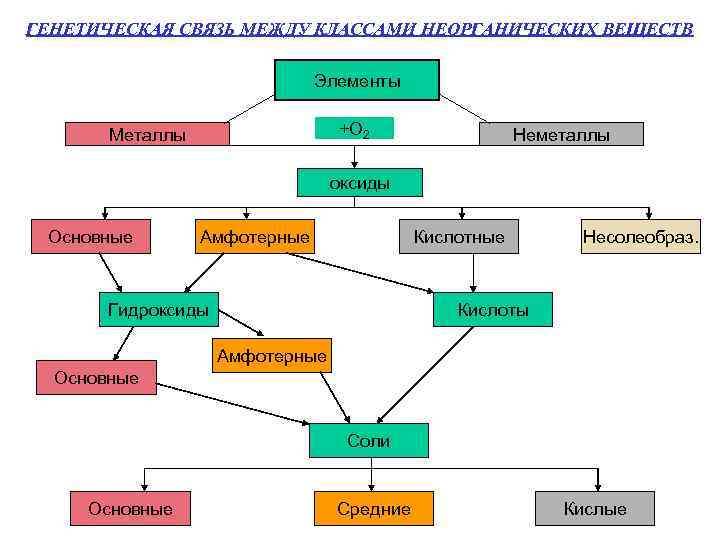 ГЕНЕТИЧЕСКАЯ СВЯЗЬ МЕЖДУ КЛАССАМИ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ Элементы +О 2 Металлы Неметаллы оксиды Основные Амфотерные Кислотные Гидроксиды Несолеобраз. Кислоты Амфотерные Основные Соли Основные Средние Кислые
ГЕНЕТИЧЕСКАЯ СВЯЗЬ МЕЖДУ КЛАССАМИ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ Элементы +О 2 Металлы Неметаллы оксиды Основные Амфотерные Кислотные Гидроксиды Несолеобраз. Кислоты Амфотерные Основные Соли Основные Средние Кислые
 ОКСИДЫ. КЛАССИФИКАЦИЯ. ПОЛУЧЕНИЕ. СВОЙСТВА • Оксиды - сложные Формула вещества, состоящие из двух химических CO элементов, один из NO которых кислород, со N 2 O 5 степенью окисления 2. Fe 2 O 3 Название оксид углерода ( II ) оксид азота (V ) оксид железа (III )
ОКСИДЫ. КЛАССИФИКАЦИЯ. ПОЛУЧЕНИЕ. СВОЙСТВА • Оксиды - сложные Формула вещества, состоящие из двух химических CO элементов, один из NO которых кислород, со N 2 O 5 степенью окисления 2. Fe 2 O 3 Название оксид углерода ( II ) оксид азота (V ) оксид железа (III )
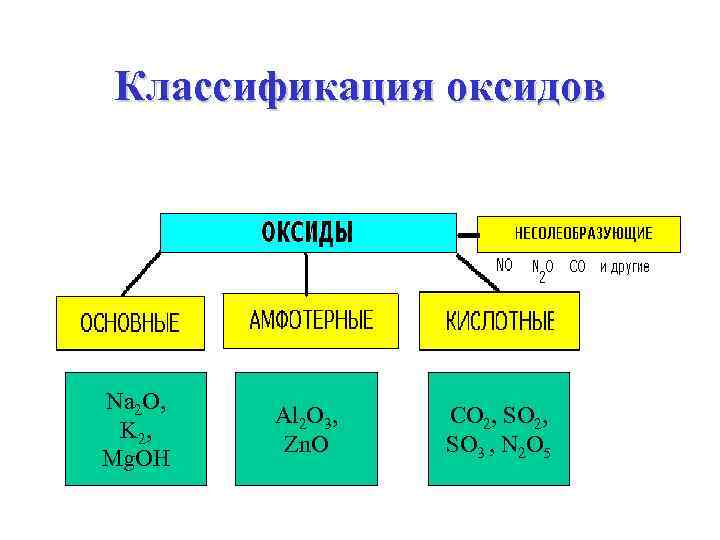 Классификация оксидов Na 2 O, K 2, Mg. OH Al 2 O 3, Zn. O CO 2, SO 3 , N 2 O 5
Классификация оксидов Na 2 O, K 2, Mg. OH Al 2 O 3, Zn. O CO 2, SO 3 , N 2 O 5
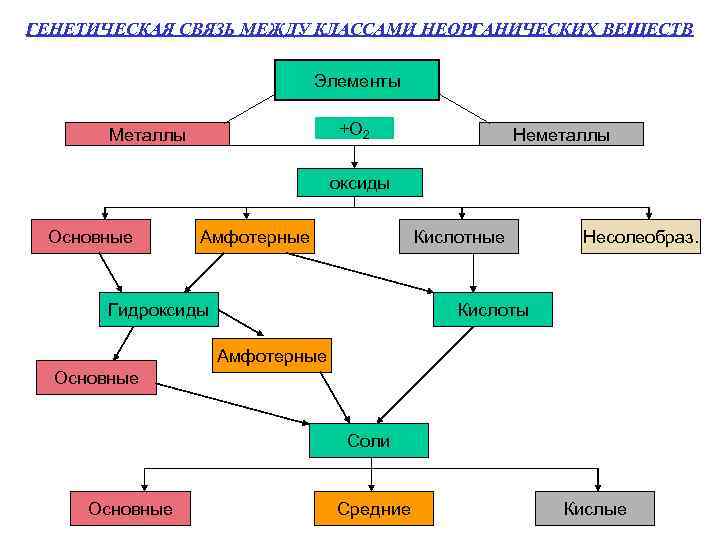 ГЕНЕТИЧЕСКАЯ СВЯЗЬ МЕЖДУ КЛАССАМИ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ Элементы +О 2 Металлы Неметаллы оксиды Основные Амфотерные Кислотные Гидроксиды Несолеобраз. Кислоты Амфотерные Основные Соли Основные Средние Кислые
ГЕНЕТИЧЕСКАЯ СВЯЗЬ МЕЖДУ КЛАССАМИ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ Элементы +О 2 Металлы Неметаллы оксиды Основные Амфотерные Кислотные Гидроксиды Несолеобраз. Кислоты Амфотерные Основные Соли Основные Средние Кислые
 Химические свойства оксидов • 1. Взаимодействие с водой : • а) основной оксид • Ca. O + H 2 O = Ca(OH)2 • гидроксид кальция основной оксид • б) кислотный оксид • • основание SO 3 + H 2 O = H 2 SO 4 • • ; оксид серы (IV) кислотный оксид серная кислота • 2. С кислотами : • • а) основной оксид Li 2 O + 2 HCl = 2 Li. Cl + 2 H 2 O ; оксид Li хлорид лития основной оксид соль б) амфотерный оксид AI 2 O 3 + 6 HCl = 2 Al. Cl 3 + 3 H 2 O оксид AI хлорид AI амфотерный оксид соль
Химические свойства оксидов • 1. Взаимодействие с водой : • а) основной оксид • Ca. O + H 2 O = Ca(OH)2 • гидроксид кальция основной оксид • б) кислотный оксид • • основание SO 3 + H 2 O = H 2 SO 4 • • ; оксид серы (IV) кислотный оксид серная кислота • 2. С кислотами : • • а) основной оксид Li 2 O + 2 HCl = 2 Li. Cl + 2 H 2 O ; оксид Li хлорид лития основной оксид соль б) амфотерный оксид AI 2 O 3 + 6 HCl = 2 Al. Cl 3 + 3 H 2 O оксид AI хлорид AI амфотерный оксид соль
 Химические свойства оксидов (продолжение) • 3. С кислотными оксидами: • а) основной оксид Ca. O + CO 2 = Ca. CO 3 основной • • • кислотный оксид соль оксид б) амфотерный оксид Zn. O + Si. O 2 = Zn. Si. O 3 амфотерный оксид кислотный оксид соль
Химические свойства оксидов (продолжение) • 3. С кислотными оксидами: • а) основной оксид Ca. O + CO 2 = Ca. CO 3 основной • • • кислотный оксид соль оксид б) амфотерный оксид Zn. O + Si. O 2 = Zn. Si. O 3 амфотерный оксид кислотный оксид соль
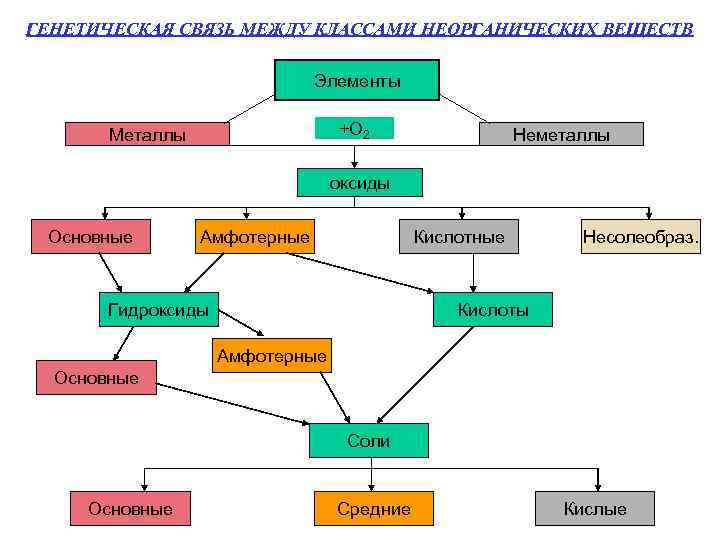 ГЕНЕТИЧЕСКАЯ СВЯЗЬ МЕЖДУ КЛАССАМИ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ Элементы +О 2 Металлы Неметаллы оксиды Основные Амфотерные Кислотные Гидроксиды Несолеобраз. Кислоты Амфотерные Основные Соли Основные Средние Кислые
ГЕНЕТИЧЕСКАЯ СВЯЗЬ МЕЖДУ КЛАССАМИ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ Элементы +О 2 Металлы Неметаллы оксиды Основные Амфотерные Кислотные Гидроксиды Несолеобраз. Кислоты Амфотерные Основные Соли Основные Средние Кислые
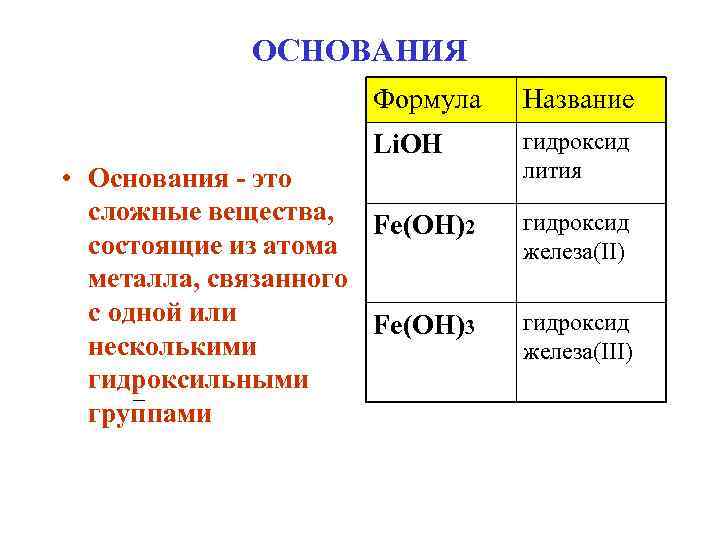 ОСНОВАНИЯ Формула Название Li. OH гидроксид лития • Основания - это сложные вещества, Fe(OH)2 состоящие из атома металла, связанного с одной или Fe(OH)3 несколькими гидроксильными группами гидроксид железа(II) гидроксид железа(III)
ОСНОВАНИЯ Формула Название Li. OH гидроксид лития • Основания - это сложные вещества, Fe(OH)2 состоящие из атома металла, связанного с одной или Fe(OH)3 несколькими гидроксильными группами гидроксид железа(II) гидроксид железа(III)
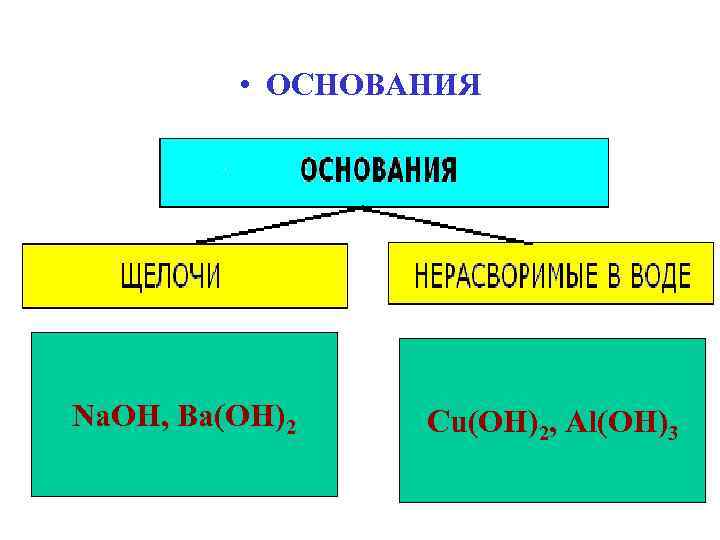 • ОСНОВАНИЯ Na. OH, Ba(OH)2 Cu(OH)2, Al(OH)3
• ОСНОВАНИЯ Na. OH, Ba(OH)2 Cu(OH)2, Al(OH)3
 • Основания (по теории электролитической диссоциации) - электролиты, при диссоциации которых в качестве анионов образуются только анионы гидроскила ОН¯ : • 1) диссоциация однокислотного основания: + + OН– ; • Na. OH Na • 2) ступенчатая диссоциация двухкислотного основания: – - 1 ступень, • Ba(OH)2 Ba + OН + Ba 2+ + OН– - 2 ступень • Ba OН + OН
• Основания (по теории электролитической диссоциации) - электролиты, при диссоциации которых в качестве анионов образуются только анионы гидроскила ОН¯ : • 1) диссоциация однокислотного основания: + + OН– ; • Na. OH Na • 2) ступенчатая диссоциация двухкислотного основания: – - 1 ступень, • Ba(OH)2 Ba + OН + Ba 2+ + OН– - 2 ступень • Ba OН + OН
 ОСНОВАНИЯ • Щелочи - растворимые гидроксиды щелочных и щелочноземельных металлов: Li. OH, Na. OH, KOH, Rb. OH, Cs. OH, Ca(OH)2, Sr(OH)2, Ba(OH)2. • Реакция нейтрализации: KOH + HCl = KCl + H 2 O • Нерастворимые - амфотерные гидроксиды, гидроксиды которые взаимодействуют • с кислотами - как основания, • а со щёлочами - как кислоты. • • Cu(OH)2 + 2 HCl = Cu. Cl 2 + 2 H 2 O Al(OH)3 + Na. OH = Na[Al(OH)4]
ОСНОВАНИЯ • Щелочи - растворимые гидроксиды щелочных и щелочноземельных металлов: Li. OH, Na. OH, KOH, Rb. OH, Cs. OH, Ca(OH)2, Sr(OH)2, Ba(OH)2. • Реакция нейтрализации: KOH + HCl = KCl + H 2 O • Нерастворимые - амфотерные гидроксиды, гидроксиды которые взаимодействуют • с кислотами - как основания, • а со щёлочами - как кислоты. • • Cu(OH)2 + 2 HCl = Cu. Cl 2 + 2 H 2 O Al(OH)3 + Na. OH = Na[Al(OH)4]
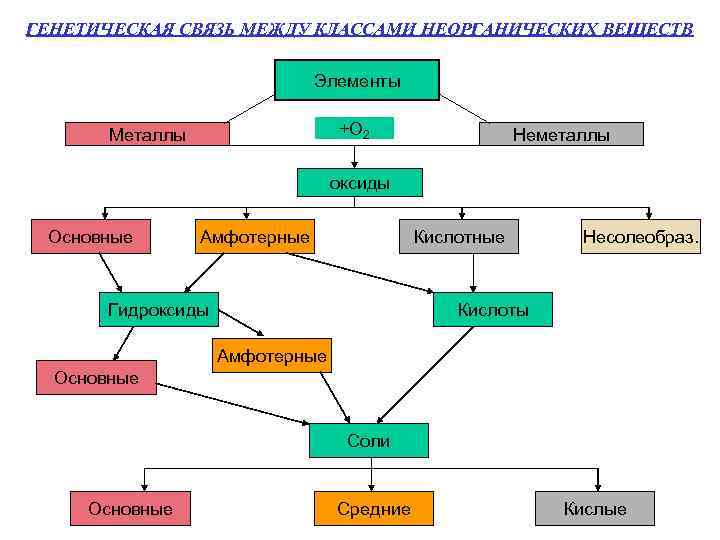 ГЕНЕТИЧЕСКАЯ СВЯЗЬ МЕЖДУ КЛАССАМИ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ Элементы +О 2 Металлы Неметаллы оксиды Основные Амфотерные Кислотные Гидроксиды Несолеобраз. Кислоты Амфотерные Основные Соли Основные Средние Кислые
ГЕНЕТИЧЕСКАЯ СВЯЗЬ МЕЖДУ КЛАССАМИ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ Элементы +О 2 Металлы Неметаллы оксиды Основные Амфотерные Кислотные Гидроксиды Несолеобраз. Кислоты Амфотерные Основные Соли Основные Средние Кислые
 КИСЛОТЫ • Кислоты - сложные вещества, состоящие из одного или нескольких атомов водорода и кислотных остатков (Hx Any). • Кислотные остатки (анионы): • Сl- (хлорид), SO 4 2 - (сульфат), РО 43(фосфат)
КИСЛОТЫ • Кислоты - сложные вещества, состоящие из одного или нескольких атомов водорода и кислотных остатков (Hx Any). • Кислотные остатки (анионы): • Сl- (хлорид), SO 4 2 - (сульфат), РО 43(фосфат)
 • Кислоты (по теории электролитической диссоциации) - электролиты, при диссоциации которых в качестве катионов образуются только катионы водорода Н+ • 1) • диссоциация одноосновной кислоты: + + NO 3– ; HNO 3 Н • 2) ступенчатая диссоциация двухосновной кислоты: + + НSO 4– • H 2 SO 4 Н - 1 ступень, – Н+ + SO 42– • НSO 4 - 2 ступень
• Кислоты (по теории электролитической диссоциации) - электролиты, при диссоциации которых в качестве катионов образуются только катионы водорода Н+ • 1) • диссоциация одноосновной кислоты: + + NO 3– ; HNO 3 Н • 2) ступенчатая диссоциация двухосновной кислоты: + + НSO 4– • H 2 SO 4 Н - 1 ступень, – Н+ + SO 42– • НSO 4 - 2 ступень
 Классификация кислот • Число атомов водорода определяет основность кислот: • 1) одноосновные: • HCl • • • HF HI HBr HNO 2 HNO 3 - хлороводородная, или соляная; фтороводородная, или плавиковая; иодоводородная кислота; бромоводородная кислота; азотистая кислота; азотная кислота;
Классификация кислот • Число атомов водорода определяет основность кислот: • 1) одноосновные: • HCl • • • HF HI HBr HNO 2 HNO 3 - хлороводородная, или соляная; фтороводородная, или плавиковая; иодоводородная кислота; бромоводородная кислота; азотистая кислота; азотная кислота;
 • 2) двухосновные: • • • H 2 SO 4 H 2 CO 3 - сероводородная кислота; серная кислота ; угольная кислота; • 2) трехосновные: • H 3 PO 4 - фосфорная кислота
• 2) двухосновные: • • • H 2 SO 4 H 2 CO 3 - сероводородная кислота; серная кислота ; угольная кислота; • 2) трехосновные: • H 3 PO 4 - фосфорная кислота
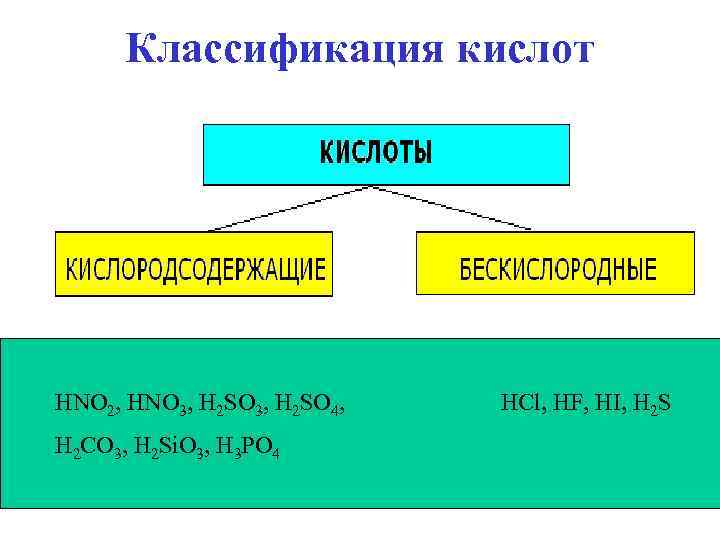 Классификация кислот HNO 2, HNO 3, H 2 SO 4, H 2 CO 3, H 2 Si. O 3, H 3 PO 4 HCl, HF, HI, H 2 S
Классификация кислот HNO 2, HNO 3, H 2 SO 4, H 2 CO 3, H 2 Si. O 3, H 3 PO 4 HCl, HF, HI, H 2 S
 Химические свойства кислот • 1. С основаниями, образуя соль и воду (реакция нейтрализации) • Н 2 SО 4 + 2 Nа. OH = Nа 2 SО 4 + 2 Н 2 О; • 2. С основными оксидами • 2 НСl + Мg. О = Мg. Сl 2 + Н 2 О ;
Химические свойства кислот • 1. С основаниями, образуя соль и воду (реакция нейтрализации) • Н 2 SО 4 + 2 Nа. OH = Nа 2 SО 4 + 2 Н 2 О; • 2. С основными оксидами • 2 НСl + Мg. О = Мg. Сl 2 + Н 2 О ;
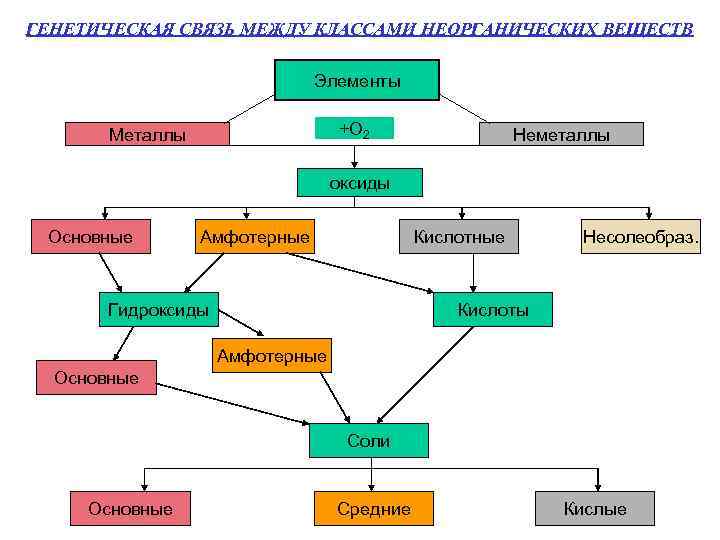 ГЕНЕТИЧЕСКАЯ СВЯЗЬ МЕЖДУ КЛАССАМИ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ Элементы +О 2 Металлы Неметаллы оксиды Основные Амфотерные Кислотные Гидроксиды Несолеобраз. Кислоты Амфотерные Основные Соли Основные Средние Кислые
ГЕНЕТИЧЕСКАЯ СВЯЗЬ МЕЖДУ КЛАССАМИ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ Элементы +О 2 Металлы Неметаллы оксиды Основные Амфотерные Кислотные Гидроксиды Несолеобраз. Кислоты Амфотерные Основные Соли Основные Средние Кислые
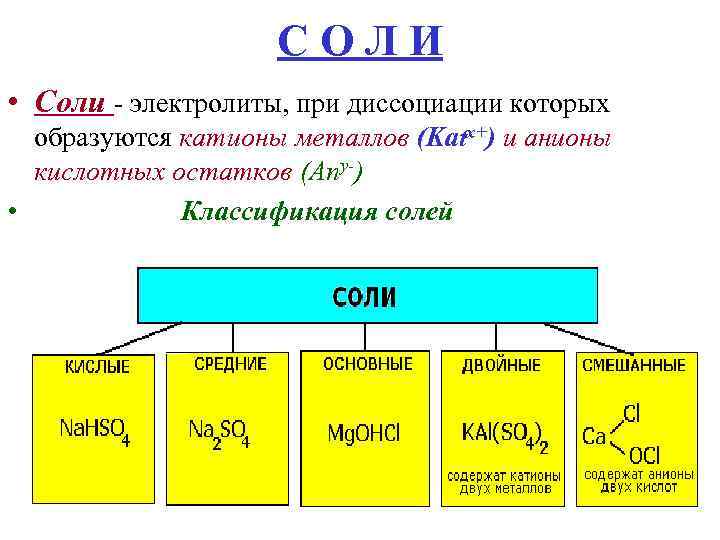 СОЛИ • Соли - электролиты, при диссоциации которых образуются катионы металлов (Katх+) и анионы кислотных остатков (Any-) • Классификация солей
СОЛИ • Соли - электролиты, при диссоциации которых образуются катионы металлов (Katх+) и анионы кислотных остатков (Any-) • Классификация солей
 Классификация солей • 1) средние (нормальные) • в реакции нейтрализации образуются средняя соль и вода: • • KOH + HNO 3 = КNO 3 + H 2 O ; нитрат калия • К+ + OH¯ + H + + NO 3 ¯ = К+ + NO 3– + H 2 O • КNO 3 К+ + NO 3–
Классификация солей • 1) средние (нормальные) • в реакции нейтрализации образуются средняя соль и вода: • • KOH + HNO 3 = КNO 3 + H 2 O ; нитрат калия • К+ + OH¯ + H + + NO 3 ¯ = К+ + NO 3– + H 2 O • КNO 3 К+ + NO 3–
 Классификация солей • 2) кислые : • в реакции нейтрализации образуются кислая соль и вода: • KOH + • H 2 S = КHS + H 2 O ; гидросульфид калия • K+ + OH¯ + H + + HS¯ = К + + HS¯ + H 2 O • КHS К+ + НS–
Классификация солей • 2) кислые : • в реакции нейтрализации образуются кислая соль и вода: • KOH + • H 2 S = КHS + H 2 O ; гидросульфид калия • K+ + OH¯ + H + + HS¯ = К + + HS¯ + H 2 O • КHS К+ + НS–
 Классификация солей • 3) основные : • в реакции нейтрализации образуются основная соль и вода: • Al(OH)3 + HCl • • = Al(OH)2 Cl + дигидроксохлорид алюминия Al(OH)2 Cl Al(OН)2+ + Cl– H 2 O
Классификация солей • 3) основные : • в реакции нейтрализации образуются основная соль и вода: • Al(OH)3 + HCl • • = Al(OH)2 Cl + дигидроксохлорид алюминия Al(OH)2 Cl Al(OН)2+ + Cl– H 2 O
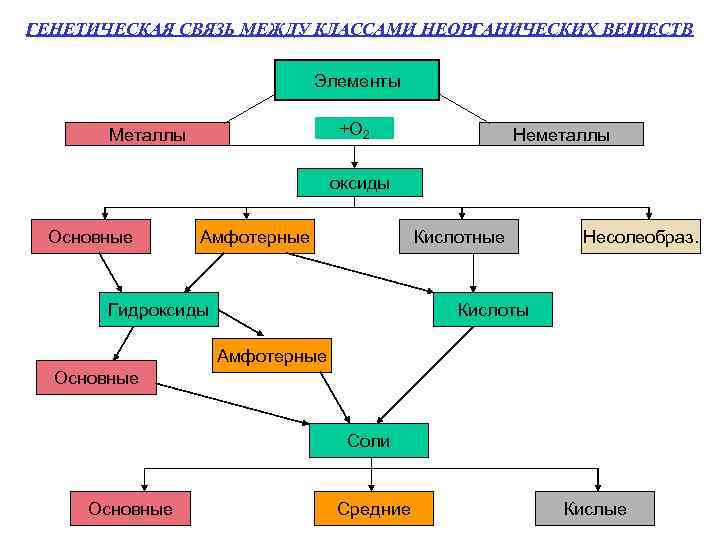 ГЕНЕТИЧЕСКАЯ СВЯЗЬ МЕЖДУ КЛАССАМИ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ Элементы +О 2 Металлы Неметаллы оксиды Основные Амфотерные Кислотные Гидроксиды Несолеобраз. Кислоты Амфотерные Основные Соли Основные Средние Кислые
ГЕНЕТИЧЕСКАЯ СВЯЗЬ МЕЖДУ КЛАССАМИ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ Элементы +О 2 Металлы Неметаллы оксиды Основные Амфотерные Кислотные Гидроксиды Несолеобраз. Кислоты Амфотерные Основные Соли Основные Средние Кислые


