Lecture4.ppt
- Количество слайдов: 32
 ОСНОВНІ ПОЛОЖЕННЯ ТЕОРІЇ РОЗЧИНІВ
ОСНОВНІ ПОЛОЖЕННЯ ТЕОРІЇ РОЗЧИНІВ
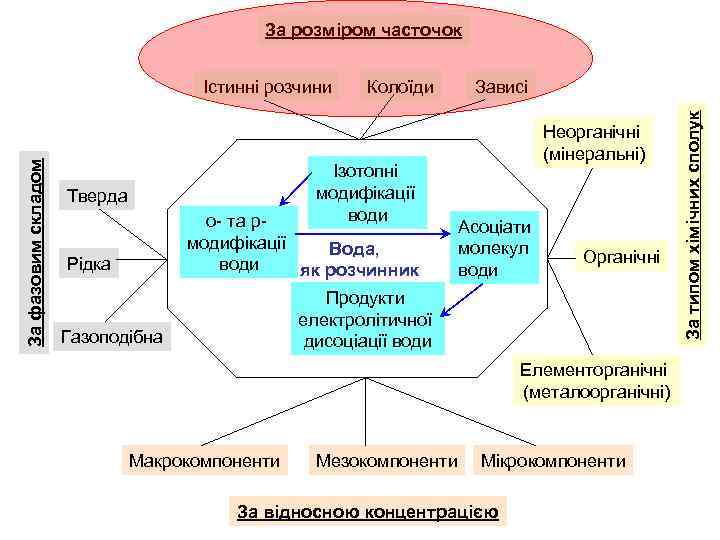 За розміром часточок Колоїди Ізотопні модифікації води Тверда о- та р- модифікації Вода, води як розчинник Рідка Зависі Неорганічні (мінеральні) Асоціати молекул води Органічні Продукти електролітичної дисоціації води Газоподібна Елементорганічні (металоорганічні) Макрокомпоненти Мезокомпоненти Мікрокомпоненти За відносною концентрацією За типом хімічних сполук За фазовим складом Істинні розчини
За розміром часточок Колоїди Ізотопні модифікації води Тверда о- та р- модифікації Вода, води як розчинник Рідка Зависі Неорганічні (мінеральні) Асоціати молекул води Органічні Продукти електролітичної дисоціації води Газоподібна Елементорганічні (металоорганічні) Макрокомпоненти Мезокомпоненти Мікрокомпоненти За відносною концентрацією За типом хімічних сполук За фазовим складом Істинні розчини
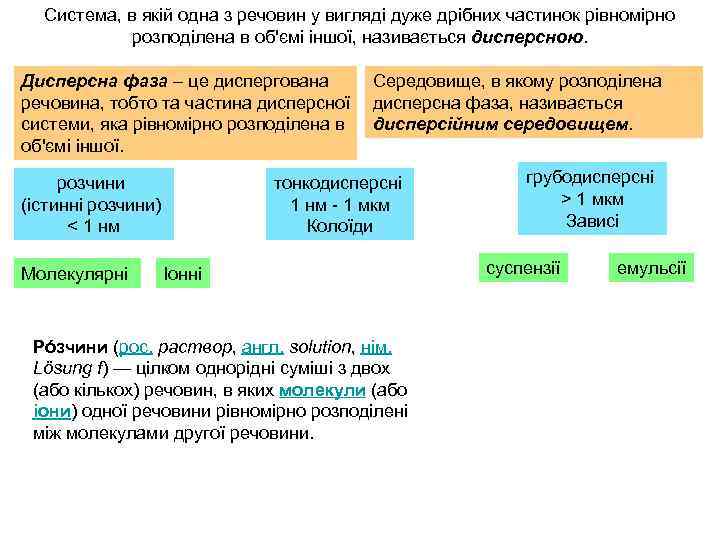 Система, в якій одна з речовин у вигляді дуже дрібних частинок рівномірно розподілена в об'ємі іншої, називається дисперсною. Дисперсна фаза – це диспергована Середовище, в якому розподілена речовина, тобто та частина дисперсної дисперсна фаза, називається системи, яка рівномірно розподілена в дисперсійним середовищем. об'ємі іншої. розчини (істинні розчини) < 1 нм Молекулярні тонкодисперсні 1 нм - 1 мкм Колоїди Іонні Рóзчини (рос. раствор, англ. solution, нім. Lösung f) — цілком однорідні суміші з двох (або кількох) речовин, в яких молекули (або іони) одної речовини рівномірно розподілені між молекулами другої речовини. грубодисперсні > 1 мкм Зависі суспензії емульсії
Система, в якій одна з речовин у вигляді дуже дрібних частинок рівномірно розподілена в об'ємі іншої, називається дисперсною. Дисперсна фаза – це диспергована Середовище, в якому розподілена речовина, тобто та частина дисперсної дисперсна фаза, називається системи, яка рівномірно розподілена в дисперсійним середовищем. об'ємі іншої. розчини (істинні розчини) < 1 нм Молекулярні тонкодисперсні 1 нм - 1 мкм Колоїди Іонні Рóзчини (рос. раствор, англ. solution, нім. Lösung f) — цілком однорідні суміші з двох (або кількох) речовин, в яких молекули (або іони) одної речовини рівномірно розподілені між молекулами другої речовини. грубодисперсні > 1 мкм Зависі суспензії емульсії
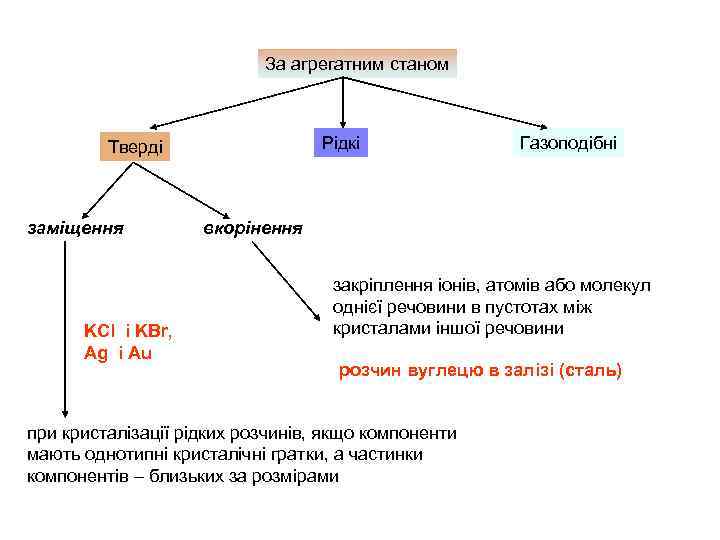 За агрегатним станом Рідкі Тверді заміщення KCl і KBr, Ag і Au Газоподібні вкорінення закріплення іонів, атомів або молекул однієї речовини в пустотах між кристалами іншої речовини розчин вуглецю в залізі (сталь) при кристалізації рідких розчинів, якщо компоненти мають однотипні кристалічні гратки, а частинки компонентів – близьких за розмірами
За агрегатним станом Рідкі Тверді заміщення KCl і KBr, Ag і Au Газоподібні вкорінення закріплення іонів, атомів або молекул однієї речовини в пустотах між кристалами іншої речовини розчин вуглецю в залізі (сталь) при кристалізації рідких розчинів, якщо компоненти мають однотипні кристалічні гратки, а частинки компонентів – близьких за розмірами
 Рідкі розчини (рідкі однофазні системи) утворюються при розчиненні газоподібних, рідких або твердих речовин в рідкому дисперсійному середовищі (розчиннику). Незалежно від вмісту розчиненої речовини розчинником вважають той компонент розчину, агрегатний стан якого не змінюється під час виготовлення розчину, тобто залишається рідким. Якщо розчин утворюється при змішуванні систем однакового агрегатного стану (газ-газ, рідина-рідина, тверда речовина-тверда речовина), то розчинником вважають компонент, кількість якого переважає
Рідкі розчини (рідкі однофазні системи) утворюються при розчиненні газоподібних, рідких або твердих речовин в рідкому дисперсійному середовищі (розчиннику). Незалежно від вмісту розчиненої речовини розчинником вважають той компонент розчину, агрегатний стан якого не змінюється під час виготовлення розчину, тобто залишається рідким. Якщо розчин утворюється при змішуванні систем однакового агрегатного стану (газ-газ, рідина-рідина, тверда речовина-тверда речовина), то розчинником вважають компонент, кількість якого переважає
 Фізико-хімічна теорія розчинів Фізична теорія розчинів (Я. Вант. Гоф, С. Арреніус) розглядає процес розчинення як простий розподіл (диспергування) однієї речовини у всьому об'ємі іншої. Властивості розчинів повинні залежати тільки від концентрації розчиненої речовини. Розчинник – це індиферентне середовище, в якому хаотично розподілені частинки розчиненої речовини Д. І. Менделєєв показав, що в розчині є сполуки, які утворюються завдяки взаємодії молекул розчиненої речовини і розчинника. Такі сполуки називаються сольватами (гідратами), а процес їх утворення в результаті взаємодії компонентів розчину – сольватацією (гідратацією). Термін “гідрати” і “гідратація” застосовують, коли розчинником є вода.
Фізико-хімічна теорія розчинів Фізична теорія розчинів (Я. Вант. Гоф, С. Арреніус) розглядає процес розчинення як простий розподіл (диспергування) однієї речовини у всьому об'ємі іншої. Властивості розчинів повинні залежати тільки від концентрації розчиненої речовини. Розчинник – це індиферентне середовище, в якому хаотично розподілені частинки розчиненої речовини Д. І. Менделєєв показав, що в розчині є сполуки, які утворюються завдяки взаємодії молекул розчиненої речовини і розчинника. Такі сполуки називаються сольватами (гідратами), а процес їх утворення в результаті взаємодії компонентів розчину – сольватацією (гідратацією). Термін “гідрати” і “гідратація” застосовують, коли розчинником є вода.
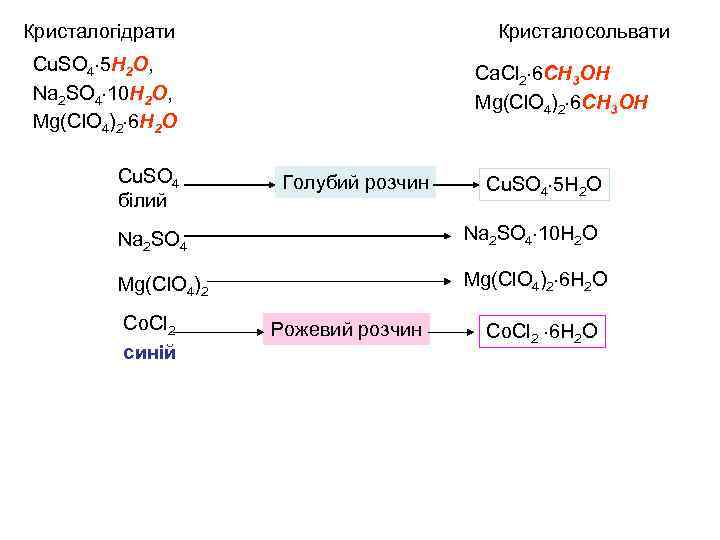 Кристалогідрати Кристалосольвати Cu. SO 4 5 H 2 O, Na 2 SO 4 10 H 2 O, Mg(Cl. O 4)2 6 H 2 O Cu. SO 4 білий Ca. Cl 2 6 CH 3 OH Mg(Cl. O 4)2 6 CH 3 OH Голубий розчин Cu. SO 4 5 H 2 O Na 2 SO 4 10 H 2 O Mg(Cl. O 4)2 6 H 2 O Co. Cl 2 синій Рожевий розчин Co. Cl 2 6 H 2 O
Кристалогідрати Кристалосольвати Cu. SO 4 5 H 2 O, Na 2 SO 4 10 H 2 O, Mg(Cl. O 4)2 6 H 2 O Cu. SO 4 білий Ca. Cl 2 6 CH 3 OH Mg(Cl. O 4)2 6 CH 3 OH Голубий розчин Cu. SO 4 5 H 2 O Na 2 SO 4 10 H 2 O Mg(Cl. O 4)2 6 H 2 O Co. Cl 2 синій Рожевий розчин Co. Cl 2 6 H 2 O
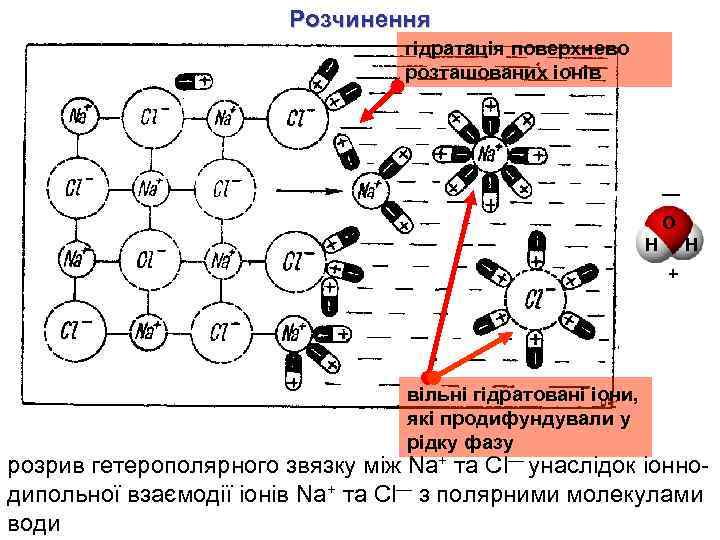 Розчинення гідратація поверхнево розташованих іонів — O H H + вільні гідратовані іони, які продифундували у рідку фазу розрив гетерополярного звязку між Na+ та Cl— унаслідок іоннодипольної взаємодії іонів Na+ та Cl— з полярними молекулами води
Розчинення гідратація поверхнево розташованих іонів — O H H + вільні гідратовані іони, які продифундували у рідку фазу розрив гетерополярного звязку між Na+ та Cl— унаслідок іоннодипольної взаємодії іонів Na+ та Cl— з полярними молекулами води
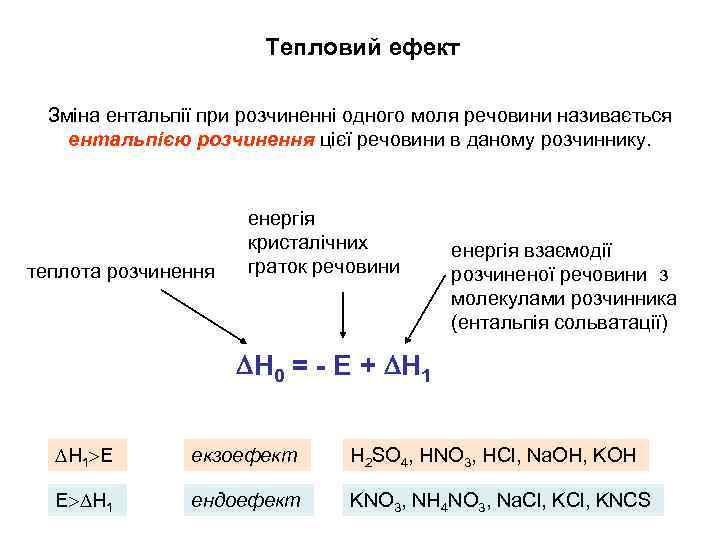 Тепловий ефект Зміна ентальпії при розчиненні одного моля речовини називається ентальпією розчинення цієї речовини в даному розчиннику. теплота розчинення енергія кристалічних граток речовини енергія взаємодії розчиненої речовини з молекулами розчинника (ентальпія сольватації) Н 0 = - Е + Н 1 Е екзоефект H 2 SO 4, HNO 3, HCl, Na. OH, KOH Е Н 1 ендоефект KNO 3, NH 4 NO 3, Na. Cl, KNCS
Тепловий ефект Зміна ентальпії при розчиненні одного моля речовини називається ентальпією розчинення цієї речовини в даному розчиннику. теплота розчинення енергія кристалічних граток речовини енергія взаємодії розчиненої речовини з молекулами розчинника (ентальпія сольватації) Н 0 = - Е + Н 1 Е екзоефект H 2 SO 4, HNO 3, HCl, Na. OH, KOH Е Н 1 ендоефект KNO 3, NH 4 NO 3, Na. Cl, KNCS
 Розчинність – кількість речовини, що здатна розчинитися (утворити однофазну дисперсну систему) в іншій речовині Насиченим розчином називається такий розчин, який знаходиться в рівновазі з твердою фазою розчиненої речовини і. містить максимально можливу за даних умов (Р, Т) кількість цієї речовини Ненасичені розчини – кількість розчиненої речовини менша за розчинність Пересичені розчини (термодинамічно нестійкі) – кількість розчиненої речовини більша за розчинність
Розчинність – кількість речовини, що здатна розчинитися (утворити однофазну дисперсну систему) в іншій речовині Насиченим розчином називається такий розчин, який знаходиться в рівновазі з твердою фазою розчиненої речовини і. містить максимально можливу за даних умов (Р, Т) кількість цієї речовини Ненасичені розчини – кількість розчиненої речовини менша за розчинність Пересичені розчини (термодинамічно нестійкі) – кількість розчиненої речовини більша за розчинність
 Розчинність газів Хімічна природа N 2 – 0. 02/V NH 3 > 700/V HCl > 400/V Утворення хімічної сполуки NH 3 + H 2 O = NH 4 OH Дисоціація на іони: Фізичні умови Залежність розчинності газу від тиску виражається законом ГенріДальтона: розчинність газу при постійній температурі в рідині прямо пропорційна його парціальному тиску. C = k·P, Залежність розчинності газів у рідинах визначається законом Клапейрона. Клазіуса
Розчинність газів Хімічна природа N 2 – 0. 02/V NH 3 > 700/V HCl > 400/V Утворення хімічної сполуки NH 3 + H 2 O = NH 4 OH Дисоціація на іони: Фізичні умови Залежність розчинності газу від тиску виражається законом ГенріДальтона: розчинність газу при постійній температурі в рідині прямо пропорційна його парціальному тиску. C = k·P, Залежність розчинності газів у рідинах визначається законом Клапейрона. Клазіуса
![Способи вираження концентрації розчинів Масова концентрація або масова частка розчиненої речовини [%, г/100 г] Способи вираження концентрації розчинів Масова концентрація або масова частка розчиненої речовини [%, г/100 г]](https://present5.com/presentation/-46204815_156756640/image-12.jpg) Способи вираження концентрації розчинів Масова концентрація або масова частка розчиненої речовини [%, г/100 г] Молярна концентрація (молярність) [моль·дм-3] Моляльна концентрація (моляльність) [моль·кг-1] Молярна концентрація еквівалентів (нормальна концентрація, нормальність) [моль-екв·дм-3] У відповідності із законом еквівалентів, розчини взаємодіють між собою в кількостях, пропорційних їх еквівалентам
Способи вираження концентрації розчинів Масова концентрація або масова частка розчиненої речовини [%, г/100 г] Молярна концентрація (молярність) [моль·дм-3] Моляльна концентрація (моляльність) [моль·кг-1] Молярна концентрація еквівалентів (нормальна концентрація, нормальність) [моль-екв·дм-3] У відповідності із законом еквівалентів, розчини взаємодіють між собою в кількостях, пропорційних їх еквівалентам
 Хімічний еквівалент - кількість грам-атомів хімічного елемента або грам-молекул хімічної сполуки, яка з'єднується з одним грам-атомом водню або може заміщувати один грам-атом водню у хімічній сполуці
Хімічний еквівалент - кількість грам-атомів хімічного елемента або грам-молекул хімічної сполуки, яка з'єднується з одним грам-атомом водню або може заміщувати один грам-атом водню у хімічній сполуці
 Задача Визначити молярну і нормальну концентрації розчину сульфатної кислоти, якщо 100 мл розчину містить 9, 8 г кислоти. 1. Визначимо кількість речовини кислоти, що міститься в 9, 8 г. 2. Визначимо молярну концентрацію. . 3. f(H 2 SO 4)=1/2, тобто z=2, то екв= 2 0, 1 = 0, 2 моль
Задача Визначити молярну і нормальну концентрації розчину сульфатної кислоти, якщо 100 мл розчину містить 9, 8 г кислоти. 1. Визначимо кількість речовини кислоти, що міститься в 9, 8 г. 2. Визначимо молярну концентрацію. . 3. f(H 2 SO 4)=1/2, тобто z=2, то екв= 2 0, 1 = 0, 2 моль

 Розділ хімії, який вивчає часові закономірності перебігу хімічних процесів, називається хімічною кінетикою. 2 Н 2(г) + О 2(г) = 2 Н 2 О(г) G = - 456, 4 к. Дж 700 0 С ( G 01000 = - 495, 3 к. Дж) Предметом хімічної кінетики є вивчення чинників, які впливають на швидкість хімічних реакцій (процесів)
Розділ хімії, який вивчає часові закономірності перебігу хімічних процесів, називається хімічною кінетикою. 2 Н 2(г) + О 2(г) = 2 Н 2 О(г) G = - 456, 4 к. Дж 700 0 С ( G 01000 = - 495, 3 к. Дж) Предметом хімічної кінетики є вивчення чинників, які впливають на швидкість хімічних реакцій (процесів)
 Фазою називають однорідну за хімічним складом та фізичними властивостями частину системи, відокремлену від інших частин поверхнею розділення Гомогенна система складається з однієї фази, гетерогенна — з кількох фаз Хімічні перетворення відбуваються в разі зіткнення молекул, якщо в результаті зіткнення перебудовуються хімічні зв’язки, тобто зв’язки у вихідних молекулах розриваються, а нові зв’язки утворюються. Швидкість хімічних реакцій характеризує інтенсивність хімічного процесу, тобто число елементарних актів взаємодії чи розкладу в одиницю часу в одиниці об’єму (для гомогенних дій) чи на одиницю поверхні поділу фаз (для гетерогенних реакцій).
Фазою називають однорідну за хімічним складом та фізичними властивостями частину системи, відокремлену від інших частин поверхнею розділення Гомогенна система складається з однієї фази, гетерогенна — з кількох фаз Хімічні перетворення відбуваються в разі зіткнення молекул, якщо в результаті зіткнення перебудовуються хімічні зв’язки, тобто зв’язки у вихідних молекулах розриваються, а нові зв’язки утворюються. Швидкість хімічних реакцій характеризує інтенсивність хімічного процесу, тобто число елементарних актів взаємодії чи розкладу в одиницю часу в одиниці об’єму (для гомогенних дій) чи на одиницю поверхні поділу фаз (для гетерогенних реакцій).
 Для гомогенних процесів, які здійснюються без зміни об’єму, швидкість хімічної реакції визначають як зміна концентрацій реагуючих речовин чи продуктів реакції за одиницю часу. Концентрація речовин у процесі реакції весь час змінюється, а це впливає на її швидкість, тому слід розглядати миттєву швидкість реакції, тобто швидкість у даний момент часу. Для гомогенних реакцій – це похідна концентрації за часом.
Для гомогенних процесів, які здійснюються без зміни об’єму, швидкість хімічної реакції визначають як зміна концентрацій реагуючих речовин чи продуктів реакції за одиницю часу. Концентрація речовин у процесі реакції весь час змінюється, а це впливає на її швидкість, тому слід розглядати миттєву швидкість реакції, тобто швидкість у даний момент часу. Для гомогенних реакцій – це похідна концентрації за часом.
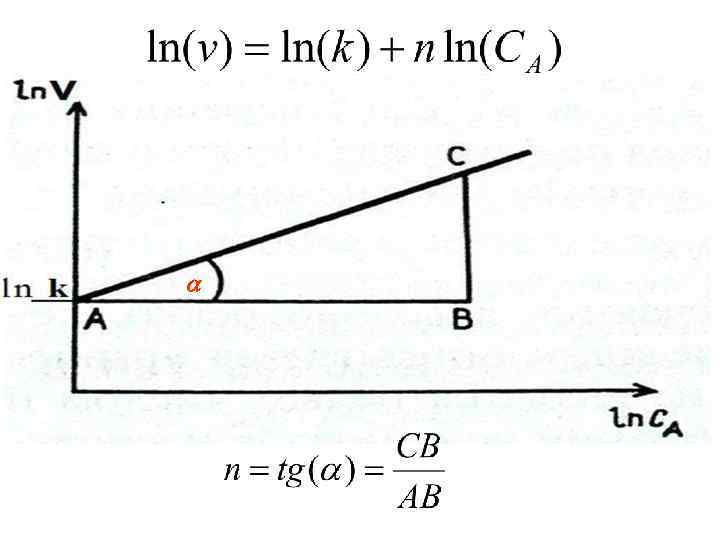
 v = tg
v = tg
 Швидкість хімічних реакцій залежить від - природи реагуючих речовин, - їх концентрацій, - температури, - наявності каталізатора і деяких інших зовнішніх факторів Необхідною умовою перебігу хімічної реакції поміж двома речовинами є зіткнення їх молекул. Швидкість хімічної реакції залежить від числа таких зіткнень в одиниці об’єму. Ймовірність зіткнення взаємодіючих молекул для гомогенної реакції пропорційна концентраціям реагуючих речовин
Швидкість хімічних реакцій залежить від - природи реагуючих речовин, - їх концентрацій, - температури, - наявності каталізатора і деяких інших зовнішніх факторів Необхідною умовою перебігу хімічної реакції поміж двома речовинами є зіткнення їх молекул. Швидкість хімічної реакції залежить від числа таких зіткнень в одиниці об’єму. Ймовірність зіткнення взаємодіючих молекул для гомогенної реакції пропорційна концентраціям реагуючих речовин
 Закон діючих мас Швидкість хімічної реакції пропорційна добутку концентрацій реагуючих речовин в ступенях, які дорівнюють коефіцієнтам, що стоять перед формулами речовин у відповідному рівнянні реакції. К. М. Гульдберг і П. Вааге, 1867
Закон діючих мас Швидкість хімічної реакції пропорційна добутку концентрацій реагуючих речовин в ступенях, які дорівнюють коефіцієнтам, що стоять перед формулами речовин у відповідному рівнянні реакції. К. М. Гульдберг і П. Вааге, 1867
![a. A + b. B = c. C + d. D v = k[A]a[B]b a. A + b. B = c. C + d. D v = k[A]a[B]b](https://present5.com/presentation/-46204815_156756640/image-22.jpg) a. A + b. B = c. C + d. D v = k[A]a[B]b Константа швидкості – це швидкість реакції за умови, що концентрації реагуючих речовин дорівнюють 1 моль·дм-3 Рівняння, що пов’язує швидкість реакції з концентраціями реагентів, називають рівнянням швидкості, або кінетичним рівнянням реакції
a. A + b. B = c. C + d. D v = k[A]a[B]b Константа швидкості – це швидкість реакції за умови, що концентрації реагуючих речовин дорівнюють 1 моль·дм-3 Рівняння, що пов’язує швидкість реакції з концентраціями реагентів, називають рівнянням швидкості, або кінетичним рівнянням реакції
 Багатостадійні реакції 2 HBr (г) = Н 2 (г) + Br 2 (г) 1) HBr +hv = H + Br v 1 = k 1[H]·[Br] 2) H + HBr = H 2 + Br v 2 = k 2[H 2]·[Br] 3) Br + Br = Br 2 v 3 = k 3 [Br 2]
Багатостадійні реакції 2 HBr (г) = Н 2 (г) + Br 2 (г) 1) HBr +hv = H + Br v 1 = k 1[H]·[Br] 2) H + HBr = H 2 + Br v 2 = k 2[H 2]·[Br] 3) Br + Br = Br 2 v 3 = k 3 [Br 2]
 Закон “горловини пляшки” принцип лімітуючої стадії: швидкість складної реакції визначається швидкістю найповільнішої (лімітуючої) елементарної стадії.
Закон “горловини пляшки” принцип лімітуючої стадії: швидкість складної реакції визначається швидкістю найповільнішої (лімітуючої) елементарної стадії.
 Порядок хімічної реакції Сума показників ступенів в рівнянні швидкості хімічної реакції (кінетичного рівняння) називається порядком хімічної реакції
Порядок хімічної реакції Сума показників ступенів в рівнянні швидкості хімічної реакції (кінетичного рівняння) називається порядком хімічної реакції
 Реакції нульового порядку швидкість не залежить від концентрації реагуючих речовин розмірність константи швидкості моль·дм -3·с-1 Ca. CO 3 Ca. O+CO 2
Реакції нульового порядку швидкість не залежить від концентрації реагуючих речовин розмірність константи швидкості моль·дм -3·с-1 Ca. CO 3 Ca. O+CO 2
 Реакції першого порядку швидкість прямо пропорційна концентрації реагуючих речовин
Реакції першого порядку швидкість прямо пропорційна концентрації реагуючих речовин
 Розмірність константи: N 2 O 5 = 2 NO 2 + 1/2 O 2.
Розмірність константи: N 2 O 5 = 2 NO 2 + 1/2 O 2.
 Реакції другого порядку Швидкість прямо пропорційна квадрату концентрації
Реакції другого порядку Швидкість прямо пропорційна квадрату концентрації
 Розмірність константи: H 2 + I 2 = 2 HI 2 NO 2 = 2 NO + O 2
Розмірність константи: H 2 + I 2 = 2 HI 2 NO 2 = 2 NO + O 2
 Молекулярність реакції Число молекул, які беруть участь в елементарному акті реакції, називають молекулярністю реакції Мономолекулярна: I 2 = 2 I; HBr = H + Br; N 2 O 5 = 2 NO 2 + 1/2 O 2 Бімолекулярна: H 2 + I 2 = 3 HI Тримолекулярна: 2 NO + O 2 = 2 NO 2
Молекулярність реакції Число молекул, які беруть участь в елементарному акті реакції, називають молекулярністю реакції Мономолекулярна: I 2 = 2 I; HBr = H + Br; N 2 O 5 = 2 NO 2 + 1/2 O 2 Бімолекулярна: H 2 + I 2 = 3 HI Тримолекулярна: 2 NO + O 2 = 2 NO 2


