химия 2015.pptx
- Количество слайдов: 29
 ОСНОВНІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК
ОСНОВНІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК
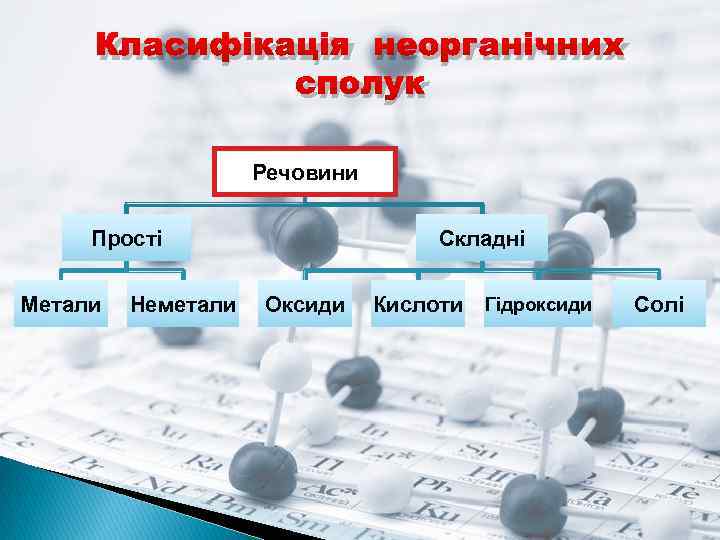 Класифікація неорганічних сполук Речовини Прості Метали Неметали Складні Оксиди Кислоти Гідроксиди Солі
Класифікація неорганічних сполук Речовини Прості Метали Неметали Складні Оксиди Кислоти Гідроксиди Солі
 Оксиди – це бінарні сполуки будь-якого хімічного елемeнта з Оксигеном. В оксидах Оксиген завжди двохвалентний Несолетвірні оксиди – це реакційно здатні сполуки, що вступають у хімічні реакції, в результаті яких солі не утворюються. Солетвірні – це такі оксиди, що вступають у реакції, в результаті яких утворюються солі.
Оксиди – це бінарні сполуки будь-якого хімічного елемeнта з Оксигеном. В оксидах Оксиген завжди двохвалентний Несолетвірні оксиди – це реакційно здатні сполуки, що вступають у хімічні реакції, в результаті яких солі не утворюються. Солетвірні – це такі оксиди, що вступають у реакції, в результаті яких утворюються солі.
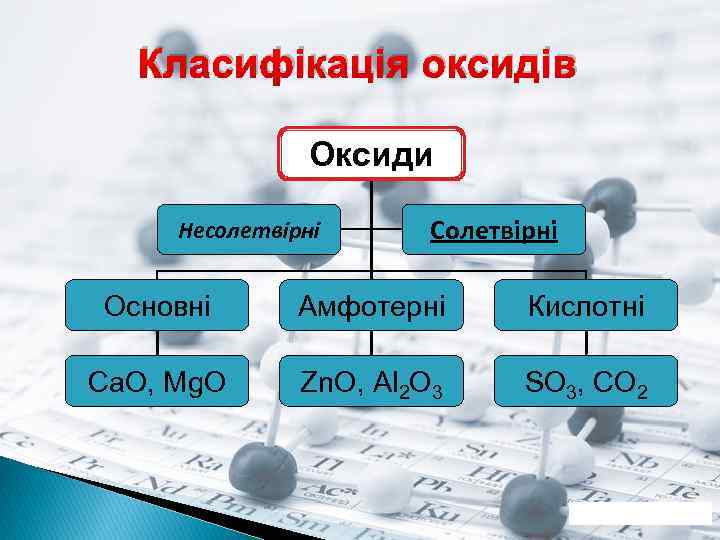 Класифікація оксидів Оксиди Несолетвірні Солетвірні Основні Амфотерні Кислотні Ca. O, Mg. O Zn. O, Al 2 O 3 SO 3, CO 2
Класифікація оксидів Оксиди Несолетвірні Солетвірні Основні Амфотерні Кислотні Ca. O, Mg. O Zn. O, Al 2 O 3 SO 3, CO 2
 Основними називаються оксиди, сполуки яких з водою є основами. Кислотними називають оксиди, сполуки яких з водою є кислотами. Амфотерними називають оксиди, яким відповідають амфотерні гідроксиди.
Основними називаються оксиди, сполуки яких з водою є основами. Кислотними називають оксиди, сполуки яких з водою є кислотами. Амфотерними називають оксиди, яким відповідають амфотерні гідроксиди.
 Фізичні властивості кислот • • Більшість оксидів, а саме оксиди елементівметалів, має немолекулярну будову і дуже високу температуру плавлення. Такі оксиди – тверді речовини. Деякі оксиди (оксиди елементів-неметалів) мають молекулярну будову і за стандартних умов перебувають в рідкому або газуватому стані.
Фізичні властивості кислот • • Більшість оксидів, а саме оксиди елементівметалів, має немолекулярну будову і дуже високу температуру плавлення. Такі оксиди – тверді речовини. Деякі оксиди (оксиди елементів-неметалів) мають молекулярну будову і за стандартних умов перебувають в рідкому або газуватому стані.
 Поширення оксидів у природі Al 2 O 3 Si. O 2
Поширення оксидів у природі Al 2 O 3 Si. O 2
 Хімічні властивості оксидів ОКСИДИ Мех. Оy; Ex. Oy + H 2 O = гідроксиди або кислоти відповідно + Мех. Оy або + Ex. Oy = солі; + амфотерні оксиди = солі; + кислоти або + гідроксиди = сіль + вода;
Хімічні властивості оксидів ОКСИДИ Мех. Оy; Ex. Oy + H 2 O = гідроксиди або кислоти відповідно + Мех. Оy або + Ex. Oy = солі; + амфотерні оксиди = солі; + кислоти або + гідроксиди = сіль + вода;
 Добування оксидів: 1. Безпосереднє сполучення простої речовини з киснем (за різних умов): С + О 2 = СО 2; 4 K + O 2 = 2 K 2 O. 2. Горіння складних речовин: CH 4 + 2 O 2 = CO 2 + 2 H 2 O. 3. Розкладання при нагріванні оксигеновмісних сполук: Ca. CO 3 = Ca. О + СО 2↑; 2 Сu(NO 3)2 = 2 Cu. O + 4 NO 2 ↑ + O 2 ↑; 2 Fe(OH)3 = Fe 2 O 3 + 3 H 2 O.
Добування оксидів: 1. Безпосереднє сполучення простої речовини з киснем (за різних умов): С + О 2 = СО 2; 4 K + O 2 = 2 K 2 O. 2. Горіння складних речовин: CH 4 + 2 O 2 = CO 2 + 2 H 2 O. 3. Розкладання при нагріванні оксигеновмісних сполук: Ca. CO 3 = Ca. О + СО 2↑; 2 Сu(NO 3)2 = 2 Cu. O + 4 NO 2 ↑ + O 2 ↑; 2 Fe(OH)3 = Fe 2 O 3 + 3 H 2 O.
 Кислоти • Кислоти — це складні речовини, що складаються з одного чи декількох атомів Гідрогену та кислотного залишку.
Кислоти • Кислоти — це складні речовини, що складаються з одного чи декількох атомів Гідрогену та кислотного залишку.
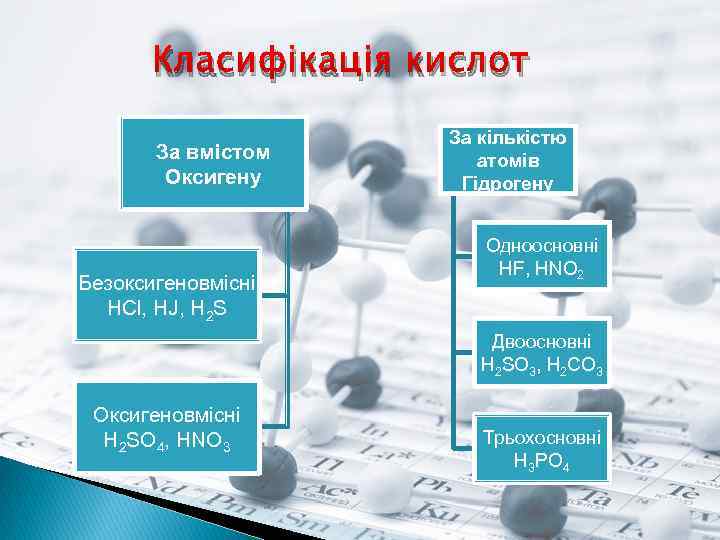 Класифікація кислот За вмістом Оксигену Безоксигеновмісні HCl, HJ, H 2 S За кількістю атомів Гідрогену Одноосновні HF, HNO 2 Двоосновні H 2 SO 3, H 2 CO 3 Оксигеновмісні H 2 SO 4, HNO 3 Трьохосновні H 3 PO 4
Класифікація кислот За вмістом Оксигену Безоксигеновмісні HCl, HJ, H 2 S За кількістю атомів Гідрогену Одноосновні HF, HNO 2 Двоосновні H 2 SO 3, H 2 CO 3 Оксигеновмісні H 2 SO 4, HNO 3 Трьохосновні H 3 PO 4
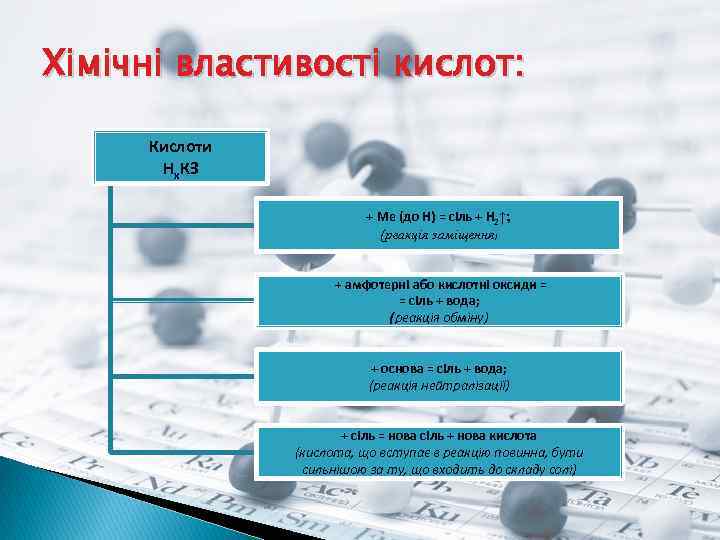 Хімічні властивості кислот: Кислоти Нx. КЗ + Ме (до Н) = сіль + Н 2↑; (реакція заміщення) + амфотерні або кислотні оксиди = = сіль + вода; (реакція обміну) + основа = сіль + вода; (реакція нейтралізації) + сіль = нова сіль + нова кислота (кислота, що вступає в реакцію повинна, бути сильнішою за ту, що входить до складу солі)
Хімічні властивості кислот: Кислоти Нx. КЗ + Ме (до Н) = сіль + Н 2↑; (реакція заміщення) + амфотерні або кислотні оксиди = = сіль + вода; (реакція обміну) + основа = сіль + вода; (реакція нейтралізації) + сіль = нова сіль + нова кислота (кислота, що вступає в реакцію повинна, бути сильнішою за ту, що входить до складу солі)
 Фізичні властивості кислот Деякі кислоти при звичайних умовах являють собою рідини, наприклад нітратна і сульфатна кислоти, а деякі — тверді речовини, як фосфатна кислота, боратна і ін. Більшість кислот добре розчиняється у воді, але деякі практично не розчиняються. Водні розчини кислот відзначаються кислим смаком, руйнують рослинні і тваринні тканини.
Фізичні властивості кислот Деякі кислоти при звичайних умовах являють собою рідини, наприклад нітратна і сульфатна кислоти, а деякі — тверді речовини, як фосфатна кислота, боратна і ін. Більшість кислот добре розчиняється у воді, але деякі практично не розчиняються. Водні розчини кислот відзначаються кислим смаком, руйнують рослинні і тваринні тканини.
 Сульфідна кислота H 2 S є у вулканічних газах і у водах мінеральних джерел. Ø Хлоридна кислота НСl входить до складу шлункового соку. Ø Карбонатна кислота Н 2 С 03 — до складу природних мінеральних вод (Боржомі, Нарзан, Миргородська). Ø Нітратна HN 03 і сульфітна H 2 S 03 кислоти трапляються в дощовій воді ( «кислотні дощі» ).
Сульфідна кислота H 2 S є у вулканічних газах і у водах мінеральних джерел. Ø Хлоридна кислота НСl входить до складу шлункового соку. Ø Карбонатна кислота Н 2 С 03 — до складу природних мінеральних вод (Боржомі, Нарзан, Миргородська). Ø Нітратна HN 03 і сульфітна H 2 S 03 кислоти трапляються в дощовій воді ( «кислотні дощі» ).
 Добування кислот: 1. При взаємодії кислотних оксидів з водою: SO 3 + H 2 O = H 2 SO 4; N 2 O 5 + H 2 O = 2 HNO 3. 2. Якщо оксиди не розчиняються у воді, то відповідні їм кислоти добувають непрямим способом, а саме дією іншої кислоти (найчастіше сульфатної) на відповідну сіль: Na 2 Si. O 3 + H 2 SO 4 = H 2 Si. O 3↓. 3. Безкисневмісні кислоти добувають синтезом з водню і неметалу з наступним розчиненням водневої сполуки у воді. Це HCl, HBr, HJ, H 2 S: H 2 + Cl 2 = 2 HCl
Добування кислот: 1. При взаємодії кислотних оксидів з водою: SO 3 + H 2 O = H 2 SO 4; N 2 O 5 + H 2 O = 2 HNO 3. 2. Якщо оксиди не розчиняються у воді, то відповідні їм кислоти добувають непрямим способом, а саме дією іншої кислоти (найчастіше сульфатної) на відповідну сіль: Na 2 Si. O 3 + H 2 SO 4 = H 2 Si. O 3↓. 3. Безкисневмісні кислоти добувають синтезом з водню і неметалу з наступним розчиненням водневої сполуки у воді. Це HCl, HBr, HJ, H 2 S: H 2 + Cl 2 = 2 HCl
 Гідроксиди – це складні речовини, утворені металічними елементами та гідроксильними групами Число гідроксильних груп у молекулі гідроксиду відповідає валентності металу і визначає кислотність основи: Na. OH – однокислотна основа; Ca(OH)2 – двокислотна основа. Валентність гідроксогрупи дорівнює І.
Гідроксиди – це складні речовини, утворені металічними елементами та гідроксильними групами Число гідроксильних груп у молекулі гідроксиду відповідає валентності металу і визначає кислотність основи: Na. OH – однокислотна основа; Ca(OH)2 – двокислотна основа. Валентність гідроксогрупи дорівнює І.
 Класифікація гідроксидів Гідроксиди Розчинні у воді Луги Na. OH, KOH Нерозчинні у воді Основи Cu(OH)2, Fe(OH)3
Класифікація гідроксидів Гідроксиди Розчинні у воді Луги Na. OH, KOH Нерозчинні у воді Основи Cu(OH)2, Fe(OH)3
 Хімічні властивості гідроксидів: Гідроксиди Ме(ОН)х + кислотні або амфотерні оксиди = = сіль + вода; + кислоти = сіль + вода; + амфотерні гідроксиди = сіль + вода; + солі = нова сіль + нова основа;
Хімічні властивості гідроксидів: Гідроксиди Ме(ОН)х + кислотні або амфотерні оксиди = = сіль + вода; + кислоти = сіль + вода; + амфотерні гідроксиди = сіль + вода; + солі = нова сіль + нова основа;
 Добування гідроксидів: 1. При взаємодії металів або їх оксидів з водою: 2 Na + 2 H 2 O = 2 Na. OH + H 2↑; Na 2 O + H 2 O = 2 Na. OH. 2. Нерозчинні у воді основи добувають непрямим способом, а саме: дією лугів на водні розчини відповідних солей: Fe. SO 4 + 2 Na. OH = Fe(OH)2↓ + Na 2 SO 4; Al. Cl 3 + 3 Na. OH = Al(OH)3↓ + 3 Na. Cl.
Добування гідроксидів: 1. При взаємодії металів або їх оксидів з водою: 2 Na + 2 H 2 O = 2 Na. OH + H 2↑; Na 2 O + H 2 O = 2 Na. OH. 2. Нерозчинні у воді основи добувають непрямим способом, а саме: дією лугів на водні розчини відповідних солей: Fe. SO 4 + 2 Na. OH = Fe(OH)2↓ + Na 2 SO 4; Al. Cl 3 + 3 Na. OH = Al(OH)3↓ + 3 Na. Cl.
 Індикатори речовини або тіла, за допомогою яких виявляють конкретну ознаку речовини, тіла або матеріалу Індикатор Кисле середовище Лужне середовище Нейтральне середовище Лакмус Червоний Синій Фіолетовий Фенолфталеїн Безбарвний Малиновий Безбарвний Метиловий оранжевий Червонорожевий Жовтий Помаранчевий
Індикатори речовини або тіла, за допомогою яких виявляють конкретну ознаку речовини, тіла або матеріалу Індикатор Кисле середовище Лужне середовище Нейтральне середовище Лакмус Червоний Синій Фіолетовий Фенолфталеїн Безбарвний Малиновий Безбарвний Метиловий оранжевий Червонорожевий Жовтий Помаранчевий
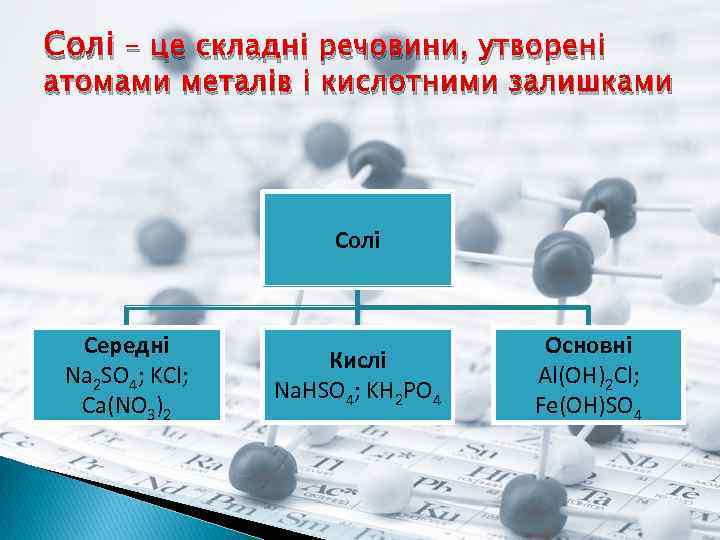 Cолі – це складні речовини, утворені атомами металів і кислотними залишками Солі Середні Na 2 SO 4; KCl; Ca(NO 3)2 Кислі Na. HSO 4; KH 2 PO 4 Основні Al(OH)2 Cl; Fe(OH)SO 4
Cолі – це складні речовини, утворені атомами металів і кислотними залишками Солі Середні Na 2 SO 4; KCl; Ca(NO 3)2 Кислі Na. HSO 4; KH 2 PO 4 Основні Al(OH)2 Cl; Fe(OH)SO 4
 Солі Середні – це продукти повного заміщення всіх атомів Гідрогену кислоти на атоми метелічного елемента (чи металоподібну групу). Кислі – це продукти заміщення лише частини атомів Гідрогену в молекулі кислоти на атоми металічного елемента. Основні – продукти заміщення лише частини гідроксогруп основ (амфотерних гідроксидів) на кислотні залишки.
Солі Середні – це продукти повного заміщення всіх атомів Гідрогену кислоти на атоми метелічного елемента (чи металоподібну групу). Кислі – це продукти заміщення лише частини атомів Гідрогену в молекулі кислоти на атоми металічного елемента. Основні – продукти заміщення лише частини гідроксогруп основ (амфотерних гідроксидів) на кислотні залишки.
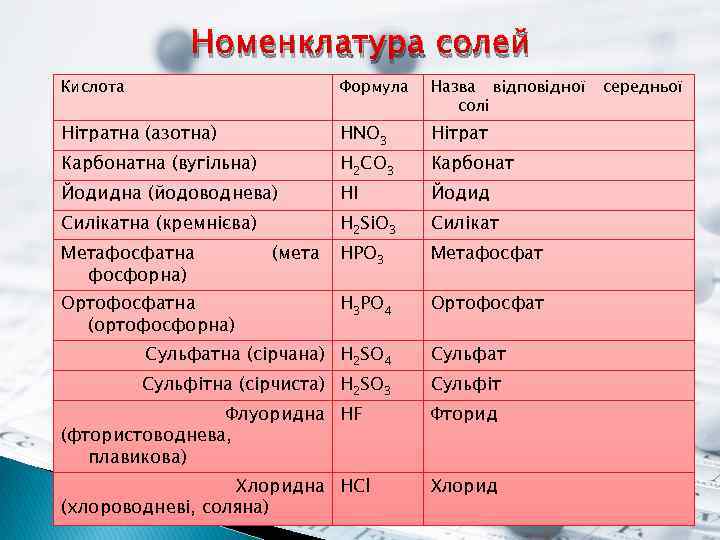 Номенклатура солей Кислота Формула Назва відповідної солі Нітратна (азотна) HNO 3 Нітрат Карбонатна (вугільна) Йодидна (йодоводнева) Силікатна (кремнієва) Метафосфатна фосфорна) Ортофосфатна (ортофосфорна) (мета H 2 CO 3 Карбонат HI Йодид H 2 Si. O 3 Силікат HPO 3 Метафосфат H 3 PO 4 Ортофосфат Сульфатна (сірчана) H 2 SO 4 Сульфітна (сірчиста) H 2 SO 3 Сульфат Сульфіт Флуоридна HF (фтористоводнева, плавикова) Фторид Хлоридна HCl (хлороводневі, соляна) Хлорид середньої
Номенклатура солей Кислота Формула Назва відповідної солі Нітратна (азотна) HNO 3 Нітрат Карбонатна (вугільна) Йодидна (йодоводнева) Силікатна (кремнієва) Метафосфатна фосфорна) Ортофосфатна (ортофосфорна) (мета H 2 CO 3 Карбонат HI Йодид H 2 Si. O 3 Силікат HPO 3 Метафосфат H 3 PO 4 Ортофосфат Сульфатна (сірчана) H 2 SO 4 Сульфітна (сірчиста) H 2 SO 3 Сульфат Сульфіт Флуоридна HF (фтористоводнева, плавикова) Фторид Хлоридна HCl (хлороводневі, соляна) Хлорид середньої
 Назви солей Fe(NO 3)3 – ферум(ІІІ) нітрат; Na 2 SO 4 – натрій сульфат; KHCO 3 – калій гідрогенкарбонат; Na. H 2 PO 4 – натрій дигідрогенортофосфат; Mg(OH)NO 3 – магній гідроксонітрат; Al(OH)2 Cl – алюміній дигідроксохлорид.
Назви солей Fe(NO 3)3 – ферум(ІІІ) нітрат; Na 2 SO 4 – натрій сульфат; KHCO 3 – калій гідрогенкарбонат; Na. H 2 PO 4 – натрій дигідрогенортофосфат; Mg(OH)NO 3 – магній гідроксонітрат; Al(OH)2 Cl – алюміній дигідроксохлорид.
 Хімічні властивості солей: + Ме = нова сіль + новий Ме; (реакція заміщення) + кислота = нова сіль + нова кислота; Солі + основа = нова сіль + нова основа; + сіль = нова сіль + нова сіль; (один із продуктів випадає в осад!)
Хімічні властивості солей: + Ме = нова сіль + новий Ме; (реакція заміщення) + кислота = нова сіль + нова кислота; Солі + основа = нова сіль + нова основа; + сіль = нова сіль + нова сіль; (один із продуктів випадає в осад!)
 Добування солей 1. Взаємодією кислот з основами (реакція нейтралізації) або амфотерними гідроксидами: Ca(OH)2 + 2 HNO 3 = Ca(NO 3)2 + 2 H 2 O; Zn(OH)2 + 2 HCl = Zn. Cl 2 + 2 H 2 O. 2. Взаємодією кислот з основними або амфотерними оксидами: Mg. O + H 2 SO 4 = Mg. SO 4 + H 2 O; Zn. O + 2 HNO 3 = Zn(NO 3)2 + H 2 O. 3. Взаємодія кислот з металами: Zn + H 2 SO 4 = Zn. SO 4 + H 2↑. 4. Взаємодією кислот з іншими солями: H 2 SO 4 + Ba. Cl 2 = Ba. SO 4 + 2 HCl.
Добування солей 1. Взаємодією кислот з основами (реакція нейтралізації) або амфотерними гідроксидами: Ca(OH)2 + 2 HNO 3 = Ca(NO 3)2 + 2 H 2 O; Zn(OH)2 + 2 HCl = Zn. Cl 2 + 2 H 2 O. 2. Взаємодією кислот з основними або амфотерними оксидами: Mg. O + H 2 SO 4 = Mg. SO 4 + H 2 O; Zn. O + 2 HNO 3 = Zn(NO 3)2 + H 2 O. 3. Взаємодія кислот з металами: Zn + H 2 SO 4 = Zn. SO 4 + H 2↑. 4. Взаємодією кислот з іншими солями: H 2 SO 4 + Ba. Cl 2 = Ba. SO 4 + 2 HCl.
 Генетичний зв’язок це зв’язок між речовинами різних класів, що ґрунтується на взаємоперетворенні речовин і показує походження одних речовин від інших. У перекладі з гр. генетичний означає – такий, що стосується походження, вивчає розвиток чого-небудь.
Генетичний зв’язок це зв’язок між речовинами різних класів, що ґрунтується на взаємоперетворенні речовин і показує походження одних речовин від інших. У перекладі з гр. генетичний означає – такий, що стосується походження, вивчає розвиток чого-небудь.
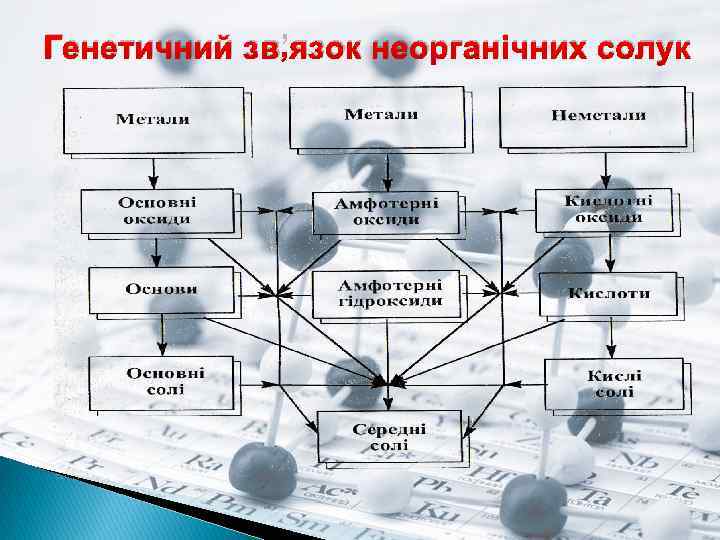 Генетичний зв’язок неорганічних солук
Генетичний зв’язок неорганічних солук
 Дякую за увагу!
Дякую за увагу!


