Лекция_3 тела.ppt
- Количество слайдов: 43
 Основная литература для подготовки : 1. Шур А. М. Высокомолекулярные соединения: Учеб. 3 -е изд. М. : Высш. шк. 1981 /в т. ч. е-вариант в формате *djvu/ 2. Семчиков Ю. Д. Высокомолекулярные соединения – М. : Академия, 2010. – 368 с. 3. Киреев В. В. Высокомолекулярные соединения: Учеб. М. : Высш. шк. 1992 4. Филимошкин А. Г. /*pdf /МАКРОМОЛЕКУЛА. ОСНОВЫ ФИЗИКИ ПОЛИМЕРНОГО ТЕЛА И ФИЗИЧЕСКОЙ ХИМИИ РАСТВОРОВ ПОЛИМЕРОВ Учебное пособие для студентов хф. 2011 Лекция 3 1
Основная литература для подготовки : 1. Шур А. М. Высокомолекулярные соединения: Учеб. 3 -е изд. М. : Высш. шк. 1981 /в т. ч. е-вариант в формате *djvu/ 2. Семчиков Ю. Д. Высокомолекулярные соединения – М. : Академия, 2010. – 368 с. 3. Киреев В. В. Высокомолекулярные соединения: Учеб. М. : Высш. шк. 1992 4. Филимошкин А. Г. /*pdf /МАКРОМОЛЕКУЛА. ОСНОВЫ ФИЗИКИ ПОЛИМЕРНОГО ТЕЛА И ФИЗИЧЕСКОЙ ХИМИИ РАСТВОРОВ ПОЛИМЕРОВ Учебное пособие для студентов хф. 2011 Лекция 3 1
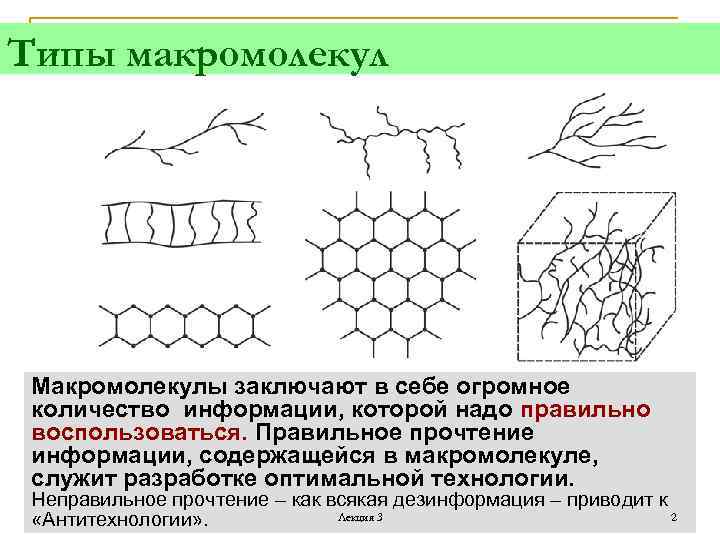 Типы макромолекул Макромолекулы заключают в себе огромное количество информации, которой надо правильно воспользоваться. Правильное прочтение информации, содержащейся в макромолекуле, служит разработке оптимальной технологии. Неправильное прочтение – как всякая дезинформация – приводит к 2 Лекция 3 «Антитехнологии» .
Типы макромолекул Макромолекулы заключают в себе огромное количество информации, которой надо правильно воспользоваться. Правильное прочтение информации, содержащейся в макромолекуле, служит разработке оптимальной технологии. Неправильное прочтение – как всякая дезинформация – приводит к 2 Лекция 3 «Антитехнологии» .
 Классификация, номенклатура и названия Макромолекула получает название путем подстановки префикса поли- к названию мономера, e. g. полиэтилен. Так сформировалась большая группа винильных полимеров как представителей гомологического ряда этана: например, полиолефины, если R–алкильные заместители, так и различных производных, содержащих функциональные группы Hal, OH, COOH, OCOR, CN, CONH 2 и т. д. Источники для подготовки по номенклатуре: Семчиков Ю. Д. , С. 19 – 34, Филимошкин А. Г. С. 81 – 96. Лекция 3 3
Классификация, номенклатура и названия Макромолекула получает название путем подстановки префикса поли- к названию мономера, e. g. полиэтилен. Так сформировалась большая группа винильных полимеров как представителей гомологического ряда этана: например, полиолефины, если R–алкильные заместители, так и различных производных, содержащих функциональные группы Hal, OH, COOH, OCOR, CN, CONH 2 и т. д. Источники для подготовки по номенклатуре: Семчиков Ю. Д. , С. 19 – 34, Филимошкин А. Г. С. 81 – 96. Лекция 3 3
 Названия винильных полимеров получены в большинстве свое от тривиальных или рациональных названий исходных мономеров с префиксом поли-, например: полиакриловая кислота –[CH 2 -CHCOOH]n–, полиакрилонитрил –[CH 2 -CHCN]n–, поливиниловый спирт –[CH 2 -CHOH]n– и т. д. Все полимеры идентифицируются в соответствии с номенклатурой и классификацией органической химии – галоидпроизводные, спирты, карбоновые кислоты и их производные (сложные и простые эфиры, нитрилы, амиды), амины и их соли и т. д. Лекция 3 4
Названия винильных полимеров получены в большинстве свое от тривиальных или рациональных названий исходных мономеров с префиксом поли-, например: полиакриловая кислота –[CH 2 -CHCOOH]n–, полиакрилонитрил –[CH 2 -CHCN]n–, поливиниловый спирт –[CH 2 -CHOH]n– и т. д. Все полимеры идентифицируются в соответствии с номенклатурой и классификацией органической химии – галоидпроизводные, спирты, карбоновые кислоты и их производные (сложные и простые эфиры, нитрилы, амиды), амины и их соли и т. д. Лекция 3 4
 РАСТВОРЫ ПОЛИМЕРОВ = h 2 1/2/ h 2 1/2 Лекция 3 5
РАСТВОРЫ ПОЛИМЕРОВ = h 2 1/2/ h 2 1/2 Лекция 3 5
 h Макромолекула располагается в трехмерном пространстве и ограничена воображаемой координационной сферой – пунктир. Ее форма определяет все свойства ж. и тв. полимерных тел! Лекция 3 6
h Макромолекула располагается в трехмерном пространстве и ограничена воображаемой координационной сферой – пунктир. Ее форма определяет все свойства ж. и тв. полимерных тел! Лекция 3 6
 а) б) в) Схематическое изображение свернутой макромолекулы (а), произвольно выбранного сегмента ее цепи (б) и проекции на плоскость макромолекулы, состоящей из 25 сегментов (в). Макромолекула располагается в трехмерном пространстве и ограничена воображаемой координационной сферой - пунктир (а). Движение «несвободной» броуновской частицы (в). Лекция 3 7
а) б) в) Схематическое изображение свернутой макромолекулы (а), произвольно выбранного сегмента ее цепи (б) и проекции на плоскость макромолекулы, состоящей из 25 сегментов (в). Макромолекула располагается в трехмерном пространстве и ограничена воображаемой координационной сферой - пунктир (а). Движение «несвободной» броуновской частицы (в). Лекция 3 7
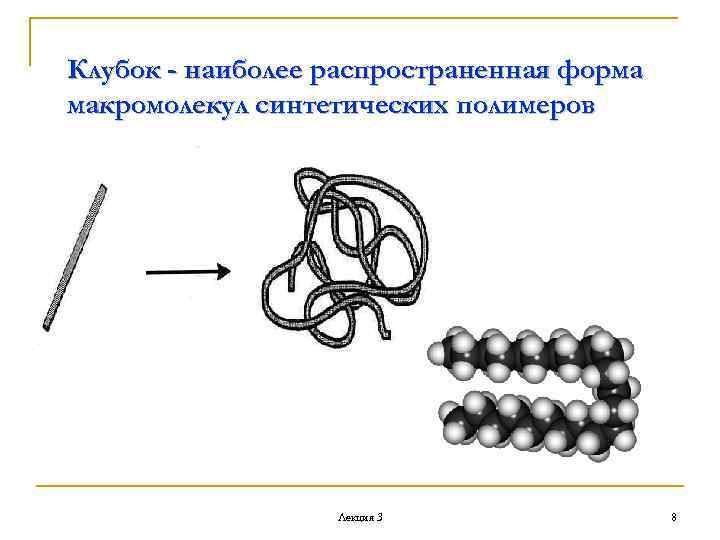 Клубок - наиболее распространенная форма макромолекул синтетических полимеров Лекция 3 8
Клубок - наиболее распространенная форма макромолекул синтетических полимеров Лекция 3 8
 Изолированный макромолекулярный клубок напоминает газовое микрооблако Сталь 2× 1011 Медь 1× 1011 Кварц 1× 1011 Каучук Газ идеальный 5× 105 1× 105 Е (Па) Прядение из расплава Слева в круге изображены молекулы газа, а справа – сегменты макромолекул, соединенные химическими связями. Модели деформированного клубка: а – при растяжении, б – при сжатии Лекция 3 9
Изолированный макромолекулярный клубок напоминает газовое микрооблако Сталь 2× 1011 Медь 1× 1011 Кварц 1× 1011 Каучук Газ идеальный 5× 105 1× 105 Е (Па) Прядение из расплава Слева в круге изображены молекулы газа, а справа – сегменты макромолекул, соединенные химическими связями. Модели деформированного клубка: а – при растяжении, б – при сжатии Лекция 3 9
 Растворы полимеров являются истинными и термодинамически устойчивыми системами. Им присуща обратимость. Правило фаз Гиббса для растворов полимеров С – число степеней свободы; К – число компонентов в системе; Ф – число фаз ? ? ? МИ НО: КИ КА они обладают специфическими свойствами, значительно отличающими их от свойств низкомолекулярных растворов. Лекция 3 10
Растворы полимеров являются истинными и термодинамически устойчивыми системами. Им присуща обратимость. Правило фаз Гиббса для растворов полимеров С – число степеней свободы; К – число компонентов в системе; Ф – число фаз ? ? ? МИ НО: КИ КА они обладают специфическими свойствами, значительно отличающими их от свойств низкомолекулярных растворов. Лекция 3 10
 1. Условные стадии растворения полимеров Набухание полимера характеризуется величиной q - степень набухания Кинетика набухания: быстро набухающий (1), медленно набухающий (2) образцы с ограниченным набуханием; (3) – неограниченно набухающий полимер. q=(m-m 0)/m 0 или q= (VV 0)/V 0, где m 0, V 0 – масса и объем исходного, а m, V – масса и объем набухшего образца полимера. Лекция 3 11
1. Условные стадии растворения полимеров Набухание полимера характеризуется величиной q - степень набухания Кинетика набухания: быстро набухающий (1), медленно набухающий (2) образцы с ограниченным набуханием; (3) – неограниченно набухающий полимер. q=(m-m 0)/m 0 или q= (VV 0)/V 0, где m 0, V 0 – масса и объем исходного, а m, V – масса и объем набухшего образца полимера. Лекция 3 11
 Схематическое изображение чередующихся надмолекулярных структур и рыхлых областей в аморфном полимерном теле (слева). Справа показана диффузия молекул растворителя S в межмакромолекулярное пространство внутри тела Лекция 3 12
Схематическое изображение чередующихся надмолекулярных структур и рыхлых областей в аморфном полимерном теле (слева). Справа показана диффузия молекул растворителя S в межмакромолекулярное пространство внутри тела Лекция 3 12
 n Макромолекулярные клубки в разбавленном растворе (стадия VI) пропитаны иммобилизованным растворителем таким образом, что каждое мономерное звено цепи окружено десятками и даже сотнями молекул растворителя, сравнимых по размерам с повторяющимся звеном. Поэтому макромолекула находится в развернутом состоянии. Лекция 3 13
n Макромолекулярные клубки в разбавленном растворе (стадия VI) пропитаны иммобилизованным растворителем таким образом, что каждое мономерное звено цепи окружено десятками и даже сотнями молекул растворителя, сравнимых по размерам с повторяющимся звеном. Поэтому макромолекула находится в развернутом состоянии. Лекция 3 13
 Координационная сфера это занятая постоянно дышащей макромолекулой сфера, которую удалось бы зафиксировать в воображаемом опыте в течение некоторого времени. Желтым цветом отмечены ММВ, зеленым – ВМВ. На рисунке координационная сфера каждой из 3 -х макромолекул обозначена пунктиром. Лекция 3 14
Координационная сфера это занятая постоянно дышащей макромолекулой сфера, которую удалось бы зафиксировать в воображаемом опыте в течение некоторого времени. Желтым цветом отмечены ММВ, зеленым – ВМВ. На рисунке координационная сфера каждой из 3 -х макромолекул обозначена пунктиром. Лекция 3 14
 2. Фазовые диаграммы растворов полимеров с верхней (ВКТС) и нижней (НКТС) критическими температурами смешения (растворения) Диаграммы состояния различных Ф + С = К + 1, систем полимер – растворитель: где Ф – число фаз, К – число а – наличие области полного компонентов, С – число степеней смешения; б – отсутствие области свободы. полного смешения; в – система полиэтилен оксид – вода Лекция 3 15
2. Фазовые диаграммы растворов полимеров с верхней (ВКТС) и нижней (НКТС) критическими температурами смешения (растворения) Диаграммы состояния различных Ф + С = К + 1, систем полимер – растворитель: где Ф – число фаз, К – число а – наличие области полного компонентов, С – число степеней смешения; б – отсутствие области свободы. полного смешения; в – система полиэтилен оксид – вода Лекция 3 15
 3. Реология полимеров. Кривые течения растворов и расплавов полимеров. Механизм течения полимеров Реология (от греческого слова – течь) изучает деформационные свойства полимерных материалов – от стеклообразных полимеров до разбавленных растворов. Основная задача - определение зависимостей между напряжениями, деформациями и их изменениями во времени (релаксационные процессы). n Реологическими уравнениями являются закон Гука и закон Ньютона = и = , – растягивающее одноосное напряжение; – относительная деформация; - модуль упругости (модуль Юнга); – касательное напряжение; – скорость деформации и – вязкость. Все полимерные материалы обладают как упругими, так и вязкими свойствами. n Лекция 3 16
3. Реология полимеров. Кривые течения растворов и расплавов полимеров. Механизм течения полимеров Реология (от греческого слова – течь) изучает деформационные свойства полимерных материалов – от стеклообразных полимеров до разбавленных растворов. Основная задача - определение зависимостей между напряжениями, деформациями и их изменениями во времени (релаксационные процессы). n Реологическими уравнениями являются закон Гука и закон Ньютона = и = , – растягивающее одноосное напряжение; – относительная деформация; - модуль упругости (модуль Юнга); – касательное напряжение; – скорость деформации и – вязкость. Все полимерные материалы обладают как упругими, так и вязкими свойствами. n Лекция 3 16
 Кривые течения. Функцию d /d (с-1) обозначают ˙ (с-1), а – (Н/м 2): = ˙ , = ˙ n, скорость сдвига в степени n, где – вязкость Н·с/см 2 (Па·с). Прологарифмируем оба уравнения: ln = ln + ln˙ , ln = ln + n ln˙ (степенной закон течения). Оба уравнения прямой с разными тангенсами наклона (n = 1 для ньютоновской жидкости). Показатель степени n называется индексом течения. Зависимость 1 - (ньютоновская жидкость). Прямая 2(неньютоновская жидкость) Лекция 3 17
Кривые течения. Функцию d /d (с-1) обозначают ˙ (с-1), а – (Н/м 2): = ˙ , = ˙ n, скорость сдвига в степени n, где – вязкость Н·с/см 2 (Па·с). Прологарифмируем оба уравнения: ln = ln + ln˙ , ln = ln + n ln˙ (степенной закон течения). Оба уравнения прямой с разными тангенсами наклона (n = 1 для ньютоновской жидкости). Показатель степени n называется индексом течения. Зависимость 1 - (ньютоновская жидкость). Прямая 2(неньютоновская жидкость) Лекция 3 17
 4. Гидродинамические свойства макромолекул в разбавленных растворах Вискозиметр Уббелоде с висящим уровнем. Поток жидкости в капилляре вискозиметра Уравнение Пуазейля: (Па с)= ( r 4Δp) 8 l. Q, Δp – разность давлений на концах капилляра, r – радиус, l –длина, Q – объем жидкости протекающей за единицу времени. Лекция 3 18
4. Гидродинамические свойства макромолекул в разбавленных растворах Вискозиметр Уббелоде с висящим уровнем. Поток жидкости в капилляре вискозиметра Уравнение Пуазейля: (Па с)= ( r 4Δp) 8 l. Q, Δp – разность давлений на концах капилляра, r – радиус, l –длина, Q – объем жидкости протекающей за единицу времени. Лекция 3 18
 Вязкость растворов полимеров Вязкость (внутреннее трение) – свойство жидких, а также газообразных и твердых тел оказывать сопротивление их течению, т. е. перемещению одного слоя относительно другого под действием внешних сил, таких как гравитационные, например, в вискозиметре. Лекция 3 19
Вязкость растворов полимеров Вязкость (внутреннее трение) – свойство жидких, а также газообразных и твердых тел оказывать сопротивление их течению, т. е. перемещению одного слоя относительно другого под действием внешних сил, таких как гравитационные, например, в вискозиметре. Лекция 3 19
 Внутреннее трение при течении раствора: Лекция 3 20
Внутреннее трение при течении раствора: Лекция 3 20
 В гидродинамике растворов полимеров используют чаще относительные вязкости уд =( - о)/ о уд /с lim ( уд /с) = [ ] с 0 уд /с=[ ] + k [ ]с2 +…. Уравнение Хаггинса Лекция 3 21
В гидродинамике растворов полимеров используют чаще относительные вязкости уд =( - о)/ о уд /с lim ( уд /с) = [ ] с 0 уд /с=[ ] + k [ ]с2 +…. Уравнение Хаггинса Лекция 3 21
 Вязкость растворов полимеров как структурно чувствительное свойство Связь со среднеквадратичным расстоянием между концами цепи уд =( - о)/ о уд /с lim ( уд /с) = [ ] с 0 Уравнение Хаггинса уд /с=[ ] + k [ ]с2 +…. где Ф = 2, 84· 1023 моль-1 – постоянная Флори; М – моляр. масса: [η] – характеристич. вязкость Лекция 3 22
Вязкость растворов полимеров как структурно чувствительное свойство Связь со среднеквадратичным расстоянием между концами цепи уд =( - о)/ о уд /с lim ( уд /с) = [ ] с 0 Уравнение Хаггинса уд /с=[ ] + k [ ]с2 +…. где Ф = 2, 84· 1023 моль-1 – постоянная Флори; М – моляр. масса: [η] – характеристич. вязкость Лекция 3 22
![Уравнение Марка – Куна – Хаувинка [ ]=К Мa [η] = К·Mа Графическое определение Уравнение Марка – Куна – Хаувинка [ ]=К Мa [η] = К·Mа Графическое определение](https://present5.com/presentation/20665849_32164008/image-23.jpg) Уравнение Марка – Куна – Хаувинка [ ]=К Мa [η] = К·Mа Графическое определение характеристической вязкости [η] = lim (ηуд/с) с→ 0 К и α – константы уравнения, индивидуальные для каждой конкретной пары полимер-растворитель. Величина α характеризует степень свёрнутости клубка, а К зависит от температуры раствора (в справочниках) Чем в более развернутой конформации находятся клубки, тем бóльшей вязкостью обладают их растворы Лекция 3 23
Уравнение Марка – Куна – Хаувинка [ ]=К Мa [η] = К·Mа Графическое определение характеристической вязкости [η] = lim (ηуд/с) с→ 0 К и α – константы уравнения, индивидуальные для каждой конкретной пары полимер-растворитель. Величина α характеризует степень свёрнутости клубка, а К зависит от температуры раствора (в справочниках) Чем в более развернутой конформации находятся клубки, тем бóльшей вязкостью обладают их растворы Лекция 3 23
![Оценка формы и размеров макромолекулы Уравнение Хаггинса уд /с=[ ] + k [ ]с2 Оценка формы и размеров макромолекулы Уравнение Хаггинса уд /с=[ ] + k [ ]с2](https://present5.com/presentation/20665849_32164008/image-24.jpg) Оценка формы и размеров макромолекулы Уравнение Хаггинса уд /с=[ ] + k [ ]с2 +…. Формула Марка-Куна-Хаувинка [ ]=К Мa a=0 – компактная сфера, не встречается при растворении макромолекул; a=0. 5 – гауссов клубок в -условиях; a=0. 6 -0. 8 – гибкие макромолекулы в хорошем растворителе; a=1. 0 -1. 5 – протекаемые клубки и жесткие макромолекулы. Формула Флори-Фокса [ ] M= h 2 3/2 где – универсальная постоянная (коэффициент Флори), равная 2. 84 · 1021 моль-1 (2. 84 · 1023 моль-1) для гауссовых цепей. Лекция 3 24
Оценка формы и размеров макромолекулы Уравнение Хаггинса уд /с=[ ] + k [ ]с2 +…. Формула Марка-Куна-Хаувинка [ ]=К Мa a=0 – компактная сфера, не встречается при растворении макромолекул; a=0. 5 – гауссов клубок в -условиях; a=0. 6 -0. 8 – гибкие макромолекулы в хорошем растворителе; a=1. 0 -1. 5 – протекаемые клубки и жесткие макромолекулы. Формула Флори-Фокса [ ] M= h 2 3/2 где – универсальная постоянная (коэффициент Флори), равная 2. 84 · 1021 моль-1 (2. 84 · 1023 моль-1) для гауссовых цепей. Лекция 3 24
 Макромолекулы в разбавленных растворах h ИНФОРМАЦИЮ h об индивидуальных изолированных макромолекулах получают при изучении разбавленных растворов полимеров при их течении. Это - сведения о конформациях и конфигурациях, размерах и форме макромолекул, молекулярных массах и ММР, о химической микроструктуре, о типе и силе взаимодействий с молекулами растворителей и др. Увеличение размеров макромолекулярных клубков описывают коэффициентом набухания посредством гидродинамического радиуса R или среднеквадратичного расстояния h =( R 2/ R 2 )1/2 = h 2 1/2/ h 2 1/2 Лекция 3 25
Макромолекулы в разбавленных растворах h ИНФОРМАЦИЮ h об индивидуальных изолированных макромолекулах получают при изучении разбавленных растворов полимеров при их течении. Это - сведения о конформациях и конфигурациях, размерах и форме макромолекул, молекулярных массах и ММР, о химической микроструктуре, о типе и силе взаимодействий с молекулами растворителей и др. Увеличение размеров макромолекулярных клубков описывают коэффициентом набухания посредством гидродинамического радиуса R или среднеквадратичного расстояния h =( R 2/ R 2 )1/2 = h 2 1/2/ h 2 1/2 Лекция 3 25
 5. Исключенный объем Двумерное изображение эффекта исключенного объема для цепей, расположенных в квадратной решетке. Всего 16 цепей, каждая из которых состоит из 6 сегментов с фиксированным положением первых двух сегментов и прямым углом между последовательными сегментами. Лекция 3 26
5. Исключенный объем Двумерное изображение эффекта исключенного объема для цепей, расположенных в квадратной решетке. Всего 16 цепей, каждая из которых состоит из 6 сегментов с фиксированным положением первых двух сегментов и прямым углом между последовательными сегментами. Лекция 3 26
 Исключенный объем и размеры = h 2 1/2/ h 2 1/2 Исключенный объем – тот объем, из Типичная форма макромолекулы и той же макромолекулы-клубка с исключенным объемом Глобула в правом нижнем углу. которого данная макромолекула вытесняет все остальные. Исключенный объем является следствием фактического отталкивания макромолекул друг от друга, в результате дальних взаимодействий. Каждая макромолекула в очень разбавленном растворе в хорошем растворителе стремится исключить из объема, который она занимает все другие макромолекулы за счет работы сил отталкивания. Понятие исключенного объема можно связать с понятием набухания , который количественно связан с R и h =(R 2/R 2 )1/2 и = h 2 1/2/ h 2 1/2 Лекция 3 27
Исключенный объем и размеры = h 2 1/2/ h 2 1/2 Исключенный объем – тот объем, из Типичная форма макромолекулы и той же макромолекулы-клубка с исключенным объемом Глобула в правом нижнем углу. которого данная макромолекула вытесняет все остальные. Исключенный объем является следствием фактического отталкивания макромолекул друг от друга, в результате дальних взаимодействий. Каждая макромолекула в очень разбавленном растворе в хорошем растворителе стремится исключить из объема, который она занимает все другие макромолекулы за счет работы сил отталкивания. Понятие исключенного объема можно связать с понятием набухания , который количественно связан с R и h =(R 2/R 2 )1/2 и = h 2 1/2/ h 2 1/2 Лекция 3 27
 6. Полиэлектролиты Макромолекулы, содержащие в своей структуре способные к диссоциации ионогенные группы, называются полиэлектролитами. Это - кислоты и основания (сильные и слабые), а также самые разные соли Полиамфолиты содержат одновременно кислотные и основные группы. Типичными полиамфолитами являются белки Лекция 3 28
6. Полиэлектролиты Макромолекулы, содержащие в своей структуре способные к диссоциации ионогенные группы, называются полиэлектролитами. Это - кислоты и основания (сильные и слабые), а также самые разные соли Полиамфолиты содержат одновременно кислотные и основные группы. Типичными полиамфолитами являются белки Лекция 3 28
 Поликислоты и полиоснования Полиакриловая и полиметакриловая кислоты Поливиниламин Лекция 3 29
Поликислоты и полиоснования Полиакриловая и полиметакриловая кислоты Поливиниламин Лекция 3 29
 II I Влияние р. Н среды на форму макромолекул (например, сополимера акриламида и акрилата натрия) Лекция 3 30
II I Влияние р. Н среды на форму макромолекул (например, сополимера акриламида и акрилата натрия) Лекция 3 30
 7. Зависимость приведенной вязкости полиметакриловой кислоты от ее степени диссоциации Лекция 3 31
7. Зависимость приведенной вязкости полиметакриловой кислоты от ее степени диссоциации Лекция 3 31
![8. Концентрированные растворы полимеров Полимерные растворы в зависимости от величины произведения [η]·с относят к 8. Концентрированные растворы полимеров Полимерные растворы в зависимости от величины произведения [η]·с относят к](https://present5.com/presentation/20665849_32164008/image-32.jpg) 8. Концентрированные растворы полимеров Полимерные растворы в зависимости от величины произведения [η]·с относят к а) разбавленными ([η]·с < 1); или к б) концентрированными ([η]·с > 1) Со свойствами разбавленных растворов уже познакомились Для концентрированных растворов характерны явления : а. Гистерезис вязкости б. Пластификация полимеров в. Образование гелей Лекция 3 32
8. Концентрированные растворы полимеров Полимерные растворы в зависимости от величины произведения [η]·с относят к а) разбавленными ([η]·с < 1); или к б) концентрированными ([η]·с > 1) Со свойствами разбавленных растворов уже познакомились Для концентрированных растворов характерны явления : а. Гистерезис вязкости б. Пластификация полимеров в. Образование гелей Лекция 3 32
 Вязкость = 1 + 2 Т 1 Т 2 Температура Гистерезис вязкости концентрированных растворов полимеров Лекция 3 33
Вязкость = 1 + 2 Т 1 Т 2 Температура Гистерезис вязкости концентрированных растворов полимеров Лекция 3 33
 ПЛАСТИФИКАЦИЯ ПОЛИМЕРОВ Термомеханические кривые исходного образца (1) и пластифицированного (2) 2 ТСТ 1 ТТек 2 Лекция 3 ТТек 1 34
ПЛАСТИФИКАЦИЯ ПОЛИМЕРОВ Термомеханические кривые исходного образца (1) и пластифицированного (2) 2 ТСТ 1 ТТек 2 Лекция 3 ТТек 1 34
 Резюме … 1. Условные стадии растворения полимеров 2. Фазовые диаграммы растворов полимеров с верхней (ВКТС) и нижней (НКТС) критическими температурами смешения (растворения) 3. Реология полимеров. Кривые течения растворов ln и расплавов полимеров. Механизм течения полимеров 4. Гидродинамические свойства макромолекул в разбавленных растворах = ln + n ln˙ 5. Исключенный объем 6. Полиэлектролиты 7. Зависимость приведенной вязкости полиметакриловой кислоты от ее степени диссоциации Лекция 3 35
Резюме … 1. Условные стадии растворения полимеров 2. Фазовые диаграммы растворов полимеров с верхней (ВКТС) и нижней (НКТС) критическими температурами смешения (растворения) 3. Реология полимеров. Кривые течения растворов ln и расплавов полимеров. Механизм течения полимеров 4. Гидродинамические свойства макромолекул в разбавленных растворах = ln + n ln˙ 5. Исключенный объем 6. Полиэлектролиты 7. Зависимость приведенной вязкости полиметакриловой кислоты от ее степени диссоциации Лекция 3 35
 ПОЛИМЕРНЫЕ ТЕЛА Лекция 3 36
ПОЛИМЕРНЫЕ ТЕЛА Лекция 3 36
 Полимерные тела состоят из веществ, находящихся в полимерном состоянии Тело физическое – любая заполненная веществом часть пространства вместе с ее границей. ? Вещество может быть низкомолекулярным или высокомолекулярным. Вещество может находиться в газообразном, жидком или кристаллическом состояниях. Вещества и тела могут быть аморфными и кристаллическими Лекция 3 37
Полимерные тела состоят из веществ, находящихся в полимерном состоянии Тело физическое – любая заполненная веществом часть пространства вместе с ее границей. ? Вещество может быть низкомолекулярным или высокомолекулярным. Вещество может находиться в газообразном, жидком или кристаллическом состояниях. Вещества и тела могут быть аморфными и кристаллическими Лекция 3 37
 Макромолекулы полимерного вещества вступают в интенсивную ассоциацию за счет работы межмолекулярных сил, образуя сначала надмолекулярные структуры, затем полимерное тело. Тела могут находиться в двух агрегатных и двух фазовых состояниях: твердом и жидком. Высокомолекулярные соединения не могут образовать газовую фазу. При анализе фазовых и агрегатных переходов высокомолекулярных веществ следует учитывать особое свойство макромолекул – их гибкость. Лекция 3 38
Макромолекулы полимерного вещества вступают в интенсивную ассоциацию за счет работы межмолекулярных сил, образуя сначала надмолекулярные структуры, затем полимерное тело. Тела могут находиться в двух агрегатных и двух фазовых состояниях: твердом и жидком. Высокомолекулярные соединения не могут образовать газовую фазу. При анализе фазовых и агрегатных переходов высокомолекулярных веществ следует учитывать особое свойство макромолекул – их гибкость. Лекция 3 38
 Физические и механические свойства тел - Эластичность Прочность Ударостойкость Хрупкость Истираемость Прочность на изгиб Диэлектрические свойства Усталость и т. д. Т. о. так или иначе вопрос о свойствах сводится к вопросу о деформации тела… Лекция 3 39
Физические и механические свойства тел - Эластичность Прочность Ударостойкость Хрупкость Истираемость Прочность на изгиб Диэлектрические свойства Усталость и т. д. Т. о. так или иначе вопрос о свойствах сводится к вопросу о деформации тела… Лекция 3 39
 n Деформация при постоянном объеме Пластина (а) и полученное тело путем ее вращения в высокоэластическом состоянии вокруг вертикальной оси (б) Куб с размерами ребер lo из полимерного материала Лекция 3 40
n Деформация при постоянном объеме Пластина (а) и полученное тело путем ее вращения в высокоэластическом состоянии вокруг вертикальной оси (б) Куб с размерами ребер lo из полимерного материала Лекция 3 40
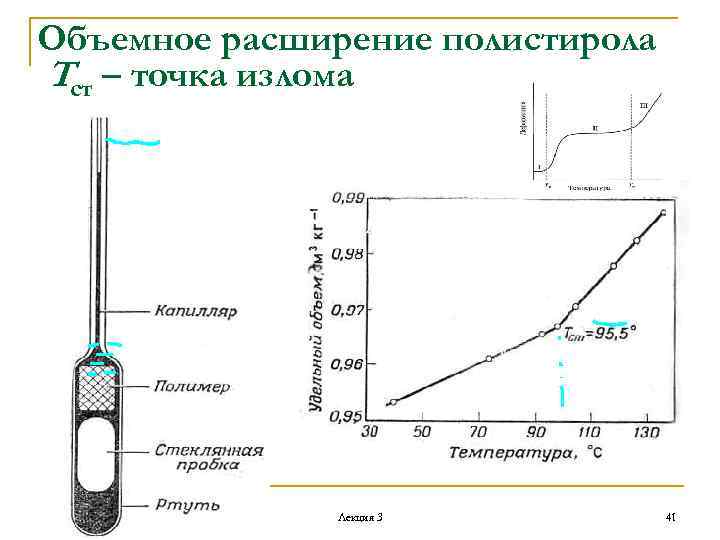 Объемное расширение полистирола Тст – точка излома Лекция 3 41
Объемное расширение полистирола Тст – точка излома Лекция 3 41
 Термомеханическая кривая аморфного полимерного тела Лекция 3 42
Термомеханическая кривая аморфного полимерного тела Лекция 3 42
 n. Особенности трех физических состояний аморфных полимеров I. Незначительные обратимые деформации в соответствии с законом Гука Δl/lо =1/E·σ. E составляет 2. 2·103 5·103 МПа n Деформация составляет 600 800 %, но может достигать и 1000 %. Это физическое состояние называется высокоэластическим (модуль E от 0. 2 до 2 МПа) n. III. Огромные необратимые деформации, когда образец по окончании эксперимента превращается в новое физическое тело – тонкую сплошную нить (удлинение до разрыва может достигать тысячи %). Лекция 3 43
n. Особенности трех физических состояний аморфных полимеров I. Незначительные обратимые деформации в соответствии с законом Гука Δl/lо =1/E·σ. E составляет 2. 2·103 5·103 МПа n Деформация составляет 600 800 %, но может достигать и 1000 %. Это физическое состояние называется высокоэластическим (модуль E от 0. 2 до 2 МПа) n. III. Огромные необратимые деформации, когда образец по окончании эксперимента превращается в новое физическое тело – тонкую сплошную нить (удлинение до разрыва может достигать тысячи %). Лекция 3 43


