IzGeoCh09-10_L1-3.ppt
- Количество слайдов: 149
 ОСНОВИ ІЗОТОПНОЇ ГЕОХІМІЇ С. Є. Шнюков Лекція 1 Поняття про сучасну ізотопну геохімію: Об’єкт та предмет, коротка історія розвитку, сучасний стан та зв’язок з іншими дисциплінами
ОСНОВИ ІЗОТОПНОЇ ГЕОХІМІЇ С. Є. Шнюков Лекція 1 Поняття про сучасну ізотопну геохімію: Об’єкт та предмет, коротка історія розвитку, сучасний стан та зв’язок з іншими дисциплінами
 Вступ (коротка характеристика дисципліни): n n n Навчальна дисципліна "Основи ізотопної геохімії" є базовою нормативною дисципліною, яка викладається у 8 -му семестрі на 4 -му курсі при підготовці фахівців‑бакалаврів за спеціальністю 6. 040103 – геологія (спеціалізації - геохімія і мінералогія та геологія ). Її викладання передбачає 32 години лекцій (16!), самостійну роботу студентів, 2 модульні контрольні роботи. Вивчення дисципліни завершується іспитом (2 кредити ECTS).
Вступ (коротка характеристика дисципліни): n n n Навчальна дисципліна "Основи ізотопної геохімії" є базовою нормативною дисципліною, яка викладається у 8 -му семестрі на 4 -му курсі при підготовці фахівців‑бакалаврів за спеціальністю 6. 040103 – геологія (спеціалізації - геохімія і мінералогія та геологія ). Її викладання передбачає 32 години лекцій (16!), самостійну роботу студентів, 2 модульні контрольні роботи. Вивчення дисципліни завершується іспитом (2 кредити ECTS).
 Згадаємо! Об ’єкт та передметгеохімії: Об’єктом вивчення навчальної дисципліни "Основи геохімії" є хімічні елементи (нейтральні атоми, іони, групи атомів), які знаходяться в умовах земної кори та інших геосфер. Предметом вивчення навчальної дисципліни "Основи геохімії" саме й є ті умови земної кори та інших геосфер (мантії, ядра, гідросфери, атмосфери, біосфери, тошо), що зумовлюють процеси міграції, концентрування і розсіяння хімічних елементів та призводять до формування хімічного складу природних об’єктів (гірських порід, руд, мінералів тощо), який ми можемо безпосередньо спостерігати у теперешній час.
Згадаємо! Об ’єкт та передметгеохімії: Об’єктом вивчення навчальної дисципліни "Основи геохімії" є хімічні елементи (нейтральні атоми, іони, групи атомів), які знаходяться в умовах земної кори та інших геосфер. Предметом вивчення навчальної дисципліни "Основи геохімії" саме й є ті умови земної кори та інших геосфер (мантії, ядра, гідросфери, атмосфери, біосфери, тошо), що зумовлюють процеси міграції, концентрування і розсіяння хімічних елементів та призводять до формування хімічного складу природних об’єктів (гірських порід, руд, мінералів тощо), який ми можемо безпосередньо спостерігати у теперешній час.
 n n Об’єктом вивчення навчальної дисципліни "Основи ізотопної геохімії" є ізотопи хімічних елементів, які знаходяться в умовах земної кори та інших геосфер. Предметом вивчення навчальної дисципліни "Основи ізотопної геохімії" саме й є ті умови земної кори та інших геосфер (мантії, ядра, гідросфери, атмосфери, біосфери, тошо), що зумовлюють процеси міграції, концентрування і розсіяння хімічних елементів та призводять до формування хімічного складу природних об’єктів (гірських порід, руд, мінералів тощо), який ми можемо безпосередньо спостерігати в теперешній час.
n n Об’єктом вивчення навчальної дисципліни "Основи ізотопної геохімії" є ізотопи хімічних елементів, які знаходяться в умовах земної кори та інших геосфер. Предметом вивчення навчальної дисципліни "Основи ізотопної геохімії" саме й є ті умови земної кори та інших геосфер (мантії, ядра, гідросфери, атмосфери, біосфери, тошо), що зумовлюють процеси міграції, концентрування і розсіяння хімічних елементів та призводять до формування хімічного складу природних об’єктів (гірських порід, руд, мінералів тощо), який ми можемо безпосередньо спостерігати в теперешній час.
 Головна відміна геохімія хімії : від n Хімія вивчає перетворення речовини в найрізноманітних! діапазонах фізико-хімічних (РТX) умов, які можуть бути спеціально та досить довільно задані дослідниками. n Геохіміядосліджує поведінку хімічних елементів та їх ізотопів лише у специфічних та більш вузьких! діапазонах фізикохімічних (РТX) умов, які властиві земним геосферам. n Наочною ілюстрацією цієї відміни є той факт, що в лабораторних умовах хіміками одержано десятки тисяч різноманітних тількі неорганічних сполук, а на Землі зараз відомо лише більше 3500 мінеральних видів, які утворені з тих самих хімічних елементів, але не в довільних, а конкретних РТX-умовах земних геосфер. n Ізотопна геохімія – частина геохімії, яка оперує концентраціями ізотопів. Значення цих концентрацій – досить низьке. Тому ізотопна геохімя – найбільш прецизійна, кількісна та “фізична” частина геохімії.
Головна відміна геохімія хімії : від n Хімія вивчає перетворення речовини в найрізноманітних! діапазонах фізико-хімічних (РТX) умов, які можуть бути спеціально та досить довільно задані дослідниками. n Геохіміядосліджує поведінку хімічних елементів та їх ізотопів лише у специфічних та більш вузьких! діапазонах фізикохімічних (РТX) умов, які властиві земним геосферам. n Наочною ілюстрацією цієї відміни є той факт, що в лабораторних умовах хіміками одержано десятки тисяч різноманітних тількі неорганічних сполук, а на Землі зараз відомо лише більше 3500 мінеральних видів, які утворені з тих самих хімічних елементів, але не в довільних, а конкретних РТX-умовах земних геосфер. n Ізотопна геохімія – частина геохімії, яка оперує концентраціями ізотопів. Значення цих концентрацій – досить низьке. Тому ізотопна геохімя – найбільш прецизійна, кількісна та “фізична” частина геохімії.
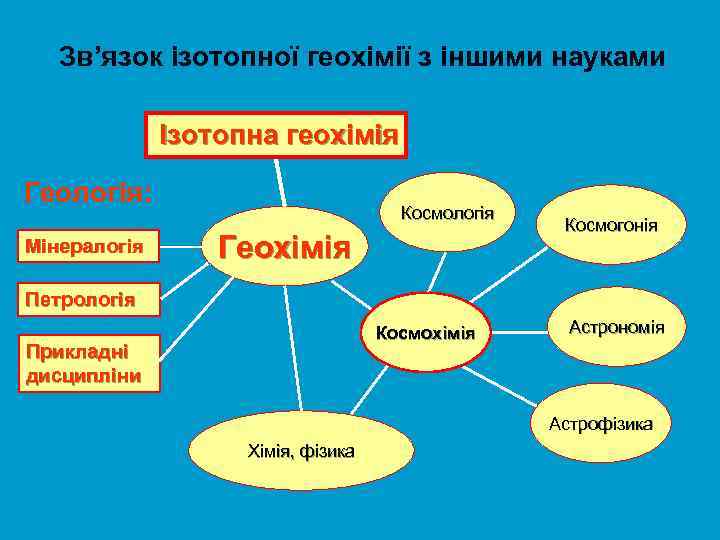 Зв’язок ізотопної геохімії з іншими науками Ізотопна геохімія Геологія: Мінералогія Космологія Геохімія Космогонія Петрологія Космохімія Прикладні дисципліни Астрономія Астрофізика Хімія, фізика
Зв’язок ізотопної геохімії з іншими науками Ізотопна геохімія Геологія: Мінералогія Космологія Геохімія Космогонія Петрологія Космохімія Прикладні дисципліни Астрономія Астрофізика Хімія, фізика
 Головні завдання та розділи ізотопної геохімії: n Визначення віку мінералів та гірських порід, датування процесів їх утворення. Відповідний розділ має назву “Ізотопна геохронологія”. n Дослідження геологічних процесів за допомогою використання ізотопів в якості природних “мічених атомів”. Основою цього підходу є контрасна геохімічна поведінка радіоактивних ізотопів (курс “Основи геохімії”!!!) – одних породах вони концентруються, а з інших виносяться (U, Th, Rb – несумісні елементи!!!). Наприклад, корові породи збагачені Rb, та, як наслідок, вміщують значно більше радіогенного 87 Sr (85 Rb – стабільний, 72%, а 87 Rb – радіоактивний, 28% дає 87 Sr) ніж мантійні деплетовані породи. Тому співвідношення 87 Sr/ 86 Sr (86 Sr – стабільний та нерадіогенний, один з 4 – 88 найбільш поширений , 87, 86, 84 ) – індикатор рівня мобілізації речовини. Відповідний розділ має назву “Геохімія радіогенних ізотопів”. n Дослідження поведінки ізотопів легких елементів (кисень, вуглець, сірка. . . ) в залежності від PTX-умов геохімічних процесів, та вирішення зворотної задачі – реставрування цих умов за спостереженими ізотопно-геохімічними даними. Відповідний розділ має назву “Геохімія стабільних ізотопів” n Ще раз: ізотопна геохімія – частина геохімії, яка оперує концентраціями ізотопів. Значення цих концентрацій – досить низьке. Тому ізотопна геохімя – найбільш прецизійна, кількісна та “фізична” частина геохімії.
Головні завдання та розділи ізотопної геохімії: n Визначення віку мінералів та гірських порід, датування процесів їх утворення. Відповідний розділ має назву “Ізотопна геохронологія”. n Дослідження геологічних процесів за допомогою використання ізотопів в якості природних “мічених атомів”. Основою цього підходу є контрасна геохімічна поведінка радіоактивних ізотопів (курс “Основи геохімії”!!!) – одних породах вони концентруються, а з інших виносяться (U, Th, Rb – несумісні елементи!!!). Наприклад, корові породи збагачені Rb, та, як наслідок, вміщують значно більше радіогенного 87 Sr (85 Rb – стабільний, 72%, а 87 Rb – радіоактивний, 28% дає 87 Sr) ніж мантійні деплетовані породи. Тому співвідношення 87 Sr/ 86 Sr (86 Sr – стабільний та нерадіогенний, один з 4 – 88 найбільш поширений , 87, 86, 84 ) – індикатор рівня мобілізації речовини. Відповідний розділ має назву “Геохімія радіогенних ізотопів”. n Дослідження поведінки ізотопів легких елементів (кисень, вуглець, сірка. . . ) в залежності від PTX-умов геохімічних процесів, та вирішення зворотної задачі – реставрування цих умов за спостереженими ізотопно-геохімічними даними. Відповідний розділ має назву “Геохімія стабільних ізотопів” n Ще раз: ізотопна геохімія – частина геохімії, яка оперує концентраціями ізотопів. Значення цих концентрацій – досить низьке. Тому ізотопна геохімя – найбільш прецизійна, кількісна та “фізична” частина геохімії.
 Місце дисципліни в структурно-логічній схемі спеціальності: Нормативна навчальна дисципліна "Основи ізотопної геохімії" є важливою та невід’ємною складовою частиною циклу професійної підготовки фахівців освітньокваліфікаційного рівня "бакалавр" за спеціальністю „Геологія” (спеціалізація „геохімія і мінералогія”). Дисципліна "Основи ізотопної геохімії" розрахована на студентів-бакалаврів, які успішно засвоїли курси “речовинного” профілю “Основи космохімії”, “Основи геохімії”, „Фізика”, „Хімія”, „Мінералогія”, „Петрографія” тощо. Поряд з іншими дисциплінами геохімічного напрямку вона складає чітку послідовність у навчальному плані спеціалізації “геохімія і мінералогія”. Тобто, для бакалаврів спеціалізації “геохімія і мінералогія” має місце наступний ряд дисциплін геохімічного напрямку: “Основи аналітичної геохімії” – “Методи дослідження мінеральної речовини” – “Основи фізична геохімія” – “Основи космохімії” – “Основи геохімії” – “Основи ізотопної геохімії” – “Геохімічні методи пошуків” – “Методи обробки геохімічних даних”.
Місце дисципліни в структурно-логічній схемі спеціальності: Нормативна навчальна дисципліна "Основи ізотопної геохімії" є важливою та невід’ємною складовою частиною циклу професійної підготовки фахівців освітньокваліфікаційного рівня "бакалавр" за спеціальністю „Геологія” (спеціалізація „геохімія і мінералогія”). Дисципліна "Основи ізотопної геохімії" розрахована на студентів-бакалаврів, які успішно засвоїли курси “речовинного” профілю “Основи космохімії”, “Основи геохімії”, „Фізика”, „Хімія”, „Мінералогія”, „Петрографія” тощо. Поряд з іншими дисциплінами геохімічного напрямку вона складає чітку послідовність у навчальному плані спеціалізації “геохімія і мінералогія”. Тобто, для бакалаврів спеціалізації “геохімія і мінералогія” має місце наступний ряд дисциплін геохімічного напрямку: “Основи аналітичної геохімії” – “Методи дослідження мінеральної речовини” – “Основи фізична геохімія” – “Основи космохімії” – “Основи геохімії” – “Основи ізотопної геохімії” – “Геохімічні методи пошуків” – “Методи обробки геохімічних даних”.
 Загальний план курсу “Основи геохімії”: ОБНОВЛЯЕМЫЙ ВАРИАНТ 1. Поняття про сучасну геохімію та її методи 2. Хімічні елементи в геохімії n Будова атомів та іонів n Важливі для геохімії властивості хімічних елементів n Геохімічна класифікація елементів 3. Загальна геохімічна характеристика планети Земля та її геосфер 4. Фактори, які контролюють розподіл хімічних елементів в геосферах n Головні поняття та засоби, які використовуються в дослідженні розподілу елементів n Структурний контроль розподілу елементів. n Термодинамічний контроль розподілу елементів. n Кінетичний контроль розподілу елементів. n Поєднаний вплив структурного, термодинамічного та кінетичного факторів на поведінку елементів в геохімічних процесах. n Розсіяний та концентрований стан елементів в природі, інтенсивність та типи їх міграції. 5. Ізотопи та радіоактивність 6. Геохімія ендогенних систем n Магматичні та магматогенно-гідротермальні системи n Метаморфічні системи n Гідротермально-метасоматичні системи n Геохімічний взаємозв’язок ендогенних рудоутворюючих систем 7. Геохімія седиментогенезу 8. Геохімічна еволюція Землі 9. Значення геохімії для вирішення актуальних теоретичних та прикладних задач
Загальний план курсу “Основи геохімії”: ОБНОВЛЯЕМЫЙ ВАРИАНТ 1. Поняття про сучасну геохімію та її методи 2. Хімічні елементи в геохімії n Будова атомів та іонів n Важливі для геохімії властивості хімічних елементів n Геохімічна класифікація елементів 3. Загальна геохімічна характеристика планети Земля та її геосфер 4. Фактори, які контролюють розподіл хімічних елементів в геосферах n Головні поняття та засоби, які використовуються в дослідженні розподілу елементів n Структурний контроль розподілу елементів. n Термодинамічний контроль розподілу елементів. n Кінетичний контроль розподілу елементів. n Поєднаний вплив структурного, термодинамічного та кінетичного факторів на поведінку елементів в геохімічних процесах. n Розсіяний та концентрований стан елементів в природі, інтенсивність та типи їх міграції. 5. Ізотопи та радіоактивність 6. Геохімія ендогенних систем n Магматичні та магматогенно-гідротермальні системи n Метаморфічні системи n Гідротермально-метасоматичні системи n Геохімічний взаємозв’язок ендогенних рудоутворюючих систем 7. Геохімія седиментогенезу 8. Геохімічна еволюція Землі 9. Значення геохімії для вирішення актуальних теоретичних та прикладних задач
 В НАВЧАЛЬНО-ТЕМАТИЧНОМУ ПЛАНІ КУРСУ “ОСНОВИ ГЕОХІМІЇ”: 4. Хімічні елементи та їх ізотопи в геохімії (1) Будова та розміри атомів та іонів n Елементарні частки та розподіл електронів в атомах. n Атомні радіуси хімічних елементів. n Іонні радіуси хімічних елементів. n Потенціали іонізації та спорідненість до електрону атомів та іонів. n Електронегативність хімічних елементів. n Кислотно-основні властивості хімічних елементів. n Типи хімічного зв’язку та їх значення для геохімії. n Кристалохімія та їзоморфізм. Головні типи ізоморфізму та його геохімічне значення.
В НАВЧАЛЬНО-ТЕМАТИЧНОМУ ПЛАНІ КУРСУ “ОСНОВИ ГЕОХІМІЇ”: 4. Хімічні елементи та їх ізотопи в геохімії (1) Будова та розміри атомів та іонів n Елементарні частки та розподіл електронів в атомах. n Атомні радіуси хімічних елементів. n Іонні радіуси хімічних елементів. n Потенціали іонізації та спорідненість до електрону атомів та іонів. n Електронегативність хімічних елементів. n Кислотно-основні властивості хімічних елементів. n Типи хімічного зв’язку та їх значення для геохімії. n Кристалохімія та їзоморфізм. Головні типи ізоморфізму та його геохімічне значення.
 В НАВЧАЛЬНО-ТЕМАТИЧНОМУ ПЛАНІ КУРСУ “ОСНОВИ ГЕОХІМІЇ”: 4. Хімічні елементи та їх ізотопи в геохімії (2) Ізотопи та радіоактивність n Будова ядер атомів і геохімічні особливості елементів. Поняття про нукліди. Розповсюдженість (поширеність) атомів у природі як функція будови їх ядер. n Ядерні процеси у природі. Значення радіоактивних (K, U, Th) елементів як джерела енергії у еволюції Землі. Поняття про "вимерлі" елементи (на прикладі “проблеми 61 -го (Pm) елементу”). n Радіоактивні ізотопи та їх значення для геохімії. Поняття про методи визначення віку геологічних об’єктів (U-Pb, K-Ar, Rb-Sr, Sm-Nd та інші). Використання радіогенних ізотопів Sr, Nd, Pb для встановлення генезису та історії формування геологічних об'єктів. n Поширення та геохімія стабільних ізотопів. Кінетичний та термодинамічний ізотопні ефекти. Ізотопна геотермометрія. Ізотопи H, O, C і S та їх роль як індикаторів генезису та умов формування геологічних об’єктів.
В НАВЧАЛЬНО-ТЕМАТИЧНОМУ ПЛАНІ КУРСУ “ОСНОВИ ГЕОХІМІЇ”: 4. Хімічні елементи та їх ізотопи в геохімії (2) Ізотопи та радіоактивність n Будова ядер атомів і геохімічні особливості елементів. Поняття про нукліди. Розповсюдженість (поширеність) атомів у природі як функція будови їх ядер. n Ядерні процеси у природі. Значення радіоактивних (K, U, Th) елементів як джерела енергії у еволюції Землі. Поняття про "вимерлі" елементи (на прикладі “проблеми 61 -го (Pm) елементу”). n Радіоактивні ізотопи та їх значення для геохімії. Поняття про методи визначення віку геологічних об’єктів (U-Pb, K-Ar, Rb-Sr, Sm-Nd та інші). Використання радіогенних ізотопів Sr, Nd, Pb для встановлення генезису та історії формування геологічних об'єктів. n Поширення та геохімія стабільних ізотопів. Кінетичний та термодинамічний ізотопні ефекти. Ізотопна геотермометрія. Ізотопи H, O, C і S та їх роль як індикаторів генезису та умов формування геологічних об’єктів.
 В НАВЧАЛЬНО-ТЕМАТИЧНОМУ ПЛАНІ КУРСУ “ОСНОВИ ГЕОХІМІЇ”: 8. Геохімічна еволюція Землі. n n n n Геохімічна диференціація первинної земної речовини. Формування мантії та ядра. Примітивна мантія Землі як джерело речовини для формування земної кори. Виникнення системи мантія — кора та загальна спрямованість її еволюції. Часткове плавлення на мантійному та коровому рівні глибин і подальша магматична еволюція розплавів як головний механізм формування континентальної кори. Роль мантійних геохімічних резервуарів в цьому процесі. Формування океанічної кори. Роль процесу корового рециклювання в геохімічній еволюції верхньої мантії та земної кори в цілому. Сучасні моделі росту континентальної кори та взаємовідносин мантія — кора. Дегазація мантії та її геохімічне значення. Головні тенденції еволюції та геохімічний взаємозв’язок процесів седиментогенезу, магматизму, метаморфізму. Металогенічні епохи, їх практичне значення.
В НАВЧАЛЬНО-ТЕМАТИЧНОМУ ПЛАНІ КУРСУ “ОСНОВИ ГЕОХІМІЇ”: 8. Геохімічна еволюція Землі. n n n n Геохімічна диференціація первинної земної речовини. Формування мантії та ядра. Примітивна мантія Землі як джерело речовини для формування земної кори. Виникнення системи мантія — кора та загальна спрямованість її еволюції. Часткове плавлення на мантійному та коровому рівні глибин і подальша магматична еволюція розплавів як головний механізм формування континентальної кори. Роль мантійних геохімічних резервуарів в цьому процесі. Формування океанічної кори. Роль процесу корового рециклювання в геохімічній еволюції верхньої мантії та земної кори в цілому. Сучасні моделі росту континентальної кори та взаємовідносин мантія — кора. Дегазація мантії та її геохімічне значення. Головні тенденції еволюції та геохімічний взаємозв’язок процесів седиментогенезу, магматизму, метаморфізму. Металогенічні епохи, їх практичне значення.
 Повернемось до ряду дисциплін геохімічного профілю: “Основи аналітичної геохімії” – “Методи дослідження мінеральної речовини” – “Основи фізична геохімія” – “Основи космохімії” – “Основи геохімії” – “Основи ізотопної геохімії” – “Геохімічні методи пошуків” – “Методи обробки геохімічних даних”. – лабораторні заняття Цей ряд продовжується у магістерській програмі за спеціальністю “геохімія і мінералогія”: “Прикладна фізична геохімія”, „Методи фізико-хімічного моделювання геологічних процесів”, „Методи ізотопної геохронології” тощо.
Повернемось до ряду дисциплін геохімічного профілю: “Основи аналітичної геохімії” – “Методи дослідження мінеральної речовини” – “Основи фізична геохімія” – “Основи космохімії” – “Основи геохімії” – “Основи ізотопної геохімії” – “Геохімічні методи пошуків” – “Методи обробки геохімічних даних”. – лабораторні заняття Цей ряд продовжується у магістерській програмі за спеціальністю “геохімія і мінералогія”: “Прикладна фізична геохімія”, „Методи фізико-хімічного моделювання геологічних процесів”, „Методи ізотопної геохронології” тощо.
 ПЕРЕЛІК РЕКОМЕНДОВАНОЇ ЛІТЕРАТУРИ n n n Основна: Барабанов В. Ф. Геохимия. — Л. : Недра, 1985. — 422 с. Войткевич Г. В. , Закруткин В. В. Основы геохимии. — М. : Высшая школа, 1976. - 365 с. Мейсон Б. Основы геохимии — М. : Недра, 1971. — 311 с. Хендерсон П. Неорганическая геохимия. — М. : Мир, 1985. — 339 с. Тугаринов А. И. Общая геохимия. — М. : Атомиздат, 1973. — 288 с. Додаткова: n n n Войткевич Г. В. , Кокин А. В. , Мирошников А. Е. , Прохоров В. Г. Справочник по геохимии. — М. : Недра, 1990. — 480 с. Geochemistry and Mineralogy of Rare Earth Elements / Ed. : B. R. Lipin & G. A. Mc. Kay. – Reviews in Mineralogy, vol. 21. — Mineralogical Society of America, 1989. – 348 p. White W. M. Geochemistry -2001
ПЕРЕЛІК РЕКОМЕНДОВАНОЇ ЛІТЕРАТУРИ n n n Основна: Барабанов В. Ф. Геохимия. — Л. : Недра, 1985. — 422 с. Войткевич Г. В. , Закруткин В. В. Основы геохимии. — М. : Высшая школа, 1976. - 365 с. Мейсон Б. Основы геохимии — М. : Недра, 1971. — 311 с. Хендерсон П. Неорганическая геохимия. — М. : Мир, 1985. — 339 с. Тугаринов А. И. Общая геохимия. — М. : Атомиздат, 1973. — 288 с. Додаткова: n n n Войткевич Г. В. , Кокин А. В. , Мирошников А. Е. , Прохоров В. Г. Справочник по геохимии. — М. : Недра, 1990. — 480 с. Geochemistry and Mineralogy of Rare Earth Elements / Ed. : B. R. Lipin & G. A. Mc. Kay. – Reviews in Mineralogy, vol. 21. — Mineralogical Society of America, 1989. – 348 p. White W. M. Geochemistry -2001
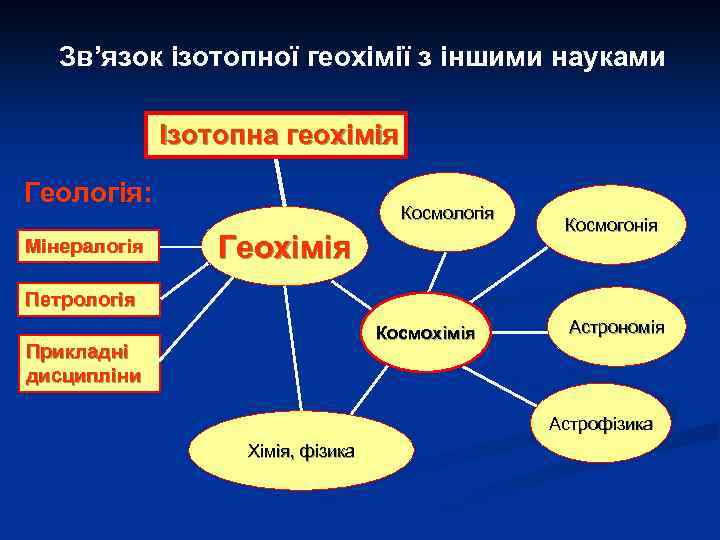 Зв’язок ізотопної геохімії з іншими науками Ізотопна геохімія Геологія: Мінералогія Космологія Геохімія Космогонія Петрологія Космохімія Прикладні дисципліни Астрономія Астрофізика Хімія, фізика
Зв’язок ізотопної геохімії з іншими науками Ізотопна геохімія Геологія: Мінералогія Космологія Геохімія Космогонія Петрологія Космохімія Прикладні дисципліни Астрономія Астрофізика Хімія, фізика
 Геохімія – молода наука. Історія її створення та розвитку є типовою для багатьох перспективних наукових галузей (ядерна фізика, космохімія, космологія, космохімія тощо). Головні періоди (етапи) історії геохімії Головні назвемо таким чином: Етап 1. “Загальнонауковий”: античність – друга половина XIX сторіччя н. е. Етап 2. “Етап формування та інтенсивного розвитку”: друга половина XIX сторіччя – 1950 -ті. . . 1960 -ті роки Етап 3. “Сучасний” : 1960 -ті роки – 2020 -ті ? ? ? роки Зауважимо що: 3 -й етап, звичайно, не є останнім. Вже зараз (починаючи з кінця 1980 -х – початку 1990 -х років) спостерігаються наявні ознаки переходу до наступного етапу розвитку геохімії та всього комплексу споріднених дисциплін. Назвемо цей етап “перспективним”. Хронологічні межи цього та інших етапів, а також реперні ознаки переходу від одного етапу до іншого раціонально обгрунтувати надаючи їх коротку характеристику.
Геохімія – молода наука. Історія її створення та розвитку є типовою для багатьох перспективних наукових галузей (ядерна фізика, космохімія, космологія, космохімія тощо). Головні періоди (етапи) історії геохімії Головні назвемо таким чином: Етап 1. “Загальнонауковий”: античність – друга половина XIX сторіччя н. е. Етап 2. “Етап формування та інтенсивного розвитку”: друга половина XIX сторіччя – 1950 -ті. . . 1960 -ті роки Етап 3. “Сучасний” : 1960 -ті роки – 2020 -ті ? ? ? роки Зауважимо що: 3 -й етап, звичайно, не є останнім. Вже зараз (починаючи з кінця 1980 -х – початку 1990 -х років) спостерігаються наявні ознаки переходу до наступного етапу розвитку геохімії та всього комплексу споріднених дисциплін. Назвемо цей етап “перспективним”. Хронологічні межи цього та інших етапів, а також реперні ознаки переходу від одного етапу до іншого раціонально обгрунтувати надаючи їх коротку характеристику.
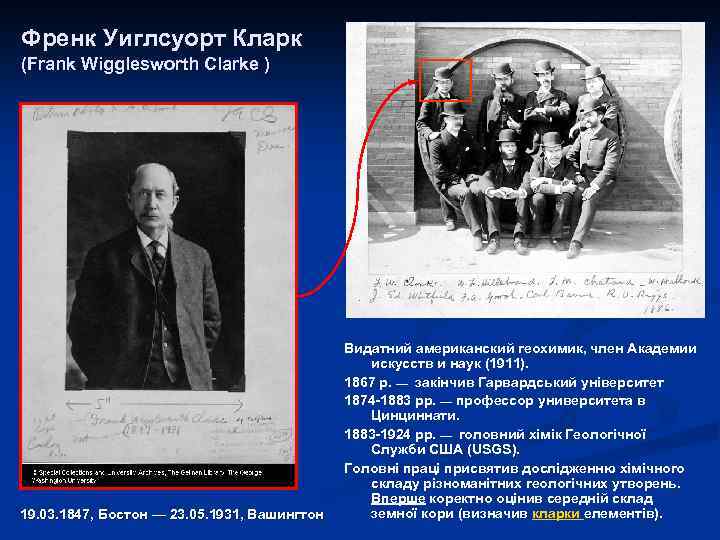 Френк Уиглсуорт Кларк (Frank Wigglesworth Clarke ) 19. 03. 1847, Бостон — 23. 05. 1931, Вашингтон Видатний американский геохимик, член Академии искусств и наук (1911). 1867 р. — закінчив Гарвардський університет 1874 -1883 рр. — профессор университета в Цинциннати. 1883 -1924 рр. — головний хімік Геологічної Служби США (USGS). Головні праці присвятив дослідженню хімічного складу різноманітних геологічних утворень. Вперше коректно оцінив середній склад земної кори (визначив кларки елементів).
Френк Уиглсуорт Кларк (Frank Wigglesworth Clarke ) 19. 03. 1847, Бостон — 23. 05. 1931, Вашингтон Видатний американский геохимик, член Академии искусств и наук (1911). 1867 р. — закінчив Гарвардський університет 1874 -1883 рр. — профессор университета в Цинциннати. 1883 -1924 рр. — головний хімік Геологічної Служби США (USGS). Головні праці присвятив дослідженню хімічного складу різноманітних геологічних утворень. Вперше коректно оцінив середній склад земної кори (визначив кларки елементів).
 Владимир Иванович Вернадский 28. 02. 1863, СПб — 6. 01. 1945, Москва Владимир Иванович Вернадский родился в Санкт-Петербурге. В 1885 окончил физико-математический факультет Петербурского университета. В 1898 — 1911 профессор Московского университета. В круг его интересов входили геология и кристаллография, минералогия и геохимия, радиогеология и биология, биогеохимия и философия. Деятельность Вернадского оказала огромное влияние на развитие наук о Земле, на становление и рост АН СССР, на мировоззрение многих людей. В 1915 — 1930 председатель Комиссии по изучению естественных производственных сил России, был одним из создателей плана ГОЭЛРО. Комиссия внесла огромный вклад в геологическое изучение Советского Союза и создание его независимой минерально-сырьевой базы. С 1912 академик РАН (позже АН СССР ). Один из основателей и первый президент ( 27 октября 1918) Украинской АН. С 1922 по 1939 директор организованного им Радиевого института. В период 1922 — 1926 работал за границей в Праге и Париже. Опубликовано более 700 научных трудов. Основал новую науку — биогеохимию, и сделал огромный вклад в геохимию. С 1927 до самой смерти занимал должность директора Биогеохимической лаборатории при АН СССР. Был учителем целой плеяды советских геохимиков. Наибольшую известность принесло учение о ноосфере. Создал закон о повсеместной распространенности х. э. Первым широко применял спектральный анализ.
Владимир Иванович Вернадский 28. 02. 1863, СПб — 6. 01. 1945, Москва Владимир Иванович Вернадский родился в Санкт-Петербурге. В 1885 окончил физико-математический факультет Петербурского университета. В 1898 — 1911 профессор Московского университета. В круг его интересов входили геология и кристаллография, минералогия и геохимия, радиогеология и биология, биогеохимия и философия. Деятельность Вернадского оказала огромное влияние на развитие наук о Земле, на становление и рост АН СССР, на мировоззрение многих людей. В 1915 — 1930 председатель Комиссии по изучению естественных производственных сил России, был одним из создателей плана ГОЭЛРО. Комиссия внесла огромный вклад в геологическое изучение Советского Союза и создание его независимой минерально-сырьевой базы. С 1912 академик РАН (позже АН СССР ). Один из основателей и первый президент ( 27 октября 1918) Украинской АН. С 1922 по 1939 директор организованного им Радиевого института. В период 1922 — 1926 работал за границей в Праге и Париже. Опубликовано более 700 научных трудов. Основал новую науку — биогеохимию, и сделал огромный вклад в геохимию. С 1927 до самой смерти занимал должность директора Биогеохимической лаборатории при АН СССР. Был учителем целой плеяды советских геохимиков. Наибольшую известность принесло учение о ноосфере. Создал закон о повсеместной распространенности х. э. Первым широко применял спектральный анализ.
 Виктор Мориц Гольдшмидт (Victor Moritz Goldschmidt) 27. 01. 1888, Цюрих — 20. 03. 1947, Осло Виктор Мориц Гольдшмидт родился в Цюрихе. Его родители, Генрих Д. Гольдшмидт (Heinrich J. Goldschmidt) и Амели Коэн (Amelie Koehne) назвали своего сына в честь учителя отца, Виктора Майера. Семья Гольдшмидта переехала в Норвегию в 1901 году, когда Генрих Гольдшмидт получил должность профессора химии в Кристиании (старое название Осло). Первая научная работа Гольдшмидта называлась «Контактовый метаморфизм в окрестностях Кристиании» . В ней он впервые применил термодинамическое правило фаз Гиббса к геологическим объектам. Серия его работ под названием «Геохимия элементов» (Geochemische Verteilungsgesetze der Elemente) считается началом геохимии. Работы Гольдшмидта о атомных и ионных радиусах оказали большое влияние на кристаллохимию. Гольдшмидт предложил геохимическую классификации элементов, закон изоморфизма названый его именем. Выдвинул одну из первых теорий относительно состава и строения глубин Земли, причем предсказания Гольдшмидта подтвердились в наибольшей степени. Одним из первых рассчитал состав верхней континентальной коры. Во время немецкой оккупации Гольдшмидт был арестован, но незадолго до запланированной отправки в концентрационный лагерь был похищен Норвежским Сопротивлением, и переправлен в Швецию. Затем он перебрался в Англию, где жили его родственники. После войны он вернулся в Осло, и умер там в возрасте 59 лет. Его главный труд — «Геохимия» — был отредактирован и издан посмертно в Англии в 1954 году.
Виктор Мориц Гольдшмидт (Victor Moritz Goldschmidt) 27. 01. 1888, Цюрих — 20. 03. 1947, Осло Виктор Мориц Гольдшмидт родился в Цюрихе. Его родители, Генрих Д. Гольдшмидт (Heinrich J. Goldschmidt) и Амели Коэн (Amelie Koehne) назвали своего сына в честь учителя отца, Виктора Майера. Семья Гольдшмидта переехала в Норвегию в 1901 году, когда Генрих Гольдшмидт получил должность профессора химии в Кристиании (старое название Осло). Первая научная работа Гольдшмидта называлась «Контактовый метаморфизм в окрестностях Кристиании» . В ней он впервые применил термодинамическое правило фаз Гиббса к геологическим объектам. Серия его работ под названием «Геохимия элементов» (Geochemische Verteilungsgesetze der Elemente) считается началом геохимии. Работы Гольдшмидта о атомных и ионных радиусах оказали большое влияние на кристаллохимию. Гольдшмидт предложил геохимическую классификации элементов, закон изоморфизма названый его именем. Выдвинул одну из первых теорий относительно состава и строения глубин Земли, причем предсказания Гольдшмидта подтвердились в наибольшей степени. Одним из первых рассчитал состав верхней континентальной коры. Во время немецкой оккупации Гольдшмидт был арестован, но незадолго до запланированной отправки в концентрационный лагерь был похищен Норвежским Сопротивлением, и переправлен в Швецию. Затем он перебрался в Англию, где жили его родственники. После войны он вернулся в Осло, и умер там в возрасте 59 лет. Его главный труд — «Геохимия» — был отредактирован и издан посмертно в Англии в 1954 году.
 Тісна співпраця наук та їх провідних представників: Важливим є те, що результати досліджень перелічених дисциплін були комплементарними. Так, наприклад, геохімія разом з астрономією забезпечувала одержання оцінок космічної розповсюдженості елементів, а фізика розробляла моделі нуклеосинтезу, які дозволяли теоретично розрахувати розповсюдженість елементів виходячи з кожної моделі. Зрозуміло, що відповідність емпіричних та модельних оцінок є критерієм адекватності моделі. Використання такого класичного підходу дозволило помітно вдосконалити теорію нуклеосинтезу та космологічні концепції, перш за все концепцію «Великого Вибуху» . Така співпраця між геохімією та фізикою була тісною та плідною. Її ілюструє досить рідкісне фото цього слайду. В. М. Гольдшмідт та А. Ейнштейн на одному з о-вів Осло-фіорду (Норвегія), де вони знайомились з палеозойскими осадочними породами (1920 р. )
Тісна співпраця наук та їх провідних представників: Важливим є те, що результати досліджень перелічених дисциплін були комплементарними. Так, наприклад, геохімія разом з астрономією забезпечувала одержання оцінок космічної розповсюдженості елементів, а фізика розробляла моделі нуклеосинтезу, які дозволяли теоретично розрахувати розповсюдженість елементів виходячи з кожної моделі. Зрозуміло, що відповідність емпіричних та модельних оцінок є критерієм адекватності моделі. Використання такого класичного підходу дозволило помітно вдосконалити теорію нуклеосинтезу та космологічні концепції, перш за все концепцію «Великого Вибуху» . Така співпраця між геохімією та фізикою була тісною та плідною. Її ілюструє досить рідкісне фото цього слайду. В. М. Гольдшмідт та А. Ейнштейн на одному з о-вів Осло-фіорду (Норвегія), де вони знайомились з палеозойскими осадочними породами (1920 р. )
 Ферсман Олександр Євгенович (1883, СПб – 1945, Сочі) n Навчався: Новоросійський та Московський ун-ти, учень В. І. Вернадського , який керував його першими роботами. n Аспірантура — Германія (рук. — В. М. Гольдшмидт), присвячена дослідженню кристалів алмазу (монография «Алмаз» ). n У 1912 р. О. Є. Ферсман стає професором Московського університету, де читає перший у світі курс геохімії. n 1917 -1945 рр. — директор Мінералогічного музею РАН, який зараз носить його ім’я. n 1920 р. — інициатор створення першого у СРСР Ільменського державного наукового заповідника. n 1920 -30 -ті рр. — відкриття унікальних родовищ світового класу — Мончегорського мідно-нікелевого та Хибинського апатитового. n 1930 -ті рр. — фундаментальна праця «Геохімія» (4 т. ), праці в області геохімії космосу та прикладної (пошукової) геохімї, детальне, класичне дослідження пегматитів (монографія «Мінералогія гранітних пегматитів» ). n Академік СПб Імператорської Академії Наук з 1912 р. , академік АН СРСР (РАН) з 1919 р. Віце-президент АН СРСР (1926 -1929 рр. ).
Ферсман Олександр Євгенович (1883, СПб – 1945, Сочі) n Навчався: Новоросійський та Московський ун-ти, учень В. І. Вернадського , який керував його першими роботами. n Аспірантура — Германія (рук. — В. М. Гольдшмидт), присвячена дослідженню кристалів алмазу (монография «Алмаз» ). n У 1912 р. О. Є. Ферсман стає професором Московського університету, де читає перший у світі курс геохімії. n 1917 -1945 рр. — директор Мінералогічного музею РАН, який зараз носить його ім’я. n 1920 р. — інициатор створення першого у СРСР Ільменського державного наукового заповідника. n 1920 -30 -ті рр. — відкриття унікальних родовищ світового класу — Мончегорського мідно-нікелевого та Хибинського апатитового. n 1930 -ті рр. — фундаментальна праця «Геохімія» (4 т. ), праці в області геохімії космосу та прикладної (пошукової) геохімї, детальне, класичне дослідження пегматитів (монографія «Мінералогія гранітних пегматитів» ). n Академік СПб Імператорської Академії Наук з 1912 р. , академік АН СРСР (РАН) з 1919 р. Віце-президент АН СРСР (1926 -1929 рр. ).
 Александр Павлович Виноградов n n n 9. 08. 1895, СПб — 16. 11. 1975, Москва n Ученик и ближайший сотрудник В. И. Вернадского. Окончил Военно-медицинскую академию и химический факультет Ленинградского университета в 1924 г. Академик АН СССР (1953), вице-президент АН СССР (1967 -1975). Ддиректор института геохимии и аналитической химии им. В. И. Вернадского АН СССР с 1947 г. Основатель его прецизионной аналитической базы. В 1953 г. основал и возглавил кафедру геохимии геологического факультета МГУ, зав. кафедрой геохимии МГУ (1953 -1975 гг. ) Геохимии: проводил идею создания физико-химической теории геологических процессов. Оопределил средний состав главных пород Земли. Предложил гипотезу универсального механизма образования оболочек планет на основе зонного плавления силикатной фазы и разработал представление о химической эволюции Земли. Развил в СССР геохимию изотопов и геохимию океана и методы изотопной геохронологии. Биогеохимия: ввёл понятие «биогеохимические провинции» , развил биогеохимический метод поисков полезных ископаемых. Космохимия: хим. состав метеоритов, планет (Луна, Венера).
Александр Павлович Виноградов n n n 9. 08. 1895, СПб — 16. 11. 1975, Москва n Ученик и ближайший сотрудник В. И. Вернадского. Окончил Военно-медицинскую академию и химический факультет Ленинградского университета в 1924 г. Академик АН СССР (1953), вице-президент АН СССР (1967 -1975). Ддиректор института геохимии и аналитической химии им. В. И. Вернадского АН СССР с 1947 г. Основатель его прецизионной аналитической базы. В 1953 г. основал и возглавил кафедру геохимии геологического факультета МГУ, зав. кафедрой геохимии МГУ (1953 -1975 гг. ) Геохимии: проводил идею создания физико-химической теории геологических процессов. Оопределил средний состав главных пород Земли. Предложил гипотезу универсального механизма образования оболочек планет на основе зонного плавления силикатной фазы и разработал представление о химической эволюции Земли. Развил в СССР геохимию изотопов и геохимию океана и методы изотопной геохронологии. Биогеохимия: ввёл понятие «биогеохимические провинции» , развил биогеохимический метод поисков полезных ископаемых. Космохимия: хим. состав метеоритов, планет (Луна, Венера).
 Бурксер Євген Самійлович • Піонер ізотопно-геохімічних та геохронологічних досліджень в Україні • • Проф. Київського Університету • Більшу частину життя працював у Інституті Геологічних наук НАНУ
Бурксер Євген Самійлович • Піонер ізотопно-геохімічних та геохронологічних досліджень в Україні • • Проф. Київського Університету • Більшу частину життя працював у Інституті Геологічних наук НАНУ
 Етап 3. “Сучасний” : 1960 -ті роки – 2020 -ті ? ? ? роки Ми можемо сказати, що саме починаючи з цього етапу почалась епоха “кількісної геохімії”. Передумовою цього етапу є подальший, ще більш інтенсивний науково-технічний розвиток: n n n Розвиток аналітичної техніки (ICP, MS, XRF, EMP, PMP, SHRIMP, LA-ICP-MS) Широке застосування фізико-хімічних підходів до інтерпретації геохімічних даних Широке використання експериментальних досліджень – моделюються системи, які наближені до прирородних (магматичних, гідротермальних) Застосування методів математичного моделювання геохімічних процесів Широке використання численних новітніх космохімічних даних Все це зумовило перехід до створення комплексних геохімічних (петрологогеохімічних) моделей ендогенних та екзогенних систем, в тому числі до моделей, які описують міграцію елементів при формуванні геосфер Землі (моделі планетарного масштабу). Таким чином, геохімія починає “віддавати”свої потужні моливості в петрологію, мінералогію, геодинаміку. . Поступово вона стає узагальнюючою науковою дисципліною, яка саме й спроможна сформувати коректне, повне та системне уявлення про планетарну еволюцію планети Земля та її геосфер. Звичайно, що такий розвиток можливостей призвів й до розквіту прикладних розділів геохімії, насамперед пошукової та екологічної геохімії. В сучасних умовах геохімія займає почесне місце серед найбільш розвинутих геологічних дисциплін. Перелік видатних постатей серед вчених, які внесли суттєвий внесок у розвиток геохімії на 3 -му етапі її розвитку дуже великий. В цьому переліку звичайно такі вчені як С. Р. Тейлор, Мак-Леннан, К. Г. Ведеполь, В. Гриффин, Д. Шоу, В. Уайт, багато інших закордонних дослідників, а також:
Етап 3. “Сучасний” : 1960 -ті роки – 2020 -ті ? ? ? роки Ми можемо сказати, що саме починаючи з цього етапу почалась епоха “кількісної геохімії”. Передумовою цього етапу є подальший, ще більш інтенсивний науково-технічний розвиток: n n n Розвиток аналітичної техніки (ICP, MS, XRF, EMP, PMP, SHRIMP, LA-ICP-MS) Широке застосування фізико-хімічних підходів до інтерпретації геохімічних даних Широке використання експериментальних досліджень – моделюються системи, які наближені до прирородних (магматичних, гідротермальних) Застосування методів математичного моделювання геохімічних процесів Широке використання численних новітніх космохімічних даних Все це зумовило перехід до створення комплексних геохімічних (петрологогеохімічних) моделей ендогенних та екзогенних систем, в тому числі до моделей, які описують міграцію елементів при формуванні геосфер Землі (моделі планетарного масштабу). Таким чином, геохімія починає “віддавати”свої потужні моливості в петрологію, мінералогію, геодинаміку. . Поступово вона стає узагальнюючою науковою дисципліною, яка саме й спроможна сформувати коректне, повне та системне уявлення про планетарну еволюцію планети Земля та її геосфер. Звичайно, що такий розвиток можливостей призвів й до розквіту прикладних розділів геохімії, насамперед пошукової та екологічної геохімії. В сучасних умовах геохімія займає почесне місце серед найбільш розвинутих геологічних дисциплін. Перелік видатних постатей серед вчених, які внесли суттєвий внесок у розвиток геохімії на 3 -му етапі її розвитку дуже великий. В цьому переліку звичайно такі вчені як С. Р. Тейлор, Мак-Леннан, К. Г. Ведеполь, В. Гриффин, Д. Шоу, В. Уайт, багато інших закордонних дослідників, а також:
 Коржинский Дмитрий Сергеевич (1899 -1985) – один из крупнейших петрологов и геохимиков всего 20 -го века. Создатель: (1) теории термодинамически открытых систем с вполне подвижными компонентами, которые являются моделью природных минералообразующих процессов, (2) теории метасоматических процессов и формирования метасоматической зональности (диффузионный и инфильтрационный типы), (3) теории кислотно-основной эволюции постмагматических гидротермальных растворов, (4) гипотезы о потоках трансмагматических флюидов …… Жариков Вилен Андреевич. Академик РАН, доктор геол. мин. наук, директор Института экспериментальной минералогии АН СССР, профессор, зав. кафедрой геохимии геологического факультета МГУ, Опубликовал более 300 научных работ в оласти теоретической и экспериментальной геохимии, минералогии, петрологии Рябчиков Игорь Дмитриевич - геохимик, доктор геол. -мин. наук, профессор кафедры геохимии геологического факультета МГУ, академик РАH. Создатель теории поведения элементов-примесей в магматических системах, предложил термодинамические методы оценки коэффициента распределения, провел комплекс экспериментальных исследований систем, моделирующих процессы формирования рудоносных флюидов при кристаллизации магм. Первым выполнил серию экспериментальных исследований, которые позволили установить механизм генерации алмазоносных лампроитовых и кимберлитовых магм.
Коржинский Дмитрий Сергеевич (1899 -1985) – один из крупнейших петрологов и геохимиков всего 20 -го века. Создатель: (1) теории термодинамически открытых систем с вполне подвижными компонентами, которые являются моделью природных минералообразующих процессов, (2) теории метасоматических процессов и формирования метасоматической зональности (диффузионный и инфильтрационный типы), (3) теории кислотно-основной эволюции постмагматических гидротермальных растворов, (4) гипотезы о потоках трансмагматических флюидов …… Жариков Вилен Андреевич. Академик РАН, доктор геол. мин. наук, директор Института экспериментальной минералогии АН СССР, профессор, зав. кафедрой геохимии геологического факультета МГУ, Опубликовал более 300 научных работ в оласти теоретической и экспериментальной геохимии, минералогии, петрологии Рябчиков Игорь Дмитриевич - геохимик, доктор геол. -мин. наук, профессор кафедры геохимии геологического факультета МГУ, академик РАH. Создатель теории поведения элементов-примесей в магматических системах, предложил термодинамические методы оценки коэффициента распределения, провел комплекс экспериментальных исследований систем, моделирующих процессы формирования рудоносных флюидов при кристаллизации магм. Первым выполнил серию экспериментальных исследований, которые позволили установить механизм генерации алмазоносных лампроитовых и кимберлитовых магм.
 n Izotope geochemistry (W. M. White, 2007) n Part I. Introduction n Lecture 1: Introduction and the Physics of the Nucleus Lecture 2: Radioactive Decay Lecture 3: Nucleosynthesis n Part II. Geohronology n Lecture 4: Basics of Radiogenic Isotope Geochemistry Lecture 5: Geochronology I: The K-Ca-Ar system Lecture 6: Geochronology II: The K-Ar and Rb-Sr systems Lecture 7: Geochronology III: The Sm-Nd system Lecture 8: Geochronology IV: The U-Th-Pb system Lecture 9: Geochronology V: The U-Th-Pb system: zircon dating Lecture 10: Geochronology VI: U-Th decay series dating Lecture 11: Geochronology VII: Other decay systems Lecture 12: Cosmogenic Isotopes in Geochronology Lecture 13: Cosmogenic Isotopes in Geochronology II Lecture 14: Fission Track Dating Lecture 15: Analytical Methods n Part III: Radiogenic Isotope Geochemistry n Lecture 16: Isotope Cosmochemistry Lecture 17: Isotope Cosmochemistry II Lecture 18: The Mantle I Lecture 19: The Mantle II: The Pb Picture Lecture 20: Mantle Models Lecture 21: Mantle Plumes; Subcontinental Lithosphere Lecture 22: The Continental Crust Lecture 23: The Continental Crust II Lecture 24: Isotope Geochemistry of Subduction Zone Magmas Lecture 25: U-Series Isotopes and Melt Generation Lecture 26: Noble Gases and Evolution of the Atmosphere n Part IV: Stable Isotope Geochemistry n Lecture 27: Stable Isotope Theory: Equilibrium Fractionations Lecture 28: Kinetic Fractionations and the Hydrologic System Lecture 29: Biological Fractionations of Stable Isotopes Lecture 30: Stable Isotope Applications I: High Temperatures Lecture 31: Stable Isotope Applications II: Assimilation-Fractional Crystallization Lecture 32: Stable Isotope Applications III: Assimilation and Subduction Lecture 33: Hydrothermal Activity, Metamorphism and Ore Deposits I Lecture 34: Hydrothermal Activity, Metamorphism and Ore Deposits II Lecture 35: Stable Isotopes in Paleontology and Archaeology Lecture 36: Stable Isotopes in Paleoclimatology I Lecture 37: Stable Isotopes in Paleoclimatology II Lecture 38: The Carbon Cycle, Isotopes, and Climate I Lecture 39: The Carbon Cycle, Isotopes, and Climate II Lecture 40: Mass Independent Fractionation; Li and B isotopes n Comments to W. M. White wmw 4@cornell. edu
n Izotope geochemistry (W. M. White, 2007) n Part I. Introduction n Lecture 1: Introduction and the Physics of the Nucleus Lecture 2: Radioactive Decay Lecture 3: Nucleosynthesis n Part II. Geohronology n Lecture 4: Basics of Radiogenic Isotope Geochemistry Lecture 5: Geochronology I: The K-Ca-Ar system Lecture 6: Geochronology II: The K-Ar and Rb-Sr systems Lecture 7: Geochronology III: The Sm-Nd system Lecture 8: Geochronology IV: The U-Th-Pb system Lecture 9: Geochronology V: The U-Th-Pb system: zircon dating Lecture 10: Geochronology VI: U-Th decay series dating Lecture 11: Geochronology VII: Other decay systems Lecture 12: Cosmogenic Isotopes in Geochronology Lecture 13: Cosmogenic Isotopes in Geochronology II Lecture 14: Fission Track Dating Lecture 15: Analytical Methods n Part III: Radiogenic Isotope Geochemistry n Lecture 16: Isotope Cosmochemistry Lecture 17: Isotope Cosmochemistry II Lecture 18: The Mantle I Lecture 19: The Mantle II: The Pb Picture Lecture 20: Mantle Models Lecture 21: Mantle Plumes; Subcontinental Lithosphere Lecture 22: The Continental Crust Lecture 23: The Continental Crust II Lecture 24: Isotope Geochemistry of Subduction Zone Magmas Lecture 25: U-Series Isotopes and Melt Generation Lecture 26: Noble Gases and Evolution of the Atmosphere n Part IV: Stable Isotope Geochemistry n Lecture 27: Stable Isotope Theory: Equilibrium Fractionations Lecture 28: Kinetic Fractionations and the Hydrologic System Lecture 29: Biological Fractionations of Stable Isotopes Lecture 30: Stable Isotope Applications I: High Temperatures Lecture 31: Stable Isotope Applications II: Assimilation-Fractional Crystallization Lecture 32: Stable Isotope Applications III: Assimilation and Subduction Lecture 33: Hydrothermal Activity, Metamorphism and Ore Deposits I Lecture 34: Hydrothermal Activity, Metamorphism and Ore Deposits II Lecture 35: Stable Isotopes in Paleontology and Archaeology Lecture 36: Stable Isotopes in Paleoclimatology I Lecture 37: Stable Isotopes in Paleoclimatology II Lecture 38: The Carbon Cycle, Isotopes, and Climate I Lecture 39: The Carbon Cycle, Isotopes, and Climate II Lecture 40: Mass Independent Fractionation; Li and B isotopes n Comments to W. M. White wmw 4@cornell. edu
 ОСНОВИ ІЗОТОПНОЇ ГЕОХІМІЇ С. Є. Шнюков Лекція 2 Нукліди: Систематика, поширеність та геохімічне значення
ОСНОВИ ІЗОТОПНОЇ ГЕОХІМІЇ С. Є. Шнюков Лекція 2 Нукліди: Систематика, поширеність та геохімічне значення
 Атом: визначення Схематичне зображення атома гелію з електронною хмарою навколо і складним за будовою ядром А том (від грец. άτομοσ — неподільний, лат. відповідник - individuum) — найменша частинка хімічного елементу, яка зберігає всі його хімічні властивості. Атом складається з щільного ядра з позитивно заряджених протонів та електрично нейтральних нейтронів, яке оточене набагато більшою хмарою негативно заряджених електронів. Коли число протонів відповідає числу електронів, атом електрично нейтральний; в іншому випадку це є іон, з певним зарядом. Атоми класифікують відповідно до числа протонів та нейтронів: число протонів визначає хімічний елемент, а число нейтронів визначає ізотоп елементу. В кінці 19 -го та на початку 20 -го столітть, фізики відкрили першу з субатомних частинок — електрон, а дещо пізніше атомне ядро, таким чином показавши, що атом не є неподільний. Розвиток квантової механіки дозволив пояснити не лише будову атомів, а також іхні властивості: оптичні спектри, здатність вступати в реакції й утворювати молекули, тощо.
Атом: визначення Схематичне зображення атома гелію з електронною хмарою навколо і складним за будовою ядром А том (від грец. άτομοσ — неподільний, лат. відповідник - individuum) — найменша частинка хімічного елементу, яка зберігає всі його хімічні властивості. Атом складається з щільного ядра з позитивно заряджених протонів та електрично нейтральних нейтронів, яке оточене набагато більшою хмарою негативно заряджених електронів. Коли число протонів відповідає числу електронів, атом електрично нейтральний; в іншому випадку це є іон, з певним зарядом. Атоми класифікують відповідно до числа протонів та нейтронів: число протонів визначає хімічний елемент, а число нейтронів визначає ізотоп елементу. В кінці 19 -го та на початку 20 -го столітть, фізики відкрили першу з субатомних частинок — електрон, а дещо пізніше атомне ядро, таким чином показавши, що атом не є неподільний. Розвиток квантової механіки дозволив пояснити не лише будову атомів, а також іхні властивості: оптичні спектри, здатність вступати в реакції й утворювати молекули, тощо.
 Атом: історія відкриття та дослідження Поняття атом, як і саме слово, має давньогрецьке походження, хоча істинність гіпотези про існування атомів знайшла своє підтвердження лише в 20 сторіччі. Першим почав проповідувати атомістичне вчення в 5 ст. до н. е філософ Левкіпп. Потім естафету підхопив його учень Демокріт (фото зверху праворуч). Основною ідеєю, яка стояла за даним поняттям протягом всіх сторіч, було уявлення про світ як про набір величезної кількості неподільних елементів, які є дуже простими за своєю структурою і існують від початку часів. Але це була лише ідея, яка дуже довго не знаходила свого експериментального підтвердження. В 17 -му та 18 -му сторіччі хіміки встановили, що хімічні речовини вступають в реакції в певних пропорціях, які виражаються за допомогою малих чисел. Крім того вони виділили певні найпростіші речовини, які назвали хімічними елементами. Ці відкриття призвели до відродження та розвитку ідеї про неподільні частинки. Але тільки в 19 столітті Джон Дальтон (1808 р. ) одержав свідчення існування атомів, але припускав, що вони неподільні. Ернест Резерфорд (1911) показав експериментально, що атом складається з ядра, оточеного електронами.
Атом: історія відкриття та дослідження Поняття атом, як і саме слово, має давньогрецьке походження, хоча істинність гіпотези про існування атомів знайшла своє підтвердження лише в 20 сторіччі. Першим почав проповідувати атомістичне вчення в 5 ст. до н. е філософ Левкіпп. Потім естафету підхопив його учень Демокріт (фото зверху праворуч). Основною ідеєю, яка стояла за даним поняттям протягом всіх сторіч, було уявлення про світ як про набір величезної кількості неподільних елементів, які є дуже простими за своєю структурою і існують від початку часів. Але це була лише ідея, яка дуже довго не знаходила свого експериментального підтвердження. В 17 -му та 18 -му сторіччі хіміки встановили, що хімічні речовини вступають в реакції в певних пропорціях, які виражаються за допомогою малих чисел. Крім того вони виділили певні найпростіші речовини, які назвали хімічними елементами. Ці відкриття призвели до відродження та розвитку ідеї про неподільні частинки. Але тільки в 19 столітті Джон Дальтон (1808 р. ) одержав свідчення існування атомів, але припускав, що вони неподільні. Ернест Резерфорд (1911) показав експериментально, що атом складається з ядра, оточеного електронами.
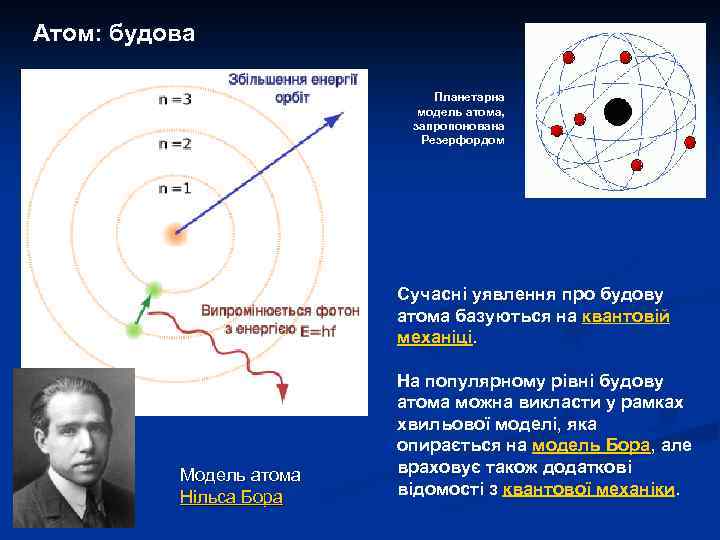 Атом: будова Планетарна модель атома, запропонована Резерфордом Сучасні уявлення про будову атома базуються на квантовій механіці. Модель атома Нільса Бора На популярному рівні будову атома можна викласти у рамках хвильової моделі, яка опирається на модель Бора, але враховує також додаткові відомості з квантової механіки.
Атом: будова Планетарна модель атома, запропонована Резерфордом Сучасні уявлення про будову атома базуються на квантовій механіці. Модель атома Нільса Бора На популярному рівні будову атома можна викласти у рамках хвильової моделі, яка опирається на модель Бора, але враховує також додаткові відомості з квантової механіки.
 Атом: електронна конфігурація Ядро оточене електронною хмарою, яка займає більшу частину його об'єму. В електронній хмарі можна виділити оболонки, для кожної з яких існує кілька можливих орбіталей. Заповнені орбіталі складають електронну конфігурацію, індивідуальну для кожного хімічного елемента. Схематичне зображення електронної конфігурації Ba Електронна конфігурація — формула розташування електронів на різних електронних оболонках атома хімічного елемента. З погляду квантової механіки, електронна конфігурація - це повний перелік одноелектронних хвильових функцій, із яких можна скласти повну хвильову функцію атома. Електронна конфігурація атома значною мірою визначає його хімічні властивості. Для позначення електронної конфігурації хімічного елементу використовують назви орбіталей: s, p, d, f, g. Перед назвою орбіталі стоїть основне квантове число, а верхній індекс після позначення орбіталі вказує на те, скільки електронів є на орбіталях даного сорту. Наприклад, для неону електронна конфігурація записується 1 s 22 p 6. Цей запис означає, що неон має два електрони на внутрішній s-орбіталі, 2 електрони на зовнішній s-орбіталі й 6 електронів на зовнішній p-орбіталі.
Атом: електронна конфігурація Ядро оточене електронною хмарою, яка займає більшу частину його об'єму. В електронній хмарі можна виділити оболонки, для кожної з яких існує кілька можливих орбіталей. Заповнені орбіталі складають електронну конфігурацію, індивідуальну для кожного хімічного елемента. Схематичне зображення електронної конфігурації Ba Електронна конфігурація — формула розташування електронів на різних електронних оболонках атома хімічного елемента. З погляду квантової механіки, електронна конфігурація - це повний перелік одноелектронних хвильових функцій, із яких можна скласти повну хвильову функцію атома. Електронна конфігурація атома значною мірою визначає його хімічні властивості. Для позначення електронної конфігурації хімічного елементу використовують назви орбіталей: s, p, d, f, g. Перед назвою орбіталі стоїть основне квантове число, а верхній індекс після позначення орбіталі вказує на те, скільки електронів є на орбіталях даного сорту. Наприклад, для неону електронна конфігурація записується 1 s 22 p 6. Цей запис означає, що неон має два електрони на внутрішній s-орбіталі, 2 електрони на зовнішній s-орбіталі й 6 електронів на зовнішній p-орбіталі.
 Атом: електронні конфігурації Кожна орбіталь може містити до двох електронів, що характеризуються трьома квантовими числами: основним (n = 1, 2…), орбітальним (l =0, 1, 2 … n-1), магнітним (m = 0, +1, +2 … +l ). Кожен електрон на орбіталі має унікальне значення четвертого квантового числа: спіну (ms = +1/2) Орбіталі визначаються специфічним розподілом ймовірності знаходження електрону. «Границею» орбіталі вважається відстань, на якій імовірність того що електрон може перебувати поза нею є меншою 90 %. Кожна орбиталь не може містити більше ніж 2 електрони з однаковим набіром трьох квантових чисел. Їх спіни повинні бути протилежними (принцип Паулі) Для позначення електронної конфігурації хімічного елементу використовують назви орбіталей: s, p, d, f, g (n = 1, 2…) Атоми можуть віддавати та приєднувати електрони, стаючи позитивно або негативно зарядженими іонами. Лише електрони зовнішньої оболонки можуть брати участь в утворенні міжатомних зв'язків. Хімічні властивості елемента визначаються тим, з якою легкістю ядро може віддавати або здобувати електрони. Це залежить як від числа електронів так і від ступеня заповненості зовнішньої оболонки.
Атом: електронні конфігурації Кожна орбіталь може містити до двох електронів, що характеризуються трьома квантовими числами: основним (n = 1, 2…), орбітальним (l =0, 1, 2 … n-1), магнітним (m = 0, +1, +2 … +l ). Кожен електрон на орбіталі має унікальне значення четвертого квантового числа: спіну (ms = +1/2) Орбіталі визначаються специфічним розподілом ймовірності знаходження електрону. «Границею» орбіталі вважається відстань, на якій імовірність того що електрон може перебувати поза нею є меншою 90 %. Кожна орбиталь не може містити більше ніж 2 електрони з однаковим набіром трьох квантових чисел. Їх спіни повинні бути протилежними (принцип Паулі) Для позначення електронної конфігурації хімічного елементу використовують назви орбіталей: s, p, d, f, g (n = 1, 2…) Атоми можуть віддавати та приєднувати електрони, стаючи позитивно або негативно зарядженими іонами. Лише електрони зовнішньої оболонки можуть брати участь в утворенні міжатомних зв'язків. Хімічні властивості елемента визначаються тим, з якою легкістю ядро може віддавати або здобувати електрони. Це залежить як від числа електронів так і від ступеня заповненості зовнішньої оболонки.
 Атом: електронні конфігурації Електро нна оболо нка — група вироджених або близьких за енергією електронних орбіталей атома. За принципом Паули , на кожній із оболонок може розташовуватися лише певне число електронів = 2 n 2, а емність кожної підоболонки — 2(2 l + 1). Из вышеприведённой схемы легко определяются ёмкости последовательных периодов: 2, 8, 8, 18, 32. . . Розрізняють внутрішні й зовнішні (валентні) електронні оболонки. Внутрішні оболонки відповідають за спектри рентгенівського випромінювання та спектри рентгенівського поглинання атомів. Зовнішні оболонки відповідають за хімічні властивості атома. Облолонки бувають заповненими, незаповненими та частково заповненими.
Атом: електронні конфігурації Електро нна оболо нка — група вироджених або близьких за енергією електронних орбіталей атома. За принципом Паули , на кожній із оболонок може розташовуватися лише певне число електронів = 2 n 2, а емність кожної підоболонки — 2(2 l + 1). Из вышеприведённой схемы легко определяются ёмкости последовательных периодов: 2, 8, 8, 18, 32. . . Розрізняють внутрішні й зовнішні (валентні) електронні оболонки. Внутрішні оболонки відповідають за спектри рентгенівського випромінювання та спектри рентгенівського поглинання атомів. Зовнішні оболонки відповідають за хімічні властивості атома. Облолонки бувають заповненими, незаповненими та частково заповненими.
 Атом: періодичний закон Д. І. Менделеєва Периодический закон Менделеева, фундаментальный закон, устанавливающий периодическое изменение свойств химических элементов в зависимости от увеличения зарядов ядер их атомов. Открыт Д. И. Менделеевым в 1869 при сопоставлении свойств всех известных в то время элементов и величин их атомных весов. Графическим (табличным) выражением П. з. явилась разработанная Менделеевым периодическая система элементов. Физический смысл П. з. был вскрыт лишь после выяснения того, что заряд ядра атома возрастает при переходе от одного химического элемента к соседнему (в периодической системе) на единицу элементарного заряда. Численно заряд ядра равен порядковому номеру (Z) соответствующего элемента в периодической системе, то есть числу протонов в ядре, в свою очередь равному числу электронов соответствующего нейтрального атома. Химические свойства атомов определяются структурой их внешних электронных оболочек, периодически изменяющейся с увеличением заряда ядра, и, следовательно, в основе П. з. лежит представление об изменении заряда ядра атомов, а не атомной массы элементов. Наглядная иллюстрация П. з. — кривые периодические изменения некоторых физических величин (ионизационных потенциалов, атомных радиусов, атомных объёмов) в зависимости от Z. Какого-либо общего математического выражения П. з. не существует.
Атом: періодичний закон Д. І. Менделеєва Периодический закон Менделеева, фундаментальный закон, устанавливающий периодическое изменение свойств химических элементов в зависимости от увеличения зарядов ядер их атомов. Открыт Д. И. Менделеевым в 1869 при сопоставлении свойств всех известных в то время элементов и величин их атомных весов. Графическим (табличным) выражением П. з. явилась разработанная Менделеевым периодическая система элементов. Физический смысл П. з. был вскрыт лишь после выяснения того, что заряд ядра атома возрастает при переходе от одного химического элемента к соседнему (в периодической системе) на единицу элементарного заряда. Численно заряд ядра равен порядковому номеру (Z) соответствующего элемента в периодической системе, то есть числу протонов в ядре, в свою очередь равному числу электронов соответствующего нейтрального атома. Химические свойства атомов определяются структурой их внешних электронных оболочек, периодически изменяющейся с увеличением заряда ядра, и, следовательно, в основе П. з. лежит представление об изменении заряда ядра атомов, а не атомной массы элементов. Наглядная иллюстрация П. з. — кривые периодические изменения некоторых физических величин (ионизационных потенциалов, атомных радиусов, атомных объёмов) в зависимости от Z. Какого-либо общего математического выражения П. з. не существует.
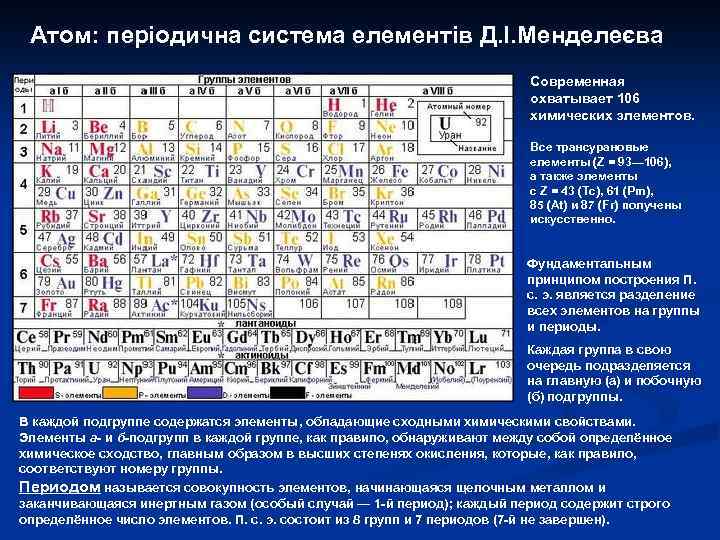 Атом: періодична система елементів Д. І. Менделеєва Современная охватывает 106 химических элементов. Все трансурановые елементы (Z = 93— 106), а также элементы с Z = 43 (Tc), 61 (Pm), 85 (At) и 87 (Fr) получены искусственно. Фундаментальным принципом построения П. с. э. является разделение всех элементов на группы и периоды. Каждая группа в свою очередь подразделяется на главную (а) и побочную (б) подгруппы. В каждой подгруппе содержатся элементы, обладающие сходными химическими свойствами. Элементы а- и б-подгрупп в каждой группе, как правило, обнаруживают между собой определённое химическое сходство, главным образом в высших степенях окисления, которые, как правило, соответствуют номеру группы. Периодом называется совокупность элементов, начинающаяся щелочным металлом и заканчивающаяся инертным газом (особый случай — 1 -й период); каждый период содержит строго определённое число элементов. П. с. э. состоит из 8 групп и 7 периодов (7 -й не завершен).
Атом: періодична система елементів Д. І. Менделеєва Современная охватывает 106 химических элементов. Все трансурановые елементы (Z = 93— 106), а также элементы с Z = 43 (Tc), 61 (Pm), 85 (At) и 87 (Fr) получены искусственно. Фундаментальным принципом построения П. с. э. является разделение всех элементов на группы и периоды. Каждая группа в свою очередь подразделяется на главную (а) и побочную (б) подгруппы. В каждой подгруппе содержатся элементы, обладающие сходными химическими свойствами. Элементы а- и б-подгрупп в каждой группе, как правило, обнаруживают между собой определённое химическое сходство, главным образом в высших степенях окисления, которые, как правило, соответствуют номеру группы. Периодом называется совокупность элементов, начинающаяся щелочным металлом и заканчивающаяся инертным газом (особый случай — 1 -й период); каждый период содержит строго определённое число элементов. П. с. э. состоит из 8 групп и 7 периодов (7 -й не завершен).
 Атом: періодична система елементів Д. І. Менделеєва Современная охватывает 106 химических элементов. Все трансурановые елементы (Z = 93— 106), а также элементы с Z = 43 (Tc), 61 (Pm), 85 (At) и 87 (Fr) получены искусственно. Фундаментальным принципом построения П. с. э. является разделение всех элементов на группы и периоды. Каждая группа в свою очередь подразделяется на главную (а) и побочную (б) подгруппы. Первый период содержит всего 2 элемента: H и He. Место H в системе неоднозначно: поскольку он проявляет свойства, общие со щелочными металлами и с галогенами, его помещают либо в Ia-, либо (предпочтительнее) в VIIa-подгруппу. Гелий — первый представитель VIIa-подгруппы (однако долгое время Не и все инертные газы объединяли в самостоятельную нулевую группу).
Атом: періодична система елементів Д. І. Менделеєва Современная охватывает 106 химических элементов. Все трансурановые елементы (Z = 93— 106), а также элементы с Z = 43 (Tc), 61 (Pm), 85 (At) и 87 (Fr) получены искусственно. Фундаментальным принципом построения П. с. э. является разделение всех элементов на группы и периоды. Каждая группа в свою очередь подразделяется на главную (а) и побочную (б) подгруппы. Первый период содержит всего 2 элемента: H и He. Место H в системе неоднозначно: поскольку он проявляет свойства, общие со щелочными металлами и с галогенами, его помещают либо в Ia-, либо (предпочтительнее) в VIIa-подгруппу. Гелий — первый представитель VIIa-подгруппы (однако долгое время Не и все инертные газы объединяли в самостоятельную нулевую группу).
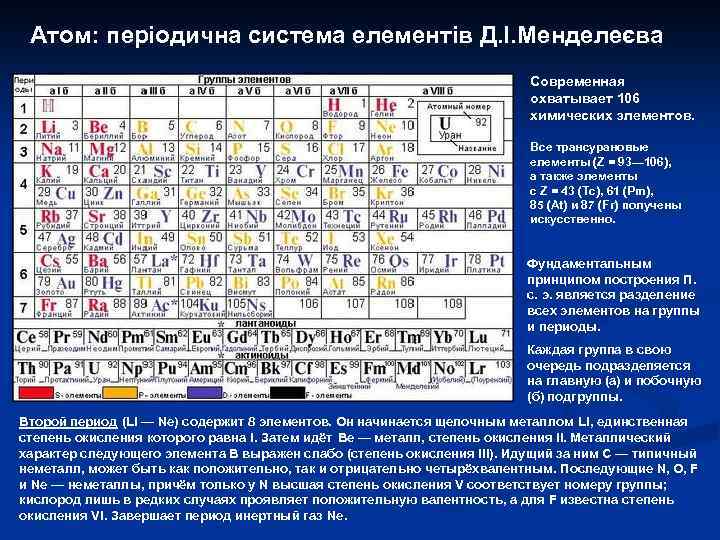 Атом: періодична система елементів Д. І. Менделеєва Современная охватывает 106 химических элементов. Все трансурановые елементы (Z = 93— 106), а также элементы с Z = 43 (Tc), 61 (Pm), 85 (At) и 87 (Fr) получены искусственно. Фундаментальным принципом построения П. с. э. является разделение всех элементов на группы и периоды. Каждая группа в свою очередь подразделяется на главную (а) и побочную (б) подгруппы. Второй период (Li — Ne) содержит 8 элементов. Он начинается щелочным металлом Li, единственная степень окисления которого равна I. Затем идёт Be — металл, степень окисления II. Металлический характер следующего элемента В выражен слабо (степень окисления III). Идущий за ним C — типичный неметалл, может быть как положительно, так и отрицательно четырёхвалентным. Последующие N, O, F и Ne — неметаллы, причём только у N высшая степень окисления V соответствует номеру группы; кислород лишь в редких случаях проявляет положительную валентность, а для F известна степень окисления VI. Завершает период инертный газ Ne.
Атом: періодична система елементів Д. І. Менделеєва Современная охватывает 106 химических элементов. Все трансурановые елементы (Z = 93— 106), а также элементы с Z = 43 (Tc), 61 (Pm), 85 (At) и 87 (Fr) получены искусственно. Фундаментальным принципом построения П. с. э. является разделение всех элементов на группы и периоды. Каждая группа в свою очередь подразделяется на главную (а) и побочную (б) подгруппы. Второй период (Li — Ne) содержит 8 элементов. Он начинается щелочным металлом Li, единственная степень окисления которого равна I. Затем идёт Be — металл, степень окисления II. Металлический характер следующего элемента В выражен слабо (степень окисления III). Идущий за ним C — типичный неметалл, может быть как положительно, так и отрицательно четырёхвалентным. Последующие N, O, F и Ne — неметаллы, причём только у N высшая степень окисления V соответствует номеру группы; кислород лишь в редких случаях проявляет положительную валентность, а для F известна степень окисления VI. Завершает период инертный газ Ne.
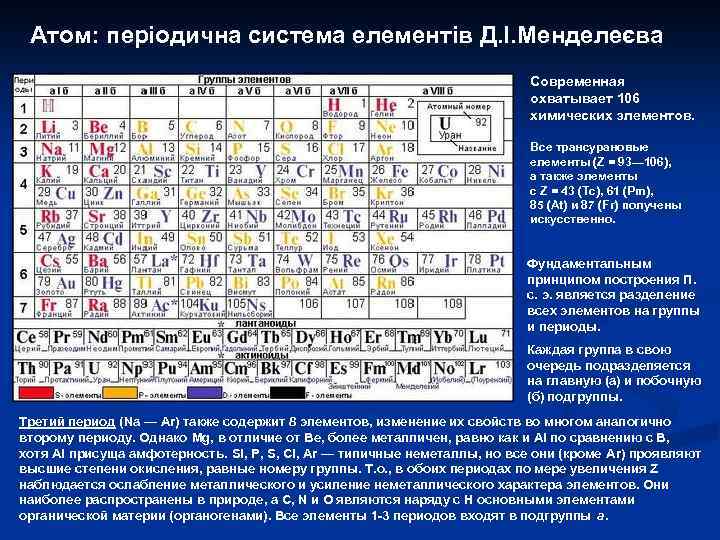 Атом: періодична система елементів Д. І. Менделеєва Современная охватывает 106 химических элементов. Все трансурановые елементы (Z = 93— 106), а также элементы с Z = 43 (Tc), 61 (Pm), 85 (At) и 87 (Fr) получены искусственно. Фундаментальным принципом построения П. с. э. является разделение всех элементов на группы и периоды. Каждая группа в свою очередь подразделяется на главную (а) и побочную (б) подгруппы. Третий период (Na — Ar) также содержит 8 элементов, изменение их свойств во многом аналогично второму периоду. Однако Mg, в отличие от Be, более металличен, равно как и Al по сравнению с В, хотя Al присуща амфотерность. Si, Р, S, Cl, Ar — типичные неметаллы, но все они (кроме Ar) проявляют высшие степени окисления, равные номеру группы. Т. о. , в обоих периодах по мере увеличения Z наблюдается ослабление металлического и усиление неметаллического характера элементов. Они наиболее распространены в природе, а С, N и O являются наряду с H основными элементами органической материи (органогенами). Все элементы 1 -3 периодов входят в подгруппы а.
Атом: періодична система елементів Д. І. Менделеєва Современная охватывает 106 химических элементов. Все трансурановые елементы (Z = 93— 106), а также элементы с Z = 43 (Tc), 61 (Pm), 85 (At) и 87 (Fr) получены искусственно. Фундаментальным принципом построения П. с. э. является разделение всех элементов на группы и периоды. Каждая группа в свою очередь подразделяется на главную (а) и побочную (б) подгруппы. Третий период (Na — Ar) также содержит 8 элементов, изменение их свойств во многом аналогично второму периоду. Однако Mg, в отличие от Be, более металличен, равно как и Al по сравнению с В, хотя Al присуща амфотерность. Si, Р, S, Cl, Ar — типичные неметаллы, но все они (кроме Ar) проявляют высшие степени окисления, равные номеру группы. Т. о. , в обоих периодах по мере увеличения Z наблюдается ослабление металлического и усиление неметаллического характера элементов. Они наиболее распространены в природе, а С, N и O являются наряду с H основными элементами органической материи (органогенами). Все элементы 1 -3 периодов входят в подгруппы а.
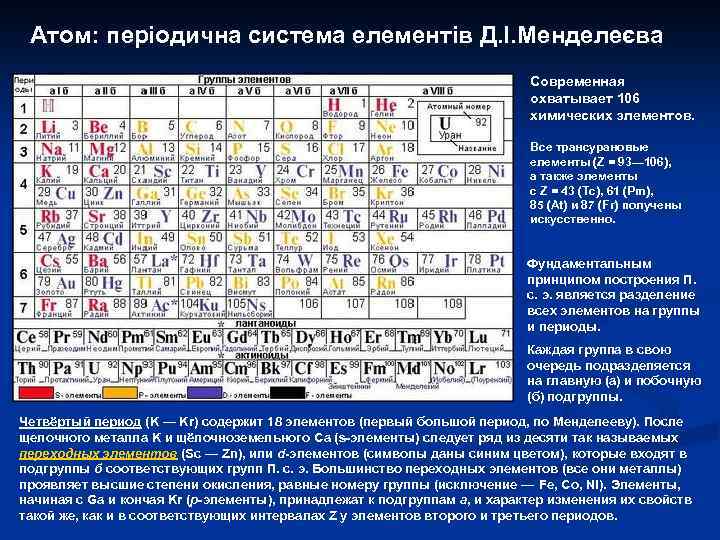 Атом: періодична система елементів Д. І. Менделеєва Современная охватывает 106 химических элементов. Все трансурановые елементы (Z = 93— 106), а также элементы с Z = 43 (Tc), 61 (Pm), 85 (At) и 87 (Fr) получены искусственно. Фундаментальным принципом построения П. с. э. является разделение всех элементов на группы и периоды. Каждая группа в свою очередь подразделяется на главную (а) и побочную (б) подгруппы. Четвёртый период (K — Kr) содержит 18 элементов (первый большой период, по Менделееву). После щелочного металла K и щёлочноземельного Ca (s-элементы) следует ряд из десяти так называемых переходных элементов (Sc — Zn), или d-элементов (символы даны синим цветом), которые входят в подгруппы б соответствующих групп П. с. э. Большинство переходных элементов (все они металлы) проявляет высшие степени окисления, равные номеру группы (исключение — Fe, Co, Ni). Элементы, начиная с Ga и кончая Kr (р-элементы), принадлежат к подгруппам а, и характер изменения их свойств такой же, как и в соответствующих интервалах Z у элементов второго и третьего периодов.
Атом: періодична система елементів Д. І. Менделеєва Современная охватывает 106 химических элементов. Все трансурановые елементы (Z = 93— 106), а также элементы с Z = 43 (Tc), 61 (Pm), 85 (At) и 87 (Fr) получены искусственно. Фундаментальным принципом построения П. с. э. является разделение всех элементов на группы и периоды. Каждая группа в свою очередь подразделяется на главную (а) и побочную (б) подгруппы. Четвёртый период (K — Kr) содержит 18 элементов (первый большой период, по Менделееву). После щелочного металла K и щёлочноземельного Ca (s-элементы) следует ряд из десяти так называемых переходных элементов (Sc — Zn), или d-элементов (символы даны синим цветом), которые входят в подгруппы б соответствующих групп П. с. э. Большинство переходных элементов (все они металлы) проявляет высшие степени окисления, равные номеру группы (исключение — Fe, Co, Ni). Элементы, начиная с Ga и кончая Kr (р-элементы), принадлежат к подгруппам а, и характер изменения их свойств такой же, как и в соответствующих интервалах Z у элементов второго и третьего периодов.
 Атом: періодична система елементів Д. І. Менделеєва Современная охватывает 106 химических элементов. Все трансурановые елементы (Z = 93— 106), а также элементы с Z = 43 (Tc), 61 (Pm), 85 (At) и 87 (Fr) получены искусственно. Фундаментальным принципом построения П. с. э. является разделение всех элементов на группы и периоды. Каждая группа в свою очередь подразделяется на главную (а) и побочную (б) подгруппы. Пятый период (Rb — Xe) построен аналогично четвёртому; в нём также имеется вставка из 10 переходных элементов (Y — Cd), d-элементов. Специфические особенности периода: 1) в триаде Ru — Rh — Pd только рутений проявляет степень окисления VIII; 2) все элементы подгрупп а проявляют высшие степени окисления, равные номеру группы; 3) у I отмечаются слабые металлические свойства. Таким образом, характер изменения свойств по мере увеличения Z у элементов четвёртого и пятого периодов более сложен (металлические свойства сохраняются в большом интервале Z).
Атом: періодична система елементів Д. І. Менделеєва Современная охватывает 106 химических элементов. Все трансурановые елементы (Z = 93— 106), а также элементы с Z = 43 (Tc), 61 (Pm), 85 (At) и 87 (Fr) получены искусственно. Фундаментальным принципом построения П. с. э. является разделение всех элементов на группы и периоды. Каждая группа в свою очередь подразделяется на главную (а) и побочную (б) подгруппы. Пятый период (Rb — Xe) построен аналогично четвёртому; в нём также имеется вставка из 10 переходных элементов (Y — Cd), d-элементов. Специфические особенности периода: 1) в триаде Ru — Rh — Pd только рутений проявляет степень окисления VIII; 2) все элементы подгрупп а проявляют высшие степени окисления, равные номеру группы; 3) у I отмечаются слабые металлические свойства. Таким образом, характер изменения свойств по мере увеличения Z у элементов четвёртого и пятого периодов более сложен (металлические свойства сохраняются в большом интервале Z).
 Атом: періодична система елементів Д. І. Менделеєва Современная охватывает 106 химических элементов. Все трансурановые елементы (Z = 93— 106), а также элементы с Z = 43 (Tc), 61 (Pm), 85 (At) и 87 (Fr) получены искусственно. Фундаментальным принципом построения П. с. э. является разделение всех элементов на группы и периоды. Каждая группа в свою очередь подразделяется на главную (а) и побочную (б) подгруппы. Шестой период (Cs — Rn) включает 32 элемента. В нём помимо 10 d-элементов (La, Hf — Hg) содержится совокупность из 14 f-элементов, лантаноидов, от Ce до Lu (символы чёрного цвета). Элементы от La до Lu химически весьма сходны. Особенности периода: 1) в триаде Os — Ir — Pt только осмий проявляет степень окисления VIII; 2) At имеет более выраженный (по сравнению с 1) металлический характер; 3) Rn, по-видимому (его химия мало изучена), должен быть наиболее реакционноспособным из инертных газов.
Атом: періодична система елементів Д. І. Менделеєва Современная охватывает 106 химических элементов. Все трансурановые елементы (Z = 93— 106), а также элементы с Z = 43 (Tc), 61 (Pm), 85 (At) и 87 (Fr) получены искусственно. Фундаментальным принципом построения П. с. э. является разделение всех элементов на группы и периоды. Каждая группа в свою очередь подразделяется на главную (а) и побочную (б) подгруппы. Шестой период (Cs — Rn) включает 32 элемента. В нём помимо 10 d-элементов (La, Hf — Hg) содержится совокупность из 14 f-элементов, лантаноидов, от Ce до Lu (символы чёрного цвета). Элементы от La до Lu химически весьма сходны. Особенности периода: 1) в триаде Os — Ir — Pt только осмий проявляет степень окисления VIII; 2) At имеет более выраженный (по сравнению с 1) металлический характер; 3) Rn, по-видимому (его химия мало изучена), должен быть наиболее реакционноспособным из инертных газов.
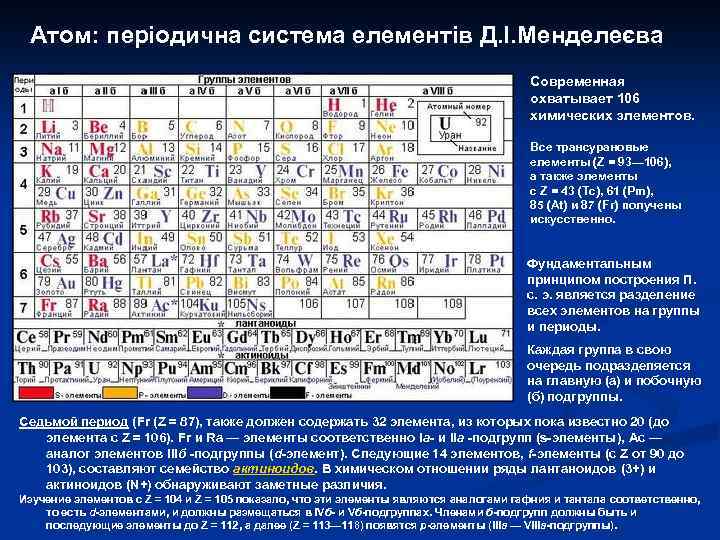 Атом: періодична система елементів Д. І. Менделеєва Современная охватывает 106 химических элементов. Все трансурановые елементы (Z = 93— 106), а также элементы с Z = 43 (Tc), 61 (Pm), 85 (At) и 87 (Fr) получены искусственно. Фундаментальным принципом построения П. с. э. является разделение всех элементов на группы и периоды. Каждая группа в свою очередь подразделяется на главную (а) и побочную (б) подгруппы. Седьмой период (Fr (Z = 87), также должен содержать 32 элемента, из которых пока известно 20 (до элемента с Z = 106). Fr и Ra — элементы соответственно Ia- и IIa -подгрупп (s-элементы), Ac — аналог элементов IIIб -подгруппы (d-элемент). Следующие 14 элементов, f-элементы (с Z от 90 до 103), составляют семейство актиноидов. В химическом отношении ряды лантаноидов (3+) и актиноидов (N+) обнаруживают заметные различия. Изучение элементов с Z = 104 и Z = 105 показало, что эти элементы являются аналогами гафния и тантала соответственно, то есть d-элементами, и должны размещаться в IVб- и Vб-подгруппах. Членами б-подгрупп должны быть и последующие элементы до Z = 112, а далее (Z = 113— 118) появятся р-элементы (IIIa — VIlla-подгруппы).
Атом: періодична система елементів Д. І. Менделеєва Современная охватывает 106 химических элементов. Все трансурановые елементы (Z = 93— 106), а также элементы с Z = 43 (Tc), 61 (Pm), 85 (At) и 87 (Fr) получены искусственно. Фундаментальным принципом построения П. с. э. является разделение всех элементов на группы и периоды. Каждая группа в свою очередь подразделяется на главную (а) и побочную (б) подгруппы. Седьмой период (Fr (Z = 87), также должен содержать 32 элемента, из которых пока известно 20 (до элемента с Z = 106). Fr и Ra — элементы соответственно Ia- и IIa -подгрупп (s-элементы), Ac — аналог элементов IIIб -подгруппы (d-элемент). Следующие 14 элементов, f-элементы (с Z от 90 до 103), составляют семейство актиноидов. В химическом отношении ряды лантаноидов (3+) и актиноидов (N+) обнаруживают заметные различия. Изучение элементов с Z = 104 и Z = 105 показало, что эти элементы являются аналогами гафния и тантала соответственно, то есть d-элементами, и должны размещаться в IVб- и Vб-подгруппах. Членами б-подгрупп должны быть и последующие элементы до Z = 112, а далее (Z = 113— 118) появятся р-элементы (IIIa — VIlla-подгруппы).
 Атом: періодична система елементів Д. І. Менделеєва В основе теории П. с. э. лежит представление о специфических закономерностях построения электронных оболочек (слоев, уровней) и подоболочек (подуровней) в атомах по мере роста Z. Нильс Бор (1913 -21) выявил три особенности формирования электронных конфигураций атомов: 1) заполнение электронных оболочек (кроме оболочек, отвечающих значениям главного квантового числа n = 1 и 2) происходит не монотонно до полной их ёмкости, а прерывается появлением совокупностей электронов, относящихся к оболочкам с большими значениями n; 2) сходные типы электронных конфигураций атомов периодически повторяются; 3) границы периодов (за исключением первого и второго) не совпадают с границами последовательных электронных оболочек. Реальная схема формирования электронных конфигураций атомов по мере роста Z может быть в общем виде записана следующим образом: Вертикальными чертами разделены периоды П. с. э. (их номера обозначены цифрами наверху); жирным шрифтом выделены подоболочки, которыми завершается построение оболочек с данным n. Под обозначениями подоболочек проставлены значения главного (n) и орбитального (l) квантовых чисел, характеризующие последовательно заполняющиеся подоболочки.
Атом: періодична система елементів Д. І. Менделеєва В основе теории П. с. э. лежит представление о специфических закономерностях построения электронных оболочек (слоев, уровней) и подоболочек (подуровней) в атомах по мере роста Z. Нильс Бор (1913 -21) выявил три особенности формирования электронных конфигураций атомов: 1) заполнение электронных оболочек (кроме оболочек, отвечающих значениям главного квантового числа n = 1 и 2) происходит не монотонно до полной их ёмкости, а прерывается появлением совокупностей электронов, относящихся к оболочкам с большими значениями n; 2) сходные типы электронных конфигураций атомов периодически повторяются; 3) границы периодов (за исключением первого и второго) не совпадают с границами последовательных электронных оболочек. Реальная схема формирования электронных конфигураций атомов по мере роста Z может быть в общем виде записана следующим образом: Вертикальными чертами разделены периоды П. с. э. (их номера обозначены цифрами наверху); жирным шрифтом выделены подоболочки, которыми завершается построение оболочек с данным n. Под обозначениями подоболочек проставлены значения главного (n) и орбитального (l) квантовых чисел, характеризующие последовательно заполняющиеся подоболочки.
 Атом: періодична система елементів Д. І. Менделеєва В соответствии с принципом Паули ёмкость каждой электронной оболочки равна 2 n 2, а ёмкость каждой подоболочки — 2(2 l + 1). Из вышеприведённой схемы легко определяются ёмкости последовательных периодов: 2, 8, 8, 18, 32. . . Каждый период начинается элементом, в атоме которого появляется электрон с новым значением n. Таким образом, периоды можно характеризовать как совокупности элементов, начинающиеся элементом со значением n, равным номеру периода, и l = 0 (ns 1 -элементы), и завершающиеся элементом с тем же n и l = 1 (np 6 -элементы); исключение — первый период, содержащий только lsэлементы. При этом к а-подгруппам принадлежат элементы, для атомов которых n равно номеру периода, а l = 0 или 1, то есть происходит построение электронной оболочки с данным n. К б-подгруппам принадлежат элементы, в атомах которых происходит достройка оболочек, остававшихся незавершёнными (в данном случае n меньше номера периода, а l = 2 или 3). Первый — третий периоды П. с. э. содержат только элементы а-подгрупп. Приведённая реальная схема формирования электронных конфигураций атомов не является безупречной, поскольку в ряде случаев чёткие границы между последовательно заполняющимися подоболочками нарушаются (например, после заполнения в атомах Cs и Ba 6 s-подоболочки в атоме лантана появляется не 4 f-, а 5 d-электрон, имеется 5 d-электрон в атоме Gd и т. д. ). Кроме того, первоначально реальная схема не могла быть выведена из каких-либо фундаментальных физических представлений; такой вывод стал возможным благодаря применению квантовой механики к проблеме строения атома.
Атом: періодична система елементів Д. І. Менделеєва В соответствии с принципом Паули ёмкость каждой электронной оболочки равна 2 n 2, а ёмкость каждой подоболочки — 2(2 l + 1). Из вышеприведённой схемы легко определяются ёмкости последовательных периодов: 2, 8, 8, 18, 32. . . Каждый период начинается элементом, в атоме которого появляется электрон с новым значением n. Таким образом, периоды можно характеризовать как совокупности элементов, начинающиеся элементом со значением n, равным номеру периода, и l = 0 (ns 1 -элементы), и завершающиеся элементом с тем же n и l = 1 (np 6 -элементы); исключение — первый период, содержащий только lsэлементы. При этом к а-подгруппам принадлежат элементы, для атомов которых n равно номеру периода, а l = 0 или 1, то есть происходит построение электронной оболочки с данным n. К б-подгруппам принадлежат элементы, в атомах которых происходит достройка оболочек, остававшихся незавершёнными (в данном случае n меньше номера периода, а l = 2 или 3). Первый — третий периоды П. с. э. содержат только элементы а-подгрупп. Приведённая реальная схема формирования электронных конфигураций атомов не является безупречной, поскольку в ряде случаев чёткие границы между последовательно заполняющимися подоболочками нарушаются (например, после заполнения в атомах Cs и Ba 6 s-подоболочки в атоме лантана появляется не 4 f-, а 5 d-электрон, имеется 5 d-электрон в атоме Gd и т. д. ). Кроме того, первоначально реальная схема не могла быть выведена из каких-либо фундаментальных физических представлений; такой вывод стал возможным благодаря применению квантовой механики к проблеме строения атома.
 Атом: періодична система елементів Д. І. Менделеєва Закон Мозли Экспериментально установлен Г. Мозли (1913). Согласно этому закону корень квадратный из частоты (ν) спектральной линии характеристического рентгеновского излучения элемента есть линейная функция его порядкового номера (Z): где R — постоянная Ридберга, Sn — постоянная экранирования, n — главное квантовое число. На диаграмме Мозли (см. рис. ) зависимость от Z представляет собой ряд прямых (К-, L-, М- и т. д. серии, соответствующие значениям n = 1, 2, 3, . . . ). Неопровержимое доказательство правильности размещения элементов в периодической системе элементов Д. И. Менделеева. Содействовал выяснению физического смысла Z. В соответствии с М. з. , рентгеновские характеристические спектры не обнаруживают периодических закономерностей, присущих оптическим спектрам (определяются внешними электронными оболочками). Это указывает на то, что проявляющиеся в характеристических рентгеновских спектрах внутренние электронные оболочки атомов всех элементов имеют аналогичное строение.
Атом: періодична система елементів Д. І. Менделеєва Закон Мозли Экспериментально установлен Г. Мозли (1913). Согласно этому закону корень квадратный из частоты (ν) спектральной линии характеристического рентгеновского излучения элемента есть линейная функция его порядкового номера (Z): где R — постоянная Ридберга, Sn — постоянная экранирования, n — главное квантовое число. На диаграмме Мозли (см. рис. ) зависимость от Z представляет собой ряд прямых (К-, L-, М- и т. д. серии, соответствующие значениям n = 1, 2, 3, . . . ). Неопровержимое доказательство правильности размещения элементов в периодической системе элементов Д. И. Менделеева. Содействовал выяснению физического смысла Z. В соответствии с М. з. , рентгеновские характеристические спектры не обнаруживают периодических закономерностей, присущих оптическим спектрам (определяются внешними электронными оболочками). Это указывает на то, что проявляющиеся в характеристических рентгеновских спектрах внутренние электронные оболочки атомов всех элементов имеют аналогичное строение.
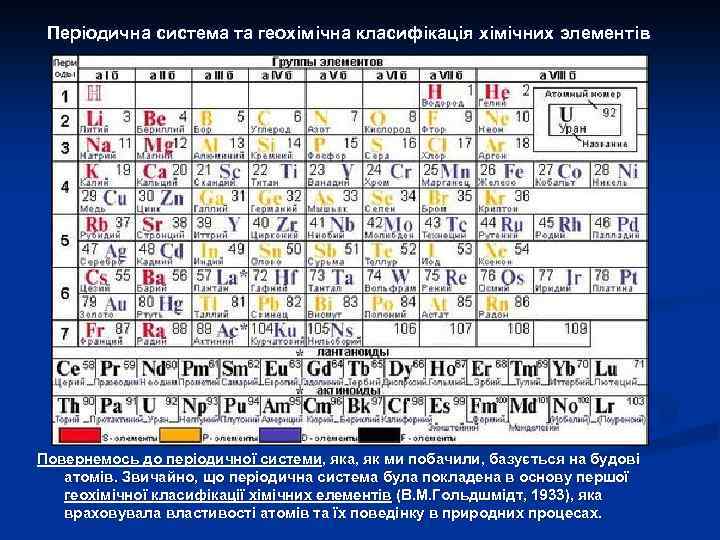 Періодична система та геохімічна класифікація хімічних элементів Повернемось до періодичної системи, яка, як ми побачили, базується на будові атомів. Звичайно, що періодична система була покладена в основу першої геохімічної класифікації хімічних елементів (В. М. Гольдшмідт, 1933), яка враховувала властивості атомів та їх поведінку в природних процесах.
Періодична система та геохімічна класифікація хімічних элементів Повернемось до періодичної системи, яка, як ми побачили, базується на будові атомів. Звичайно, що періодична система була покладена в основу першої геохімічної класифікації хімічних елементів (В. М. Гольдшмідт, 1933), яка враховувала властивості атомів та їх поведінку в природних процесах.
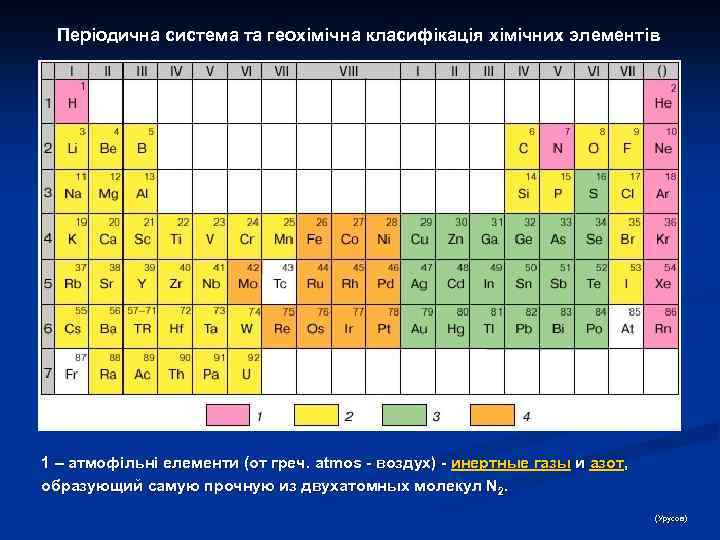 Періодична система та геохімічна класифікація хімічних элементів 1 – атмофільні елементи (от греч. atmos - воздух) - инертные газы и азот, образующий самую прочную из двухатомных молекул N 2. (Урусов)
Періодична система та геохімічна класифікація хімічних элементів 1 – атмофільні елементи (от греч. atmos - воздух) - инертные газы и азот, образующий самую прочную из двухатомных молекул N 2. (Урусов)
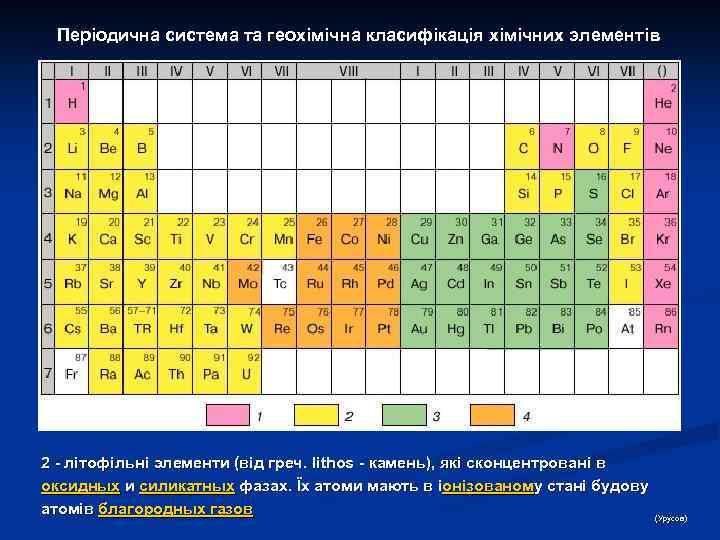 Періодична система та геохімічна класифікація хімічних элементів 2 - літофільні элементи (від греч. lithos - камень), які сконцентровані в оксидных и силикатных фазах. Їх атоми мають в іонізованому стані будову атомів благородных газов (Урусов)
Періодична система та геохімічна класифікація хімічних элементів 2 - літофільні элементи (від греч. lithos - камень), які сконцентровані в оксидных и силикатных фазах. Їх атоми мають в іонізованому стані будову атомів благородных газов (Урусов)
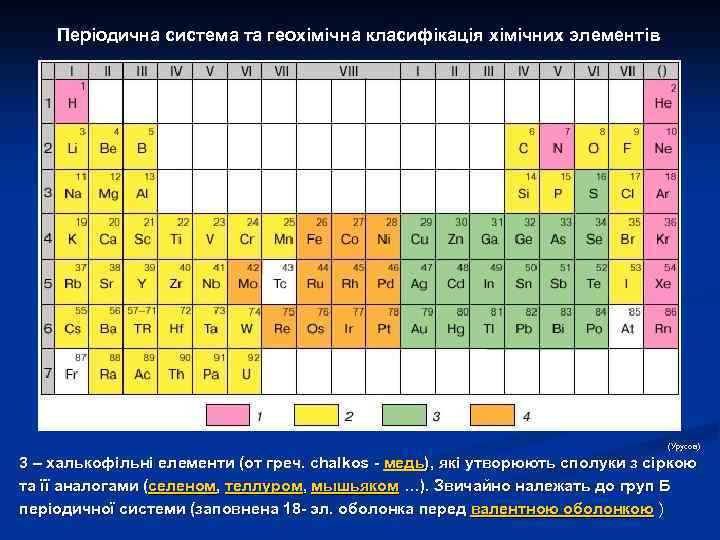 Періодична система та геохімічна класифікація хімічних элементів (Урусов) 3 – халькофільні елементи (от греч. chalkos - медь), які утворюють сполуки з сіркою та її аналогами (селеном, теллуром, мышьяком …). Звичайно належать до груп Б періодичної системи (заповнена 18 - эл. оболонка перед валентною оболонкою )
Періодична система та геохімічна класифікація хімічних элементів (Урусов) 3 – халькофільні елементи (от греч. chalkos - медь), які утворюють сполуки з сіркою та її аналогами (селеном, теллуром, мышьяком …). Звичайно належать до груп Б періодичної системи (заповнена 18 - эл. оболонка перед валентною оболонкою )
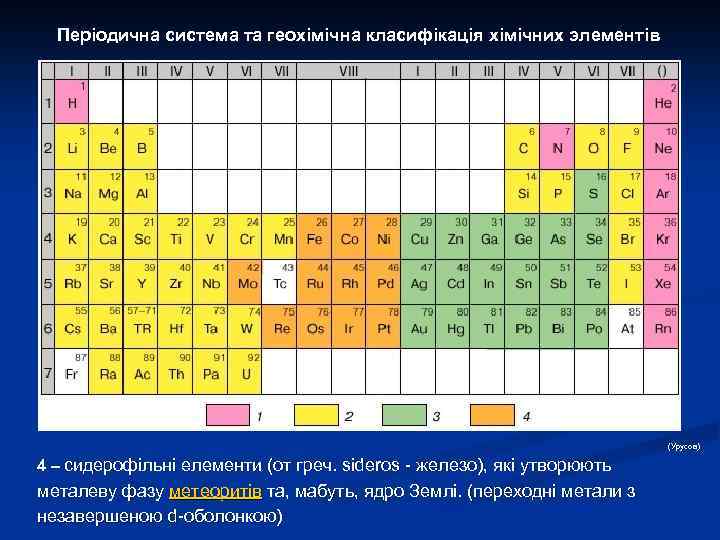 Періодична система та геохімічна класифікація хімічних элементів (Урусов) 4 – сидерофільні елементи (от греч. sideros - железо), які утворюють металеву фазу метеоритів та, мабуть, ядро Землі. (переходні метали з незавершеною d-оболонкою)
Періодична система та геохімічна класифікація хімічних элементів (Урусов) 4 – сидерофільні елементи (от греч. sideros - железо), які утворюють металеву фазу метеоритів та, мабуть, ядро Землі. (переходні метали з незавершеною d-оболонкою)
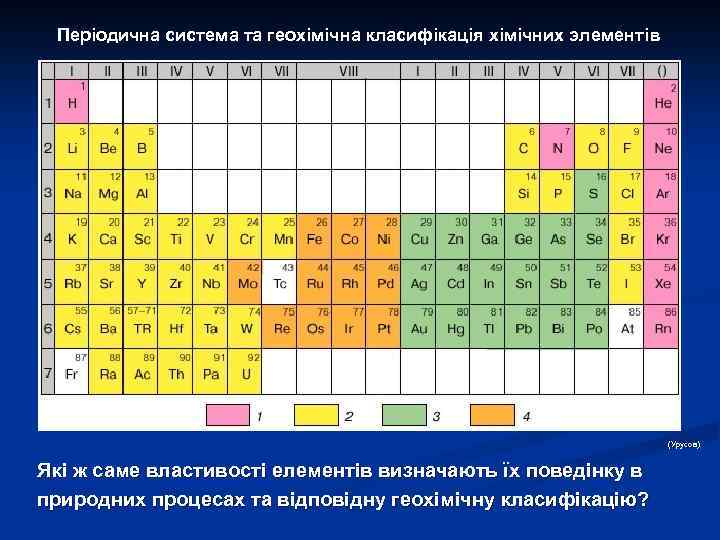 Періодична система та геохімічна класифікація хімічних элементів (Урусов) Які ж саме властивості елементів визначають їх поведінку в природних процесах та відповідну геохімічну класифікацію?
Періодична система та геохімічна класифікація хімічних элементів (Урусов) Які ж саме властивості елементів визначають їх поведінку в природних процесах та відповідну геохімічну класифікацію?
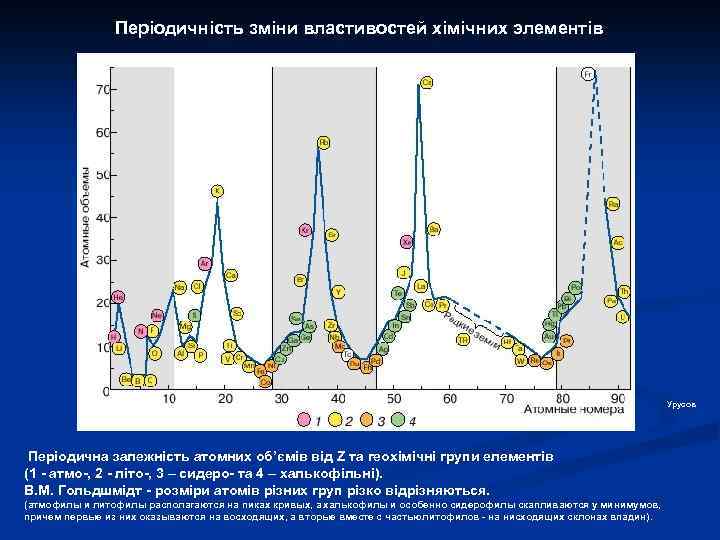 Періодичність зміни властивостей хімічних элементів Урусов Періодична залежність атомних об’ємів від Z та геохімічні групи елементів (1 - атмо-, 2 - літо-, 3 – сидеро- та 4 – халькофільні). В. М. Гольдшмідт - розміри атомів різних груп різко відрізняються. (атмофилы и литофилы располагаются на пиках кривых, а халькофилы и особенно сидерофилы скапливаются у минимумов, причем первые из них оказываются на восходящих, а вторые вместе с частью литофилов - на нисходящих склонах впадин).
Періодичність зміни властивостей хімічних элементів Урусов Періодична залежність атомних об’ємів від Z та геохімічні групи елементів (1 - атмо-, 2 - літо-, 3 – сидеро- та 4 – халькофільні). В. М. Гольдшмідт - розміри атомів різних груп різко відрізняються. (атмофилы и литофилы располагаются на пиках кривых, а халькофилы и особенно сидерофилы скапливаются у минимумов, причем первые из них оказываются на восходящих, а вторые вместе с частью литофилов - на нисходящих склонах впадин).
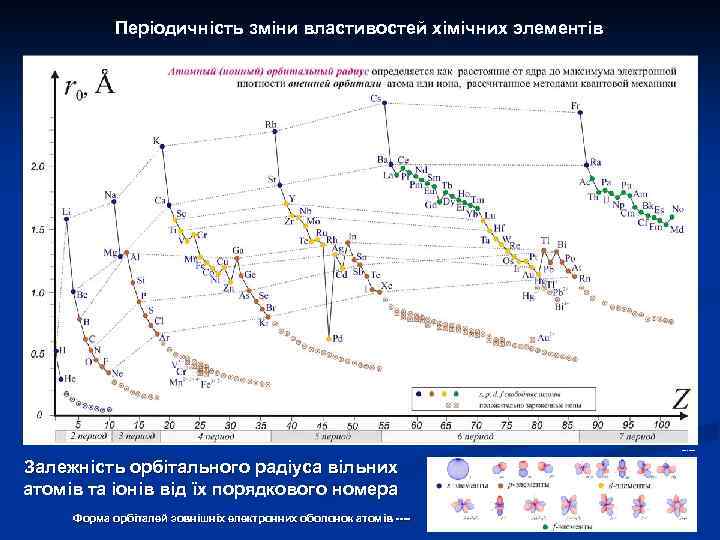 Періодичність зміни властивостей хімічних элементів МГУ -Урусов Залежність орбітального радіуса вільних атомів та іонів від їх порядкового номера Форма орбіталей зовнішніх електронних оболонок атомів ----
Періодичність зміни властивостей хімічних элементів МГУ -Урусов Залежність орбітального радіуса вільних атомів та іонів від їх порядкового номера Форма орбіталей зовнішніх електронних оболонок атомів ----
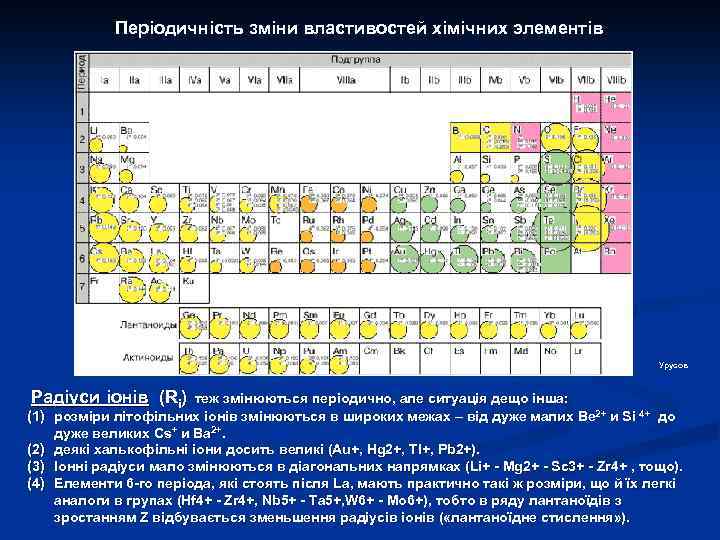 Періодичність зміни властивостей хімічних элементів Урусов Радіуси іонів (Ri) теж змінюються періодично, але ситуація дещо інша: (1) розміри літофільних іонів змінюються в широких межах – від дуже малих Ве 2+ и Si 4+ до дуже великих Cs+ и Ва 2+. (2) деякі халькофільні іони досить великі (Au+, Hg 2+, Tl+, Pb 2+). (3) Іонні радіуси мало змінюються в діагональних напрямках (Li+ - Mg 2+ - Sc 3+ - Zr 4+ , тощо). (4) Елементи 6 -го періода, які стоять після La, мають практично такі ж розміри, що й їх легкі аналоги в групах (Hf 4+ - Zr 4+, Nb 5+ - Ta 5+, W 6+ - Mo 6+), тобто в ряду лантаноїдів з зростанням Z відбувається зменьшення радіусів іонів ( «лантаноїдне стислення» ).
Періодичність зміни властивостей хімічних элементів Урусов Радіуси іонів (Ri) теж змінюються періодично, але ситуація дещо інша: (1) розміри літофільних іонів змінюються в широких межах – від дуже малих Ве 2+ и Si 4+ до дуже великих Cs+ и Ва 2+. (2) деякі халькофільні іони досить великі (Au+, Hg 2+, Tl+, Pb 2+). (3) Іонні радіуси мало змінюються в діагональних напрямках (Li+ - Mg 2+ - Sc 3+ - Zr 4+ , тощо). (4) Елементи 6 -го періода, які стоять після La, мають практично такі ж розміри, що й їх легкі аналоги в групах (Hf 4+ - Zr 4+, Nb 5+ - Ta 5+, W 6+ - Mo 6+), тобто в ряду лантаноїдів з зростанням Z відбувається зменьшення радіусів іонів ( «лантаноїдне стислення» ).
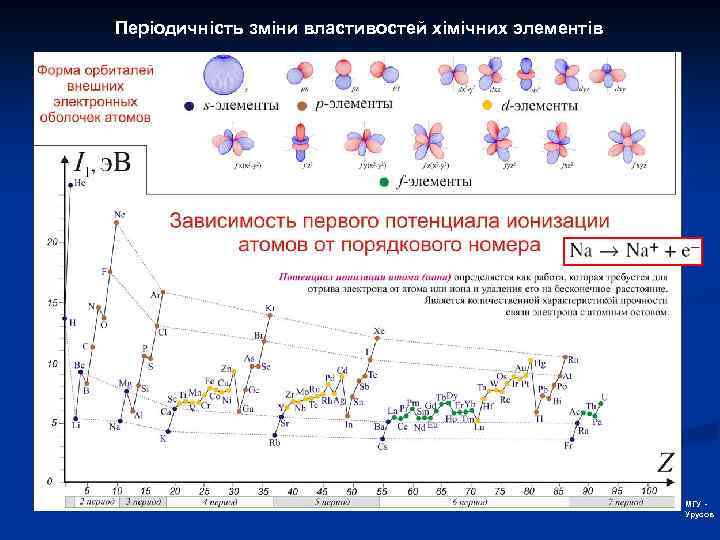 Періодичність зміни властивостей хімічних элементів МГУ Урусов
Періодичність зміни властивостей хімічних элементів МГУ Урусов
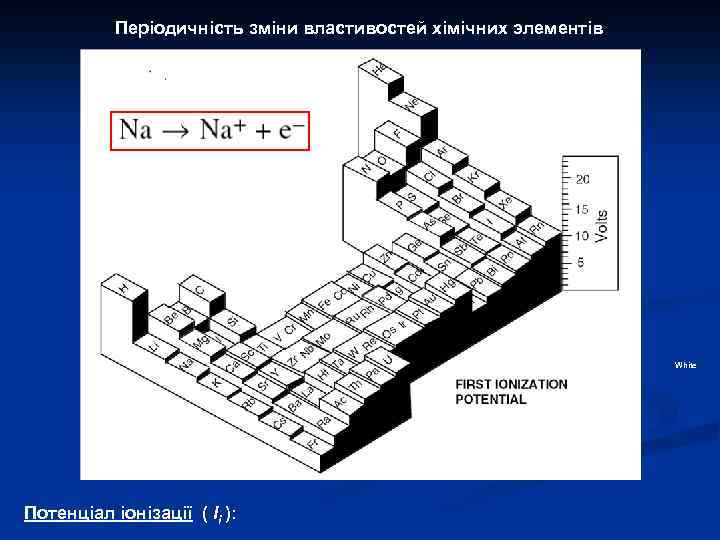 Періодичність зміни властивостей хімічних элементів White Потенціал іонізації ( Ii ):
Періодичність зміни властивостей хімічних элементів White Потенціал іонізації ( Ii ):
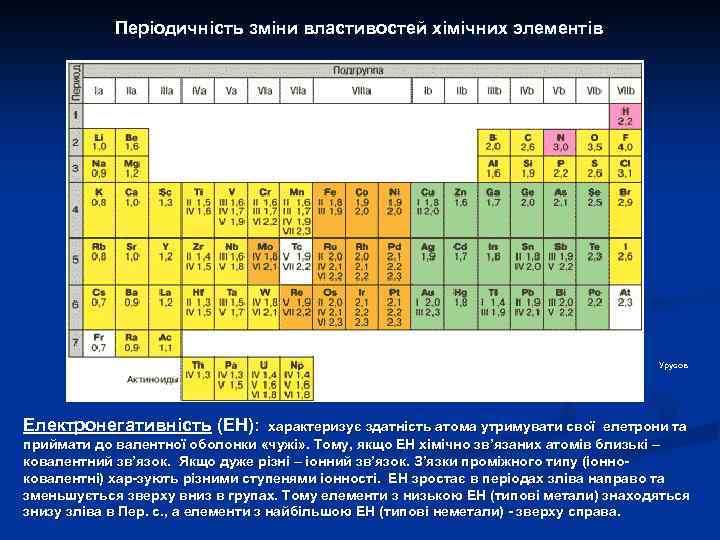 Періодичність зміни властивостей хімічних элементів Урусов Електронегативність (ЕН): характеризує здатність атома утримувати свої елетрони та приймати до валентної оболонки «чужі» . Тому, якщо ЕН хімічно зв’язаних атомів близькі – ковалентний зв’язок. Якщо дуже різні – іонний зв’язок. З’язки проміжного типу (іонноковалентні) хар-зують різними ступенями іонності. ЕН зростає в періодах зліва направо та зменьшується зверху вниз в групах. Тому елементи з низькою ЕН (типові метали) знаходяться знизу зліва в Пер. с. , а елементи з найбільшою ЕН (типові неметали) - зверху справа.
Періодичність зміни властивостей хімічних элементів Урусов Електронегативність (ЕН): характеризує здатність атома утримувати свої елетрони та приймати до валентної оболонки «чужі» . Тому, якщо ЕН хімічно зв’язаних атомів близькі – ковалентний зв’язок. Якщо дуже різні – іонний зв’язок. З’язки проміжного типу (іонноковалентні) хар-зують різними ступенями іонності. ЕН зростає в періодах зліва направо та зменьшується зверху вниз в групах. Тому елементи з низькою ЕН (типові метали) знаходяться знизу зліва в Пер. с. , а елементи з найбільшою ЕН (типові неметали) - зверху справа.
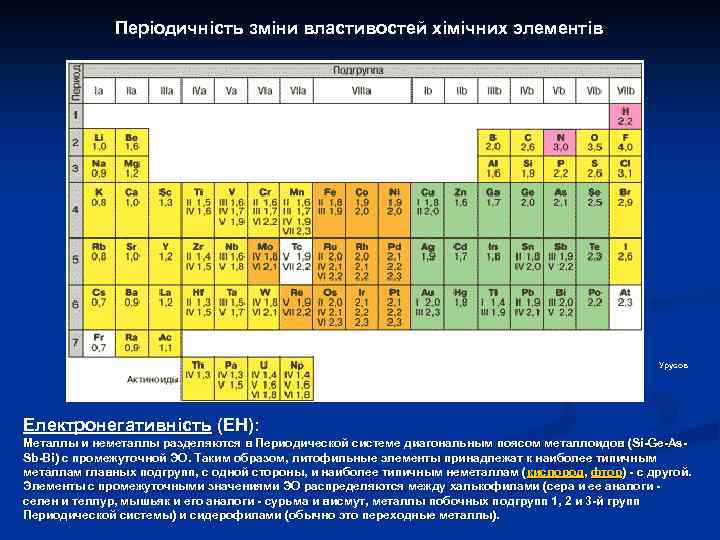 Періодичність зміни властивостей хімічних элементів Урусов Електронегативність (ЕН): Металлы и неметаллы разделяются в Периодической системе диагональным поясом металлоидов (Si-Ge-As. Sb-Bi) с промежуточной ЭО. Таким образом, литофильные элементы принадлежат к наиболее типичным Sb-Bi) с промежуточной ЭО. Таким образом, литофильные элементы принадлежат к наиболее типичным металлам главных подгрупп, с одной стороны, и наиболее типичным неметаллам (кислород, фтор) - с другой. Элементы с промежуточными значениями ЭО распределяются между халькофилами (сера и ее аналоги - селен и теллур, мышьяк и его аналоги - сурьма и висмут, металлы побочных подгрупп 1, 2 и 3 -й групп Периодической системы) и сидерофилами (обычно это переходные металлы).
Періодичність зміни властивостей хімічних элементів Урусов Електронегативність (ЕН): Металлы и неметаллы разделяются в Периодической системе диагональным поясом металлоидов (Si-Ge-As. Sb-Bi) с промежуточной ЭО. Таким образом, литофильные элементы принадлежат к наиболее типичным Sb-Bi) с промежуточной ЭО. Таким образом, литофильные элементы принадлежат к наиболее типичным металлам главных подгрупп, с одной стороны, и наиболее типичным неметаллам (кислород, фтор) - с другой. Элементы с промежуточными значениями ЭО распределяются между халькофилами (сера и ее аналоги - селен и теллур, мышьяк и его аналоги - сурьма и висмут, металлы побочных подгрупп 1, 2 и 3 -й групп Периодической системы) и сидерофилами (обычно это переходные металлы).
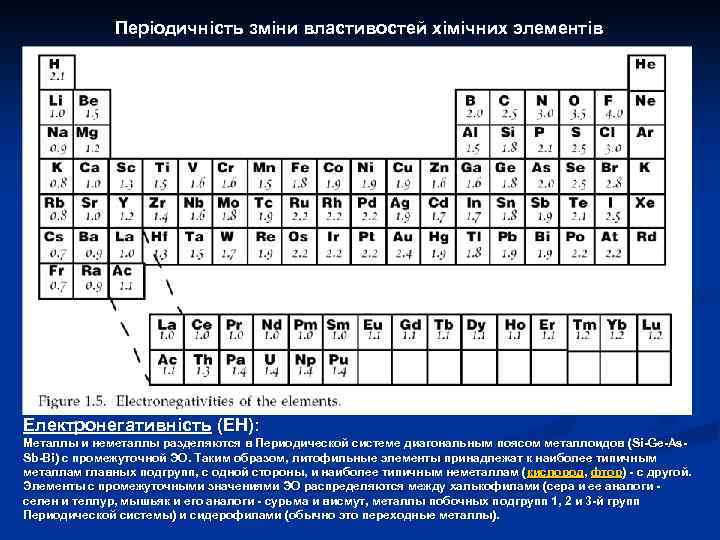 Періодичність зміни властивостей хімічних элементів White Електронегативність (ЕН): Металлы и неметаллы разделяются в Периодической системе диагональным поясом металлоидов (Si-Ge-As. Sb-Bi) с промежуточной ЭО. Таким образом, литофильные элементы принадлежат к наиболее типичным Sb-Bi) с промежуточной ЭО. Таким образом, литофильные элементы принадлежат к наиболее типичным металлам главных подгрупп, с одной стороны, и наиболее типичным неметаллам (кислород, фтор) - с другой. Элементы с промежуточными значениями ЭО распределяются между халькофилами (сера и ее аналоги - селен и теллур, мышьяк и его аналоги - сурьма и висмут, металлы побочных подгрупп 1, 2 и 3 -й групп Периодической системы) и сидерофилами (обычно это переходные металлы).
Періодичність зміни властивостей хімічних элементів White Електронегативність (ЕН): Металлы и неметаллы разделяются в Периодической системе диагональным поясом металлоидов (Si-Ge-As. Sb-Bi) с промежуточной ЭО. Таким образом, литофильные элементы принадлежат к наиболее типичным Sb-Bi) с промежуточной ЭО. Таким образом, литофильные элементы принадлежат к наиболее типичным металлам главных подгрупп, с одной стороны, и наиболее типичным неметаллам (кислород, фтор) - с другой. Элементы с промежуточными значениями ЭО распределяются между халькофилами (сера и ее аналоги - селен и теллур, мышьяк и его аналоги - сурьма и висмут, металлы побочных подгрупп 1, 2 и 3 -й групп Периодической системы) и сидерофилами (обычно это переходные металлы).
 Властивості (характеристики) хімічних элементів Таким чином: Радіуси іонів (Ri) та електронегативність (ЕН) хімічних елементів періодично змінюються в залежності від Z, зумовлюють їх поведінку в геохімічних процесах та визначають належність елементів до груп геохімічної класифікації, яка вперше була запропонована ще В. М. Гольдшмідтом (1933 р. ). Треба зауважити, що ця класифікація досі не втратила свого значення. Вона враховується у сучасних геохімічних класифікаціях елементів, з якими ми познайомимось наприкінці лекцій з розділу “Хімічні елементи в геохімії”. Далі ми докладніше розглянемо ці (та деякі інші) найбільш важливі для геохімії властивості (характеристики) хімічних елементів.
Властивості (характеристики) хімічних элементів Таким чином: Радіуси іонів (Ri) та електронегативність (ЕН) хімічних елементів періодично змінюються в залежності від Z, зумовлюють їх поведінку в геохімічних процесах та визначають належність елементів до груп геохімічної класифікації, яка вперше була запропонована ще В. М. Гольдшмідтом (1933 р. ). Треба зауважити, що ця класифікація досі не втратила свого значення. Вона враховується у сучасних геохімічних класифікаціях елементів, з якими ми познайомимось наприкінці лекцій з розділу “Хімічні елементи в геохімії”. Далі ми докладніше розглянемо ці (та деякі інші) найбільш важливі для геохімії властивості (характеристики) хімічних елементів.
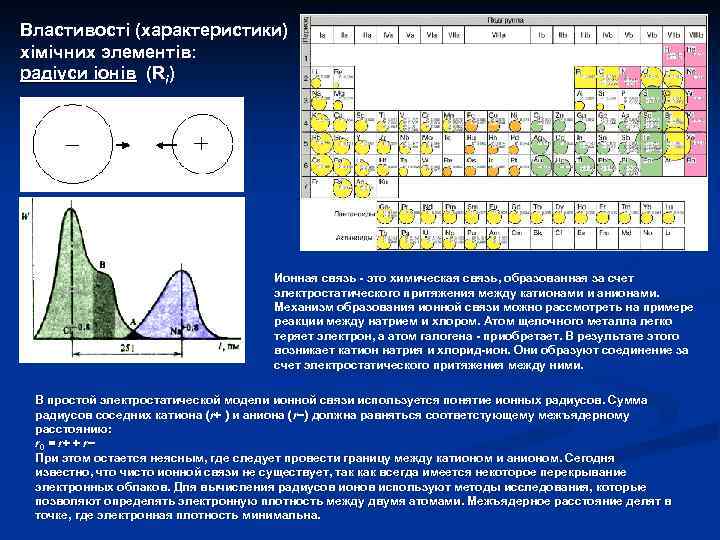 Властивості (характеристики) хімічних элементів: радіуси іонів (Ri) Ионная связь - это химическая связь, образованная за счет электростатического притяжения между катионами и анионами. Механизм образования ионной связи можно рассмотреть на примере реакции между натрием и хлором. Атом щелочного металла легко теряет электрон, а атом галогена - приобретает. В результате этого возникает катион натрия и хлорид-ион. Они образуют соединение за счет электростатического притяжения между ними. В простой электростатической модели ионной связи используется понятие ионных радиусов. Сумма радиусов соседних катиона (r+ ) и аниона (r−) должна равняться соответстующему межъядерному радиусов соседних катиона (r ) и аниона (r −) должна равняться соответстующему межъядерному расстоянию: r 0 = r+ + r− = r + r При этом остается неясным, где следует провести границу между катионом и анионом. Сегодня известно, что чисто ионной связи не существует, так как всегда имеется некоторое перекрывание электронных облаков. Для вычисления радиусов ионов используют методы исследования, которые позволяют определять электронную плотность между двумя атомами. Межъядерное расстояние делят в точке, где электронная плотность минимальна.
Властивості (характеристики) хімічних элементів: радіуси іонів (Ri) Ионная связь - это химическая связь, образованная за счет электростатического притяжения между катионами и анионами. Механизм образования ионной связи можно рассмотреть на примере реакции между натрием и хлором. Атом щелочного металла легко теряет электрон, а атом галогена - приобретает. В результате этого возникает катион натрия и хлорид-ион. Они образуют соединение за счет электростатического притяжения между ними. В простой электростатической модели ионной связи используется понятие ионных радиусов. Сумма радиусов соседних катиона (r+ ) и аниона (r−) должна равняться соответстующему межъядерному радиусов соседних катиона (r ) и аниона (r −) должна равняться соответстующему межъядерному расстоянию: r 0 = r+ + r− = r + r При этом остается неясным, где следует провести границу между катионом и анионом. Сегодня известно, что чисто ионной связи не существует, так как всегда имеется некоторое перекрывание электронных облаков. Для вычисления радиусов ионов используют методы исследования, которые позволяют определять электронную плотность между двумя атомами. Межъядерное расстояние делят в точке, где электронная плотность минимальна.
 Властивості (характеристики) хімічних элементів: радіуси іонів (Ri) Размеры иона зависят от многих факторов. (1) Заряд иона - обратнопропорционально (2) Координационное число - прямопропорционально. Сравнение ионных радиусов можно проводить только при одинаковом координационном числе, поскольку оно оказывает влияние на размер иона из-за сил отталкивания между противоионами. Это хорошо видно на примере иона Ag+; его ионных радиус равен 81, 114 и 129 пм для координационных чисел 2, 4 и 6, соответственно. Структура идеального ионного соединения, обусловленная максимальным притяжением между разноименными ионами и минимальным отталкиванием одноименных ионов, во многом определяется соотношением ионных радиусов катионов и анионов: Отношение r+ / r− КЧ катиона Окружение Пример 0, 225− 0, 414 4 Тетраэдрическое Zn. S 0, 414− 0, 732 6 Октаэдрическое Na. Cl 0, 732− 1, 000 8 Кубическое Cs. Cl Додекаэдрическое В ионных кристаллах не обнаружено >1, 000 12
Властивості (характеристики) хімічних элементів: радіуси іонів (Ri) Размеры иона зависят от многих факторов. (1) Заряд иона - обратнопропорционально (2) Координационное число - прямопропорционально. Сравнение ионных радиусов можно проводить только при одинаковом координационном числе, поскольку оно оказывает влияние на размер иона из-за сил отталкивания между противоионами. Это хорошо видно на примере иона Ag+; его ионных радиус равен 81, 114 и 129 пм для координационных чисел 2, 4 и 6, соответственно. Структура идеального ионного соединения, обусловленная максимальным притяжением между разноименными ионами и минимальным отталкиванием одноименных ионов, во многом определяется соотношением ионных радиусов катионов и анионов: Отношение r+ / r− КЧ катиона Окружение Пример 0, 225− 0, 414 4 Тетраэдрическое Zn. S 0, 414− 0, 732 6 Октаэдрическое Na. Cl 0, 732− 1, 000 8 Кубическое Cs. Cl Додекаэдрическое В ионных кристаллах не обнаружено >1, 000 12
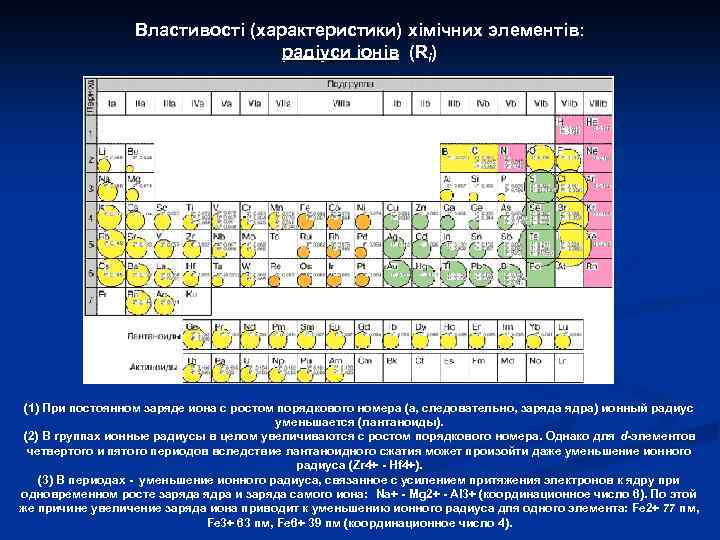 Властивості (характеристики) хімічних элементів: радіуси іонів (Ri) (1) При постоянном заряде иона с ростом порядкового номера (а, следовательно, заряда ядра) ионный радиус уменьшается (лантаноиды). (2) В группах ионные радиусы в целом увеличиваются с ростом порядкового номера. Однако для d-элементов четвертого и пятого периодов вследствие лантаноидного сжатия может произойти даже уменьшение ионного радиуса (Zr 4+ - Hf 4+). (3) В периодах - уменьшение ионного радиуса, связанное с усилением притяжения электронов к ядру при одновременном росте заряда ядра и заряда самого иона: Na+ - Mg 2+ - Al 3+ (координационное число 6). По этой же причине увеличение заряда иона приводит к уменьшению ионного радиуса для одного элемента: Fe 2+ 77 пм, Fe 3+ 63 пм, Fe 6+ 39 пм (координационное число 4).
Властивості (характеристики) хімічних элементів: радіуси іонів (Ri) (1) При постоянном заряде иона с ростом порядкового номера (а, следовательно, заряда ядра) ионный радиус уменьшается (лантаноиды). (2) В группах ионные радиусы в целом увеличиваются с ростом порядкового номера. Однако для d-элементов четвертого и пятого периодов вследствие лантаноидного сжатия может произойти даже уменьшение ионного радиуса (Zr 4+ - Hf 4+). (3) В периодах - уменьшение ионного радиуса, связанное с усилением притяжения электронов к ядру при одновременном росте заряда ядра и заряда самого иона: Na+ - Mg 2+ - Al 3+ (координационное число 6). По этой же причине увеличение заряда иона приводит к уменьшению ионного радиуса для одного элемента: Fe 2+ 77 пм, Fe 3+ 63 пм, Fe 6+ 39 пм (координационное число 4).
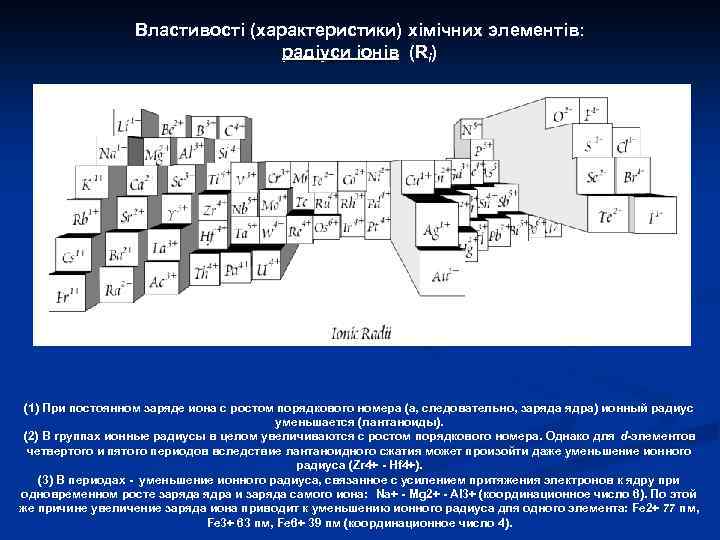 Властивості (характеристики) хімічних элементів: радіуси іонів (Ri) (1) При постоянном заряде иона с ростом порядкового номера (а, следовательно, заряда ядра) ионный радиус уменьшается (лантаноиды). (2) В группах ионные радиусы в целом увеличиваются с ростом порядкового номера. Однако для d-элементов четвертого и пятого периодов вследствие лантаноидного сжатия может произойти даже уменьшение ионного радиуса (Zr 4+ - Hf 4+). (3) В периодах - уменьшение ионного радиуса, связанное с усилением притяжения электронов к ядру при одновременном росте заряда ядра и заряда самого иона: Na+ - Mg 2+ - Al 3+ (координационное число 6). По этой же причине увеличение заряда иона приводит к уменьшению ионного радиуса для одного элемента: Fe 2+ 77 пм, Fe 3+ 63 пм, Fe 6+ 39 пм (координационное число 4).
Властивості (характеристики) хімічних элементів: радіуси іонів (Ri) (1) При постоянном заряде иона с ростом порядкового номера (а, следовательно, заряда ядра) ионный радиус уменьшается (лантаноиды). (2) В группах ионные радиусы в целом увеличиваются с ростом порядкового номера. Однако для d-элементов четвертого и пятого периодов вследствие лантаноидного сжатия может произойти даже уменьшение ионного радиуса (Zr 4+ - Hf 4+). (3) В периодах - уменьшение ионного радиуса, связанное с усилением притяжения электронов к ядру при одновременном росте заряда ядра и заряда самого иона: Na+ - Mg 2+ - Al 3+ (координационное число 6). По этой же причине увеличение заряда иона приводит к уменьшению ионного радиуса для одного элемента: Fe 2+ 77 пм, Fe 3+ 63 пм, Fe 6+ 39 пм (координационное число 4).
 На попередніх лекціях ми з’ясували, що: Радіуси іонів (Ri) та електронегативність (ЕН) хімічних елементів періодично змінюються в залежності від Z, зумовлюють їх поведінку в геохімічних процесах, в тому числі при реалізаціїї ізоморфізму в мінералах. Ці властивості й визначають належність елементів до груп геохімічної класифікації, яка вперше була запропонована ще В. М. Гольдшмідтом (1933 р. ). Треба зауважити, що ця класифікація досі не втратила свого значення. Вона досить повно враховується у сучасних геохімічних класифікаціях елементів, які ми й розглянемо зараз завершуючи розділ “Хімічні елементи в геохімії” нашого курсу.
На попередніх лекціях ми з’ясували, що: Радіуси іонів (Ri) та електронегативність (ЕН) хімічних елементів періодично змінюються в залежності від Z, зумовлюють їх поведінку в геохімічних процесах, в тому числі при реалізаціїї ізоморфізму в мінералах. Ці властивості й визначають належність елементів до груп геохімічної класифікації, яка вперше була запропонована ще В. М. Гольдшмідтом (1933 р. ). Треба зауважити, що ця класифікація досі не втратила свого значення. Вона досить повно враховується у сучасних геохімічних класифікаціях елементів, які ми й розглянемо зараз завершуючи розділ “Хімічні елементи в геохімії” нашого курсу.
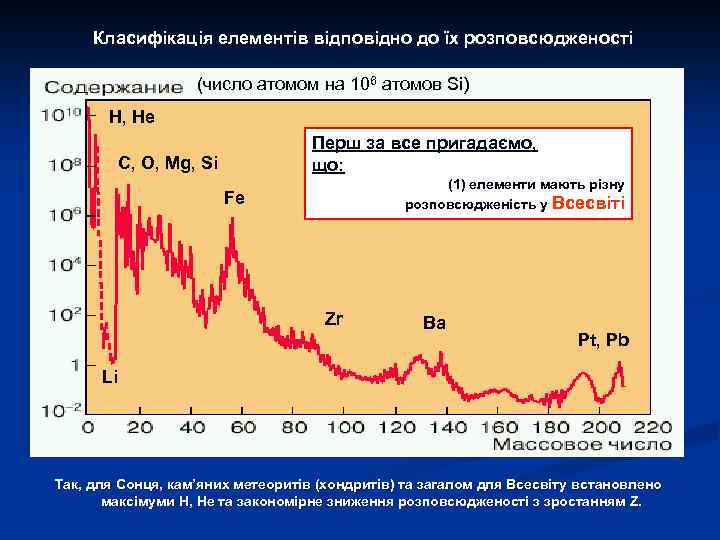 Класифікація елементів відповідно до їх розповсюдженості (число атомом на 106 атомов Si) H, He Перш за все пригадаємо, що: C, O, Mg, Si (1) елементи мають різну розповсюдженість у Всесвіті Fe Zr Ba Pt, Pb Li Так, для Сонця, кам’яних метеоритів (хондритів) та загалом для Всесвіту встановлено максімуми H, He та закономірне зниження розповсюдженості з зростанням Z.
Класифікація елементів відповідно до їх розповсюдженості (число атомом на 106 атомов Si) H, He Перш за все пригадаємо, що: C, O, Mg, Si (1) елементи мають різну розповсюдженість у Всесвіті Fe Zr Ba Pt, Pb Li Так, для Сонця, кам’яних метеоритів (хондритів) та загалом для Всесвіту встановлено максімуми H, He та закономірне зниження розповсюдженості з зростанням Z.
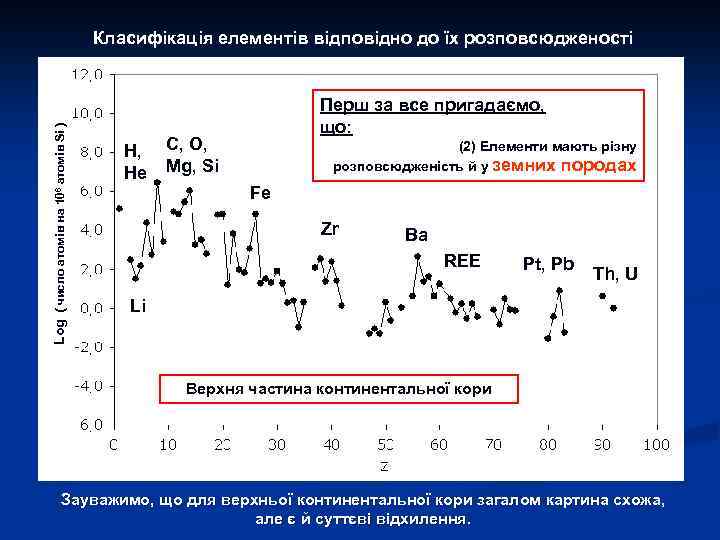 Log ( число атомів на 106 атомів Si ) Класифікація елементів відповідно до їх розповсюдженості H, He Перш за все пригадаємо, що: C, O, Mg, Si (2) Елементи мають різну розповсюдженість й у земних породах Fe Zr Ba REE Pt, Pb Th, U Li Верхня частина континентальної кори Зауважимо, що для верхньої континентальної кори загалом картина схожа, але є й суттєві відхилення.
Log ( число атомів на 106 атомів Si ) Класифікація елементів відповідно до їх розповсюдженості H, He Перш за все пригадаємо, що: C, O, Mg, Si (2) Елементи мають різну розповсюдженість й у земних породах Fe Zr Ba REE Pt, Pb Th, U Li Верхня частина континентальної кори Зауважимо, що для верхньої континентальної кори загалом картина схожа, але є й суттєві відхилення.
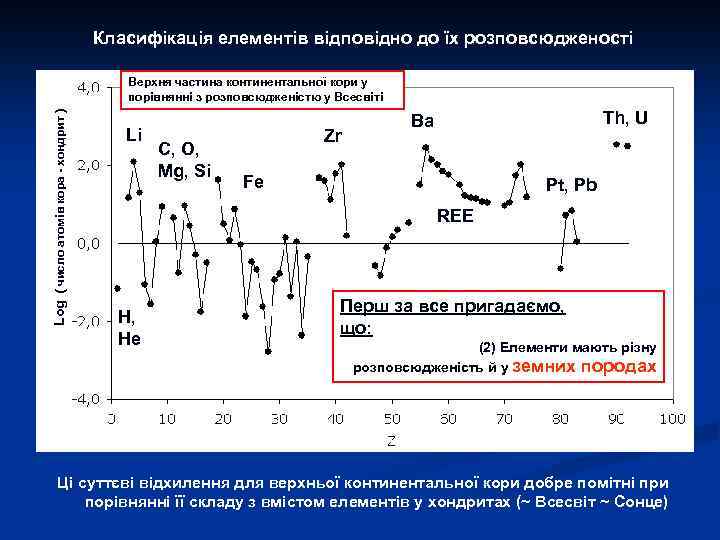 Класифікація елементів відповідно до їх розповсюдженості Log ( число атомів кора - хондрит ) Верхня частина континентальної кори у порівнянні з розповсюдженістю у Всесвіті Li C, O, Mg, Si Zr Th, U Ba Fe Pt, Pb REE H, He Перш за все пригадаємо, що: (2) Елементи мають різну розповсюдженість й у земних породах Ці суттєві відхилення для верхньої континентальної кори добре помітні при порівнянні її складу з вмістом елементів у хондритах (~ Всесвіт ~ Сонце)
Класифікація елементів відповідно до їх розповсюдженості Log ( число атомів кора - хондрит ) Верхня частина континентальної кори у порівнянні з розповсюдженістю у Всесвіті Li C, O, Mg, Si Zr Th, U Ba Fe Pt, Pb REE H, He Перш за все пригадаємо, що: (2) Елементи мають різну розповсюдженість й у земних породах Ці суттєві відхилення для верхньої континентальної кори добре помітні при порівнянні її складу з вмістом елементів у хондритах (~ Всесвіт ~ Сонце)
 Класифікація елементів відповідно до їх розповсюдженості Перш за все пригадаємо, що: (2) Елементи мають різну розповсюдженість й у земних породах. У валовому складі силікатної частини Землі (BSE – “Bulk Silicate Earth”) 6 елементів - O, Mg, Si, Fe, Al, Ca займають 99, 1 wt%. Тому ці елементи прийнято відносити до групи “провідних” (“головних”), або “major elements”. Інші елементи з низькими концентраціями відносять до групи мікроелементів (“trace elements”). Треба зауважити, що обсяги груп “major elements” та “trace elements” змінюються в залежності від геологічних утворень, що розглядаються геохімією (верхня кора, мантія, ядро, граніти, базальти тощо).
Класифікація елементів відповідно до їх розповсюдженості Перш за все пригадаємо, що: (2) Елементи мають різну розповсюдженість й у земних породах. У валовому складі силікатної частини Землі (BSE – “Bulk Silicate Earth”) 6 елементів - O, Mg, Si, Fe, Al, Ca займають 99, 1 wt%. Тому ці елементи прийнято відносити до групи “провідних” (“головних”), або “major elements”. Інші елементи з низькими концентраціями відносять до групи мікроелементів (“trace elements”). Треба зауважити, що обсяги груп “major elements” та “trace elements” змінюються в залежності від геологічних утворень, що розглядаються геохімією (верхня кора, мантія, ядро, граніти, базальти тощо).
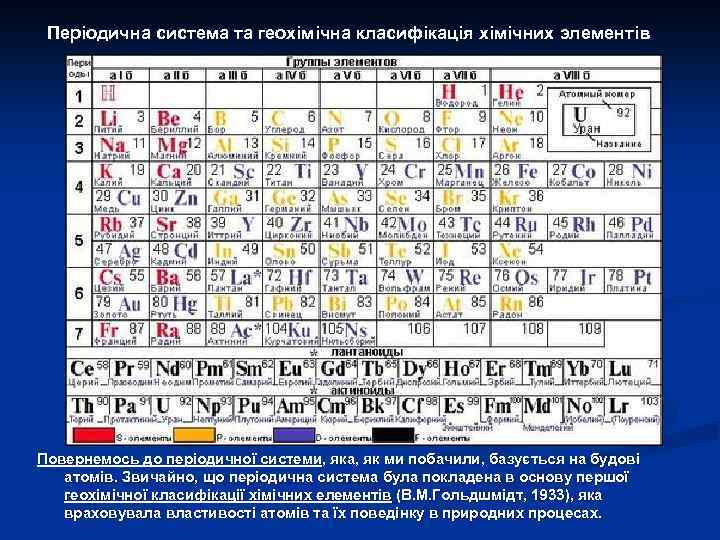 Періодична система та геохімічна класифікація хімічних элементів Повернемось до періодичної системи, яка, як ми побачили, базується на будові атомів. Звичайно, що періодична система була покладена в основу першої геохімічної класифікації хімічних елементів (В. М. Гольдшмідт, 1933), яка враховувала властивості атомів та їх поведінку в природних процесах.
Періодична система та геохімічна класифікація хімічних элементів Повернемось до періодичної системи, яка, як ми побачили, базується на будові атомів. Звичайно, що періодична система була покладена в основу першої геохімічної класифікації хімічних елементів (В. М. Гольдшмідт, 1933), яка враховувала властивості атомів та їх поведінку в природних процесах.
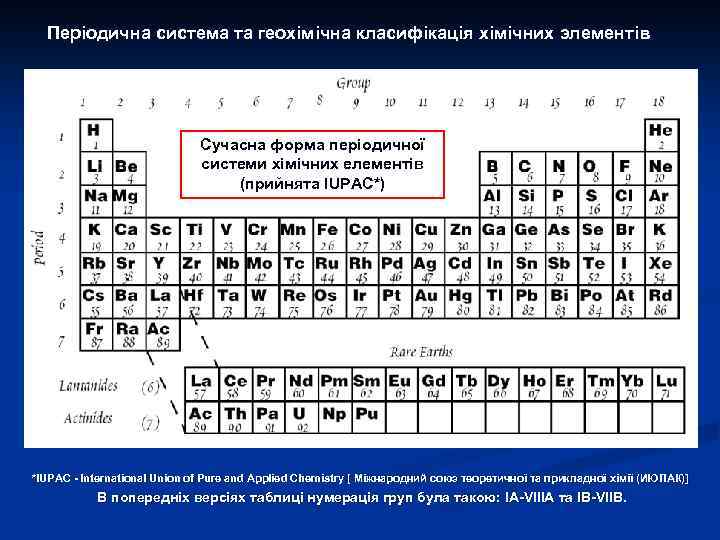 Періодична система та геохімічна класифікація хімічних элементів Сучасна форма періодичної системи хімічних елементів (прийнята IUPAC*) *IUPAC - International Union of Pure and Applied Chemistry [ Міжнародний союз теоретичної та прикладної хімії (ИЮПАК)] *IUPAC - International Union of Pure and Applied Chemistry Мі жнародний союз теоретичної та прикладної хімії ИЮПАК)] В попередніх версіях таблиці нумерація груп була такою: IA-VIIIA та IB-VIIB.
Періодична система та геохімічна класифікація хімічних элементів Сучасна форма періодичної системи хімічних елементів (прийнята IUPAC*) *IUPAC - International Union of Pure and Applied Chemistry [ Міжнародний союз теоретичної та прикладної хімії (ИЮПАК)] *IUPAC - International Union of Pure and Applied Chemistry Мі жнародний союз теоретичної та прикладної хімії ИЮПАК)] В попередніх версіях таблиці нумерація груп була такою: IA-VIIIA та IB-VIIB.
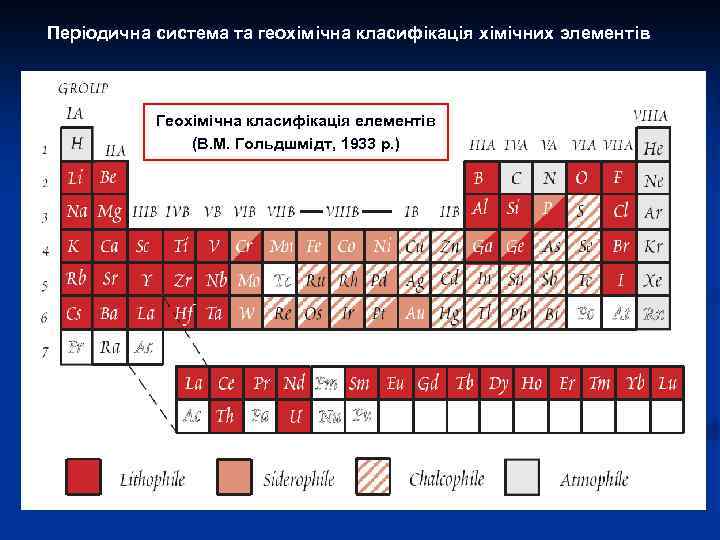 Періодична система та геохімічна класифікація хімічних элементів Геохімічна класифікація елементів (В. М. Гольдшмідт, 1933 р. ) К
Періодична система та геохімічна класифікація хімічних элементів Геохімічна класифікація елементів (В. М. Гольдшмідт, 1933 р. ) К
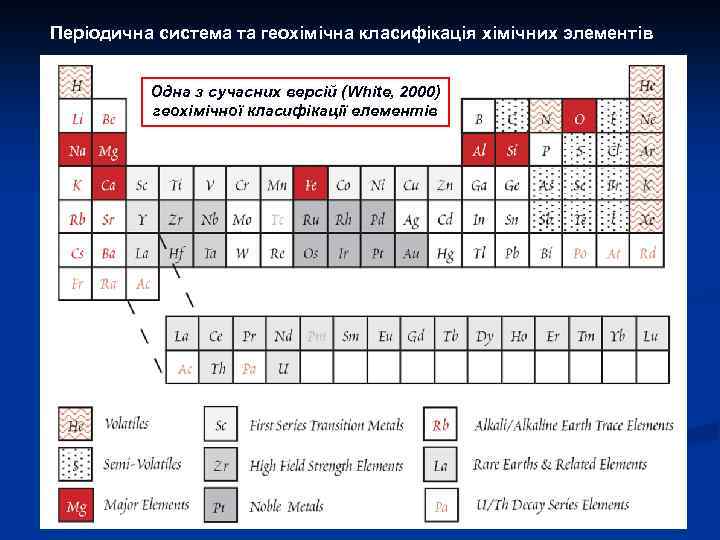 Періодична система та геохімічна класифікація хімічних элементів Одна з сучасних версій (White, 2000) геохімічної класифікації елементів
Періодична система та геохімічна класифікація хімічних элементів Одна з сучасних версій (White, 2000) геохімічної класифікації елементів
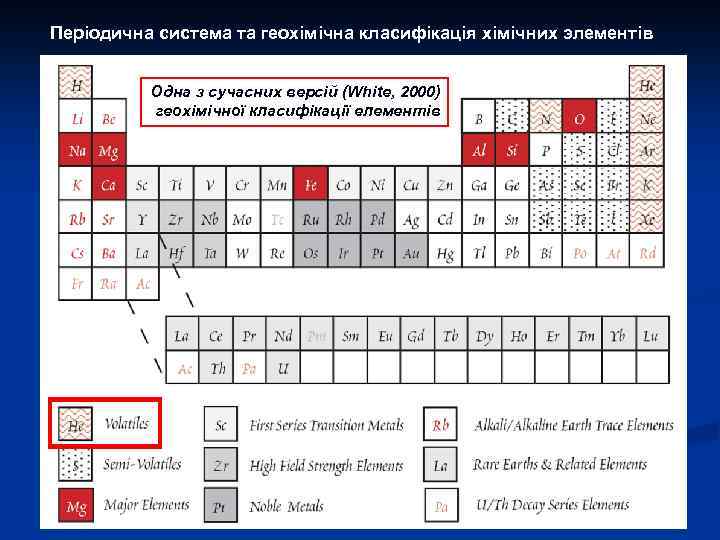 Періодична система та геохімічна класифікація хімічних элементів Одна з сучасних версій (White, 2000) геохімічної класифікації елементів
Періодична система та геохімічна класифікація хімічних элементів Одна з сучасних версій (White, 2000) геохімічної класифікації елементів
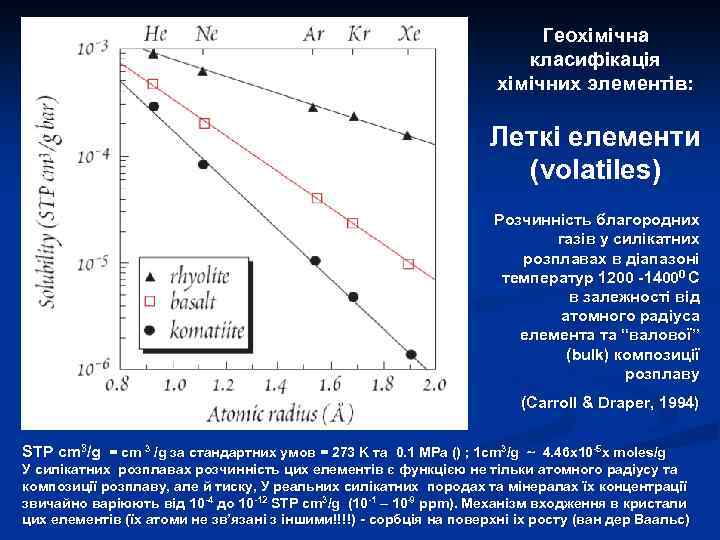 Геохімічна класифікація хімічних элементів: Леткі елементи (volatiles) Розчинність благородних газів у силікатних розплавах в діапазоні температур 1200 -14000 С в залежності від атомного радіуса елемента та “валової” (bulk) композиції розплаву (Carroll & Draper, 1994) STP cm 3/g = cm 3 /g за стандартних умов = 273 K та 0. 1 MPa () ; 1 cm 3/g ~ 4. 46 x 10 -5 x moles/g У силікатних розплавах розчинність цих елементів є функцією не тільки атомного радіусу та композиції розплаву, але й тиску, У реальних силікатних породах та мінералах їх концентрації звичайно варіюють від 10 -4 до 10 -12 STP cm 3/g (10 -1 – 10 -9 ppm). Механізм входження в кристали цих елементів (їх атоми не зв’язані з іншими!!!!) - сорбція на поверхні іх росту (ван дер Ваальс)
Геохімічна класифікація хімічних элементів: Леткі елементи (volatiles) Розчинність благородних газів у силікатних розплавах в діапазоні температур 1200 -14000 С в залежності від атомного радіуса елемента та “валової” (bulk) композиції розплаву (Carroll & Draper, 1994) STP cm 3/g = cm 3 /g за стандартних умов = 273 K та 0. 1 MPa () ; 1 cm 3/g ~ 4. 46 x 10 -5 x moles/g У силікатних розплавах розчинність цих елементів є функцією не тільки атомного радіусу та композиції розплаву, але й тиску, У реальних силікатних породах та мінералах їх концентрації звичайно варіюють від 10 -4 до 10 -12 STP cm 3/g (10 -1 – 10 -9 ppm). Механізм входження в кристали цих елементів (їх атоми не зв’язані з іншими!!!!) - сорбція на поверхні іх росту (ван дер Ваальс)
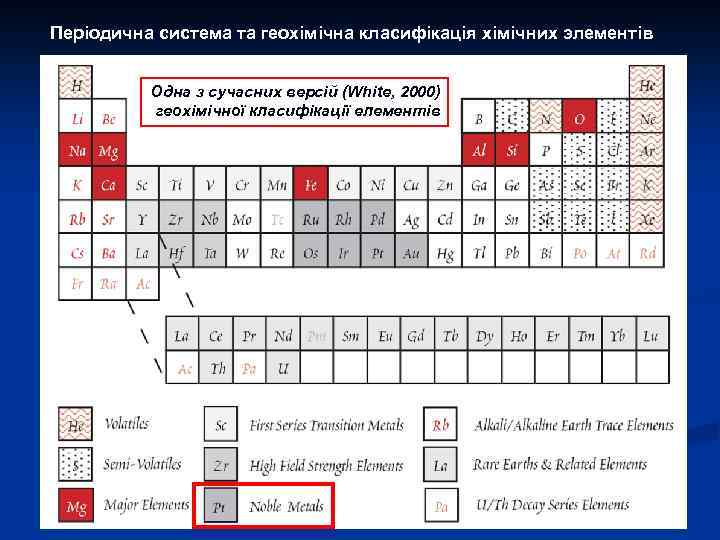 Періодична система та геохімічна класифікація хімічних элементів Одна з сучасних версій (White, 2000) геохімічної класифікації елементів
Періодична система та геохімічна класифікація хімічних элементів Одна з сучасних версій (White, 2000) геохімічної класифікації елементів
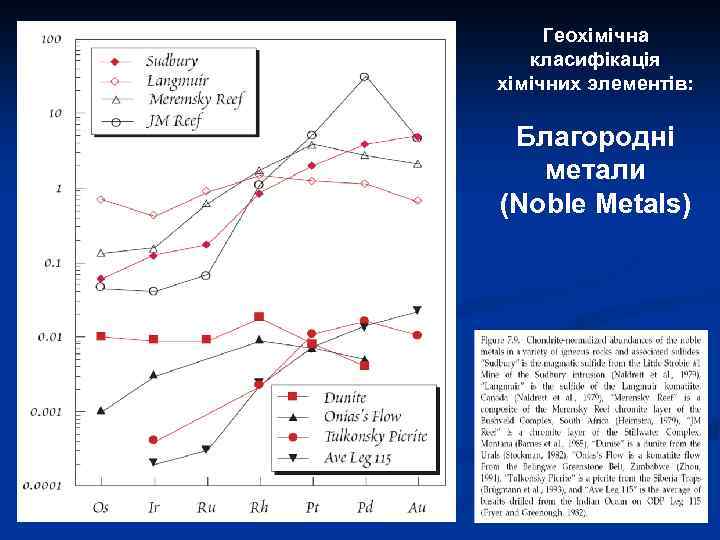 Геохімічна класифікація хімічних элементів: Благородні метали (Noble Metals)
Геохімічна класифікація хімічних элементів: Благородні метали (Noble Metals)
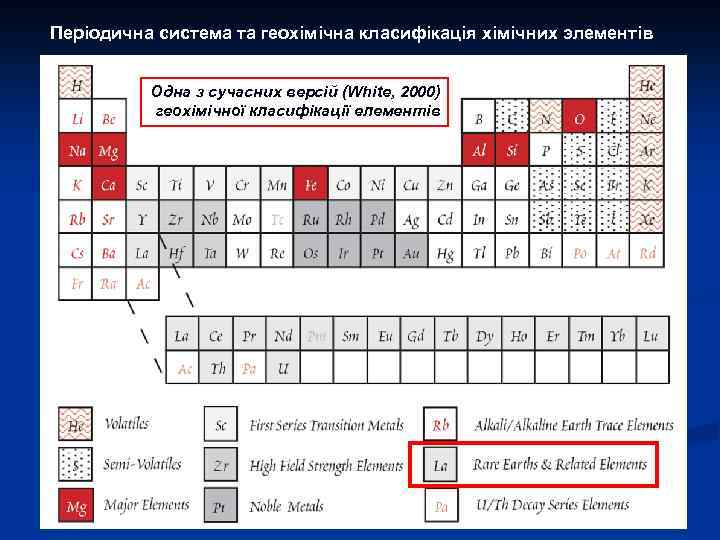 Періодична система та геохімічна класифікація хімічних элементів Одна з сучасних версій (White, 2000) геохімічної класифікації елементів
Періодична система та геохімічна класифікація хімічних элементів Одна з сучасних версій (White, 2000) геохімічної класифікації елементів
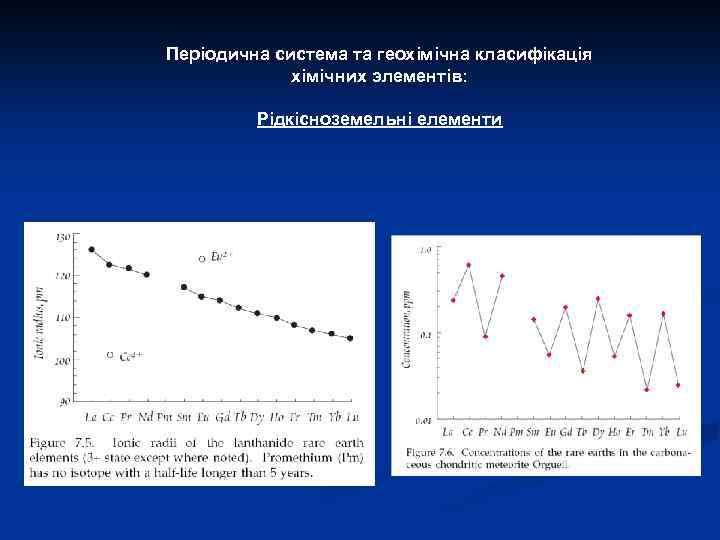 Періодична система та геохімічна класифікація хімічних элементів: Рідкісноземельні елементи
Періодична система та геохімічна класифікація хімічних элементів: Рідкісноземельні елементи
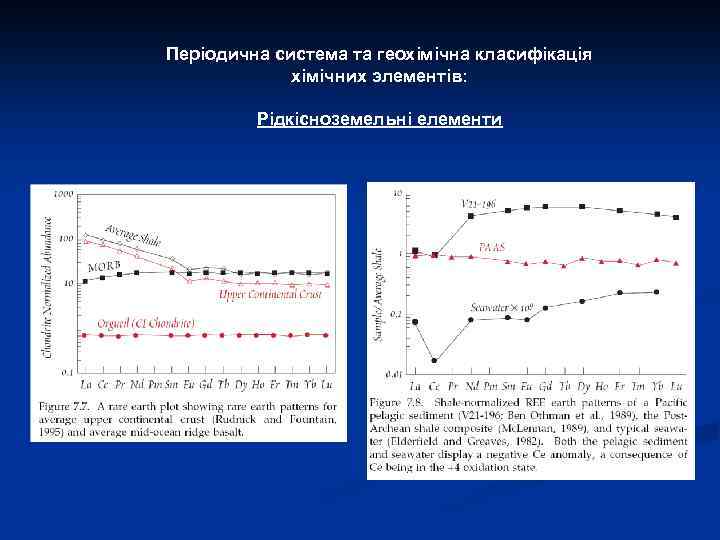 Періодична система та геохімічна класифікація хімічних элементів: Рідкісноземельні елементи
Періодична система та геохімічна класифікація хімічних элементів: Рідкісноземельні елементи
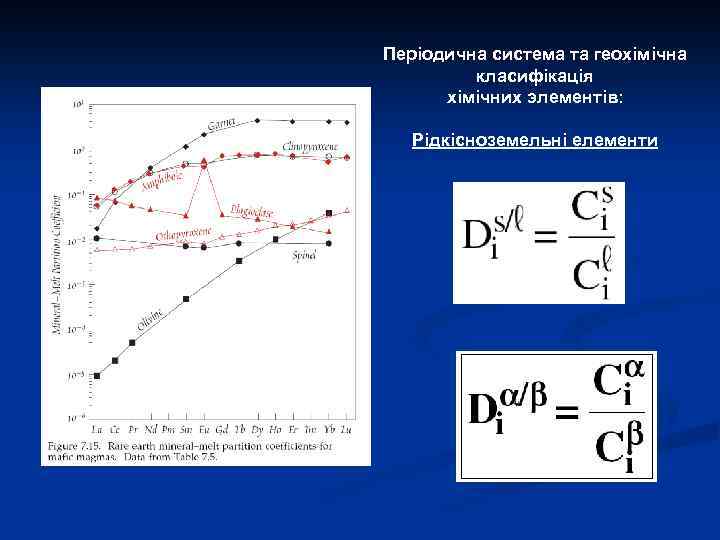 Періодична система та геохімічна класифікація хімічних элементів: Рідкісноземельні елементи
Періодична система та геохімічна класифікація хімічних элементів: Рідкісноземельні елементи
 Геохімічна класифікація хімічних элементів
Геохімічна класифікація хімічних элементів
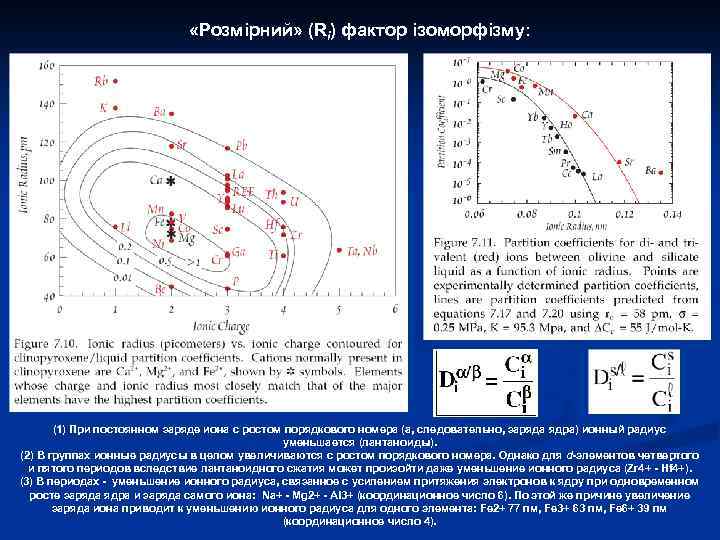 «Розмірний» (Ri) фактор ізоморфізму: (1) При постоянном заряде иона с ростом порядкового номера (а, следовательно, заряда ядра) ионный радиус уменьшается (лантаноиды). (2) В группах ионные радиусы в целом увеличиваются с ростом порядкового номера. Однако для d-элементов четвертого и пятого периодов вследствие лантаноидного сжатия может произойти даже уменьшение ионного радиуса (Zr 4+ - Hf 4+). (3) В периодах - уменьшение ионного радиуса, связанное с усилением притяжения электронов к ядру при одновременном росте заряда ядра и заряда самого иона: Na+ - Mg 2+ - Al 3+ (координационное число 6). По этой же причине увеличение заряда иона приводит к уменьшению ионного радиуса для одного элемента: Fe 2+ 77 пм, Fe 3+ 63 пм, Fe 6+ 39 пм (координационное число 4).
«Розмірний» (Ri) фактор ізоморфізму: (1) При постоянном заряде иона с ростом порядкового номера (а, следовательно, заряда ядра) ионный радиус уменьшается (лантаноиды). (2) В группах ионные радиусы в целом увеличиваются с ростом порядкового номера. Однако для d-элементов четвертого и пятого периодов вследствие лантаноидного сжатия может произойти даже уменьшение ионного радиуса (Zr 4+ - Hf 4+). (3) В периодах - уменьшение ионного радиуса, связанное с усилением притяжения электронов к ядру при одновременном росте заряда ядра и заряда самого иона: Na+ - Mg 2+ - Al 3+ (координационное число 6). По этой же причине увеличение заряда иона приводит к уменьшению ионного радиуса для одного элемента: Fe 2+ 77 пм, Fe 3+ 63 пм, Fe 6+ 39 пм (координационное число 4).
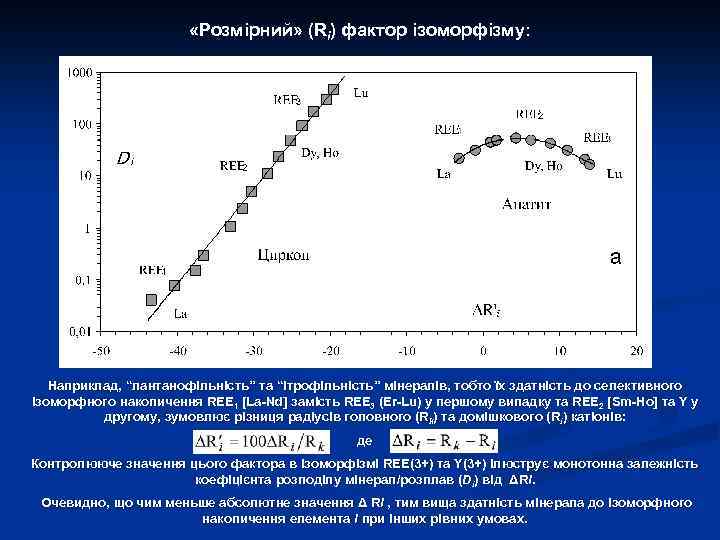 «Розмірний» (Ri) фактор ізоморфізму: Наприклад, “лантанофільність” та “ітрофільність” мінералів, тобто їх здатність до селективного ізоморфного накопичення REE 1 [La-Nd] замість REE 3 (Er-Lu) у першому випадку та REE 2 [Sm-Ho] та Y у другому, зумовлює різниця радіусів головного (Rk) та домішкового (Ri) катіонів: де Контролююче значення цього фактора в ізоморфізмі REE(3+) та Y(3+) ілюструє монотонна залежність коефіцієнта розподілу мінерал/розплав (Di) від ΔRi. Очевидно, що чим меньше абсолютне значення Δ Ri , тим вища здатність мінерала до ізоморфного накопичення елемента i при інших рівних умовах.
«Розмірний» (Ri) фактор ізоморфізму: Наприклад, “лантанофільність” та “ітрофільність” мінералів, тобто їх здатність до селективного ізоморфного накопичення REE 1 [La-Nd] замість REE 3 (Er-Lu) у першому випадку та REE 2 [Sm-Ho] та Y у другому, зумовлює різниця радіусів головного (Rk) та домішкового (Ri) катіонів: де Контролююче значення цього фактора в ізоморфізмі REE(3+) та Y(3+) ілюструє монотонна залежність коефіцієнта розподілу мінерал/розплав (Di) від ΔRi. Очевидно, що чим меньше абсолютне значення Δ Ri , тим вища здатність мінерала до ізоморфного накопичення елемента i при інших рівних умовах.
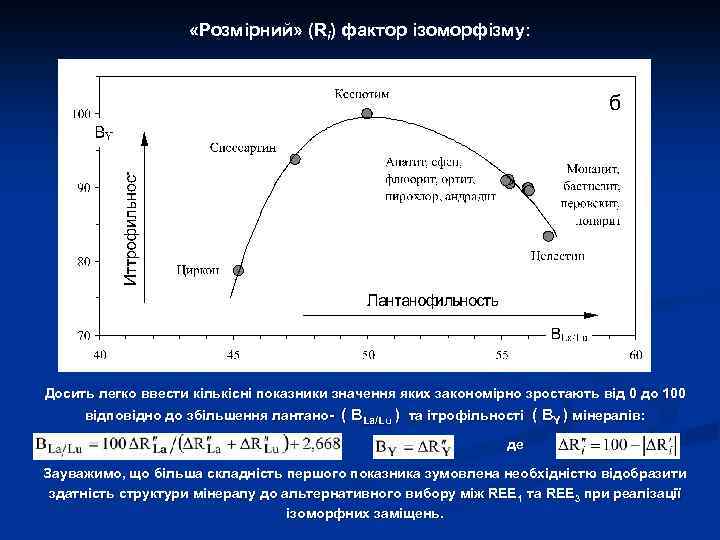 «Розмірний» (Ri) фактор ізоморфізму: Досить легко ввести кількісні показники значення яких закономірно зростають від 0 до 100 відповідно до збільшення лантано- ( BLa/Lu ) та ітрофільності ( BY ) мінералів: La/Lu де Зауважимо, що більша складність першого показника зумовлена необхідністю відобразити здатність структури мінералу до альтернативного вибору між REE 1 та REE 3 при реалізації ізоморфних заміщень.
«Розмірний» (Ri) фактор ізоморфізму: Досить легко ввести кількісні показники значення яких закономірно зростають від 0 до 100 відповідно до збільшення лантано- ( BLa/Lu ) та ітрофільності ( BY ) мінералів: La/Lu де Зауважимо, що більша складність першого показника зумовлена необхідністю відобразити здатність структури мінералу до альтернативного вибору між REE 1 та REE 3 при реалізації ізоморфних заміщень.
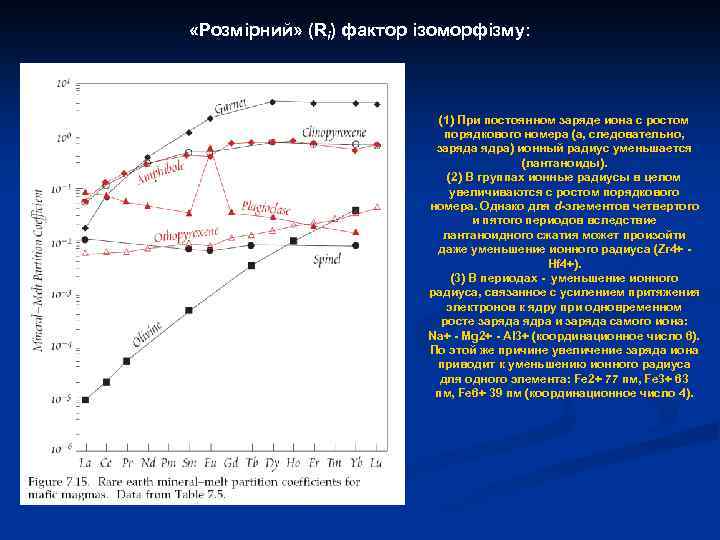 «Розмірний» (Ri) фактор ізоморфізму: (1) При постоянном заряде иона с ростом порядкового номера (а, следовательно, заряда ядра) ионный радиус уменьшается (лантаноиды). (2) В группах ионные радиусы в целом увеличиваются с ростом порядкового номера. Однако для d-элементов четвертого и пятого периодов вследствие лантаноидного сжатия может произойти даже уменьшение ионного радиуса (Zr 4+ - Hf 4+). (3) В периодах - уменьшение ионного радиуса, связанное с усилением притяжения электронов к ядру при одновременном росте заряда ядра и заряда самого иона: Na+ - Mg 2+ - Al 3+ (координационное число 6). По этой же причине увеличение заряда иона приводит к уменьшению ионного радиуса для одного элемента: Fe 2+ 77 пм, Fe 3+ 63 пм, Fe 6+ 39 пм (координационное число 4).
«Розмірний» (Ri) фактор ізоморфізму: (1) При постоянном заряде иона с ростом порядкового номера (а, следовательно, заряда ядра) ионный радиус уменьшается (лантаноиды). (2) В группах ионные радиусы в целом увеличиваются с ростом порядкового номера. Однако для d-элементов четвертого и пятого периодов вследствие лантаноидного сжатия может произойти даже уменьшение ионного радиуса (Zr 4+ - Hf 4+). (3) В периодах - уменьшение ионного радиуса, связанное с усилением притяжения электронов к ядру при одновременном росте заряда ядра и заряда самого иона: Na+ - Mg 2+ - Al 3+ (координационное число 6). По этой же причине увеличение заряда иона приводит к уменьшению ионного радиуса для одного элемента: Fe 2+ 77 пм, Fe 3+ 63 пм, Fe 6+ 39 пм (координационное число 4).
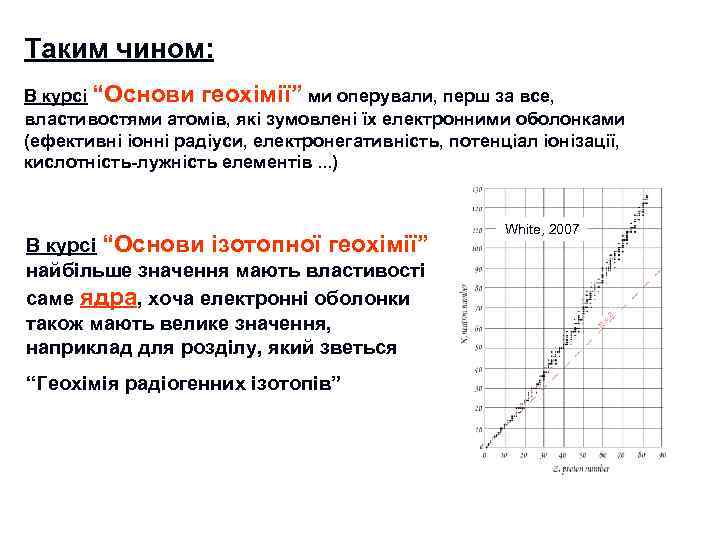 Таким чином: В курсі “Основи геохімії” ми оперували, перш за все, властивостями атомів, які зумовлені їх електронними оболонками (ефективні іонні радіуси, електронегативність, потенціал іонізації, кислотність-лужність елементів. . . ) В курсі “Основи ізотопної геохімії” найбільше значення мають властивості саме ядра, хоча електронні оболонки також мають велике значення, наприклад для розділу, який зветься “Геохімія радіогенних ізотопів” White, 2007
Таким чином: В курсі “Основи геохімії” ми оперували, перш за все, властивостями атомів, які зумовлені їх електронними оболонками (ефективні іонні радіуси, електронегативність, потенціал іонізації, кислотність-лужність елементів. . . ) В курсі “Основи ізотопної геохімії” найбільше значення мають властивості саме ядра, хоча електронні оболонки також мають велике значення, наприклад для розділу, який зветься “Геохімія радіогенних ізотопів” White, 2007
 Головні завдання та розділи ізотопної геохімії: n Визначення віку мінералів та гірських порід, датування процесів їх утворення. Відповідний розділ має назву “Ізотопна геохронологія”. n Дослідження геологічних процесів за допомогою використання ізотопів в якості природних “мічених атомів”. Основою цього підходу є контрасна геохімічна поведінка радіоактивних ізотопів (курс “Основи геохімії”!!!) – одних породах вони концентруються, а з інших виносяться (U, Th, Rb – несумісні елементи!!!). Наприклад, корові породи збагачені Rb, та, як наслідок, вміщують значно більше радіогенного 87 Sr (85 Rb – стабільний, 72%, а 87 Rb – радіоактивний, 28% дає 87 Sr) ніж мантійні деплетовані породи. Тому співвідношення 87 Sr/ 86 Sr (86 Sr – стабільний та нерадіогенний, один з 4 – 88 найбільш поширений , 87, 86, 84 ) – індикатор рівня мобілізації речовини. Відповідний розділ має назву “Геохімія радіогенних ізотопів”. n Дослідження поведінки ізотопів легких елементів (кисень, вуглець, сірка. . . ) в залежності від PTX-умов геохімічних процесів, та вирішення зворотної задачі – реставрування цих умов за спостереженими ізотопно-геохімічними даними. Відповідний розділ має назву “Геохімія стабільних ізотопів” n Ще раз: ізотопна геохімія – частина геохімії, яка оперує концентраціями ізотопів. Значення цих концентрацій – досить низьке. Тому ізотопна геохімя – найбільш прецизійна, кількісна та “фізична” частина геохімії.
Головні завдання та розділи ізотопної геохімії: n Визначення віку мінералів та гірських порід, датування процесів їх утворення. Відповідний розділ має назву “Ізотопна геохронологія”. n Дослідження геологічних процесів за допомогою використання ізотопів в якості природних “мічених атомів”. Основою цього підходу є контрасна геохімічна поведінка радіоактивних ізотопів (курс “Основи геохімії”!!!) – одних породах вони концентруються, а з інших виносяться (U, Th, Rb – несумісні елементи!!!). Наприклад, корові породи збагачені Rb, та, як наслідок, вміщують значно більше радіогенного 87 Sr (85 Rb – стабільний, 72%, а 87 Rb – радіоактивний, 28% дає 87 Sr) ніж мантійні деплетовані породи. Тому співвідношення 87 Sr/ 86 Sr (86 Sr – стабільний та нерадіогенний, один з 4 – 88 найбільш поширений , 87, 86, 84 ) – індикатор рівня мобілізації речовини. Відповідний розділ має назву “Геохімія радіогенних ізотопів”. n Дослідження поведінки ізотопів легких елементів (кисень, вуглець, сірка. . . ) в залежності від PTX-умов геохімічних процесів, та вирішення зворотної задачі – реставрування цих умов за спостереженими ізотопно-геохімічними даними. Відповідний розділ має назву “Геохімія стабільних ізотопів” n Ще раз: ізотопна геохімія – частина геохімії, яка оперує концентраціями ізотопів. Значення цих концентрацій – досить низьке. Тому ізотопна геохімя – найбільш прецизійна, кількісна та “фізична” частина геохімії.
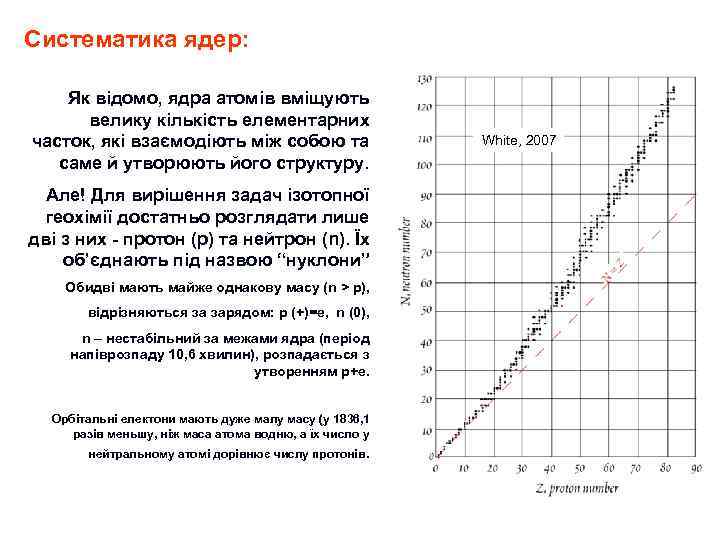 Систематика ядер: Як відомо, ядра атомів вміщують велику кількість елементарних часток, які взаємодіють між собою та саме й утворюють його структуру. Але! Для вирішення задач ізотопної геохімії достатньо розглядати лише дві з них - протон (p) та нейтрон (n). Їх об’єднають під назвою “нуклони” Обидві мають майже однакову масу (n > p), відрізняються за зарядом: p (+)=е, n (0), n – нестабільний за межами ядра (період напіврозпаду 10, 6 хвилин), розпадається з утворенням p+e. Орбітальні електони мають дуже малу масу (у 1836, 1 разів меньшу, ніж маса атома водню, а їх число у нейтральному атомі дорівнює числу протонів. White, 2007
Систематика ядер: Як відомо, ядра атомів вміщують велику кількість елементарних часток, які взаємодіють між собою та саме й утворюють його структуру. Але! Для вирішення задач ізотопної геохімії достатньо розглядати лише дві з них - протон (p) та нейтрон (n). Їх об’єднають під назвою “нуклони” Обидві мають майже однакову масу (n > p), відрізняються за зарядом: p (+)=е, n (0), n – нестабільний за межами ядра (період напіврозпаду 10, 6 хвилин), розпадається з утворенням p+e. Орбітальні електони мають дуже малу масу (у 1836, 1 разів меньшу, ніж маса атома водню, а їх число у нейтральному атомі дорівнює числу протонів. White, 2007
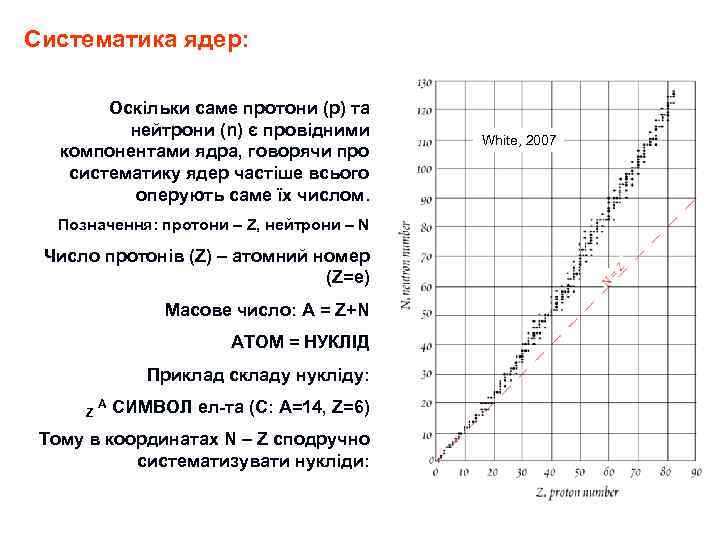 Систематика ядер: Оскільки саме протони (p) та нейтрони (n) є провідними компонентами ядра, говорячи про систематику ядер частіше всього оперують саме їх числом. Позначення: протони – Z, нейтрони – N Число протонів (Z) – атомний номер (Z=e) Масове число: A = Z+N АТОМ = НУКЛІД Приклад складу нукліду: Z A СИМВОЛ ел-та (C: A=14, Z=6) Тому в координатах N – Z сподручно систематизувати нукліди: White, 2007
Систематика ядер: Оскільки саме протони (p) та нейтрони (n) є провідними компонентами ядра, говорячи про систематику ядер частіше всього оперують саме їх числом. Позначення: протони – Z, нейтрони – N Число протонів (Z) – атомний номер (Z=e) Масове число: A = Z+N АТОМ = НУКЛІД Приклад складу нукліду: Z A СИМВОЛ ел-та (C: A=14, Z=6) Тому в координатах N – Z сподручно систематизувати нукліди: White, 2007
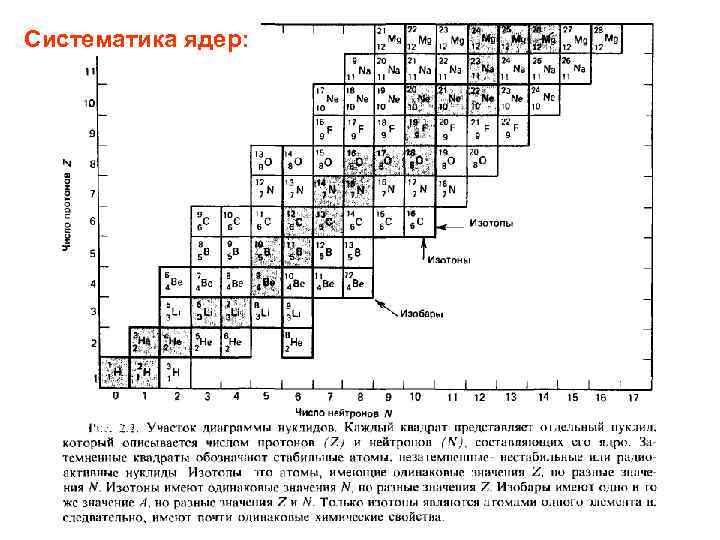 Систематика ядер:
Систематика ядер:
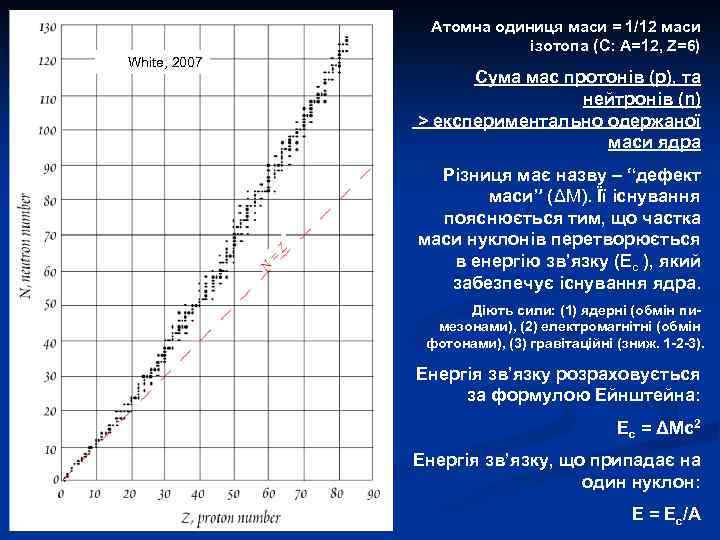 White, 2007 Атомна одиниця маси = 1/12 маси ізотопа (C: A=12, Z=6) Cума мас протонів (p), та нейтронів (n) > експериментально одержаної маси ядра Різниця має назву – “дефект маси” (ΔM). Її існування пояснюється тим, що частка маси нуклонів перетворюється в енергію зв’язку (Ec ), який забезпечує існування ядра. Діють сили: (1) ядерні (обмін пимезонами), (2) електромагнітні (обмін фотонами), (3) гравітаційні (зниж. 1 -2 -3). Енергія зв’язку розраховується за формулою Ейнштейна: Ec = ΔMc 2 Енергія зв’язку, що припадає на один нуклон: E = Ec/A
White, 2007 Атомна одиниця маси = 1/12 маси ізотопа (C: A=12, Z=6) Cума мас протонів (p), та нейтронів (n) > експериментально одержаної маси ядра Різниця має назву – “дефект маси” (ΔM). Її існування пояснюється тим, що частка маси нуклонів перетворюється в енергію зв’язку (Ec ), який забезпечує існування ядра. Діють сили: (1) ядерні (обмін пимезонами), (2) електромагнітні (обмін фотонами), (3) гравітаційні (зниж. 1 -2 -3). Енергія зв’язку розраховується за формулою Ейнштейна: Ec = ΔMc 2 Енергія зв’язку, що припадає на один нуклон: E = Ec/A
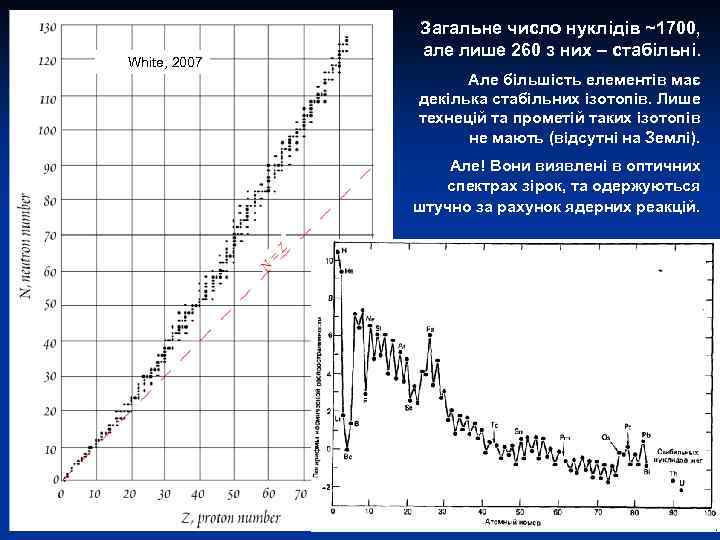 White, 2007 Загальне число нуклідів ~1700, але лише 260 з них – стабільні. Але більшість елементів має декілька стабільних ізотопів. Лише технецій та прометій таких ізотопів не мають (відсутні на Землі). Але! Вони виявлені в оптичних спектрах зірок, та одержуються штучно за рахунок ядерних реакцій.
White, 2007 Загальне число нуклідів ~1700, але лише 260 з них – стабільні. Але більшість елементів має декілька стабільних ізотопів. Лише технецій та прометій таких ізотопів не мають (відсутні на Землі). Але! Вони виявлені в оптичних спектрах зірок, та одержуються штучно за рахунок ядерних реакцій.
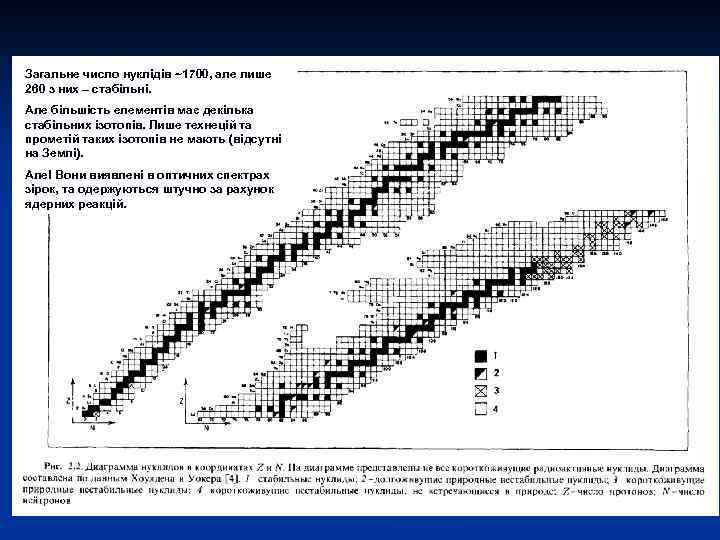 Загальне число нуклідів ~1700, але лише 260 з них – стабільні. Але більшість елементів має декілька стабільних ізотопів. Лише технецій та прометій таких ізотопів не мають (відсутні на Землі). Але! Вони виявлені в оптичних спектрах зірок, та одержуються штучно за рахунок ядерних реакцій.
Загальне число нуклідів ~1700, але лише 260 з них – стабільні. Але більшість елементів має декілька стабільних ізотопів. Лише технецій та прометій таких ізотопів не мають (відсутні на Землі). Але! Вони виявлені в оптичних спектрах зірок, та одержуються штучно за рахунок ядерних реакцій.
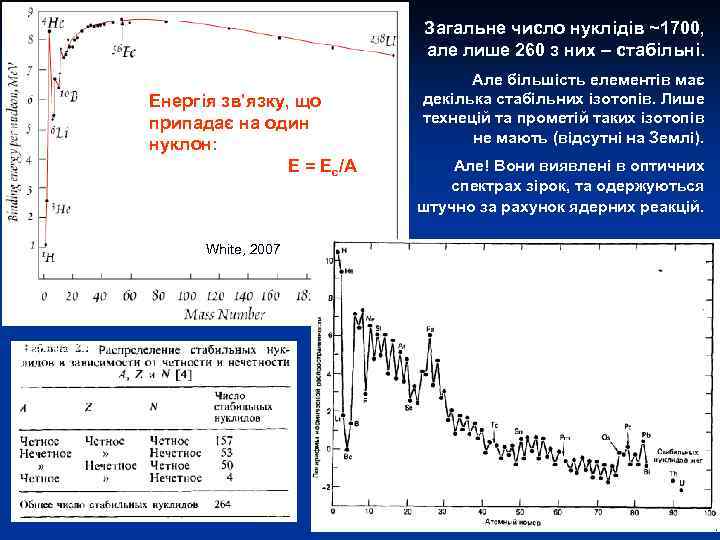 Загальне число нуклідів ~1700, але лише 260 з них – стабільні. Енергія зв’язку, що припадає на один нуклон: E = Ec/A White, 2007 Але більшість елементів має декілька стабільних ізотопів. Лише технецій та прометій таких ізотопів не мають (відсутні на Землі). Але! Вони виявлені в оптичних спектрах зірок, та одержуються штучно за рахунок ядерних реакцій.
Загальне число нуклідів ~1700, але лише 260 з них – стабільні. Енергія зв’язку, що припадає на один нуклон: E = Ec/A White, 2007 Але більшість елементів має декілька стабільних ізотопів. Лише технецій та прометій таких ізотопів не мають (відсутні на Землі). Але! Вони виявлені в оптичних спектрах зірок, та одержуються штучно за рахунок ядерних реакцій.
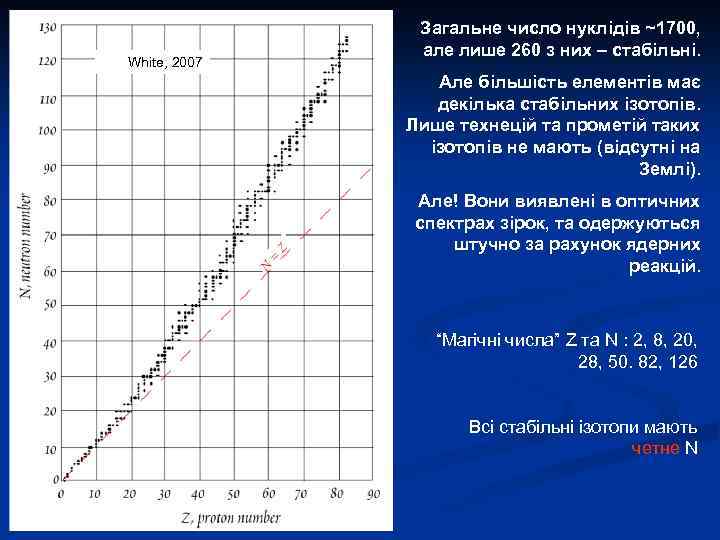 White, 2007 Загальне число нуклідів ~1700, але лише 260 з них – стабільні. Але більшість елементів має декілька стабільних ізотопів. Лише технецій та прометій таких ізотопів не мають (відсутні на Землі). Але! Вони виявлені в оптичних спектрах зірок, та одержуються штучно за рахунок ядерних реакцій. “Магічні числа” Z та N : 2, 8, 20, 28, 50. 82, 126 Всі стабільні ізотопи мають четне N
White, 2007 Загальне число нуклідів ~1700, але лише 260 з них – стабільні. Але більшість елементів має декілька стабільних ізотопів. Лише технецій та прометій таких ізотопів не мають (відсутні на Землі). Але! Вони виявлені в оптичних спектрах зірок, та одержуються штучно за рахунок ядерних реакцій. “Магічні числа” Z та N : 2, 8, 20, 28, 50. 82, 126 Всі стабільні ізотопи мають четне N
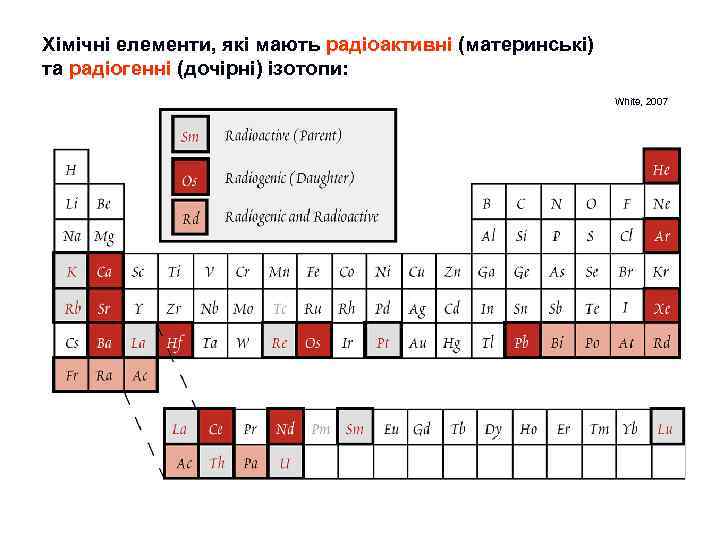 Хімічні елементи, які мають радіоактивні (материнські) та радіогенні (дочірні) ізотопи: White, 2007
Хімічні елементи, які мають радіоактивні (материнські) та радіогенні (дочірні) ізотопи: White, 2007
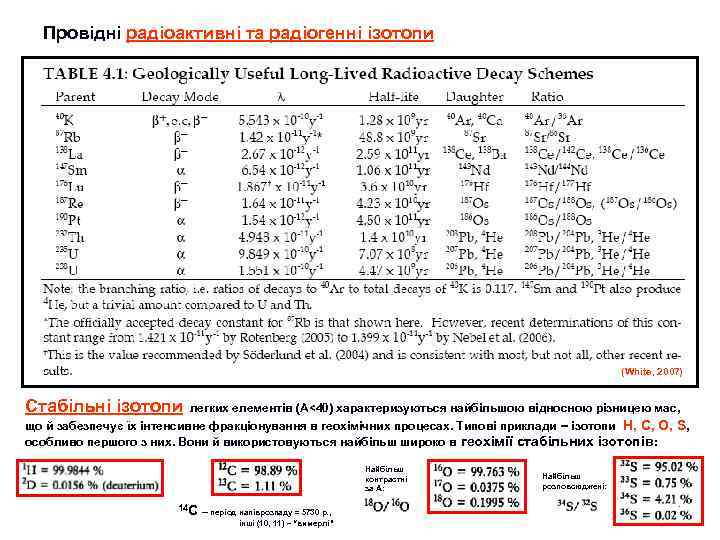 Провідні радіоактивні та радіогенні ізотопи (White, 2007) Стабільні ізотопи легких елементів (A<40) характеризуються найбільшою відносною різницею мас, що й забезпечує їх інтенсивне фракціонування в геохімічних процесах. Типові приклади − ізотопи H, C, O, S, особливо першого з них. Вони й використовуються найбільш широко в геохімії стабільних ізотопів: Найбільш контрастні за А: 14 C – період напіврозпаду = 5730 р. , інші (10, 11) – “вимерлі” Найбільш розповсюджені:
Провідні радіоактивні та радіогенні ізотопи (White, 2007) Стабільні ізотопи легких елементів (A<40) характеризуються найбільшою відносною різницею мас, що й забезпечує їх інтенсивне фракціонування в геохімічних процесах. Типові приклади − ізотопи H, C, O, S, особливо першого з них. Вони й використовуються найбільш широко в геохімії стабільних ізотопів: Найбільш контрастні за А: 14 C – період напіврозпаду = 5730 р. , інші (10, 11) – “вимерлі” Найбільш розповсюджені:
 Ще раз: Головні завдання та розділи ізотопної геохімії: n Визначення віку мінералів та гірських порід, датування процесів їх утворення. Відповідний розділ має назву “Ізотопна геохронологія”. n Дослідження геологічних процесів за допомогою використання ізотопів в якості природних “мічених атомів”. Основою цього підходу є контрасна геохімічна поведінка радіоактивних ізотопів (курс “Основи геохімії”!!!) – одних породах вони концентруються, а з інших виносяться (U, Th, Rb – несумісні елементи!!!). Наприклад, корові породи збагачені Rb, та, як наслідок, вміщують значно більше радіогенного 87 Sr (85 Rb – стабільний, 72%, а 87 Rb – радіоактивний, 28% дає 87 Sr) ніж мантійні деплетовані породи. Тому співвідношення 87 Sr/ 86 Sr (86 Sr – стабільний та нерадіогенний, один з 4 – 88 найбільш поширений , 87, 86, 84 ) – індикатор рівня мобілізації речовини. Відповідний розділ має назву “Геохімія радіогенних ізотопів”. n Дослідження поведінки ізотопів легких елементів (кисень, вуглець, сірка. . . ) в залежності від PTX-умов геохімічних процесів, та вирішення зворотної задачі – реставрування цих умов за спостереженими ізотопно-геохімічними даними. Відповідний розділ має назву “Геохімія стабільних ізотопів” n Ще раз: ізотопна геохімія – частина геохімії, яка оперує концентраціями ізотопів. Значення цих концентрацій – досить низьке. Тому ізотопна геохімія – найбільш прецизійна, кількісна та “фізична” частина геохімії.
Ще раз: Головні завдання та розділи ізотопної геохімії: n Визначення віку мінералів та гірських порід, датування процесів їх утворення. Відповідний розділ має назву “Ізотопна геохронологія”. n Дослідження геологічних процесів за допомогою використання ізотопів в якості природних “мічених атомів”. Основою цього підходу є контрасна геохімічна поведінка радіоактивних ізотопів (курс “Основи геохімії”!!!) – одних породах вони концентруються, а з інших виносяться (U, Th, Rb – несумісні елементи!!!). Наприклад, корові породи збагачені Rb, та, як наслідок, вміщують значно більше радіогенного 87 Sr (85 Rb – стабільний, 72%, а 87 Rb – радіоактивний, 28% дає 87 Sr) ніж мантійні деплетовані породи. Тому співвідношення 87 Sr/ 86 Sr (86 Sr – стабільний та нерадіогенний, один з 4 – 88 найбільш поширений , 87, 86, 84 ) – індикатор рівня мобілізації речовини. Відповідний розділ має назву “Геохімія радіогенних ізотопів”. n Дослідження поведінки ізотопів легких елементів (кисень, вуглець, сірка. . . ) в залежності від PTX-умов геохімічних процесів, та вирішення зворотної задачі – реставрування цих умов за спостереженими ізотопно-геохімічними даними. Відповідний розділ має назву “Геохімія стабільних ізотопів” n Ще раз: ізотопна геохімія – частина геохімії, яка оперує концентраціями ізотопів. Значення цих концентрацій – досить низьке. Тому ізотопна геохімія – найбільш прецизійна, кількісна та “фізична” частина геохімії.
 Методи визначення ізотопного складу природних об’єктів
Методи визначення ізотопного складу природних об’єктів
 Згадаємо! Розділи геохімії: n Геохімія геосфер (кори, мантії, атмосфери, гідросфери). Геохімія природних, в тому числі рудогенеруючих систем/процесів (магматичних, гідротермальних, метаморфічних, тощо). Геохімія окремих елементів та їх груп (геохімія платиноїдів, елементів групи заліза, рідкісних елементів, рідкісноземельних елементів, радіоактивних елементів, тощо). Ізотопна геохімія (визначення віку геологічних утворень, встановлення генетичного зв’язку рудної речовини з різноманітними ендогенними джерелами, оцінка пропорцій змішування різних джерел речовини та їх хімічного складу, термометрія). Біогеохімія. Геохімія техногенезу та екологічна геохімія. Пошукова геохімія. n Аналітична геохімія n n n
Згадаємо! Розділи геохімії: n Геохімія геосфер (кори, мантії, атмосфери, гідросфери). Геохімія природних, в тому числі рудогенеруючих систем/процесів (магматичних, гідротермальних, метаморфічних, тощо). Геохімія окремих елементів та їх груп (геохімія платиноїдів, елементів групи заліза, рідкісних елементів, рідкісноземельних елементів, радіоактивних елементів, тощо). Ізотопна геохімія (визначення віку геологічних утворень, встановлення генетичного зв’язку рудної речовини з різноманітними ендогенними джерелами, оцінка пропорцій змішування різних джерел речовини та їх хімічного складу, термометрія). Біогеохімія. Геохімія техногенезу та екологічна геохімія. Пошукова геохімія. n Аналітична геохімія n n n
 Згадаємо! Ці завдання геохімія вирішує за допомогою раціональної системи методів - дослідницьких “інструментів” кожного її розділу: n Аналітичні методи n Статистичний аналіз n Термодинамічний аналіз n Кількісне геохімічне моделювання процесів та систем
Згадаємо! Ці завдання геохімія вирішує за допомогою раціональної системи методів - дослідницьких “інструментів” кожного її розділу: n Аналітичні методи n Статистичний аналіз n Термодинамічний аналіз n Кількісне геохімічне моделювання процесів та систем
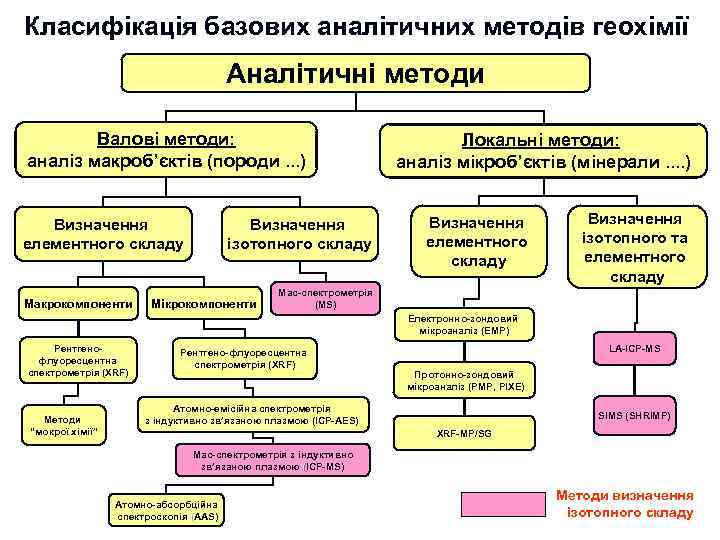 Класифікація базових аналітичних методів геохімії Аналітичні методи Валові методи: аналіз макроб’єктів (породи. . . ) Визначення елементного складу Макрокомпоненти Визначення ізотопного складу Мікрокомпоненти Локальні методи: аналіз мікроб’єктів (мінерали. . ) Визначення елементного складу Визначення ізотопного та елементного складу Мас-спектрометрія (MS) Електронно-зондовий мікроаналіз (EMP) Рентгенофлуоресцентна спектрометрія (XRF) Методи “мокрої хімії” Рентгено-флуоресцентна спектрометрія (XRF) LA-ICP-MS Протонно-зондовий мікроаналіз (PMP, PIXE) Атомно-емісійна спектрометрія з індуктивно зв’язаною плазмою (ICP-AES) SIMS (SHRIMP) XRF-MP/SG Мас-спектрометрія з індуктивно зв’язаною плазмою (ICP-MS) ( Атомно-абсорбційна спектроскопія (AAS) ( Методи визначення ізотопного складу
Класифікація базових аналітичних методів геохімії Аналітичні методи Валові методи: аналіз макроб’єктів (породи. . . ) Визначення елементного складу Макрокомпоненти Визначення ізотопного складу Мікрокомпоненти Локальні методи: аналіз мікроб’єктів (мінерали. . ) Визначення елементного складу Визначення ізотопного та елементного складу Мас-спектрометрія (MS) Електронно-зондовий мікроаналіз (EMP) Рентгенофлуоресцентна спектрометрія (XRF) Методи “мокрої хімії” Рентгено-флуоресцентна спектрометрія (XRF) LA-ICP-MS Протонно-зондовий мікроаналіз (PMP, PIXE) Атомно-емісійна спектрометрія з індуктивно зв’язаною плазмою (ICP-AES) SIMS (SHRIMP) XRF-MP/SG Мас-спектрометрія з індуктивно зв’язаною плазмою (ICP-MS) ( Атомно-абсорбційна спектроскопія (AAS) ( Методи визначення ізотопного складу
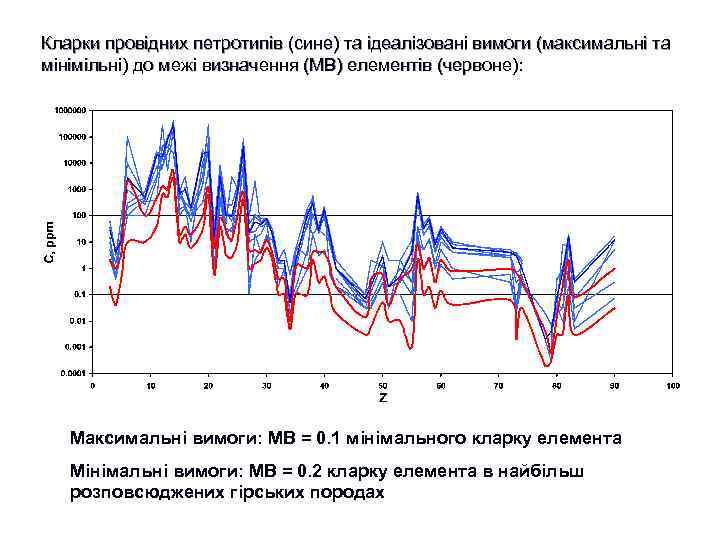 Кларки провідних петротипів (сине) та ідеалізовані вимоги (максимальні та мінімільні) до межі визначення (МВ) елементів (червоне): Максимальні вимоги: МВ = 0. 1 мінімального кларку елемента Мінімальні вимоги: МВ = 0. 2 кларку елемента в найбільш розповсюджених гірських породах
Кларки провідних петротипів (сине) та ідеалізовані вимоги (максимальні та мінімільні) до межі визначення (МВ) елементів (червоне): Максимальні вимоги: МВ = 0. 1 мінімального кларку елемента Мінімальні вимоги: МВ = 0. 2 кларку елемента в найбільш розповсюджених гірських породах
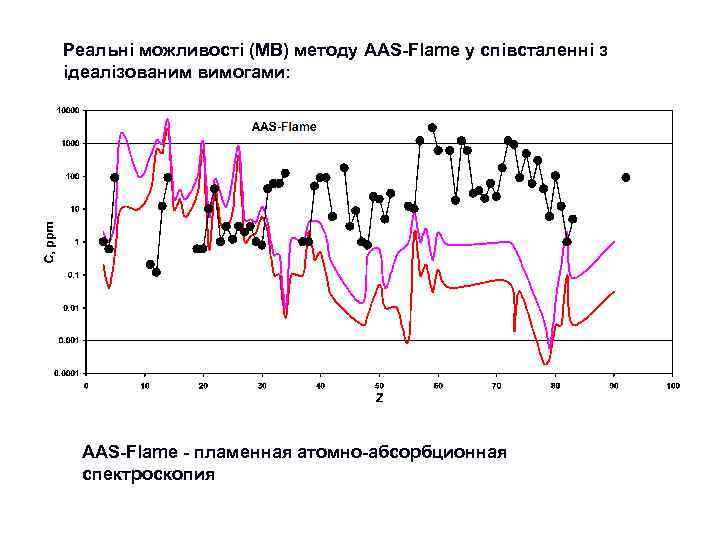 Реальні можливості (МВ) методу AAS-Flame у співсталенні з ідеалізованим вимогами: AAS-Flame - пламенная атомно-абсорбционная спектроскопия
Реальні можливості (МВ) методу AAS-Flame у співсталенні з ідеалізованим вимогами: AAS-Flame - пламенная атомно-абсорбционная спектроскопия
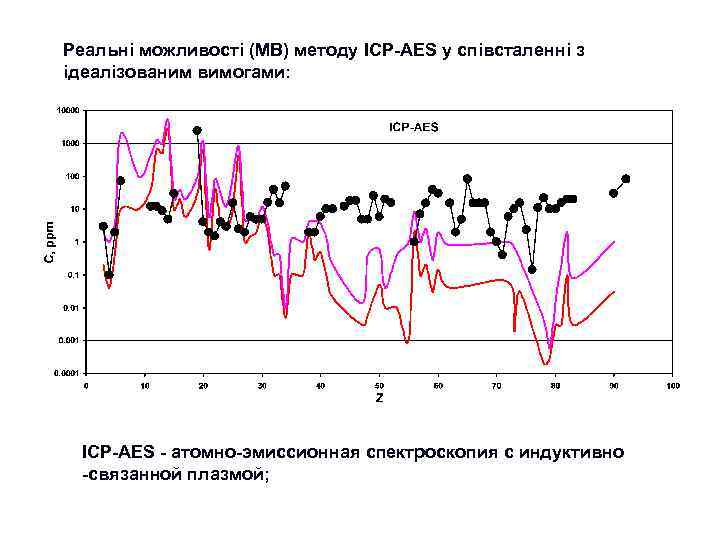 Реальні можливості (МВ) методу ICP-AES у співсталенні з ідеалізованим вимогами: ICP-AES - атомно-эмиссионная спектроскопия с индуктивно -связанной плазмой;
Реальні можливості (МВ) методу ICP-AES у співсталенні з ідеалізованим вимогами: ICP-AES - атомно-эмиссионная спектроскопия с индуктивно -связанной плазмой;
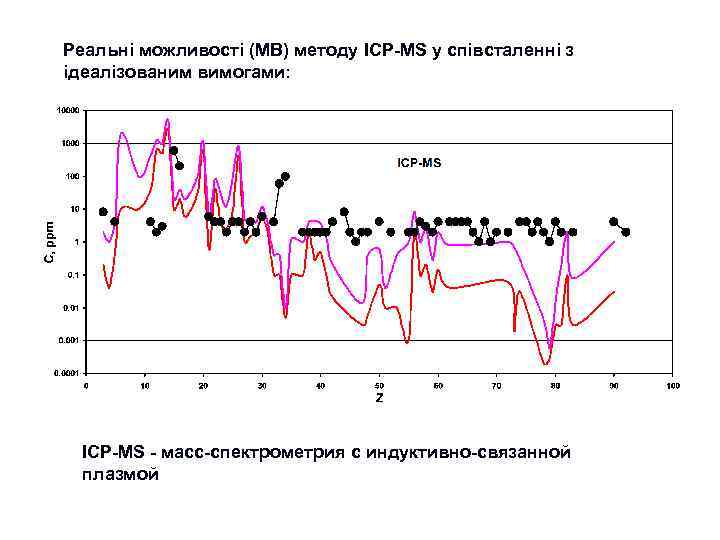 Реальні можливості (МВ) методу ICP-MS у співсталенні з ідеалізованим вимогами: ICP-MS - масс-спектрометрия с индуктивно-связанной плазмой
Реальні можливості (МВ) методу ICP-MS у співсталенні з ідеалізованим вимогами: ICP-MS - масс-спектрометрия с индуктивно-связанной плазмой
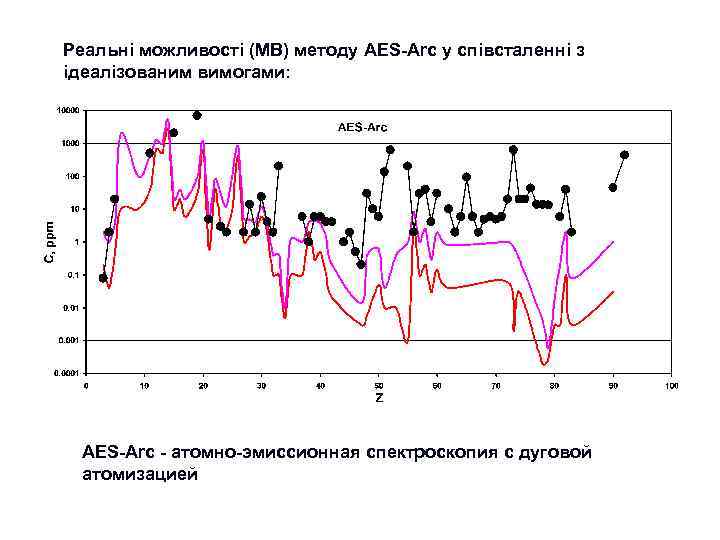 Реальні можливості (МВ) методу AES-Arc у співсталенні з ідеалізованим вимогами: AES-Arc - атомно-эмиссионная спектроскопия с дуговой атомизацией
Реальні можливості (МВ) методу AES-Arc у співсталенні з ідеалізованим вимогами: AES-Arc - атомно-эмиссионная спектроскопия с дуговой атомизацией
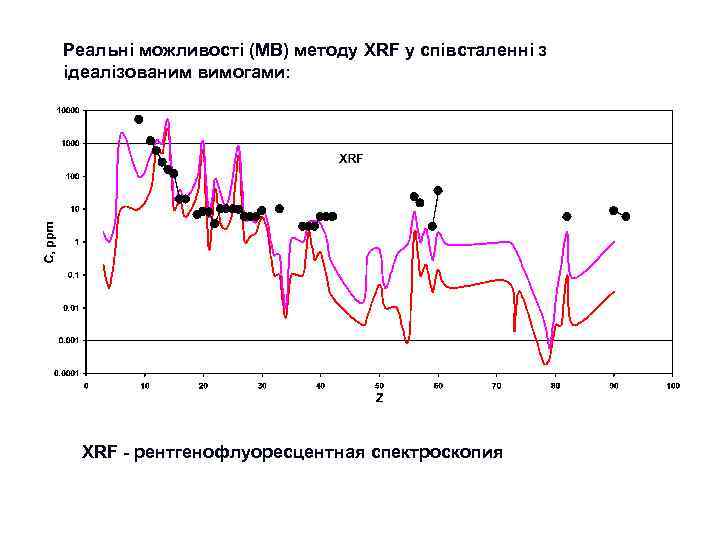 Реальні можливості (МВ) методу XRF у співсталенні з ідеалізованим вимогами: XRF - рентгенофлуоресцентная спектроскопия
Реальні можливості (МВ) методу XRF у співсталенні з ідеалізованим вимогами: XRF - рентгенофлуоресцентная спектроскопия
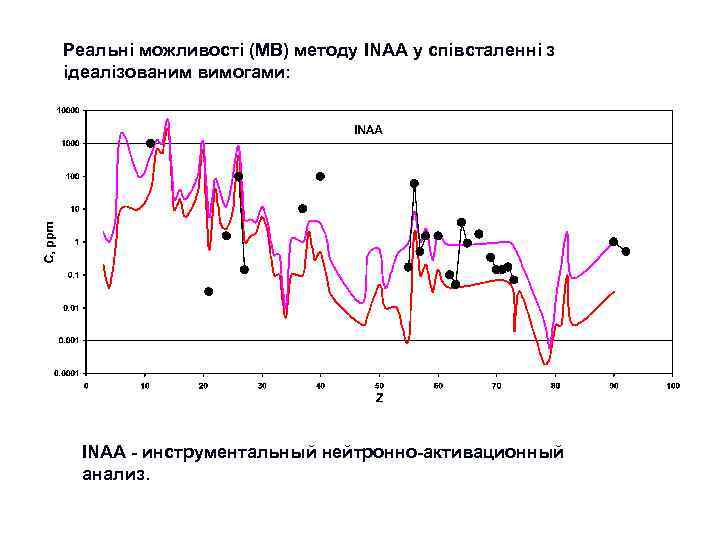 Реальні можливості (МВ) методу INAA у співсталенні з ідеалізованим вимогами: INAA - инструментальный нейтронно-активационный анализ.
Реальні можливості (МВ) методу INAA у співсталенні з ідеалізованим вимогами: INAA - инструментальный нейтронно-активационный анализ.
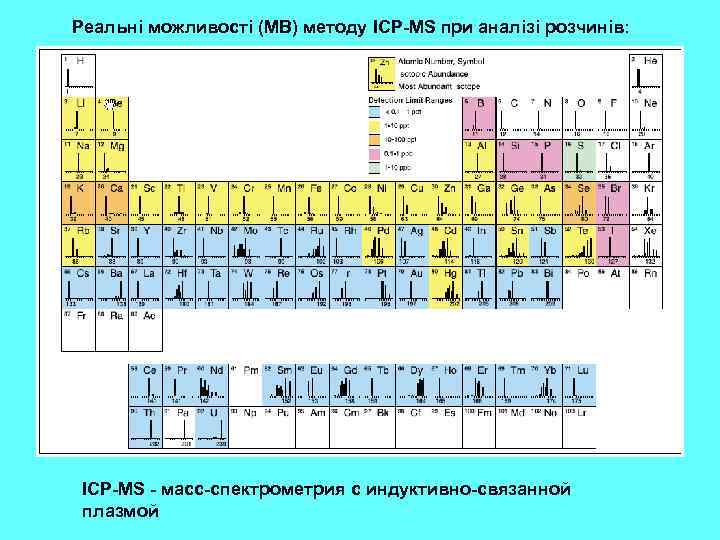 Реальні можливості (МВ) методу ICP-MS при аналізі розчинів: ICP-MS - масс-спектрометрия с индуктивно-связанной плазмой
Реальні можливості (МВ) методу ICP-MS при аналізі розчинів: ICP-MS - масс-спектрометрия с индуктивно-связанной плазмой
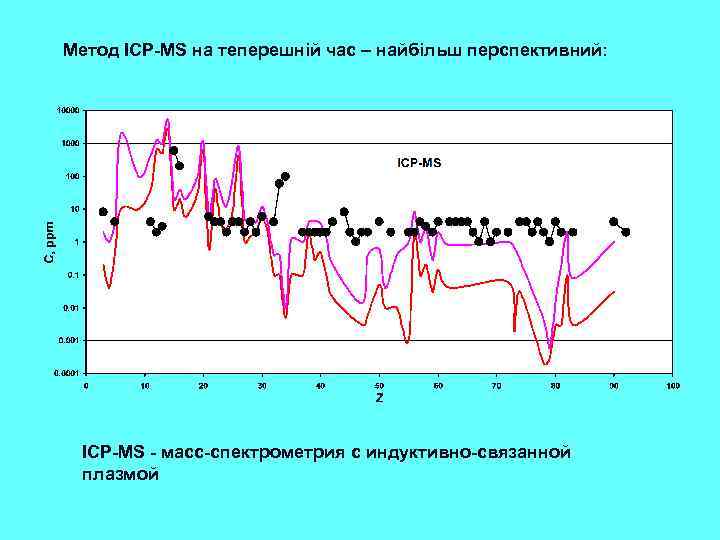 Метод ICP-MS на теперешній час – найбільш перспективний: ICP-MS - масс-спектрометрия с индуктивно-связанной плазмой
Метод ICP-MS на теперешній час – найбільш перспективний: ICP-MS - масс-спектрометрия с индуктивно-связанной плазмой
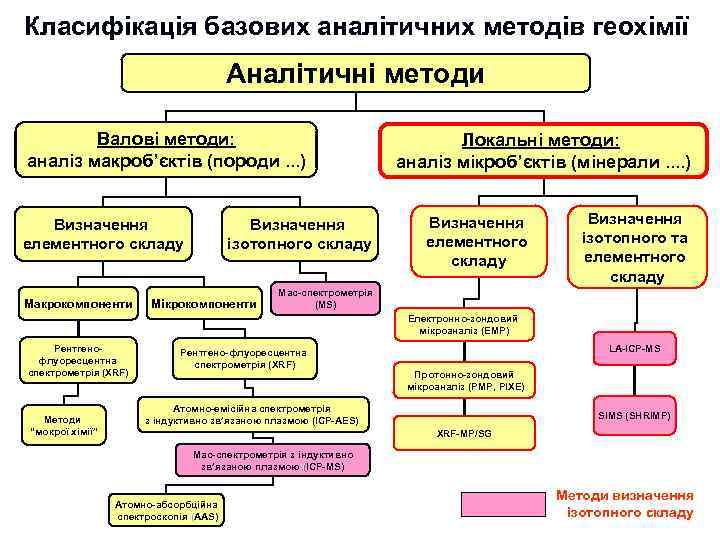 Класифікація базових аналітичних методів геохімії Аналітичні методи Валові методи: аналіз макроб’єктів (породи. . . ) Визначення елементного складу Макрокомпоненти Визначення ізотопного складу Мікрокомпоненти Локальні методи: аналіз мікроб’єктів (мінерали. . ) Визначення елементного складу Визначення ізотопного та елементного складу Мас-спектрометрія (MS) Електронно-зондовий мікроаналіз (EMP) Рентгенофлуоресцентна спектрометрія (XRF) Методи “мокрої хімії” Рентгено-флуоресцентна спектрометрія (XRF) LA-ICP-MS Протонно-зондовий мікроаналіз (PMP, PIXE) Атомно-емісійна спектрометрія з індуктивно зв’язаною плазмою (ICP-AES) SIMS (SHRIMP) XRF-MP/SG Мас-спектрометрія з індуктивно зв’язаною плазмою (ICP-MS) ( Атомно-абсорбційна спектроскопія (AAS) ( Методи визначення ізотопного складу
Класифікація базових аналітичних методів геохімії Аналітичні методи Валові методи: аналіз макроб’єктів (породи. . . ) Визначення елементного складу Макрокомпоненти Визначення ізотопного складу Мікрокомпоненти Локальні методи: аналіз мікроб’єктів (мінерали. . ) Визначення елементного складу Визначення ізотопного та елементного складу Мас-спектрометрія (MS) Електронно-зондовий мікроаналіз (EMP) Рентгенофлуоресцентна спектрометрія (XRF) Методи “мокрої хімії” Рентгено-флуоресцентна спектрометрія (XRF) LA-ICP-MS Протонно-зондовий мікроаналіз (PMP, PIXE) Атомно-емісійна спектрометрія з індуктивно зв’язаною плазмою (ICP-AES) SIMS (SHRIMP) XRF-MP/SG Мас-спектрометрія з індуктивно зв’язаною плазмою (ICP-MS) ( Атомно-абсорбційна спектроскопія (AAS) ( Методи визначення ізотопного складу
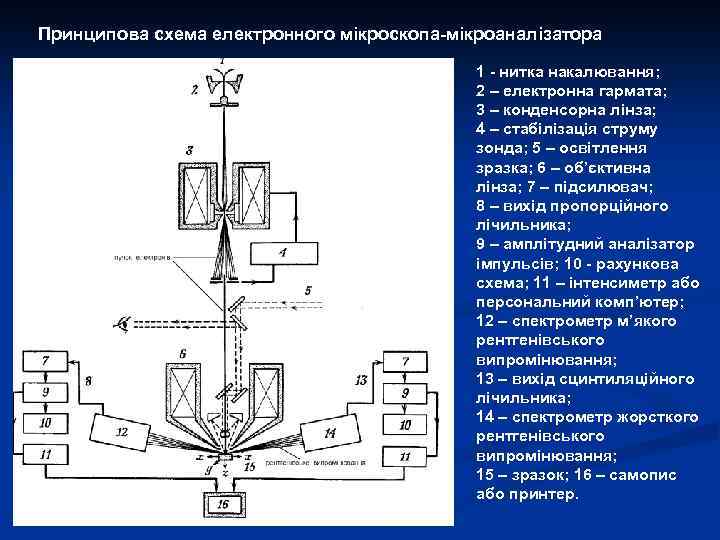 Принципова схема електронного мікроскопа-мікроаналізатора 1 - нитка накалювання; 2 – електронна гармата; 3 – конденсорна лінза; 4 – стабілізація струму зонда; 5 – освітлення зразка; 6 – об’єктивна лінза; 7 – підсилювач; 8 – вихід пропорційного лічильника; 9 – амплітудний аналізатор імпульсів; 10 - рахункова схема; 11 – інтенсиметр або персональний комп’ютер; 12 – спектрометр м’якого рентгенівського випромінювання; 13 – вихід сцинтиляційного лічильника; 14 – спектрометр жорсткого рентгенівського випромінювання; 15 – зразок; 16 – самопис або принтер.
Принципова схема електронного мікроскопа-мікроаналізатора 1 - нитка накалювання; 2 – електронна гармата; 3 – конденсорна лінза; 4 – стабілізація струму зонда; 5 – освітлення зразка; 6 – об’єктивна лінза; 7 – підсилювач; 8 – вихід пропорційного лічильника; 9 – амплітудний аналізатор імпульсів; 10 - рахункова схема; 11 – інтенсиметр або персональний комп’ютер; 12 – спектрометр м’якого рентгенівського випромінювання; 13 – вихід сцинтиляційного лічильника; 14 – спектрометр жорсткого рентгенівського випромінювання; 15 – зразок; 16 – самопис або принтер.
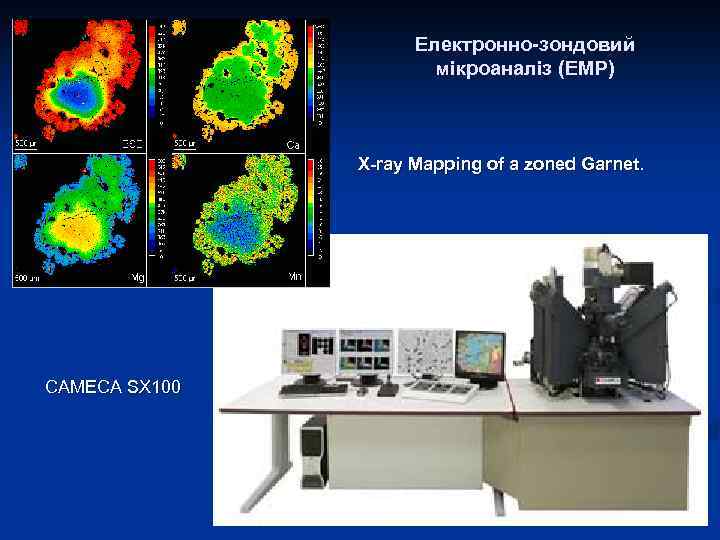 Електронно-зондовий мікроаналіз (EMP) X-ray Mapping of a zoned Garnet. CAMECA SX 100
Електронно-зондовий мікроаналіз (EMP) X-ray Mapping of a zoned Garnet. CAMECA SX 100
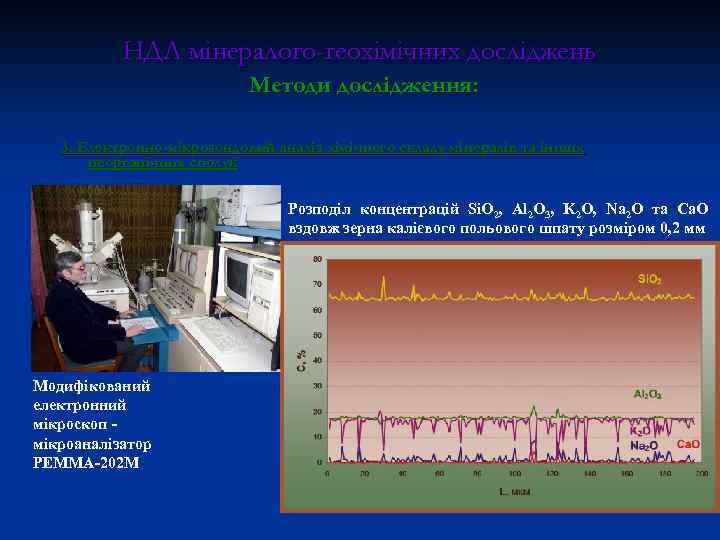 НДЛ мінералого-геохімічних досліджень Методи дослідження: 3. Електронно-мікрозондовий аналіз хімічного складу мінералів та інших неорганічних сполук Розподіл концентрацій Si. O 2, Al 2 O 3, K 2 O, Na 2 O та Ca. O вздовж зерна калієвого польового шпату розміром 0, 2 мм Модифікований електронний мікроскоп мікроаналізатор РЕММА-202 М
НДЛ мінералого-геохімічних досліджень Методи дослідження: 3. Електронно-мікрозондовий аналіз хімічного складу мінералів та інших неорганічних сполук Розподіл концентрацій Si. O 2, Al 2 O 3, K 2 O, Na 2 O та Ca. O вздовж зерна калієвого польового шпату розміром 0, 2 мм Модифікований електронний мікроскоп мікроаналізатор РЕММА-202 М
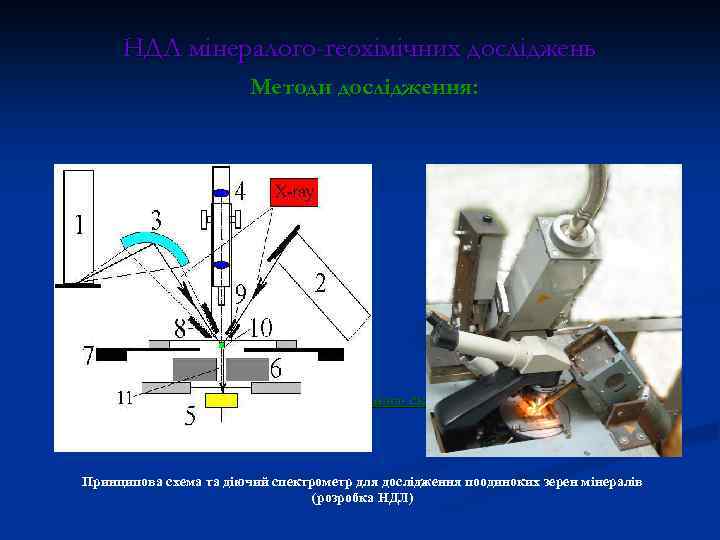 НДЛ мінералого-геохімічних досліджень Методи дослідження: 6. Рентгенофлуоресцентний аналіз хімічного складу поодиноких зерен мінералів розміром від 0. 02 мм Принципова схема та діючий спектрометр для дослідження поодиноких зерен мінералів (розробка НДЛ)
НДЛ мінералого-геохімічних досліджень Методи дослідження: 6. Рентгенофлуоресцентний аналіз хімічного складу поодиноких зерен мінералів розміром від 0. 02 мм Принципова схема та діючий спектрометр для дослідження поодиноких зерен мінералів (розробка НДЛ)
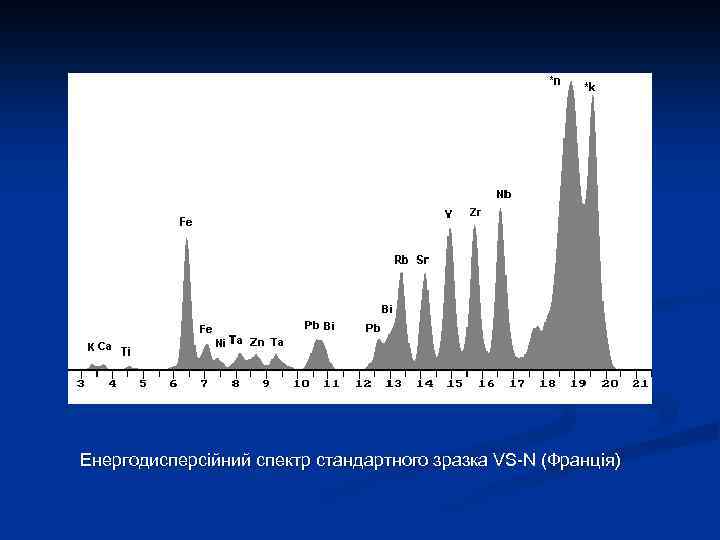 Енергодисперсійний спектр стандартного зразка VS-N (Франція)
Енергодисперсійний спектр стандартного зразка VS-N (Франція)
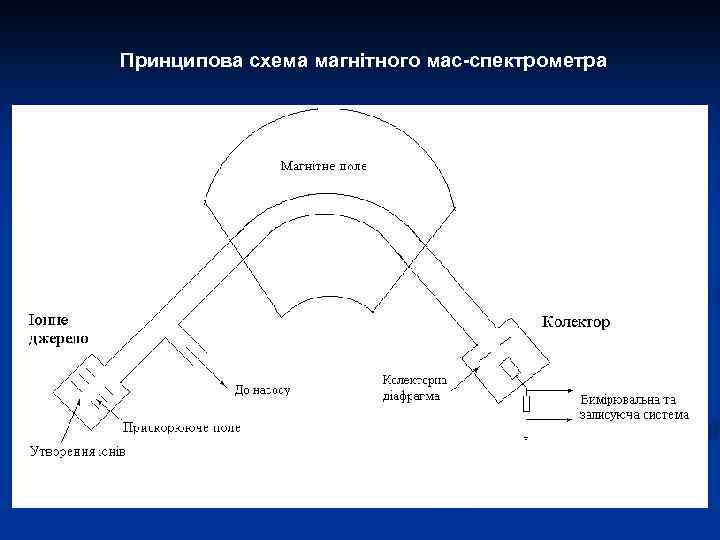 Принципова схема магнітного мас-спектрометра
Принципова схема магнітного мас-спектрометра
 Мас-спектрометрія вторинних іонів SIMS CAMECA IMS 7 f is a magnetic sector SIMS with top performances in trace element depth profiling and secondary ion microscopy. CAMECA IMS 1280 -LARGE RADIUS MAGNETIC SECTOR SIMS FOR GEOLOGY
Мас-спектрометрія вторинних іонів SIMS CAMECA IMS 7 f is a magnetic sector SIMS with top performances in trace element depth profiling and secondary ion microscopy. CAMECA IMS 1280 -LARGE RADIUS MAGNETIC SECTOR SIMS FOR GEOLOGY
 LA-ICP-MS Мас-спектрометр Система лазерної абляції
LA-ICP-MS Мас-спектрометр Система лазерної абляції
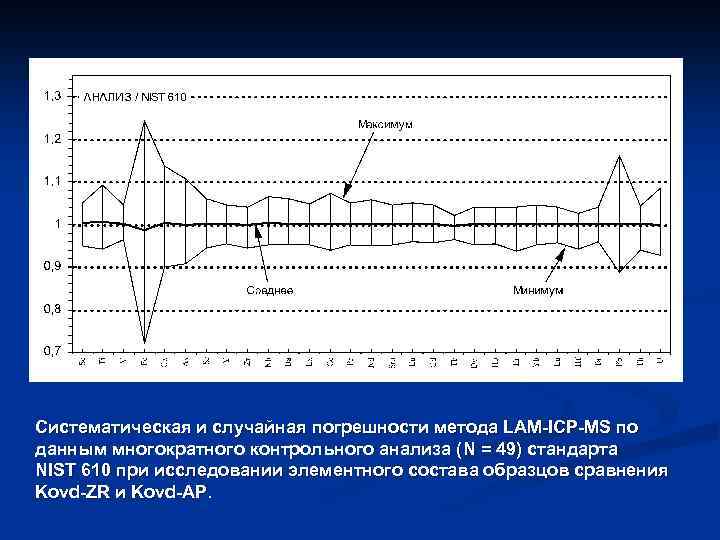 Систематическая и случайная погрешности метода LAM-ICP-MS по данным многократного контрольного анализа (N = 49) стандарта NIST 610 при исследовании элементного состава образцов сравнения Kovd-ZR и Kovd-AP.
Систематическая и случайная погрешности метода LAM-ICP-MS по данным многократного контрольного анализа (N = 49) стандарта NIST 610 при исследовании элементного состава образцов сравнения Kovd-ZR и Kovd-AP.
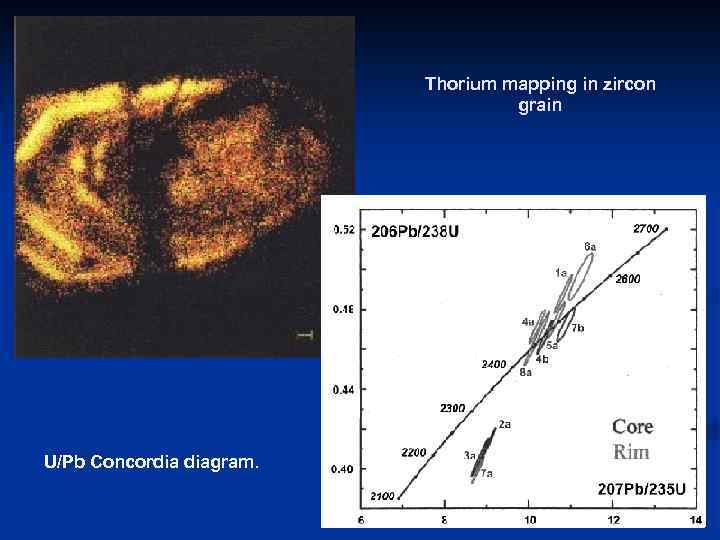 Thorium mapping in zircon grain U/Pb Concordia diagram.
Thorium mapping in zircon grain U/Pb Concordia diagram.

 ОСНОВИ ІЗОТОПНОЇ ГЕОХІМІЇ С. Є. Шнюков Лекція 3 Нукліди: Механізми радіоактивного розпаду та його головний закон
ОСНОВИ ІЗОТОПНОЇ ГЕОХІМІЇ С. Є. Шнюков Лекція 3 Нукліди: Механізми радіоактивного розпаду та його головний закон
 Ядра нестабільних атомів здатні самостійно розпадатися. Цей процес, як відомо, супроводжується радіоактивністю, яка відкрита А. Беккерелем у 1896 р. , досліджувалась П. та М. Кюри, Е. Резерфордом та ін. вченими. Ці та подальші дослідження (Е. Фермі, Паулі, Н. Бор, П. Дірак …) дозволили встановити, що: • результатом розпаду є перетворення нестабільних (материнських, радіоактивних) атомів в атоми інших (дочірних, радіогенних) хімічних елементів з зміною N та Z; • дочірні атоми можуть теж бути нестабільними та, після розпаду, утворювати нові дочірні ізотопи до тих пір, поки в якості продукту розпаду не утвориться стабільний нуклід; • цей процес супроводжується α, β та γ-випромінюванням. Відомо декілька типів розпаду радіоактивних нуклідів. Але, як випливає з розгляду провідних для ізотопної геохїмії радіоактивних та радіогенних нуклідів, найбільше значення для нашого курсу мають: (1) альфа (α)―розпад (2) бета (β-, β+)―розпад (3) захоплення електрону
Ядра нестабільних атомів здатні самостійно розпадатися. Цей процес, як відомо, супроводжується радіоактивністю, яка відкрита А. Беккерелем у 1896 р. , досліджувалась П. та М. Кюри, Е. Резерфордом та ін. вченими. Ці та подальші дослідження (Е. Фермі, Паулі, Н. Бор, П. Дірак …) дозволили встановити, що: • результатом розпаду є перетворення нестабільних (материнських, радіоактивних) атомів в атоми інших (дочірних, радіогенних) хімічних елементів з зміною N та Z; • дочірні атоми можуть теж бути нестабільними та, після розпаду, утворювати нові дочірні ізотопи до тих пір, поки в якості продукту розпаду не утвориться стабільний нуклід; • цей процес супроводжується α, β та γ-випромінюванням. Відомо декілька типів розпаду радіоактивних нуклідів. Але, як випливає з розгляду провідних для ізотопної геохїмії радіоактивних та радіогенних нуклідів, найбільше значення для нашого курсу мають: (1) альфа (α)―розпад (2) бета (β-, β+)―розпад (3) захоплення електрону
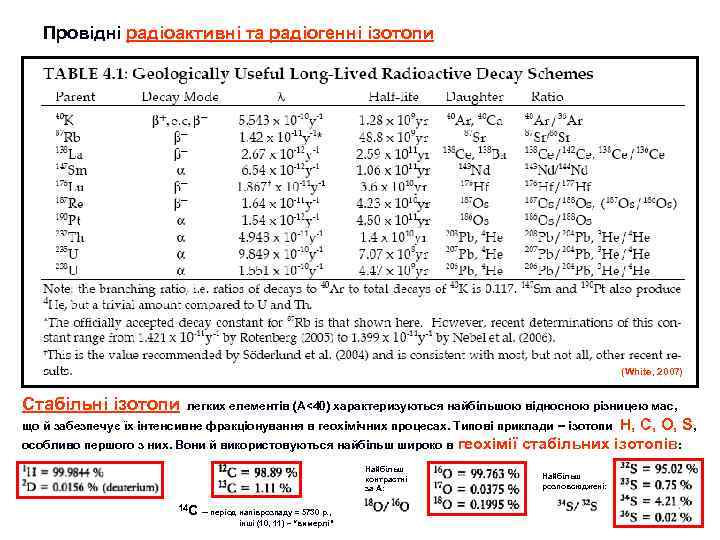 Провідні радіоактивні та радіогенні ізотопи (White, 2007) Стабільні ізотопи легких елементів (A<40) характеризуються найбільшою відносною різницею мас, що й забезпечує їх інтенсивне фракціонування в геохімічних процесах. Типові приклади − ізотопи H, C, O, S, особливо першого з них. Вони й використовуються найбільш широко в геохімії стабільних ізотопів: Найбільш контрастні за А: 14 C – період напіврозпаду = 5730 р. , інші (10, 11) – “вимерлі” Найбільш розповсюджені:
Провідні радіоактивні та радіогенні ізотопи (White, 2007) Стабільні ізотопи легких елементів (A<40) характеризуються найбільшою відносною різницею мас, що й забезпечує їх інтенсивне фракціонування в геохімічних процесах. Типові приклади − ізотопи H, C, O, S, особливо першого з них. Вони й використовуються найбільш широко в геохімії стабільних ізотопів: Найбільш контрастні за А: 14 C – період напіврозпаду = 5730 р. , інші (10, 11) – “вимерлі” Найбільш розповсюджені:
 Бета-розпад (β-)–частка — електрон, який генерується ядром в результаті його розпаду Е. Фермі (1934): нейтрон = протон + електрон + нейтрино Ізобари!
Бета-розпад (β-)–частка — електрон, який генерується ядром в результаті його розпаду Е. Фермі (1934): нейтрон = протон + електрон + нейтрино Ізобари!
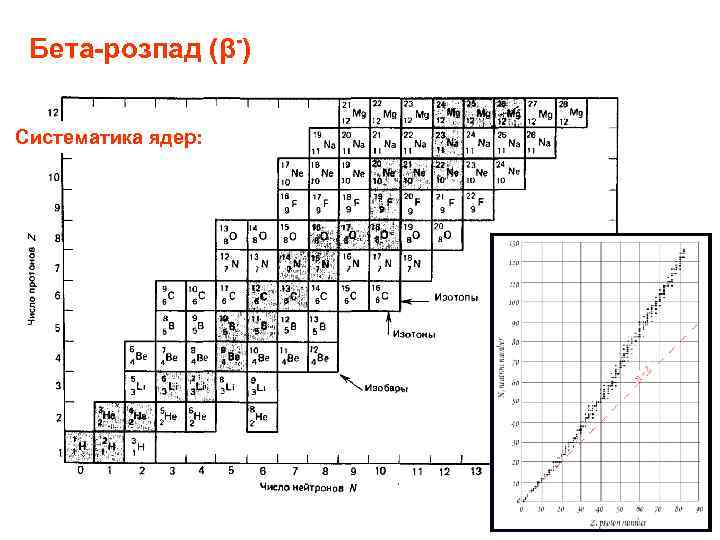 Бета-розпад (β-) Систематика ядер:
Бета-розпад (β-) Систематика ядер:
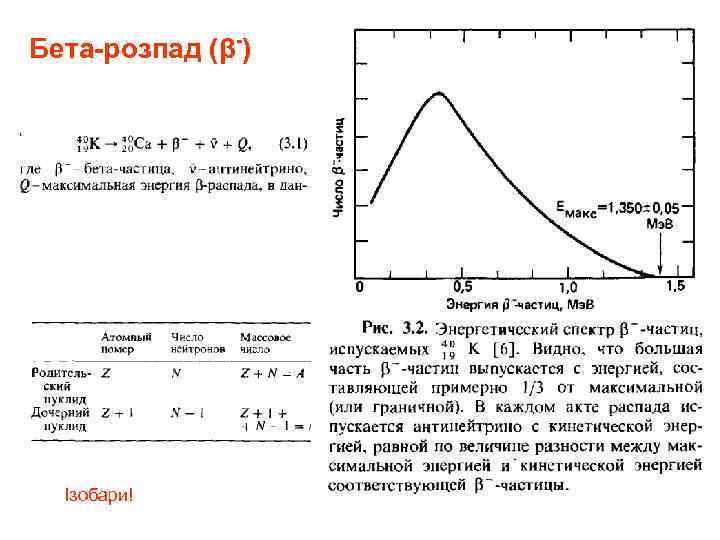 Бета-розпад (β-) Ізобари!
Бета-розпад (β-) Ізобари!
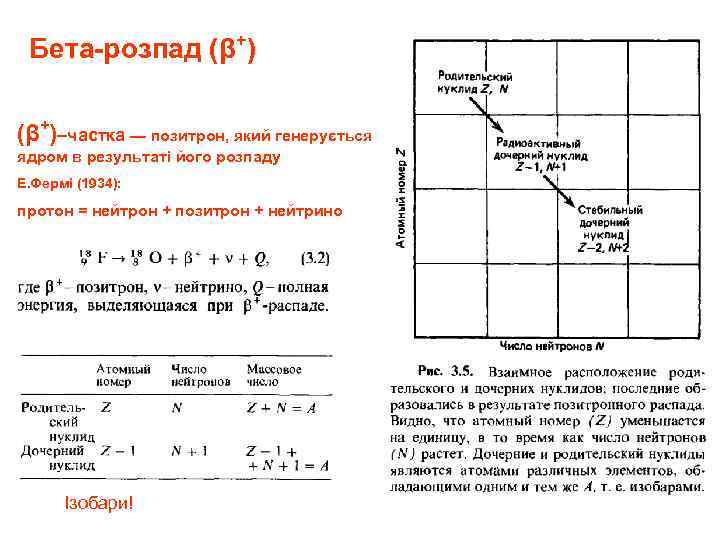 Бета-розпад (β+)–частка — позитрон, який генерується ядром в результаті його розпаду Е. Фермі (1934): протон = нейтрон + позитрон + нейтрино Ізобари!
Бета-розпад (β+)–частка — позитрон, який генерується ядром в результаті його розпаду Е. Фермі (1934): протон = нейтрон + позитрон + нейтрино Ізобари!
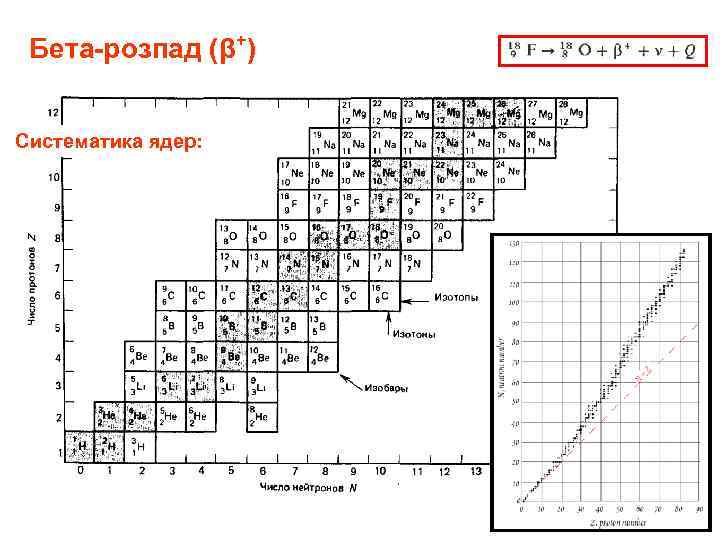 Бета-розпад (β+) Систематика ядер:
Бета-розпад (β+) Систематика ядер:
 Захоплення електрону ( «электронный захват» ) Схема перетворення: протон + електрон = нейтрон + нейтрино Аналогічно випадку позитронного розпаду: Ізобари!
Захоплення електрону ( «электронный захват» ) Схема перетворення: протон + електрон = нейтрон + нейтрино Аналогічно випадку позитронного розпаду: Ізобари!
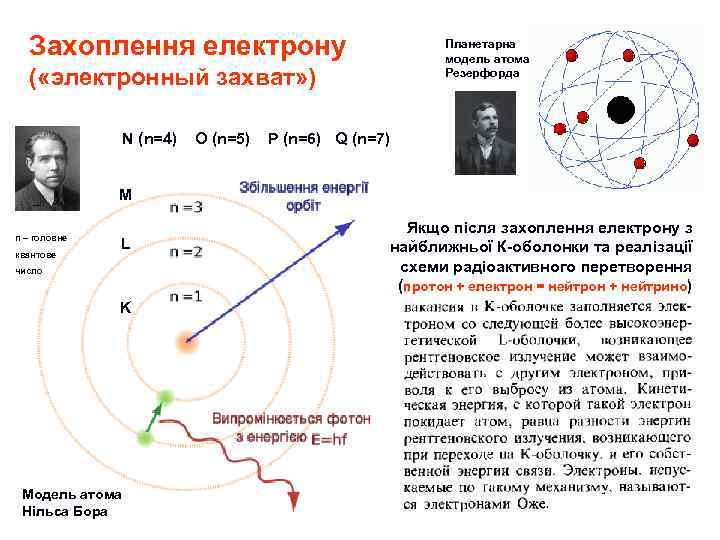 Захоплення електрону Планетарна модель атома Резерфорда ( «электронный захват» ) N (n=4) O (n=5) P (n=6) Q (n=7) M n – головне квантове L число K Модель атома Нільса Бора Якщо після захоплення електрону з найближньої К-оболонки та реалізації схеми радіоактивного перетворення (протон + електрон = нейтрон + нейтрино)
Захоплення електрону Планетарна модель атома Резерфорда ( «электронный захват» ) N (n=4) O (n=5) P (n=6) Q (n=7) M n – головне квантове L число K Модель атома Нільса Бора Якщо після захоплення електрону з найближньої К-оболонки та реалізації схеми радіоактивного перетворення (протон + електрон = нейтрон + нейтрино)
 Атом: електронні конфігурації Пригадайте! Кожна орбіталь може містити до двох електронів, що характеризуються трьома квантовими числами: основним (n = 1, 2…), орбітальним (l =0, 1, 2 … n-1), магнітним (m = 0, +1, +2 … +l ). Кожен електрон на орбіталі має унікальне значення четвертого квантового числа: спіну (ms = +1/2) Орбіталі визначаються специфічним розподілом ймовірності знаходження електрону. «Границею» орбіталі вважається відстань, на якій імовірність того що електрон може перебувати поза нею є меншою 90 %. Кожна орбиталь не може містити більше ніж 2 електрони з однаковим набіром трьох квантових чисел. Їх спіни повинні бути протилежними (принцип Паулі) Для позначення електронної конфігурації хімічного елементу використовують назви орбіталей: s, p, d, f, g (n = 1, 2…) Атоми можуть віддавати та приєднувати електрони, стаючи позитивно або негативно зарядженими іонами. Лише електрони зовнішньої оболонки можуть брати участь в утворенні міжатомних зв'язків. Хімічні властивості елемента визначаються тим, з якою легкістю ядро може віддавати або здобувати електрони. Це залежить як від числа електронів так і від ступеня заповненості зовнішньої оболонки.
Атом: електронні конфігурації Пригадайте! Кожна орбіталь може містити до двох електронів, що характеризуються трьома квантовими числами: основним (n = 1, 2…), орбітальним (l =0, 1, 2 … n-1), магнітним (m = 0, +1, +2 … +l ). Кожен електрон на орбіталі має унікальне значення четвертого квантового числа: спіну (ms = +1/2) Орбіталі визначаються специфічним розподілом ймовірності знаходження електрону. «Границею» орбіталі вважається відстань, на якій імовірність того що електрон може перебувати поза нею є меншою 90 %. Кожна орбиталь не може містити більше ніж 2 електрони з однаковим набіром трьох квантових чисел. Їх спіни повинні бути протилежними (принцип Паулі) Для позначення електронної конфігурації хімічного елементу використовують назви орбіталей: s, p, d, f, g (n = 1, 2…) Атоми можуть віддавати та приєднувати електрони, стаючи позитивно або негативно зарядженими іонами. Лише електрони зовнішньої оболонки можуть брати участь в утворенні міжатомних зв'язків. Хімічні властивості елемента визначаються тим, з якою легкістю ядро може віддавати або здобувати електрони. Це залежить як від числа електронів так і від ступеня заповненості зовнішньої оболонки.
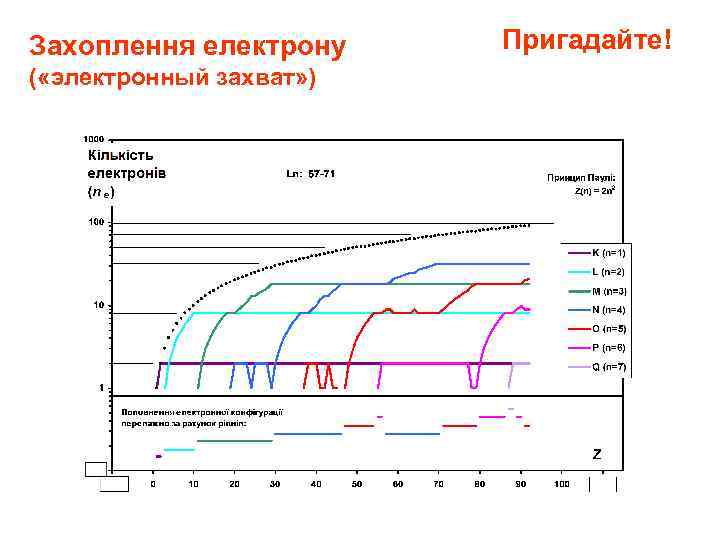 Захоплення електрону ( «электронный захват» ) Пригадайте!
Захоплення електрону ( «электронный захват» ) Пригадайте!
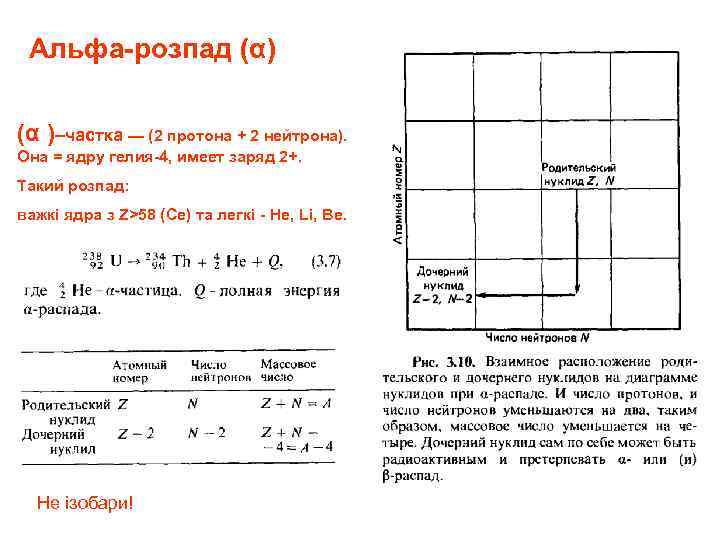 Альфа-розпад (α) (α )–частка — (2 протона + 2 нейтрона). Она = ядру гелия-4, имеет заряд 2+. Такий розпад: важкі ядра з Z>58 (Ce) та легкі - He, Li, Be. Не ізобари!
Альфа-розпад (α) (α )–частка — (2 протона + 2 нейтрона). Она = ядру гелия-4, имеет заряд 2+. Такий розпад: важкі ядра з Z>58 (Ce) та легкі - He, Li, Be. Не ізобари!
 Головний закон радіоактивного розпаду Майже відразу за відкриттям радіоактивності А. Беккерелем у 1896 р. , але вже на початку 20 -го століття Е. Резерфорд та Ф. Содді встановили, що: • результатом розпаду є перетворення нестабільних (материнських, радіоактивних) атомів в атоми інших (дочірних, радіогенних) хімічних елементів, причому за рахунок кожного материнського нукліду утворюється один дочірній атом. • швидкість процесу самостійного розпаду ядер нестабільних атомів пропорційна числу атомів материнського нукліда (N), яке має місце на даний момент часу, Тобто: − d. N/dt ~ N , де d. N/dt – швидкість зміни числа атомів материнського нукліда, а t – час (знак мінус означає, що швидкість процесу з часом зменьшується). Якщо ввести коефіцієнт пропорційності (ламбда)(– “стала розпаду”, то це співвідношення перетвориться на рівняння головного закону радіоактивного розпаду, яке описує розпад будь-якого нестабільного материнського нукліда: − d. N/dt = N або N = N 0 e - t , де N 0 – кількість атомів материнського нукліда при t = 0, а e – основа натурального логарифма (е = 2, 718. . . ).
Головний закон радіоактивного розпаду Майже відразу за відкриттям радіоактивності А. Беккерелем у 1896 р. , але вже на початку 20 -го століття Е. Резерфорд та Ф. Содді встановили, що: • результатом розпаду є перетворення нестабільних (материнських, радіоактивних) атомів в атоми інших (дочірних, радіогенних) хімічних елементів, причому за рахунок кожного материнського нукліду утворюється один дочірній атом. • швидкість процесу самостійного розпаду ядер нестабільних атомів пропорційна числу атомів материнського нукліда (N), яке має місце на даний момент часу, Тобто: − d. N/dt ~ N , де d. N/dt – швидкість зміни числа атомів материнського нукліда, а t – час (знак мінус означає, що швидкість процесу з часом зменьшується). Якщо ввести коефіцієнт пропорційності (ламбда)(– “стала розпаду”, то це співвідношення перетвориться на рівняння головного закону радіоактивного розпаду, яке описує розпад будь-якого нестабільного материнського нукліда: − d. N/dt = N або N = N 0 e - t , де N 0 – кількість атомів материнського нукліда при t = 0, а e – основа натурального логарифма (е = 2, 718. . . ).
 Цей закон, враховуючи, що за рахунок кожного материнського нукліду утворюється один дочірний атом, водночас дозволяє кількісно охарактеризувати накопичення продуктів розпаду для будь-якого часу t. Так, якщо розпад материнського нукліда призводить до формування стабільного радіогенного продукта та число його атомів (D*) дорівнює нулю при t = 0, то для закритої системи та часу t : - t D* = N 0 – N або D* = N 0(1 – e ) Період напіврозпаду Т ½ − час, за який первинна кількість материнських атомів зменьшиться в два рази (тобто, якщо t = T 1/2 , то N = 0, 5 N 0): Т 1/2 = 0, 693/ . Звичайно, що розмірність - од. часу-1, а Т ½ - од. часу. Але в більшості випадків (наприклад в геохронології) актуальним є співвідносити число радіогенних (дочірних) атомів (D*) на час t не з первинним числом материнських (радіоактивних) атомів (N 0), а з їх числом на той же час t (N): t D* = N(e – 1) Необхідно також враховувати можливість присутності в системі деякої кількості первинних дочірних атомів (D 0 ) при t = 0 та оперувати загальним їх числом (D = D 0 + D*): t D = D 0 + N(e – 1) Це рівняння є головним для використання в ізотопній геохронології для методів, які базуються на перетворенні: материнський – дочірній стабільний нуклід.
Цей закон, враховуючи, що за рахунок кожного материнського нукліду утворюється один дочірний атом, водночас дозволяє кількісно охарактеризувати накопичення продуктів розпаду для будь-якого часу t. Так, якщо розпад материнського нукліда призводить до формування стабільного радіогенного продукта та число його атомів (D*) дорівнює нулю при t = 0, то для закритої системи та часу t : - t D* = N 0 – N або D* = N 0(1 – e ) Період напіврозпаду Т ½ − час, за який первинна кількість материнських атомів зменьшиться в два рази (тобто, якщо t = T 1/2 , то N = 0, 5 N 0): Т 1/2 = 0, 693/ . Звичайно, що розмірність - од. часу-1, а Т ½ - од. часу. Але в більшості випадків (наприклад в геохронології) актуальним є співвідносити число радіогенних (дочірних) атомів (D*) на час t не з первинним числом материнських (радіоактивних) атомів (N 0), а з їх числом на той же час t (N): t D* = N(e – 1) Необхідно також враховувати можливість присутності в системі деякої кількості первинних дочірних атомів (D 0 ) при t = 0 та оперувати загальним їх числом (D = D 0 + D*): t D = D 0 + N(e – 1) Це рівняння є головним для використання в ізотопній геохронології для методів, які базуються на перетворенні: материнський – дочірній стабільний нуклід.
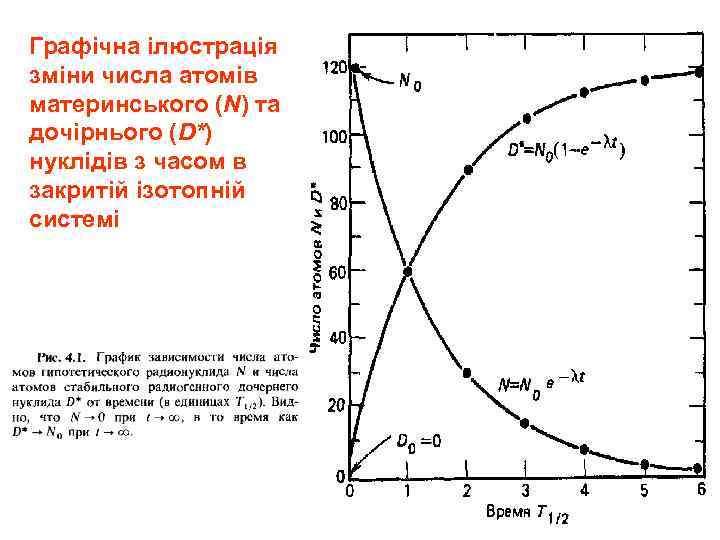 Графічна ілюстрація зміни числа атомів материнського (N) та дочірнього (D*) нуклідів з часом в закритій ізотопній системі
Графічна ілюстрація зміни числа атомів материнського (N) та дочірнього (D*) нуклідів з часом в закритій ізотопній системі
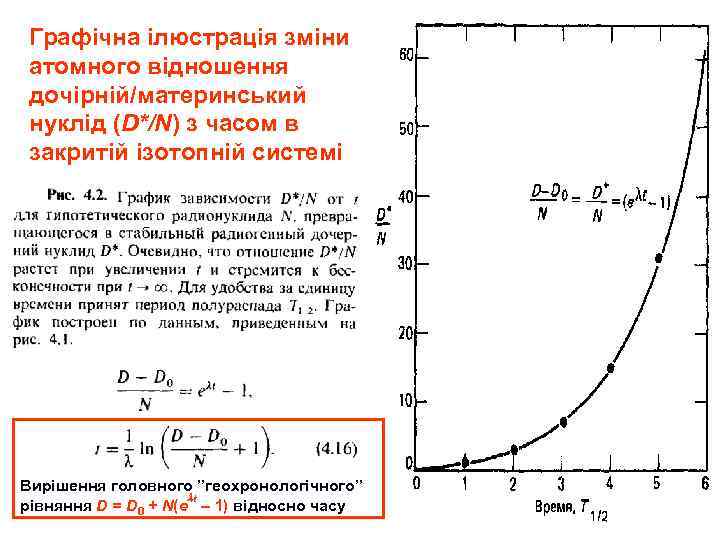 Графічна ілюстрація зміни атомного відношення дочірній/материнський нуклід (D*/N) з часом в закритій ізотопній системі Вирішення головного ”геохронологічного” t рівняння D = D 0 + N(e – 1) відносно часу
Графічна ілюстрація зміни атомного відношення дочірній/материнський нуклід (D*/N) з часом в закритій ізотопній системі Вирішення головного ”геохронологічного” t рівняння D = D 0 + N(e – 1) відносно часу
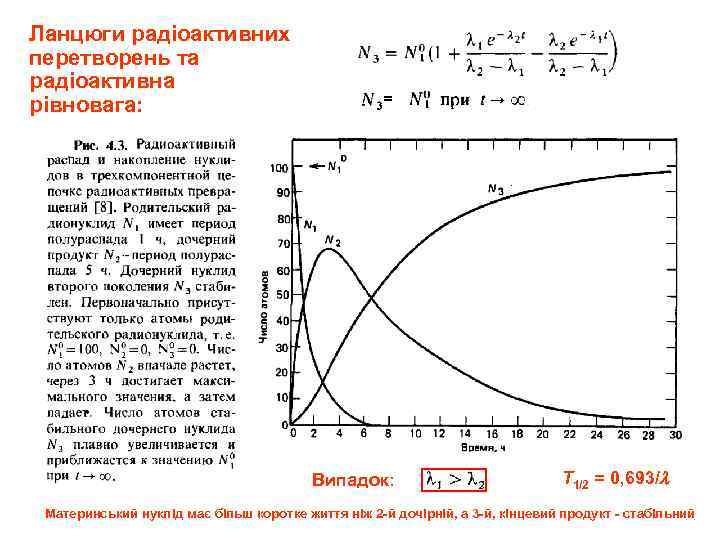 Ланцюги радіоактивних перетворень та радіоактивна рівновага: = Випадок: Т 1/2 = 0, 693/ Материнський нуклід має більш коротке життя ніж 2 -й дочірній, а 3 -й, кінцевий продукт - стабільний
Ланцюги радіоактивних перетворень та радіоактивна рівновага: = Випадок: Т 1/2 = 0, 693/ Материнський нуклід має більш коротке життя ніж 2 -й дочірній, а 3 -й, кінцевий продукт - стабільний
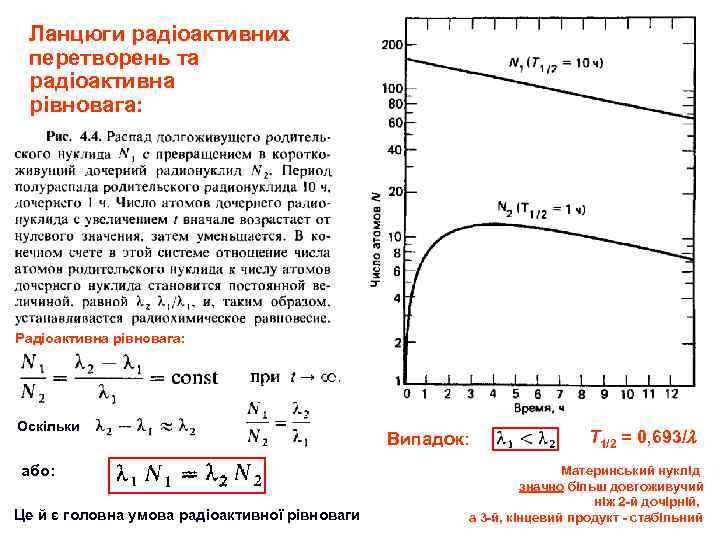 Ланцюги радіоактивних перетворень та радіоактивна рівновага: Радіоактивна рівновага: Оскільки або: Це й є головна умова радіоактивної рівноваги Випадок: Т 1/2 = 0, 693/ Материнський нуклід значно більш довгоживучий ніж 2 -й дочірній, а 3 -й, кінцевий продукт - стабільний
Ланцюги радіоактивних перетворень та радіоактивна рівновага: Радіоактивна рівновага: Оскільки або: Це й є головна умова радіоактивної рівноваги Випадок: Т 1/2 = 0, 693/ Материнський нуклід значно більш довгоживучий ніж 2 -й дочірній, а 3 -й, кінцевий продукт - стабільний
 Ланцюги радіоактивних перетворень та радіоактивна (секулярна, радіохімічна) рівновага: Оскільки − d. N/dt = N це швидкість розпаду, вираз як головна умова радіоактивної рівноваги означає, що після її досягнення швидкість розпаду дочірнього продукту буде дорівнювати швидкості розпаду материнського. Для складних ланцюгів радіоактивних перетворень, які складаються з довгоживучого материнського радіонукліда та багатьох короткоживучих проміжних дочірних радіонуклідів, ця умова є справедливою для всіх членів ланцюга: Важливий наслідок: за умови радіоактивної рівноваги швидкість накопичення кінцевого для всього ланцюга стабільного нукліду дорівнює швидкості розпаду первинного материнського: Тобто: кількість атомів кінцевого для ланцюга стабільного нукліду можно розраховувати у такий же спосіб, як у випадку безпосереднього (одноактного!) перетворення материнського радіонукліду в стабільний кінцевий продукт: Проміжні короткоживучі члени ланцюга просто вилучаються з розгляду!
Ланцюги радіоактивних перетворень та радіоактивна (секулярна, радіохімічна) рівновага: Оскільки − d. N/dt = N це швидкість розпаду, вираз як головна умова радіоактивної рівноваги означає, що після її досягнення швидкість розпаду дочірнього продукту буде дорівнювати швидкості розпаду материнського. Для складних ланцюгів радіоактивних перетворень, які складаються з довгоживучого материнського радіонукліда та багатьох короткоживучих проміжних дочірних радіонуклідів, ця умова є справедливою для всіх членів ланцюга: Важливий наслідок: за умови радіоактивної рівноваги швидкість накопичення кінцевого для всього ланцюга стабільного нукліду дорівнює швидкості розпаду первинного материнського: Тобто: кількість атомів кінцевого для ланцюга стабільного нукліду можно розраховувати у такий же спосіб, як у випадку безпосереднього (одноактного!) перетворення материнського радіонукліду в стабільний кінцевий продукт: Проміжні короткоживучі члени ланцюга просто вилучаються з розгляду!
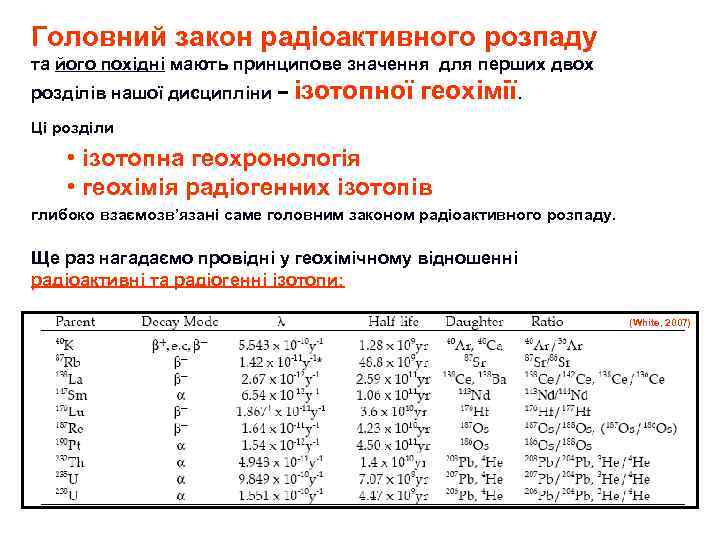 Головний закон радіоактивного розпаду та його похідні мають принципове значення для перших двох розділів нашої дисципліни − ізотопної геохімії. Ці розділи • ізотопна геохронологія • геохімія радіогенних ізотопів глибоко взаємозв’язані саме головним законом радіоактивного розпаду. Ще раз нагадаємо провідні у геохімічному відношенні радіоактивні та радіогенні ізотопи: (White, 2007)
Головний закон радіоактивного розпаду та його похідні мають принципове значення для перших двох розділів нашої дисципліни − ізотопної геохімії. Ці розділи • ізотопна геохронологія • геохімія радіогенних ізотопів глибоко взаємозв’язані саме головним законом радіоактивного розпаду. Ще раз нагадаємо провідні у геохімічному відношенні радіоактивні та радіогенні ізотопи: (White, 2007)
 Третій розділ ізотопної геохімії, а саме • геохімія стабільних ізотопів має зовсім іншу теоретичну основу. Він базується на ефекті інтенсивного природного фракціонування ізотопів “легких” елементів з відносно великою різницею атомних мас внаслідок: • реакцій ізотопного обміну, • дифузії, • процесів плавлення/кристалізації, випарування/конденсації тощо. Ці фактори ізотопного фракціонування ми розглянемо далі на відповідних лекціях. Ще раз нагадаємо провідні у геохімічному відношенні стабільні ізотопи: Стабільні ізотопи легких елементів (A<40) характеризуються найбільшою відносною різницею мас, що й забезпечує їх інтенсивне фракціонування в геохімічних процесах. Типові приклади − ізотопи H, C, O, S, особливо першого з них. Вони й використовуються найбільш широко в геохімії стабільних ізотопів: Найбільш контрастні за А: 14 C – період напіврозпаду = 5730 р. , інші (10, 11) – “вимерлі” Найбільш розповсюджені:
Третій розділ ізотопної геохімії, а саме • геохімія стабільних ізотопів має зовсім іншу теоретичну основу. Він базується на ефекті інтенсивного природного фракціонування ізотопів “легких” елементів з відносно великою різницею атомних мас внаслідок: • реакцій ізотопного обміну, • дифузії, • процесів плавлення/кристалізації, випарування/конденсації тощо. Ці фактори ізотопного фракціонування ми розглянемо далі на відповідних лекціях. Ще раз нагадаємо провідні у геохімічному відношенні стабільні ізотопи: Стабільні ізотопи легких елементів (A<40) характеризуються найбільшою відносною різницею мас, що й забезпечує їх інтенсивне фракціонування в геохімічних процесах. Типові приклади − ізотопи H, C, O, S, особливо першого з них. Вони й використовуються найбільш широко в геохімії стабільних ізотопів: Найбільш контрастні за А: 14 C – період напіврозпаду = 5730 р. , інші (10, 11) – “вимерлі” Найбільш розповсюджені:
 Ще раз: Головні завдання та розділи ізотопної геохімії: n Визначення віку мінералів та гірських порід, датування процесів їх утворення. Відповідний розділ має назву “Ізотопна геохронологія”. n Дослідження геологічних процесів за допомогою використання ізотопів в якості природних “мічених атомів”. Основою цього підходу є контрасна геохімічна поведінка радіоактивних ізотопів (курс “Основи геохімії”!!!) – одних породах вони концентруються, а з інших виносяться (U, Th, Rb – несумісні елементи!!!). Наприклад, корові породи збагачені Rb, та, як наслідок, вміщують значно більше радіогенного 87 Sr (85 Rb – стабільний, 72%, а 87 Rb – радіоактивний, 28% дає 87 Sr) ніж мантійні деплетовані породи. Тому співвідношення 87 Sr/ 86 Sr (86 Sr – стабільний та нерадіогенний, один з 4 – 88 найбільш поширений , 87, 86, 84 ) – індикатор рівня мобілізації речовини. Відповідний розділ має назву “Геохімія радіогенних ізотопів”. n Дослідження поведінки ізотопів легких елементів (кисень, вуглець, сірка. . . ) в залежності від PTX-умов геохімічних процесів, та вирішення зворотної задачі – реставрування цих умов за спостереженими ізотопно-геохімічними даними. Відповідний розділ має назву “Геохімія стабільних ізотопів” n Ще раз: ізотопна геохімія – частина геохімії, яка оперує концентраціями ізотопів. Значення цих концентрацій – досить низьке. Тому ізотопна геохімія – найбільш прецизійна, кількісна та “фізична” частина геохімії.
Ще раз: Головні завдання та розділи ізотопної геохімії: n Визначення віку мінералів та гірських порід, датування процесів їх утворення. Відповідний розділ має назву “Ізотопна геохронологія”. n Дослідження геологічних процесів за допомогою використання ізотопів в якості природних “мічених атомів”. Основою цього підходу є контрасна геохімічна поведінка радіоактивних ізотопів (курс “Основи геохімії”!!!) – одних породах вони концентруються, а з інших виносяться (U, Th, Rb – несумісні елементи!!!). Наприклад, корові породи збагачені Rb, та, як наслідок, вміщують значно більше радіогенного 87 Sr (85 Rb – стабільний, 72%, а 87 Rb – радіоактивний, 28% дає 87 Sr) ніж мантійні деплетовані породи. Тому співвідношення 87 Sr/ 86 Sr (86 Sr – стабільний та нерадіогенний, один з 4 – 88 найбільш поширений , 87, 86, 84 ) – індикатор рівня мобілізації речовини. Відповідний розділ має назву “Геохімія радіогенних ізотопів”. n Дослідження поведінки ізотопів легких елементів (кисень, вуглець, сірка. . . ) в залежності від PTX-умов геохімічних процесів, та вирішення зворотної задачі – реставрування цих умов за спостереженими ізотопно-геохімічними даними. Відповідний розділ має назву “Геохімія стабільних ізотопів” n Ще раз: ізотопна геохімія – частина геохімії, яка оперує концентраціями ізотопів. Значення цих концентрацій – досить низьке. Тому ізотопна геохімія – найбільш прецизійна, кількісна та “фізична” частина геохімії.
 Тому для всіх трьох розділів ізотопної геохімії величезне значення мають методи визначення ізотопного складу природних об’єктів
Тому для всіх трьох розділів ізотопної геохімії величезне значення мають методи визначення ізотопного складу природних об’єктів
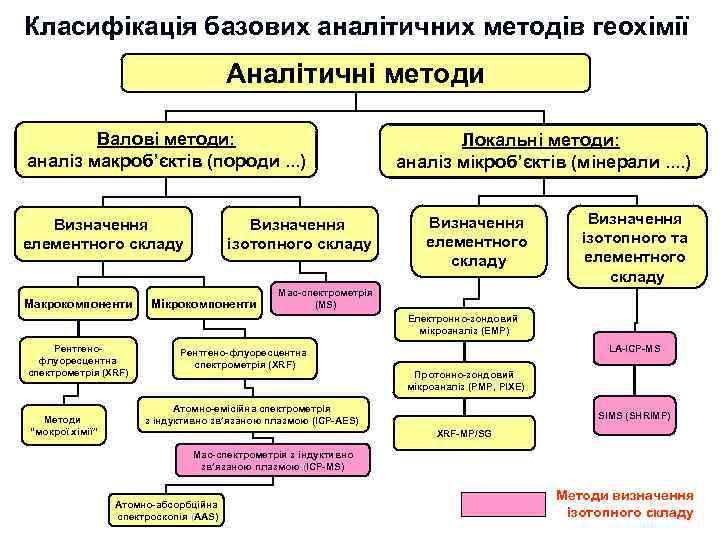 Класифікація базових аналітичних методів геохімії Аналітичні методи Валові методи: аналіз макроб’єктів (породи. . . ) Визначення елементного складу Макрокомпоненти Визначення ізотопного складу Мікрокомпоненти Локальні методи: аналіз мікроб’єктів (мінерали. . ) Визначення елементного складу Визначення ізотопного та елементного складу Мас-спектрометрія (MS) Електронно-зондовий мікроаналіз (EMP) Рентгенофлуоресцентна спектрометрія (XRF) Методи “мокрої хімії” Рентгено-флуоресцентна спектрометрія (XRF) LA-ICP-MS Протонно-зондовий мікроаналіз (PMP, PIXE) Атомно-емісійна спектрометрія з індуктивно зв’язаною плазмою (ICP-AES) SIMS (SHRIMP) XRF-MP/SG Мас-спектрометрія з індуктивно зв’язаною плазмою (ICP-MS) ( Атомно-абсорбційна спектроскопія (AAS) ( Методи визначення ізотопного складу
Класифікація базових аналітичних методів геохімії Аналітичні методи Валові методи: аналіз макроб’єктів (породи. . . ) Визначення елементного складу Макрокомпоненти Визначення ізотопного складу Мікрокомпоненти Локальні методи: аналіз мікроб’єктів (мінерали. . ) Визначення елементного складу Визначення ізотопного та елементного складу Мас-спектрометрія (MS) Електронно-зондовий мікроаналіз (EMP) Рентгенофлуоресцентна спектрометрія (XRF) Методи “мокрої хімії” Рентгено-флуоресцентна спектрометрія (XRF) LA-ICP-MS Протонно-зондовий мікроаналіз (PMP, PIXE) Атомно-емісійна спектрометрія з індуктивно зв’язаною плазмою (ICP-AES) SIMS (SHRIMP) XRF-MP/SG Мас-спектрометрія з індуктивно зв’язаною плазмою (ICP-MS) ( Атомно-абсорбційна спектроскопія (AAS) ( Методи визначення ізотопного складу


