Lecture 2 (amino acids).ppt
- Количество слайдов: 35

Основи біохімії. Лекція 2 Біохімія Лектор: доктор фіз. -мат. наук, професор Рожицький Миколайович
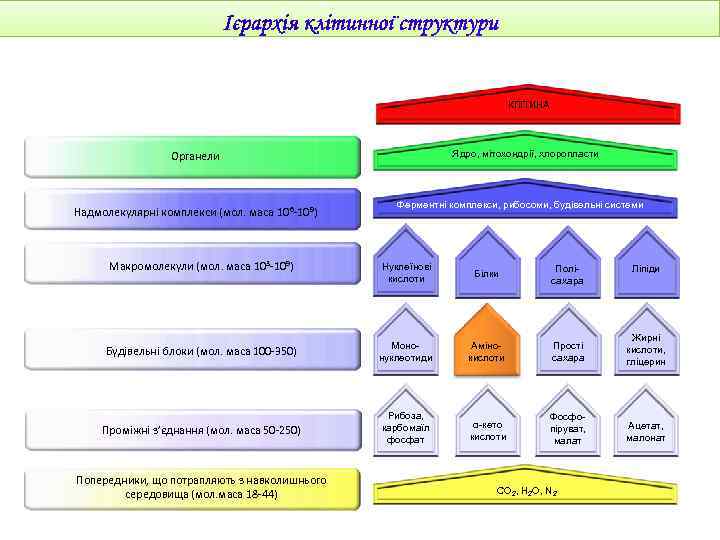
КЛІТИНА Ядро, мітохондрії, хлоропласти Органели Надмолекулярні комплекси (мол. маса 10 6 -109) Ферментні комплекси, рибосоми, будівельні системи Макромолекули (мол. маса 10 3 -109) Нуклеїнові кислоти Білки Полісахара Будівельні блоки (мол. маса 100 -350) Мононуклеотиди Амінокислоти Прості сахара Жирні кислоти, гліцерин Проміжні з’єднання (мол. маса 50 -250) Рибоза, карбомаїл фосфат α-кето кислоти Фосфопіруват, малат Ацетат, малонат Попередники, що потрапляють з навколишнього середовища (мол. маса 18 -44) CO 2, H 2 O, N 2 Ліпіди
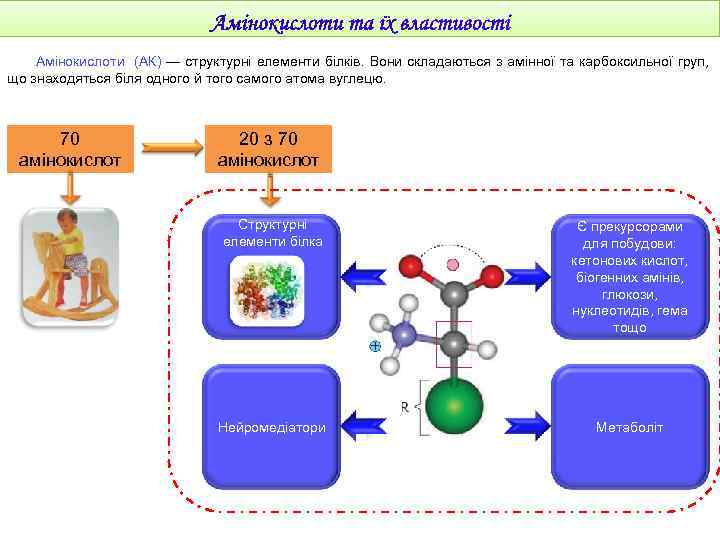
Амінокислоти (АК) — структурні елементи білків. Вони складаються з амінної та карбоксильної груп, що знаходяться біля одного й того самого атома вуглецю. 70 амінокислот 20 з 70 амінокислот Структурні елементи білка Є прекурсорами для побудови: кетонових кислот, біогенних амінів, глюкози, нуклеотидів, гема тощо Нейромедіатори Метаболіт
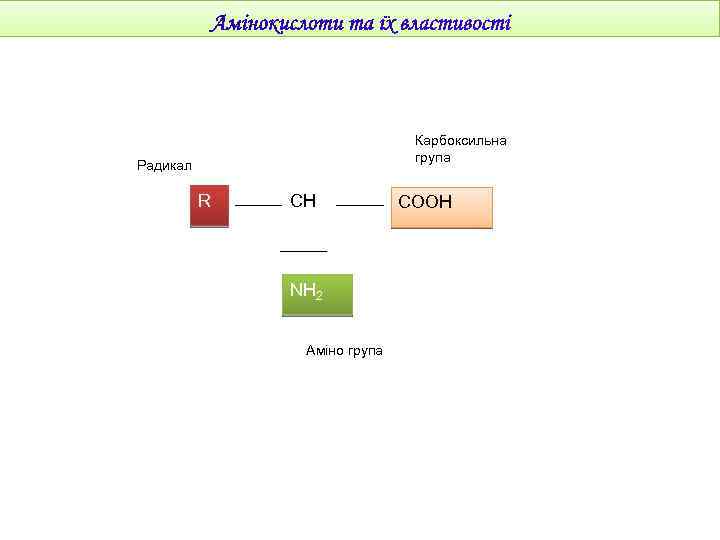
Карбоксильна група Радикал R CH NH 2 Аміно група COOH

В 1811 році французький фізик Франсуа Домінік Араго при досліджені кристалів кварцу з'ясував, що при проходженні поляризованого світла через деякі речовини відбувається цікаве явище: площина, в якій розміщенні «стрілки» коливне електричне поле, поступово повертається навколо осі, вздовж якої йде промінь. Природні кристали кварцу мають неправильну, асиметричну будову, причому вони бувають двох типів, які відрізняються за своєю формою, як предмет від свого дзеркального відображення. Ці кристали обертають площину поляризації світла в протилежних напрямках; їх назвали право- та лівообертальними. В 1815 інший французький фізик Жан Батіст Біо та німецький фізик Томас Зеєбек встановили, що деякі органічні речовини (наприклад, цукор або скипидар) теж володіють цією властивістю, причому не лише в кристалічному, але й в рідкому, розчиненому та навіть газоподібному стані. Так було доведено, що оптична активність може бути пов'язана не лише з асиметрією кристалів, але й з невідомими властивостями самих молекул. З'ясувалося, що як і у випадку кристалів, деякі хімічні з'єднання можуть існувати у вигляді як право-, так і лівообертових різновидів, причому самий ретельний хімічний аналіз не виявляє між ними ніяких різниць! Фактично це був новий тип ізомерії, яку назвали оптичною ізомерією. Виявилося, що окрім право- та лівообертальних, є й третій тип ізомерів – оптично неактивні. Домінік Франсуа Араго (1786 - 1853) Жан-Батіст Біо (1774 - 1862)
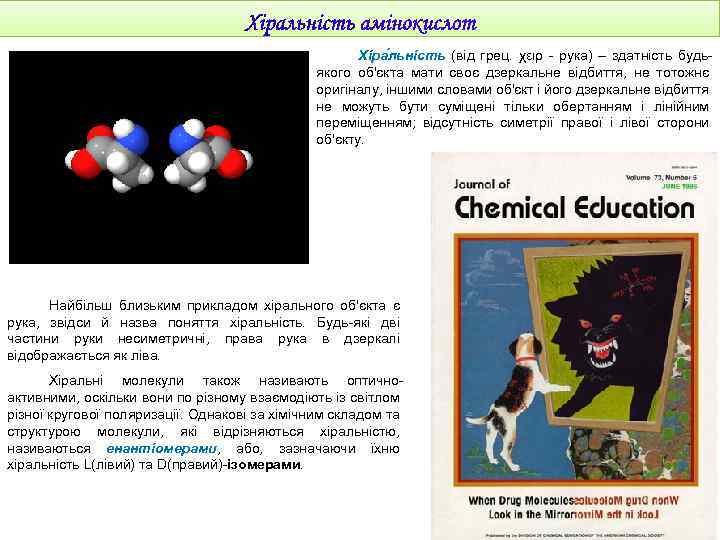
Хіра льність (від грец. χειρ - рука) – здатність будьякого об'єкта мати своє дзеркальне відбиття, не тотожнє оригіналу, іншими словами об'єкт і його дзеркальне відбиття не можуть бути суміщені тільки обертанням і лінійним переміщенням; відсутність симетрії правої і лівої сторони об'єкту. Найбільш близьким прикладом хірального об'єкта є рука, звідси й назва поняття хіральність. Будь-які дві частини руки несиметричні, права рука в дзеркалі відображається як ліва. Хіральні молекули також називають оптичноактивними, оскільки вони по різному взаємодіють із світлом різної кругової поляризації. Однакові за хімічним складом та структурою молекули, які відрізняються хіральністю, називаються енантіомерами, або, зазначаючи їхню енантіомерами хіральність L(лівий) та D(правий)-ізомерами.

Всі амінокислоти проявляють оптичну активність, тобто здатні обертати площину поляризованого променя (виключенням є гліцин). Оптичною активністю володіють усі з'єднання, що здатні існувати в двох формах, що представляють по своїй структурі несумісні дзеркальні відображення одне одного. Цією властивістю володіють з'єднання, в молекулі яких є асиметричний атом вуглецю, тобто вуглецю з чотирма різними замісниками. Е. Фішер запропонував, що якщо аміногрупа знаходиться в зліва, то АК відносяться до Lконфігурації, а якщо аміногрупа знаходиться справа, то АК відноситься до D- конфігурації. Протеїногенні амінокислоти існують лише в L-формі, але в живій природі відмічена наявність Dамінокислот, що знаходяться у вільному стані або в складі коротких пептидів. Живі організми синтезують лише L-форми. У результаті хімічного синтезу утворюється однакова кількість D- та L- енантиомерів, тобто має місце рацемічна суміш, яку складно розділити на окремі форми. Розділені D- та L-ізомери у результаті кип’ятіння або при тривалому зберіганні знову перетворюються в рацемати. L - амінокислота Фішерівські проекції D – амінокислота (дзеркальне відображення)
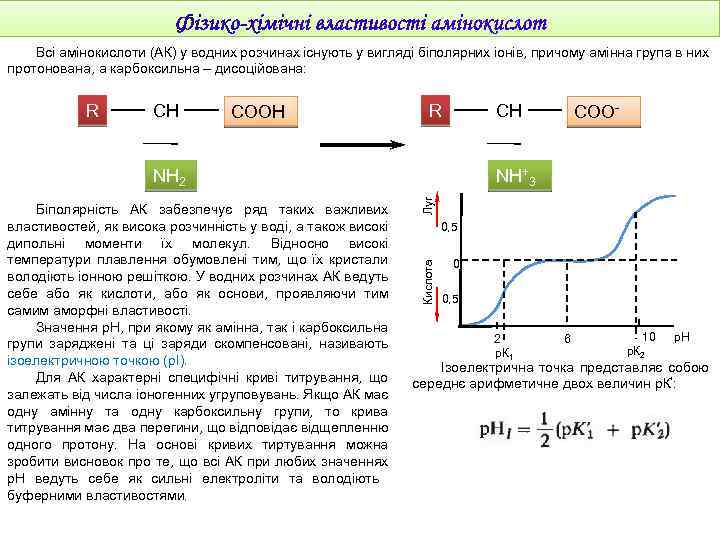
Всі амінокислоти (АК) у водних розчинах існують у вигляді біполярних іонів, причому амінна група в них протонована, а карбоксильна – дисоційована: R CH COOH R CH NH 2 Луг NH+3 0, 5 Кислота Біполярність АК забезпечує ряд таких важливих властивостей, як висока розчинність у воді, а також високі дипольні моменти їх молекул. Відносно високі температури плавлення обумовлені тим, що їх кристали володіють іонною решіткою. У водних розчинах АК ведуть себе або як кислоти, або як основи, проявляючи тим самим аморфні властивості. Значення р. Н, при якому як амінна, так і карбоксильна групи заряджені та ці заряди скомпенсовані, називають ізоелектричною точкою (рІ). Для АК характерні специфічні криві титрування, що залежать від числа іоногенних угруповувань. Якщо АК має одну амінну та одну карбоксильну групи, то крива титрування має два перегини, що відповідає відщепленню одного протону. На основі кривих тиртування можна зробити висновок про те, що всі АК при любих значеннях р. Н ведуть себе як сильні електроліти та володіють буферними властивостями. COO- 0 0, 5 2 р. К 1 6 10 р. К 2 р. Н Ізоелектрична точка представляє собою середнє арифметичне двох величин р. К’:
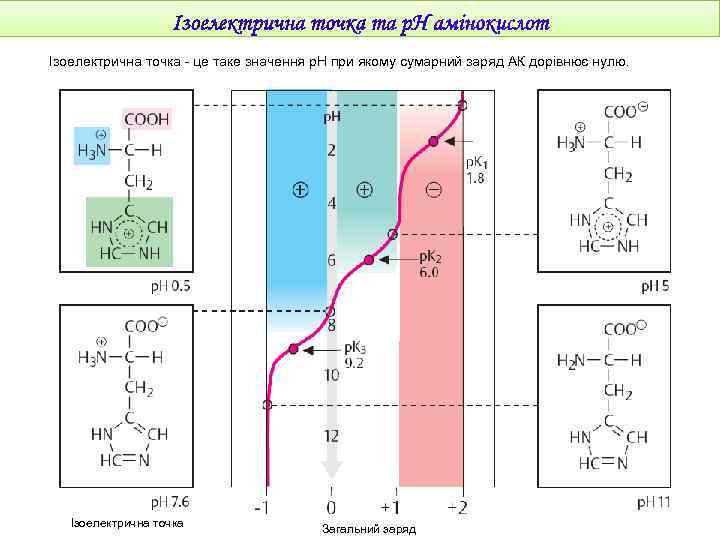
Ізоелектрична точка - це таке значення р. Н при якому сумарний заряд АК дорівнює нулю. Ізоелектрична точка Загальний заряд
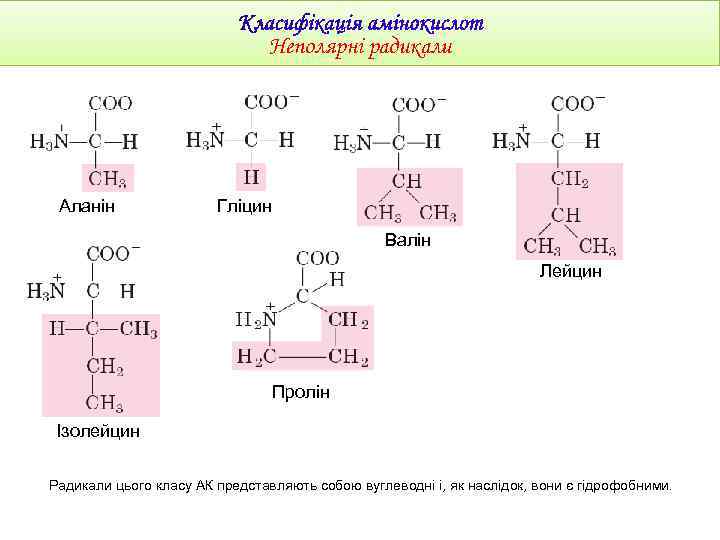
Неполярні радикали Аланін Гліцин Валін Лейцин Пролін Ізолейцин Радикали цього класу АК представляють собою вуглеводні і, як наслідок, вони є гідрофобними.
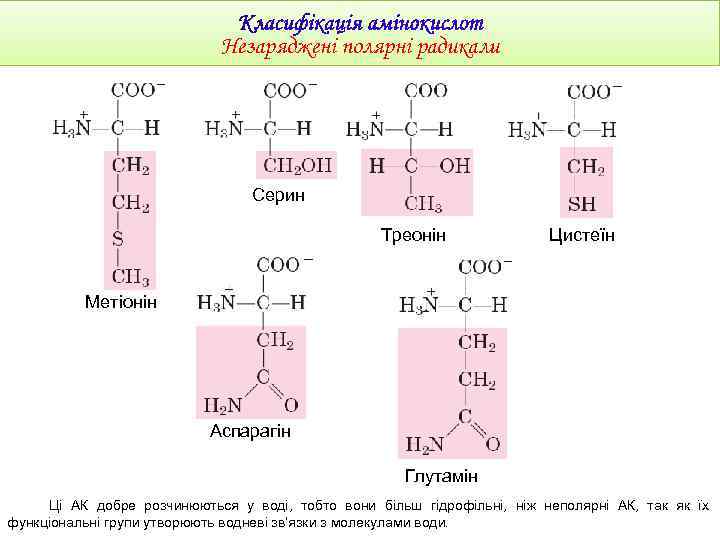
Незаряджені полярні радикали Серин Треонін Цистеїн Метіонін Аспарагін Глутамін Ці АК добре розчинюються у воді, тобто вони більш гідрофільні, ніж неполярні АК, так як їх функціональні групи утворюють водневі зв’язки з молекулами води.

Позитивно заряджені радикали Гістидин Лізин Аргінін Це АК, у яких радикал при р. Н 7, 0 несуть сумарний позитивний заряд.
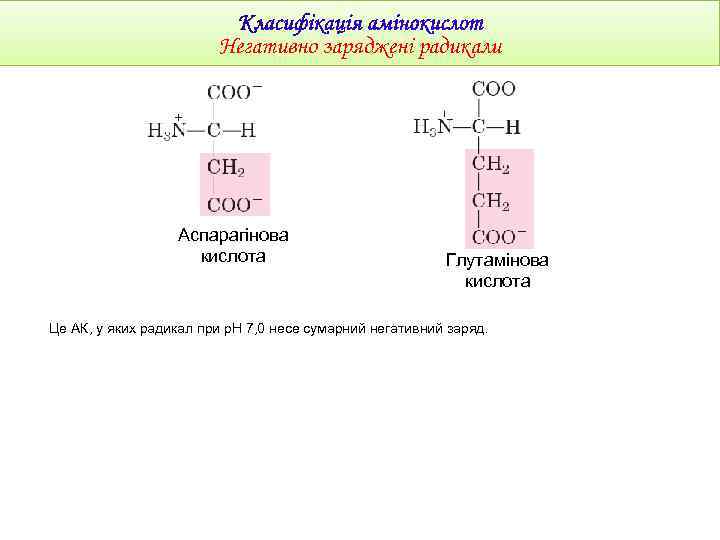
Негативно заряджені радикали Аспарагінова кислота Глутамінова кислота Це АК, у яких радикал при р. Н 7, 0 несе сумарний негативний заряд.
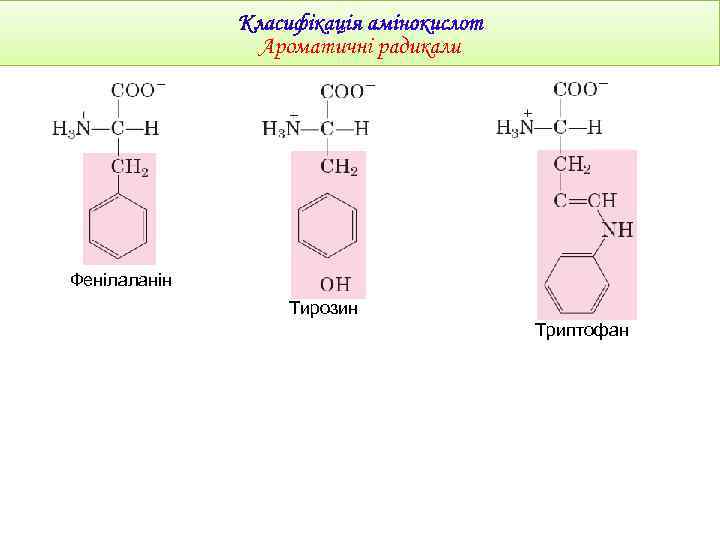
Ароматичні радикали Фенілаланін Тирозин Триптофан

Так як АК містять по декілька заряджених груп, вони легко сольватуються та добре розчинюються в полярних розчинниках (вода, етанол) та не розчиняються в неполярних розчинниках (бензол, гексан, ефір). Температура плавлення АК досить висока – більше 200ºС. Ця властивість обумовлена наявністю в них заряджених груп. Біохемілюмінесценція Звуколюмінесценція Термохемілюмінесценція Сонолюмінесценція Фотолюмінесценція Ліолюмінесценція Радіолюмінесценція Хімілюмінесценція Рентгенолюмінесценція Катодолюмінесценція Триболюмінесценція Електрохемілюмінесценція
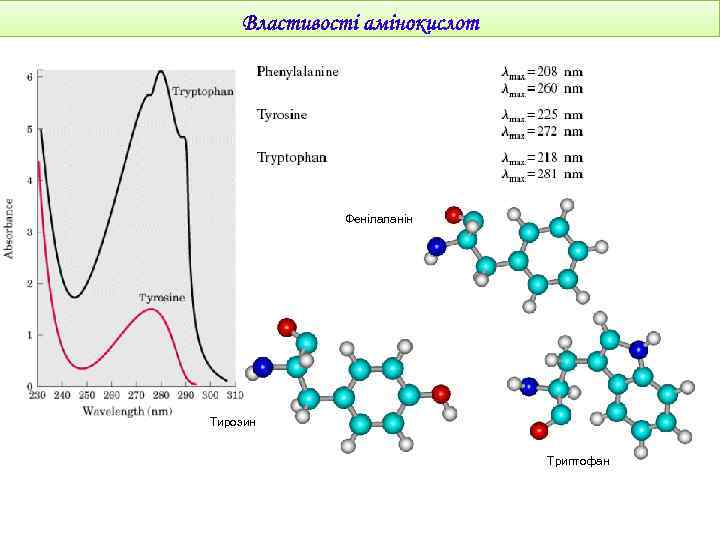
Фенілаланін Тирозин Триптофан

Синтез АК Ферментативний Хімічний У всіх випадках отримується рацемічна суміш, яку необхідно розділяти на оптично активні стереоізомери. Розділення ізомерів здійснюється за Утворюються лише L-ізомери. допомого хроматографії. Що є Однією з суттєвих переваг для промислового виготовлення є те, неефективним та тривалим. що процес відбувається в одну стадію. Мікробіологічний Мікроорганізми синтезують вільні АК, що мають промислове значення. Генна модифікація мікроорганізмів призводить до синтезу ними більше одних АК, ніж інших. Це головний метод отримання промислових АК
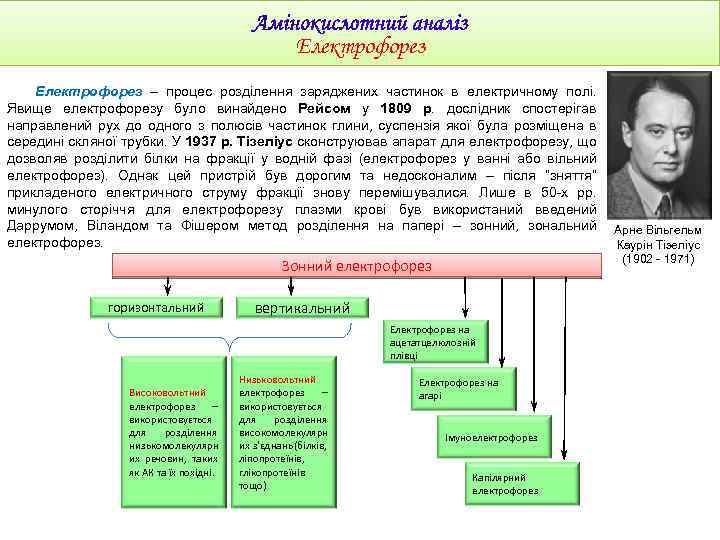
Електрофорез – процес розділення заряджених частинок в електричному полі. Явище електрофорезу було винайдено Рейсом у 1809 р. дослідник спостерігав направлений рух до одного з полюсів частинок глини, суспензія якої була розміщена в середині скляної трубки. У 1937 р. Тізеліус сконструював апарат для електрофорезу, що дозволяв розділити білки на фракції у водній фазі (електрофорез у ванні або вільний електрофорез). Однак цей пристрій був дорогим та недосконалим – після “зняття” прикладеного електричного струму фракції знову перемішувалися. Лише в 50 -х рр. минулого сторіччя для електрофорезу плазми крові був використаний введений Даррумом, Віландом та Фішером метод розділення на папері – зонний, зональний електрофорез. Зонний електрофорез горизонтальний вертикальний Електрофорез на ацетатцелюлозній плівці Високовольтний електрофорез – використовується для розділення низькомолекулярн их речовин, таких як АК та їх похідні. Низьковольтний електрофорез – використовується для розділення високомолекулярн их з'єднань (білків, ліпопротеїнів, глікопротеїнів тощо) Електрофорез на агарі Імуноелектрофорез Капілярний електрофорез Арне Вільгельм Каурін Тізеліус (1902 - 1971)
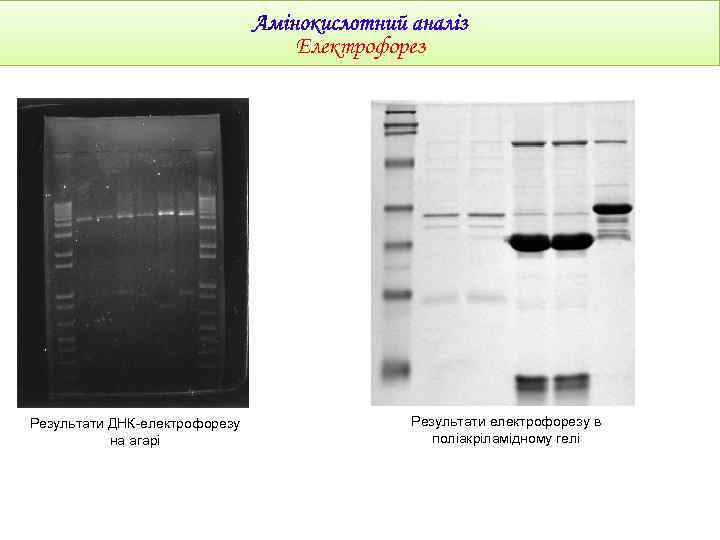
Електрофорез Результати ДНК-електрофорезу на агарі Результати електрофорезу в поліакріламідному гелі
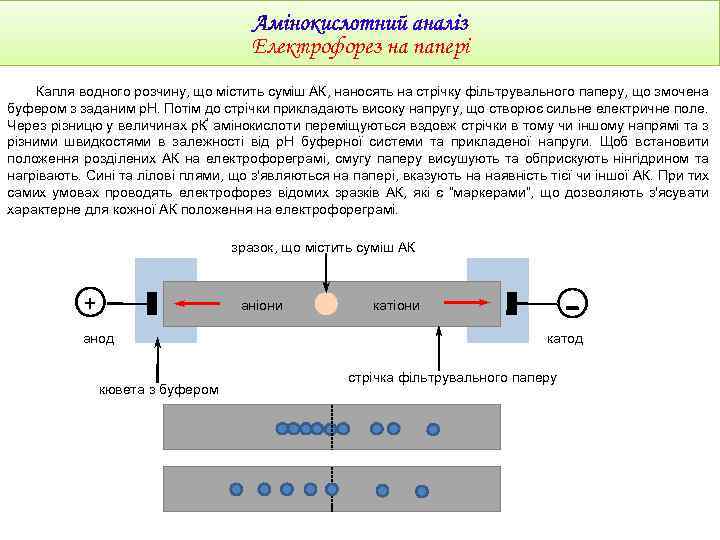
Електрофорез на папері Капля водного розчину, що містить суміш АК, наносять на стрічку фільтрувального паперу, що змочена буфером з заданим р. Н. Потім до стрічки прикладають високу напругу, що створює сильне електричне поле. Через різницю у величинах р. К’ амінокислоти переміщуються вздовж стрічки в тому чи іншому напрямі та з різними швидкостями в залежності від р. Н буферної системи та прикладеної напруги. Щоб встановити положення розділених АК на електрофореграмі, смугу паперу висушують та обприскують нінгідрином та нагрівають. Сині та лілові плями, що з'являються на папері, вказують на наявність тієї чи іншої АК. При тих самих умовах проводять електрофорез відомих зразків АК, які є “маркерами”, що дозволяють з'ясувати характерне для кожної АК положення на електрофореграмі. зразок, що містить суміш АК + аніони анод кювета з буфером катіони - катод стрічка фільтрувального паперу
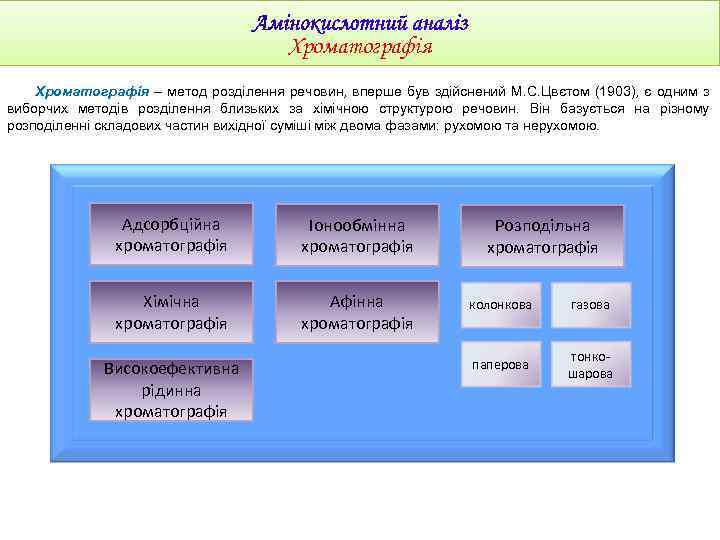
Хроматографія – метод розділення речовин, вперше був здійснений М. С. Цвєтом (1903), є одним з виборчих методів розділення близьких за хімічною структурою речовин. Він базується на різному розподіленні складових частин вихідної суміші між двома фазами: рухомою та нерухомою. Адсорбційна хроматографія Іонообмінна хроматографія Хімічна хроматографія Афінна хроматографія Високоефективна рідинна хроматографія Розподільна хроматографія колонкова газова паперова тонкошарова
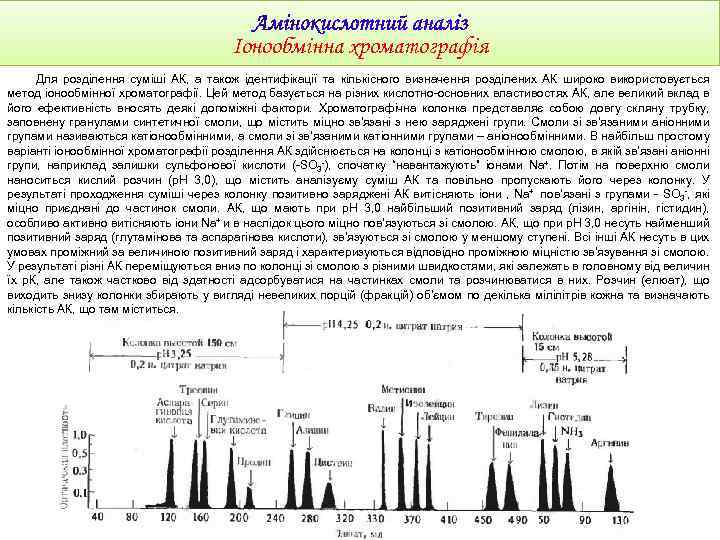
Іонообмінна хроматографія Для розділення суміші АК, а також ідентифікації та кількісного визначення розділених АК широко використовується метод іонообмінної хроматографії. Цей метод базується на різних кислотно-основних властивостях АК, але великий вклад в його ефективність вносять деякі допоміжні фактори. Хроматографічна колонка представляє собою довгу скляну трубку, заповнену гранулами синтетичної смоли, що містить міцно зв'язані з нею заряджені групи. Смоли зі зв’язаними аніонними групами називаються катіонообмінними, а смоли зі зв’язаними катіонними групами – аніонообмінними. В найбільш простому варіанті іонообмінної хроматографії розділення АК здійснюється на колонці з катіонообмінною смолою, в якій зв'язані аніонні групи, наприклад залишки сульфонової кислоти (-SO 3 -), спочатку “навантажують” іонами Na+. Потім на поверхню смоли наноситься кислий розчин (р. Н 3, 0), що містить аналізуєму суміш АК та повільно пропускають його через колонку. У результаті проходження суміші через колонку позитивно заряджені АК витісняють іони , Na+ пов’язані з групами - SO 3 -, які міцно приєднані до частинок смоли. АК, що мають при р. Н 3, 0 найбільший позитивний заряд (лізин, аргінін, гістидин), особливо активно витісняють іони Na+ и в наслідок цього міцно пов’язуються зі смолою. АК, що при р. Н 3, 0 несуть найменший позитивний заряд (глутамінова та аспарагінова кислоти), зв’язуються зі смолою у меншому ступені. Всі інші АК несуть в цих умовах проміжний за величиною позитивний заряд і характеризуються відповідно проміжною міцністю зв’язування зі смолою. У результаті різні АК переміщуються вниз по колонці зі смолою з різними швидкостями, які залежать в головному від величин їх р. К, але також частково від здатності адсорбуватися на частинках смоли та розчинюватися в них. Розчин (елюат), що виходить знизу колонки збирають у вигляді невеликих порцій (фракцій) об’ємом по декілька мілілітрів кожна та визначають кількість АК, що там міститься.
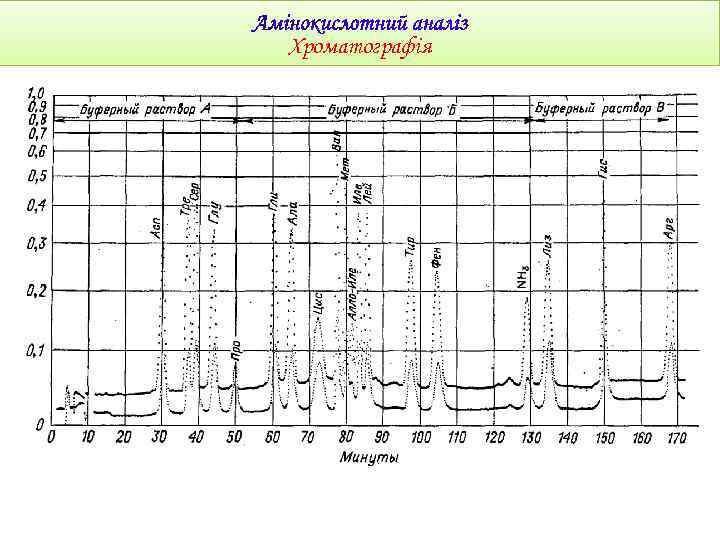
Хроматографія

Характерні хімічні реакції Здібність АК вступати в хімічні реакції визначається наявністю в їх складі функціональних груп. Оскільки АК містять аміногрупу та карбоксильну групу, кожна з них може вступати в хімічні реакції, характерні для цих груп. Наприклад, аміногрупи можуть бути ацитильовані, а карбоксильні групи – етирифіковані. Однією з широко використовуваних реакцій для ідентифікації Ак є нінгідринова реакція. При нагріванні АК з залишком нінгідрина утворюється продукт лілового кольору, якщо АК містить вільну аміногрупу, та жовтий колір продукту, якщо аміногрупа є заміщеною. При відповідно підібраних умовах інтенсивність фарбування можна використовувати для колориметричного визначення концентрацій АК. Другою важливою реакцією АК є їх взаємодія з 1 -фтор-2, 4 -динітробензолом (ФДНБ). В м’якому лужному розчині ФДНБ реагує з АК, в результаті чого утворюється 2, 4 -динітрофенольні похідні, які можна використовувати для ідентифікації окремих АК. Окрім цих основних реакцій, існують реакції, що є специфічними для виявлення певних АК Реакція Адамкевича Реакція Ван Слайка Реакція Вуазена Реакція Мілона Реакція Гопкінса. Коле Реакція Мак Карті та Салівана Реакція Паулі

Аланін – входить до складу багатьох білків. Легко перетворюється в печінці в глюкозу та навпаки. Цей процес носить назву глюкозо-аланінового циклу та є одним з основних шляхів глюконеогенеза в печінці. Аланін відноситься до числа замінних АК, так як легко синтезується в організмі тварин та людини з безазотистих попередників та азоту, що засвоюється. Є важливим джерелом енергії для м’язових тканин, головного мозку та центральної нервової системи; укріпляє імунну систему шляхом вироблення антитіл; активно приймає участь в метаболізмі цукрів та органічних кислот. Аргінін – АК, яка є замінною для дорослих та незамінною для дітей. Входить до складу білків, особливо протамінів (85%), та гістонів. Аргінін сприяє прискоренню синтезу гормону росту та інших гормонів. Приймає участь в синтезі сечовини та процесах азотного обміну. Аргінін є донором та природнім переносником азоту. Аргінін постачає азот в систему ферментів, що називаються NO-синтетазами, які синтезують NO, або нітрозо-групу. Нітрозо-група – це медіатор міорелаксації судин артеріального русла. Тобто нітрозо-група – це головна речовина, що регулює тонус судин артеріального русла, від якого залежить діастолічний тиск. Аргінін приймає участь в процесі переамінування та виведення з організму кінцевого азоту, тобто продукту розпаду відпрацьованих білків. Аргінін є носієм та донором азоту, який необхідний для при синтезі м’язової тканини. Сприяє збільшенню м’язової маси та зменшенню жирів при адекватному фізичному навантаженню. Окрім того, аргінін володіє вираженим психотропним ефектом, сприяє покращенню настрою, робить людину активною та витривалою. Аргінін є присутнім в рецептурі гепатопротекторів, імуномодуляторів, кардіологічних препаратів, лікарських препаратів опікових хворих, хворих на ВІЧ/СПІД, а також в рецептурах для парентерального харчування в післяопераційний період. Аспарагін – амід аспарагінової кислоти. Шляхом утворення аспарагіна з аспарагінової кислоти в організмі зв’язується токсичний аміак. Аспарагінова кислота є присутньою в організмі в складі білків та у вільному вигляді; відіграє важливу роль в обміні азотистих речовин; приймає участь в утворенні піримідинових основ та сечовини; так само як аспарагін є критично важливими для росту та розмноження лейкозних клітин при деяких типах лімфолейкоза; сприяє підвищенню споживання кисню серцевим м'язом. Володіє антитератогенною дією.

Валін – входить до складу білків. Названа на честь валеріани. Валін є вихідною речовиною при біосинтезі пантотенової кислоти (вітамін В 3) та пеніциліну. Окрім того, валін є незамінною АК. Є одним з головних компонентів в рості та синтезі тканин тіла. Головне джерело – тваринні продукти. Входить до складу комплексонів, що використовуються для виведення радіонуклідів із організму. Валін підвищує м’язову координацію та знижує чутливість організму до болі, холоду та спеки. Гістидин входить до складу активних центрів більшості ферментів, є попередником в біосинтезі гістаміну, піддаючись декарбоксилюванню. Один з “суттєвих” АК, сприяє росту та відновленню тканин. В великій кількості знаходиться в гемоглобіні; використовується при лікуванні ревматоїдних артритів, алергій, різних видів гепатиту, виразкової хвороби шлунку та дванадцятипалої кишки, анемій. Нестача гістидина може визвати послаблення слуху. Гістидином багаті наступні продукти тунець, лосось, свиняча вирізка, курині грудки, соєві боби, арахіс, чечевиця. Гліцин входить до складу білків та біологічно активних з’єднань. Із гліцина в організмі синтезуються порфірини та пуринові основи. Окрім того подібно ГАМК, гліцин є медіатором гальмування в ЦНС. В медичній практиці використовується для лікування хронічного алкоголізму, похідна гліцину – бетаїн – покращує процеси травлення. Чинить позитивний вплив при м'язовій дистрофії. Гліцин застосовують при депресивних розладах, підвищенній дратівливості. Він нормалізує сон. Глутамін є амідом моноамнодікарбонової глутамінової кислоти. Є досить розповсюдженим в природі, для людини є умовно замінною АК. В тілі людини циркулює в крові та накопичується в м'язах. Входить в основу синтезу ДНК; відіграє важливу роль при синтезі білка; головне джерело ентероцитів; стимулятор ділення імунних клітин, чим підсилює імунні функції; регулятор кислотно-основного балансу в нирковому виробництві амонію; альтернативне джерело енергії мозку. Знаходиться в куриці, рибі, яйцях, молоці, йогурті тощо. Глутамінова кислота - використовується в психіатрії при епілепсії, для лікування дитячого слабоумства, післяродових травм. Окрім того вона використовується в комплексній терапії виразки шлунку та при гіпоксії. Досить ефективним препаратом є похідна речовина глутамінової кислоти – гамааміномасляна кислота або ГАМК гальмує передачу нервового імпульсу в синапсах центральної нервової системи (ЦНС). Окрім того, ГАМК впливає на обмін глюкози, тканинне дихання та окислювальне фосфорилювання в головному мозку.

Ізолейцин входить до складу всіх природних білків. Є незамінною АК. Приймає участь в енергетичному обміні. При нестачі ферментів, що каталізують декарбоксилювання ізолейцину, виникає кетоацидурія. Лейцин – незамінна АК. Входить до складу всіх природних білків, використовується для лікування хвороб печінки, анемій тощо. Лізин – незамінна АК. Лізин входить до складу білків. Є необхідною для росту та відновлення тканин, виробництва антитіл, гормонів, ферментів та альбумінів. Ця АК здійснює противовірусну дію, особливо по відношенню до вірусів, що викликають герпес та гострі респіраторні інфекції. Лізин підтримує рівень енергії та зберігає здоровим серце, завдяки карнитину, який в організмі з нього утворюється. Лізин приймає участь в формуванні колагена та відновленні тканин. Його використовують у відновлювальний період після операцій та спортивних травм. Лізин покращую засвоєння кальцію з крові та транспортує його в кісткову тканину. Лізин посилює дію аргініну. Лізин у сполуці з вітаміном С попереджує утворення ліпопротеїнів, що викликають закупорювання артерій. Лізин уповільнює пошкодження кришталика. Лізин знаходиться в рибі, м'ясі, молочних продуктах, горіхах, бобах, фруктах, овочах. Метионін має в своєму складі рухому метильну групу, яка здатна переноситися на інші клітинні структури в процесах метилювання, наприклад в процесах кон'югації чи синтезу холіну. Захищає організм при отруєннях бактеріальними ендотоксинами та деякими іншими отрутами. Володіє радіопротектними властивостями. Серин бере участь в утворенні аміноспирту сфінгозину, що входить до складу сфінгомієліну – ліпіду, який є у складі головного мозку та переферійних нервових волокон. Тирозин є вихідною речовиною для синтезу всіх йодовмісних гормонів щитоподібної залози, а також адреналіну, норадреналіну та меланіну. Цистеїн синтезується в організмі за наявності метіоніну. За відсутності метіоніну або в разі порушення його перетворення на цистеїн може призводити до порушення обмінних процесів в організмі. Цистеїн бере участь в обміні речовин кришталика ока, а при зміні його вмісту виникає катаракта. Виявлено позитивну дію цистеїну при отруєнні солями важких металів.
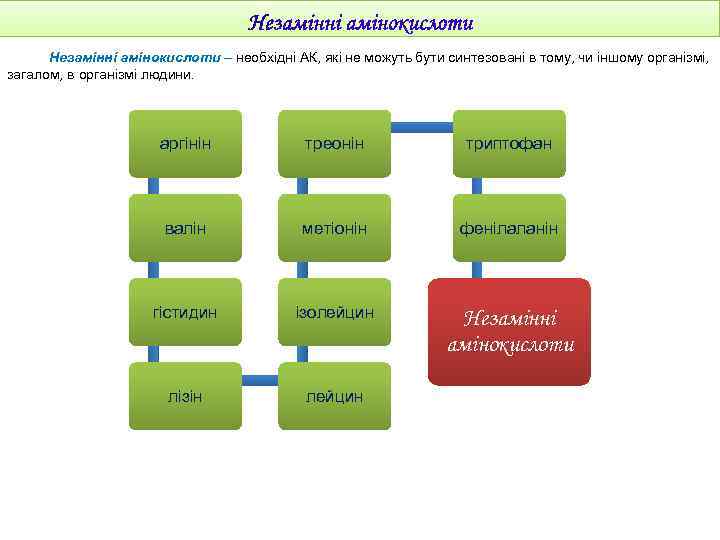
Незамінні амінокислоти – необхідні АК, які не можуть бути синтезовані в тому, чи іншому організмі, загалом, в організмі людини. аргінін треонін триптофан валін метіонін фенілаланін гістидин ізолейцин Незамінні амінокислоти лізін лейцин
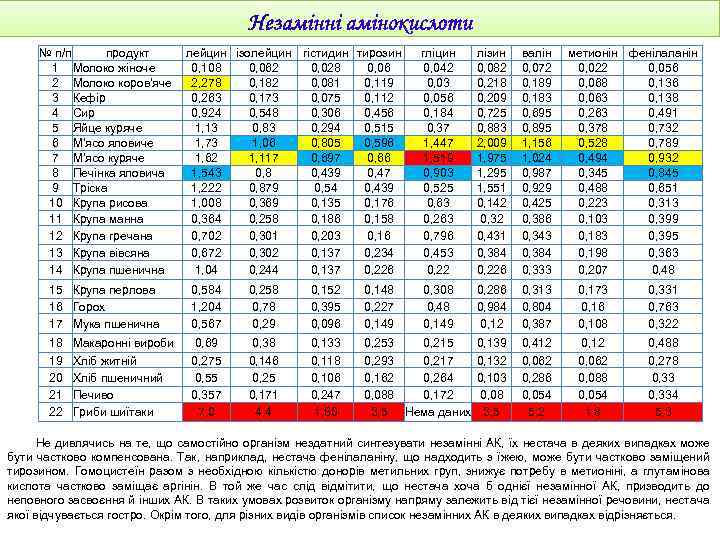
№ п/п продукт 1 Молоко жіноче 2 Молоко коров'яче 3 Кефір 4 Сир 5 Яйце куряче 6 М'ясо яловиче 7 М'ясо куряче 8 Печінка яловича 9 Тріска 10 Крупа рисова 11 Крупа манна 12 Крупа гречана 13 Крупа вівсяна 14 Крупа пшенична лейцин ізолейцин гістидин тирозин 0, 108 0, 062 0, 028 0, 06 2, 278 0, 182 0, 081 0, 119 0, 263 0, 173 0, 075 0, 112 0, 924 0, 548 0, 306 0, 456 1, 13 0, 83 0, 294 0, 515 1, 73 1, 06 0, 805 0, 596 1, 62 1, 117 0, 697 0, 66 1, 543 0, 8 0, 439 0, 47 1, 222 0, 879 0, 54 0, 439 1, 008 0, 369 0, 135 0, 176 0, 364 0, 258 0, 186 0, 158 0, 702 0, 301 0, 203 0, 16 0, 672 0, 302 0, 137 0, 234 1, 04 0, 244 0, 137 0, 226 гліцин 0, 042 0, 03 0, 056 0, 184 0, 37 1, 447 1, 519 0, 903 0, 525 0, 63 0, 263 0, 796 0, 453 0, 22 лізин 0, 082 0, 218 0, 209 0, 725 0, 883 2, 009 1, 975 1, 295 1, 551 0, 142 0, 32 0, 431 0, 384 0, 226 валін 0, 072 0, 189 0, 183 0, 695 0, 895 1, 156 1, 024 0, 987 0, 929 0, 425 0, 386 0, 343 0, 384 0, 333 0, 308 0, 48 0, 149 0, 286 0, 984 0, 12 0, 313 0, 804 0, 387 0, 173 0, 16 0, 108 0, 331 0, 763 0, 322 0, 139 0, 132 0, 103 0, 08 3, 5 0, 412 0, 062 0, 286 0, 054 5, 2 0, 12 0, 062 0, 088 0, 054 1, 8 0, 488 0, 278 0, 334 5, 3 15 Крупа перлова 16 Горох 17 Мука пшенична 0, 584 1, 204 0, 567 0, 258 0, 78 0, 29 0, 152 0, 395 0, 096 0, 148 0, 227 0, 149 18 19 20 21 22 0, 69 0, 275 0, 55 0, 357 7, 0 0, 38 0, 146 0, 25 0, 171 4, 4 0, 133 0, 118 0, 106 0, 247 1, 80 0, 253 0, 215 0, 293 0, 217 0, 162 0, 264 0, 088 0, 172 3, 5 Нема даних Макаронні вироби Хліб житній Хліб пшеничний Печиво Гриби шиїтаки метионін фенілаланін 0, 022 0, 056 0, 068 0, 136 0, 063 0, 138 0, 263 0, 491 0, 378 0, 732 0, 528 0, 789 0, 494 0, 932 0, 345 0, 845 0, 488 0, 651 0, 223 0, 313 0, 103 0, 399 0, 183 0, 395 0, 198 0, 363 0, 207 0, 48 Не дивлячись на те, що самостійно організм нездатний синтезувати незамінні АК, їх нестача в деяких випадках може бути частково компенсована. Так, наприклад, нестача фенілаланіну, що надходить з їжею, може бути частково заміщений тирозином. Гомоцистеїн разом з необхідною кількістю донорів метильних груп, знижує потребу в метионіні, а глутамінова кислота частково заміщає аргінін. В той же час слід відмітити, що нестача хоча б однієї незамінної АК, призводить до неповного засвоєння й інших АК. В таких умовах розвиток організму напряму залежить від тієї незамінної речовини, нестача якої відчувається гостро. Окрім того, для різних видів організмів список незамінних АК в деяких випадках відрізняється.
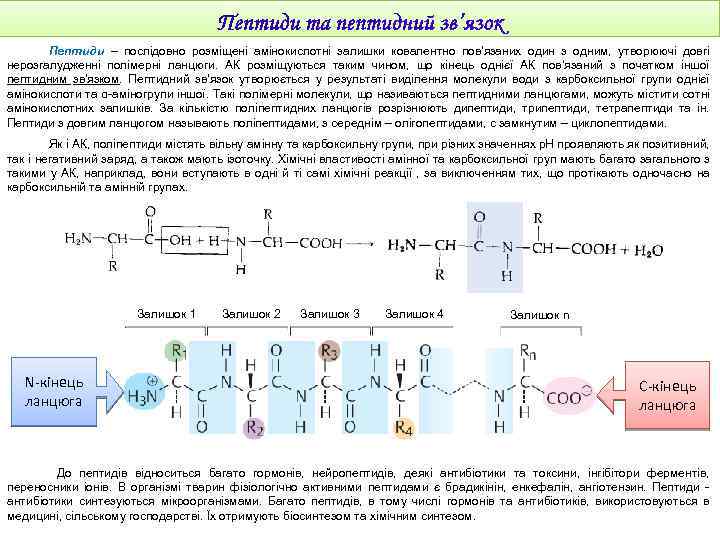
Пептиди – послідовно розміщені амінокислотні залишки ковалентно пов'язаних один з одним, утворюючі довгі нерозгалудженні полімерні ланцюги. АК розміщуються таким чином, що кінець однієї АК пов’язаний з початком іншої пептидним зв'язком. Пептидний зв’язок утворюється у результаті виділення молекули води з карбоксильної групи однієї амінокислоти та α-аміногрупи іншої. Такі полімерні молекули, що називаються пептидними ланцюгами, можуть містити сотні амінокислотних залишків. За кількістю поліпептидних ланцюгів розрізнюють дипептиди, трипептиди, тетрапептиди та ін. Пептиди з довгим ланцюгом называють поліпептидами, з середнім – олігопептидами, с замкнутим – циклопептидами. Як і АК, поліпептиди містять вільну амінну та карбоксильну групи, при різних значеннях р. Н проявляють як позитивний, так і негативний заряд, а також мають ізоточку. Хімічні властивості амінної та карбоксильної груп мають багато загального з такими у АК, наприклад, вони вступають в одні й ті самі хімічні реакції , за виключенням тих, що протікають одночасно на карбоксильній та амінній групах. Залишок 1 N-кінець ланцюга Залишок 2 Залишок 3 Залишок 4 Залишок n С-кінець ланцюга До пептидів відноситься багато гормонів, нейропептидів, деякі антибіотики та токсини, інгібітори ферментів, переносники іонів. В організмі тварин фізіологічно активними пептидами є брадикінін, енкефалін, ангіотензин. Пептиди антибіотики синтезуються мікроорганізмами. Багато пептидів, в тому числі гормонів та антибіотиків, використовуються в медицині, сільському господарстві. Їх отримують біосинтезом та хімічним синтезом.

На сьогодні виділено та вивчено декілька сотень природних пептидів, причому з’ясувалося, що багато з них відіграють самостійну фізіологічну роль. Пептидні антибіотики. Вони синтезуються мікроорганізмами, часто не за матричним механізмом. До їх складу входять непротеїногенні АК, а також їх D-ізомери. В якості прикладу може служити граміцидин S, в молекулі якого присутня амінокислота – орнітин та D-ізомери фенілаланіну: D-фен L-лей L-орн L-вал L-про L-вал L-орн L-лей D-фен граміцидин S Регуляторні пептиди – речовини, що регулюють більшість хімічних реакцій в клітинах та тканинах організму. До них відносяться пептидні гормони, наприклад інсулін, що контролює вміст глюкози в крові та інших клітинах, окситоцин, що стимулює скорочення гладкої мускулатури, вазопресин – регулятор водного обміну тощо. Окрім того, в останні роки інтенсивно розвивається вчення про нейропептиди. Деякі з них, наприклад опоїдні пептиди, за рецепторним принципом взаємодіють з різними ділянками головного мозку та формують ефект анальгезії, тобто зменшення больових відчуттів. Їх розділяють на ендорфіни, енкефаліни, динорфіни. Енкефаліни володіють нетривалою болезаспокійливою дією через швидку їх інактивацію пептидазами, в той час, коли довголанцюгові ендорфіни та динорфіни проявляють більш сильний та тривалий анальгетичний ефект.

Окрім того, слід відмітити такий біологічно активний пептид як глутатіон, що приймає участь в окислювально-відновлювальних процесах, а також в переносі АК через плазматичні мембрани O O ‖ ‖ HOOC―CH 2 ―C ―NH ―CH 2 ―COOH | | NH 2 CH 2 ―SH глутатіон Брадикінін – важливий компонент кінинової системи, що забезпечує регуляцію кровотоку та проникності клітинних стінок. Арг – Про – Фен – Сер – Фен – Арг брадикінін

Хімічний Синтез пептидів Ферментативний Це органічний синтез, характерною особливістю якого є необхідність тимчасового захисту тих хімічних угруповувань, які не повинні приймати участь в хімічних реакціях. При виборі блокувального агенту керуються можливістю його легкого відщеплення без зміни структури пептиду. Деякі біологічні каталізатори, що гідролізують пептидні зв'язки, в певних умовах здатні каталізувати оборотну реакцію, а саме утворювати пептидні зв'язки між окремими АК.

Розробка та дизайн слайд-лекції здійснено співробітниками кафедри БМЕ ХНУРЕ: науковим співробітником, аспіранткою Галайченко Оленою Миколаївною докт. фіз. -мат. наук, професором Рожицьким Миколою Миколайовичем
Lecture 2 (amino acids).ppt