 Основания
Основания
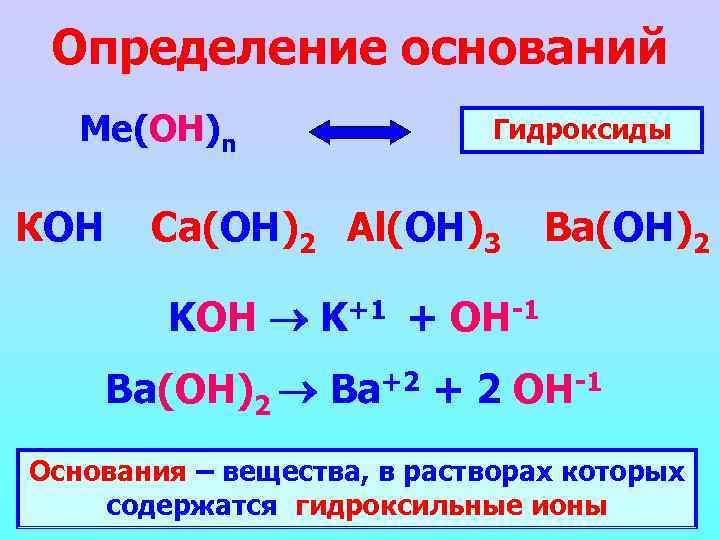 Определение оснований Ме(ОН)n Гидроксиды КОН Ca(ОН)2 Al(ОН)3 Ba(ОН)2 KOH K+1 + OH-1 Ba(ОН)2 Ba+2 + 2 OH-1 Основания – вещества, в растворах которых содержатся гидроксильные ионы
Определение оснований Ме(ОН)n Гидроксиды КОН Ca(ОН)2 Al(ОН)3 Ba(ОН)2 KOH K+1 + OH-1 Ba(ОН)2 Ba+2 + 2 OH-1 Основания – вещества, в растворах которых содержатся гидроксильные ионы
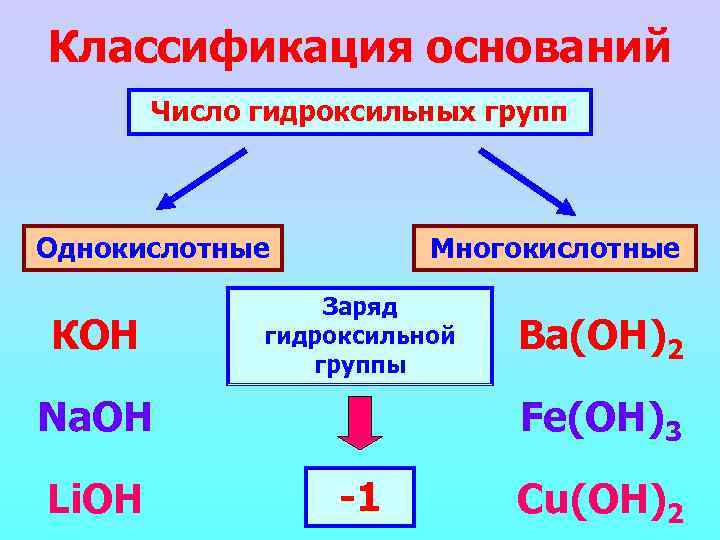 Классификация оснований Число гидроксильных групп Однокислотные КОН Многокислотные Заряд гидроксильной группы Na. OH Li. OH Ba(ОН)2 Fe(OH)3 -1 Cu(OH)2
Классификация оснований Число гидроксильных групп Однокислотные КОН Многокислотные Заряд гидроксильной группы Na. OH Li. OH Ba(ОН)2 Fe(OH)3 -1 Cu(OH)2
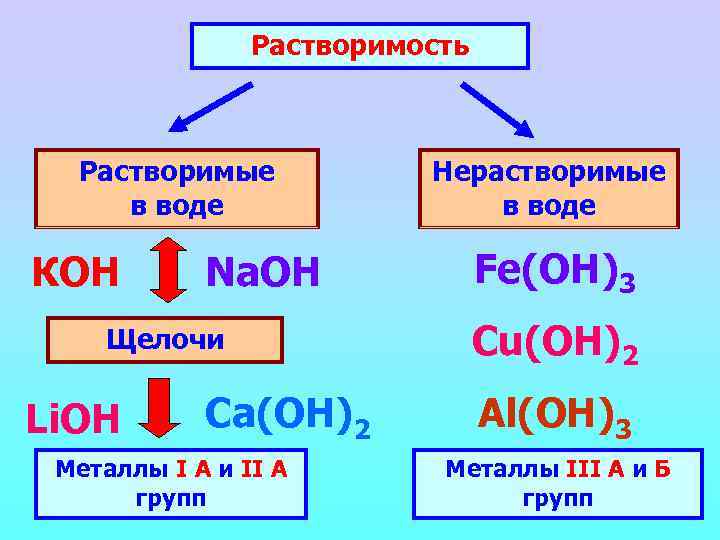 Растворимость Растворимые в воде КОН Na. OH Щелочи Li. OH Ca(ОН)2 Металлы I А и II А групп Нерастворимые в воде Fe(OH)3 Cu(OH)2 Al(ОН)3 Металлы III А и Б групп
Растворимость Растворимые в воде КОН Na. OH Щелочи Li. OH Ca(ОН)2 Металлы I А и II А групп Нерастворимые в воде Fe(OH)3 Cu(OH)2 Al(ОН)3 Металлы III А и Б групп
 Сильные и слабые основания Сильные основания Слабые основания Na. OH гидроксид Mg(OH)2 гидроксид натрия (едкий натр) магния KOH гидроксид калия Fe(OH)2 гидроксид (едкое кали) железа (II) Li. OH гидроксид Zn(OH)2 гидроксид лития цинка Ba(OH)2 гидроксид NH 4 OH гидроксид бария аммония Ca(OH)2 гидроксид Fe(OH)3 гидроксид кальция железа (III)
Сильные и слабые основания Сильные основания Слабые основания Na. OH гидроксид Mg(OH)2 гидроксид натрия (едкий натр) магния KOH гидроксид калия Fe(OH)2 гидроксид (едкое кали) железа (II) Li. OH гидроксид Zn(OH)2 гидроксид лития цинка Ba(OH)2 гидроксид NH 4 OH гидроксид бария аммония Ca(OH)2 гидроксид Fe(OH)3 гидроксид кальция железа (III)
 Получение оснований Щелочи Активный металл + вода 2 Na + 2 H 2 O 2 Na. OH + H 2 Основной оксид + вода K 2 O + H 2 O 2 KOH
Получение оснований Щелочи Активный металл + вода 2 Na + 2 H 2 O 2 Na. OH + H 2 Основной оксид + вода K 2 O + H 2 O 2 KOH
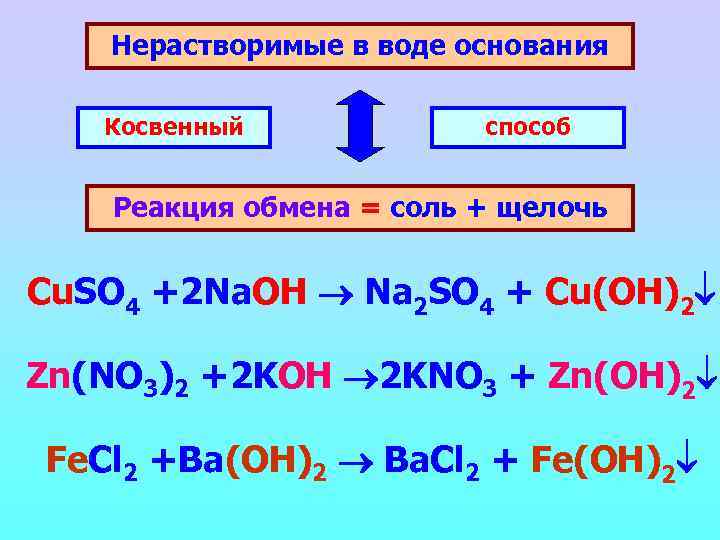 Нерастворимые в воде основания Косвенный способ Реакция обмена = соль + щелочь Cu. SO 4 +2 Na. OH Na 2 SO 4 + Cu(OH)2 Zn(NO 3)2 +2 KOH 2 KNO 3 + Zn(OH)2 Fe. Cl 2 +Ba(OH)2 Ba. Cl 2 + Fe(OH)2
Нерастворимые в воде основания Косвенный способ Реакция обмена = соль + щелочь Cu. SO 4 +2 Na. OH Na 2 SO 4 + Cu(OH)2 Zn(NO 3)2 +2 KOH 2 KNO 3 + Zn(OH)2 Fe. Cl 2 +Ba(OH)2 Ba. Cl 2 + Fe(OH)2
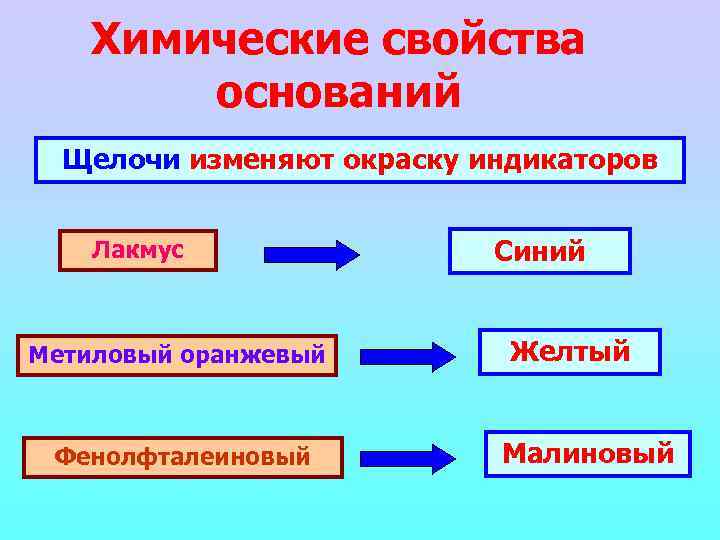 Химические свойства оснований Щелочи изменяют окраску индикаторов Лакмус Метиловый оранжевый Фенолфталеиновый Синий Желтый Малиновый
Химические свойства оснований Щелочи изменяют окраску индикаторов Лакмус Метиловый оранжевый Фенолфталеиновый Синий Желтый Малиновый
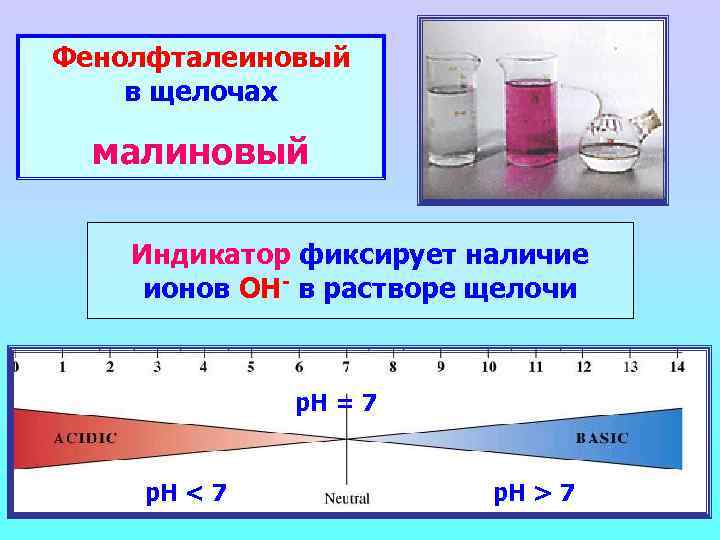 Фенолфталеиновый в щелочах малиновый Индикатор фиксирует наличие ионов ОН- в растворе щелочи р. Н = 7 р. Н < 7 р. Н > 7
Фенолфталеиновый в щелочах малиновый Индикатор фиксирует наличие ионов ОН- в растворе щелочи р. Н = 7 р. Н < 7 р. Н > 7
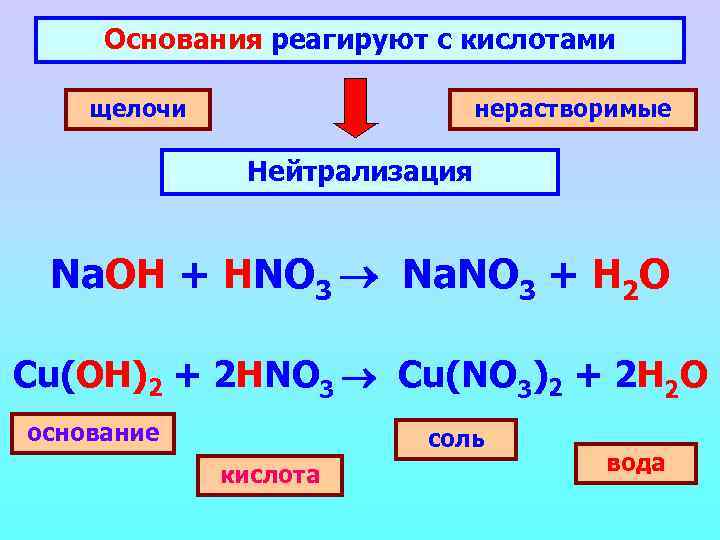 Основания реагируют с кислотами щелочи нерастворимые Нейтрализация Na. OH + HNO 3 Na. NO 3 + H 2 O Cu(OH)2 + 2 HNO 3 Cu(NO 3)2 + 2 H 2 O основание соль кислота вода
Основания реагируют с кислотами щелочи нерастворимые Нейтрализация Na. OH + HNO 3 Na. NO 3 + H 2 O Cu(OH)2 + 2 HNO 3 Cu(NO 3)2 + 2 H 2 O основание соль кислота вода
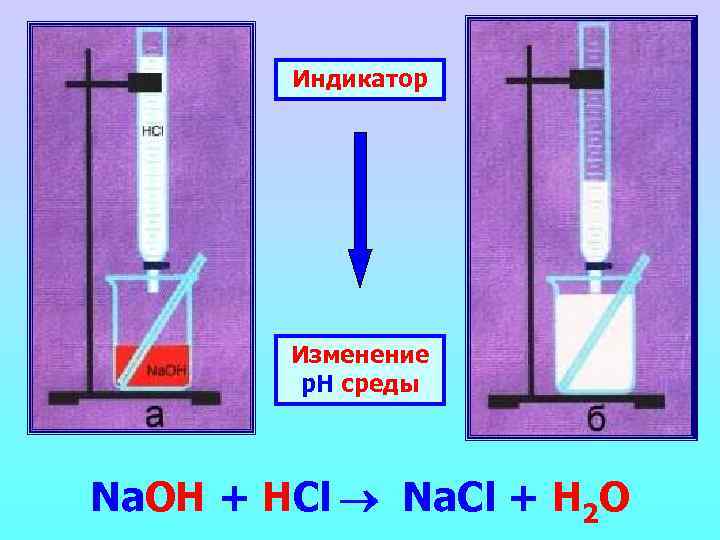 Индикатор Изменение р. Н среды Na. OH + HCl Na. Cl + H 2 O
Индикатор Изменение р. Н среды Na. OH + HCl Na. Cl + H 2 O
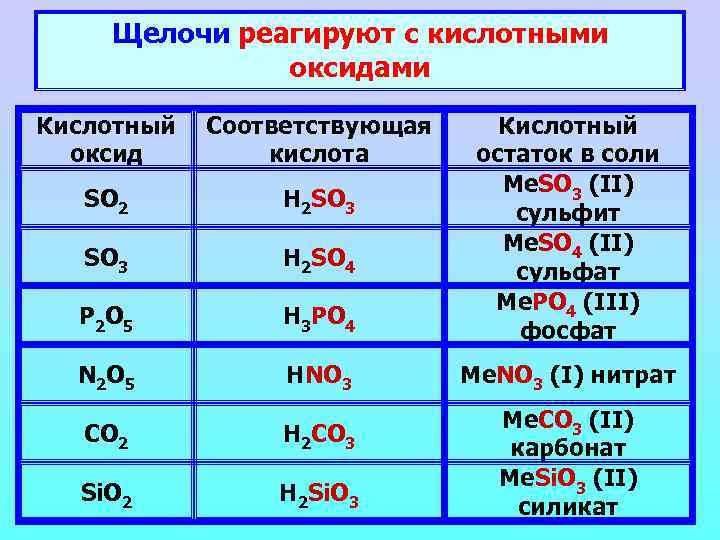 Щелочи реагируют с кислотными оксидами Кислотный Соответствующая оксид кислота SO 2 H 2 SO 3 H 2 SO 4 P 2 O 5 H 3 PO 4 Кислотный остаток в соли Me. SO 3 (II) сульфит Me. SO 4 (II) сульфат Me. PO 4 (III) фосфат N 2 O 5 HNO 3 Me. NO 3 (I) нитрат CO 2 H 2 CO 3 Si. O 2 H 2 Si. O 3 Me. CO 3 (II) карбонат Me. Si. O 3 (II) силикат
Щелочи реагируют с кислотными оксидами Кислотный Соответствующая оксид кислота SO 2 H 2 SO 3 H 2 SO 4 P 2 O 5 H 3 PO 4 Кислотный остаток в соли Me. SO 3 (II) сульфит Me. SO 4 (II) сульфат Me. PO 4 (III) фосфат N 2 O 5 HNO 3 Me. NO 3 (I) нитрат CO 2 H 2 CO 3 Si. O 2 H 2 Si. O 3 Me. CO 3 (II) карбонат Me. Si. O 3 (II) силикат
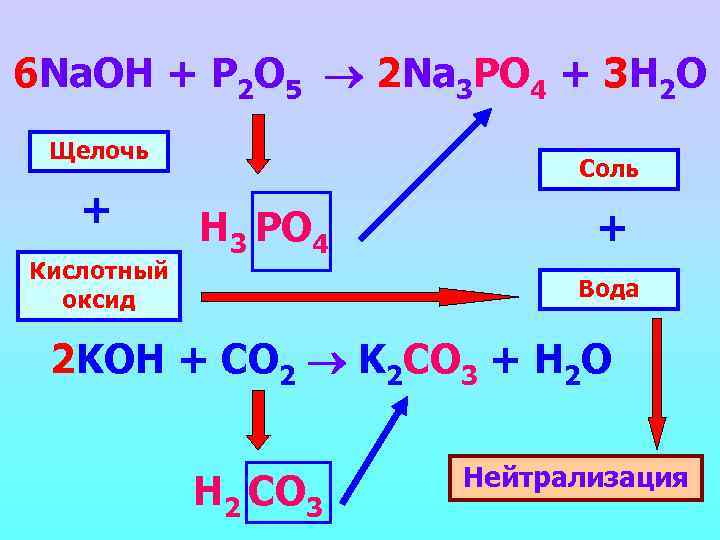 6 Na. OH + P 2 O 5 2 Na 3 PO 4 + 3 H 2 O Щелочь + Кислотный оксид Соль Н 3 PO 4 + Вода 2 KOH + CO 2 K 2 CO 3 + H 2 O Н 2 CO 3 Нейтрализация
6 Na. OH + P 2 O 5 2 Na 3 PO 4 + 3 H 2 O Щелочь + Кислотный оксид Соль Н 3 PO 4 + Вода 2 KOH + CO 2 K 2 CO 3 + H 2 O Н 2 CO 3 Нейтрализация
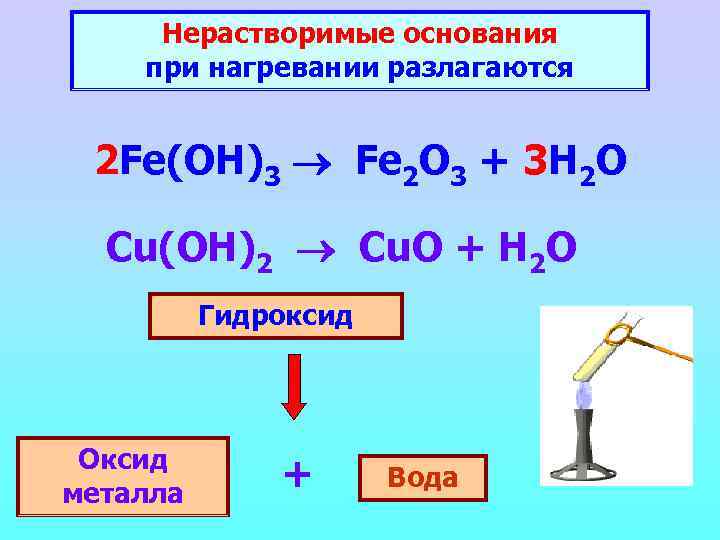 Нерастворимые основания при нагревании разлагаются 2 Fe(OH)3 Fe 2 O 3 + 3 H 2 O Cu(OH)2 Cu. O + H 2 O Гидроксид Оксид металла + Вода
Нерастворимые основания при нагревании разлагаются 2 Fe(OH)3 Fe 2 O 3 + 3 H 2 O Cu(OH)2 Cu. O + H 2 O Гидроксид Оксид металла + Вода
 –– Cu(OH)2 –t° Cu. O + H 2 O
–– Cu(OH)2 –t° Cu. O + H 2 O