основания.ppt
- Количество слайдов: 31

Основания. Электронное пособие для учащихся 8 -го класса. Ознакомление с классом «Основания»

Определение Основания – это сложные вещества, состоящие из атомов металлов и одной или нескольких гидроксильных групп (ОН). Общая формула: Ме (ОН)n, где n – валентность металла.

Классификация оснований Растворимые Нерастворимые Na. OH Mg(OH)2 Li. OH Cu(OH)2 KOH Fe(OH)3 Ba(OH)2 Al(OH)3 Ca(OH)2 Zn(OH)2 Образуют только активные металлы Образуют все остальные металлы

Составление химических формул оснований 1. Записывается металл и гидроксильная группа (ОН). 2. Над металлом записывается валентность. Валентность гидроксильной группы равна I. 3. Количество гидроксильных групп зависит от валентности металла. 4. Рядом с гидроксильной группой записывается индекс, равный валентности металла.

Построение формулы и названия основания III I Сr(OH)3 Название: гидроксид хрома (III). Если металл имеет постоянную валентность, то валентность в названии не указывается.

Потренируйся в составлении формул оснований Гидроксид меди (II) Гидроксид железа (III) Гидроксид кальция Гидроксид свинца (II) Гидроксид лития Сu(OH)2 Fe(OH)3 Ca(OH)2 Pb(OH)2 Li. OH

Физические свойства оснований: Растворимые основания - это твердые белые кристаллические вещества, хорошо растворимые в воде. Растворение как правило сопровождается выделением тепла. Нерастворимые основания – это твердые вещества, нерастворимые в воде. Имеют разнообразную окраску.

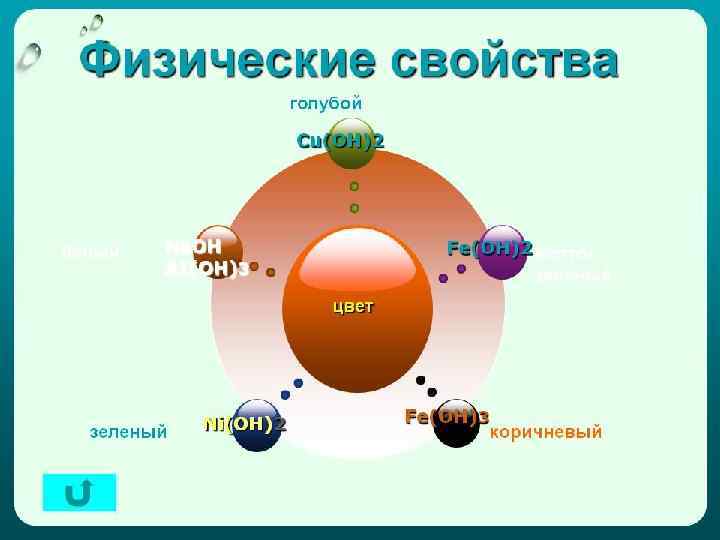
Физические свойства

Физические свойства оснований Ba(OH)2 Ca(OH)2 Li. OH Na. OH Cu(OH)2 Co(OH)2

Растворимые основания


Получение растворимых оснований
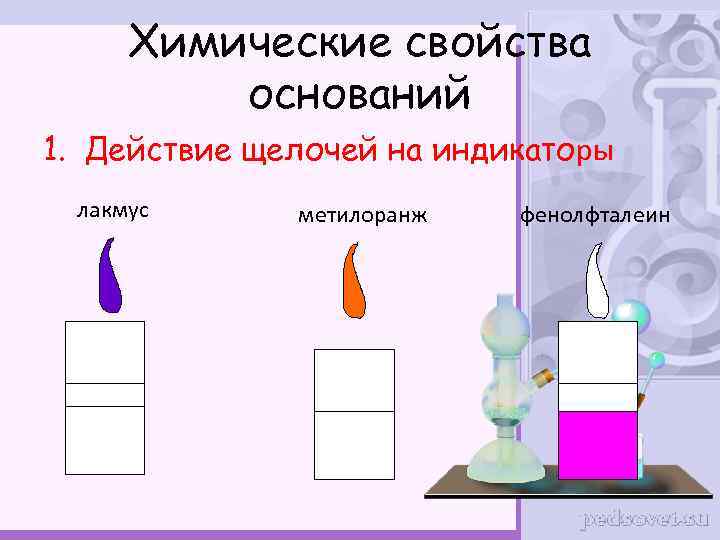
Химические свойства оснований 1. Действие щелочей на индикаторы лакмус метилоранж фенолфталеин

Химические свойства оснований 2. Взаимодействие с кислотными оксидами: Правило: При взаимодействии растворимых оснований с кислотными оксидами образуются соль и вода. 2 KOH + SO 2 = K 2 SO 3 + H 2 O (При составлении солей, напоминаю, что нужно вспомнить, какая кислота соответствует кислотному оксиду и записать ее кислотный остаток. В нашем случае SO 2 соответствует Н 2 SO 3, значит записываем кислотный остаток SO 3)

Химические свойства оснований 3. Взаимодействие с кислотами: Правило: При взаимодействии растворимых оснований с кислотами образуется соль и вода. HCl + Na. OH = Na. Cl + H 2 O Реакция взаимодействия кислоты и основания называется реакцией нейтрализации.

Химические свойства оснований

Химические свойства оснований 4. Взаимодействие с растворимыми солями: Правило: При взаимодействии растворимых солей с растворимыми основаниями образуются нерастворимые основания. Cu. Cl 2 + 2 KOH = Cu(OH)2↓+ 2 KCl Заметьте, что если в качестве продуктов реакции образуется растворимое основание, то реакция теряет смысл!

Нерастворимые основания

Получение нерастворимых оснований Правило: Чтобы получить нерастворимое основание, необходимо взять растворимую соль, содержащую необходимый металл и растворимое основание. Итак, получим Fe(OH)3 1. Находим по таблице растворимости растворимую соль железа (III).
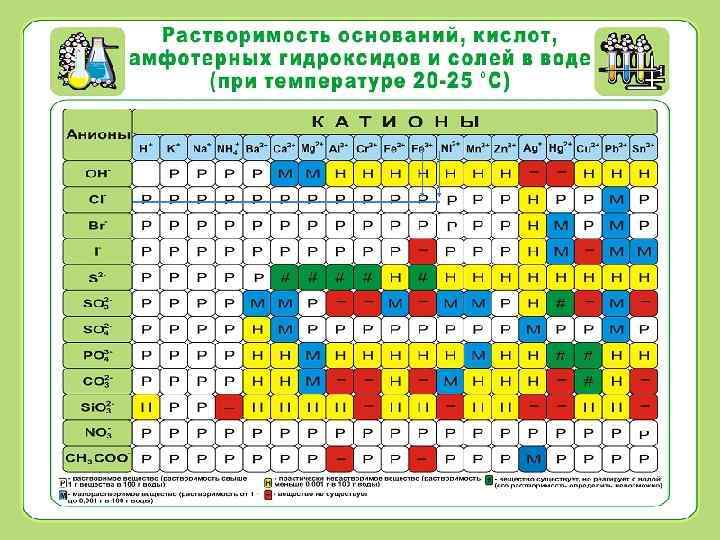

Получение нерастворимых оснований Это Fe. Cl 3, к нему добавляем растворимое основание Na. OH: Fe. Cl 3 + 3 Na. OH = Fe(OH)3 ↓+ 3 Na. Cl Чтобы посмотреть видео перейдите по ссылке: . . ВидеоГалиев Ильяс 10 А Опыты по химииНеорганикаоснов. классы неорг. соединполуч. нераств. оснований. wmv

Химические свойства нерастворимых оснований 1. Взаимодействие с кислотами: Правило: При взаимодействии нерастворимых оснований с кислотами образуется соль и вода. Zn(OH)2 + 2 HNO 3 = Zn(NO 3)2 + 2 H 2 O

Химические свойства нерастворимых оснований 2. При нагревании разлагаются Правило: При нагревании нерастворимые основания разлагаются на основной оксид и воду. II t II Сu(OH)2 = Cu. O + H 2 O При составлении формулы основного оксида, не забудьте учесть валентность металла. Какова она в основании, такая же валентность металла будет и в оксиде.

Химические свойства нерастворимых оснований Чтобы посмотреть видео перейдите по ссылке: . . ВидеоГалиев Ильяс 10 А Опыты по химииНеорганикаоснов. классы неорг. соединсвойства нераст. основан. . wmv
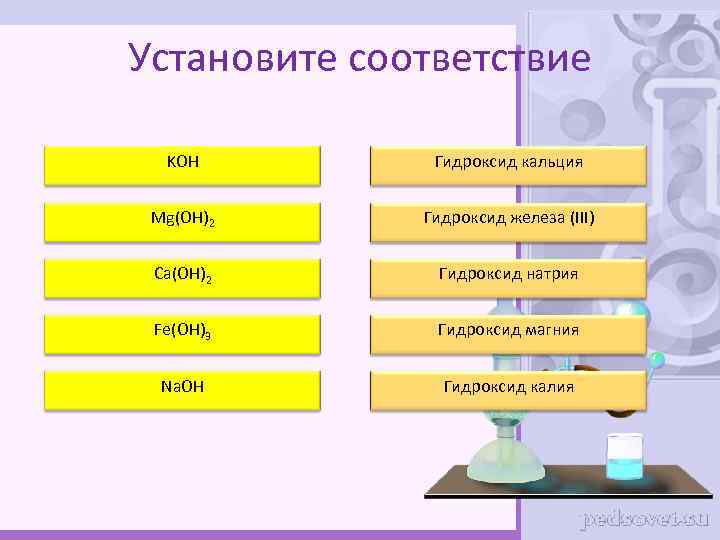
Установите соответствие KOH Гидроксид кальция Mg(OH)2 Гидроксид железа (III) Ca(OH)2 Гидроксид натрия Fe(OH)3 Гидроксид магния Na. OH Гидроксид калия

Выберите только основания. Ba. O P 2 O 5 KOH H 2 SO 4 Li. OH Ca(OH)2 Al(OH)3 HCl Mg(OH)2 Na. Cl H 2 O Mg. OHCl Fe(OH)3 Ba(OH)2 K 2 O NO Ag. NO 3 Ca. O Al 2 O 3

Напишите уравнения реакций Гидроксида калия с: - Азотной кислотой; - Оксидом фосфора (V); - Раствором нитрата меди (II) – Cu(NO 3)2 Гидроксида магния: - Серной кислотой; - Соляной кислотой; - Разложите при нагревании

Напишите уравнения реакций, с помощью которых можно получить - Гидроксид бария; - Гидроксид лития - Гидроксид цинка; - Гидроксид алюминия

Закончите уравнения осуществимых реакций: Са + H 2 O = SO 3 + Na. OH = Fe + H 2 O = P 2 O 5 + Pb(OH)2 = KOH + H 3 PO 4 = Be(OH)2 +H 2 SO 4 = Al. Cl 3 + Na. OH = Ca(OH)2 + CO 2 = Fe(OH)3 + N 2 O 5 = Al(OH)3 + H 2 SO 4 = Ba(OH)2 + HCl = Cu. SO 4 + Li. OH = Ca(NO 3)2 + KOH = P 2 O 5 + Na. OH = K + H 2 O = Sn(OH)2 = … + … Ba(OH)2 = … + … H 2 Si. O 3 + Na. OH =

Осуществите цепочки превращений: 1. Na → Na. OH→Na 2 SO 3 ↓ Fe(OH)3 2. Zn→Zn. O→Zn(NO 3)2→Zn(OH)2→Zn. O 3. Cu→Cu. O→Cu. Cl 2→Cu(OH)2→Cu. SO 4→Cu(OH)2 ↓ Cu. O
основания.ppt