Осмий и Иридий..ppt
- Количество слайдов: 38
 Осмий открыт в 1804 году английским химиком Смитсоном Теннантом в сотрудничестве с Уильямом Х. Уолластоном в осадке, остающемся после растворения платины в царской водке. ОСМИЙ (лат. Osmium), Os, химический элемент VIII группы периодической системы, атомный номер 76, атомная масса 190, 2, относится к платиновым металлам. 5 s 25 p 65 d 66 s 2
Осмий открыт в 1804 году английским химиком Смитсоном Теннантом в сотрудничестве с Уильямом Х. Уолластоном в осадке, остающемся после растворения платины в царской водке. ОСМИЙ (лат. Osmium), Os, химический элемент VIII группы периодической системы, атомный номер 76, атомная масса 190, 2, относится к платиновым металлам. 5 s 25 p 65 d 66 s 2
 Изотопы В природе осмий встречается в виде семи изотопов, 6 из которых стабильны: 184 Os, 187 Os, 188 Os, 189 Os, 190 Os и 192 Os. На долю самого тяжёлого изотопа (осмия-192) приходится 41 %, на долю самого лёгкого изотопа (осмий 184) лишь 0, 018 % общих «запасов» . Осмий-186 подвержен альфа-распаду, но учитывая его исключительно большой период полураспада — (2, 0 ± 1, 1)· 1015 лет, — его можно считать практически стабильным. Согласно расчётам, остальные естественные изотопы тоже способны к альфа-распаду, но с ещё большим полупериодом, поэтому их альфа-распад экспериментально не наблюдался. Теоретически для 184 Os и 192 Os возможен двойной бета-распад, наблюдениями также не зафиксированный. Изотоп осмий-187 является результатом распада изотопа рения (187 Re, период полураспада 4, 56· 1010 лет). Он активно используется при датировке горных пород и метеоритов (рений-осмиевый метод). Наиболее известным применением осмия в методах датировки является иридиево-осмиевый метод, применявшийся для анализа кварцев из пограничного слоя, разделяющего меловой и третичны периоды. Разделение изотопов осмия представляет собой достаточно сложную задачу. Именно поэтому некоторые изотопы довольно дороги. Первый и единственный экспортёр чистого осмия-187 — Казахстан, с января 2004 года официально предлагающий это вещество по цене 10 000 долларов за 1 грамм. Широкого практического применения осмий-187 не имеет. По некоторым данным, целью операций с этим изотопом было отмывание нелегальных капиталов.
Изотопы В природе осмий встречается в виде семи изотопов, 6 из которых стабильны: 184 Os, 187 Os, 188 Os, 189 Os, 190 Os и 192 Os. На долю самого тяжёлого изотопа (осмия-192) приходится 41 %, на долю самого лёгкого изотопа (осмий 184) лишь 0, 018 % общих «запасов» . Осмий-186 подвержен альфа-распаду, но учитывая его исключительно большой период полураспада — (2, 0 ± 1, 1)· 1015 лет, — его можно считать практически стабильным. Согласно расчётам, остальные естественные изотопы тоже способны к альфа-распаду, но с ещё большим полупериодом, поэтому их альфа-распад экспериментально не наблюдался. Теоретически для 184 Os и 192 Os возможен двойной бета-распад, наблюдениями также не зафиксированный. Изотоп осмий-187 является результатом распада изотопа рения (187 Re, период полураспада 4, 56· 1010 лет). Он активно используется при датировке горных пород и метеоритов (рений-осмиевый метод). Наиболее известным применением осмия в методах датировки является иридиево-осмиевый метод, применявшийся для анализа кварцев из пограничного слоя, разделяющего меловой и третичны периоды. Разделение изотопов осмия представляет собой достаточно сложную задачу. Именно поэтому некоторые изотопы довольно дороги. Первый и единственный экспортёр чистого осмия-187 — Казахстан, с января 2004 года официально предлагающий это вещество по цене 10 000 долларов за 1 грамм. Широкого практического применения осмий-187 не имеет. По некоторым данным, целью операций с этим изотопом было отмывание нелегальных капиталов.
 Физические свойства: 1) Цвет у него оловянно-белый, а оттенок – голубовато-серый 2) Считается самым тяжёлым металлом 3) Плотность: 22, 587 ± 0, 009 г/см³ 4) Твёрдый, но при этом хрупкий, и из него легко получается порошок 5) t кип осмия точно неизвестна – учёные считают, что это примерно 5500°C, а t плав=3000°C 6) При сравнении различных изотопов этих металлов, наиплотнейшим оказывается 192 Os 7) Необычайно высокая плотность осмия объясняется лантаноидным сжатием, а также гексагональной плотноупакованной кристаллической решёткой 8) Высокая твёрдость и исключительная тугоплавкость позволяет использовать осмий в качестве покрытия в узлах трения
Физические свойства: 1) Цвет у него оловянно-белый, а оттенок – голубовато-серый 2) Считается самым тяжёлым металлом 3) Плотность: 22, 587 ± 0, 009 г/см³ 4) Твёрдый, но при этом хрупкий, и из него легко получается порошок 5) t кип осмия точно неизвестна – учёные считают, что это примерно 5500°C, а t плав=3000°C 6) При сравнении различных изотопов этих металлов, наиплотнейшим оказывается 192 Os 7) Необычайно высокая плотность осмия объясняется лантаноидным сжатием, а также гексагональной плотноупакованной кристаллической решёткой 8) Высокая твёрдость и исключительная тугоплавкость позволяет использовать осмий в качестве покрытия в узлах трения
 Свойства атома 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 13. 14. 15. 16. 17. Атомная масса(молярная масса) - 190, 23 а. е. м. (г/моль) Электронная конфигурация[Xe] - 4 f 14 5 d 6 6 s 2 Радиус атома - 135 Нм Ковалентный радиус - 126 Нм Радиус иона - (+6 e) 69 (+4 e) 88 Нм Электроотрицательность - 2, 2 (шкала Полинга) Энергия ионизации -(первый электрон)819, 8(8, 50) к. Дж/моль (э. В) Плотность (при н. у. ) - 22, 587 г/см³ Температура плавления -3327 K Температура кипения - 5300 K Теплота плавления - 31, 7 к. Дж/моль Теплота испарения - 738 к. Дж/моль Молярная теплоёмкость - 24, 7 Дж/(K·моль) Молярный объём - 8, 43 см³/моль Структура решётки - гексагональная Теплопроводность - (300 K) (87, 6) Вт/(м·К) Eион(Ме=>Ме++e) = 8, 7 э. В.
Свойства атома 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 13. 14. 15. 16. 17. Атомная масса(молярная масса) - 190, 23 а. е. м. (г/моль) Электронная конфигурация[Xe] - 4 f 14 5 d 6 6 s 2 Радиус атома - 135 Нм Ковалентный радиус - 126 Нм Радиус иона - (+6 e) 69 (+4 e) 88 Нм Электроотрицательность - 2, 2 (шкала Полинга) Энергия ионизации -(первый электрон)819, 8(8, 50) к. Дж/моль (э. В) Плотность (при н. у. ) - 22, 587 г/см³ Температура плавления -3327 K Температура кипения - 5300 K Теплота плавления - 31, 7 к. Дж/моль Теплота испарения - 738 к. Дж/моль Молярная теплоёмкость - 24, 7 Дж/(K·моль) Молярный объём - 8, 43 см³/моль Структура решётки - гексагональная Теплопроводность - (300 K) (87, 6) Вт/(м·К) Eион(Ме=>Ме++e) = 8, 7 э. В.
![Степени окисления осмия − 2 Na 2[Os(CO)4] − 1 Na 2[Os 4(CO)13] 0 Os Степени окисления осмия − 2 Na 2[Os(CO)4] − 1 Na 2[Os 4(CO)13] 0 Os](https://present5.com/presentation/3/23900203_100082030.pdf-img/23900203_100082030.pdf-5.jpg) Степени окисления осмия − 2 Na 2[Os(CO)4] − 1 Na 2[Os 4(CO)13] 0 Os 3(CO)12 +1 Os. I +2 Os. I 2 +3 Os. Br 3 +4 Os. O 2, Os. Cl 4 +5 Os. F 5 +6 Os. F 6 +7 Os. OF 5, Os. F 7 +8 (стабильна) Os. O 4, Os(NCH 3)4
Степени окисления осмия − 2 Na 2[Os(CO)4] − 1 Na 2[Os 4(CO)13] 0 Os 3(CO)12 +1 Os. I +2 Os. I 2 +3 Os. Br 3 +4 Os. O 2, Os. Cl 4 +5 Os. F 5 +6 Os. F 6 +7 Os. OF 5, Os. F 7 +8 (стабильна) Os. O 4, Os(NCH 3)4
 Самый дорогой металл – это изотоп Осмия 187 Os Для того чтобы получить осмий 187 OS – необходимо провести много химических реакций и технологических процессов. Первым экспертом в «производстве» этого изотопа является Казахстан. В 2004 году цена озвученная за 1 грамм составила $10000. До этого никто его не продавал. На черном рынке стоимость самого дорогого метала, доходит до $200 000 за грамм. Узнать цену такого металла вряд ли можно по телефону. Но стоит заметить, что любая современная организация, каким бы видом деятельности она не занималась, старается сделать свой коллектив самым профессиональным и квалифицированным. А качественная корпоративная сотовая связь — это возможность быть в курсе всех событий компании.
Самый дорогой металл – это изотоп Осмия 187 Os Для того чтобы получить осмий 187 OS – необходимо провести много химических реакций и технологических процессов. Первым экспертом в «производстве» этого изотопа является Казахстан. В 2004 году цена озвученная за 1 грамм составила $10000. До этого никто его не продавал. На черном рынке стоимость самого дорогого метала, доходит до $200 000 за грамм. Узнать цену такого металла вряд ли можно по телефону. Но стоит заметить, что любая современная организация, каким бы видом деятельности она не занималась, старается сделать свой коллектив самым профессиональным и квалифицированным. А качественная корпоративная сотовая связь — это возможность быть в курсе всех событий компании.
 Получение 1. Осмий выделяют из обогащённого сырья платиновых металлов путём прокаливания этого концентрата на воздухе при температурах 800— 900 °C. При этом сублимируют пары Os. O 4, которые далее поглощают раствором Na. OH. 2. Упариванием раствора выделяют соль — перосмат натрия, который далее восстанавливают водородом при 120°C до осмия: Na 2[Os. O 2(OH)4] + 3 H 2 = 2 Na. OH + Os + 4 H 2 O. (Осмий при этом получается в виде губки. ) 3. Отделение основано на летучести Os. O 4. После перевода сырья в раствор добавляют окислитель, газообразный Os. O 4 улавливают раствором КОН, осаждают в виде [Os. O 2(NH 3)4]Cl 2, который восстанавливают водородом.
Получение 1. Осмий выделяют из обогащённого сырья платиновых металлов путём прокаливания этого концентрата на воздухе при температурах 800— 900 °C. При этом сублимируют пары Os. O 4, которые далее поглощают раствором Na. OH. 2. Упариванием раствора выделяют соль — перосмат натрия, который далее восстанавливают водородом при 120°C до осмия: Na 2[Os. O 2(OH)4] + 3 H 2 = 2 Na. OH + Os + 4 H 2 O. (Осмий при этом получается в виде губки. ) 3. Отделение основано на летучести Os. O 4. После перевода сырья в раствор добавляют окислитель, газообразный Os. O 4 улавливают раствором КОН, осаждают в виде [Os. O 2(NH 3)4]Cl 2, который восстанавливают водородом.
 Распространённость: в земной коре — 0, 007 г/т в перидотитах — 0, 15 г/т в эклогитах — 0, 16 г/т в формациях дунитов -перидотитов — 0, 013 г/т в формациях пироксенитов — 0, 007 г/т
Распространённость: в земной коре — 0, 007 г/т в перидотитах — 0, 15 г/т в эклогитах — 0, 16 г/т в формациях дунитов -перидотитов — 0, 013 г/т в формациях пироксенитов — 0, 007 г/т
 Химические свойства 1. Компактный осмий не растворяется в горячей соляной кислоте и кипящей царской водке, а мелко раздробленный осмий окисляется в азотной кислоте и кипящей серной кислоте до высшего оксида: Os + 8 HNO 3 = Os. O 4 + 4 H 2 O + 8 NO 2 2. При нагревании осмий реагирует со фтором, хлором, кислородом, серой, другими халькогенами и неметаллами. Os + 3 F 2 = Os. F 6 (при 250– 300°C), Os + Cl 2 = Os. Cl 4 (при 650– 700°C). 3. При сплавлении в присутствии окислителей осмий реагирует со щелочами. При этом образуются осматы (VI) — соли неустойчивой осмиевой кислоты H 2 Os. O 4: 2 Os + 4 Na. OH + 3 O 2 = 2 Na 2 Os. O 4 + 2 H 2 O 4. Для осмия наиболее характерно образование оксидов Os. O 4 и Os. O 2. В газовой фазе существуют оксиды Os. O и Os. O 3. 5. Не растворяется в холодной и горячей воде.
Химические свойства 1. Компактный осмий не растворяется в горячей соляной кислоте и кипящей царской водке, а мелко раздробленный осмий окисляется в азотной кислоте и кипящей серной кислоте до высшего оксида: Os + 8 HNO 3 = Os. O 4 + 4 H 2 O + 8 NO 2 2. При нагревании осмий реагирует со фтором, хлором, кислородом, серой, другими халькогенами и неметаллами. Os + 3 F 2 = Os. F 6 (при 250– 300°C), Os + Cl 2 = Os. Cl 4 (при 650– 700°C). 3. При сплавлении в присутствии окислителей осмий реагирует со щелочами. При этом образуются осматы (VI) — соли неустойчивой осмиевой кислоты H 2 Os. O 4: 2 Os + 4 Na. OH + 3 O 2 = 2 Na 2 Os. O 4 + 2 H 2 O 4. Для осмия наиболее характерно образование оксидов Os. O 4 и Os. O 2. В газовой фазе существуют оксиды Os. O и Os. O 3. 5. Не растворяется в холодной и горячей воде.
 6. Тетраоксид осмия Os. O 4 проявляет кислотные свойства и является сильным окислителем. Os. O 4 + Na. OH = Na 2[Os. O 4(OH)2]. 7. Диоксид осмия Os. O 2 получают аккуратным обезвоживанием в атмосфере азота Os(OH)4. При этом образуется черная модификация Os. O 2. Она реакционноспособнее коричневой модификации Os. O 2, получаемой электровосстановлением щелочного раствора Os. O 4 или реакцией осмия с Os. O 4: Os + Os. O 4 = 2 Os. O 2. 8. Гидроксид осмия(IV) Os(OH)4 (Os. O 2· 2 H 2 O) получают восстановлением солей осмия (VI) — осматов этиловым спиртом. 9. Для степеней окисления осмия 0 и +2 наиболее характерно образование осмийорганических соединений со связью Os—C или карбонилов: Os + 5 CO = Os(CO)5. 3 Os(CO)5 = Os 3(CO)12 + 3 CO Os 3(CO)12 + 6 Na = 3 Na 2 Os(CO)4.
6. Тетраоксид осмия Os. O 4 проявляет кислотные свойства и является сильным окислителем. Os. O 4 + Na. OH = Na 2[Os. O 4(OH)2]. 7. Диоксид осмия Os. O 2 получают аккуратным обезвоживанием в атмосфере азота Os(OH)4. При этом образуется черная модификация Os. O 2. Она реакционноспособнее коричневой модификации Os. O 2, получаемой электровосстановлением щелочного раствора Os. O 4 или реакцией осмия с Os. O 4: Os + Os. O 4 = 2 Os. O 2. 8. Гидроксид осмия(IV) Os(OH)4 (Os. O 2· 2 H 2 O) получают восстановлением солей осмия (VI) — осматов этиловым спиртом. 9. Для степеней окисления осмия 0 и +2 наиболее характерно образование осмийорганических соединений со связью Os—C или карбонилов: Os + 5 CO = Os(CO)5. 3 Os(CO)5 = Os 3(CO)12 + 3 CO Os 3(CO)12 + 6 Na = 3 Na 2 Os(CO)4.
 10. Та же соль получается, особенно при нагревании, и из раствора Os. O 4 просто в избытке крепкого КОН, при чем, конечно, должен выделиться кислород. 11. Соответствующая осмистая кислота H 2 Os. O 4 получается при разложении водой калиевой соли в присутствии спирта и в струе водорода, так как при доступе воздуха образуется Os. O 4; эта кислота обладает цветом сажи и нерастворима в воде; серная кислота на нее не действует, соляная на холоде слабо действует, а азотная легко, превращая в Os. O 4; способ получения: K 2 Os. O 4 + 2 Н 2 О= H 2 Os. O 4 + 2 КОН Показывает, что это тоже очень слабая кислота; ангидрид её Os. O 3 неизвестен. 12. Соединения осмия ускоряют реакцию восстановления нитратиона до нитрит-иона а-нафтилами-ном.
10. Та же соль получается, особенно при нагревании, и из раствора Os. O 4 просто в избытке крепкого КОН, при чем, конечно, должен выделиться кислород. 11. Соответствующая осмистая кислота H 2 Os. O 4 получается при разложении водой калиевой соли в присутствии спирта и в струе водорода, так как при доступе воздуха образуется Os. O 4; эта кислота обладает цветом сажи и нерастворима в воде; серная кислота на нее не действует, соляная на холоде слабо действует, а азотная легко, превращая в Os. O 4; способ получения: K 2 Os. O 4 + 2 Н 2 О= H 2 Os. O 4 + 2 КОН Показывает, что это тоже очень слабая кислота; ангидрид её Os. O 3 неизвестен. 12. Соединения осмия ускоряют реакцию восстановления нитратиона до нитрит-иона а-нафтилами-ном.
 Соединения двухвалентного осмия. Оксид осмия (II) Os. O Серовато-черный порошок, мало растворимый в воде и кислотах. Получают: Нагреванием смеси осмия, сульфита осмия (II) и карбоната натрия в токе диоксида углерода. Хлорид осмия (II) Os. Cl 2 Расплывающийся на воздухе темно-коричневый порошок, мало растворимый в воде и в щелочах. Растворяется в спирте, эфире и азотной кислоте. Получают: Нагреванием хлорида осмия (III) при 500 о. С и пониженном давлении. Иодид осмия (II) Os. I 2 Зеленое твердое вещество, которое образуется при обработке кислых растворов солей осмия (IV) иодидом калия.
Соединения двухвалентного осмия. Оксид осмия (II) Os. O Серовато-черный порошок, мало растворимый в воде и кислотах. Получают: Нагреванием смеси осмия, сульфита осмия (II) и карбоната натрия в токе диоксида углерода. Хлорид осмия (II) Os. Cl 2 Расплывающийся на воздухе темно-коричневый порошок, мало растворимый в воде и в щелочах. Растворяется в спирте, эфире и азотной кислоте. Получают: Нагреванием хлорида осмия (III) при 500 о. С и пониженном давлении. Иодид осмия (II) Os. I 2 Зеленое твердое вещество, которое образуется при обработке кислых растворов солей осмия (IV) иодидом калия.
 Соединения трехвалентного осмия. Оксид осмия (III) Os 2 O 3 Темно-коричневый порошок (или медно-красные чешуйки), мало растворимый в воде. Получают: Восстановлением Os. O 4 металлическим осмием при нагревании или нагреванием солей осмия (III) с карбонатом натрия в токе диоксида углерода. Хлорид осмия (III) Os. Cl 3 Гигроскопичные коричневые кубические кристаллы. Легко растворяется в воде и спирте. Разлагается на Os. Cl 2 и Cl 2 выше 500 о. С. Превращается в Os. О 4 при длительном кипячении с азотной кислотой. Известен кристаллогидрат Os. Cl 3. 3 Н 2 О. Получают: Быстрым охлаждением паров, выделяющихся при нагревании металлического осмия в хлоре при 1050 о. С.
Соединения трехвалентного осмия. Оксид осмия (III) Os 2 O 3 Темно-коричневый порошок (или медно-красные чешуйки), мало растворимый в воде. Получают: Восстановлением Os. O 4 металлическим осмием при нагревании или нагреванием солей осмия (III) с карбонатом натрия в токе диоксида углерода. Хлорид осмия (III) Os. Cl 3 Гигроскопичные коричневые кубические кристаллы. Легко растворяется в воде и спирте. Разлагается на Os. Cl 2 и Cl 2 выше 500 о. С. Превращается в Os. О 4 при длительном кипячении с азотной кислотой. Известен кристаллогидрат Os. Cl 3. 3 Н 2 О. Получают: Быстрым охлаждением паров, выделяющихся при нагревании металлического осмия в хлоре при 1050 о. С.
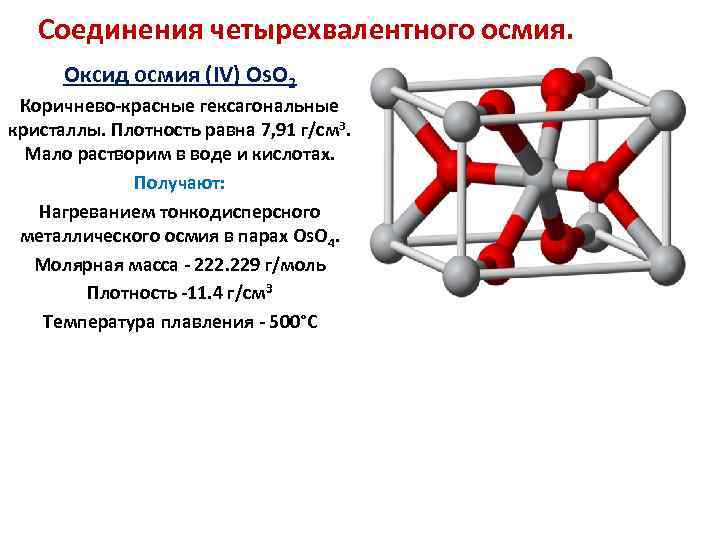 Соединения четырехвалентного осмия. Оксид осмия (IV) Os. O 2 Коричнево-красные гексагональные кристаллы. Плотность равна 7, 91 г/см 3. Мало растворим в воде и кислотах. Получают: Нагреванием тонкодисперсного металлического осмия в парах Os. O 4. Молярная масса - 222. 229 г/моль Плотность -11. 4 г/см³ Температура плавления - 500°C
Соединения четырехвалентного осмия. Оксид осмия (IV) Os. O 2 Коричнево-красные гексагональные кристаллы. Плотность равна 7, 91 г/см 3. Мало растворим в воде и кислотах. Получают: Нагреванием тонкодисперсного металлического осмия в парах Os. O 4. Молярная масса - 222. 229 г/моль Плотность -11. 4 г/см³ Температура плавления - 500°C
 Фторид осмия (IV) Os. F 4 Коричневый порошок, который Сульфид осмия (IV) Os. S 2 разлагается водой или при нагревании. tпл=230°С. Черные кубические Получают: кристаллы. Мало растворим в Пропусканием фтора над нагретым воде и спирте. При до 280°С металлическим осмием. нагревании на воздухе Хлорид осмия (IV) Os. Cl 4 превращается в Os. O 4. Коричнево-красные игольчатые Восстанавливается кристаллы, которые водой медленно водородом до металла. переводятся в Os. O 2. 2 Н 2 О. Разлагается Получают: при нагревании до 323°С. Прямым взаимодействием Получают: Обработкой Os. О 4 концентрированной элементов при нагревании. HCl или охлаждением коричневожелтых паров, образующихся при пропускании хлора над нагретым до 650 -700 о. С металлическим осмием.
Фторид осмия (IV) Os. F 4 Коричневый порошок, который Сульфид осмия (IV) Os. S 2 разлагается водой или при нагревании. tпл=230°С. Черные кубические Получают: кристаллы. Мало растворим в Пропусканием фтора над нагретым воде и спирте. При до 280°С металлическим осмием. нагревании на воздухе Хлорид осмия (IV) Os. Cl 4 превращается в Os. O 4. Коричнево-красные игольчатые Восстанавливается кристаллы, которые водой медленно водородом до металла. переводятся в Os. O 2. 2 Н 2 О. Разлагается Получают: при нагревании до 323°С. Прямым взаимодействием Получают: Обработкой Os. О 4 концентрированной элементов при нагревании. HCl или охлаждением коричневожелтых паров, образующихся при пропускании хлора над нагретым до 650 -700 о. С металлическим осмием.
![Соединения щестивалентного осмия. Фторид осмия (VI) Os. F 6 Желтые кристаллы. tпл=33°С [1], tкип=47°С Соединения щестивалентного осмия. Фторид осмия (VI) Os. F 6 Желтые кристаллы. tпл=33°С [1], tкип=47°С](https://present5.com/presentation/3/23900203_100082030.pdf-img/23900203_100082030.pdf-16.jpg) Соединения щестивалентного осмия. Фторид осмия (VI) Os. F 6 Желтые кристаллы. tпл=33°С [1], tкип=47°С [1]. Разъедает стекло. Гидролизуется водой. Взаимодействует со многими металлами и неметаллами. Пары фторида осмия (VI) бесцветны и токсичны. Получают: вместе с Os. F 4 и Os. F 8 при нагревании осмия в среде фтора. Осмат калия K 2 Os. O 4 Фиолетовые октаэдрические кристаллы. При нагревании превращается в Os. O 4. Разлагается кислотами. Получают: Восстановлением нитритом калия или спиртом Os. O 4 в растворе едкого кали.
Соединения щестивалентного осмия. Фторид осмия (VI) Os. F 6 Желтые кристаллы. tпл=33°С [1], tкип=47°С [1]. Разъедает стекло. Гидролизуется водой. Взаимодействует со многими металлами и неметаллами. Пары фторида осмия (VI) бесцветны и токсичны. Получают: вместе с Os. F 4 и Os. F 8 при нагревании осмия в среде фтора. Осмат калия K 2 Os. O 4 Фиолетовые октаэдрические кристаллы. При нагревании превращается в Os. O 4. Разлагается кислотами. Получают: Восстановлением нитритом калия или спиртом Os. O 4 в растворе едкого кали.
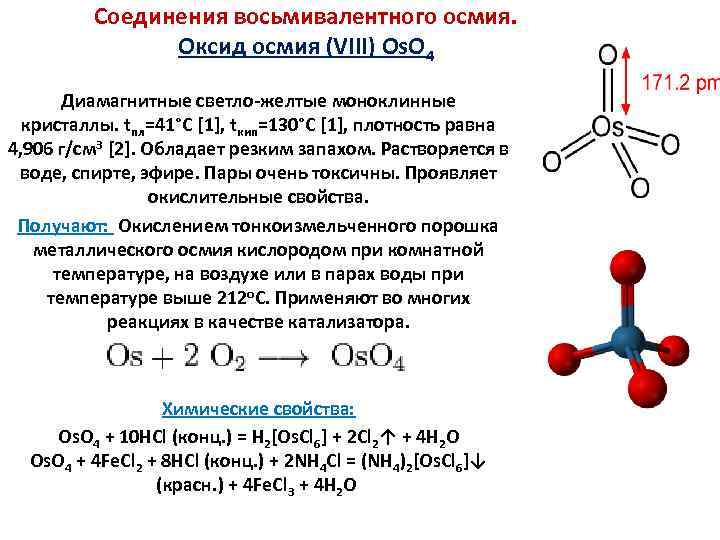 Соединения восьмивалентного осмия. Оксид осмия (VIII) Os. O 4 Диамагнитные светло-желтые моноклинные кристаллы. tпл=41°С [1], tкип=130°С [1], плотность равна 4, 906 г/см 3 [2]. Обладает резким запахом. Растворяется в воде, спирте, эфире. Пары очень токсичны. Проявляет окислительные свойства. Получают: Окислением тонкоизмельченного порошка металлического осмия кислородом при комнатной температуре, на воздухе или в парах воды при температуре выше 212 о. С. Применяют во многих реакциях в качестве катализатора. Химические свойства: Os. O 4 + 10 HCl (конц. ) = H 2[Os. Cl 6] + 2 Cl 2↑ + 4 H 2 O Os. O 4 + 4 Fe. Cl 2 + 8 HCl (конц. ) + 2 NH 4 Cl = (NH 4)2[Os. Cl 6]↓ (красн. ) + 4 Fe. Cl 3 + 4 H 2 O
Соединения восьмивалентного осмия. Оксид осмия (VIII) Os. O 4 Диамагнитные светло-желтые моноклинные кристаллы. tпл=41°С [1], tкип=130°С [1], плотность равна 4, 906 г/см 3 [2]. Обладает резким запахом. Растворяется в воде, спирте, эфире. Пары очень токсичны. Проявляет окислительные свойства. Получают: Окислением тонкоизмельченного порошка металлического осмия кислородом при комнатной температуре, на воздухе или в парах воды при температуре выше 212 о. С. Применяют во многих реакциях в качестве катализатора. Химические свойства: Os. O 4 + 10 HCl (конц. ) = H 2[Os. Cl 6] + 2 Cl 2↑ + 4 H 2 O Os. O 4 + 4 Fe. Cl 2 + 8 HCl (конц. ) + 2 NH 4 Cl = (NH 4)2[Os. Cl 6]↓ (красн. ) + 4 Fe. Cl 3 + 4 H 2 O
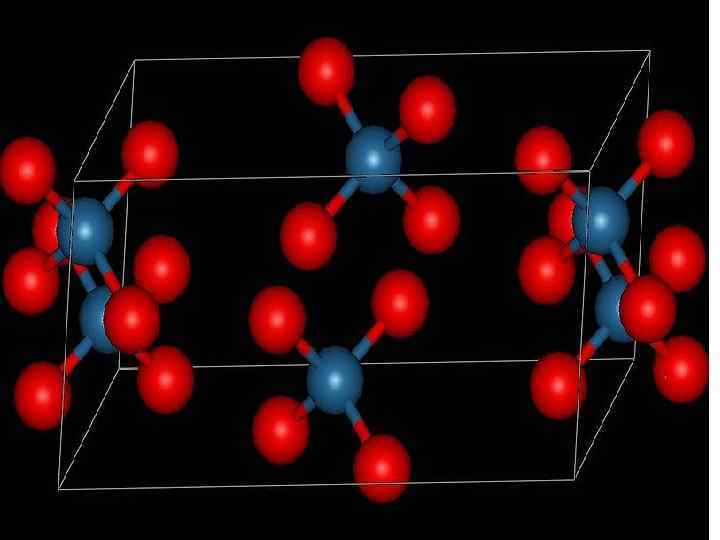
 Фторид осмия (VIII) Os. F 8 Желтые кристаллы. tпл=34, 4°С , tкип=47, 3°С. Разлагается при нагревании выше 225 о. С. Обладает окислительными свойствами. При попадании на кожу образует ожоги. Взаимодействует с водой с образованием Os. О 4 и плавиковой кислоты. Образуется при быстром охлаждении паров, полученных пропусканием фтора над нагретым до 250 о. С металлическим осмием. Молекулярная масса (в а. е. м. ): 304, 22 Стандартная энтропия образования S (298 К, Дж/моль·K): 358 (г) Стандартная мольная теплоемкость Cp (298 К, Дж/моль·K): 120, 9 (г) Энтальпия плавления ΔHпл (к. Дж/моль): 7 Энтальпия кипения ΔHкип (к. Дж/моль): 27, 6 Химические свойства: 1. Не окисляет трифториды сурьмы, брома. 2. Окисляет воду до кислорода. Окисляет иод до IF 5 при комнатной температуре. Реакция с жидким бромом дает Br 2(OSF 6). 3. С избытком трихлорида бора дает пентахлорид осмия.
Фторид осмия (VIII) Os. F 8 Желтые кристаллы. tпл=34, 4°С , tкип=47, 3°С. Разлагается при нагревании выше 225 о. С. Обладает окислительными свойствами. При попадании на кожу образует ожоги. Взаимодействует с водой с образованием Os. О 4 и плавиковой кислоты. Образуется при быстром охлаждении паров, полученных пропусканием фтора над нагретым до 250 о. С металлическим осмием. Молекулярная масса (в а. е. м. ): 304, 22 Стандартная энтропия образования S (298 К, Дж/моль·K): 358 (г) Стандартная мольная теплоемкость Cp (298 К, Дж/моль·K): 120, 9 (г) Энтальпия плавления ΔHпл (к. Дж/моль): 7 Энтальпия кипения ΔHкип (к. Дж/моль): 27, 6 Химические свойства: 1. Не окисляет трифториды сурьмы, брома. 2. Окисляет воду до кислорода. Окисляет иод до IF 5 при комнатной температуре. Реакция с жидким бромом дает Br 2(OSF 6). 3. С избытком трихлорида бора дает пентахлорид осмия.
 Сульфид осмия (VIII) Os. S 4 Темно-коричневый порошок. Получают: Пропусканием сероводорода через подкисленный раствор Os. O 4 или действием сульфидов аммония или натрия на щелочные растворы Os. O 4.
Сульфид осмия (VIII) Os. S 4 Темно-коричневый порошок. Получают: Пропусканием сероводорода через подкисленный раствор Os. O 4 или действием сульфидов аммония или натрия на щелочные растворы Os. O 4.
 Применение 1. Применяется как катализатор для синтеза аммиака, гидрирования органических соединений, в катализаторах метанольных топливных элементов. 2. Сплав «осрам» (осмия с вольфрамом) использовался для изготовления нитей ламп накаливания. 3. Есть сведения о применении осмия в военных целях, как часть артиллерийских снарядов и боеголовок ракет. Также применяется в электронной аппаратуре авиа- и ракетной техники. 4. Компонент сверхтвёрдых и износостойких сплавов с иридием и рутением (опорные оси точных приборов, наконечники перьев для авторучек). 5. Тетраоксид осмия применяется в электронно микроскопии для фиксации биологических объектов.
Применение 1. Применяется как катализатор для синтеза аммиака, гидрирования органических соединений, в катализаторах метанольных топливных элементов. 2. Сплав «осрам» (осмия с вольфрамом) использовался для изготовления нитей ламп накаливания. 3. Есть сведения о применении осмия в военных целях, как часть артиллерийских снарядов и боеголовок ракет. Также применяется в электронной аппаратуре авиа- и ракетной техники. 4. Компонент сверхтвёрдых и износостойких сплавов с иридием и рутением (опорные оси точных приборов, наконечники перьев для авторучек). 5. Тетраоксид осмия применяется в электронно микроскопии для фиксации биологических объектов.
 Иридий был открыт в 1803 году английским химиком С. Теннантом одновременно с осмием Ири дий — химический элемент с атомным номером 77 в периодической системе, обозначается символом Ir (лат. Iridium). очень твёрдый, тугоплавкий, серебристобелый переходный металл платиновой группы, обладающий высокой плотностью и сравнимый по этому параметру только с осмием (плотности Os и Ir практически равны с учетом расчетной погрешности). Имеет высокую коррозионную стойкость даже при температуре 2000 °C.
Иридий был открыт в 1803 году английским химиком С. Теннантом одновременно с осмием Ири дий — химический элемент с атомным номером 77 в периодической системе, обозначается символом Ir (лат. Iridium). очень твёрдый, тугоплавкий, серебристобелый переходный металл платиновой группы, обладающий высокой плотностью и сравнимый по этому параметру только с осмием (плотности Os и Ir практически равны с учетом расчетной погрешности). Имеет высокую коррозионную стойкость даже при температуре 2000 °C.
 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 13. 14. 15. 16. 17. 18. 19. 20. 21. 22. 23. 24. 25. 26. 27. Физические свойства: Атомный вес - 192. 22 Плотность - 22. 5 Температура плавления - 2447 °C Температура кипения - 4380 °C Атомная масса (молярная масса) - 192, 22 а. е. м. (г/моль) Электронная конфигурация - 4 f 14 5 d 7 6 s 2 Радиус атома - 136 Нм Радиус - 127 Нм Радиус иона - (+4 e) 68 Нм Электроотрицательность - 2, 20 (шкала Полинга) Электродный потенциал - Ir←Ir 3+ 1, 00 В Степени окисления - 6, 4, 3, 2, 1, 0, − 1 Энергия ионизации - (первый электрон)868, 1 (9, 00) к. Дж/моль (э. В) Плотность (при н. у. ) - 22. 65± 0. 01, 22, 65 г/см³ Температура плавления - 2447 K Температура кипения - 4380 K Теплота плавления - 26, 0 к. Дж/моль Теплота испарения - 610 к. Дж/моль Молярная теплоёмкость - 25, 1 Дж/(K·моль) Молярный объём - 8, 54 см³/моль Решётка кубическая гранецентрированная, а 0=0, 38387 нм H 0 пл 26 к. Дж/моль, H 0 исп 612 к. Дж/моль; S 0298 35, 4 Дж/(моль. К) Электрическое сопротивление — 5, 3· 10− 8 Ом·м (при 0 °C) Коэффициент линейного расширения — 6, 5× 10− 6 град Модуль нормальной упругости — 52, 029× 106 кг/мм²
1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 13. 14. 15. 16. 17. 18. 19. 20. 21. 22. 23. 24. 25. 26. 27. Физические свойства: Атомный вес - 192. 22 Плотность - 22. 5 Температура плавления - 2447 °C Температура кипения - 4380 °C Атомная масса (молярная масса) - 192, 22 а. е. м. (г/моль) Электронная конфигурация - 4 f 14 5 d 7 6 s 2 Радиус атома - 136 Нм Радиус - 127 Нм Радиус иона - (+4 e) 68 Нм Электроотрицательность - 2, 20 (шкала Полинга) Электродный потенциал - Ir←Ir 3+ 1, 00 В Степени окисления - 6, 4, 3, 2, 1, 0, − 1 Энергия ионизации - (первый электрон)868, 1 (9, 00) к. Дж/моль (э. В) Плотность (при н. у. ) - 22. 65± 0. 01, 22, 65 г/см³ Температура плавления - 2447 K Температура кипения - 4380 K Теплота плавления - 26, 0 к. Дж/моль Теплота испарения - 610 к. Дж/моль Молярная теплоёмкость - 25, 1 Дж/(K·моль) Молярный объём - 8, 54 см³/моль Решётка кубическая гранецентрированная, а 0=0, 38387 нм H 0 пл 26 к. Дж/моль, H 0 исп 612 к. Дж/моль; S 0298 35, 4 Дж/(моль. К) Электрическое сопротивление — 5, 3· 10− 8 Ом·м (при 0 °C) Коэффициент линейного расширения — 6, 5× 10− 6 град Модуль нормальной упругости — 52, 029× 106 кг/мм²
 Получение: Основной источник иридия — анодные шламы медноникелевого производства. Полученный шлам обогащают. Потом, действуя на него царской водкой, при нагревании переводят в раствор платину, палладий, родий, иридий и рутений в виде хлоридных комплексов H 2[Pt. Cl 6], H 2[Pd. Cl 4], H 3[Rh. Cl 6], H 2[Ir. Cl 6] и H 2[Ru. Cl 6]. Осмий остается в нерастворимом осадке. Из полученного раствора добавлением хлорида аммония NH 4 Cl сначала осаждают комплекс платины (NH 4)2[Pt. Cl 6], а затем комплекс иридия (NH 4)2[Ir. Cl 6] и рутения (NH 4)2[Ru. Cl 6]. При прокаливании (NH 4)2[Ir. Cl 6] на воздухе получают металлический иридий: (NH 4)2[Ir. Cl 6] = Ir + N 2 + 6 HCl + H 2.
Получение: Основной источник иридия — анодные шламы медноникелевого производства. Полученный шлам обогащают. Потом, действуя на него царской водкой, при нагревании переводят в раствор платину, палладий, родий, иридий и рутений в виде хлоридных комплексов H 2[Pt. Cl 6], H 2[Pd. Cl 4], H 3[Rh. Cl 6], H 2[Ir. Cl 6] и H 2[Ru. Cl 6]. Осмий остается в нерастворимом осадке. Из полученного раствора добавлением хлорида аммония NH 4 Cl сначала осаждают комплекс платины (NH 4)2[Pt. Cl 6], а затем комплекс иридия (NH 4)2[Ir. Cl 6] и рутения (NH 4)2[Ru. Cl 6]. При прокаливании (NH 4)2[Ir. Cl 6] на воздухе получают металлический иридий: (NH 4)2[Ir. Cl 6] = Ir + N 2 + 6 HCl + H 2.
 Химические свойства: - Отличается высокой химической стойкостью. С неметаллами взаимодействует только в мелкораздробленном состоянии при температуре красного каления. -Взаимодействие с кислородом происходит только при температуре выше 1000 °C, при этом образуется диоксид иридия Ir. O 2. - Оксиды иридия не растворяются в воде, кислотах и щелочах. - Компактный иридий при температурах до 100 °C не реагирует со всеми известными кислотами и их смесями, в том числе и с царской водкой. Для перевода этих металлов в растворимые в воде хлорокомплексы порошок, содержащий эти металлы, хлорируют при нагревании в присутствии комплексообразователя Na. Cl: Ir + 2 Cl 2 + 2 Na. Cl = Na 2[Ir. Cl 6] -Гидроксид Ir(OH)4 (Ir. O 2· 2 H 2 O) образуется при нейтрализации растворов хлороиридатов(IV) в присутствии окислителей. Осадок Ir 2 O 3·x. H 2 O выпадает при нейтрализации щелочью хлороиридатов (III) и легко окисляется на воздухе до Ir. O 2. - Гидроксиды иридия практически не растворяются в воде. В растворимую форму оксиды иридия переводят, окисляя их в присутствии комплексообразователя: Ir. O 2 + 4 HCl + 2 Na. Cl = Na 2[Ir. Cl 6] + 2 H 2 O. - Продуктом прямого взаимодействия иридия с фтором является гексафторид иридия Ir. F 6. Это соединение очень активно, оно не только реагирует с водой по уравнению Ir. F 6 + 5 H 2 O = Ir(OH)4 + 6 HF + 1/2 O 2, но окисляет даже хлор, причем образуются Ir. F 4 и Cl. F.
Химические свойства: - Отличается высокой химической стойкостью. С неметаллами взаимодействует только в мелкораздробленном состоянии при температуре красного каления. -Взаимодействие с кислородом происходит только при температуре выше 1000 °C, при этом образуется диоксид иридия Ir. O 2. - Оксиды иридия не растворяются в воде, кислотах и щелочах. - Компактный иридий при температурах до 100 °C не реагирует со всеми известными кислотами и их смесями, в том числе и с царской водкой. Для перевода этих металлов в растворимые в воде хлорокомплексы порошок, содержащий эти металлы, хлорируют при нагревании в присутствии комплексообразователя Na. Cl: Ir + 2 Cl 2 + 2 Na. Cl = Na 2[Ir. Cl 6] -Гидроксид Ir(OH)4 (Ir. O 2· 2 H 2 O) образуется при нейтрализации растворов хлороиридатов(IV) в присутствии окислителей. Осадок Ir 2 O 3·x. H 2 O выпадает при нейтрализации щелочью хлороиридатов (III) и легко окисляется на воздухе до Ir. O 2. - Гидроксиды иридия практически не растворяются в воде. В растворимую форму оксиды иридия переводят, окисляя их в присутствии комплексообразователя: Ir. O 2 + 4 HCl + 2 Na. Cl = Na 2[Ir. Cl 6] + 2 H 2 O. - Продуктом прямого взаимодействия иридия с фтором является гексафторид иридия Ir. F 6. Это соединение очень активно, оно не только реагирует с водой по уравнению Ir. F 6 + 5 H 2 O = Ir(OH)4 + 6 HF + 1/2 O 2, но окисляет даже хлор, причем образуются Ir. F 4 и Cl. F.
 - Реакция диспропорционирования Ir 2 O 3 =Ir + Ir. O 2 (при нагревании) - Соли иридия(III) с комплексными катионами аналогичны соответствующим солям хрома (III) и кобальта(III), представляют собой прочные комплексные соединения [Ir(NH 3)6]X 3, [Ir(OH 2)(NH 3)5]X 3, [Ir. X(NH 3)5]X 2. - Карбонилы иридия: желто-зеленый Ir 2(CO)8, возгоняется, и яркожелтый Ir 4(CO)12, при нагревании разлагается. Используются для нанесения покрытий.
- Реакция диспропорционирования Ir 2 O 3 =Ir + Ir. O 2 (при нагревании) - Соли иридия(III) с комплексными катионами аналогичны соответствующим солям хрома (III) и кобальта(III), представляют собой прочные комплексные соединения [Ir(NH 3)6]X 3, [Ir(OH 2)(NH 3)5]X 3, [Ir. X(NH 3)5]X 2. - Карбонилы иридия: желто-зеленый Ir 2(CO)8, возгоняется, и яркожелтый Ir 4(CO)12, при нагревании разлагается. Используются для нанесения покрытий.
 -Высшая степень окисления +6 проявляется у иридия в гексафториде Ir. F 6. Это очень сильный окислитель, способный окислить даже воду: 2 Ir. F 6 + 10 H 2 O = 2 Ir(OH)4 + 12 HF + O 2, или NO: NO + Ir. F 6 = NO+[Ir. F 6]–. - Как и для других d-элементов, для иридия характерно образование комплексных соединений с координационным числом 6. - Известно большое число иридийорганических соединений со связью Ir—C.
-Высшая степень окисления +6 проявляется у иридия в гексафториде Ir. F 6. Это очень сильный окислитель, способный окислить даже воду: 2 Ir. F 6 + 10 H 2 O = 2 Ir(OH)4 + 12 HF + O 2, или NO: NO + Ir. F 6 = NO+[Ir. F 6]–. - Как и для других d-элементов, для иридия характерно образование комплексных соединений с координационным числом 6. - Известно большое число иридийорганических соединений со связью Ir—C.

 Соединения двухвалентного иридия. Хлорид иридия (II) Ir. Cl 2 темно-зелен. Кристаллы, Брутто-формула (система Хилла): Cl 3 Ir , Молекулярная масса (в а. е. м. ): 298, 58, Температура разложения (в °C): 765, Растворимость (в г/100 г или характеристика): вода: не растворим Плотность: 5, 3 (20°C, г/см 3) Стандартная энтальпия образования ΔH (298 К, к. Дж/моль): -242, 7 (т) Стандартная энергия Гиббса образования ΔG (298 К, к. Дж/моль): -198, 7 (т) Дополнительная информация: Не растворим в кислотах, щелочах. Получают: Нагреванием металлического иридия или Ir. Cl 3 в токе хлора при 763 °C. Сульфид иридия (II) Ir. S — блестящее тёмно-синее твёрдое вещество. Мало растворим в воде и кислотах. Растворяется в сульфиде калия. Получают: Нагреванием металлического иридия в парах серы.
Соединения двухвалентного иридия. Хлорид иридия (II) Ir. Cl 2 темно-зелен. Кристаллы, Брутто-формула (система Хилла): Cl 3 Ir , Молекулярная масса (в а. е. м. ): 298, 58, Температура разложения (в °C): 765, Растворимость (в г/100 г или характеристика): вода: не растворим Плотность: 5, 3 (20°C, г/см 3) Стандартная энтальпия образования ΔH (298 К, к. Дж/моль): -242, 7 (т) Стандартная энергия Гиббса образования ΔG (298 К, к. Дж/моль): -198, 7 (т) Дополнительная информация: Не растворим в кислотах, щелочах. Получают: Нагреванием металлического иридия или Ir. Cl 3 в токе хлора при 763 °C. Сульфид иридия (II) Ir. S — блестящее тёмно-синее твёрдое вещество. Мало растворим в воде и кислотах. Растворяется в сульфиде калия. Получают: Нагреванием металлического иридия в парах серы.
 Соединения трехвалентного иридия. Оксид иридия (III) Ir 2 O 3 Твердое темно-синее вещество. Мало растворим в воде и спирте. Растворяется в серной кислоте. Получают: при легком прокаливании сульфида иридия (III). Хлорид иридия (III) Ir. Cl 3 Летучее соединение оливково-зеленого цвета. Плотность равна 5, 30 г/см 3 [2]. Мало растворим в воде, щелочах и кислотах. При 765 о. С разлагается на Ir. Cl 2 и хлор, при 773 о. С на Ir. Cl и хлор, а выше 798 о. С - на составные элементы. Получают: действием хлора на нагретый до 600 о. С иридий. Бромид иридия (III) Ir. Br 3 Оливково-зеленые кристаллы. Растворяется в воде, мало растворим в спирте. Дегидратируется при нагревании до 105 -120°С. При сильном нагревании разлагается на элементы. Получают: взаимодействием Ir. O 2 с бромоводородной кислотой. Сульфид иридия (III) Ir 2 S 3 Твердое коричневое вещество. Разлагается на элементы при нагревании выше 1050 о. С. Мало растворим в воде. Растворяется в азотной кислоте и растворе сульфида калия. Получают: действием сероводорода на хлорид иридия (III) или нагреванием порошкообразного металлического иридия с серой при температуре не выше 1050 о. С в вакууме.
Соединения трехвалентного иридия. Оксид иридия (III) Ir 2 O 3 Твердое темно-синее вещество. Мало растворим в воде и спирте. Растворяется в серной кислоте. Получают: при легком прокаливании сульфида иридия (III). Хлорид иридия (III) Ir. Cl 3 Летучее соединение оливково-зеленого цвета. Плотность равна 5, 30 г/см 3 [2]. Мало растворим в воде, щелочах и кислотах. При 765 о. С разлагается на Ir. Cl 2 и хлор, при 773 о. С на Ir. Cl и хлор, а выше 798 о. С - на составные элементы. Получают: действием хлора на нагретый до 600 о. С иридий. Бромид иридия (III) Ir. Br 3 Оливково-зеленые кристаллы. Растворяется в воде, мало растворим в спирте. Дегидратируется при нагревании до 105 -120°С. При сильном нагревании разлагается на элементы. Получают: взаимодействием Ir. O 2 с бромоводородной кислотой. Сульфид иридия (III) Ir 2 S 3 Твердое коричневое вещество. Разлагается на элементы при нагревании выше 1050 о. С. Мало растворим в воде. Растворяется в азотной кислоте и растворе сульфида калия. Получают: действием сероводорода на хлорид иридия (III) или нагреванием порошкообразного металлического иридия с серой при температуре не выше 1050 о. С в вакууме.
 Соединения четырехвалентного иридия. Оксид иридия (IV) Ir. O 2 Черные тетрагональные кристаллы с решеткой типа рутила. Плотность равна 3, 15 г/см 3. Мало растворим в воде, спирте и кислотах. Восстанавливается до металла водородом. Термически диссоциирует на элементы при нагревании. Получают: нагреванием порошкообразного иридия на воздухе или в кислороде при 700°С, нагреванием Ir. О 2. n. Н 2 О. Фторид иридия (IV) Ir. F 4 Желтая маслянистая жидкость, которая разлагается на воздухе и гидролизуется водой. tпл=106 о. С. Получают: нагреванием Ir. F 6 с порошком иридия при 150°С. Хлорид иридия (IV) Ir. Cl 4 Гигроскопичное коричневое твердое вещество. Растворяется в холодной воде и разлагается теплой. Получают: нагреванием (600 -700 о. С) металлического иридия с хлором при повышенном давлении. Бромид иридия (IV) Ir. Br 4 Расплывающееся на воздухе синее вещество. Растворяется в спирте. Растворяется в воде с разложением и диссоциирует при нагревании на элементы. Получают: взаимодействием Ir. O 2 с бромоводородной кислотой при низкой температуре. Сульфид иридия (IV) Ir. S 2 Твердое коричневое вещество. Мало растворим в воде. Получают: пропусканием сероводорода через растворы солей иридия (IV) или нагреванием порошкообразного металлического иридия с серой без доступа воздуха в вакууме.
Соединения четырехвалентного иридия. Оксид иридия (IV) Ir. O 2 Черные тетрагональные кристаллы с решеткой типа рутила. Плотность равна 3, 15 г/см 3. Мало растворим в воде, спирте и кислотах. Восстанавливается до металла водородом. Термически диссоциирует на элементы при нагревании. Получают: нагреванием порошкообразного иридия на воздухе или в кислороде при 700°С, нагреванием Ir. О 2. n. Н 2 О. Фторид иридия (IV) Ir. F 4 Желтая маслянистая жидкость, которая разлагается на воздухе и гидролизуется водой. tпл=106 о. С. Получают: нагреванием Ir. F 6 с порошком иридия при 150°С. Хлорид иридия (IV) Ir. Cl 4 Гигроскопичное коричневое твердое вещество. Растворяется в холодной воде и разлагается теплой. Получают: нагреванием (600 -700 о. С) металлического иридия с хлором при повышенном давлении. Бромид иридия (IV) Ir. Br 4 Расплывающееся на воздухе синее вещество. Растворяется в спирте. Растворяется в воде с разложением и диссоциирует при нагревании на элементы. Получают: взаимодействием Ir. O 2 с бромоводородной кислотой при низкой температуре. Сульфид иридия (IV) Ir. S 2 Твердое коричневое вещество. Мало растворим в воде. Получают: пропусканием сероводорода через растворы солей иридия (IV) или нагреванием порошкообразного металлического иридия с серой без доступа воздуха в вакууме.
 Соединения шестивалентного иридия. Фторид иридия (VI) Ir. F 6 Желтые тетрагональные кристаллы. tпл=44 о. С, tкип=53 о. С, плотность равна 6, 0 г/см 3 [2]. Под действием металлического иридия превращается в Ir. F 4, восстанавливается водородом до металлического иридия. Разъедает влажное стекло. Получают: нагреванием иридия в атмосфере фтора в трубке из флюорита. Сульфид иридия (VI) Ir. S 3 Серый, мало растворимый в воде порошок. Получают: нагреванием порошкообразного металлического иридия с избытком серы в вакууме.
Соединения шестивалентного иридия. Фторид иридия (VI) Ir. F 6 Желтые тетрагональные кристаллы. tпл=44 о. С, tкип=53 о. С, плотность равна 6, 0 г/см 3 [2]. Под действием металлического иридия превращается в Ir. F 4, восстанавливается водородом до металлического иридия. Разъедает влажное стекло. Получают: нагреванием иридия в атмосфере фтора в трубке из флюорита. Сульфид иридия (VI) Ir. S 3 Серый, мало растворимый в воде порошок. Получают: нагреванием порошкообразного металлического иридия с избытком серы в вакууме.
 Применение Особый интерес в качестве источника электроэнергии вызывает его ядерный изомер иридий-192 m 2 (имеющий период полураспада 241 год). Сплавы с W и Th — материалы термоэлектрических генераторов, с Hf — материалы для топливных баков в космических аппаратах, с Rh, Re, W — материалы для термопар, эксплуатируемых выше 2000 °C, с La и Се — материалы термоэмиссионных катодов. Иридий используется также для изготовления перьев для ручек. Небольшой шарик из иридия можно встретить на кончиках перьев и чернильных стержней, особенно хорошо его видно на золотых перьях, где он отличается по цвету от самого пера. Иридий в палеонтологии и геологии является индикатором слоя, который сформировался сразу после падения метеоритов. Иридий, наряду с медью и платиной, применяется в свечах зажигания двигателей внутреннего сгорания (ДВС) в качестве материала для изготовления электродов, делая такие свечи наиболее долговечными (100— 160 тыс. км пробега автомобиля) и снижая требования к напряжению искрообразования. Изначально использовался в авиации и гоночных автомобилях, затем, по мере снижения стоимости продукции, стал употребляться и на массовых автомобилях. В настоящее время такие свечи доступны для большинства двигателей, однако являясь наиболее дорогими.
Применение Особый интерес в качестве источника электроэнергии вызывает его ядерный изомер иридий-192 m 2 (имеющий период полураспада 241 год). Сплавы с W и Th — материалы термоэлектрических генераторов, с Hf — материалы для топливных баков в космических аппаратах, с Rh, Re, W — материалы для термопар, эксплуатируемых выше 2000 °C, с La и Се — материалы термоэмиссионных катодов. Иридий используется также для изготовления перьев для ручек. Небольшой шарик из иридия можно встретить на кончиках перьев и чернильных стержней, особенно хорошо его видно на золотых перьях, где он отличается по цвету от самого пера. Иридий в палеонтологии и геологии является индикатором слоя, который сформировался сразу после падения метеоритов. Иридий, наряду с медью и платиной, применяется в свечах зажигания двигателей внутреннего сгорания (ДВС) в качестве материала для изготовления электродов, делая такие свечи наиболее долговечными (100— 160 тыс. км пробега автомобиля) и снижая требования к напряжению искрообразования. Изначально использовался в авиации и гоночных автомобилях, затем, по мере снижения стоимости продукции, стал употребляться и на массовых автомобилях. В настоящее время такие свечи доступны для большинства двигателей, однако являясь наиболее дорогими.
 Биологическая роль Не играет никакой биологической роли. Металлический иридий нетоксичен, но некоторые соединения иридия, например, его гексафторид (Ir. F 6), очень ядовиты.
Биологическая роль Не играет никакой биологической роли. Металлический иридий нетоксичен, но некоторые соединения иридия, например, его гексафторид (Ir. F 6), очень ядовиты.




