М.В_.Проценко_.ppt
- Количество слайдов: 46
 Оригинальные и воспроизведенные лекарственные средства Проценко Марина Валерьевна ГБОУ ВПО Первый МГМУ им. И. М. Сеченова Кафедра организации лекарственного обеспечения и фармакоэкономики Научный сотрудник НИИФ
Оригинальные и воспроизведенные лекарственные средства Проценко Марина Валерьевна ГБОУ ВПО Первый МГМУ им. И. М. Сеченова Кафедра организации лекарственного обеспечения и фармакоэкономики Научный сотрудник НИИФ
 Сегодня Большая часть лекарственных средств (ЛС) на современном фармрынке являются воспроизведенными (генерическими) препаратами Доля генериков в настоящее время составляет порядка 30%, при этом согласно прогнозам эта доля будет неуклонно расти (рис. 1) По объему генерического сектора стран БРИК Россия занимает 3 место в после Китая и Бразилии Структура рынка стран большой семерки по состоянию на 2010 г. формируется следующим образом: в США – 13, 4% дженериков, в Японии - 5%, в Германии – 16, 2%, во Франции – 15, 3%, в Англии – 21, 3%, в Италии - 60%, в Канаде – 24, 2% (рис 2) Данные IMS Health
Сегодня Большая часть лекарственных средств (ЛС) на современном фармрынке являются воспроизведенными (генерическими) препаратами Доля генериков в настоящее время составляет порядка 30%, при этом согласно прогнозам эта доля будет неуклонно расти (рис. 1) По объему генерического сектора стран БРИК Россия занимает 3 место в после Китая и Бразилии Структура рынка стран большой семерки по состоянию на 2010 г. формируется следующим образом: в США – 13, 4% дженериков, в Японии - 5%, в Германии – 16, 2%, во Франции – 15, 3%, в Англии – 21, 3%, в Италии - 60%, в Канаде – 24, 2% (рис 2) Данные IMS Health
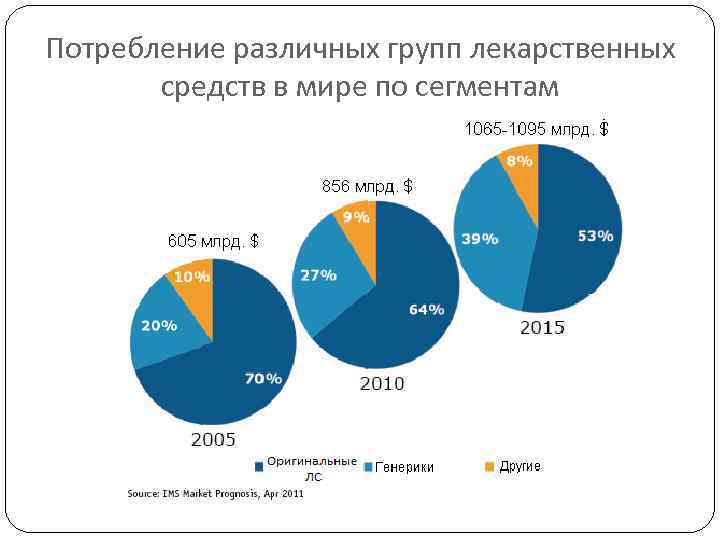 Потребление различных групп лекарственных средств в мире по сегментам
Потребление различных групп лекарственных средств в мире по сегментам
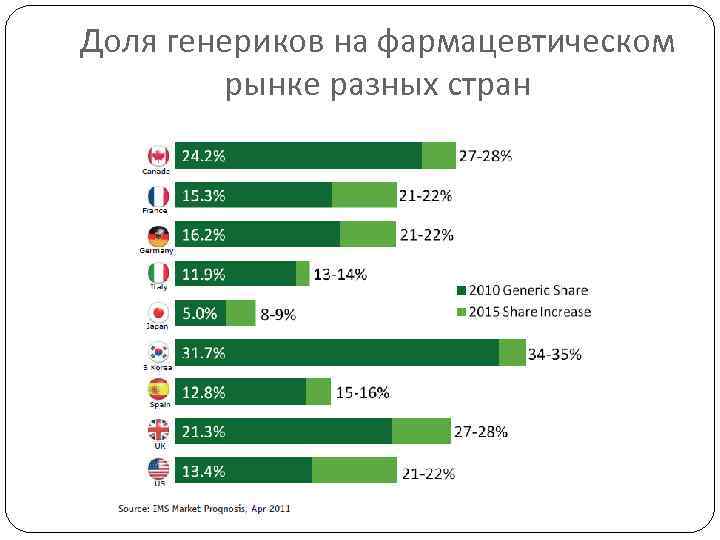 Доля генериков на фармацевтическом рынке разных стран
Доля генериков на фармацевтическом рынке разных стран
 Рынок генерических препаратов растет Генерики дешевле Предполагается, что в терапевтическом отношении они эквивалентны оригинальному препарату Качество препаратов беспокоит всех: – пациентов – фармацевтов и врачей – фармацевтические компании – правительства – фармакопею
Рынок генерических препаратов растет Генерики дешевле Предполагается, что в терапевтическом отношении они эквивалентны оригинальному препарату Качество препаратов беспокоит всех: – пациентов – фармацевтов и врачей – фармацевтические компании – правительства – фармакопею
 Согласно ФЗ № 61, при оценке генериков в Российской Федерации каждый зарегистрированный и допущенный к реализации генерический препарат должен соответствовать оригинальному препарату по следующим показателям: -обладать фармацевтической (химической) эквивалентностью; - обладать биоэквивалентностью. Фармацевтическая эквивалентность - это эквивалентность воспроизведенного ЛС по качественному и количественному составу оригинальному ЛС, а именно: - по составу активных веществ; - по силе действия или концентрации активных веществ; - по идентичности лекарственных форм; - по способу введения. Однако фармацевтический эквивалент может отличаться от оригинала по таким характеристикам как: пространственная конфигурация, механизму выведения, по составу вспомогательных веществ (красители, ароматизаторы, консерванты), сроку хранения. В связи с этим фармацевтический эквивалент подвергается анализу фармакокинетической эквивалентности (биоэквивалентности) оригинальному ЛС.
Согласно ФЗ № 61, при оценке генериков в Российской Федерации каждый зарегистрированный и допущенный к реализации генерический препарат должен соответствовать оригинальному препарату по следующим показателям: -обладать фармацевтической (химической) эквивалентностью; - обладать биоэквивалентностью. Фармацевтическая эквивалентность - это эквивалентность воспроизведенного ЛС по качественному и количественному составу оригинальному ЛС, а именно: - по составу активных веществ; - по силе действия или концентрации активных веществ; - по идентичности лекарственных форм; - по способу введения. Однако фармацевтический эквивалент может отличаться от оригинала по таким характеристикам как: пространственная конфигурация, механизму выведения, по составу вспомогательных веществ (красители, ароматизаторы, консерванты), сроку хранения. В связи с этим фармацевтический эквивалент подвергается анализу фармакокинетической эквивалентности (биоэквивалентности) оригинальному ЛС.
 Хорошо известен пример контрольной проверки биоэквивалентности дженериков оригинальному кларитромицину. Работа C. N. Nightingale была представлена в 2000 г. на 5–й Конференции по макролидам, азалидам, стрептограминам, кетолидам и оксазолидинонам в Севилье . Автор сравнил оригинальный препарат кларитромицина с 40 копиями в отношении биоэквивалентности, применив стандарты Американской фармакопеи. Исследование показало, что 70% дженериков растворяются значительно медленнее оригинального препарата, что критично для их усвоения. 80% дженериков отличаются от оригинала по количеству действующего начала в одной единице продукта. Количество примесей, не имеющих отношения к действующему началу, в большинстве образцов больше, чем в оригинале. В «лучшем» дженерике их было 2%, в «худшем» – 32%.
Хорошо известен пример контрольной проверки биоэквивалентности дженериков оригинальному кларитромицину. Работа C. N. Nightingale была представлена в 2000 г. на 5–й Конференции по макролидам, азалидам, стрептограминам, кетолидам и оксазолидинонам в Севилье . Автор сравнил оригинальный препарат кларитромицина с 40 копиями в отношении биоэквивалентности, применив стандарты Американской фармакопеи. Исследование показало, что 70% дженериков растворяются значительно медленнее оригинального препарата, что критично для их усвоения. 80% дженериков отличаются от оригинала по количеству действующего начала в одной единице продукта. Количество примесей, не имеющих отношения к действующему началу, в большинстве образцов больше, чем в оригинале. В «лучшем» дженерике их было 2%, в «худшем» – 32%.
 В России ежегодно регистрируется больше дженериков, чем оригинальных ЛС Отдельные оригинальные препараты имеют значительное количество воспроизведенных ЛС Оригинальное лекарственное средство Вольтарен (действующее вещество – диклофенак натрия) сегодня имеет 155 дженериков, зарегистрированных к медицинскому применению. Также в РФ зарегистрировано около 150 генерических ЛС эналаприла Около 100 - нифедипина, атенолола, ципрофлоксацина и порядка 50 – нитроглицерина, аспирина и парацетамола (причем количество комбинированных генерических последних двух ЛС превышает 300) В ряде стран с развитой системой контроля качества, эффективности и безопасности ЛС, число дженериков инновационного препарата в большинстве случаев не превышает 4 -5* * Laroche M. , Merle L. Generic and brand-name drugs. Are different criteria sufficiently taken into account before granting market authorisation? // Acta Clin Belg Suppl. – 2006. – № 1: – pp. 48 -50
В России ежегодно регистрируется больше дженериков, чем оригинальных ЛС Отдельные оригинальные препараты имеют значительное количество воспроизведенных ЛС Оригинальное лекарственное средство Вольтарен (действующее вещество – диклофенак натрия) сегодня имеет 155 дженериков, зарегистрированных к медицинскому применению. Также в РФ зарегистрировано около 150 генерических ЛС эналаприла Около 100 - нифедипина, атенолола, ципрофлоксацина и порядка 50 – нитроглицерина, аспирина и парацетамола (причем количество комбинированных генерических последних двух ЛС превышает 300) В ряде стран с развитой системой контроля качества, эффективности и безопасности ЛС, число дженериков инновационного препарата в большинстве случаев не превышает 4 -5* * Laroche M. , Merle L. Generic and brand-name drugs. Are different criteria sufficiently taken into account before granting market authorisation? // Acta Clin Belg Suppl. – 2006. – № 1: – pp. 48 -50
 Особенности генерических ЛС в России • Появление многих дженериков в России раньше соответствующих оригинальных ЛС; • Отсутствие данных о терапевтической эквивалентности с оригинальным ЛС; • Относительно высокие цены дженериков; • Самая высокая доля дженериков на фармацевтическом рынке
Особенности генерических ЛС в России • Появление многих дженериков в России раньше соответствующих оригинальных ЛС; • Отсутствие данных о терапевтической эквивалентности с оригинальным ЛС; • Относительно высокие цены дженериков; • Самая высокая доля дженериков на фармацевтическом рынке
 Термины и определения *Оригинальное лекарственное средство - лекарственное средство (ЛС), содержащее впервые полученную фармацевтическую субстанцию или новую комбинацию фармацевтических субстанций, эффективность и безопасность которых подтверждены результатами доклинических исследований лекарственных средств и клинических исследований лекарственных препаратов *ФЗ № 61 от 12 апреля 2010 г. «Об обращении лекарственных средств» *Внесено в государственный реестр ЛС
Термины и определения *Оригинальное лекарственное средство - лекарственное средство (ЛС), содержащее впервые полученную фармацевтическую субстанцию или новую комбинацию фармацевтических субстанций, эффективность и безопасность которых подтверждены результатами доклинических исследований лекарственных средств и клинических исследований лекарственных препаратов *ФЗ № 61 от 12 апреля 2010 г. «Об обращении лекарственных средств» *Внесено в государственный реестр ЛС
 Термины и определения *Воспроизведенное лекарственное средство - это лекарственное средство, содержащее то же действующее вещество или комбинацию действующих веществ в той же лекарственной форме, что и оригинальное лекарственное средство, и поступившее в обращение после оригинального лекарственного средства *ФЗ № 61 от 12 апреля 2010 г. «Об обращении лекарственных средств» *Внесено в государственный реестр ЛС
Термины и определения *Воспроизведенное лекарственное средство - это лекарственное средство, содержащее то же действующее вещество или комбинацию действующих веществ в той же лекарственной форме, что и оригинальное лекарственное средство, и поступившее в обращение после оригинального лекарственного средства *ФЗ № 61 от 12 апреля 2010 г. «Об обращении лекарственных средств» *Внесено в государственный реестр ЛС
 Термины и определения Воспроизведенные ЛС имеют ряд равнозначных общеупотребляемых синонимов – «генерики» , «дженерики» , «генерические лекарственные средства» , «многоисточниковые (мультиисточниковые) лекарственные средства» [1, 2], однако согласно Федеральному закону № 61 -ФЗ именно термин «воспроизведенные лекарственные средства» должен применяться в первую очередь. В то же время Всемирная организация здравоохранения в качестве основного понятия таких ЛС рекомендует употреблять термин «многоисточниковые лекарственные средства» (multisource drugs) [3]. 1 Талибов О. Б. Генерики и эквивалентность лекарственных препаратов. // Медицинская газета «Здоровье Украины» . – Киев, 2008. – № 5. – С. 12 -16. 2. Тарловская Е. И. Генерики и оригинальные препараты: взгляд практического врача. // Российский Медицинский Журнал. – М. , 2008, – т. 16. – № 5. – С. 30 – 35. 3. Multisource (Generic) Pharmaceutical Products: Guidelines on Registration Requirements to Establish Interchangeability. — WHO Technical Report Series, № 937. – WHO, 2006.
Термины и определения Воспроизведенные ЛС имеют ряд равнозначных общеупотребляемых синонимов – «генерики» , «дженерики» , «генерические лекарственные средства» , «многоисточниковые (мультиисточниковые) лекарственные средства» [1, 2], однако согласно Федеральному закону № 61 -ФЗ именно термин «воспроизведенные лекарственные средства» должен применяться в первую очередь. В то же время Всемирная организация здравоохранения в качестве основного понятия таких ЛС рекомендует употреблять термин «многоисточниковые лекарственные средства» (multisource drugs) [3]. 1 Талибов О. Б. Генерики и эквивалентность лекарственных препаратов. // Медицинская газета «Здоровье Украины» . – Киев, 2008. – № 5. – С. 12 -16. 2. Тарловская Е. И. Генерики и оригинальные препараты: взгляд практического врача. // Российский Медицинский Журнал. – М. , 2008, – т. 16. – № 5. – С. 30 – 35. 3. Multisource (Generic) Pharmaceutical Products: Guidelines on Registration Requirements to Establish Interchangeability. — WHO Technical Report Series, № 937. – WHO, 2006.
 Термины и определения *В новом ФЗ № 61 нет определения «биотехнологического ЛС» , «биоаналога» , однако присутствует определение иммунобиологических лекарственных препаратов. Это - лекарственные препараты биологического происхождения, предназначенные для иммунологических диагностики, профилактики и лечения заболеваний * ФЗ № 61 от 12 апреля 2010 г. «Об обращении лекарственных средств» * Внесено в государственный реестр ЛС
Термины и определения *В новом ФЗ № 61 нет определения «биотехнологического ЛС» , «биоаналога» , однако присутствует определение иммунобиологических лекарственных препаратов. Это - лекарственные препараты биологического происхождения, предназначенные для иммунологических диагностики, профилактики и лечения заболеваний * ФЗ № 61 от 12 апреля 2010 г. «Об обращении лекарственных средств» * Внесено в государственный реестр ЛС
 Термины и определения. Биоподобное ЛС ØЕвропейский Союз Данная генерация лекарственных средств носит название «биоаналоги» или «биоподобные препараты» ( «biosimilars» ) ØСоединенных Штаты Америки «аналогичные белковые лекарства» , «биофармацевтические препараты» ( «follow-on protein products» )
Термины и определения. Биоподобное ЛС ØЕвропейский Союз Данная генерация лекарственных средств носит название «биоаналоги» или «биоподобные препараты» ( «biosimilars» ) ØСоединенных Штаты Америки «аналогичные белковые лекарства» , «биофармацевтические препараты» ( «follow-on protein products» )
 Термины и определения Биотехнологическое лекарственное средство, по определению Европейского агентства по лекарственным средствам (EMEA - European Medicines Agency), – это лекарственные средства, произведенные путем биотехнологических процессов с применением: • технологии рекомбинантной ДНК; • методконтролируемой экспрессии генов, кодирующих выработку биологически активных белков; • метода гибрида и моноклональных антител, а также генотерапевтические и соматотерапевтические лекарственные средства. Биосимиляр – биотехнологическое ЛС, схожее с произведенным впервые (оригинальным) ЛС и представленное на регистрацию после истечения срока действия патента оригинального ЛС ( «similar biological medicinal product» ) согласно Директиве 2003/63/ЕС
Термины и определения Биотехнологическое лекарственное средство, по определению Европейского агентства по лекарственным средствам (EMEA - European Medicines Agency), – это лекарственные средства, произведенные путем биотехнологических процессов с применением: • технологии рекомбинантной ДНК; • методконтролируемой экспрессии генов, кодирующих выработку биологически активных белков; • метода гибрида и моноклональных антител, а также генотерапевтические и соматотерапевтические лекарственные средства. Биосимиляр – биотехнологическое ЛС, схожее с произведенным впервые (оригинальным) ЛС и представленное на регистрацию после истечения срока действия патента оригинального ЛС ( «similar biological medicinal product» ) согласно Директиве 2003/63/ЕС
 Патентная защита ЛС В настоящее время все ЛС патентуются Патентная защита направлена: - способа производства ЛС (биоаналога) - активной субстанции (дженерик химического ЛС) Патент выдается государственным органом исполнительной власти по интеллектуальной собственности, в Российской Федерации таким органом является Федеральная служба по интеллектуальной собственности, патентам и товарным знакам Роспатент. Патентная защита инновационного лекарственного средства действует в зависимости от патентного законодательства конкретной страны * *Патентный закон Российской Федерации (редакция на 07. 02. 2003), статья 3
Патентная защита ЛС В настоящее время все ЛС патентуются Патентная защита направлена: - способа производства ЛС (биоаналога) - активной субстанции (дженерик химического ЛС) Патент выдается государственным органом исполнительной власти по интеллектуальной собственности, в Российской Федерации таким органом является Федеральная служба по интеллектуальной собственности, патентам и товарным знакам Роспатент. Патентная защита инновационного лекарственного средства действует в зависимости от патентного законодательства конкретной страны * *Патентный закон Российской Федерации (редакция на 07. 02. 2003), статья 3
 Основные характеристики оригинального ЛС Длительность разработки (10 -15 лет) на основании отбора действующего вещества из значительного количества молекул Фармакологический эффект Токсичность Мутагенность Тератогенность Проверены в доклинических исследованиях на животных; прохождение всех фаз клинических исследований в соответствии со стандартами GСP
Основные характеристики оригинального ЛС Длительность разработки (10 -15 лет) на основании отбора действующего вещества из значительного количества молекул Фармакологический эффект Токсичность Мутагенность Тератогенность Проверены в доклинических исследованиях на животных; прохождение всех фаз клинических исследований в соответствии со стандартами GСP
 Причины различий оригинальных и воспроизведенных ЛС Фармацевтическая технология производства препарата Вспомогательные вещества (неактивные ингредиенты, наполнители, консерванты и др. ) Их природа и количество Полиморфизм Солевая форма Упаковка препарата Условия его хранения Транспортировка
Причины различий оригинальных и воспроизведенных ЛС Фармацевтическая технология производства препарата Вспомогательные вещества (неактивные ингредиенты, наполнители, консерванты и др. ) Их природа и количество Полиморфизм Солевая форма Упаковка препарата Условия его хранения Транспортировка
 Сравнение стоимости оригинальных и воспроизведенных препаратов 80% стоимости оригинального ЛС – стоимость исследований эффективности и безопасности препарата, 20% - стоимость его синтеза WHO Technical Report Series 937, annex 7 « Multisource (generic) pharmaceutical products: guidelines on registration requirements to establish interchangeability» . WHO Expert Committee on Specifications for Pharmaceutical Preparations. – WHO, 2006.
Сравнение стоимости оригинальных и воспроизведенных препаратов 80% стоимости оригинального ЛС – стоимость исследований эффективности и безопасности препарата, 20% - стоимость его синтеза WHO Technical Report Series 937, annex 7 « Multisource (generic) pharmaceutical products: guidelines on registration requirements to establish interchangeability» . WHO Expert Committee on Specifications for Pharmaceutical Preparations. – WHO, 2006.
 Качество исходных препаратов Стоимость сырья оригинального препарата составляет 10% себестоимости его производства* Стоимость сырья дженерика часто превышает 50% себестоимости производства, что может подтолкнуть производителей к поиску более дешевого и менее качественного сырья* *Videau J-Y. Воспроизведенные препараты: скрытые проблемы качества и стоимости // Журнал «Фарматека» . – 2001. – № 2. Зырянов С. К. Материалы V Конгресса «Развитие фармакоэкономики и фармакоэпидемиологии в РФ»
Качество исходных препаратов Стоимость сырья оригинального препарата составляет 10% себестоимости его производства* Стоимость сырья дженерика часто превышает 50% себестоимости производства, что может подтолкнуть производителей к поиску более дешевого и менее качественного сырья* *Videau J-Y. Воспроизведенные препараты: скрытые проблемы качества и стоимости // Журнал «Фарматека» . – 2001. – № 2. Зырянов С. К. Материалы V Конгресса «Развитие фармакоэкономики и фармакоэпидемиологии в РФ»
 Метод синтеза субстанции является важным фактором, обеспечивающим качество препарата. Изменение метода синтеза приводит к получению продукта, обладающими отличными от оригинального препарата свойствами чаще всего за счет высокого содержания продуктов деградации и технологических примесей* *Videau J-Y. Воспроизведенные препараты: скрытые проблемы качества и стоимости // Журнал «Фарматека» . – 2001. – № 2. Зырянов С. К. Материалы V Конгресса «Развитие фармакоэкономики и фармакоэпидемиологии в РФ»
Метод синтеза субстанции является важным фактором, обеспечивающим качество препарата. Изменение метода синтеза приводит к получению продукта, обладающими отличными от оригинального препарата свойствами чаще всего за счет высокого содержания продуктов деградации и технологических примесей* *Videau J-Y. Воспроизведенные препараты: скрытые проблемы качества и стоимости // Журнал «Фарматека» . – 2001. – № 2. Зырянов С. К. Материалы V Конгресса «Развитие фармакоэкономики и фармакоэпидемиологии в РФ»
 Производство биотехнологических препаратов-это комплексный процесс, каждый шаг которого уникален Другой протокол очистки вектор ДНК (Вероятно) Другой вектор ДНК Клонирован ие в вектор ДНК Перенос в клетку хозяина. Экспрессия Одинаковый ААвозможно, одинаковая генетическая последовательность Другой процесс ферментации Разработка Другая система рекомбинантных клеток например, клеточная культура бактерий или млекопитающих Процесс промышленной ферментации Технология изготовления Другой процесс контроля Вероятно другая технология изготовления
Производство биотехнологических препаратов-это комплексный процесс, каждый шаг которого уникален Другой протокол очистки вектор ДНК (Вероятно) Другой вектор ДНК Клонирован ие в вектор ДНК Перенос в клетку хозяина. Экспрессия Одинаковый ААвозможно, одинаковая генетическая последовательность Другой процесс ферментации Разработка Другая система рекомбинантных клеток например, клеточная культура бактерий или млекопитающих Процесс промышленной ферментации Технология изготовления Другой процесс контроля Вероятно другая технология изготовления
 Вспомогательные вещества • Вспомогательные вещества часто составляют основную часть прописи готового продукта (8090%)* • Любое изменение в составе вспомогательных веществ может неблагоприятно повлиять на биодоступность и вызвать токсические явления или аллергию* *Videau J-Y. Воспроизведенные препараты: скрытые проблемы качества и стоимости // Журнал «Фарматека» . – 2001. – № 2. Зырянов С. К. Материалы V Конгресса «Развитие фармакоэкономики и фармакоэпидемиологии в РФ»
Вспомогательные вещества • Вспомогательные вещества часто составляют основную часть прописи готового продукта (8090%)* • Любое изменение в составе вспомогательных веществ может неблагоприятно повлиять на биодоступность и вызвать токсические явления или аллергию* *Videau J-Y. Воспроизведенные препараты: скрытые проблемы качества и стоимости // Журнал «Фарматека» . – 2001. – № 2. Зырянов С. К. Материалы V Конгресса «Развитие фармакоэкономики и фармакоэпидемиологии в РФ»
 Антидепрессанты. Оригинальный и генерический циталопрам МНН Циталопрам Лекарственная форма таблетки покрытые пленочной оболочкой Химическое название 1 - [3 - (диметиламино) пропил] - 1 - (n - фторфенил) - 5 – фталанкарбонитрил 1 - [3 - (диметиламино) пропил] - 1 - (n - фторфенил) - 5 - фталанкарбонитрил СОСТАВ: активное вещество - циталопрама гидробромид; СОСТАВ: вспомогательные вещества: крахмал кукурузный, лактозы моногидрат, коповидон, глицерин 85%, микрокристаллическая целлюлоза, натрия кроскармелоза, магния стеарат. Таблетки, покрытые оболочкой 1 табл. циталопрама гидробромид (эквивалентно циталопраму основанию) 20 мг 40 мг вспомогательные вещества: маннитол; МКЦ; кремния оксид коллоидный безводный; магния стеарат; гипромеллоза; титана диоксид; макрогол 6000
Антидепрессанты. Оригинальный и генерический циталопрам МНН Циталопрам Лекарственная форма таблетки покрытые пленочной оболочкой Химическое название 1 - [3 - (диметиламино) пропил] - 1 - (n - фторфенил) - 5 – фталанкарбонитрил 1 - [3 - (диметиламино) пропил] - 1 - (n - фторфенил) - 5 - фталанкарбонитрил СОСТАВ: активное вещество - циталопрама гидробромид; СОСТАВ: вспомогательные вещества: крахмал кукурузный, лактозы моногидрат, коповидон, глицерин 85%, микрокристаллическая целлюлоза, натрия кроскармелоза, магния стеарат. Таблетки, покрытые оболочкой 1 табл. циталопрама гидробромид (эквивалентно циталопраму основанию) 20 мг 40 мг вспомогательные вещества: маннитол; МКЦ; кремния оксид коллоидный безводный; магния стеарат; гипромеллоза; титана диоксид; макрогол 6000
 Упаковочные материалы/контейнеры Первичная упаковка (блистеры, стрипы, флаконы) находится в прямом контакте с фармацевтическим продуктом. Адсорбция упаковочных материалов может изменить стабильность продукции. Изменения состава лекарственного продукта в результате прилипания к стенкам контейнера может также изменить стабильность, что может вызвать плохую переносимость или токсические явления* *Videau J-Y. Воспроизведенные препараты: скрытые проблемы качества и стоимости // Журнал «Фарматека» . – 2001. – № 2. Зырянов С. К. Материалы V Конгресса «Развитие фармакоэкономики и фармакоэпидемиологии в РФ»
Упаковочные материалы/контейнеры Первичная упаковка (блистеры, стрипы, флаконы) находится в прямом контакте с фармацевтическим продуктом. Адсорбция упаковочных материалов может изменить стабильность продукции. Изменения состава лекарственного продукта в результате прилипания к стенкам контейнера может также изменить стабильность, что может вызвать плохую переносимость или токсические явления* *Videau J-Y. Воспроизведенные препараты: скрытые проблемы качества и стоимости // Журнал «Фарматека» . – 2001. – № 2. Зырянов С. К. Материалы V Конгресса «Развитие фармакоэкономики и фармакоэпидемиологии в РФ»
 Параметры оценки эквивалентности дженериков Фармацевтическая эквивалентность Препараты должны быть: • в одинаковой лекарственной форме и содержать одинаковые активные ингредиенты; • предназначены для одного способа введения; • идентичными по силе воздействия или концентрации активных веществ Биологическая (фармакокинетическая) эквивалентность По результатам исследований, основные параметры дженерика и оригинального средства идентичны или отличаются не более чем на 15– 20% по следующим параметрам: • степень и скорость всасывания лекарства; • время достижения и уровень максимальной концентрации в крови; • характер распределения в тканях и жидкостях организма; • тип и скорость экскреции Терапевтическая эквивалентность дженериков Препарат-дженерик по сравнению с оригиналом (по результатам клинических исследований) должен: • содержать ту же активную субстанцию; • обладать такой же эффективностью; • быть таким же безопасным
Параметры оценки эквивалентности дженериков Фармацевтическая эквивалентность Препараты должны быть: • в одинаковой лекарственной форме и содержать одинаковые активные ингредиенты; • предназначены для одного способа введения; • идентичными по силе воздействия или концентрации активных веществ Биологическая (фармакокинетическая) эквивалентность По результатам исследований, основные параметры дженерика и оригинального средства идентичны или отличаются не более чем на 15– 20% по следующим параметрам: • степень и скорость всасывания лекарства; • время достижения и уровень максимальной концентрации в крови; • характер распределения в тканях и жидкостях организма; • тип и скорость экскреции Терапевтическая эквивалентность дженериков Препарат-дженерик по сравнению с оригиналом (по результатам клинических исследований) должен: • содержать ту же активную субстанцию; • обладать такой же эффективностью; • быть таким же безопасным
 Фармацевтическая эквивалентность ЛС считаются фармацевтически эквивалентными, если они содержат одни и те же действующие вещества в одинаковом количестве и в одинаковой лекарственной форме и отвечают требованиям одних и тех же или сходных стандартов. То есть фармацевтическая эквивалентность – это полное соответствие состава и лекарственной формы препаратов.
Фармацевтическая эквивалентность ЛС считаются фармацевтически эквивалентными, если они содержат одни и те же действующие вещества в одинаковом количестве и в одинаковой лекарственной форме и отвечают требованиям одних и тех же или сходных стандартов. То есть фармацевтическая эквивалентность – это полное соответствие состава и лекарственной формы препаратов.
 Оценка биоэквивалентности ЛС является основным видом медико-биологического контроля воспроизведенных (генерических) ЛС, не отличающихся лекарственной формой и содержанием действующих веществ от соответствующих оригинальных ЛС. Биоэквивалентность ЛС обозначает их одинаковую биодоступность. Под биодоступностью понимают количество неизмененного действующего вещества, достигающего системного кровотока (степень всасывания) относительно исходной дозы ЛС. Исследования биоэквивалентности позволяют сделать обоснованные заключения о качестве сравниваемых препаратов по относительно меньшему объему первичной информации и в более сжатые сроки, чем при проведении клинических исследований
Оценка биоэквивалентности ЛС является основным видом медико-биологического контроля воспроизведенных (генерических) ЛС, не отличающихся лекарственной формой и содержанием действующих веществ от соответствующих оригинальных ЛС. Биоэквивалентность ЛС обозначает их одинаковую биодоступность. Под биодоступностью понимают количество неизмененного действующего вещества, достигающего системного кровотока (степень всасывания) относительно исходной дозы ЛС. Исследования биоэквивалентности позволяют сделать обоснованные заключения о качестве сравниваемых препаратов по относительно меньшему объему первичной информации и в более сжатые сроки, чем при проведении клинических исследований
 Терапевтическая эквивалентность Терапевтически эквивалентными лекарственные препараты могут считаться только в том случае, если они фармацевтически эквивалентны и можно ожидать, что они будут иметь одинаковый клинический эффект и одинаковый профиль безопасности при использовании пациентами в соответствии с указаниями инструкции по применению. Терапевтическая эквивалентность означает, что два препарата обеспечивают одинаковый терапевтический эффект и безопасность. Терапевтически эквивалентные лекарственные препараты должны отвечать следующим требованиям: иметь доказанную эффективность и безопасность; быть фармацевтически эквивалентными; быть биоэквивалентными; иметь сходные инструкции по применению; производиться в условиях стандарта GMP. Доказанную клиническую эффективность и безопасность устанавливают на основании клинических исследований.
Терапевтическая эквивалентность Терапевтически эквивалентными лекарственные препараты могут считаться только в том случае, если они фармацевтически эквивалентны и можно ожидать, что они будут иметь одинаковый клинический эффект и одинаковый профиль безопасности при использовании пациентами в соответствии с указаниями инструкции по применению. Терапевтическая эквивалентность означает, что два препарата обеспечивают одинаковый терапевтический эффект и безопасность. Терапевтически эквивалентные лекарственные препараты должны отвечать следующим требованиям: иметь доказанную эффективность и безопасность; быть фармацевтически эквивалентными; быть биоэквивалентными; иметь сходные инструкции по применению; производиться в условиях стандарта GMP. Доказанную клиническую эффективность и безопасность устанавливают на основании клинических исследований.
 Оранжевая книга FDA В 1984 году Управление по контролю за пищевыми продуктами и лекарственными препаратами США (FDA) впервые опубликовало перечень одобренных к применению препаратов с доказанной терапевтической эквивалентностью (Approved Drug Products with Therapeutic Equivalence and Evaluations) «Оранжевую книгу» (Orange-book). FDA признает терапевтически эквивалентными препараты только в том случае, если они удовлетворяют следующим критериям: 1. Разрешены к применению как эффективные и безопасные. 2. Являются фармацевтическими эквивалентами, то есть идентичны по качественному и количественному составу, а также идентичны по силе действия, дозировке и способах введения. 3. Являются биоэквивалентными 4. Имеют надлежащую маркировку. 5. Производятся в соответствии с требованиями GMP
Оранжевая книга FDA В 1984 году Управление по контролю за пищевыми продуктами и лекарственными препаратами США (FDA) впервые опубликовало перечень одобренных к применению препаратов с доказанной терапевтической эквивалентностью (Approved Drug Products with Therapeutic Equivalence and Evaluations) «Оранжевую книгу» (Orange-book). FDA признает терапевтически эквивалентными препараты только в том случае, если они удовлетворяют следующим критериям: 1. Разрешены к применению как эффективные и безопасные. 2. Являются фармацевтическими эквивалентами, то есть идентичны по качественному и количественному составу, а также идентичны по силе действия, дозировке и способах введения. 3. Являются биоэквивалентными 4. Имеют надлежащую маркировку. 5. Производятся в соответствии с требованиями GMP
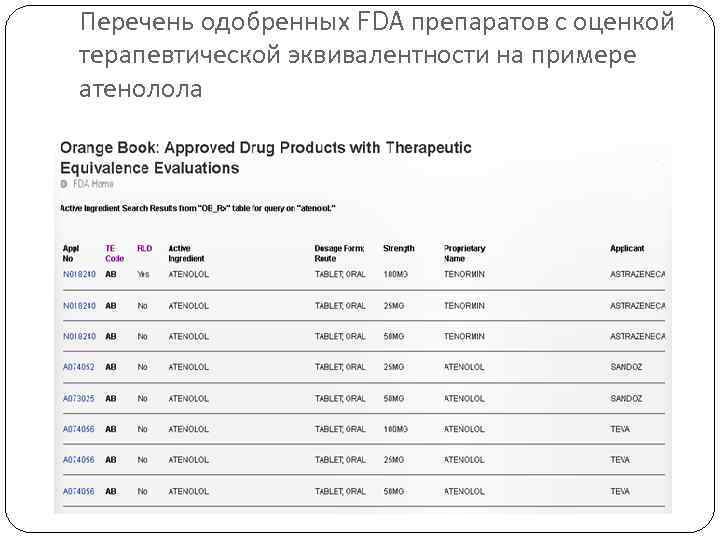 Перечень одобренных FDA препаратов с оценкой терапевтической эквивалентности на примере атенолола
Перечень одобренных FDA препаратов с оценкой терапевтической эквивалентности на примере атенолола
 Биотехнологические препараты Первый человеческий соматропин Эритропоэтин Рекомбинантный человеческий инсулин Рекомбинантный интерферон Моноклональные антитела ü 1977 - человеческий белок (соматропин), произведенный ü ü ü методом генной инженерии с использованием микроорганизмов (E. coli) 1978 - создан рекомбинантный человеческий инсулин 1982 – первый рекомбинантный человеческий инсулин стал первым биофармацевтическим препаратом, выпущенным на рынок 1981 - разработан рекомбинантный интерферон γ, противовирусный препарат 1985 -1986 - на рынок выведен рекомбинантный интерферон α 1989 - на фармацевтическом рынке появился первый препарат ЭПО (эритропоэтин) 2000 -е годы – моноклональные антитела
Биотехнологические препараты Первый человеческий соматропин Эритропоэтин Рекомбинантный человеческий инсулин Рекомбинантный интерферон Моноклональные антитела ü 1977 - человеческий белок (соматропин), произведенный ü ü ü методом генной инженерии с использованием микроорганизмов (E. coli) 1978 - создан рекомбинантный человеческий инсулин 1982 – первый рекомбинантный человеческий инсулин стал первым биофармацевтическим препаратом, выпущенным на рынок 1981 - разработан рекомбинантный интерферон γ, противовирусный препарат 1985 -1986 - на рынок выведен рекомбинантный интерферон α 1989 - на фармацевтическом рынке появился первый препарат ЭПО (эритропоэтин) 2000 -е годы – моноклональные антитела
 Терапия, основанная на применении антител Терапия антителами включает противоопухолевые антитела, активность которых проявляется - только на опухолевую клетку, не влияя на нормальную ткань Другое название этой терапии – таргетная от «target» -мишень
Терапия, основанная на применении антител Терапия антителами включает противоопухолевые антитела, активность которых проявляется - только на опухолевую клетку, не влияя на нормальную ткань Другое название этой терапии – таргетная от «target» -мишень
 Основополагающая разница между химическими и биотехнологическими препаратами Химические препараты Простые химические компоненты Однотипная прогнозируемая структура, которую можно легко описать Дженерики • Идентичные • Похожая биологическая активность • Важный момент: путь введения • Для получения регистрации достаточно фармакокинетических исследований Биотехнологические препараты Большие, живые и сложные Гетерогенные, трудно описать Биоподобные препараты • Сходные, но не идентичные • Биологическая активность точно не известна • Важный момент: механизм действия после попадания в организм • Фармакокинетические исследования не достаточны для регистрации
Основополагающая разница между химическими и биотехнологическими препаратами Химические препараты Простые химические компоненты Однотипная прогнозируемая структура, которую можно легко описать Дженерики • Идентичные • Похожая биологическая активность • Важный момент: путь введения • Для получения регистрации достаточно фармакокинетических исследований Биотехнологические препараты Большие, живые и сложные Гетерогенные, трудно описать Биоподобные препараты • Сходные, но не идентичные • Биологическая активность точно не известна • Важный момент: механизм действия после попадания в организм • Фармакокинетические исследования не достаточны для регистрации
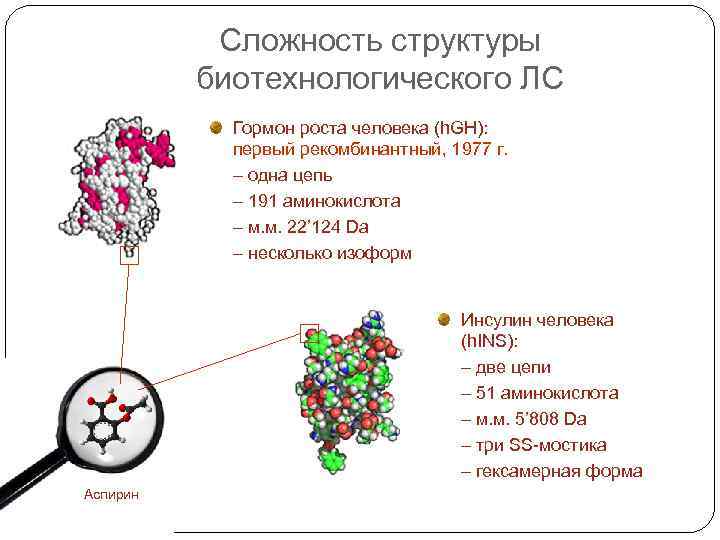 Сложность структуры биотехнологического ЛС Гормон роста человека (h. GH): первый рекомбинантный, 1977 г. – одна цепь – 191 аминокислота – м. м. 22’ 124 Da – несколько изоформ Инсулин человека (h. INS): – две цепи – 51 аминокислота – м. м. 5’ 808 Da – три SS-мостика – гексамерная форма Аспирин
Сложность структуры биотехнологического ЛС Гормон роста человека (h. GH): первый рекомбинантный, 1977 г. – одна цепь – 191 аминокислота – м. м. 22’ 124 Da – несколько изоформ Инсулин человека (h. INS): – две цепи – 51 аминокислота – м. м. 5’ 808 Da – три SS-мостика – гексамерная форма Аспирин
 Вопросы идентичности
Вопросы идентичности
 Отличие биоаналогов от дженериков, резюме В отличие от дженериков, биосимиляры могут быть схожими по фармакокинетическим параметрам, но не идентичными по эффекту оригинальному биологическому лекарственному средству. простое фармакокинетическое исследование не является достаточным для подтверждения качества биологического лекарственного средства, его безопасности и эффективности. особенности строения, производства, действия, безопасность и иммуногенность биологических лекарственных средств существенно отличают их от других лекарственных средств.
Отличие биоаналогов от дженериков, резюме В отличие от дженериков, биосимиляры могут быть схожими по фармакокинетическим параметрам, но не идентичными по эффекту оригинальному биологическому лекарственному средству. простое фармакокинетическое исследование не является достаточным для подтверждения качества биологического лекарственного средства, его безопасности и эффективности. особенности строения, производства, действия, безопасность и иммуногенность биологических лекарственных средств существенно отличают их от других лекарственных средств.
 Нормативно-правовая база по регулированию производства и регистрации биоподобных препаратов в США, Европе, Российской Федерации
Нормативно-правовая база по регулированию производства и регистрации биоподобных препаратов в США, Европе, Российской Федерации
 Руководства по биоподобным препаратам Руководство EMEA, 2006 Руководство в США в стадии формирования Руководство WHO, 2009 Австралия, Малазия, Турция, Япония, Израиль, Канада, Южная Корея имеют свои руководства, которые основаны на принципах ЕМЕА В России с 01 сентября 2010 года в ступил в силу Федеральный закон Российской Федерации от 12 апреля 2010 г. N 61 -ФЗ "Об обращении лекарственных средств"
Руководства по биоподобным препаратам Руководство EMEA, 2006 Руководство в США в стадии формирования Руководство WHO, 2009 Австралия, Малазия, Турция, Япония, Израиль, Канада, Южная Корея имеют свои руководства, которые основаны на принципах ЕМЕА В России с 01 сентября 2010 года в ступил в силу Федеральный закон Российской Федерации от 12 апреля 2010 г. N 61 -ФЗ "Об обращении лекарственных средств"
 Законодательное регулирование обращения ЛС в России Нормативно-правовое регулирование обращения ЛС в РФ отнесено к компетенции Минздравсоцразвития России. Основной процедурой допуска ЛС к медицинскому применению является процедура его регистрации с предшествующей предрегистрационной экспертизой качества, эффективности и безопасности ЛС. Мониторинг безопасности ЛС осуществляет Федеральная служба по надзору в сфере здравоохранения и социального развития и ее территориальные управления по субъектам РФ
Законодательное регулирование обращения ЛС в России Нормативно-правовое регулирование обращения ЛС в РФ отнесено к компетенции Минздравсоцразвития России. Основной процедурой допуска ЛС к медицинскому применению является процедура его регистрации с предшествующей предрегистрационной экспертизой качества, эффективности и безопасности ЛС. Мониторинг безопасности ЛС осуществляет Федеральная служба по надзору в сфере здравоохранения и социального развития и ее территориальные управления по субъектам РФ
 Нормативная база ЕС Директива 2004/27/EC Art. 10. 4 (Дополнение к директиве 2001/83/ЕС) В случае, если биологический лекарственный препарат, имеющий сходство с оригинальным биологическим препаратом, не отвечает условиям определения для генериковых лекарственных препаратов, в частности, из-за имеющихся различий между исходными материалами или процессами производства биологического лекарственного препарата и оригинального биологического лекарственного препарата, необходимо предоставить результаты соответствующих доклинических или клинических испытаний, касающиеся данных различий. Тип и количество предоставляемых дополнительных данных должны соответствовать необходимым критериям, определенным в Приложении 1 и соответствующем полном руководстве. Результаты других тестов и испытаний из регистрационного досье оригинального лекарственного препарата не предоставляются. В странах Евросоюза применение биопрепаратов регулируется специальными законодательными актами Европейского сообщества (Directive 2001/83/EC, Directive 2003/63/EC, Directive 2004/27/EC, Council regulation (EEC) №. 2309/93), национальными законами (France Law № 2007 -248 from 26. 02. 2007) и подзаконными актами, обязательными для исполнения.
Нормативная база ЕС Директива 2004/27/EC Art. 10. 4 (Дополнение к директиве 2001/83/ЕС) В случае, если биологический лекарственный препарат, имеющий сходство с оригинальным биологическим препаратом, не отвечает условиям определения для генериковых лекарственных препаратов, в частности, из-за имеющихся различий между исходными материалами или процессами производства биологического лекарственного препарата и оригинального биологического лекарственного препарата, необходимо предоставить результаты соответствующих доклинических или клинических испытаний, касающиеся данных различий. Тип и количество предоставляемых дополнительных данных должны соответствовать необходимым критериям, определенным в Приложении 1 и соответствующем полном руководстве. Результаты других тестов и испытаний из регистрационного досье оригинального лекарственного препарата не предоставляются. В странах Евросоюза применение биопрепаратов регулируется специальными законодательными актами Европейского сообщества (Directive 2001/83/EC, Directive 2003/63/EC, Directive 2004/27/EC, Council regulation (EEC) №. 2309/93), национальными законами (France Law № 2007 -248 from 26. 02. 2007) и подзаконными актами, обязательными для исполнения.
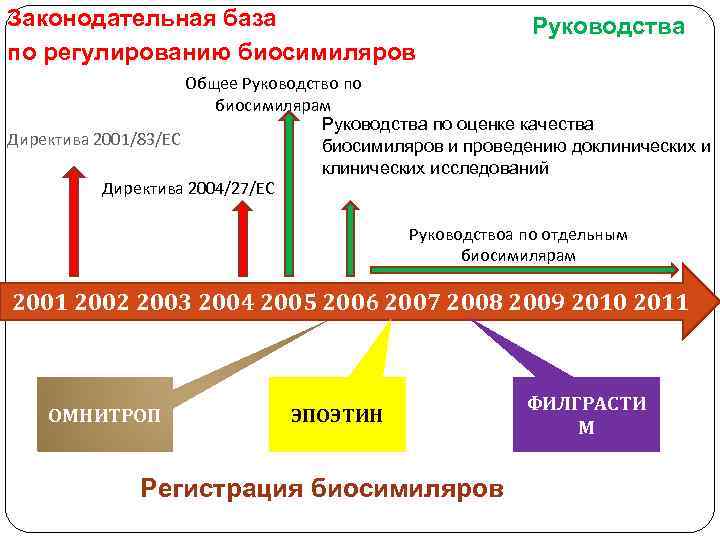 Законодательная база по регулированию биосимиляров Руководства Общее Руководство по биосимилярам Руководства по оценке качества Директива 2001/83/ЕС биосимиляров и проведению доклинических исследований Директива 2004/27/ЕС Руководствоа по отдельным биосимилярам 2001 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011 ОМНИТРОП ЭПОЭТИН Регистрация биосимиляров ФИЛГРАСТИ М
Законодательная база по регулированию биосимиляров Руководства Общее Руководство по биосимилярам Руководства по оценке качества Директива 2001/83/ЕС биосимиляров и проведению доклинических исследований Директива 2004/27/ЕС Руководствоа по отдельным биосимилярам 2001 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011 ОМНИТРОП ЭПОЭТИН Регистрация биосимиляров ФИЛГРАСТИ М
 Выводы Необходимы регуляторные стандарты, которые помогут защитить безопасность пациента Требуется подтверждение полной сопоставимости (по качеству, доклиническим и клиническим данным) Все белковые препараты должны назначаться по торговому наименованию для идентификации Отслеживание препаратов и сообщение о побочных явлениях Фармаконадзор План управления риском и пострегистрационные обязательства производителя по безопасности в равной степени применимы к оригинальному препарату и биоаналогу Маркировка/инструкция по применению препарата должны быть ясной и понятной Должна содержать обзор сравнительных клинических данных биоаналога и эталонного препарата Четкое руководство по взаимозаменяемости/замещению препаратов, исходя из имеющихся данных Автоматическая замена вызывает серьезные опасения В «стандартных» процедурах подтверждения сопоставимости отсутствуют данные о повторном переводе с одного препарата на другой 15 Европейских стран ввели новые правила, запрещающие автоматическое замещение биоаналогами оригинальных лекарственных биопрепаратов (Source: APM Health Europe, 21 February 2008).
Выводы Необходимы регуляторные стандарты, которые помогут защитить безопасность пациента Требуется подтверждение полной сопоставимости (по качеству, доклиническим и клиническим данным) Все белковые препараты должны назначаться по торговому наименованию для идентификации Отслеживание препаратов и сообщение о побочных явлениях Фармаконадзор План управления риском и пострегистрационные обязательства производителя по безопасности в равной степени применимы к оригинальному препарату и биоаналогу Маркировка/инструкция по применению препарата должны быть ясной и понятной Должна содержать обзор сравнительных клинических данных биоаналога и эталонного препарата Четкое руководство по взаимозаменяемости/замещению препаратов, исходя из имеющихся данных Автоматическая замена вызывает серьезные опасения В «стандартных» процедурах подтверждения сопоставимости отсутствуют данные о повторном переводе с одного препарата на другой 15 Европейских стран ввели новые правила, запрещающие автоматическое замещение биоаналогами оригинальных лекарственных биопрепаратов (Source: APM Health Europe, 21 February 2008).
 Решение проблемы Жесткий контроль качества каждого пути ЛС от врача к пациенту Врач – профессиональный эксперт, имеет полноценную информацию о том, какое ЛС является оригинальным препаратом, а также о качестве дженерических препаратов Качество дженерика удовлетворительно, если ЛС зарегистрировано в странах с развитой контрольно-разрешительной системой Терапевтическая эквивалентность дженерика доказана пострегистрационных исследованиях, производство соответствует GMP в
Решение проблемы Жесткий контроль качества каждого пути ЛС от врача к пациенту Врач – профессиональный эксперт, имеет полноценную информацию о том, какое ЛС является оригинальным препаратом, а также о качестве дженерических препаратов Качество дженерика удовлетворительно, если ЛС зарегистрировано в странах с развитой контрольно-разрешительной системой Терапевтическая эквивалентность дженерика доказана пострегистрационных исследованиях, производство соответствует GMP в

 Благодарю за внимание! Проценко Марина Валерьевна mpro 2006@mail. ru
Благодарю за внимание! Проценко Марина Валерьевна mpro 2006@mail. ru


