Организация работы процедурного кабинета Правила и этапы стерилизации


Организация работы процедурного кабинета Правила и этапы стерилизации инструментов

Процедурный кабинет ¡ ПЕРЕЧЕНЬ НЕОБХОДИМОГО ОБОРУДОВАНИЯ ПРОЦЕДУРНОГО КАБИНЕТА l шкаф для инструментов и медикаментов; l одноразовые шприцы, термометры, тонометр, электроотсос; l холодильник для хранения бакпрепаратов с маркированными полками; l шкаф с набором средств противошоковой терапии; l медицинскую кушетку; l биксы со стерильным материалом; l стол или шкаф для хранения медицинской документации; l емкости с дезинфицирующими растворами; l бактерицидные лампы; l средства противошоковой терапии.

¡ Подготовка процедурного кабинета к работе. mp 4

САНИТАРНО-ЭПИДЕМИОЛОГИЧЕСКИЕ ТРЕБОВАНИЯ К ОРГАНИЗАЦИЯМ, ОСУЩЕСТВЛЯЮЩИМ МЕДИЦИНСКУЮ ДЕЯТЕЛЬНОСТЬ Сан. Пи. Н 2. 1. 3. 2630 -10

Сан. Пи. Н 2. 1. 3. 2630 – 10 12. Правила обработки рук медицинского персонала и кожных покровов пациентов. ¡ В целях профилактики ВБИ обеззараживанию подлежат: l руки медицинских работников (гигиеническая обработка рук, обработка рук хирургов) l кожные покровы пациентов (обработка операционного и инъекционного полей, локтевых сгибов доноров, санитарная обработка кожных покровов)

Сан. Пи. Н 2. 1. 3. 2630 – 10 12. Правила обработки рук медицинского персонала и кожных покровов пациентов. ¡ коротко подстриженные ногти, ¡ отсутствие лака на ногтях, ¡ отсутствие искусственных ногтей, ¡ отсутствие на руках колец, перстней, часов, браслетов, других ювелирных украшений. ¡ Для высушивания рук применяют чистые тканевые полотенца или бумажные салфетки однократного использования, при обработке рук хирургов – только стерильные тканевые

Сан. Пи. Н 2. 1. 3. 2630 – 10 12. Правила обработки рук медицинского персонала и кожных покровов пациентов. ¡ Гигиеническая обработка рук l перед непосредственным контактом с пациентом; l после контакта с неповрежденной кожей пациента (например, при измерении пульса или артериального давления); l после контакта с секретами или экскретами организма, слизистыми оболочками, повязками; l перед выполнением различных манипуляций по уходу за пациентом; l после контакта с медицинским оборудованием и другими объектами, находящимися в непосредственной близости от пациента. l после лечения пациентов с гнойными воспалительными процессами, после каждого контакта с загрязненными поверхностями и оборудованием.

Сан. Пи. Н 2. 1. 3. 2630 – 10 12. Правила обработки рук медицинского персонала и кожных покровов пациентов. ¡ Гигиеническая обработка рук ¡ 2 способа: l гигиеническое мытье рук мылом и водой для удаления загрязнений и снижения количества микроорганизмов; l обработка рук кожным антисептиком для снижения количества микроорганизмов до безопасного уровня.

¡ Антисептическая обработка рук. mp 4 ¡ Профилактика ВБИ обработка рук хирурга. mp 4 ¡ Техника одевания стерильных перчаток. avi. mp 4 ¡ одевания халата в операционной - Dressing gown clothing in the operational. mp 4

Сан. Пи. Н 2. 1. 3. 2630 – 10 12. Правила обработки рук медицинского персонала и кожных покровов пациентов. ¡ Использование перчаток l Перчатки необходимо надевать во всех случаях, когда возможен контакт с кровью или другими биологическими субстратами, потенциально или явно контаминированными микроорганизмами, слизистыми оболочками, поврежденной кожей. l Не допускается использование одной и той же пары перчаток при контакте (для ухода) с двумя и более пациентами, при переходе от одного пациента к другому или от контаминированного микроорганизмами участка тела - к чистому. После снятия перчаток проводят гигиеническую обработку рук. l При загрязнении перчаток выделениями, кровью и т. п. во избежание загрязнения рук в процессе их снятия следует тампоном (салфеткой), смоченной раствором дезинфицирующего средства (или антисептика), убрать видимые загрязнения. Снять перчатки, погрузить их в раствор средства, затем утилизировать. Руки обработать антисептиком.

Сан. Пи. Н 2. 1. 3. 2630 – 10 12. Правила обработки рук медицинского персонала и кожных покровов пациентов. ¡ Обеззараживание кожных покровов пациентов l Обработку операционного поля пациента перед хирургическим вмешательством и другими манипуляциями, связанными с нарушением целостности кожных покровов (пункции, биопсии), предпочтительно проводить антисептиком, содержащим краситель. l Обработка инъекционного поля предусматривает обеззараживание кожи с помощью спиртосодержащего антисептика в месте инъекций (подкожных, внутримышечных, внутривенных) и взятия крови. l Для обработки локтевых сгибов доноров используют те же антисептики, что и для обработки операционного поля. l Для санитарной обработки кожных покровов пациентов (общей или частичной) используют антисептики, не содержащие спирты, обладающие дезинфицирующими и моющими свойствами. Санитарную обработку проводят накануне оперативного вмешательства или при уходе за пациентом.

¡ Профилактика ВБИ - дезинфекция поверхностей. avi. mp 4

Асептика и Антисептика ¡ Асе птика — комплекс мероприятий, направленных на предупреждение попадания микроорганизмов в рану. ¡ Антисептика (лат. anti — против, septicus — гниение) — система мероприятий, направленных на уничтожение микроорганизмов в ране, патологическом очаге, органах и тканях, а также в организме больного в целом.

Сан. Пи. Н 2. 1. 3. 2630 – 10 Дезинфекционные и стерилизационные мероприятия ¡ В целях профилактики внутрибольничных инфекций (ВБИ) ¡ включают в себя работы по профилактической и очаговой l дезинфекции, l дезинсекции, l дератизации, l обеззараживанию, l предстерилизационной очистке, l стерилизации изделий медицинского назначения

Сан. Пи. Н 2. 1. 3. 2630 – 10 Дезинфекционные и стерилизационные мероприятия ¡ Дезинфе кция — это комплекс мероприятий, направленных на уничтожение возбудителей инфекционных заболеваний и разрушение токсинов на объектах внешней среды.

Сан. Пи. Н 2. 1. 3. 2630 – 10 Дезинфекционные и стерилизационные мероприятия ¡ Дезинсекция – обеспечивает освобождение или снижение численности членистоногих в помещении и на окружающей территории. ¡ Дератизация – обеспечивает освобождение помещений от грызунов и снижение их численности на окружающей территории.

Сан. Пи. Н 2. 1. 3. 2630 – 10 Дезинфекционные и стерилизационные мероприятия ¡ Профилактическая дезинфекция осуществляется в формах: l плановой; l по эпидемиологическим показаниям; l по санитарно-гигиеническим показаниям.

Сан. Пи. Н 2. 1. 3. 2630 – 10 Дезинфекционные и стерилизационные мероприятия l Плановая профилактическая дезинфекция проводится систематически в ЛПО при отсутствии в них ВБИ, когда источник возбудителя не выявлен и возбудитель не выделен. l Профилактическая дезинфекция по эпидемиологическим показаниям проводится с целью не допустить распространения возбудителей ВБИ и их переносчиков в отделениях (палатах) из соседних отделений (палат). l Профилактическая дезинфекция по санитарно-гигиеническим показаниям проводится как разовое мероприятие в помещениях организаций, находящихся в неудовлетворительном санитарном состоянии по методике проведения генеральных уборок.

Уборка процедурного кабинета ¡ Виды уборки: l Предварительная уборка - удаление пыли осевшей за ночь на горизонтальных поверхностях l Текущая уборка - уборка, которая проводиться в течение рабочего дня. l Заключительная уборка – уборка, которая проводиться по окончании рабочего дня. l Генеральная уборка – уборка, которая проводится 1 раз в семь дней.

Уборка процедурного кабинета ¡ 3% раствор хлорамина /30 г хлорамина на 1 л теплой воды/ ¡ 3% перекись водорода с 0, 5% раствором моющих средств, ¡ Лизоформин 3000, Лизоформин специаль и пр.

Предварительная уборка ¡ В начале рабочего дня все плоские горизонтальные поверхности – столы, стулья должны протираться чистой тряпкой (ветошью без ворсинок) смоченной в дезинфицирующем растворе (0, 6% гипосульфит Са или 1% велтолен или 0, 5% септустин)

Текущая уборка ¡ Проводится в процессе работы, при этом подбираются, упавшие на пол шарики, салфетки и собираются в специальные емкости. Обеззараживаются места контаминированные биологическими жидкостями (кровь, экссудат). ¡ Отходы собираются в водонепроницаемый контейнер. При заполнении контейнера на три четверти объема вынести из процедурного или перевязочного кабинета в места сбора мусора. ¡ После каждой процедуры манипуляционный (перевязочный) стол обрабатывается дезинфицирующим раствором (0, 6% гипосульфит Са или 1% велтолен или 0, 5%септустин) ¡ При необходимости проводится влажная уборка пола с применением дезинфицирующего средства

Заключительная уборка ¡ Мусор собирают в специальные водонепроницаемые емкости и направляют на утилизацию. ¡ Для уборки кабинета готовиться моющий раствор (5 г моющего средства на 1 литр воды). ¡ В первую очередь протираются влажной тряпкой смоченной дезинфицирующим раствором - стены, двери, дверные ручки, стулья, стойки. Раковины чистятся щеткой, смоченной в дезинфицирующем растворе или с использованием дезинфицирующих чистящих средств. ¡ Мытье поверхностей (например стен) должно осуществляться по направлению сверху вниз для того, чтобы частицы мусора падали сверху на пол и убирались в последнюю очередь. ¡ В заключение вымыть пол моющим раствором и водой или при необходимости (при подозрении на контаминацию пола биологическими жидкостями) с применением дезинфицирующих средств

Сан. Пи. Н 2. 1. 3. 2630 – 10 Дезинфекционные и стерилизационные мероприятия ¡ Генеральная уборка ¡ При генеральной уборке проводится мытье, очистка и обеззараживание поверхностей помещений (в том числе труднодоступных), дверей, мебели, оборудования (в том числе осветительных приборов), аппаратуры с использованием моющих и дезинфицирующих средств и последующим обеззараживанием воздуха. ¡ Генеральная уборка функциональных помещений, палат и кабинетов проводится по графику не реже одного раза в месяц; операционных блоков, перевязочных, родильных залов, процедурных, манипуляционных, стерилизационных – один раз в неделю.

Сан. Пи. Н 2. 1. 3. 2630 – 10 Дезинфекционные и стерилизационные мероприятия ¡ Очаговая дезинфекция проводится при выявлении источника инфекции (больные, носители) в стационарах (отделениях), амбулаторно-поликлинических организациях любого профиля с учетом эпидемиологических особенностей инфекции и механизма передачи ее возбудителя. ¡ Целью очаговой дезинфекции является предупреждение распространения возбудителей инфекций от больных (носителей) с их выделениями и через объекты, имевшие контакт с больными в стационаре (отделении) и за его пределами. ¡ Очаговая дезинфекция осуществляется в формах текущей и заключительной очаговой дезинфекции.

Сан. Пи. Н 2. 1. 3. 2630 – 10 Дезинфекционные и стерилизационные мероприятия ¡ При проведении инвазивных манипуляций во всех отделениях и амбулаторно-поликлинических организациях используются стерильные изделия медицинского назначения, которые после использования подвергаются при профилактической и очаговой дезинфекции обеззараживанию, а изделия многократного применения - также предстерилизационной очистке и стерилизации.

Сан. Пи. Н 2. 1. 3. 2630 – 10 Дезинфекционные и стерилизационные мероприятия ¡ Предстерилизационная очистка осуществляется в качестве самостоятельного процесса после дезинфекции изделий или при совмещении с ней. ¡ Цель: удаление с изделий медицинского назначения любых неорганических и органических загрязнений (включая белковые, жировые, механические и другие), в том числе остатков лекарственных препаратов, сопровождающееся снижением общей микробной контаминации для облегчения последующей стерилизации этих изделий.

Сан. Пи. Н 2. 1. 3. 2630 – 10 Дезинфекционные и стерилизационные мероприятия ¡ Стерилизация изделий медицинского назначения, в том числе эндоскопов и инструментов к ним, используемых в диагностических и лечебных целях с нарушением целостности тканей (то есть используемых при стерильных эндоскопических манипуляциях) ¡ Цель: обеспечение гибели на изделиях (и внутри них) микроорганизмов всех видов, в том числе и споровых форм.

Сан. Пи. Н 2. 1. 3. 2630 – 10 Дезинфекционные и стерилизационные мероприятия ¡ Емкости с дезинфицирующими, моющими и стерилизующими средствами должны быть снабжены крышками, иметь четкие надписи с указанием названия дезинфицирующего средства, его концентрации, назначения, даты приготовления рабочих растворов.

Сан. Пи. Н 2. 1. 3. 2630 – 10 Дезинфекционные и стерилизационные мероприятия ¡ Медицинские изделия многократного применения подлежат последовательно: l дезинфекции, l предстерилизационной очистке, l стерилизации, l последующему хранению в условиях, исключающих вторичную контаминацию микроорганизмами. ¡ Изделия однократного применения после использования при манипуляциях у пациентов подлежат обеззараживанию/обезвреживанию, их повторное использование запрещается.

ФИЗИЧЕСКИЕ ФАКТОРЫ, влияющие на микроорганизмы ¡ ТЕМПЕРАТУРА ¡ ВЫСУШИВАНИЕ ¡ ЛУЧИСТАЯ ЭНЕРГИЯ ¡ УЛЬТРАЗВУК ¡ ДАВЛЕНИЕ

ТЕМПЕРАТУРА ¡ Высокая температура вызывает коагуляцию структурных белков и ферментов микроорганизмов. Большинство вегетативных форм гибнет при температуре 60°С в течение 30 мин, а при 80 -100°С – через 1 мин. ¡ Споры бактерий устойчивы к температуре 100°С, гибнут при 130°С и более при длительной экспозиции. ¡ Для сохранения жизнеспособности относительно благоприятны низкие температуры. Бактерии выживают при температуре ниже – 100°С; споры бактерий и вирусы годами сохраняются в жидком азоте (до – 250°С).

КЛАССИФИКАЦИЯ МИКРООРГАНИЗМОВ ПО ОТНОШЕНИЮ К ТЕМПЕРАТУРЕ ¡ Термофильные виды (теплолюбивые) Зона оптимального роста равна 50 -60°С, верхняя зона задержки роста - 75°С. Термофилы обитают в горячих сточниках. ¡ Психрофильные виды (холодолюбивые) растут в диапазоне температур 0 -10°С, максимальная зона задержки роста 20 -30°С. К ним относит большинство сапрофитов, обитающих в почве, пресной и морской воде. Но есть некоторые виды, вызывающие заболевания у человека. ¡ Мезофильные виды лучше растут в пределах 20 -40°С; максимальная 43 -45°С, минимальная 15 -20°С. В окружающей среде могут переживать, но обычно не размножаются. К ним относится большинство патогенных и условно-патогенных микроорганизмов.

ВЫСУШИВАНИЕ ¡ Высушивание приводит к обезвоживанию цитоплазмы, нарушается целостность цитоплазматической мембраны, что ведет к гибели клетки. При относительной влажности окружающей среды ниже 30% жизнедеятельность большинства бактерий прекращается. Время их отмирания при высушивании различно. Особой устойчивостью обладают споры бактерий.

ЛУЧИСТАЯ ЭНЕРГИЯ ¡ Солнечный свет губительно действует на микроорганизмы. Наибольший бактерицидный эффект оказывает коротковолновые УФ-лучи. Они инактивируют ферменты клетки и разрушают ДНК. Энергию излучения используют для дезинфекции, а также для стерилизации термолабильных материалов.
УЛЬТРАЗВУК Ультразвук вызывает поражение клетки. Под действием ультразвука внутри клетки возникает очень высокое давление. Это приводит к разрыву клеточной стенки и гибели клетки. Ультразвук используют для стерилизации и хранения стерильных материалов.

ВЫСОКОЕ ДАВЛЕНИЕ К атмосферному давлению бактерии, а особенно споры, очень устойчивы. Сочетанное действие повышенных температур и повышенного давления используется в паровых стерилизаторах для стерилизации паром под давлением.

ХИМИЧЕСКИЕ ФАКТОРЫ В малых концентрациях химическое вещество может являться питанием для бактерий, а в больших — оказывать на них губительное действие. Способность ряда химических веществ подавлять жизнедеятельность микроорганизмов зависит от концентрации химических веществ и времени контакта с микробом.

Сан. Пи. Н 2. 1. 3. 2630 – 10 Дезинфекционные и стерилизационные мероприятия ¡ Методы дезинфекции: l Физические l Химические ¡ Способы дезинфекции: l ручной (в специально предназначенных для этой цели емкостях) l механизированный (моюще- дезинфицирующие машины, ультразвуковые установки)

СПОСОБЫ ДЕЗИНФЕКЦИИ: ¡ КИПЯЧЕНИЕ ¡ ОРОШЕНИЕ ¡ ПРОТИРАНИЕ ¡ ПОГРУЖЕНИЕ (ЗАМАЧИВАНИЕ) ¡ ЗАСЫПАНИЕ

Сан. Пи. Н 2. 1. 3. 2630 – 10 Дезинфекционные и стерилизационные мероприятия ¡ При проведении дезинфекции, предстерилизационной очистки и стерилизации растворами химических средств изделия медицинского назначения погружают в рабочий раствор средства с заполнением каналов и полостей. ¡ Разъемные изделия погружают в разобранном виде, инструменты с замковыми частями замачивают раскрытыми, сделав этими инструментами в растворе несколько рабочих движений. ¡ Объем емкости для проведения обработки и объем раствора средства в ней должны быть достаточными для обеспечения полного погружения изделий медицинского назначения в раствор; толщина слоя раствора над изделиями должна быть не менее 1 см.

ТРЕБОВАНИЯ К ДЕЗИНФЕКАНТАМ ДЕЗИНФЕКТАНТЫ должны обладать ¡ широким спектром действия ¡ микробицидным эффектом, ¡ хорошо растворяться в воде и образовывать стойкие активные растворы ¡ обладать низкой токсичностью и аллергенностью ¡ сохранять активность в обеззараживаемой среде ¡ не повреждать обеззараживаемые объекты ¡ не иметь неприятного запаха ¡ быть экологически чистыми При химических способах дезинфекции применяются кислоты, щелочи, окислители, соли тяжелых металлов, фенолы, крезолы

Растворы, применяемые для дезинфекции ¡ 3% раствор хлорамина – 60 мин; ¡ 6% раствор перекиси водорода на 60 мин или 4% - 90 мин; ¡ 0, 03% раствор нейтрального анолита - экспозиция 30 мин; ¡ пресепт 0, 056% - экспозиция 90 мин (10 таб по 0, 5 г); ¡ лизетол 5% - экспозиция 15 мин (50 мл препарата + 960 мл воды); ¡ лизоформин 3000 1, 5% - экспозиция 15 мин (20 мл препарата + 980 мл воды); ¡ виркон 1% - экспозиция 10 мин (10 г препарата + 980 мл воды); ¡ дезоформ - экспозиция 60 мин (10 мл препарата + 990 мл воды); ¡ дезоформ 3% - экспозиция 30 мин (30 мл препарата + 970 мл воды); ¡ дезоформ 5% - экспозиция 10 мин (50 мл препарата + 950 мл); ¡ глутарал 2% - экспозиция 15 мин; ¡ спирт 70%-ный - экспозиция 30 мин.

1 этап стерилизации - дезинфекция ¡ После использования медицинский инструментарий и перчатки погружают в емкость с дезинфицирующим средством, затем промывают под проточной водой до исчезновения запаха хлора ¡ Дезинфекция кипячением металлических инструментов, стекла.

Сан. Пи. Н 2. 1. 3. 2630 – 10 Дезинфекционные и стерилизационные мероприятия ¡ Предстерилизационная очистка ¡ осуществляется после дезинфекции или при совмещении с дезинфекцией в одном процессе ¡ Способы: l Ручной l Механизированный

Правила предстерилизационной обработки (2 этап) ¡ После дезинфекции медицинские инструментарии ополаскиваются проточной водой. Время выдержки 0, 5 мин Затем: замачиваются при полном погружении в один из растворов моющего средства разрешенных уполномоченным органом в области санитарно- эпидемиологического благополучия населения. Первоначальная температура раствора 20 -25, время выдержки 15 мин. ¡ 2. Мытьё каждого изделия в моющем растворе при помощи ерша или ватно-марлевого тампона. Время выдержки 0, 5 мин. ¡ 3. Ополаскивание проточной водой. Время выдержки 10 мин. ¡ 4. Ополаскивание дистиллированной водой. Время выдержки 0, 5 мин ¡ 5. Сушка горячим воздухом в сушильном шкафу. Первоначальная температура раствора 85. До полного исчезновения влаги.

¡ 2. Мытьё каждого изделия в моющем растворе при помощи ерша или ватно- марлевого тампона. Время выдержки 0, 5 мин. ¡ 3. Ополаскивание проточной водой. Время выдержки 10 мин. ¡ 4. Ополаскивание дистиллированной водой. Время выдержки 0, 5 мин ¡ 5. Сушка горячим воздухом в сушильном шкафу. Первоначальная температура раствора 85. До полного исчезновения влаги.

Фенолфталеиновая проба ¡ Проверяется 1% из партии, но не менее 3 -5 изделий каждого наименования. ¡ Методика пробы. l Ватой, смоченной в 1%-ном растворе фенолфталеина, протирают рабочие поверхности, места соединения. l Проба считается положительной (некачественная промывка), если появляется розовое окрашивание. В данном случае вся партия подвергается повторной промывке.

Азопирамовая проба ¡ Предварительно готовят раствор, состоящий из азопирама и 3%-ного раствора перекиси водорода в равных количествах. ¡ Приготовленный раствор испытывают на пригодность ватой с кровью. Появление фиолетового окрашивания, быстро переходящего в розово-сиреневый цвет, говорит о пригодности препарата. ¡ Рабочий раствор можно использовать не более 2 ч. Чистый раствор азопирама хранится в холодильнике сроком до 2 месяцев. ¡ Трактовка результатов: при появлении фиолетового окрашивания вся партия инструментов обрабатывается повторно - некачественная предстерилизационная очистка.

Сан. Пи. Н 2. 1. 3. 2630 – 10 Дезинфекционные и стерилизационные мероприятия ¡ Оценка качества предстерилизационной очистки l азопирамовая или амидопириновая пробы на наличие остаточных количеств крови, l фенолфталеиновая проба на наличие остаточных количеств щелочных компонентов моющих средств (только в случаях применения средств, рабочие растворы которых имеют р. Н более 8, 5) ¡ Контроль качества предстерилизационной очистки проводят ежедневно.

Сан. Пи. Н 2. 1. 3. 2630 – 10 Дезинфекционные и стерилизационные мероприятия ¡ Стерилизации подвергают все изделия медицинского назначения, контактирующие с раневой поверхностью, кровью (в организме пациента или вводимой в него) и/или инъекционными препаратами, а также отдельные виды медицинских инструментов, которые в процессе эксплуатации соприкасаются со слизистой оболочкой и могут вызвать ее повреждение. ¡ Изделия однократного применения, предназначенные для осуществления таких манипуляций, выпускаются в стерильном виде предприятиями- изготовителями. Их повторное использование запрещается.

Сан. Пи. Н 2. 1. 3. 2630 – 10 Дезинфекционные и стерилизационные мероприятия ¡ Методы стерилизации l Физические ¡ Паровой ¡ Воздушный ¡ Инфракрасный l Химические ¡ Применение растворов химических средств ¡ Газовый ¡ Плазменный
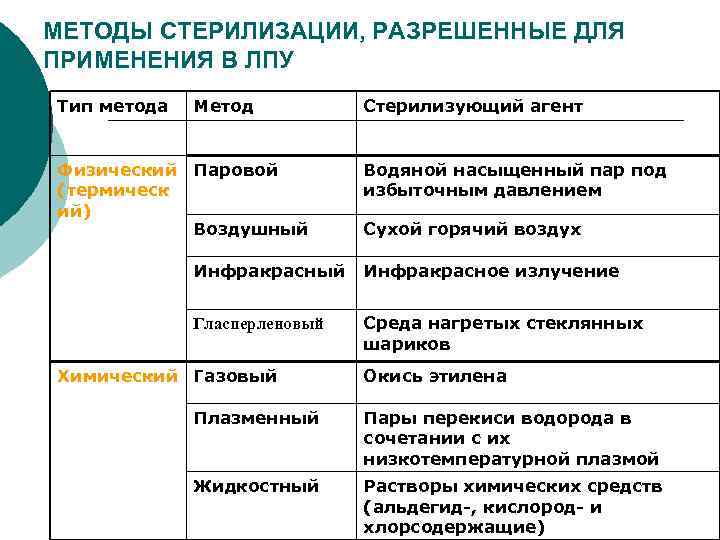
МЕТОДЫ СТЕРИЛИЗАЦИИ, РАЗРЕШЕННЫЕ ДЛЯ ПРИМЕНЕНИЯ В ЛПУ Тип метода Метод Стерилизующий агент Физический Паровой Водяной насыщенный пар под (термическ избыточным давлением ий) Воздушный Сухой горячий воздух Инфракрасный Инфракрасное излучение Гласперленовый Среда нагретых стеклянных шариков Химический Газовый Окись этилена Плазменный Пары перекиси водорода в сочетании с их низкотемпературной плазмой Жидкостный Растворы химических средств (альдегид-, кислород- и хлорсодержащие)

Термическая стерилизация ¡ Кипячение долгое время было основным способом стерилизации инструментов, но в последнее время применяется редко, так как при этом методе достигается температура лишь в 100°С, что недостаточно для уничтожения спороносных бактерий. Инструменты кипятят в специальных электрических стерилизаторах различной емкости. Инструменты в раскрытом виде (шприцы в разобранном виде) укладывают на сетку и погружают в дистиллированную воду (возможно добавление гидрокарбоната натрия - до 2% раствора). Обычное время стерилизации - 30 минут с момента закипания.
¡ В бактериологических лабораториях используется следующие методы стерилизации: ¡ Прокаливание. Этот способ применяют для обеззараживания бактериологических петель и шпателей. Для прокаливания над огнем используют спиртовки или газовые горелки. ¡ Чаще всего в бактериологических лабораториях используются паровая и суховоздушная стерилизация.

Термическая стерилизация (паровой метод) ¡ Для достижения температур выше точки кипения воды пользуются автоклавом. Автоклав представляет собой установку для стерилизации паром под давлением. Температура насыщенного пара зависит от давления. ¡ Режимы работы автоклава: v 132 °C — 2 атмосферы(2 кгс/см 2) — 20 минут — основной режим. Стерилизуют все изделия (стекло, металл, текстиль, КРОМЕ РЕЗИНОВЫХ). v 120 °C — 1, 1 атмосфера(1, 1 кгс/см 2) — 45 минут — щадящий режим. (стекло, металл, резиновые изделия, полимерные изделия — согласно паспорту, текстиль) v 110 °C — 0, 5 атмосферы(0, 5 кгс/см 2) — 180 мин — особо щадящий режим(нестойкие препараты, питательные среды)

Термическая стерилизация ¡ Дробная стерилизация в текучем паре при 100°С (тиндализация). l Жидкость стерилизуется в этом случае при 100°С три дня подряд по 30 мин ежедневно; в промежутках между нагреваниями ее хранят в термостате, для того чтобы споры проросли, а затем вегетативные клетки были уничтожены при следующем нагревании. ¡ Частичная стерилизация: уничтожение вегетативных форм микроорганизмов. l Пастеризация - 5 -10 мин при 75 или 80°С. Пастеризацией частично стерилизуют, в частности, молоко, вина.

ПАРОВАЯ СТЕРИЛИЗАЦИЯ Преимущества: ¡ Наиболее распространенный метод стерилизации в ЛПУ. ¡ Безопасен для окружающей среды и медицинского персонала. ¡ Короткая экспозиция. ¡ Не обладает токсичностью. ¡ Низкая стоимость. Недостатки: Качество стерилизации может быть нарушено при попадании воздуха, повышенной влажности материалов и плохом качестве пара. Могут повреждаться изделия, чувствительные к действию высокой температуры и влажности (коррозия металлических инструментов).

ПАРОВАЯ СТЕРИЛИЗАЦИЯ Сроки хранения стерильного материала после паровой стерилизации (не вскрывая упаковки) ¡ бикс простой – 3 суток ¡ бикс с бактериальным фильтром – 20 суток ¡ крафт - пакет, заклеенный с двух сторон – 20 суток ¡ крафт - пакет с двумя скрепками - 3 суток ¡ бязевая упаковка - 3 суток

Сан. Пи. Н 2. 1. 3. 2630 – 10 Дезинфекционные и стерилизационные мероприятия ¡ Паровым методом стерилизуют общие хирургические и специальные инструменты, детали приборов, аппаратов из коррозионностойких металлов, стекла, бельё, перевязочный материал, изделия из резин, латекса и отдельных видов пластмасс.

СУХОВОЗДУШНАЯ СТЕРИЛИЗАЦИЯ ¡ Сухой жар. Стерилизация осуществляется в специальных аппаратах - сухо-жаровых шкафах-стерилизаторах. Стерилизация в сухожаровом шкафу происходит при помощи циркуляции внутри него горячего воздуха.

СУХОВОЗДУШНАЯ СТЕРИЛИЗАЦИЯ ОСТ – 42 -21 -2 -85. Отраслевой стандарт. Стерилизация и дезинфекция изделий медицинского назначения. Методы, средства, режимы. Особенности суховоздушной стерилизации: горячий воздух плохо перемещается по камере и могут образоваться «холодные» точки, поэтому, при загрузке шкафа материал должен занимать только 2/3 объема шкафа. ¡ Режимы стерилизации: 1800 С – 1 час 160 0 С – 2, 5 часа Сроки хранения стерильного материала после суховоздушной стерилизации: ¡ материал, простерилизованный без упаковки, используется непосредственно сразу ¡ крафт - пакет, заклеенный с двух сторон – 20 суток ¡ крафт - пакет с двумя скрепками - 3 суток

СУХОВОЗДУШНАЯ СТЕРИЛИЗАЦИЯ Преимущества: Низкие коррозийные свойства. Глубокое проникновение в материал Безопасен для окружающей среды Не требует аэрации. Недостатки: Длительная экспозиция. Температурные режимы и время стерилизации отличаются в разных странах. Могут повреждаться термолабильные изделия.

Сан. Пи. Н 2. 1. 3. 2630 – 10 Дезинфекционные и стерилизационные мероприятия ¡ Воздушным методом стерилизуют хирургические, гинекологические, стоматологические инструменты, детали приборов и аппаратов, в том числе изготовленные из коррозионно- нестойких металлов, изделия из силиконовой резины. ¡ Перед стерилизацией воздушным методом изделия после предстерилизационной очистки обязательно высушивают в сушильном шкафу при температуре 85 С до исчезновения видимой влаги.

Термическая стерилизация (гласперленовый метод) ¡ Принцип действия – контакт с маленькими стеклянными сферами, имеющими температуру 250 С. ¡ Стерилизатор предназначен для быстрой стерилизации цельнометаллических, не имеющих полостей, каналов и замковых частей, стоматологических и других медицинских инструментов и приспособлений в среде нагретых до температуры 190 -290ºС стеклянных шариков при полном погружении в них мелких изделий, а также рабочих частей более крупных изделий. ¡ Временя экспозиции — не более 20 секунд. Благодаря такому короткому периоду и неразрушающему воздействию стерилизационных (глассперленовых) шариков на инструмент, негативное влияние высокой температуры практически отсутствует.

Термическая стерилизация (инфракрасный метод) ¡ Малогабаритный стерилизатор предназначен для стерилизации стоматологических и микрохирургических инструментов из металлов в условиях госпиталей, поликлиник, больниц и других лечебных и косметологических учреждений. ¡ Стерилизация осуществляется инфракрасным мощным кратковременным тепловым воздействием.
Сан. Пи. Н 2. 1. 3. 2630 – 10 Дезинфекционные и стерилизационные мероприятия ¡ Инфракрасным методом стерилизуют стоматологические и некоторые другие инструменты из металлов.

Химическая стерилизация (растворами антисептиков) v Стерилизация растворами химических антисептиков относится к холодным способам стерилизации и не приводит к затуплению инструментов, в связи с чем применяется для обработки прежде всего режущих хирургических инструментов. v Для стерилизации в основном используют три раствора: l тройной раствор (карболовая кислота — 3 г, формалин — 20 г, сода — 15 г, вода — 1000 мл) l 96° этиловый спирт l 6% перекись водорода. v В последнее время для холодной стерилизации оптических инструментов стали применять спиртовой раствор хлоргексидина, первомур и другие. v Для холодной стерилизации инструменты полностью погружают в раскрытом (или разобранном) виде в один из указанных растворов. При замачивании в спирте и тройном растворе инструменты считаются стерильными через 2 -3 часа, в перекиси водорода - через 6 часов.

Сан. Пи. Н 2. 1. 3. 2630 – 10 Дезинфекционные и стерилизационные мероприятия ¡ Химический метод применяют, для стерилизации изделий, в конструкции которых использованы термолабильные материалы, не позволяющие использовать другие официально рекомендуемые, доступные методы стерилизации. ¡ Для химической стерилизации применяют растворы альдегидсодержащих, кислородсодержащих и некоторых хлорсодержащих средств, проявляющих спороцидное действием.

Химическая стерилизация (газовый метод) ¡ 3 метода низкотемпературной стерилизации: l газовый этиленоксидный, l газовый формальдегидный l плазменный. ¡ Газовая стерилизация осуществляется в специальных герметичных камерах. ¡ Стерилизующим агентом обычно являются: пары формалина (на дно камеры кладут таблетки формальдегида) или окись этилена. ¡ Инструменты, уложенные на сетку, считаются стерильными через 6 -48 часов (в зависимости от компонентов газовой смеси и температуры в камере). ¡ Отличительной чертой метода является его минимальное отрицательное влияние на качество инструментария, в связи с чем способ используют прежде всего для стерилизации оптических, особо точных и дорогостоящих инструментов.

Сан. Пи. Н 2. 1. 3. 2630 – 10 Дезинфекционные и стерилизационные мероприятия ¡ Газовым методом стерилизуют изделия из различных, в том числе термолабильных материалов, используя в качестве стерилизующих средств окись этилена, формальдегид, озон. ¡ Перед стерилизацией газовым методом с изделий после предстерилизационной очистки удаляют видимую влагу.

Химическая стерилизация (плазменный метод) ¡ Плазменный метод позволяет создать биоцидную среду на основе водного раствора пероксида водорода, а также низкотемпературной плазмы (ионизированный газ, образующийся при низком давлении). ¡ Это самый современный метод стерилизации, известный на сегодняшний день. Он позволяет стерилизовать любые медицинские изделия, от полых инструментов до кабелей, электроприборов, к которым в ряде случаев вообще не удается применить ни один из известных методов стерилизации. ¡ При этом методе после впрыскивания раствора перекиси водорода в стерилизационную камеру включается источник электромагнитного излучения частотой 13, 56 Мгц, под воздействием которого одновременно происходит деление одной части молекул Н 2 О 2 на две группы (ОН-), а другой части - на одну гидропероксильную группу (ООН-) и один атом водорода, сопровождающееся выделением видимого и ультрафиолетового излучения. В результате создается биоцидная среда, состоящая из молекул перекиси водорода, свободных радикалов и ультрафиолетового излучения. ¡ Плазма образуется под воздействием сильного электромагнитного излучения в атмосфере паров перекиси водорода. При отключении электромагнитного поля свободные радикалы преобразуются в молекулы воды и кислорода, не оставляя никаких токсичных отходов. ¡ Минимальное время обработки в плазменном стерилизаторе – от 35 минут, рабочая температура – 36 -60°С. Одно из основных преимуществ этого метода – отсутствие токсичных отходов, образуются только кислород и водный пар. Плазменная стерилизация уничтожает все формы и виды микроорганизмов.

Сан. Пи. Н 2. 1. 3. 2630 – 10 Дезинфекционные и стерилизационные мероприятия ¡ Плазменным методом, стерилизуют хирургические, эндоскопические инструменты, эндоскопы, оптические устройства и приспособления, волоконные световодные кабели, зонды и датчики, электропроводные шнуры и кабели и другие изделия из металлов, латекса, пластмасс, стекла и кремния. ¡ Используют стерилизующие средства на основе перекиси водорода в плазменных стерилизаторах.

Стерилизация ультрафиолетовым излучением ¡ Источники УФ-излучения (длина волны 260 нм) — ртутные кварцевые лампы. Их мощное бактериостатическое действие основано на совпадении спектра испускания лампы и спектра поглощения ДНК микроорганизмов, что может является причиной их гибели при длительной обработке излучением кварцевых ламп, ¡ Метод применяется для стерилизации помещений, оборудования в биксах, а также для стерилизации дистиллированной воды.
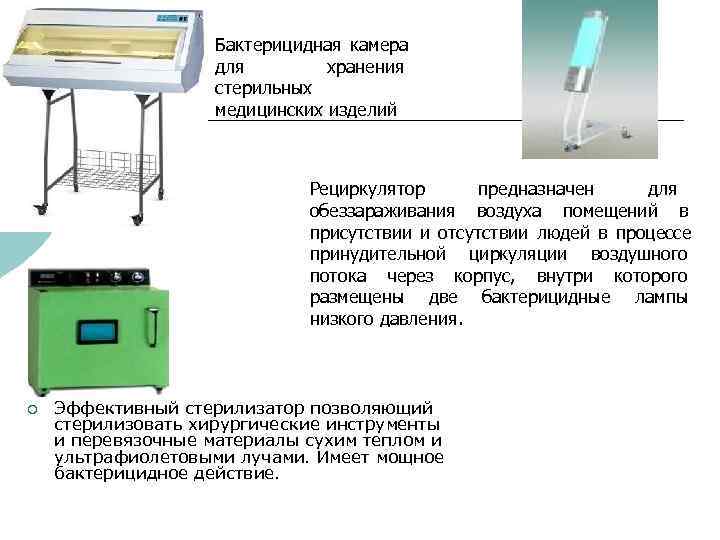
Бактерицидная камера для хранения стерильных медицинских изделий Рециркулятор предназначен для обеззараживания воздуха помещений в присутствии и отсутствии людей в процессе принудительной циркуляции воздушного потока через корпус, внутри которого размещены две бактерицидные лампы низкого давления. ¡ Эффективный стерилизатор позволяющий стерилизовать хирургические инструменты и перевязочные материалы сухим теплом и ультрафиолетовыми лучами. Имеет мощное бактерицидное действие.
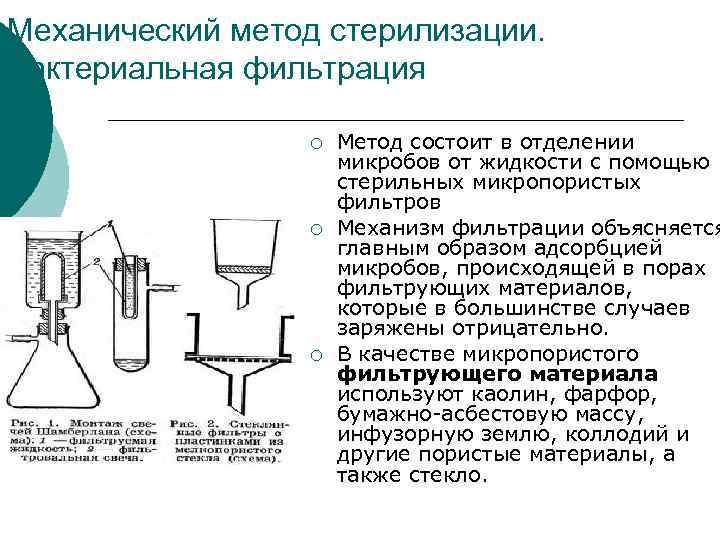
Механический метод стерилизации. Бактериальная фильтрация ¡ Метод состоит в отделении микробов от жидкости с помощью стерильных микропористых фильтров ¡ Механизм фильтрации объясняется главным образом адсорбцией микробов, происходящей в порах фильтрующих материалов, которые в большинстве случаев заряжены отрицательно. ¡ В качестве микропористого фильтрующего материала используют каолин, фарфор, бумажно-асбестовую массу, инфузорную землю, коллодий и другие пористые материалы, а также стекло.

Механический метод стерилизации. Бактериальная фильтрация ¡ Механический метод стерилизации с помощью микропористых фильтров имеет некоторые преимущества по сравнению с методами тепловой стерилизации, когда раствор подвергается воздействию высокой температуры. Для многих растворов термолабильных веществ он по существу является вообще единственным доступным методом стерилизации. ¡ Широкое применение находят микропористые фильтры на химико-фармацевтических заводах и производстве вакцин и сывороток. Бактериальные фильтры

Сан. Пи. Н 2. 1. 3. 2630 – 10 Дезинфекционные и стерилизационные мероприятия ¡ Контроль стерилизации включает: l контроль работы стерилизаторов, l проверку значений параметров режимов стерилизации, l оценку ее эффективности. ¡ Стерилизаторы подлежат бактериологическому контролю после их установки (ремонта), а также в ходе эксплуатации не реже двух раз в год в порядке производственного контроля.

Сан. Пи. Н 2. 1. 3. 2630 – 10 Дезинфекционные и стерилизационные мероприятия ¡ Контроль работы стерилизаторов ¡ Методы: l физический (с использованием контрольно-измерительных приборов) l химический (с использованием химических индикаторов) l бактериологический (с использованием биологических индикаторов)

КОНТРОЛЬ КАЧЕСТВА СТЕРИЛИЗАЦИИ ¡ химический — при каждой загрузке помещают химические тесты - индикаторы стерилизации При достижении заданного режима стерилизации тесты меняют свой цвет ¡ термический — 2 раза в месяц максимальным термометром во время стерилизации проводят замер температуры в контрольных точках, которая должна достичь заданных параметров ¡ биологический — проводится 2 раза в год. В контрольных точках помещают биотесты с термоустойчивой споровой культурой.

Сан. Пи. Н 2. 1. 3. 2630 – 10 Дезинфекционные и стерилизационные мероприятия ¡ Параметры режимов стерилизации контролируют физическим и химическим методами. ¡ Эффективность стерилизации оценивают на основании результатов бактериологических исследований при контроле стерильности изделий медицинского назначения.

Правила работы с биологическими жидкостями Приложение к письму Департамента здравоохранения города Москвы от 26. 10. 2006 г. N 44 -18 -3461 ПРИМЕРНАЯ ИНСТРУКЦИЯ ПО ОХРАНЕ ТРУДА ПРИ ВЫПОЛНЕНИИ РАБОТ С КРОВЬЮ И ДРУГИМИ БИОЛОГИЧЕСКИМИ ЖИДКОСТЯМИ ПАЦИЕНТОВ

Правила работы с биологическими жидкостями ¡ К самостоятельной работе, при которой возможен контакт с кровью и другими биологическими жидкостями, допускаются лица не моложе 18 лет, не имеющие медицинских противопоказаний, обученные безопасным методам работы и прошедшие инструктаж в объеме данной инструкции. ¡ При работе персоналу следует руководствоваться принципом, что все пациенты потенциально инфицированы.

Правила работы с биологическими жидкостями ¡ При выполнении работ с кровью и другими биологическими жидкостями пациентов возможны механические повреждения кожи: l колотые раны при неосторожном обращении со шприцами и другими колющими инструментами (предметами); l порезы кистей рук: ¡ при открывании бутылок, флаконов, пробирок с кровью или сывороткой; ¡ при работе с контаминированными ВИЧ- инструментами; l укусы психических больных при нападении на персонал.

Правила работы с биологическими жидкостями ¡ Аварийная аптечка «Анти-СПИД» l 70% этиловый спирт, ватно-марлевые тампоны; l 0, 05% раствор марганцовокислого калия или навеска препарата в сухом виде с необходимым количеством дистиллированной воды для приготовления раствора; l 5% спиртовой раствор йода; l бактерицидный пластырь; l глазные пипетки, одноразовый шприц; l перевязочный материал.

Правила работы с биологическими жидкостями ¡ Персонал должен выполнять работу в средствах индивидуальной защиты, предусмотренных отраслевыми нормами: халат х/б, медицинская шапочка, медицинские перчатки, надетые поверх рукавов медицинского халата. ¡ Для проведения инвазивных процедур рекомендуется надевать две пары перчаток, водонепроницаемый халат и фартук. ¡ При угрозе разбрызгивания крови и других биологических жидкостей работы следует выполнять в масках, защитных очках, при необходимости, использовать защитные экраны, клеенчатые фартуки.

Правила работы с биологическими жидкостями ¡ К проведению инвазивных процедур не допускается, персонал в случае: l обширных повреждений кожного покрова; l экссудативных повреждений кожи; l мокнущего дерматита.

Правила работы с биологическими жидкостями ¡ Меры индивидуальной защиты l работать в резиновых перчатках, при повышенной опасности заражения - в двух парах перчаток; l использовать маски, очки, экраны; l использовать маски и перчатки при обработке использованной одежды и инструментов; l осторожно обращаться с острым медицинским инструментарием; l не надевать колпачок на использованную иглу; l после дезинфекции использованные одноразовые острые инструменты утилизировать в твердых контейнерах; l собирать упавшие на пол иглы магнитом, щеткой и совком; l микротравмы на руках закрывать лейкопластырем, лифузолем или начальчником. До и во время работы следует проверять, не пропускают ли перчатки влагу, нет ли в них повреждений;

Правила работы с биологическими жидкостями ¡ Меры индивидуальной защиты l поврежденные перчатки немедленной заменять. Обработанные после использования перчатки менее прочны, чем новые, и повреждаются значительно чаще. Применение кремов на жировой основе, жировых смазок разрушает перчатки; l взятие крови у пациентов или проведение других процедур, когда медработник может случайно пораниться использованной иглой, необходимо производить в латексных перчатках, т. к. они уменьшают количество инокулята крови, который передается при уколе; l после снятия перчаток замочить их в дезрастворе на 1 час, руки вымыть с мылом и вытереть индивидуальным полотенцем; l снимать перчатки осторожно, чтобы не загрязнить руки; l резиновые перчатки снятые единожды, повторно не использовать из-за возможности загрязнения рук.

Правила работы с биологическими жидкостями ¡ Для предохранения себя от инфицирования через кожу и слизистые оболочки медперсонал должен соблюдать следующие правила l избегать притирающих движений при пользовании бумажным полотенцем, т. к. при этом повреждается поверхностный эпителий; l применять спиртовые дезинфекционные растворы для рук; дезинфекцию рук никогда не следует предпочитать использованию одноразовых перчаток; руки необходимо мыть водой с мылом, каждый раз после снятия защитных перчаток; l после любой процедуры необходимо двукратно тщательно мыть руки в проточной воде с мылом; l руки следует вытирать только индивидуальным полотенцем, сменяемым ежедневно, или салфетками одноразового использования;

Правила работы с биологическими жидкостями l избегать частой обработки рук раздражающими кожу дезинфектантами, не пользоваться жесткими щетками; l никогда не принимать пищу на рабочем месте, где может оказаться кровь или отделяемое пациента; l сделать прививку против гепатита B; l для защиты слизистых оболочек ротовой полости и носа применять 4 -х-слойную марлевую маску. Маска должна плотно прилегать к лицу; l надевать халат или фартук либо и халат, и фартук, чтобы обеспечить надежную защиту от попадания на участки тела биологических жидкостей. Защитная одежда должна закрывать кожу и одежду медперсонала, не пропускать жидкость, поддерживать кожу и одежду в сухом состоянии.

Правила работы с биологическими жидкостями ¡ При оказании медицинской помощи ВИЧ- инфицированным и больным СПИД в медицинских документах и направлениях, на манипуляции с парентеральными вмешательствами указывается на хроническое носительство Hbs Ag с соответствующей маркировкой. ¡ Все диагностические исследования, лечебные процедуры, оперативные вмешательства ВИЧ- инфицированным пациентам необходимо проводить в последнюю очередь, весь биологический материал дезинфицируется и уничтожается, о чем делаются отметки в истории болезни.

Правила работы с биологическими жидкостями ¡ Требования охраны труда в аварийных ситуациях ¡ К аварийным ситуациям относятся: l разрыв перчаток; l проколы и порезы колющими и режущими инструментами; l попадание крови и других биологических жидкостей на слизистые оболочки и кожные покровы; l разбрызгивание крови во время центрифугирования и др.

Правила работы с биологическими жидкостями ¡ Требования охраны труда в аварийных ситуациях ¡ К манипуляциям, которые могут привести к аварийной ситуации, в частности, относятся: l инвазивные процедуры; l соприкосновение со слизистыми оболочками (целыми и поврежденными); l соприкосновение с поврежденной кожей пациентов; l контакт с поверхностями, загрязненными кровью или другими биологическими жидкостями.

Правила работы с биологическими жидкостями ¡ При загрязнении рук кровью, биологическими жидкостями следует немедленно обработать их в течение не менее 30 секунд тампоном, смоченным кожным антисептиком, вымыть их двукратно водой с мылом и насухо вытереть чистым полотенцем, (салфеткой). ¡ При загрязнении рук, защищенных перчатками, - перчатки обработать салфеткой, затем вымыть проточной водой, снять перчатки рабочей поверхностью внутрь, вымыть руки и обработать их кожным антисептиком.

Правила работы с биологическими жидкостями ¡ Если контакт с кровью, другими биологическими жидкостями или биоматериалами сопровождается нарушением целостности кожи (уколом, порезом) l вымыть руки не снимая перчаток проточной водой с мылом; l снять перчатки рабочей поверхностью внутрь и сбросить их в дезраствор; l выдавить кровь из раны; l вымыть руки с мылом; l обработать рану 70% спиртом, затем кожу вокруг раны 5% спиртовым раствором йода; l на рану наложить бактерицидный пластырь, надеть напальчник, а при необходимости продолжать работу - надеть новые резиновые перчатки.

Правила работы с биологическими жидкостями ¡ При попадании крови или жидкостей на слизистую носа – закапать 0, 05% раствор марганцовокислого калия, рот и горло немедленно прополоскать 70% спиртом или 0, 05% раствором марганцовокислого калия. ¡ При попадании биологических жидкостей в глаза следует немедленно промыть их проточной водой, затем промыть их раствором марганцовокислого калия при помощи одноразового шприца в соотношении 1: 10000. l Раствор приготовляют из навески 0, 01 г марганцовокислого калия и 100 мл дистиллированной воды, до полного растворения кристаллов (3 мин. ).

Правила работы с биологическими жидкостями ¡ При попадании биологического материала на халат, одежду предпринять следующее: l одежду снять и замочить в одном из дезрастворов; l кожу рук и других участков тела при их загрязнении, через одежду, после снятия одежды, протереть 70% раствором этилового спирта; l поверхность промыть водой с мылом и повторно протереть спиртом; l загрязненную обувь двукратно протереть тампоном, смоченным в растворе одного из дезинфекционных средств.

Правила работы с биологическими жидкостями ¡ После обработки слизистых и кожных покровов пострадавшего необходимо: 1. Внести запись в Журнал учета микротравм учреждения (отделения). 2. Оповестить об аварии старшую медсестру и заведующего отделением (кабинетом). Старшая медсестра ставит в известность о случившемся заместителя главного врача по эпидемиологии (или помощника эпидемиолога), главную медсестру, диспансерного врача. 3. Внести записи в медицинскую карту пострадавшего, о полученной микротравме с указанием проведенных профилактических мероприятий. ¡ При подозрении на заражение медработника инфекционным заболеванием проводится расследование в соответствии с "Положением о расследовании и учете профессиональных заболеваний" (утв. постановлением Правительства РФ от 15. 12. 2000 г. N 967).

Правила работы с биологическими жидкостями ¡ Требования охраны труда по окончании работы l Разовые шприцы и инструменты после использования поместить в непротекаемый контейнер. l Острые предметы, подлежащие повторному использованию, поместить в прочную ёмкость для обработки. l Использованные иглы не ломать вручную, не сгибать, не одевать повторно колпачки. l Загрязненные кровью перчатки обработать тампоном с дезраствором, снять и погрузить их в ёмкость с дезраствором на 60 минут (3% раствор хлорамина или 6% раствор перекиси водорода с 0, 06% НГК) или кипятить в дистиллированной воде 30 минут. l Поверхности рабочих столов обработать в конце рабочего дня дезинфицирующими средствами, обладающими вирулоцидным действием.
Организация работы процедурного кабинета.ppt
- Количество слайдов: 100

