Лекция 11 органическая химия - копия.ppt
- Количество слайдов: 43
 Органическая химия
Органическая химия
 Теория органических соединений А. М. Бутлерова, 1861 г. • Атомы в молекулах соединены друг с другом в определенной последовательности согласно их валентностям. Последовательность межатомных связей в молекуле называется ее химическим строением и отражается одной структурной формулой. • Химическое строение можно устанавливать химическими методами. (используются также современные физические методы).
Теория органических соединений А. М. Бутлерова, 1861 г. • Атомы в молекулах соединены друг с другом в определенной последовательности согласно их валентностям. Последовательность межатомных связей в молекуле называется ее химическим строением и отражается одной структурной формулой. • Химическое строение можно устанавливать химическими методами. (используются также современные физические методы).
 • Свойства веществ зависят от их химического строения. • По свойствам данного вещества можно определить строение его молекулы, а по строению молекулы - предвидеть свойства. • Атомы и группы атомов в молекуле оказывают взаимное влияние друг на друга.
• Свойства веществ зависят от их химического строения. • По свойствам данного вещества можно определить строение его молекулы, а по строению молекулы - предвидеть свойства. • Атомы и группы атомов в молекуле оказывают взаимное влияние друг на друга.
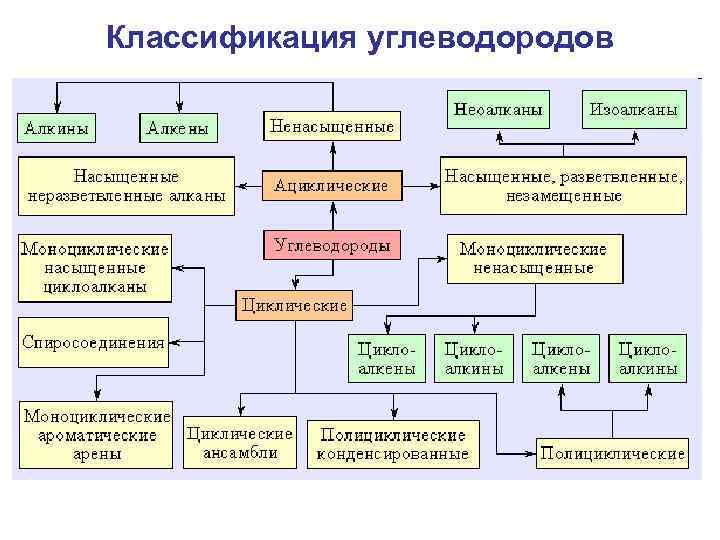 Классификация углеводородов
Классификация углеводородов
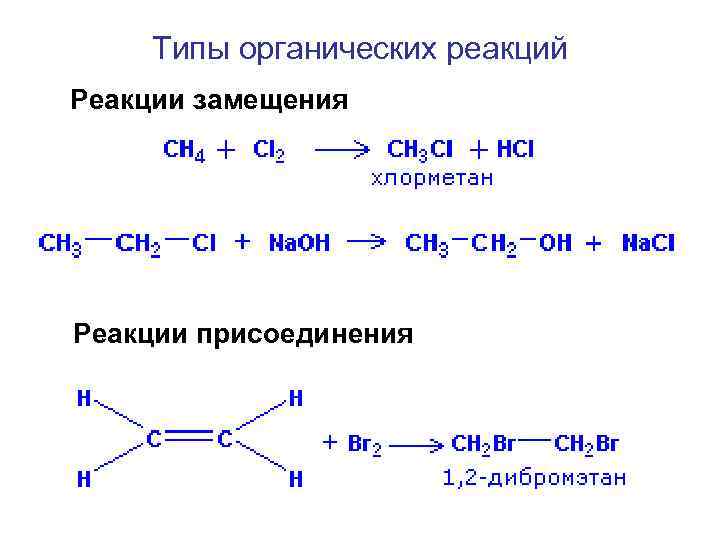 Типы органических реакций Реакции замещения Реакции присоединения
Типы органических реакций Реакции замещения Реакции присоединения
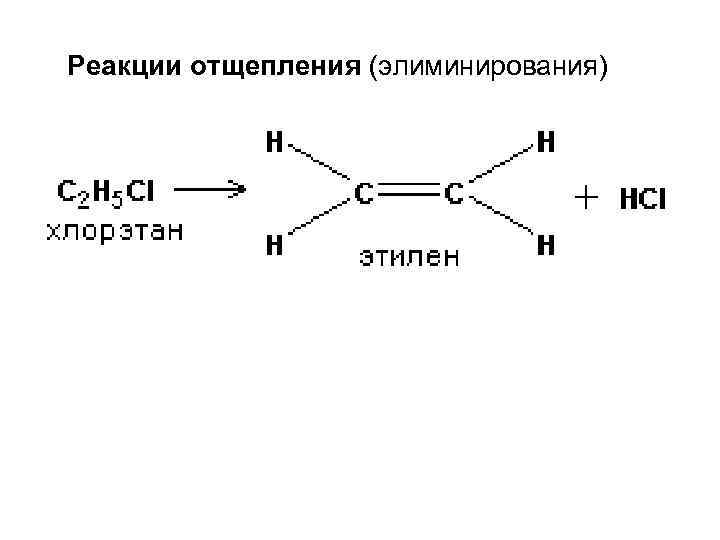 Реакции отщепления (элиминирования)
Реакции отщепления (элиминирования)
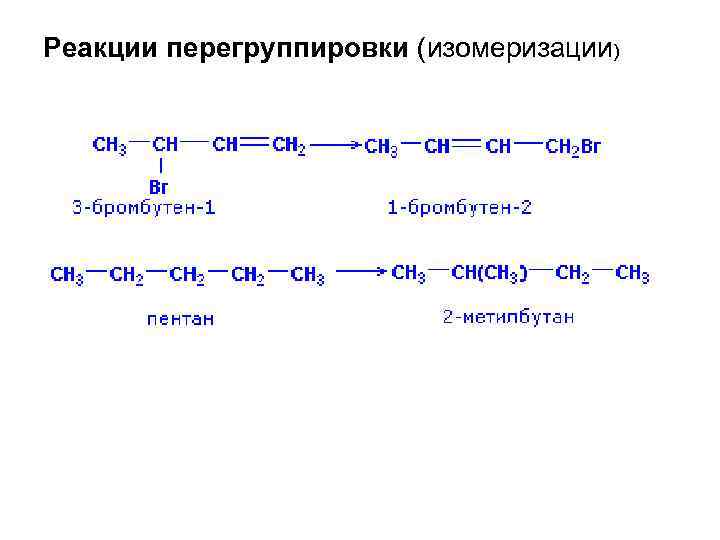 Реакции перегруппировки (изомеризации)
Реакции перегруппировки (изомеризации)
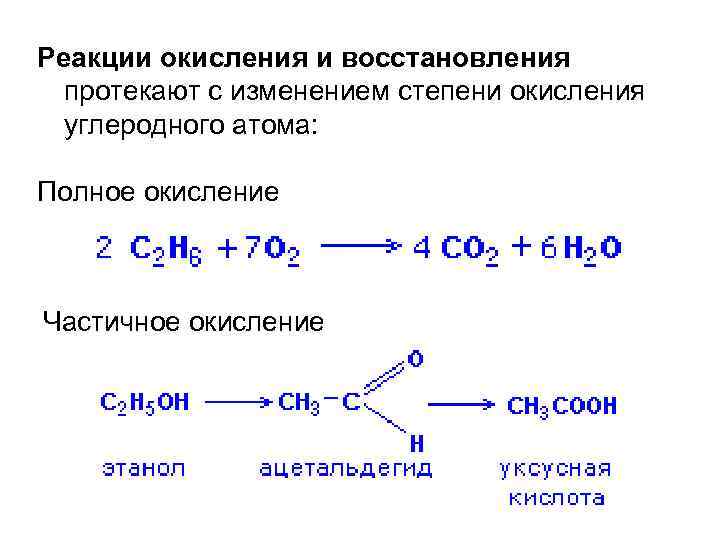 Реакции окисления и восстановления протекают с изменением степени окисления углеродного атома: Полное окисление Частичное окисление
Реакции окисления и восстановления протекают с изменением степени окисления углеродного атома: Полное окисление Частичное окисление
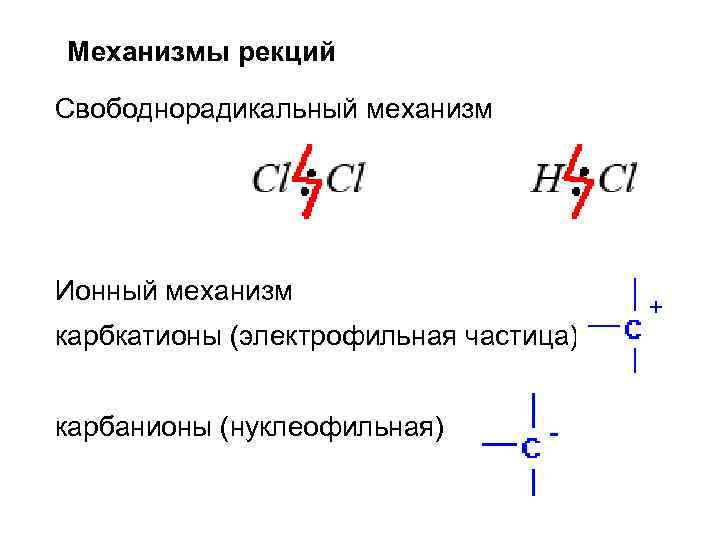 Механизмы рекций Свободнорадикальный механизм Ионный механизм карбкатионы (электрофильная частица) карбанионы (нуклеофильная)
Механизмы рекций Свободнорадикальный механизм Ионный механизм карбкатионы (электрофильная частица) карбанионы (нуклеофильная)
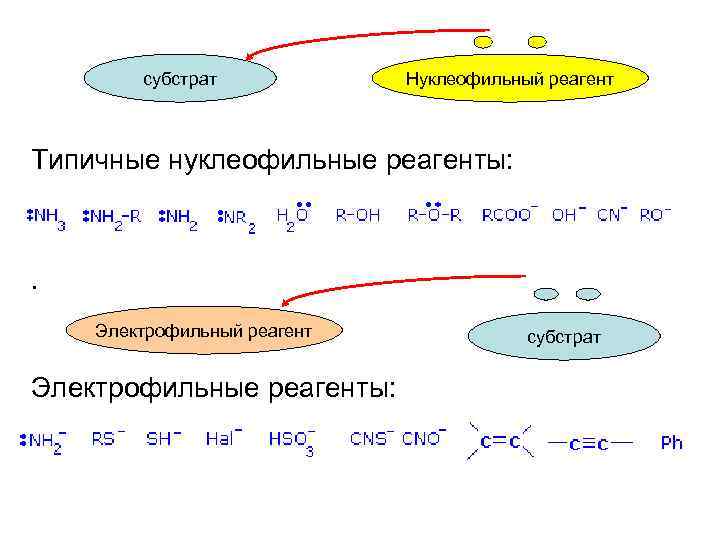 субстрат Нуклеофильный реагент Типичные нуклеофильные реагенты: . Электрофильный реагент Электрофильные реагенты: субстрат
субстрат Нуклеофильный реагент Типичные нуклеофильные реагенты: . Электрофильный реагент Электрофильные реагенты: субстрат
 Получение алканов Cn. H 2 n+1 H Действие металлического натрия на моногалогенпроизводные (Реакция Вюрца) C 2 H 5 I+CH 3 I+2 Na=C 3 H 8+2 Na. I Восстановление непредельных углеводородов H 3 C- CH=CH 2+H 2 H 3 C-CH 2 -CH 3 Сплавление солей карбоновых кислот со щелочью CH 3 COONa + Na. OH Na 2 CO 3+CH 4↑
Получение алканов Cn. H 2 n+1 H Действие металлического натрия на моногалогенпроизводные (Реакция Вюрца) C 2 H 5 I+CH 3 I+2 Na=C 3 H 8+2 Na. I Восстановление непредельных углеводородов H 3 C- CH=CH 2+H 2 H 3 C-CH 2 -CH 3 Сплавление солей карбоновых кислот со щелочью CH 3 COONa + Na. OH Na 2 CO 3+CH 4↑
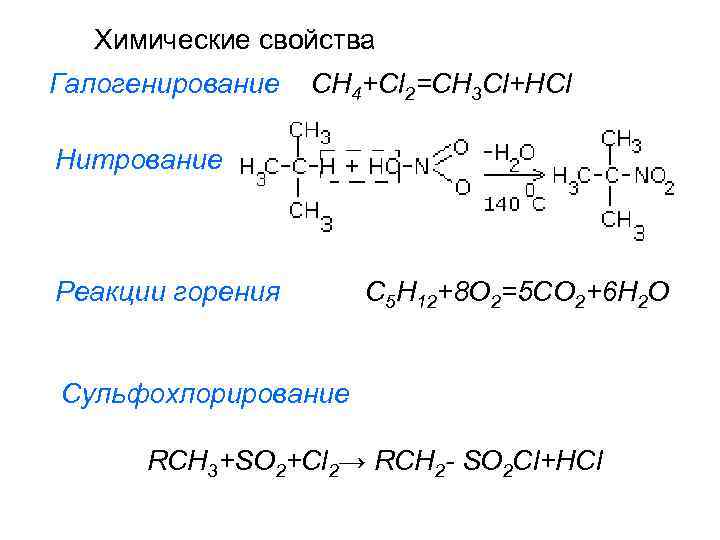 Химические свойства Галогенирование СH 4+Cl 2=CH 3 Cl+HCl Нитрование Реакции горения С 5 H 12+8 O 2=5 CO 2+6 H 2 O Сульфохлорирование RCH 3+SO 2+Cl 2→ RCH 2 - SO 2 Cl+HCl
Химические свойства Галогенирование СH 4+Cl 2=CH 3 Cl+HCl Нитрование Реакции горения С 5 H 12+8 O 2=5 CO 2+6 H 2 O Сульфохлорирование RCH 3+SO 2+Cl 2→ RCH 2 - SO 2 Cl+HCl
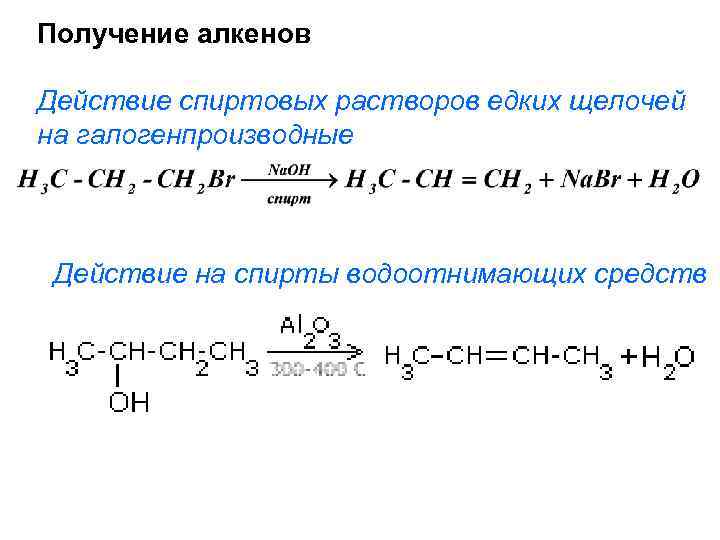 Получение алкенов Действие спиртовых растворов едких щелочей на галогенпроизводные Действие на спирты водоотнимающих средств
Получение алкенов Действие спиртовых растворов едких щелочей на галогенпроизводные Действие на спирты водоотнимающих средств
 Действие Zn или Mg на дигалогенпроизводные Гидрирование ацетиленовых углеводородов над катализаторами с пониженной активностью ( Fe)
Действие Zn или Mg на дигалогенпроизводные Гидрирование ацетиленовых углеводородов над катализаторами с пониженной активностью ( Fe)
 Химические свойства Присоединение галогенов CH 2=CH-CH 3+Cl 2 →CH 2 Cl-CH 3 Присоединение водорода CH 2=CH-CH 3+Н 2 → CH 3 -CH 2 -CH 3 Присоединение галогеноводородов (по правилу Марковникова) CH 2=CH-CH 3+НCl →CH 3 -CHCl-CH 3
Химические свойства Присоединение галогенов CH 2=CH-CH 3+Cl 2 →CH 2 Cl-CH 3 Присоединение водорода CH 2=CH-CH 3+Н 2 → CH 3 -CH 2 -CH 3 Присоединение галогеноводородов (по правилу Марковникова) CH 2=CH-CH 3+НCl →CH 3 -CHCl-CH 3
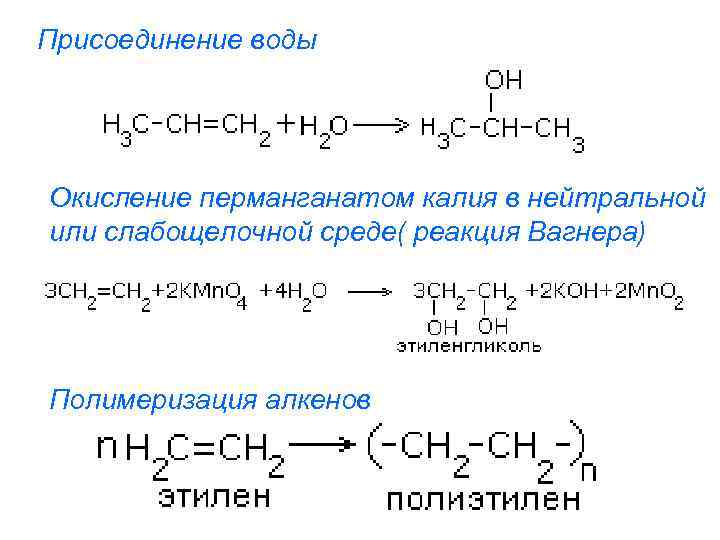 Присоединение воды Окисление перманганатом калия в нейтральной или слабощелочной среде( реакция Вагнера) Полимеризация алкенов
Присоединение воды Окисление перманганатом калия в нейтральной или слабощелочной среде( реакция Вагнера) Полимеризация алкенов
 Получение алкинов Высокотемпературный крекинг метана Гидролиз карбида кальция
Получение алкинов Высокотемпературный крекинг метана Гидролиз карбида кальция
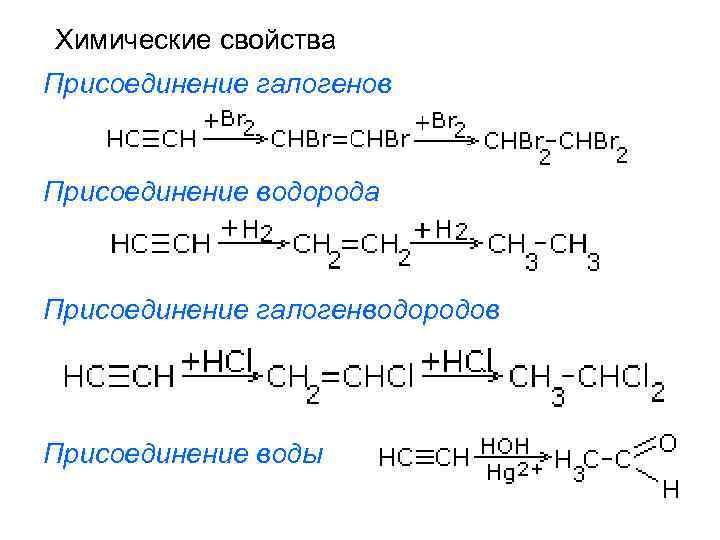 Химические свойства Присоединение галогенов Присоединение водорода Присоединение галогенводородов Присоединение воды
Химические свойства Присоединение галогенов Присоединение водорода Присоединение галогенводородов Присоединение воды
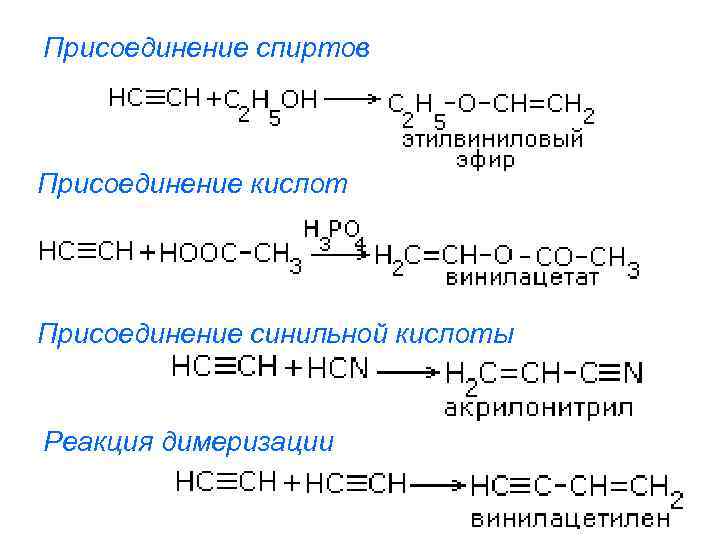 Присоединение спиртов Присоединение кислот Присоединение синильной кислоты Реакция димеризации
Присоединение спиртов Присоединение кислот Присоединение синильной кислоты Реакция димеризации
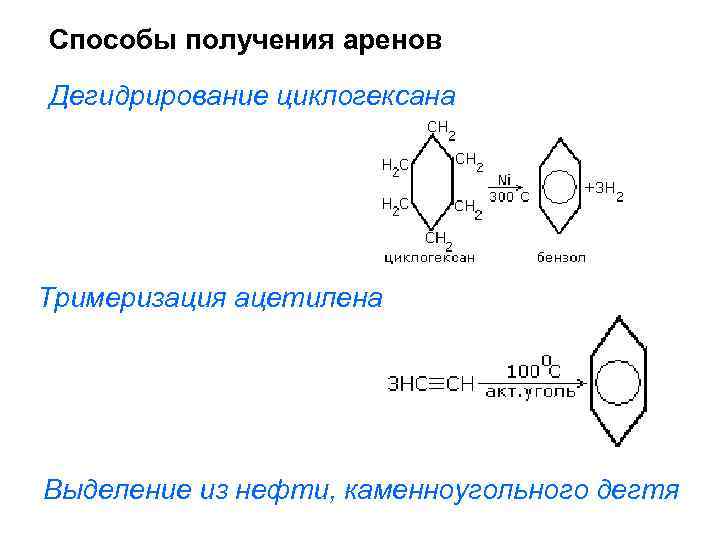 Способы получения аренов Дегидрирование циклогексана Тримеризация ацетилена Выделение из нефти, каменноугольного дегтя
Способы получения аренов Дегидрирование циклогексана Тримеризация ацетилена Выделение из нефти, каменноугольного дегтя
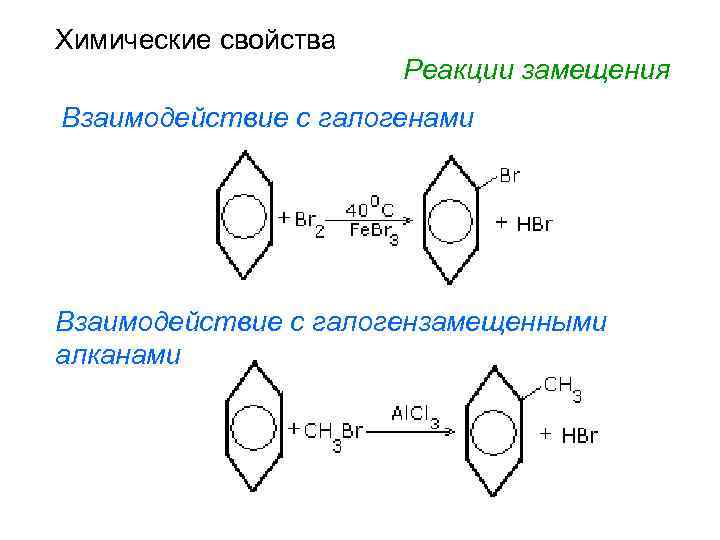 Химические свойства Реакции замещения Взаимодействие с галогенами Взаимодействие с галогензамещенными алканами
Химические свойства Реакции замещения Взаимодействие с галогенами Взаимодействие с галогензамещенными алканами
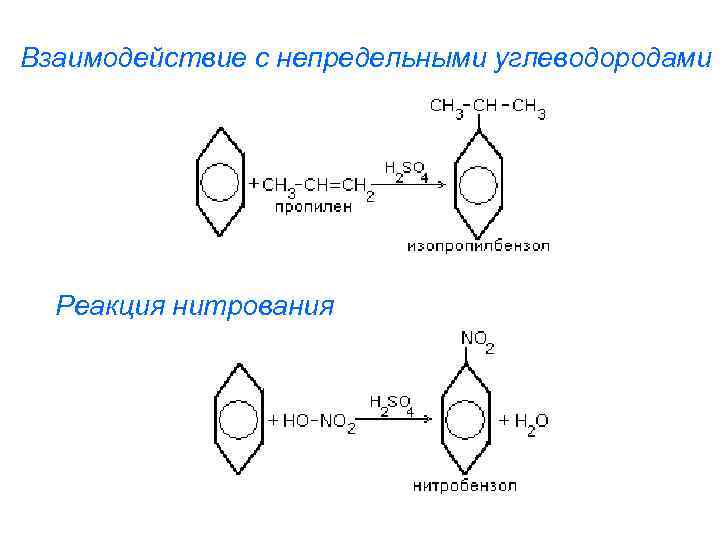 Взаимодействие с непредельными углеводородами Реакция нитрования
Взаимодействие с непредельными углеводородами Реакция нитрования
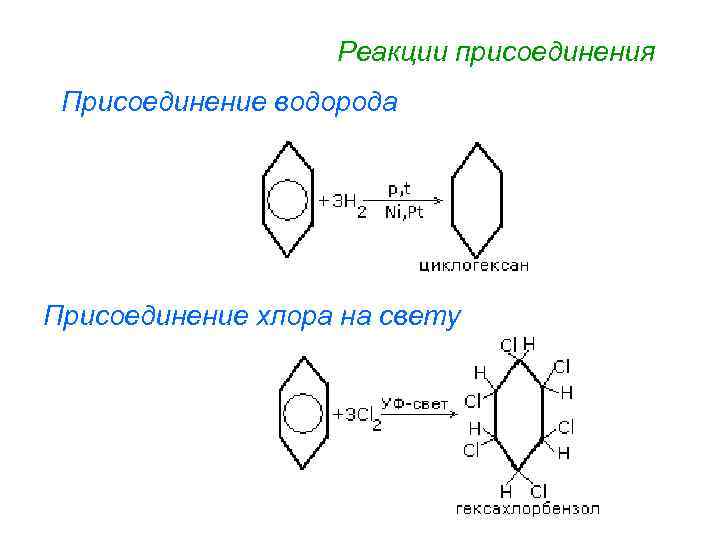 Реакции присоединения Присоединение водорода Присоединение хлора на свету
Реакции присоединения Присоединение водорода Присоединение хлора на свету
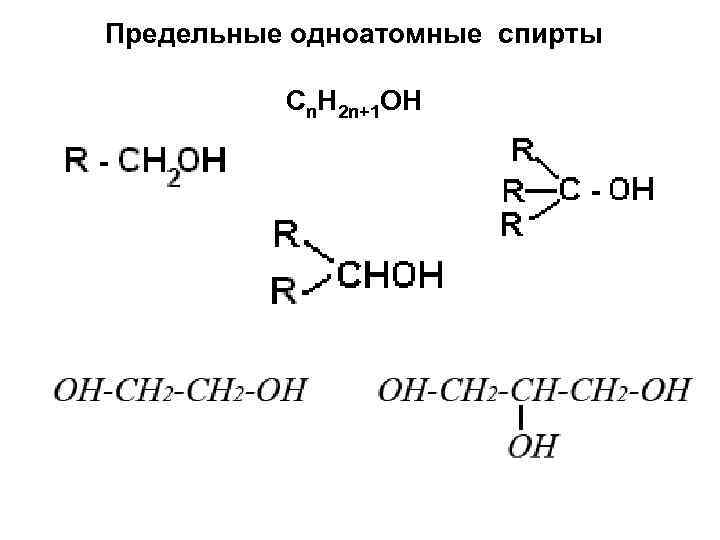 Предельные одноатомные спирты Cn. H 2 n+1 OH
Предельные одноатомные спирты Cn. H 2 n+1 OH
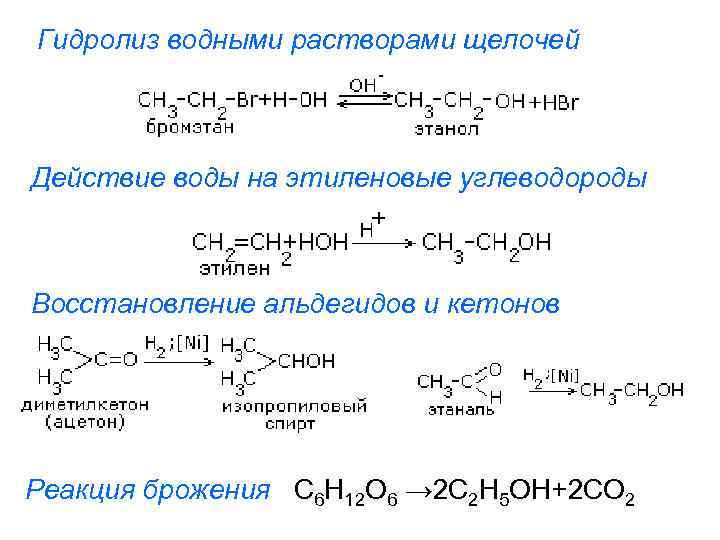 Гидролиз водными растворами щелочей Действие воды на этиленовые углеводороды Восстановление альдегидов и кетонов Реакция брожения С 6 H 12 O 6 → 2 C 2 H 5 OH+2 CO 2
Гидролиз водными растворами щелочей Действие воды на этиленовые углеводороды Восстановление альдегидов и кетонов Реакция брожения С 6 H 12 O 6 → 2 C 2 H 5 OH+2 CO 2
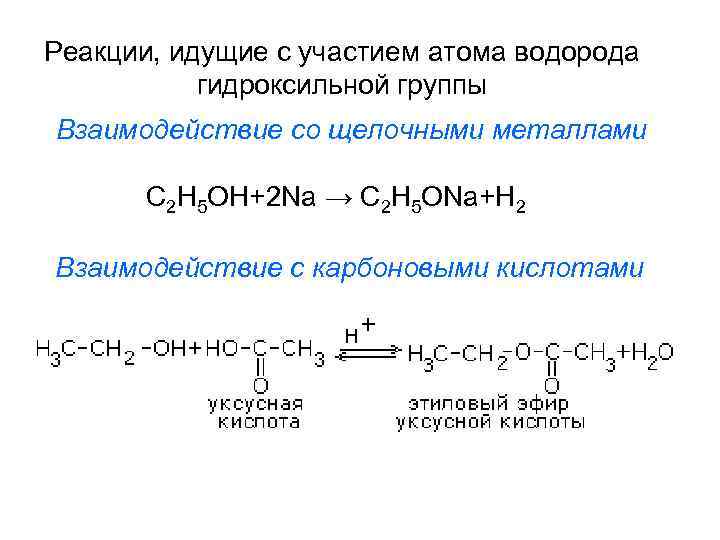 Реакции, идущие с участием атома водорода гидроксильной группы Взаимодействие со щелочными металлами C 2 H 5 OH+2 Na → C 2 H 5 ONa+H 2 Взаимодействие с карбоновыми кислотами
Реакции, идущие с участием атома водорода гидроксильной группы Взаимодействие со щелочными металлами C 2 H 5 OH+2 Na → C 2 H 5 ONa+H 2 Взаимодействие с карбоновыми кислотами
 Реакции, идущие с участием гидроксильной группы Взаимодействие с галогеноводородами C 2 H 5 OH+HBr → C 2 H 5 Br+HOH Отщепление воды C 2 H 5 OH →CH 2=CH 2+H 20 Межмолекулярная дегидратация C 2 H 5 OH+HOC 2 H 5 → (C 2 H 5)2 O+H 2 O
Реакции, идущие с участием гидроксильной группы Взаимодействие с галогеноводородами C 2 H 5 OH+HBr → C 2 H 5 Br+HOH Отщепление воды C 2 H 5 OH →CH 2=CH 2+H 20 Межмолекулярная дегидратация C 2 H 5 OH+HOC 2 H 5 → (C 2 H 5)2 O+H 2 O
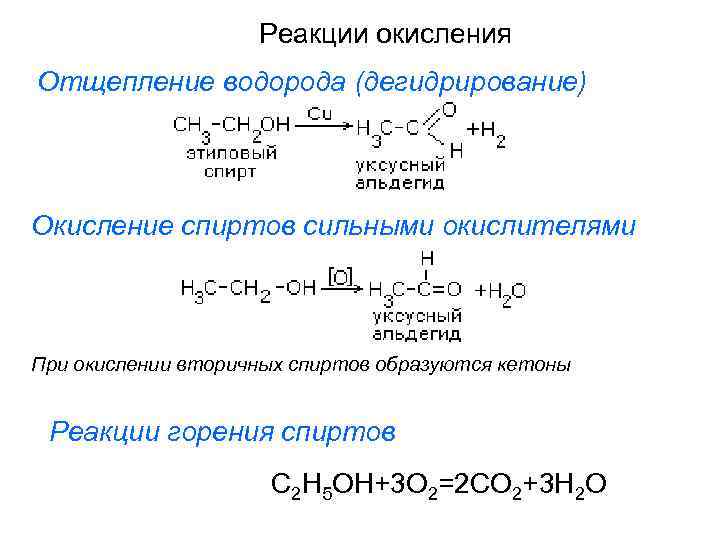 Реакции окисления Отщепление водорода (дегидрирование) Окисление спиртов сильными окислителями При окислении вторичных спиртов образуются кетоны Реакции горения спиртов C 2 H 5 OH+3 O 2=2 CO 2+3 H 2 O
Реакции окисления Отщепление водорода (дегидрирование) Окисление спиртов сильными окислителями При окислении вторичных спиртов образуются кетоны Реакции горения спиртов C 2 H 5 OH+3 O 2=2 CO 2+3 H 2 O
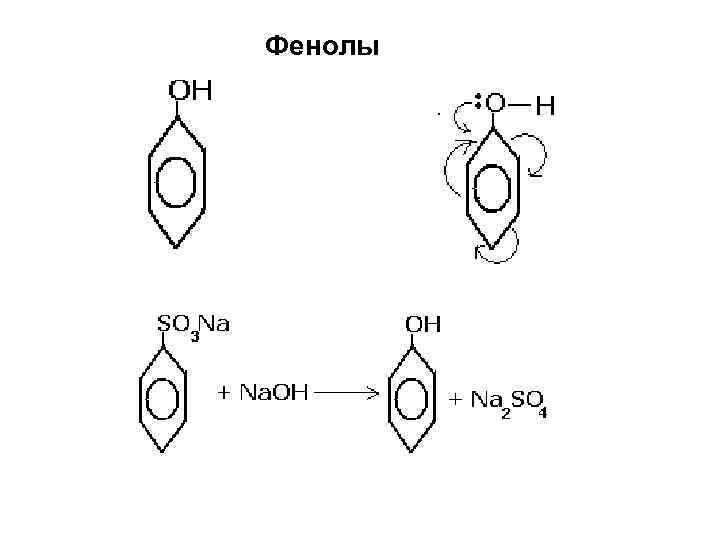 Фенолы
Фенолы
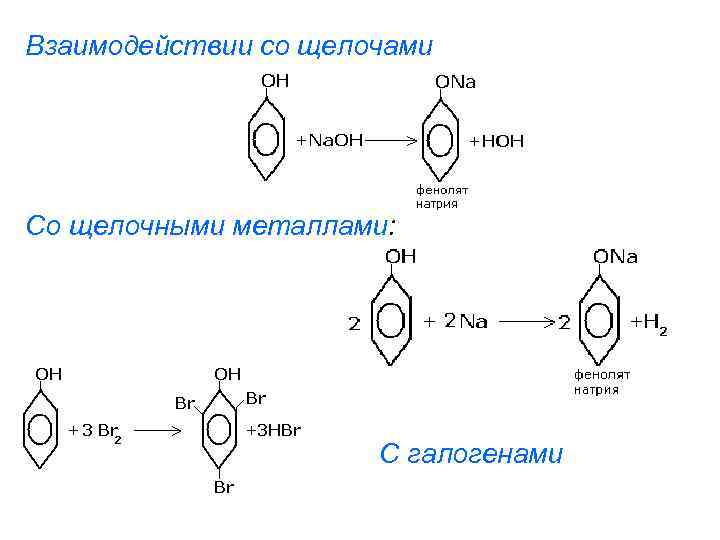 Взаимодействии со щелочами Со щелочными металлами: С галогенами
Взаимодействии со щелочами Со щелочными металлами: С галогенами
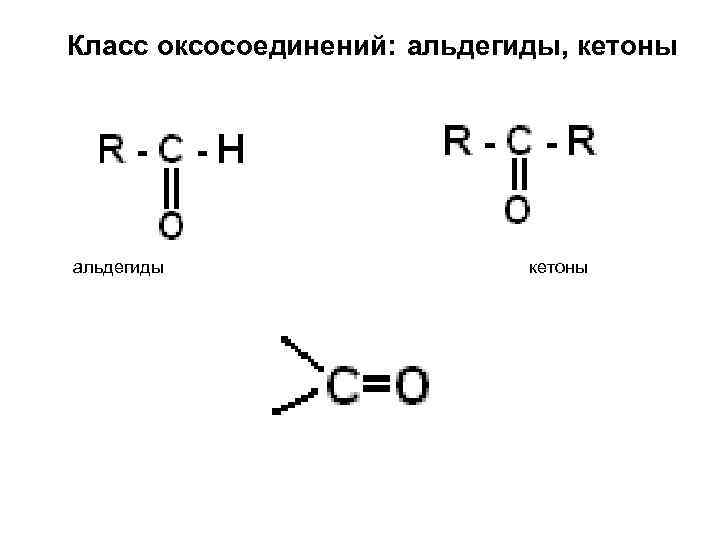 Класс оксосоединений: альдегиды, кетоны альдегиды кетоны
Класс оксосоединений: альдегиды, кетоны альдегиды кетоны
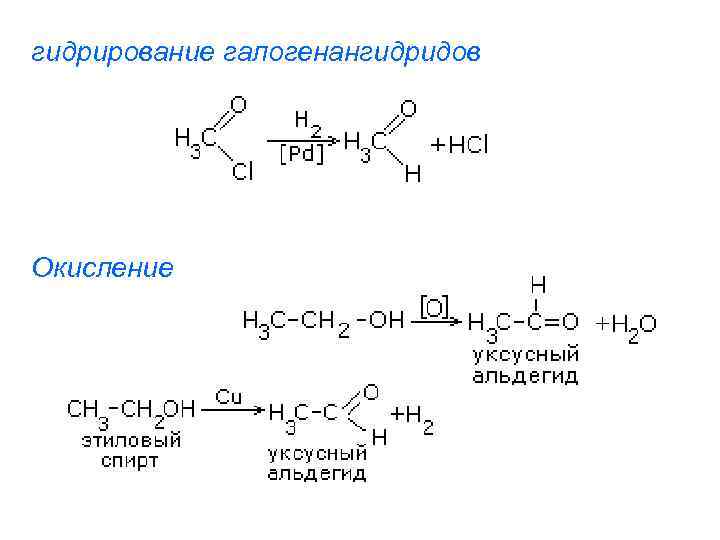 гидрирование галогенангидридов Окисление
гидрирование галогенангидридов Окисление
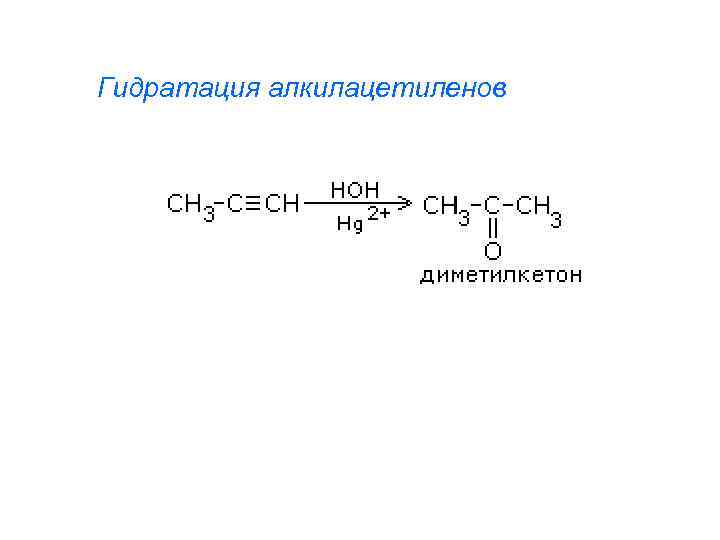 Гидратация алкилацетиленов
Гидратация алкилацетиленов
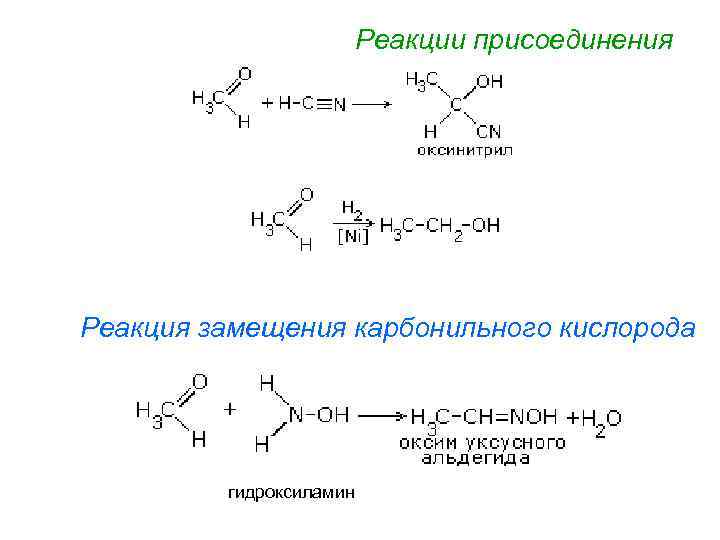 Реакции присоединения Реакция замещения карбонильного кислорода гидроксиламин
Реакции присоединения Реакция замещения карбонильного кислорода гидроксиламин
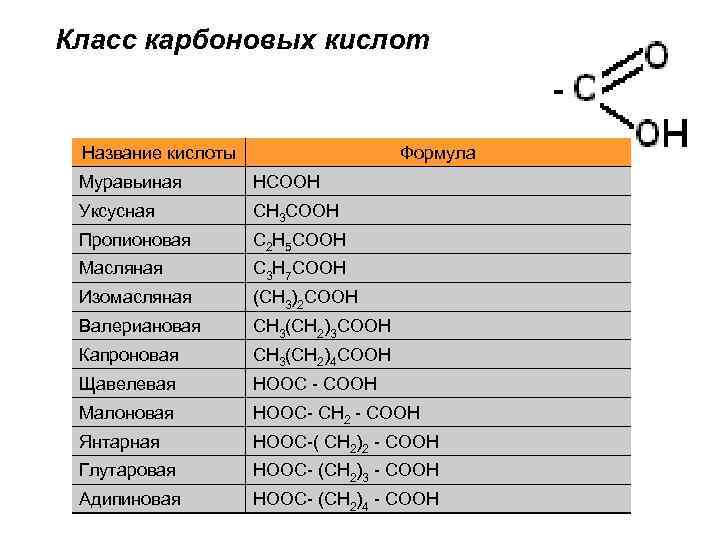 Класс карбоновых кислот Название кислоты Формула Муравьиная НСООН Уксусная СН 3 СООН Пропионовая С 2 Н 5 СООН Масляная С 3 Н 7 СООН Изомасляная (СН 3)2 СООН Валериановая СН 3(СН 2)3 СООН Капроновая СН 3(СН 2)4 СООН Щавелевая НООС - СООН Малоновая НООС- СН 2 - СООН Янтарная НООС-( СН 2)2 - СООН Глутаровая НООС- (СН 2)3 - СООН Адипиновая НООС- (СН 2)4 - СООН
Класс карбоновых кислот Название кислоты Формула Муравьиная НСООН Уксусная СН 3 СООН Пропионовая С 2 Н 5 СООН Масляная С 3 Н 7 СООН Изомасляная (СН 3)2 СООН Валериановая СН 3(СН 2)3 СООН Капроновая СН 3(СН 2)4 СООН Щавелевая НООС - СООН Малоновая НООС- СН 2 - СООН Янтарная НООС-( СН 2)2 - СООН Глутаровая НООС- (СН 2)3 - СООН Адипиновая НООС- (СН 2)4 - СООН
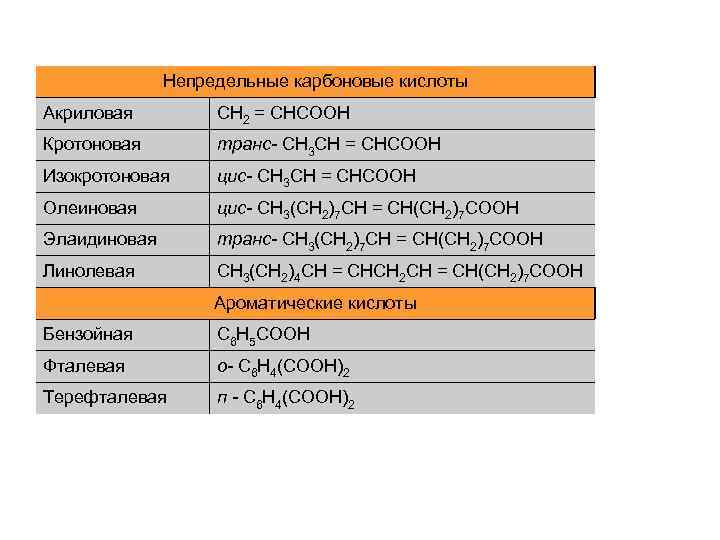 Непредельные карбоновые кислоты Акриловая СН 2 = СНСООН Кротоновая транс- СН 3 СН = СНСООН Изокротоновая цис- СН 3 СН = СНСООН Олеиновая цис- СН 3(СН 2)7 СН = СН(СН 2)7 СООН Элаидиновая транс- СН 3(СН 2)7 СН = СН(СН 2)7 СООН Линолевая СН 3(СН 2)4 СН = СНСН 2 СН = СН(СН 2)7 СООН Ароматические кислоты Бензойная С 6 Н 5 СООН Фталевая о- С 6 Н 4(СООН)2 Терефталевая п - С 6 Н 4(СООН)2
Непредельные карбоновые кислоты Акриловая СН 2 = СНСООН Кротоновая транс- СН 3 СН = СНСООН Изокротоновая цис- СН 3 СН = СНСООН Олеиновая цис- СН 3(СН 2)7 СН = СН(СН 2)7 СООН Элаидиновая транс- СН 3(СН 2)7 СН = СН(СН 2)7 СООН Линолевая СН 3(СН 2)4 СН = СНСН 2 СН = СН(СН 2)7 СООН Ароматические кислоты Бензойная С 6 Н 5 СООН Фталевая о- С 6 Н 4(СООН)2 Терефталевая п - С 6 Н 4(СООН)2
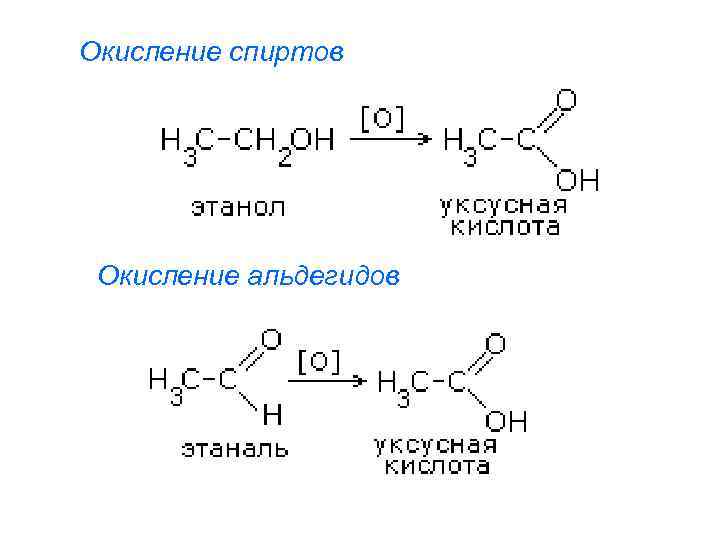 Окисление спиртов Окисление альдегидов
Окисление спиртов Окисление альдегидов
 Взаимодействие с металлами 2 CH 3 COOH+Ca → (CH 3 COO)2 Ca+H 2 Взаимодействие с оксидами металлов 2 CH 3 COOH+Ca. O → (CH 3 COO)2 Ca+H 2 O Реакция нейтрализации 2 CH 3 COOH+Ca(OH)2 → (CH 3 COO)2 Ca+2 H 2 O
Взаимодействие с металлами 2 CH 3 COOH+Ca → (CH 3 COO)2 Ca+H 2 Взаимодействие с оксидами металлов 2 CH 3 COOH+Ca. O → (CH 3 COO)2 Ca+H 2 O Реакция нейтрализации 2 CH 3 COOH+Ca(OH)2 → (CH 3 COO)2 Ca+2 H 2 O
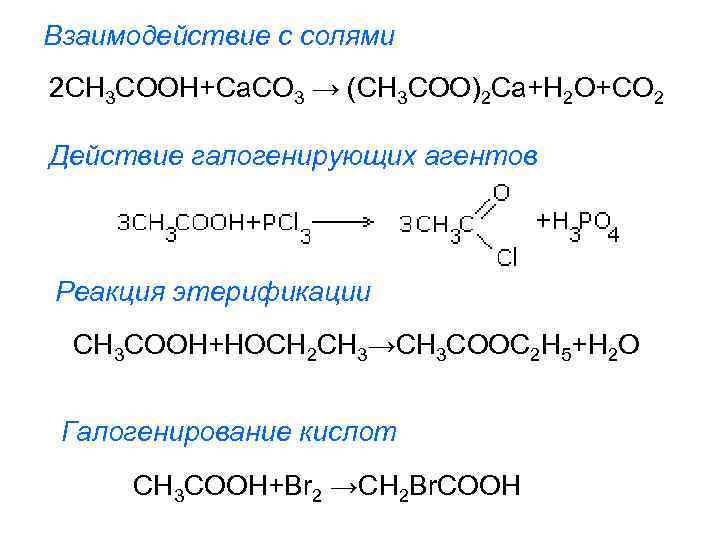 Взаимодействие с солями 2 CH 3 COOH+Ca. CO 3 → (CH 3 COO)2 Ca+H 2 O+CO 2 Действие галогенирующих агентов Реакция этерификации CH 3 COOH+HOСH 2 CH 3→CH 3 COOC 2 H 5+H 2 O Галогенирование кислот CH 3 COOH+Br 2 →CH 2 Br. COOH
Взаимодействие с солями 2 CH 3 COOH+Ca. CO 3 → (CH 3 COO)2 Ca+H 2 O+CO 2 Действие галогенирующих агентов Реакция этерификации CH 3 COOH+HOСH 2 CH 3→CH 3 COOC 2 H 5+H 2 O Галогенирование кислот CH 3 COOH+Br 2 →CH 2 Br. COOH
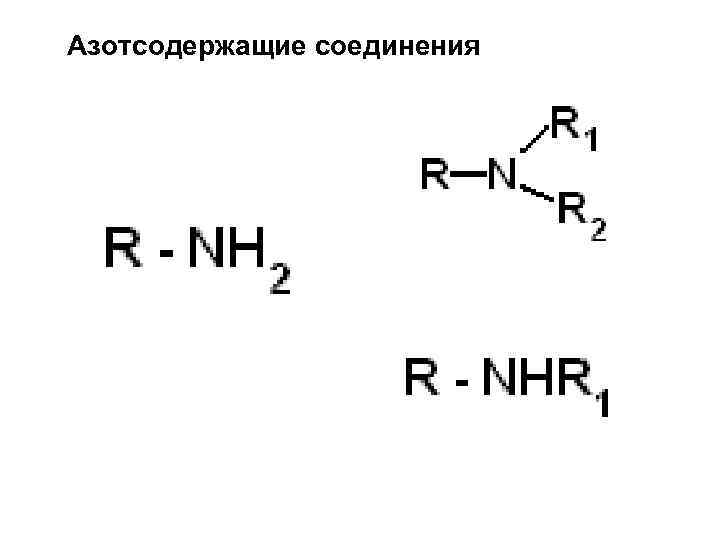 Азотсодержащие соединения
Азотсодержащие соединения
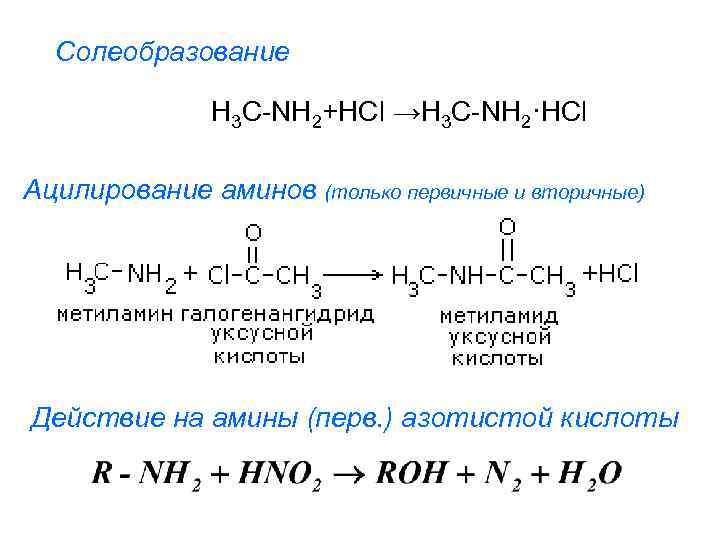 Солеобразование H 3 C-NH 2+HCl →H 3 C-NH 2·HCl Ацилирование аминов (только первичные и вторичные) Действие на амины (перв. ) азотистой кислоты
Солеобразование H 3 C-NH 2+HCl →H 3 C-NH 2·HCl Ацилирование аминов (только первичные и вторичные) Действие на амины (перв. ) азотистой кислоты
 Действие аммиака на алкилгалогениды (реакция Гофмана) H 3 C-I+NH 3 +Na. OH →CH 3 NH 2+Na. I+H 2 O Восстановление нитросоединений H 3 C-NO 2+3 H 2 →H 3 CNH 2+2 H 2 O Нагревание амидов кислот с щелочными растворами бромноватистых солей CH 3 -CO-NH 2+2 Na. OH+Na. OBr → CH 3 NH 2+Na 2 CO 3+Na. Br+H 2 O
Действие аммиака на алкилгалогениды (реакция Гофмана) H 3 C-I+NH 3 +Na. OH →CH 3 NH 2+Na. I+H 2 O Восстановление нитросоединений H 3 C-NO 2+3 H 2 →H 3 CNH 2+2 H 2 O Нагревание амидов кислот с щелочными растворами бромноватистых солей CH 3 -CO-NH 2+2 Na. OH+Na. OBr → CH 3 NH 2+Na 2 CO 3+Na. Br+H 2 O
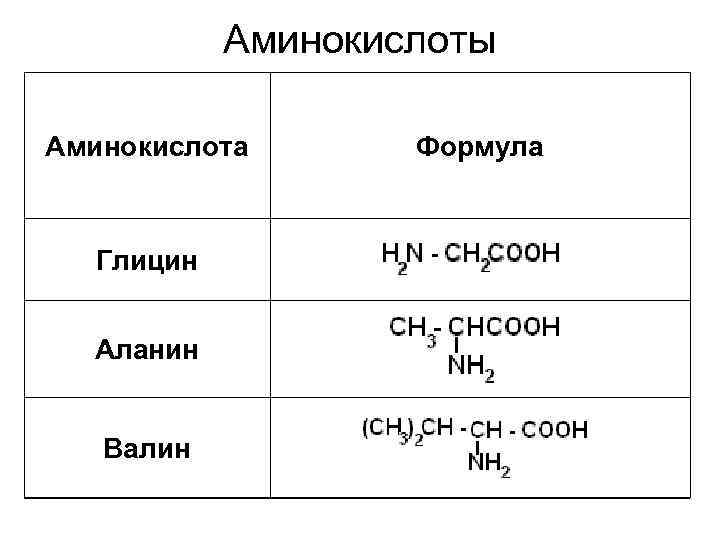 Аминокислоты Аминокислота Формула Глицин Аланин Валин
Аминокислоты Аминокислота Формула Глицин Аланин Валин


