1_Вводная_2013.pptx
- Количество слайдов: 68

 Органическая химия Лектор: Строганова Татьяна Арнольдовна, доцент кафедры биоорганической химии и ТМ
Органическая химия Лектор: Строганова Татьяна Арнольдовна, доцент кафедры биоорганической химии и ТМ
 Рекомендуемая литература: Ф. Л. Вайзман «Основы органической химии» 1. И. И. Грандберг «Органическая химия» 2. Петров, Бальян, Трощенко «Органическая химия» 3. Иванов, Горленко, Гева «Органическая химия» 4. Березин, Березин «Органическая химия» 5.
Рекомендуемая литература: Ф. Л. Вайзман «Основы органической химии» 1. И. И. Грандберг «Органическая химия» 2. Петров, Бальян, Трощенко «Органическая химия» 3. Иванов, Горленко, Гева «Органическая химия» 4. Березин, Березин «Органическая химия» 5.
 http: //www. orgsensei. moy. su
http: //www. orgsensei. moy. su

 Лекция № 1 Теоретические основы органической химии
Лекция № 1 Теоретические основы органической химии
 что же такое органическая химия? Органическая химия — это химия соединений, содержащих углерод
что же такое органическая химия? Органическая химия — это химия соединений, содержащих углерод
 Этапы развития органической химии: 1. эмпирический (до конца 18 века) 2. аналитический (18 – середина 19 века) 3. структурный (конец 19 - начало 20 века) 4. современный период
Этапы развития органической химии: 1. эмпирический (до конца 18 века) 2. аналитический (18 – середина 19 века) 3. структурный (конец 19 - начало 20 века) 4. современный период
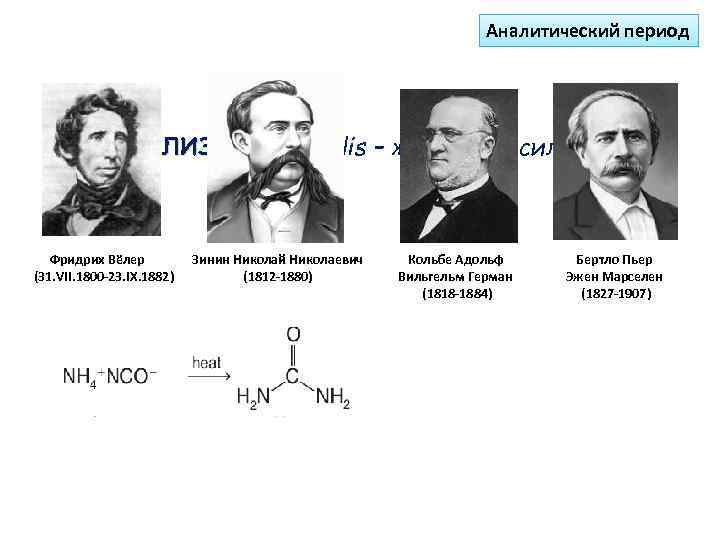 Аналитический период ВИТАЛИЗМ (vitalis – жизненная сила) Фридрих Вёлер (31. VII. 1800 -23. IX. 1882) Зинин Николай Николаевич (1812 -1880) Кольбе Адольф Вильгельм Герман (1818 -1884) Бертло Пьер Эжен Марселен (1827 -1907)
Аналитический период ВИТАЛИЗМ (vitalis – жизненная сила) Фридрих Вёлер (31. VII. 1800 -23. IX. 1882) Зинин Николай Николаевич (1812 -1880) Кольбе Адольф Вильгельм Герман (1818 -1884) Бертло Пьер Эжен Марселен (1827 -1907)
 Структурный период Бертло Пьер Эжен Марселен (1827 -1907) Бутлеров Александр Михайлович (1828 -1886)
Структурный период Бертло Пьер Эжен Марселен (1827 -1907) Бутлеров Александр Михайлович (1828 -1886)
 Теория химического строения А. М. Бутлерова 1) Все атомы в органических соединениях могут образовывать определенное число связей с участием своих внешних валентных электронов. Углерод в органических соединениях четырехвалентен, т. е. атом углерода имеет 4 валентных электрона и может образовать 4 связи Кислород двухвалентен, водород и галогены — одновалентны. 2) Атом углерода для образования связи с другим углеродным атомом может использовать один или более своих валентных электронов, т. е. Возможно образование одинарных, двойных, тройных углерод-углеродных связей и циклов.
Теория химического строения А. М. Бутлерова 1) Все атомы в органических соединениях могут образовывать определенное число связей с участием своих внешних валентных электронов. Углерод в органических соединениях четырехвалентен, т. е. атом углерода имеет 4 валентных электрона и может образовать 4 связи Кислород двухвалентен, водород и галогены — одновалентны. 2) Атом углерода для образования связи с другим углеродным атомом может использовать один или более своих валентных электронов, т. е. Возможно образование одинарных, двойных, тройных углерод-углеродных связей и циклов.
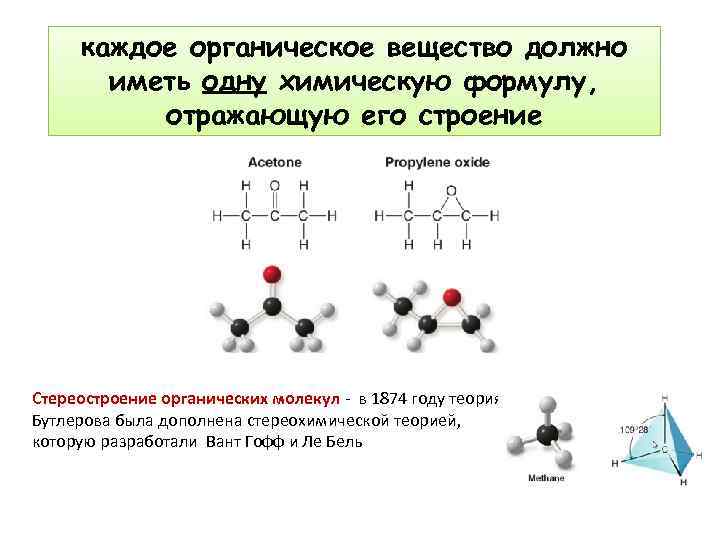 каждое органическое вещество должно иметь одну химическую формулу, отражающую его строение Стереостроение органических молекул - в 1874 году теория Бутлерова была дополнена стереохимической теорией, которую разработали Вант Гофф и Ле Бель
каждое органическое вещество должно иметь одну химическую формулу, отражающую его строение Стереостроение органических молекул - в 1874 году теория Бутлерова была дополнена стереохимической теорией, которую разработали Вант Гофф и Ле Бель
 Современный период Ознаменован развитием синтетической органической химии, внедрением квантово-механических представлений и физических методов исследования веществ, таких как инфракрасная, электронная, флуоресцентная спектроскопия, спектроскопия ЯМР, рентгеноструктурный анализ. Современная органическая химия тесно связана с другими дисциплинами – с физической, неорганической и координационной химией.
Современный период Ознаменован развитием синтетической органической химии, внедрением квантово-механических представлений и физических методов исследования веществ, таких как инфракрасная, электронная, флуоресцентная спектроскопия, спектроскопия ЯМР, рентгеноструктурный анализ. Современная органическая химия тесно связана с другими дисциплинами – с физической, неорганической и координационной химией.
 Теория химической связи Под определением ХИМИЧЕСКАЯ СВЯЗЬ понимают силу, удерживающую вместе несколько атомов, ионов, молекул. Типы связи: • ионная — образуется в результате переноса одного или нескольких электронов от одного атома к другому. В результате образуются заряженные частицы — ионы. • Ковалентная — образуется в результате обобществления электронов. Тип связи определяется разностью электроотрицательностей атомов, участвующих её образовании.
Теория химической связи Под определением ХИМИЧЕСКАЯ СВЯЗЬ понимают силу, удерживающую вместе несколько атомов, ионов, молекул. Типы связи: • ионная — образуется в результате переноса одного или нескольких электронов от одного атома к другому. В результате образуются заряженные частицы — ионы. • Ковалентная — образуется в результате обобществления электронов. Тип связи определяется разностью электроотрицательностей атомов, участвующих её образовании.
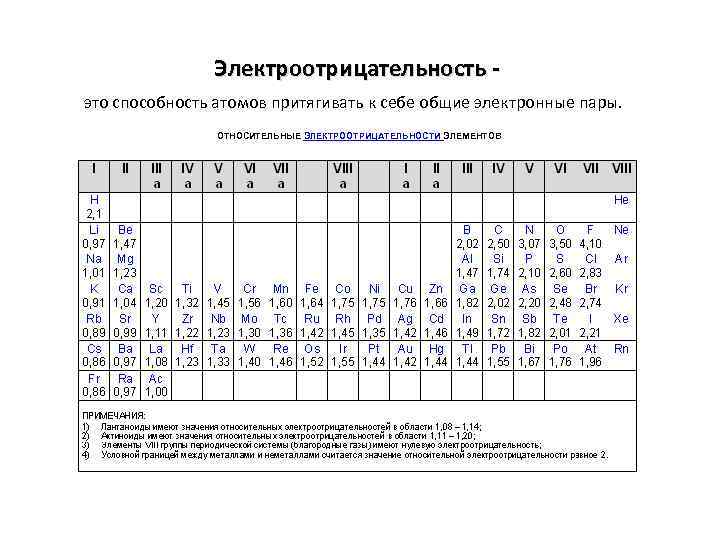 Электроотрицательность это способность атомов притягивать к себе общие электронные пары. ОТНОСИТЕЛЬНЫЕ ЭЛЕКТРООТРИЦАТЕЛЬНОСТИ ЭЛЕМЕНТОВ
Электроотрицательность это способность атомов притягивать к себе общие электронные пары. ОТНОСИТЕЛЬНЫЕ ЭЛЕКТРООТРИЦАТЕЛЬНОСТИ ЭЛЕМЕНТОВ
 Основы теории химической связи были сформулированы Льюисом и Кёсселем в 1916 году Главной идеей их теории образования связи стало утверждение о том, что любой атом реагирует, чтобы получить заполненный электронами внешний электронный уровень, подобный строению благородных газов. Для всех благородных газов, кроме гелия, это означает наличие 8 -ми электронов (октета) на внешнем электронном уровне. Поэтому стремление атомов достигать конфигурации, в которой на внешнем электронном уровне содержатся 8 электронов, называется правилом октета
Основы теории химической связи были сформулированы Льюисом и Кёсселем в 1916 году Главной идеей их теории образования связи стало утверждение о том, что любой атом реагирует, чтобы получить заполненный электронами внешний электронный уровень, подобный строению благородных газов. Для всех благородных газов, кроме гелия, это означает наличие 8 -ми электронов (октета) на внешнем электронном уровне. Поэтому стремление атомов достигать конфигурации, в которой на внешнем электронном уровне содержатся 8 электронов, называется правилом октета
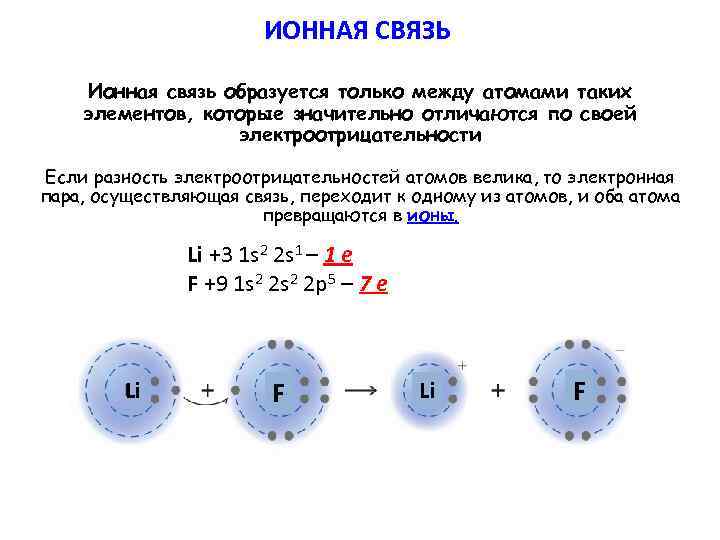 ИОННАЯ СВЯЗЬ Ионная связь образуется только между атомами таких элементов, которые значительно отличаются по своей электроотрицательности Если разность электроотрицательностей атомов велика, то электронная пара, осуществляющая связь, переходит к одному из атомов, и оба атома превращаются в ионы. Li +3 1 s 2 2 s 1 – 1 e F +9 1 s 2 2 p 5 – 7 e Li F
ИОННАЯ СВЯЗЬ Ионная связь образуется только между атомами таких элементов, которые значительно отличаются по своей электроотрицательности Если разность электроотрицательностей атомов велика, то электронная пара, осуществляющая связь, переходит к одному из атомов, и оба атома превращаются в ионы. Li +3 1 s 2 2 s 1 – 1 e F +9 1 s 2 2 p 5 – 7 e Li F
 Ковалентная связь – осуществляется общими электронными парами, сильно взаимодействующими с ядрами обоих соединяемых атомов. При образовании ковалентной связи обобществление электронов возможно по двум механизмам: 1 – обменный – каждый из атомов, вступающих в химическую связь, дает в общее пользование по одному, два или три электрона (Cl-Cl) 2 – донорно-акцепторный – в общее пользование один атом предоставляет пару электронов, а второй – свободную орбиталь (NH 4+).
Ковалентная связь – осуществляется общими электронными парами, сильно взаимодействующими с ядрами обоих соединяемых атомов. При образовании ковалентной связи обобществление электронов возможно по двум механизмам: 1 – обменный – каждый из атомов, вступающих в химическую связь, дает в общее пользование по одному, два или три электрона (Cl-Cl) 2 – донорно-акцепторный – в общее пользование один атом предоставляет пару электронов, а второй – свободную орбиталь (NH 4+).
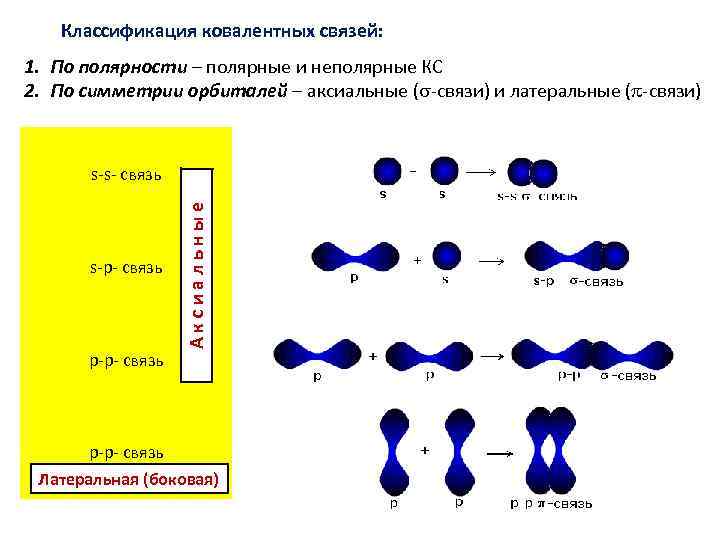 Классификация ковалентных связей: 1. По полярности – полярные и неполярные КС 2. По симметрии орбиталей – аксиальные (s-связи) и латеральные (p-связи) s-p- связь p-p- связь Аксиальные s-s- связь p-p- связь Латеральная (боковая)
Классификация ковалентных связей: 1. По полярности – полярные и неполярные КС 2. По симметрии орбиталей – аксиальные (s-связи) и латеральные (p-связи) s-p- связь p-p- связь Аксиальные s-s- связь p-p- связь Латеральная (боковая)
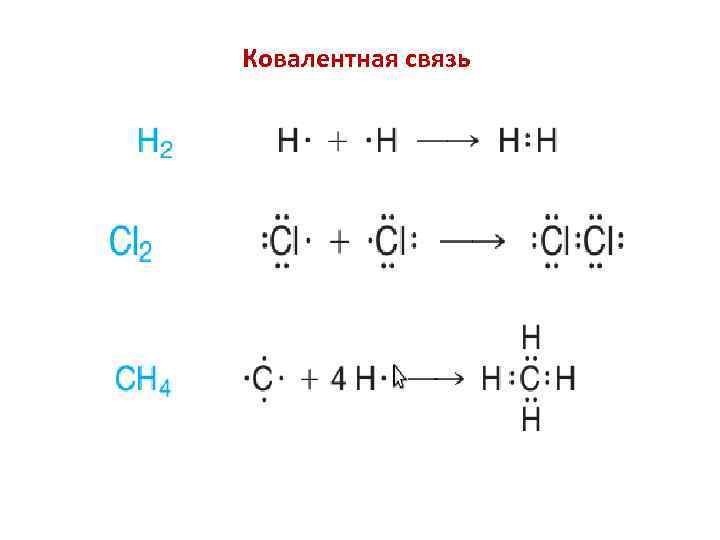 Ковалентная связь
Ковалентная связь
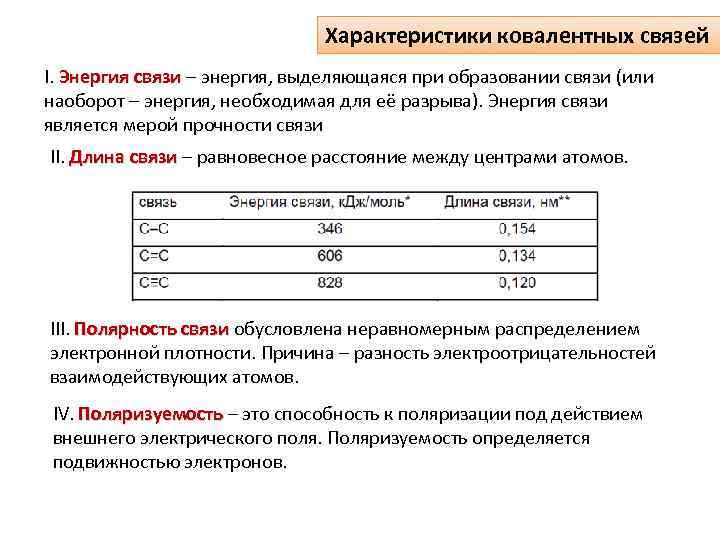 Характеристики ковалентных связей Ι. Энергия связи – энергия, выделяющаяся при образовании связи (или наоборот – энергия, необходимая для её разрыва). Энергия связи является мерой прочности связи ΙΙ. Длина связи – равновесное расстояние между центрами атомов. связи ΙΙΙ. Полярность связи обусловлена неравномерным распределением электронной плотности. Причина – разность электроотрицательностей взаимодействующих атомов. IV. Поляризуемость – это способность к поляризации под действием внешнего электрического поля. Поляризуемость определяется подвижностью электронов.
Характеристики ковалентных связей Ι. Энергия связи – энергия, выделяющаяся при образовании связи (или наоборот – энергия, необходимая для её разрыва). Энергия связи является мерой прочности связи ΙΙ. Длина связи – равновесное расстояние между центрами атомов. связи ΙΙΙ. Полярность связи обусловлена неравномерным распределением электронной плотности. Причина – разность электроотрицательностей взаимодействующих атомов. IV. Поляризуемость – это способность к поляризации под действием внешнего электрического поля. Поляризуемость определяется подвижностью электронов.
 органические молекулы могут быть связаны чисто механически – без какого-либо электростатического взаимодействия. Такая связь называется топологической.
органические молекулы могут быть связаны чисто механически – без какого-либо электростатического взаимодействия. Такая связь называется топологической.
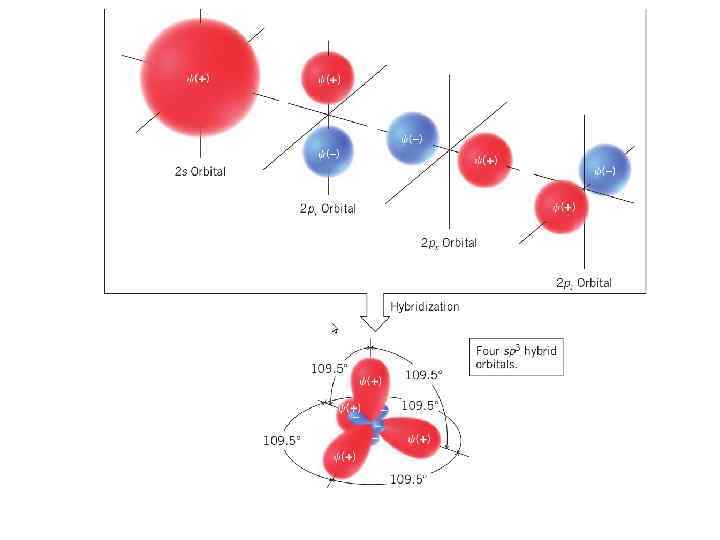
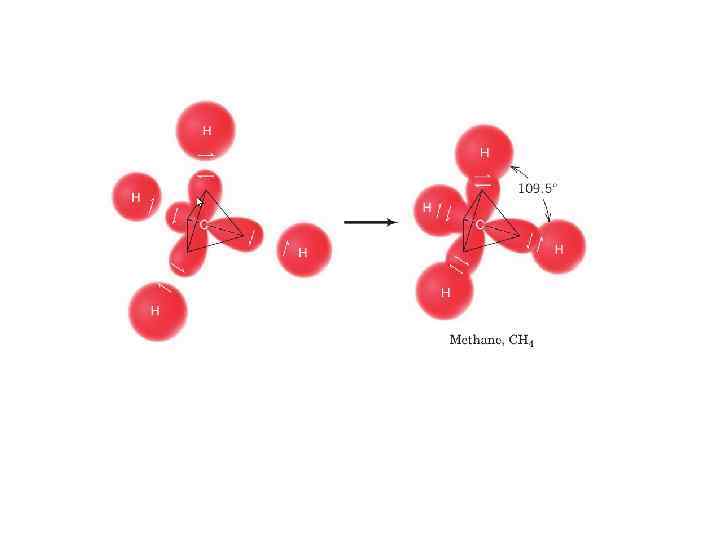
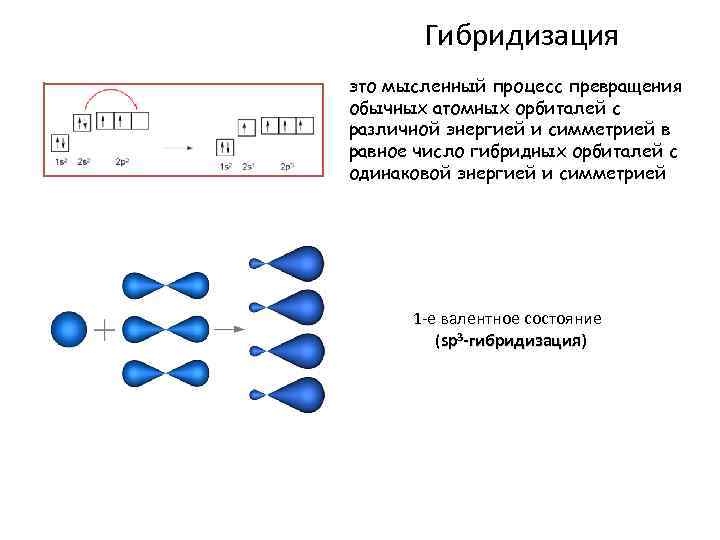 Гибридизация это мысленный процесс превращения обычных атомных орбиталей с различной энергией и симметрией в равное число гибридных орбиталей с одинаковой энергией и симметрией 1 -е валентное состояние (sp 3 -гибридизация) -гибридизация
Гибридизация это мысленный процесс превращения обычных атомных орбиталей с различной энергией и симметрией в равное число гибридных орбиталей с одинаковой энергией и симметрией 1 -е валентное состояние (sp 3 -гибридизация) -гибридизация
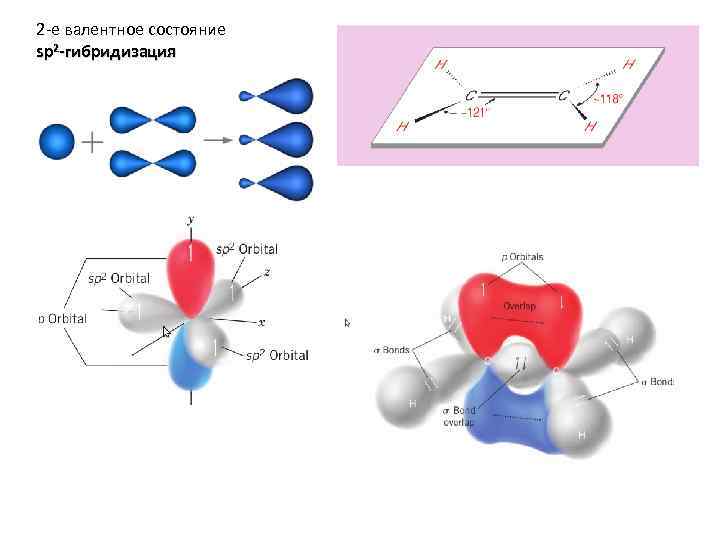 2 -е валентное состояние sp 2 -гибридизация
2 -е валентное состояние sp 2 -гибридизация
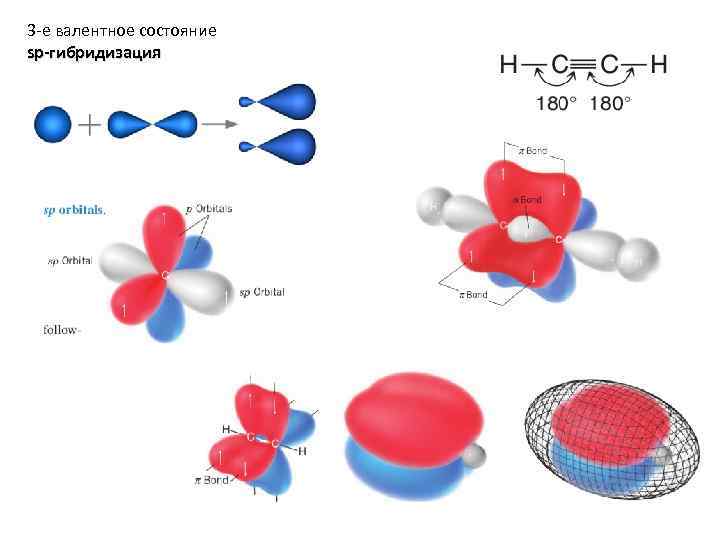 3 -е валентное состояние sp-гибридизация
3 -е валентное состояние sp-гибридизация
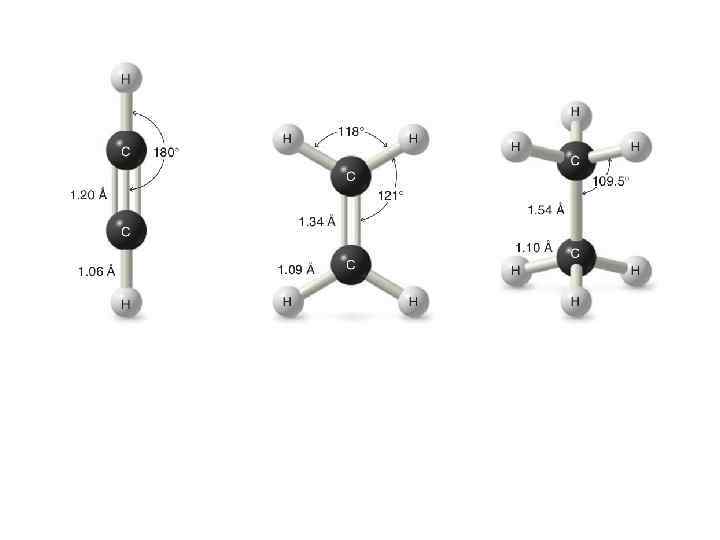
 Делокализованная химическая связь. Сопряжение Делокализованная связь охватывает три или более атомов. Сопряжение – взаимодействие между орбиталями отдельных фрагментов молекулы. Различают: Ø -сопряжение , Ø p, -сопряжение Ø другие виды сопряжения
Делокализованная химическая связь. Сопряжение Делокализованная связь охватывает три или более атомов. Сопряжение – взаимодействие между орбиталями отдельных фрагментов молекулы. Различают: Ø -сопряжение , Ø p, -сопряжение Ø другие виды сопряжения
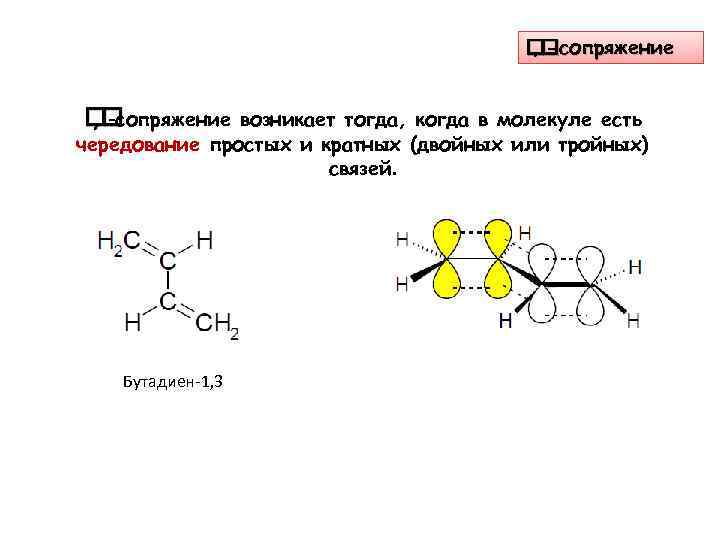 -сопряжение , -сопряжение возникает тогда, когда в молекуле есть , чередование простых и кратных (двойных или тройных) связей. Бутадиен-1, 3
-сопряжение , -сопряжение возникает тогда, когда в молекуле есть , чередование простых и кратных (двойных или тройных) связей. Бутадиен-1, 3
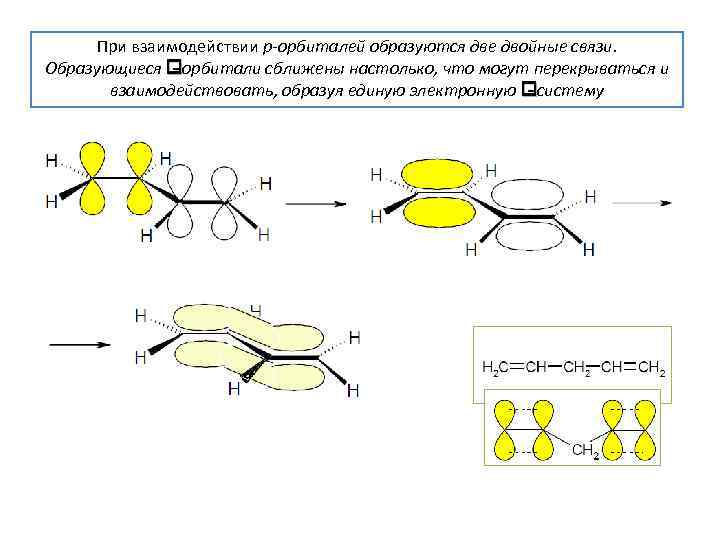 При взаимодействии p-орбиталей образуются две двойные связи. Образующиеся орбитали сближены настолько, что могут перекрываться и взаимодействовать, образуя единую электронную систему -
При взаимодействии p-орбиталей образуются две двойные связи. Образующиеся орбитали сближены настолько, что могут перекрываться и взаимодействовать, образуя единую электронную систему -
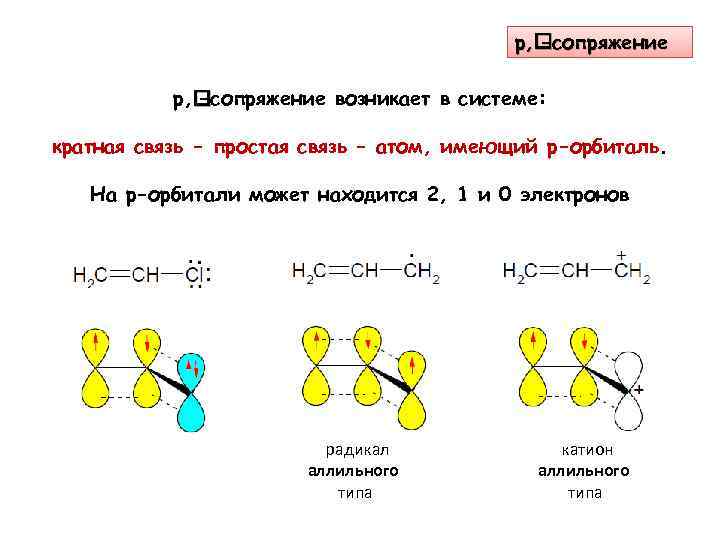 р, -сопряжение возникает в системе: кратная связь - простая связь - атом, имеющий p-орбиталь. На p-орбитали может находится 2, 1 и 0 электронов радикал аллильного типа катион аллильного типа
р, -сопряжение возникает в системе: кратная связь - простая связь - атом, имеющий p-орбиталь. На p-орбитали может находится 2, 1 и 0 электронов радикал аллильного типа катион аллильного типа
 Поляризация связей. Электронные эффекты: индуктивный, мезомерный. Электронодонорные, электроноакцепторные заместители Атомы в молекуле влияют друг на друга, поляризуя связи. При этом на атомах появляется частичный заряд: или +. Влияние может осуществляться: по системе σ-связей (индуктивный эффект, I-эффект) и по цепи сопряжения (мезомерный эффект, М-эффект)
Поляризация связей. Электронные эффекты: индуктивный, мезомерный. Электронодонорные, электроноакцепторные заместители Атомы в молекуле влияют друг на друга, поляризуя связи. При этом на атомах появляется частичный заряд: или +. Влияние может осуществляться: по системе σ-связей (индуктивный эффект, I-эффект) и по цепи сопряжения (мезомерный эффект, М-эффект)
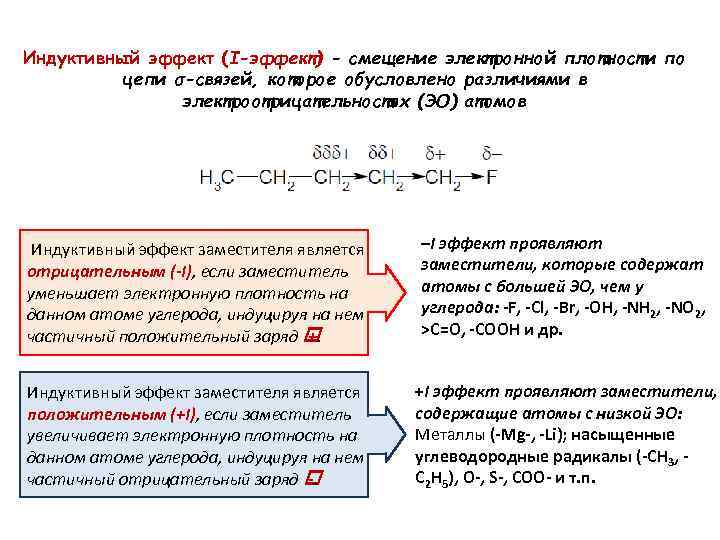 Индуктивный эффект (I-эффект) - смещение электронной плотности по цепи σ-связей, которое обусловлено различиями в электроотрицательностях (ЭО) атомов Индуктивный эффект заместителя является отрицательным (-I), если заместитель уменьшает электронную плотность на данном атоме углерода, индуцируя на нем частичный положительный заряд +. –I эффект проявляют заместители, которые содержат атомы с большей ЭО, чем у углерода: -F, -Cl, -Br, -OH, -NH 2, -NO 2, >C=O, -COOH и др. Индуктивный эффект заместителя является положительным (+I), если заместитель увеличивает электронную плотность на данном атоме углерода, индуцируя на нем частичный отрицательный заряд -. +I эффект проявляют заместители, содержащие атомы с низкой ЭО: Металлы (-Mg-, -Li); насыщенные углеводородные радикалы (-CH 3, C 2 H 5), О-, S-, COO- и т. п.
Индуктивный эффект (I-эффект) - смещение электронной плотности по цепи σ-связей, которое обусловлено различиями в электроотрицательностях (ЭО) атомов Индуктивный эффект заместителя является отрицательным (-I), если заместитель уменьшает электронную плотность на данном атоме углерода, индуцируя на нем частичный положительный заряд +. –I эффект проявляют заместители, которые содержат атомы с большей ЭО, чем у углерода: -F, -Cl, -Br, -OH, -NH 2, -NO 2, >C=O, -COOH и др. Индуктивный эффект заместителя является положительным (+I), если заместитель увеличивает электронную плотность на данном атоме углерода, индуцируя на нем частичный отрицательный заряд -. +I эффект проявляют заместители, содержащие атомы с низкой ЭО: Металлы (-Mg-, -Li); насыщенные углеводородные радикалы (-CH 3, C 2 H 5), О-, S-, COO- и т. п.
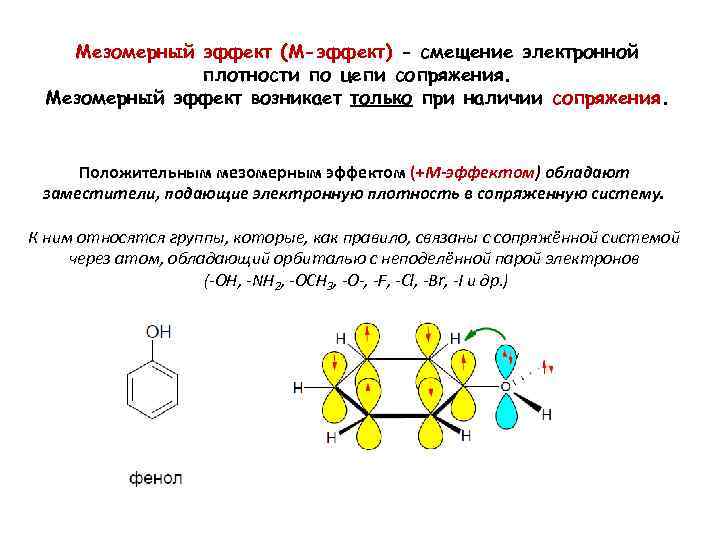 Мезомерный эффект (M-эффект) - смещение электронной плотности по цепи сопряжения. Мезомерный эффект возникает только при наличии сопряжения. Положительным мезомерным эффектом (+М-эффектом) обладают заместители, подающие электронную плотность в сопряженную систему. К ним относятся группы, которые, как правило, связаны с сопряжённой системой через атом, обладающий орбиталью с неподелённой парой электронов (-OH, -NH 2, -OCH 3, -O-, -F, -Cl, -Br, -I и др. )
Мезомерный эффект (M-эффект) - смещение электронной плотности по цепи сопряжения. Мезомерный эффект возникает только при наличии сопряжения. Положительным мезомерным эффектом (+М-эффектом) обладают заместители, подающие электронную плотность в сопряженную систему. К ним относятся группы, которые, как правило, связаны с сопряжённой системой через атом, обладающий орбиталью с неподелённой парой электронов (-OH, -NH 2, -OCH 3, -O-, -F, -Cl, -Br, -I и др. )
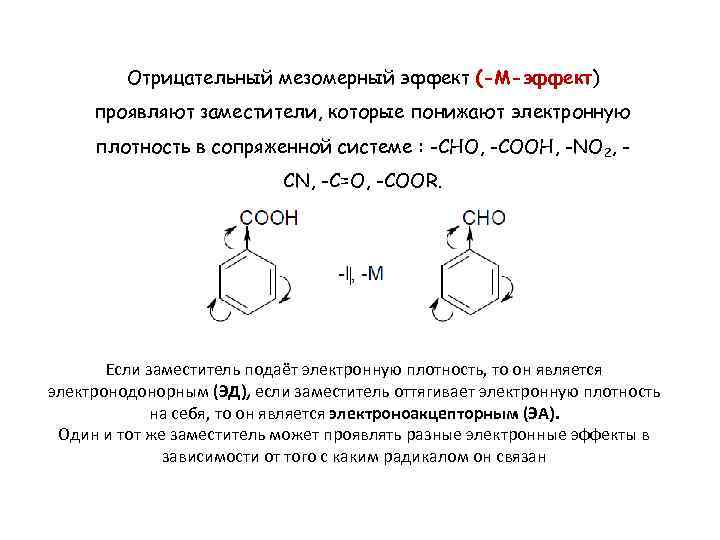 Отрицательный мезомерный эффект (-М-эффект) проявляют заместители, которые понижают электронную плотность в сопряженной системе : -CHO, -COOH, -NO 2, CN, -С=О, -COOR. Если заместитель подаёт электронную плотность, то он является электронодонорным (ЭД), если заместитель оттягивает электронную плотность на себя, то он является электроноакцепторным (ЭА). Один и тот же заместитель может проявлять разные электронные эффекты в зависимости от того с каким радикалом он связан
Отрицательный мезомерный эффект (-М-эффект) проявляют заместители, которые понижают электронную плотность в сопряженной системе : -CHO, -COOH, -NO 2, CN, -С=О, -COOR. Если заместитель подаёт электронную плотность, то он является электронодонорным (ЭД), если заместитель оттягивает электронную плотность на себя, то он является электроноакцепторным (ЭА). Один и тот же заместитель может проявлять разные электронные эффекты в зависимости от того с каким радикалом он связан
 Кислотность и основность органических соединений Существует три теории кислот и оснований: Аррениуса, Брёнстеда-Лоури и Льюиса. В органической химии в основном используется теории Брёнстеда-Лоури и Льюиса. Кислоты Брёнстеда-Лоури – это молекулы или ионы, способные отдавать протон. Основания Брёнстеда-Лоури – это молекулы или ионы, способные принимать протон. Кислота, отдавая протон, превращается в основание, а основание, принимая протон, превращается в кислоту. Сила кислоты количественно выражается через константу диссоциации: чем больше константа диссоциации, тем кислота сильнее.
Кислотность и основность органических соединений Существует три теории кислот и оснований: Аррениуса, Брёнстеда-Лоури и Льюиса. В органической химии в основном используется теории Брёнстеда-Лоури и Льюиса. Кислоты Брёнстеда-Лоури – это молекулы или ионы, способные отдавать протон. Основания Брёнстеда-Лоури – это молекулы или ионы, способные принимать протон. Кислота, отдавая протон, превращается в основание, а основание, принимая протон, превращается в кислоту. Сила кислоты количественно выражается через константу диссоциации: чем больше константа диссоциации, тем кислота сильнее.
 Факторы, влияющие на силу кислоты 1. Чем больше электроотрицательность (ЭО) атома, с которым связан протон, тем больше кислотность Электроотрицательность : C < N < O < F Кислотность: CH 4 < NH 3 < H 2 O < HF 2. Чем больше поляризуемость атома кислотного центра, тем больше кислотность 3. Электроноакцепторные заместители увеличивают кислотность, электронодонорные уменьшают.
Факторы, влияющие на силу кислоты 1. Чем больше электроотрицательность (ЭО) атома, с которым связан протон, тем больше кислотность Электроотрицательность : C < N < O < F Кислотность: CH 4 < NH 3 < H 2 O < HF 2. Чем больше поляризуемость атома кислотного центра, тем больше кислотность 3. Электроноакцепторные заместители увеличивают кислотность, электронодонорные уменьшают.
 Факторы, влияющие на основность 1) Чем больше электроотрицательность атома основного центра, тем сильнее удерживается НЭП, тем меньше основность 2) Чем больше поляризуемость атома основного центра, тем меньше основность. 3) Электронодонорные заместители увеличивают основность, электроноакцепторные уменьшают.
Факторы, влияющие на основность 1) Чем больше электроотрицательность атома основного центра, тем сильнее удерживается НЭП, тем меньше основность 2) Чем больше поляризуемость атома основного центра, тем меньше основность. 3) Электронодонорные заместители увеличивают основность, электроноакцепторные уменьшают.
 Основы теории реакций органических соединений
Основы теории реакций органических соединений
 Химическая реакция представляет собой процесс перераспределения электронов между реагентом и субстратом, сопровождающийся разрывом одних и образованием других связей Химические реакции характеризуются понятиями «региоселективность» и «региоспецифичность» Реакцию считают региоселективной, если преобладает одно из возможных направлений реакции. Реакция называется региоспецифичной, если реализуется только одно направление
Химическая реакция представляет собой процесс перераспределения электронов между реагентом и субстратом, сопровождающийся разрывом одних и образованием других связей Химические реакции характеризуются понятиями «региоселективность» и «региоспецифичность» Реакцию считают региоселективной, если преобладает одно из возможных направлений реакции. Реакция называется региоспецифичной, если реализуется только одно направление
 Механизмы органических реакций Под механизмом реакции подразумевают детальное описание процесса, в результате которого исходные вещества превращаются в продукты реакции Теория активного столкновения (Аррениус) Основа теории активных столкновений: Для того чтобы произошла химическая реакция, молекулы реагентов должны: 1) столкнуться; 2) обладать достаточной энергией - энергией активации, большей, чем энергия разрыва связей; 3) иметь благоприятную ориентацию для скорейшего взаимодействия друг с другом.
Механизмы органических реакций Под механизмом реакции подразумевают детальное описание процесса, в результате которого исходные вещества превращаются в продукты реакции Теория активного столкновения (Аррениус) Основа теории активных столкновений: Для того чтобы произошла химическая реакция, молекулы реагентов должны: 1) столкнуться; 2) обладать достаточной энергией - энергией активации, большей, чем энергия разрыва связей; 3) иметь благоприятную ориентацию для скорейшего взаимодействия друг с другом.
 Теория переходного состояния (1935 год) химическая реакция между началом и завершением претерпевает некое «переходное состояние» , как его назвали Эванс и Поляни, при котором образуется неустойчивый «активированный комплекс» (термин Эйринга). Время существования активированного комплекса равно периоду колебания одной молекулы ( 10 -13 с), поэтому он не может быть обнаружен экспериментально и, соответственно, его нельзя выделить и изучить. Следовательно, доказать истинность теории переходного состояния можно только с помощью расчетов.
Теория переходного состояния (1935 год) химическая реакция между началом и завершением претерпевает некое «переходное состояние» , как его назвали Эванс и Поляни, при котором образуется неустойчивый «активированный комплекс» (термин Эйринга). Время существования активированного комплекса равно периоду колебания одной молекулы ( 10 -13 с), поэтому он не может быть обнаружен экспериментально и, соответственно, его нельзя выделить и изучить. Следовательно, доказать истинность теории переходного состояния можно только с помощью расчетов.
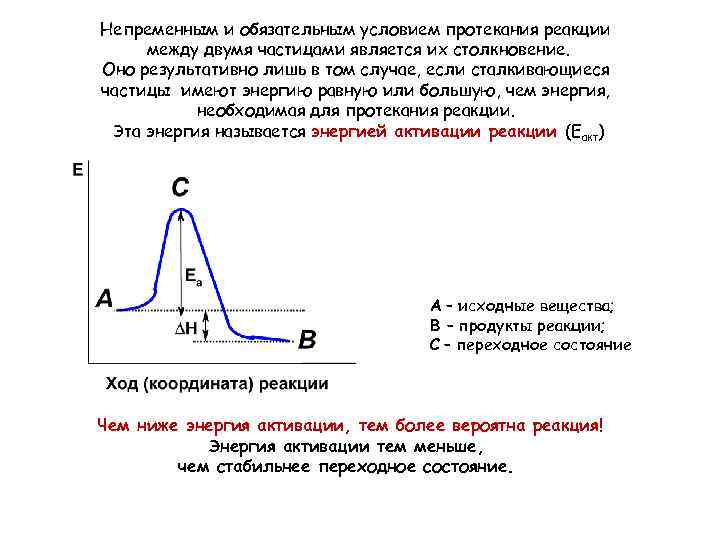 Непременным и обязательным условием протекания реакции между двумя частицами является их столкновение. Оно результативно лишь в том случае, если сталкивающиеся частицы имеют энергию равную или большую, чем энергия, необходимая для протекания реакции. Эта энергия называется энергией активации реакции (Еакт) А – исходные вещества; B – продукты реакции; С – переходное состояние Чем ниже энергия активации, тем более вероятна реакция! Энергия активации тем меньше, чем стабильнее переходное состояние.
Непременным и обязательным условием протекания реакции между двумя частицами является их столкновение. Оно результативно лишь в том случае, если сталкивающиеся частицы имеют энергию равную или большую, чем энергия, необходимая для протекания реакции. Эта энергия называется энергией активации реакции (Еакт) А – исходные вещества; B – продукты реакции; С – переходное состояние Чем ниже энергия активации, тем более вероятна реакция! Энергия активации тем меньше, чем стабильнее переходное состояние.
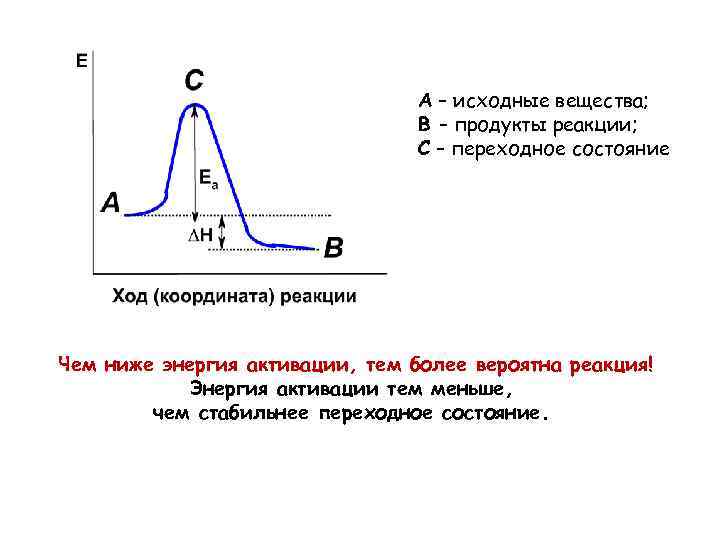 А – исходные вещества; B – продукты реакции; С – переходное состояние Чем ниже энергия активации, тем более вероятна реакция! Энергия активации тем меньше, чем стабильнее переходное состояние.
А – исходные вещества; B – продукты реакции; С – переходное состояние Чем ниже энергия активации, тем более вероятна реакция! Энергия активации тем меньше, чем стабильнее переходное состояние.
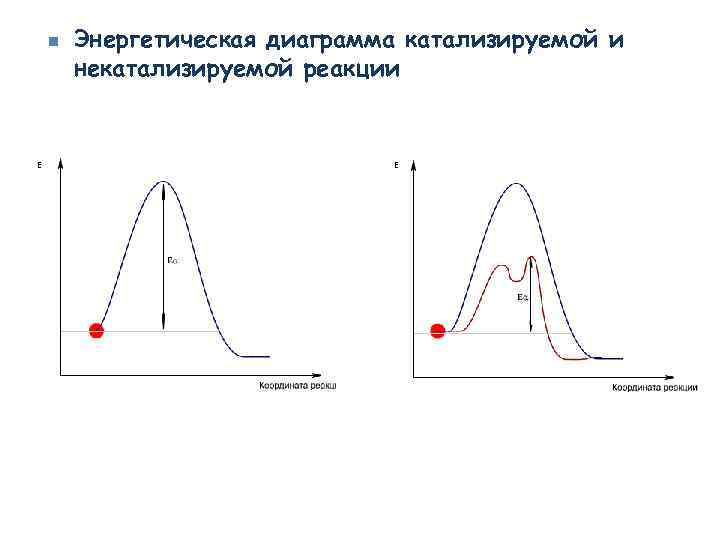 n E Энергетическая диаграмма катализируемой и некатализируемой реакции E
n E Энергетическая диаграмма катализируемой и некатализируемой реакции E
 Молекулярность химических реакций Число молекул, участвующих в элементарном акте химического взаимодействия, называется молекулярностью реакции. По числу молекул, принимающих участие в элементарном акте химического превращения, различают моно- (одно), би- (двух), тримолекулярные реакции. Вероятность соударения одновременно большего числа частиц очень мала; поэтому тримолекулярные реакции очень редки, а 4 х - неизвестны.
Молекулярность химических реакций Число молекул, участвующих в элементарном акте химического взаимодействия, называется молекулярностью реакции. По числу молекул, принимающих участие в элементарном акте химического превращения, различают моно- (одно), би- (двух), тримолекулярные реакции. Вероятность соударения одновременно большего числа частиц очень мала; поэтому тримолекулярные реакции очень редки, а 4 х - неизвестны.
 Типы разрыва ковалентной связи: - гомолитический разрыв связи (гомолиз) – при разрыве ковалентной связи пара электронов поровну делится между двумя атомами. Такие частицы с неспаренным электроном называются радикалами - гетеролитический разрыв связи (гетеролиз) – оба электрона переходят к одному из атомов, принимавших участие в образовании ковалентной связи.
Типы разрыва ковалентной связи: - гомолитический разрыв связи (гомолиз) – при разрыве ковалентной связи пара электронов поровну делится между двумя атомами. Такие частицы с неспаренным электроном называются радикалами - гетеролитический разрыв связи (гетеролиз) – оба электрона переходят к одному из атомов, принимавших участие в образовании ковалентной связи.
 В зависимости от способа разрыва ковалентной связи органические реакции можно разделить на : - гомолитические (радикальные) ; - гетеролитические (ионные); - электроциклические (согласованные, синхронные).
В зависимости от способа разрыва ковалентной связи органические реакции можно разделить на : - гомолитические (радикальные) ; - гетеролитические (ионные); - электроциклические (согласованные, синхронные).
 Свободнорадикальные реакции: - инициируются светом, высокой температурой или свободными радикалами, полученными при разложении других веществ; - протекают в неполярных растворителях или газовой фазе; - являются цепными; - тормозятся веществами, легко реагирующими с радикалами. Ионные реакции: - катализируются кислотами или основаниями и не подвержены действию радикалов; - на ход реакции влияет природа растворителя; - редко проходят в паровой фазе; - на ход реакции не влияют «ловушки радикалов»
Свободнорадикальные реакции: - инициируются светом, высокой температурой или свободными радикалами, полученными при разложении других веществ; - протекают в неполярных растворителях или газовой фазе; - являются цепными; - тормозятся веществами, легко реагирующими с радикалами. Ионные реакции: - катализируются кислотами или основаниями и не подвержены действию радикалов; - на ход реакции влияет природа растворителя; - редко проходят в паровой фазе; - на ход реакции не влияют «ловушки радикалов»
 Классификация реагентов Радикалы (R) – частицы с неспаренным электроном. Нуклеофильные реагенты (Nu) – атакуют атом с пониженной электронной плотностью и отдают свою пару электронов для образования связи с молекулой-партнёром по реакции. Примеры нуклеофилов: H-, F-, Cl-, Br-, I-, OH-, CH 3 O-, H 2 O, спирты, NH 3, амины и т. д. Электрофильные реагенты (Е) – атакуют атом с повышенной электронной плотностью и образуют новую связь за счёт обобществления пары электронов, ранее полностью принадлежавших другой молекуле. Примеры электрофилов: H+, Br+, Cl+, NO 2+ (катион нитрония), карбокатионы, Br 2, Cl 2, SO 3 и т. д.
Классификация реагентов Радикалы (R) – частицы с неспаренным электроном. Нуклеофильные реагенты (Nu) – атакуют атом с пониженной электронной плотностью и отдают свою пару электронов для образования связи с молекулой-партнёром по реакции. Примеры нуклеофилов: H-, F-, Cl-, Br-, I-, OH-, CH 3 O-, H 2 O, спирты, NH 3, амины и т. д. Электрофильные реагенты (Е) – атакуют атом с повышенной электронной плотностью и образуют новую связь за счёт обобществления пары электронов, ранее полностью принадлежавших другой молекуле. Примеры электрофилов: H+, Br+, Cl+, NO 2+ (катион нитрония), карбокатионы, Br 2, Cl 2, SO 3 и т. д.
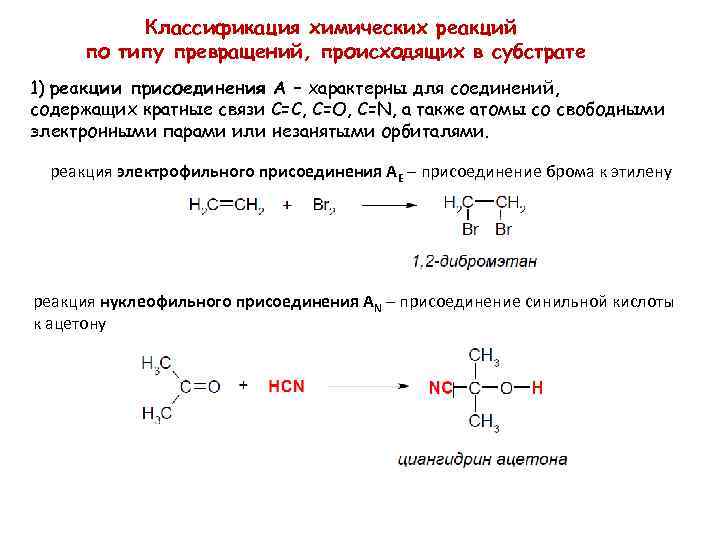 Классификация химических реакций по типу превращений, происходящих в субстрате 1) реакции присоединения А – характерны для соединений, содержащих кратные связи С=С, С=О, C=N, а также атомы со свободными электронными парами или незанятыми орбиталями. реакция электрофильного присоединения AE – присоединение брома к этилену реакция нуклеофильного присоединения AN – присоединение синильной кислоты к ацетону
Классификация химических реакций по типу превращений, происходящих в субстрате 1) реакции присоединения А – характерны для соединений, содержащих кратные связи С=С, С=О, C=N, а также атомы со свободными электронными парами или незанятыми орбиталями. реакция электрофильного присоединения AE – присоединение брома к этилену реакция нуклеофильного присоединения AN – присоединение синильной кислоты к ацетону
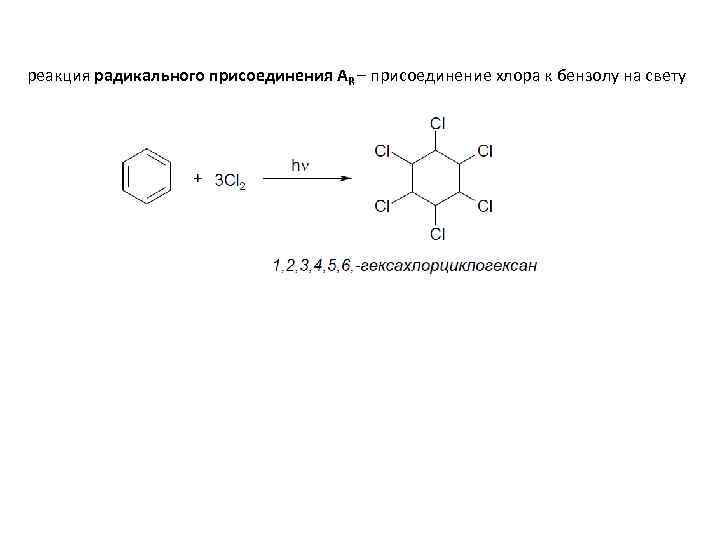 реакция радикального присоединения AR – присоединение хлора к бензолу на свету
реакция радикального присоединения AR – присоединение хлора к бензолу на свету
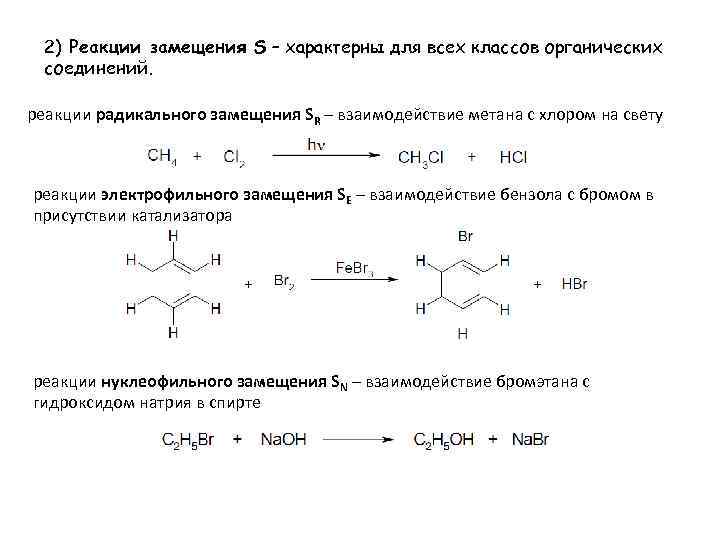 2) Реакции замещения S – характерны для всех классов органических соединений. реакции радикального замещения SR – взаимодействие метана с хлором на свету реакции электрофильного замещения SE – взаимодействие бензола с бромом в присутствии катализатора реакции нуклеофильного замещения SN – взаимодействие бромэтана с гидроксидом натрия в спирте
2) Реакции замещения S – характерны для всех классов органических соединений. реакции радикального замещения SR – взаимодействие метана с хлором на свету реакции электрофильного замещения SE – взаимодействие бензола с бромом в присутствии катализатора реакции нуклеофильного замещения SN – взаимодействие бромэтана с гидроксидом натрия в спирте
 3) Реакции отщепления (элиминирования) особенно характерны для орг. соединений, содержащих электроотрицательные заместители. Элиминирование обычно приводит к образованию кратной связи 4) Перегруппировки (межмолекулярные и внутримолекулярные) часто встречаются среди ненасыщенных соединений и их производных. 5) ОВР. Это реакции, сопровождающиеся изменением степени окисления атомов, входящих в состав реагирующих веществ, в результате перемещения электронов от восстановителя к окислителю
3) Реакции отщепления (элиминирования) особенно характерны для орг. соединений, содержащих электроотрицательные заместители. Элиминирование обычно приводит к образованию кратной связи 4) Перегруппировки (межмолекулярные и внутримолекулярные) часто встречаются среди ненасыщенных соединений и их производных. 5) ОВР. Это реакции, сопровождающиеся изменением степени окисления атомов, входящих в состав реагирующих веществ, в результате перемещения электронов от восстановителя к окислителю
 59
59
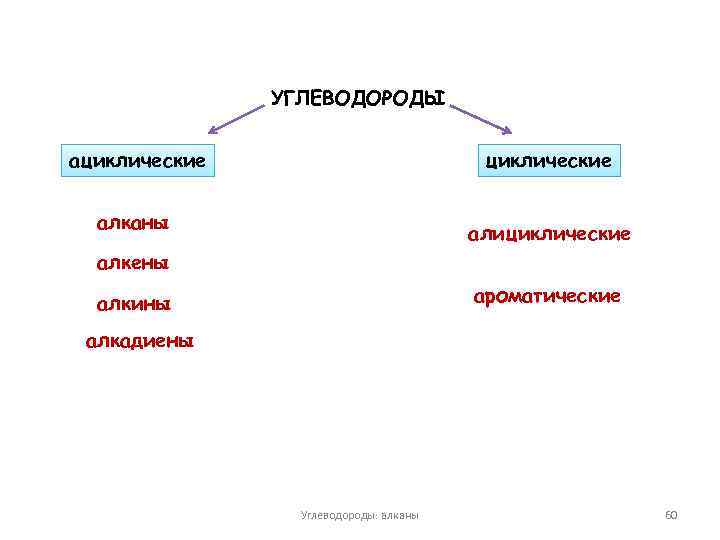 УГЛЕВОДОРОДЫ ациклические алканы алициклические алкены ароматические алкины алкадиены Углеводороды: алканы 60
УГЛЕВОДОРОДЫ ациклические алканы алициклические алкены ароматические алкины алкадиены Углеводороды: алканы 60
 Насыщенные углеводороды (алканы) Способы получения: а) промышленные – перегонка и крекинг нефтепродуктов б) лабораторные: 1) Восстановление галогеналканов 2) Гидрирование алкенов и алкинов Углеводороды: алканы 61
Насыщенные углеводороды (алканы) Способы получения: а) промышленные – перегонка и крекинг нефтепродуктов б) лабораторные: 1) Восстановление галогеналканов 2) Гидрирование алкенов и алкинов Углеводороды: алканы 61
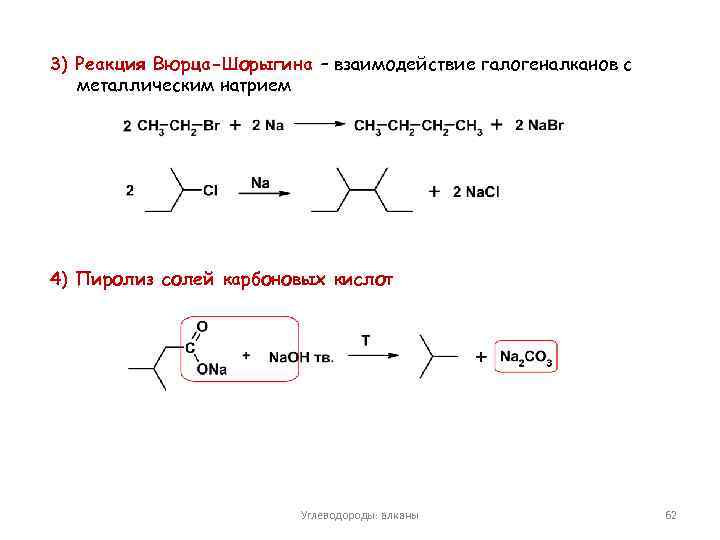 3) Реакция Вюрца-Шорыгина – взаимодействие галогеналканов с металлическим натрием 4) Пиролиз солей карбоновых кислот Углеводороды: алканы 62
3) Реакция Вюрца-Шорыгина – взаимодействие галогеналканов с металлическим натрием 4) Пиролиз солей карбоновых кислот Углеводороды: алканы 62
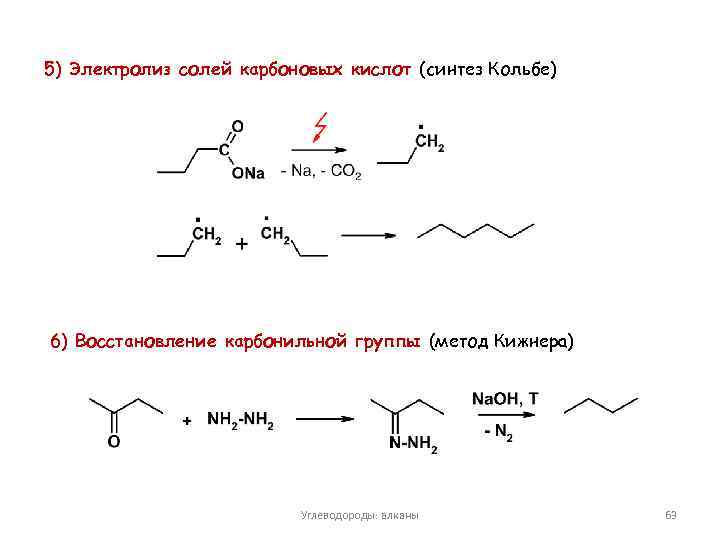 5) Электролиз солей карбоновых кислот (синтез Кольбе) 6) Восстановление карбонильной группы (метод Кижнера) Углеводороды: алканы 63
5) Электролиз солей карбоновых кислот (синтез Кольбе) 6) Восстановление карбонильной группы (метод Кижнера) Углеводороды: алканы 63
 Химические свойства алканов В ряду алканов характерны реакции замещения, а именно, реакции радикального замещения SR) 1) 2) 3) 4) 5) Галогенирование SR; Сульфохлорирование SR; Нитрование SR; Дегидрирование; Окисление Углеводороды: алканы 64
Химические свойства алканов В ряду алканов характерны реакции замещения, а именно, реакции радикального замещения SR) 1) 2) 3) 4) 5) Галогенирование SR; Сульфохлорирование SR; Нитрование SR; Дегидрирование; Окисление Углеводороды: алканы 64
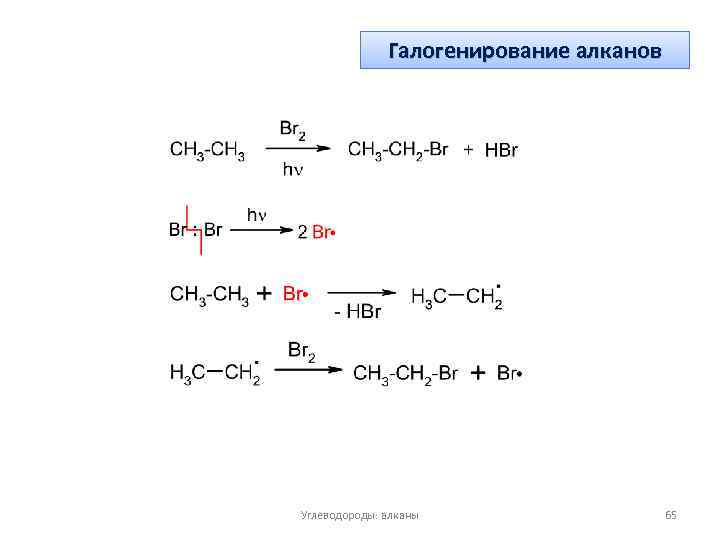 Галогенирование алканов Углеводороды: алканы 65
Галогенирование алканов Углеводороды: алканы 65
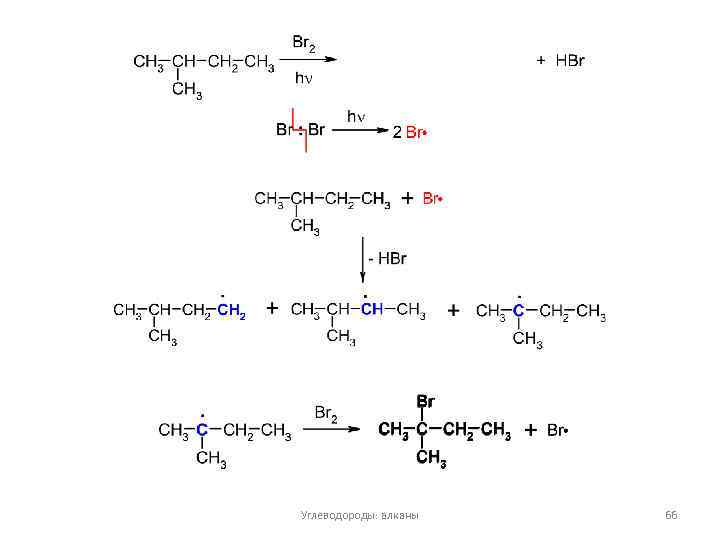 Углеводороды: алканы 66
Углеводороды: алканы 66
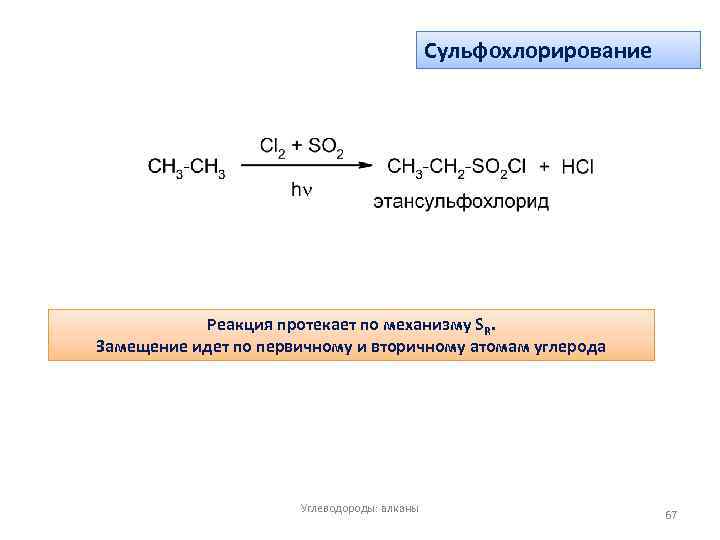 Сульфохлорирование Реакция протекает по механизму SR. Замещение идет по первичному и вторичному атомам углерода Углеводороды: алканы 67
Сульфохлорирование Реакция протекает по механизму SR. Замещение идет по первичному и вторичному атомам углерода Углеводороды: алканы 67
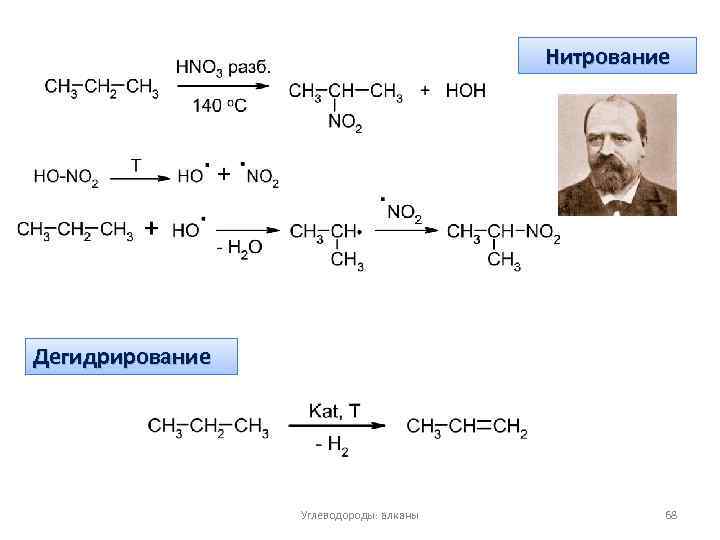 Нитрование Дегидрирование Углеводороды: алканы 68
Нитрование Дегидрирование Углеводороды: алканы 68


