1_введение-классификация(43).ppt
- Количество слайдов: 39
 ОРГАНИЧЕСКАЯ ХИМИЯ КОНСТАНТИНОВА ОЛЬГА ВИТАЛЬЕВНА
ОРГАНИЧЕСКАЯ ХИМИЯ КОНСТАНТИНОВА ОЛЬГА ВИТАЛЬЕВНА
 Литература основная: 1. Органическая химия: Учебник для вузов в 2 кн. (Под ред. Н. А. Тюкавкиной) - М. : Дрофа, 2002 или более поздние издания. 2. Грандберг И. И. Органическая химия. - М. : Дрофа, 2001 (или Грандберг И. Л. Органическая химия. - М. : Высшая школа, 1987. ) 3. Терней А. . Современная органическая химия в 2 т. Пер. с англ. - М. , Мир, 1981 4. Райлс А. , Смит К. , Уорд Р. Основы органической химии. Пер. с англ. - М. : Мир, 1982.
Литература основная: 1. Органическая химия: Учебник для вузов в 2 кн. (Под ред. Н. А. Тюкавкиной) - М. : Дрофа, 2002 или более поздние издания. 2. Грандберг И. И. Органическая химия. - М. : Дрофа, 2001 (или Грандберг И. Л. Органическая химия. - М. : Высшая школа, 1987. ) 3. Терней А. . Современная органическая химия в 2 т. Пер. с англ. - М. , Мир, 1981 4. Райлс А. , Смит К. , Уорд Р. Основы органической химии. Пер. с англ. - М. : Мир, 1982.
 ДОПОЛНИТЕЛЬНАЯ ЛИТЕРАТУРА: 1. Ельницкий А. П. Номенклатура органических соединений. Сборник упражнений. - Минск: «Сэр. Вит» , 2003 2. Ельницкий А. П. , Ильина Н. А, Козырьков Ю. Ю. , Матюшенков Е. А. , Бубель О. Н, Шевчук Т. А. , Асташко Д. А. , Райман М. В. Задачи и упражнения по органической химии. ч. 1. - Минск: БГУ, 2007. 3. Тюкавкина Н. А. , Бауков Ю. И. Биоорганическая химия. - М. : Медицина. 1991 4. Тейлор Г. Основы органической химии. Пер. с англ. - М. : Мир, 1989 5. Моррисон Р. , Бойд Р. Органическая химия. Пер. с англ. - М. : Мир, 1974.
ДОПОЛНИТЕЛЬНАЯ ЛИТЕРАТУРА: 1. Ельницкий А. П. Номенклатура органических соединений. Сборник упражнений. - Минск: «Сэр. Вит» , 2003 2. Ельницкий А. П. , Ильина Н. А, Козырьков Ю. Ю. , Матюшенков Е. А. , Бубель О. Н, Шевчук Т. А. , Асташко Д. А. , Райман М. В. Задачи и упражнения по органической химии. ч. 1. - Минск: БГУ, 2007. 3. Тюкавкина Н. А. , Бауков Ю. И. Биоорганическая химия. - М. : Медицина. 1991 4. Тейлор Г. Основы органической химии. Пер. с англ. - М. : Мир, 1989 5. Моррисон Р. , Бойд Р. Органическая химия. Пер. с англ. - М. : Мир, 1974.
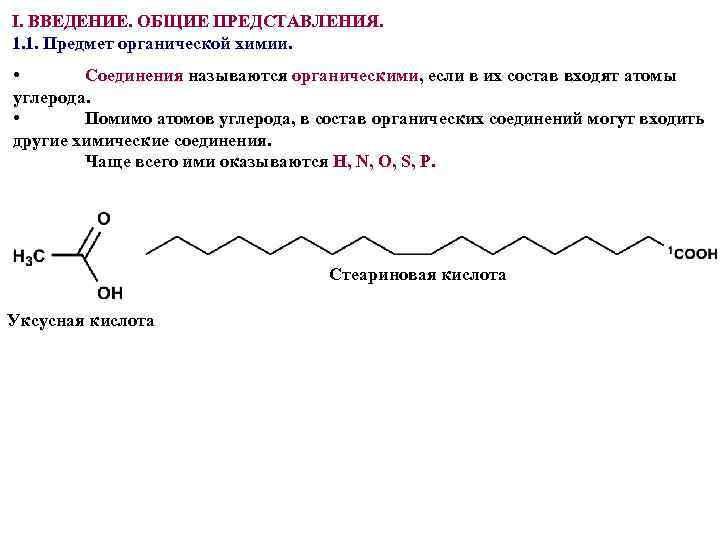 I. ВВЕДЕНИЕ. ОБЩИЕ ПРЕДСТАВЛЕНИЯ. 1. 1. Предмет органической химии. • Соединения называются органическими, если в их состав входят атомы углерода. • Помимо атомов углерода, в состав органических соединений могут входить другие химические соединения. Чаще всего ими оказываются H, N, O, S, P. Стеариновая кислота Уксусная кислота
I. ВВЕДЕНИЕ. ОБЩИЕ ПРЕДСТАВЛЕНИЯ. 1. 1. Предмет органической химии. • Соединения называются органическими, если в их состав входят атомы углерода. • Помимо атомов углерода, в состав органических соединений могут входить другие химические соединения. Чаще всего ими оказываются H, N, O, S, P. Стеариновая кислота Уксусная кислота
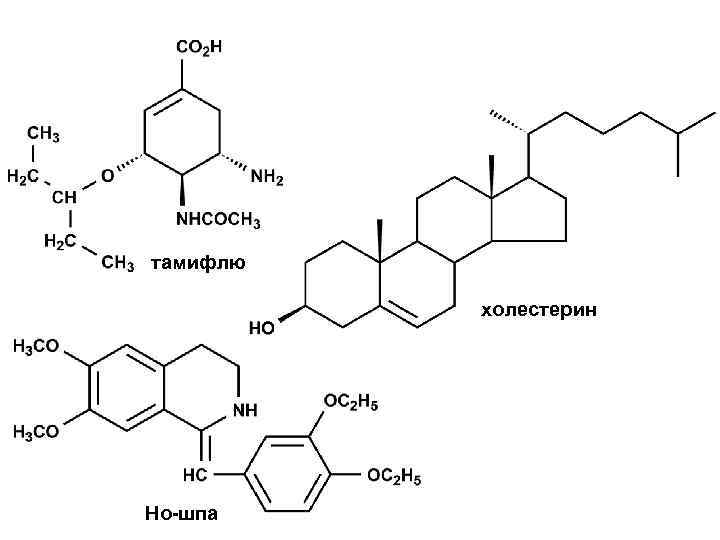 тамифлю холестерин Но-шпа
тамифлю холестерин Но-шпа
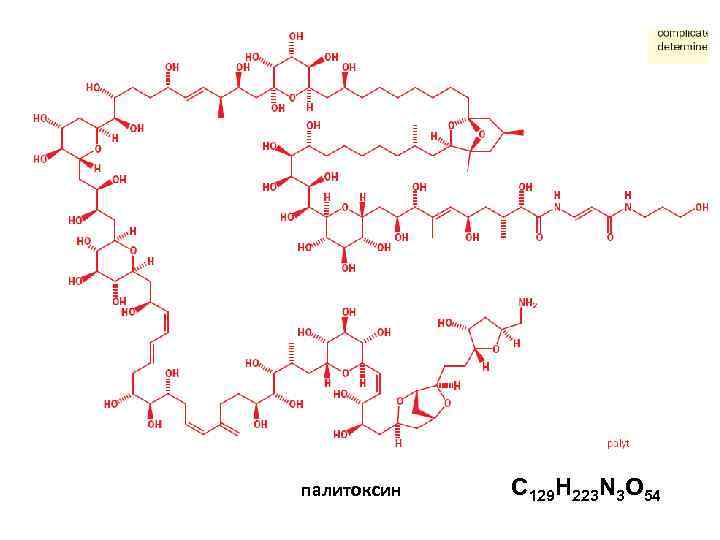 палитоксин C 129 H 223 N 3 O 54
палитоксин C 129 H 223 N 3 O 54
 ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ В ПРИРОДЕ Органические молекулы лежат в основе всех живых организмов: ДНК, РНК, АТФ, белки, ферменты, рецепторы, углеводы, жиры, нейромедиаторы и др.
ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ В ПРИРОДЕ Органические молекулы лежат в основе всех живых организмов: ДНК, РНК, АТФ, белки, ферменты, рецепторы, углеводы, жиры, нейромедиаторы и др.
 Основные источники органических веществ – это нефть, уголь, газ, древесина. Множество синтетических органических соединений производится промышленностью для использования в самых разных отраслях человеческой деятельности: • горючее для различных двигателей • полимерные материалы (каучуки, пластмассы, волокна, пленки, лаки, клеи и т. д. ) • поверхностно-активные вещества • красители • средства защиты растений • лекарственные препараты • ароматизаторы, красители, стабилизаторы для пищевой и косметической продукции • парфюмерные вещества и т. п.
Основные источники органических веществ – это нефть, уголь, газ, древесина. Множество синтетических органических соединений производится промышленностью для использования в самых разных отраслях человеческой деятельности: • горючее для различных двигателей • полимерные материалы (каучуки, пластмассы, волокна, пленки, лаки, клеи и т. д. ) • поверхностно-активные вещества • красители • средства защиты растений • лекарственные препараты • ароматизаторы, красители, стабилизаторы для пищевой и косметической продукции • парфюмерные вещества и т. п.
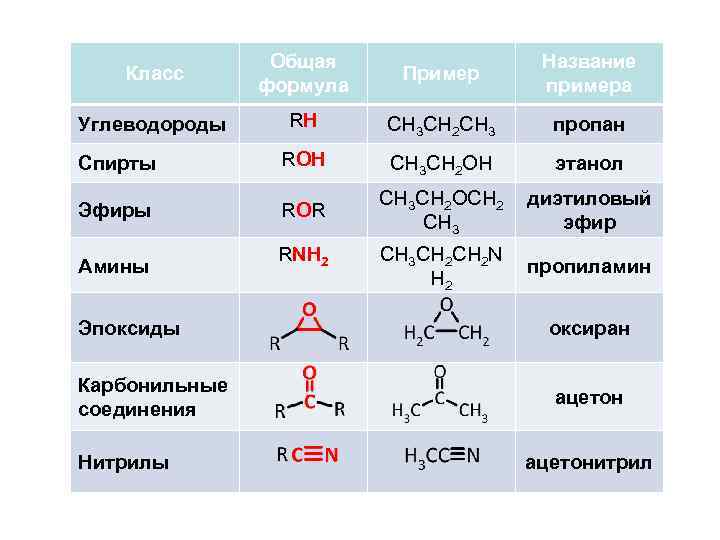 Класс Общая формула Пример Название примера Углеводороды RH CH 3 CH 2 CH 3 пропан Спирты ROH CH 3 CH 2 OH этанол Эфиры ROR CH 3 CH 2 OCH 2 CH 3 диэтиловый эфир Амины RNH 2 CH 3 CH 2 N H 2 пропиламин Эпоксиды Карбонильные соединения Нитрилы оксиран ацетонитрил
Класс Общая формула Пример Название примера Углеводороды RH CH 3 CH 2 CH 3 пропан Спирты ROH CH 3 CH 2 OH этанол Эфиры ROR CH 3 CH 2 OCH 2 CH 3 диэтиловый эфир Амины RNH 2 CH 3 CH 2 N H 2 пропиламин Эпоксиды Карбонильные соединения Нитрилы оксиран ацетонитрил
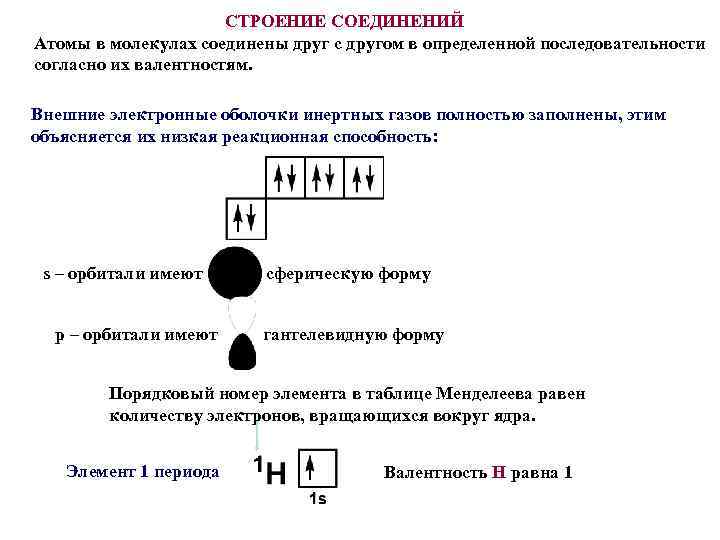 СТРОЕНИЕ СОЕДИНЕНИЙ Атомы в молекулах соединены друг с другом в определенной последовательности согласно их валентностям. Внешние электронные оболочки инертных газов полностью заполнены, этим объясняется их низкая реакционная способность: s – орбитали имеют p – орбитали имеют сферическую форму гантелевидную форму Порядковый номер элемента в таблице Менделеева равен количеству электронов, вращающихся вокруг ядра. Элемент 1 периода Валентность H равна 1
СТРОЕНИЕ СОЕДИНЕНИЙ Атомы в молекулах соединены друг с другом в определенной последовательности согласно их валентностям. Внешние электронные оболочки инертных газов полностью заполнены, этим объясняется их низкая реакционная способность: s – орбитали имеют p – орбитали имеют сферическую форму гантелевидную форму Порядковый номер элемента в таблице Менделеева равен количеству электронов, вращающихся вокруг ядра. Элемент 1 периода Валентность H равна 1
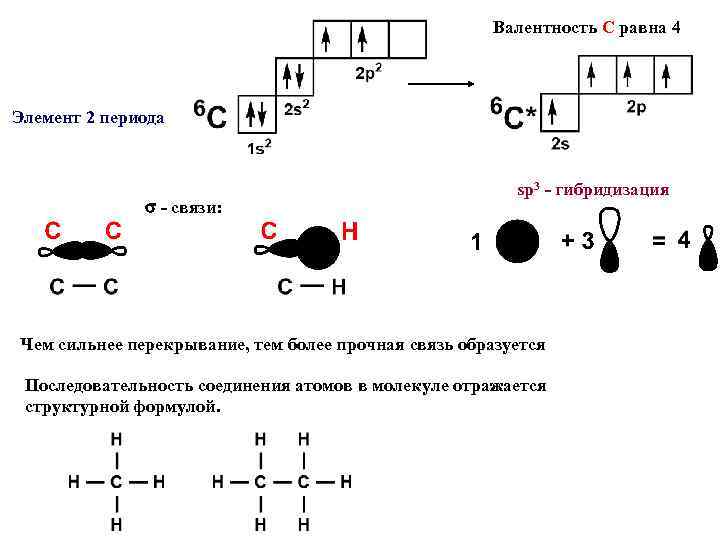 Валентность С равна 4 Элемент 2 периода - связи: sp 3 - гибридизация Чем сильнее перекрывание, тем более прочная связь образуется Последовательность соединения атомов в молекуле отражается структурной формулой.
Валентность С равна 4 Элемент 2 периода - связи: sp 3 - гибридизация Чем сильнее перекрывание, тем более прочная связь образуется Последовательность соединения атомов в молекуле отражается структурной формулой.
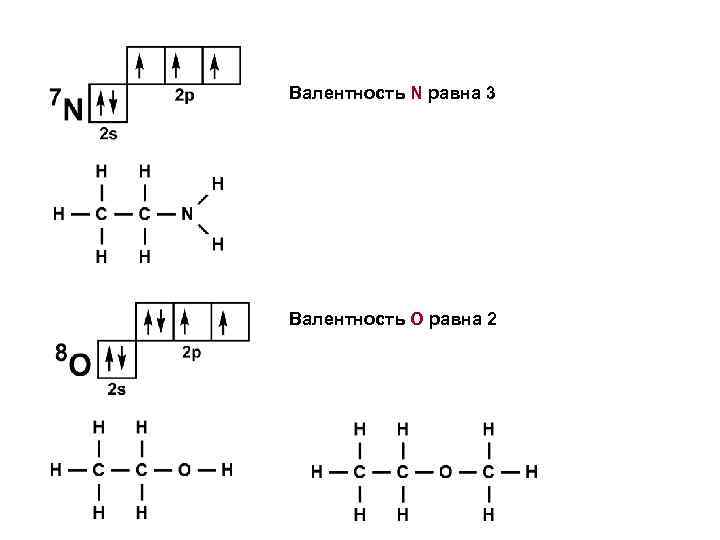 Валентность N равна 3 Валентность О равна 2
Валентность N равна 3 Валентность О равна 2
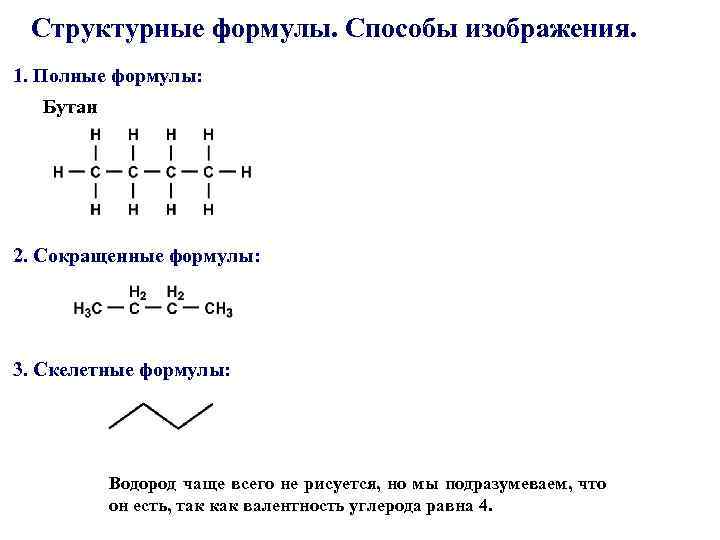 Структурные формулы. Способы изображения. 1. Полные формулы: Бутан 2. Сокращенные формулы: 3. Скелетные формулы: Водород чаще всего не рисуется, но мы подразумеваем, что он есть, так как валентность углерода равна 4.
Структурные формулы. Способы изображения. 1. Полные формулы: Бутан 2. Сокращенные формулы: 3. Скелетные формулы: Водород чаще всего не рисуется, но мы подразумеваем, что он есть, так как валентность углерода равна 4.
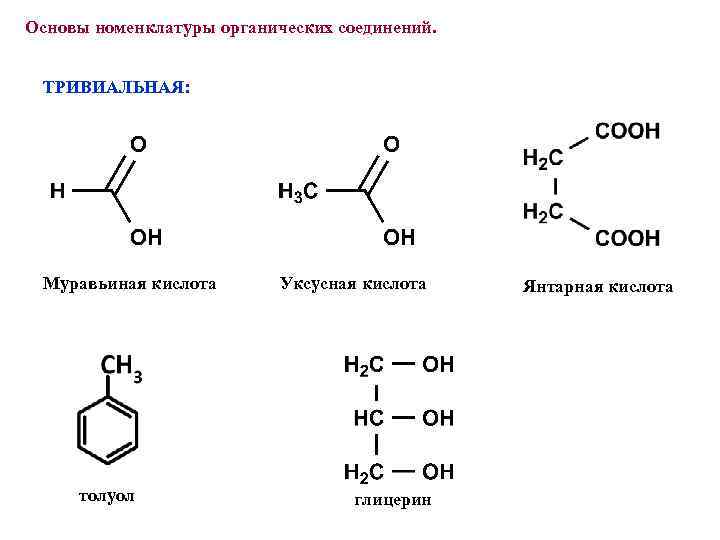 Основы номенклатуры органических соединений. ТРИВИАЛЬНАЯ: Муравьиная кислота толуол Уксусная кислота глицерин Янтарная кислота
Основы номенклатуры органических соединений. ТРИВИАЛЬНАЯ: Муравьиная кислота толуол Уксусная кислота глицерин Янтарная кислота
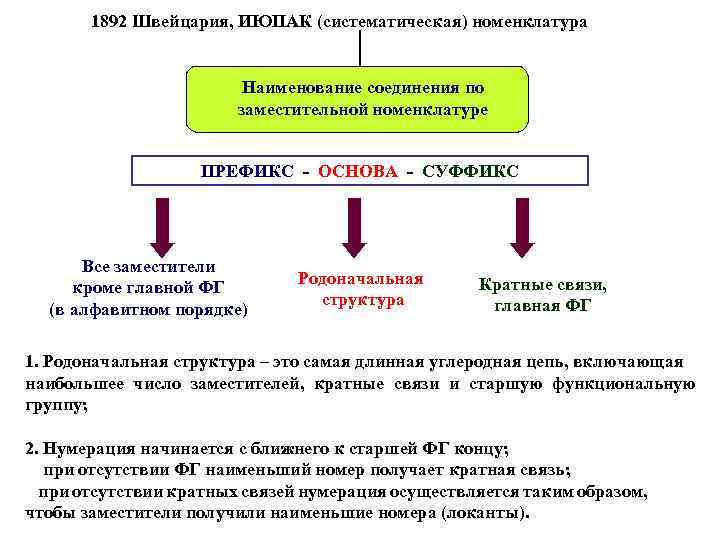 1892 Швейцария, ИЮПАК (систематическая) номенклатура Наименование соединения по заместительной номенклатуре ПРЕФИКС - ОСНОВА - СУФФИКС Все заместители кроме главной ФГ (в алфавитном порядке) Родоначальная структура Кратные связи, главная ФГ 1. Родоначальная структура – это самая длинная углеродная цепь, включающая наибольшее число заместителей, кратные связи и старшую функциональную группу; 2. Нумерация начинается с ближнего к старшей ФГ концу; при отсутствии ФГ наименьший номер получает кратная связь; при отсутствии кратных связей нумерация осуществляется таким образом, чтобы заместители получили наименьшие номера (локанты).
1892 Швейцария, ИЮПАК (систематическая) номенклатура Наименование соединения по заместительной номенклатуре ПРЕФИКС - ОСНОВА - СУФФИКС Все заместители кроме главной ФГ (в алфавитном порядке) Родоначальная структура Кратные связи, главная ФГ 1. Родоначальная структура – это самая длинная углеродная цепь, включающая наибольшее число заместителей, кратные связи и старшую функциональную группу; 2. Нумерация начинается с ближнего к старшей ФГ концу; при отсутствии ФГ наименьший номер получает кратная связь; при отсутствии кратных связей нумерация осуществляется таким образом, чтобы заместители получили наименьшие номера (локанты).
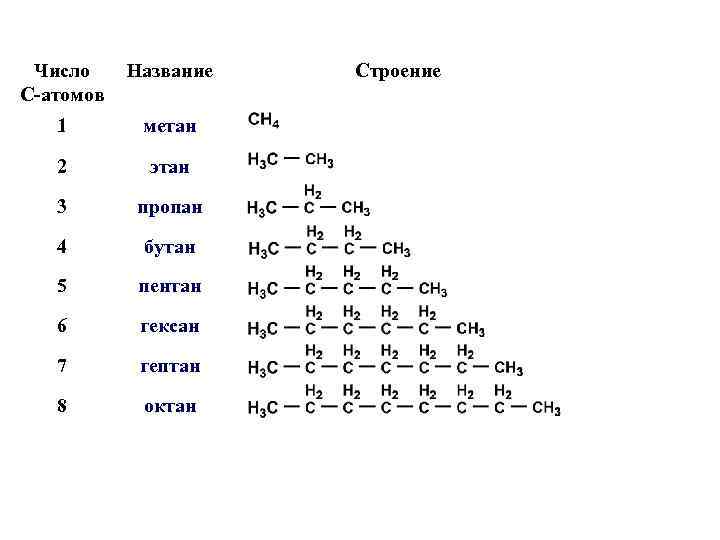 Число С-атомов Название 1 метан 2 этан 3 пропан 4 бутан 5 пентан 6 гексан 7 гептан 8 октан Строение
Число С-атомов Название 1 метан 2 этан 3 пропан 4 бутан 5 пентан 6 гексан 7 гептан 8 октан Строение
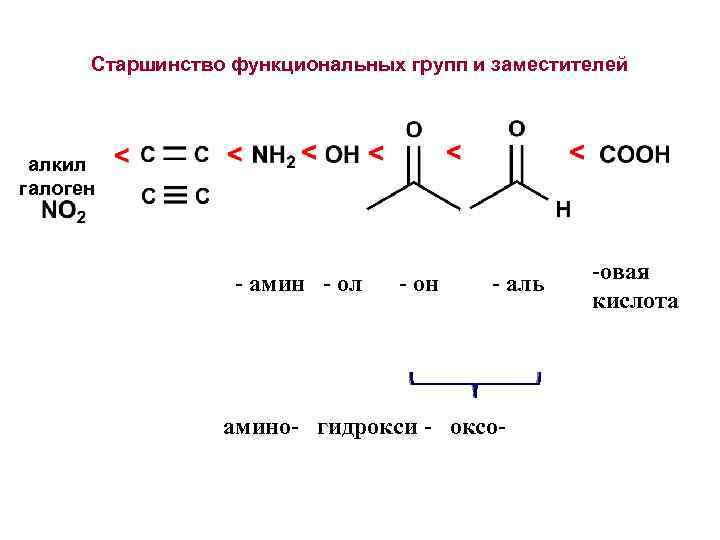 Старшинство функциональных групп и заместителей алкил галоген - амин - ол - он - аль амино- гидрокси - оксо- -овая кислота
Старшинство функциональных групп и заместителей алкил галоген - амин - ол - он - аль амино- гидрокси - оксо- -овая кислота
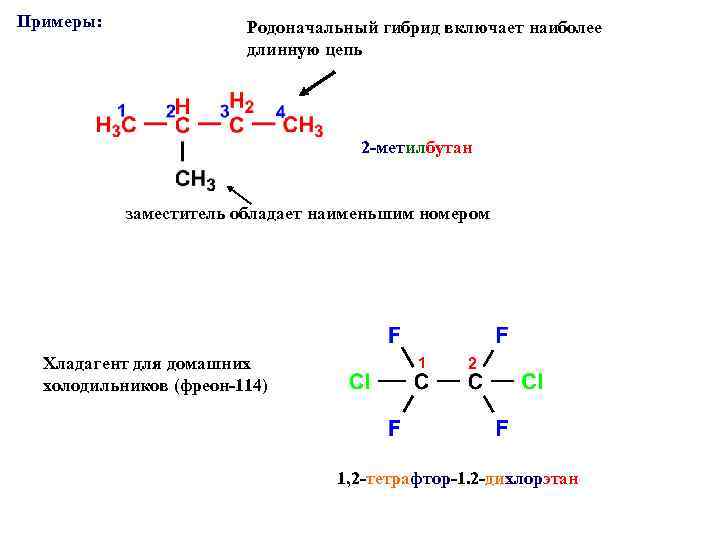 Примеры: Родоначальный гибрид включает наиболее длинную цепь 2 -метилбутан заместитель обладает наименьшим номером Хладагент для домашних холодильников (фреон-114) 1, 2 -тетрафтор-1. 2 -дихлорэтан
Примеры: Родоначальный гибрид включает наиболее длинную цепь 2 -метилбутан заместитель обладает наименьшим номером Хладагент для домашних холодильников (фреон-114) 1, 2 -тетрафтор-1. 2 -дихлорэтан
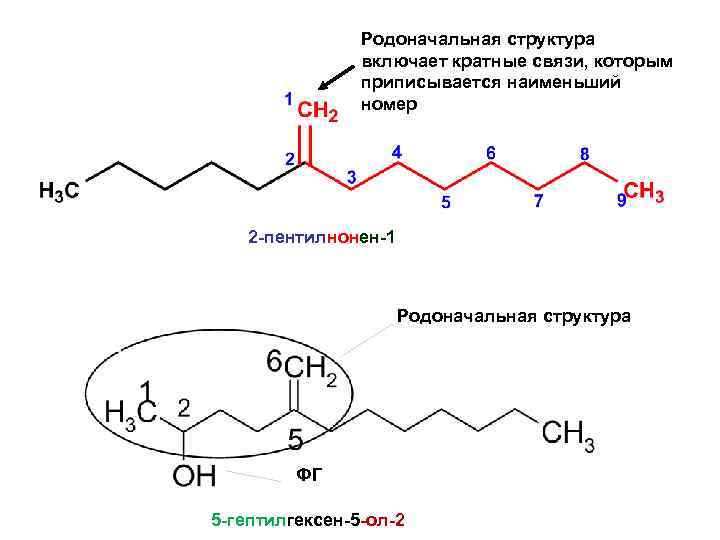 Родоначальная структура включает кратные связи, которым приписывается наименьший номер 2 -пентилнонен-1 Родоначальная структура ФГ 5 -гептилгексен-5 -ол-2
Родоначальная структура включает кратные связи, которым приписывается наименьший номер 2 -пентилнонен-1 Родоначальная структура ФГ 5 -гептилгексен-5 -ол-2
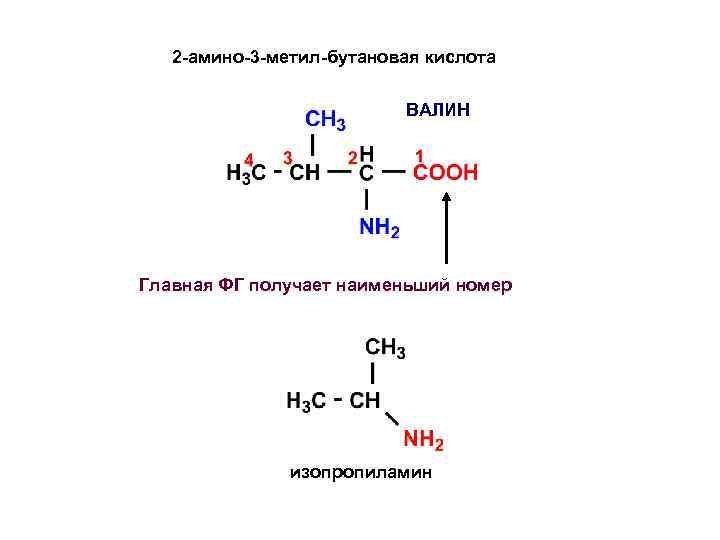 2 -амино-3 -метил-бутановая кислота ВАЛИН Главная ФГ получает наименьший номер изопропиламин
2 -амино-3 -метил-бутановая кислота ВАЛИН Главная ФГ получает наименьший номер изопропиламин
 Изомерия органических соединений. ИЗОМЕРИЯ – явление, заключающееся в существовании химических соединений (изомеров), одинаковых по составу и молекулярной массе, но различающихся по строению или расположению атомов в пространстве и, вследствие этого, по свойствам. Типы изомерии в органической химии: • структурная • пространственная (стереоизомерия) СТРУКТУРНАЯ ИЗОМЕРИЯ: Структурные изомеры – соединения одинакового качественного и количественного состава, отличающиеся порядком соединения атомов между собой, т. е химическим строением. Структурные изомеры различаются физическими свойствами, реакционной способностью.
Изомерия органических соединений. ИЗОМЕРИЯ – явление, заключающееся в существовании химических соединений (изомеров), одинаковых по составу и молекулярной массе, но различающихся по строению или расположению атомов в пространстве и, вследствие этого, по свойствам. Типы изомерии в органической химии: • структурная • пространственная (стереоизомерия) СТРУКТУРНАЯ ИЗОМЕРИЯ: Структурные изомеры – соединения одинакового качественного и количественного состава, отличающиеся порядком соединения атомов между собой, т. е химическим строением. Структурные изомеры различаются физическими свойствами, реакционной способностью.
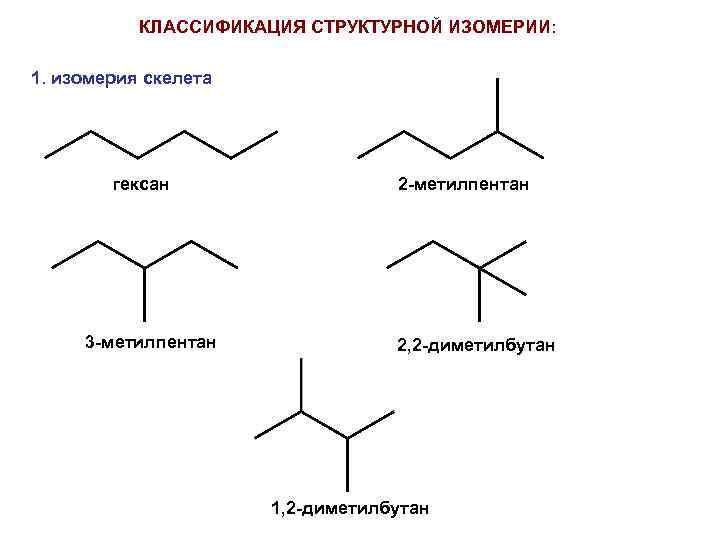 КЛАССИФИКАЦИЯ СТРУКТУРНОЙ ИЗОМЕРИИ: 1. изомерия скелета гексан 3 -метилпентан 2, 2 -диметилбутан 1, 2 -диметилбутан
КЛАССИФИКАЦИЯ СТРУКТУРНОЙ ИЗОМЕРИИ: 1. изомерия скелета гексан 3 -метилпентан 2, 2 -диметилбутан 1, 2 -диметилбутан
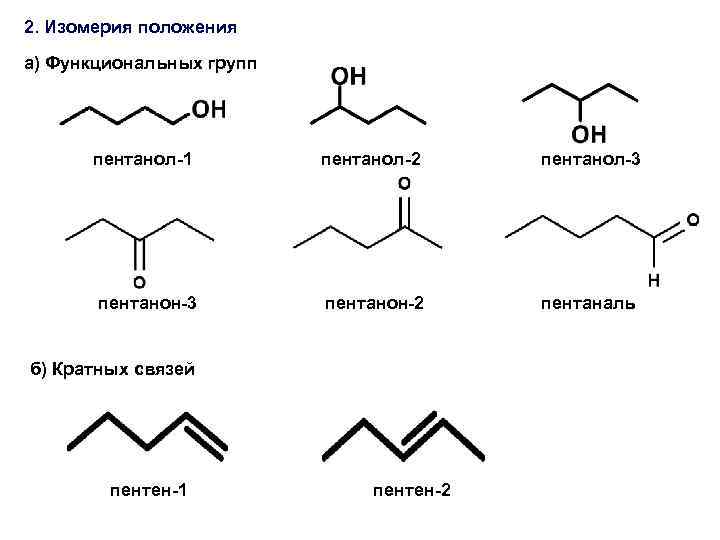 2. Изомерия положения a) Функциональных групп пентанол-1 пентанол-2 пентанол-3 пентанон-2 пентаналь б) Кратных связей пентен-1 пентен-2
2. Изомерия положения a) Функциональных групп пентанол-1 пентанол-2 пентанол-3 пентанон-2 пентаналь б) Кратных связей пентен-1 пентен-2
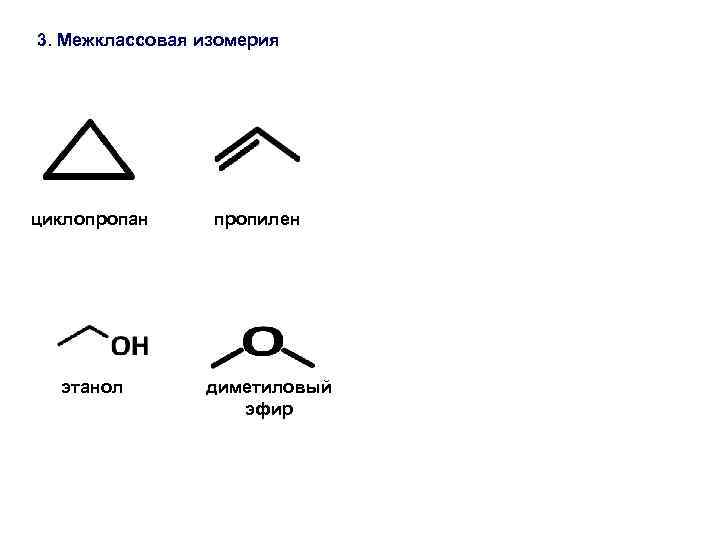 3. Межклассовая изомерия циклопропан этанол пропилен диметиловый эфир
3. Межклассовая изомерия циклопропан этанол пропилен диметиловый эфир
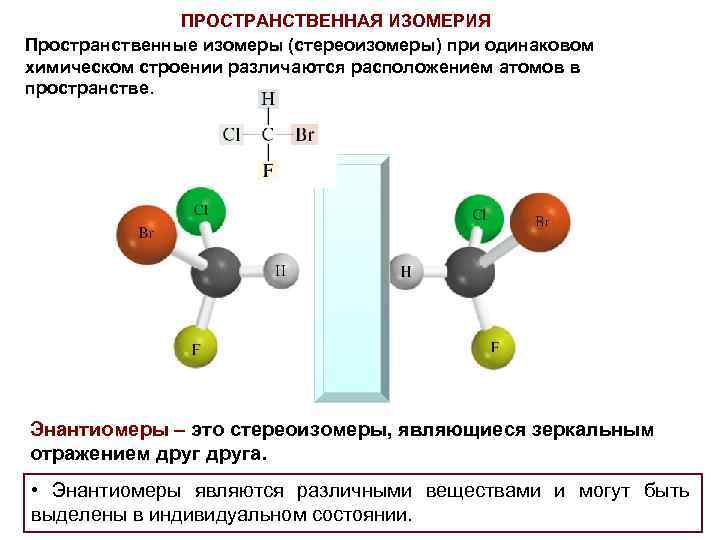 ПРОСТРАНСТВЕННАЯ ИЗОМЕРИЯ Пространственные изомеры (стереоизомеры) при одинаковом химическом строении различаются расположением атомов в пространстве. Энантиомеры – это стереоизомеры, являющиеся зеркальным отражением друга. • Энантиомеры являются различными веществами и могут быть выделены в индивидуальном состоянии.
ПРОСТРАНСТВЕННАЯ ИЗОМЕРИЯ Пространственные изомеры (стереоизомеры) при одинаковом химическом строении различаются расположением атомов в пространстве. Энантиомеры – это стереоизомеры, являющиеся зеркальным отражением друга. • Энантиомеры являются различными веществами и могут быть выделены в индивидуальном состоянии.
 CHEIR (греч. ) – рука Сhiral – хиральный Chirality - хиральность Молекула хиральна, если она не идентична своему зеркальному отражению.
CHEIR (греч. ) – рука Сhiral – хиральный Chirality - хиральность Молекула хиральна, если она не идентична своему зеркальному отражению.
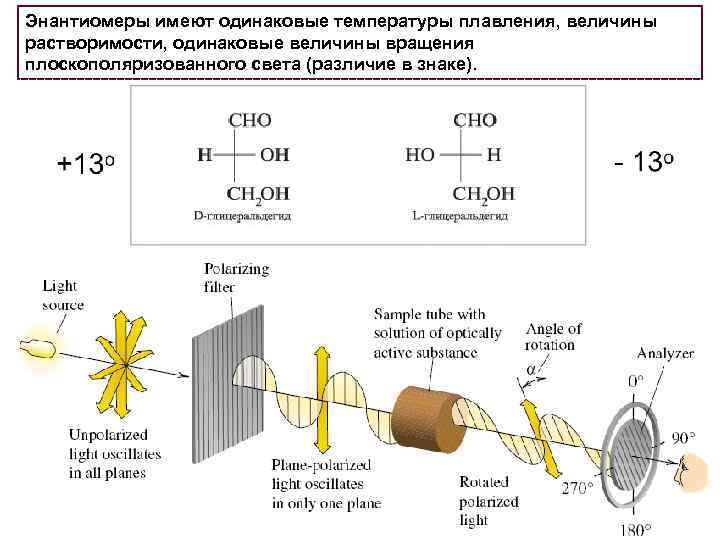 Энантиомеры имеют одинаковые температуры плавления, величины растворимости, одинаковые величины вращения плоскополяризованного света (различие в знаке).
Энантиомеры имеют одинаковые температуры плавления, величины растворимости, одинаковые величины вращения плоскополяризованного света (различие в знаке).
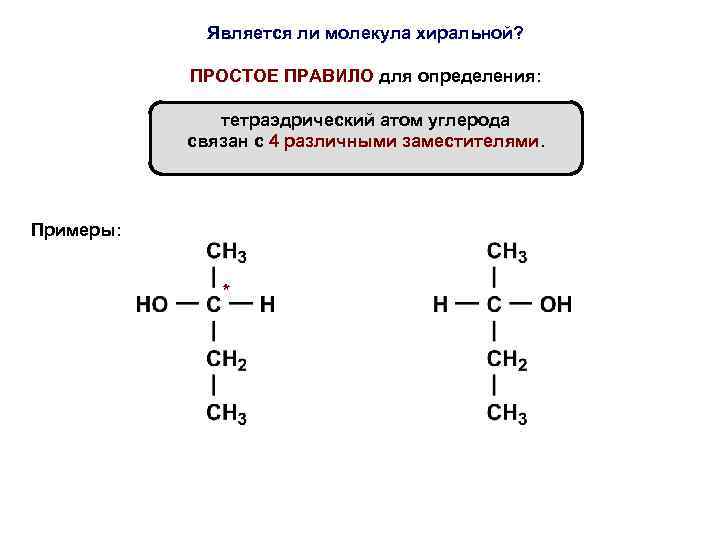 Является ли молекула хиральной? ПРОСТОЕ ПРАВИЛО для определения: тетраэдрический атом углерода связан с 4 различными заместителями. Примеры: *
Является ли молекула хиральной? ПРОСТОЕ ПРАВИЛО для определения: тетраэдрический атом углерода связан с 4 различными заместителями. Примеры: *
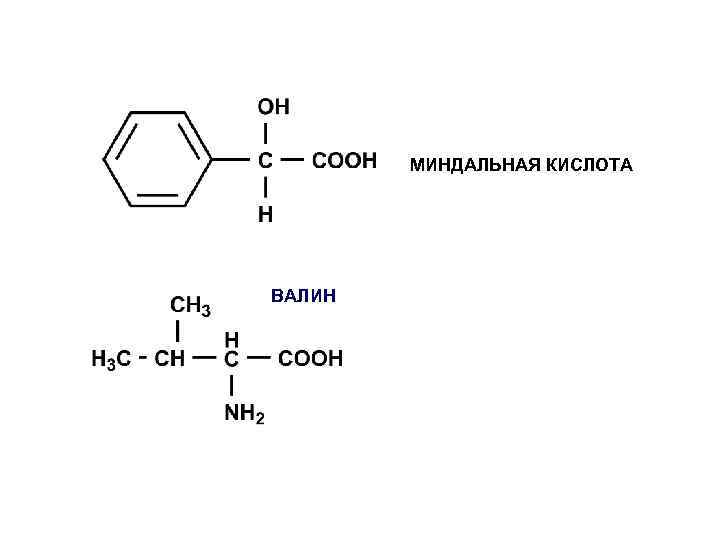 МИНДАЛЬНАЯ КИСЛОТА ВАЛИН
МИНДАЛЬНАЯ КИСЛОТА ВАЛИН
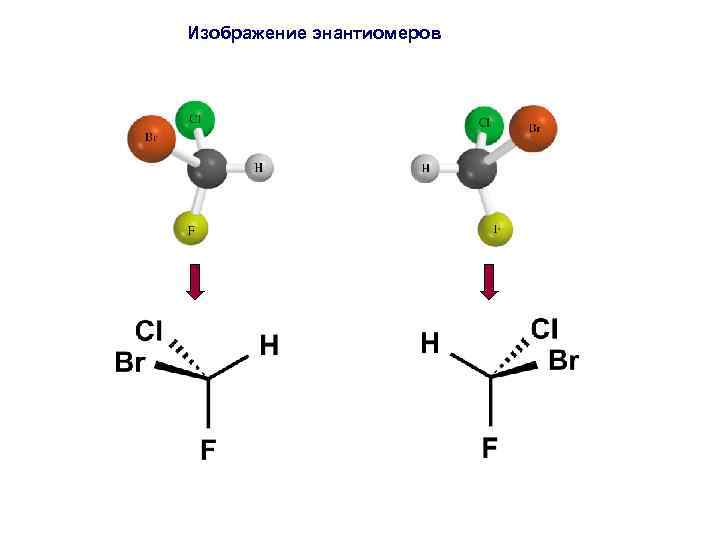 Изображение энантиомеров
Изображение энантиомеров
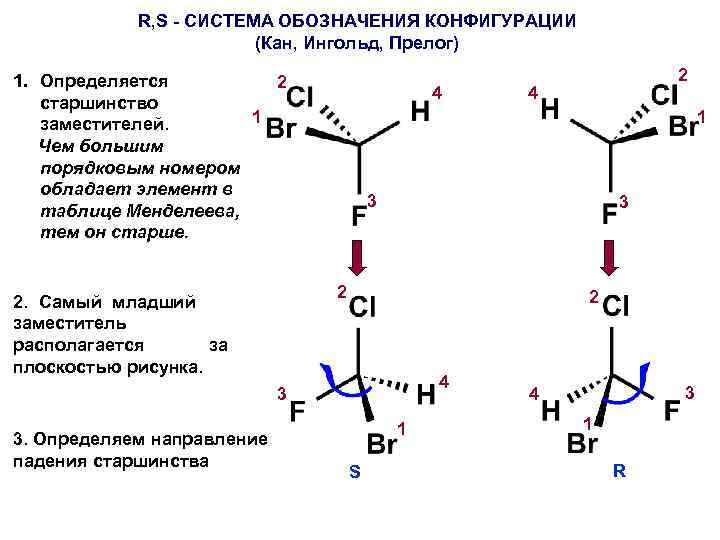 R, S - СИСТЕМА ОБОЗНАЧЕНИЯ КОНФИГУРАЦИИ (Кан, Ингольд, Прелог) 1. Определяется 2 старшинство 1 заместителей. Чем большим порядковым номером обладает элемент в таблице Менделеева, тем он старше. 4 1 3 3 2 4 3 3. Определяем направление падения старшинства 4 2 2. Самый младший заместитель располагается за плоскостью рисунка. 2 1 S 3 4 1 R
R, S - СИСТЕМА ОБОЗНАЧЕНИЯ КОНФИГУРАЦИИ (Кан, Ингольд, Прелог) 1. Определяется 2 старшинство 1 заместителей. Чем большим порядковым номером обладает элемент в таблице Менделеева, тем он старше. 4 1 3 3 2 4 3 3. Определяем направление падения старшинства 4 2 2. Самый младший заместитель располагается за плоскостью рисунка. 2 1 S 3 4 1 R
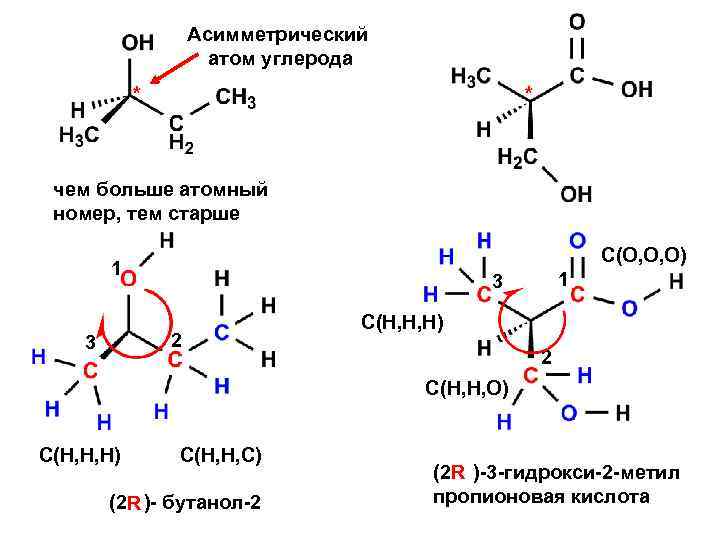 Асимметрический атом углерода * * чем больше атомный номер, тем старше C(O, O, O) 1 2 3 1 3 С(H, H, H) 2 C(H, H, O) С(H, H, H) C(H, H, C) (2 )- бутанол-2 R (2 )-3 -гидрокси-2 -метил R пропионовая кислота
Асимметрический атом углерода * * чем больше атомный номер, тем старше C(O, O, O) 1 2 3 1 3 С(H, H, H) 2 C(H, H, O) С(H, H, H) C(H, H, C) (2 )- бутанол-2 R (2 )-3 -гидрокси-2 -метил R пропионовая кислота
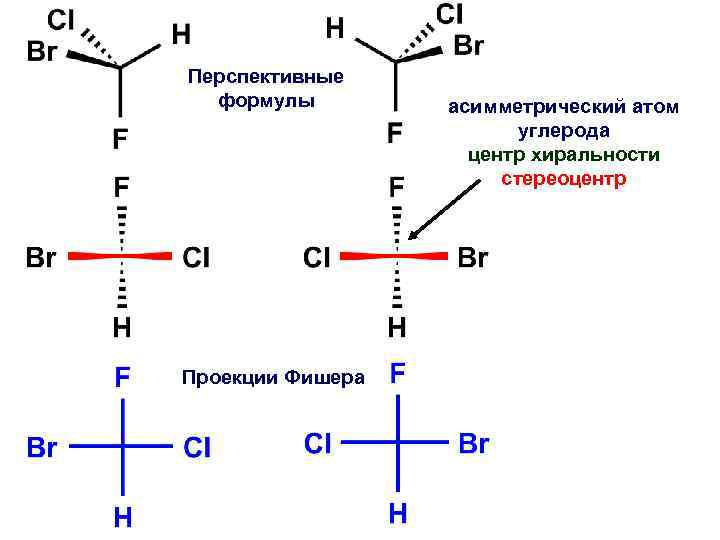 Перспективные формулы Проекции Фишера асимметрический атом углерода центр хиральности стереоцентр
Перспективные формулы Проекции Фишера асимметрический атом углерода центр хиральности стереоцентр
 ОПРЕДЕЛЕНИЕ R/S КОНФИГУРАЦИИ НА ПРОЕКЦИИ ФИШЕРА Операции, не изменяющие конфигурацию стереоцентра: 1. Поворот на 180 о. 2. Четное число перестановок заместителей. Операции, изменяющие конфигурацию стереоцентра противоположную: 1. Поворот на 90 о. 2. Нечетное число перестановок заместителей. на
ОПРЕДЕЛЕНИЕ R/S КОНФИГУРАЦИИ НА ПРОЕКЦИИ ФИШЕРА Операции, не изменяющие конфигурацию стереоцентра: 1. Поворот на 180 о. 2. Четное число перестановок заместителей. Операции, изменяющие конфигурацию стереоцентра противоположную: 1. Поворот на 90 о. 2. Нечетное число перестановок заместителей. на
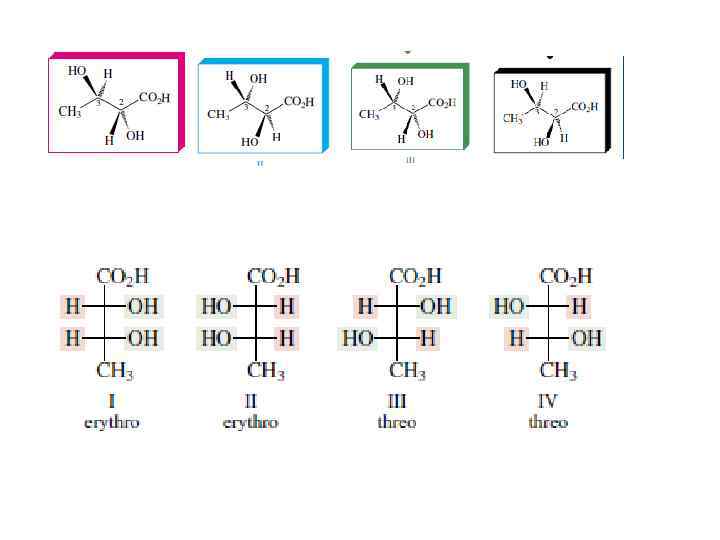
 Молекулы с 1 стереоцентром 2 возможных энантиомера (R и S) Молекулы с n стереоцентрами Все возможные комбинации R и S изомеров 2 n - стереоизомеров
Молекулы с 1 стереоцентром 2 возможных энантиомера (R и S) Молекулы с n стереоцентрами Все возможные комбинации R и S изомеров 2 n - стереоизомеров
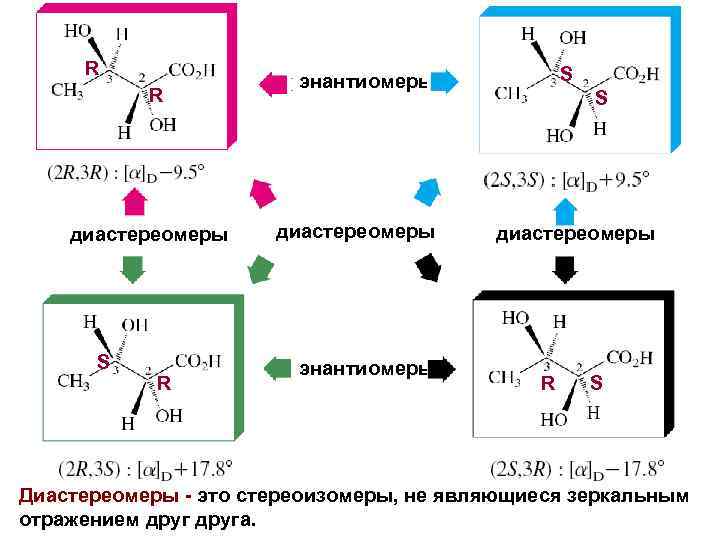 R R диастереомеры S R S энантиомеры диастереомеры энантиомеры S диастереомеры R S Диастереомеры - это стереоизомеры, не являющиеся зеркальным отражением друга.
R R диастереомеры S R S энантиомеры диастереомеры энантиомеры S диастереомеры R S Диастереомеры - это стереоизомеры, не являющиеся зеркальным отражением друга.
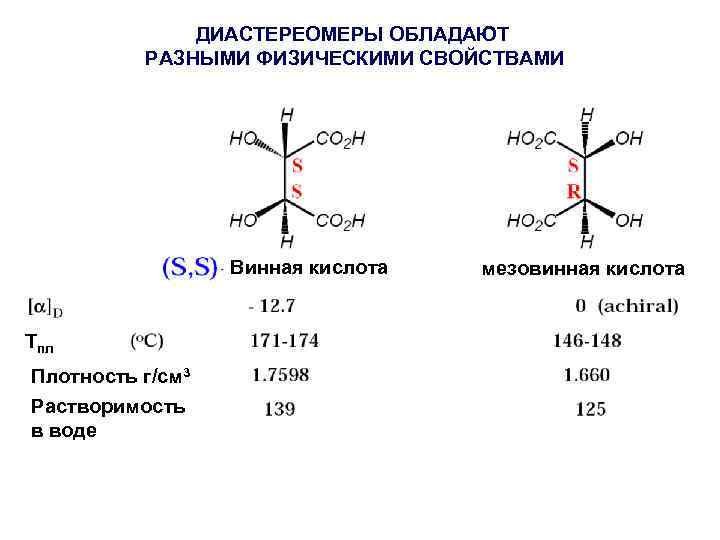 ДИАСТЕРЕОМЕРЫ ОБЛАДАЮТ РАЗНЫМИ ФИЗИЧЕСКИМИ СВОЙСТВАМИ Винная кислота Тпл Плотность г/см 3 Растворимость в воде мезовинная кислота
ДИАСТЕРЕОМЕРЫ ОБЛАДАЮТ РАЗНЫМИ ФИЗИЧЕСКИМИ СВОЙСТВАМИ Винная кислота Тпл Плотность г/см 3 Растворимость в воде мезовинная кислота
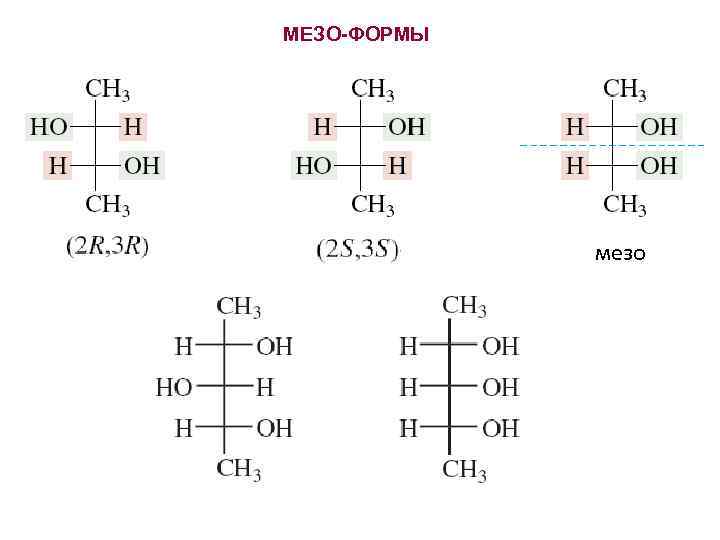 МЕЗО-ФОРМЫ мезо
МЕЗО-ФОРМЫ мезо


