4aff6d9b3185fed3e7516fb2ee5451b5.ppt
- Количество слайдов: 73

Органическая химия http: //www. chem. asu. ru/org/ochem_bio/index. html Лектор: Маркин Вадим Иванович доцент кафедры органической химии, канд. хим. наук E-mail: markin@chem. asu. ru

Преподаватели КАТРАКОВ Игорь Борисович, доцент, канд. хим. наук СИЯНКО Петр Иванович, доцент, канд. хим. наук ЧЕПРАСОВА Марина Юрьевна, ассистент 2

Модульно-рейтинговая технология обучения Модули – 4 Лекции – 20 ч Лабораторные работы – 14 ч Семинары – 14 ч Контрольные работы – 2 ЭКЗАМЕН 3

Модульно-рейтинговая технология обучения Модульная программа (модуль) • самостоятельная работа (выполнение индивидуального задания); • посещение лекций; • индивидуальная консультация у преподавателя; • семинарское занятие; • лабораторный практикум. 4
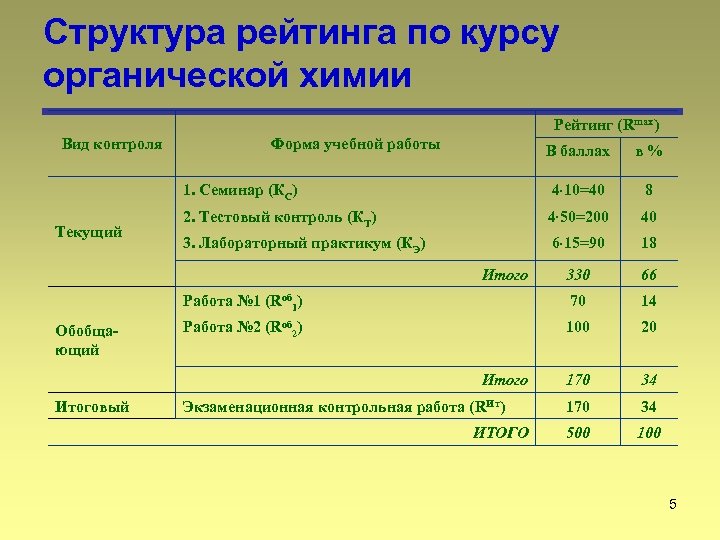
Структура рейтинга по курсу органической химии Рейтинг (Rmax) Вид контроля Форма учебной работы в% 1. Семинар (КС) 4 10=40 8 2. Тестовый контроль (КТ) 4 50=200 40 3. Лабораторный практикум (КЭ) 6 15=90 18 330 66 Работа № 1 (Rоб 1) Текущий В баллах 70 14 Работа № 2 (Rоб 2) 100 20 170 34 500 100 Итого Обобща ющий Итоговый Экзаменационная контрольная работа (RИт) ИТОГО 5
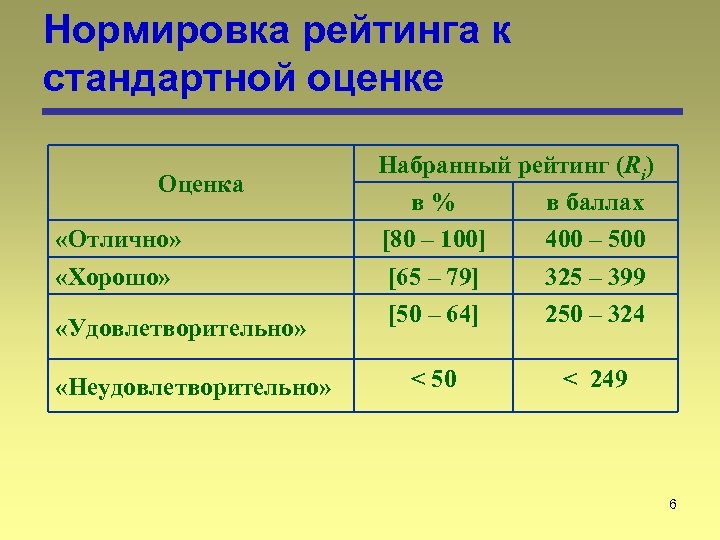
Нормировка рейтинга к стандартной оценке Оценка «Отлично» «Хорошо» «Удовлетворительно» «Неудовлетворительно» Набранный рейтинг (Ri) в% в баллах [80 – 100] 400 – 500 [65 – 79] 325 – 399 [50 – 64] 250 – 324 < 50 < 249 6

Сайт курса «Органическая химия» http: //www. chem. asu. ru/org/ochem_bio/index. html 7

ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ОРГАНИЧЕСКОЙ ХИМИИ 8

Органическая химия в ряду других наук Органическая химия вполне может свести человека с ума. Она создает у меня впечатление девственного тропического леса, полного самых удивительных вещей; из этой чудовищной и безграничной чащи невозможно выбраться и в нее страшно войти. Фридрих Велер (1835) Фридрих Велер (1800 -1882) 9
Органическая химия в ряду других наук 10
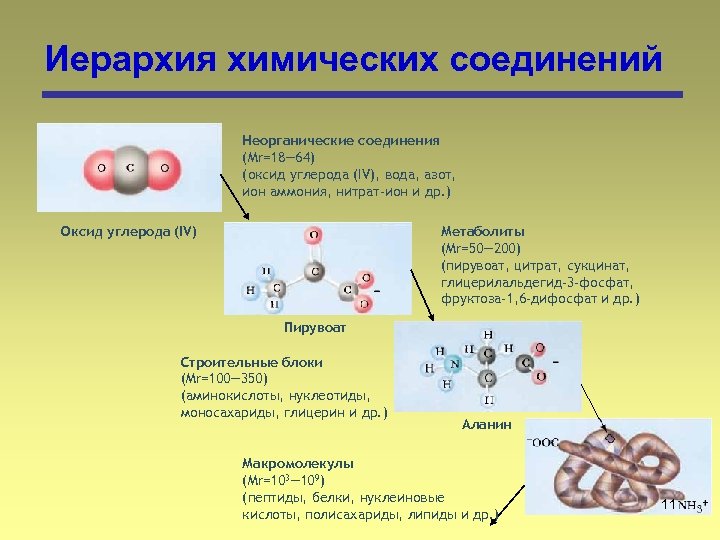
Иерархия химических соединений Неорганические соединения (Mr=18― 64) (оксид углерода (IV), вода, азот, ион аммония, нитрат-ион и др. ) Оксид углерода (IV) Метаболиты (Mr=50― 200) (пирувоат, цитрат, сукцинат, глицерилальдегид-3 -фосфат, фруктоза-1, 6 -дифосфат и др. ) Пирувоат Строительные блоки (Mr=100― 350) (аминокислоты, нуклеотиды, моносахариды, глицерин и др. ) Аланин Макромолекулы (Mr=103― 109) (пептиды, белки, нуклеиновые кислоты, полисахариды, липиды и др. ) 11

Предмет органической химии Органическая химия — химия соединений углерода. Элементы С, Н, О, N (S, галогены) – называют органогенами Органическая химия — химия углеводородов и их производных. 12
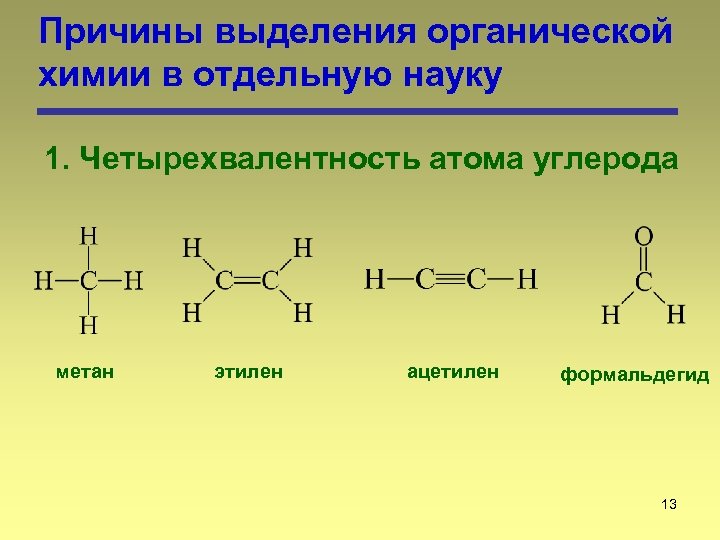
Причины выделения органической химии в отдельную науку 1. Четырехвалентность атома углерода метан этилен ацетилен формальдегид 13
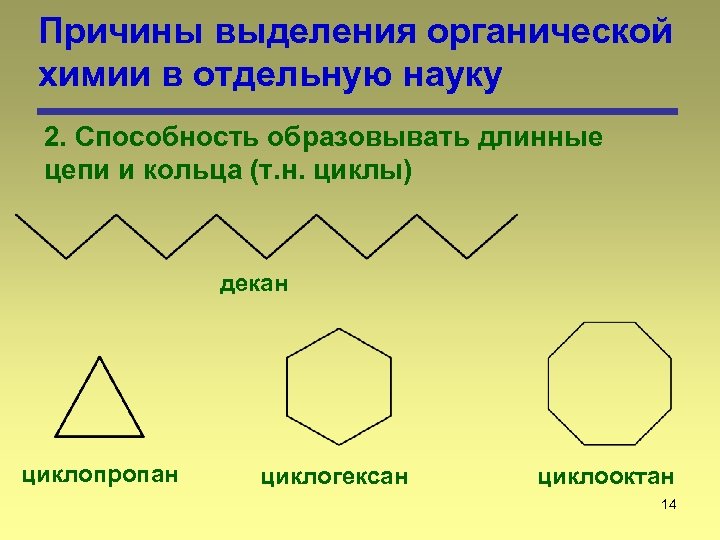
Причины выделения органической химии в отдельную науку 2. Способность образовывать длинные цепи и кольца (т. н. циклы) декан циклопропан циклогексан циклооктан 14
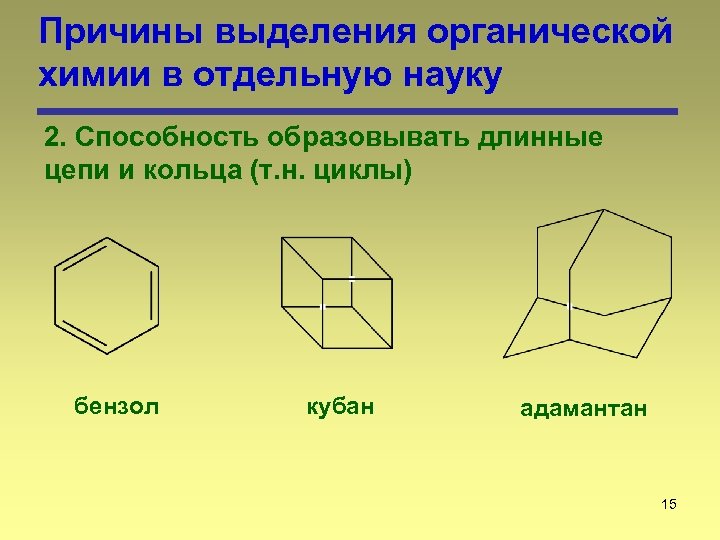
Причины выделения органической химии в отдельную науку 2. Способность образовывать длинные цепи и кольца (т. н. циклы) бензол кубан адамантан 15
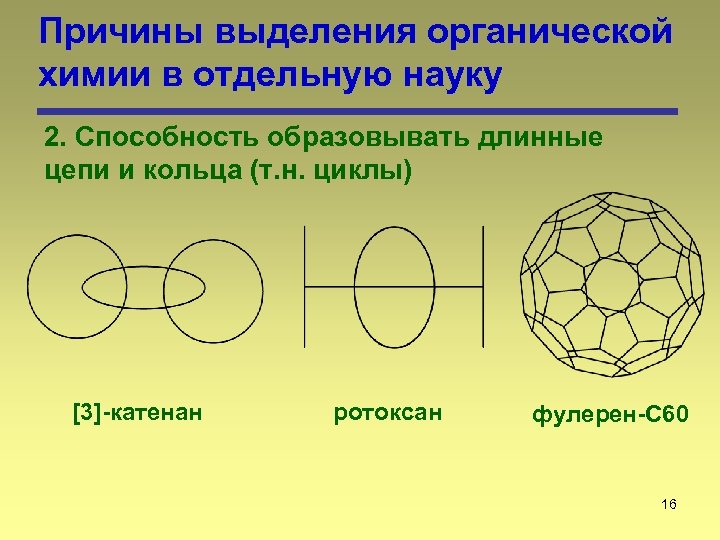
Причины выделения органической химии в отдельную науку 2. Способность образовывать длинные цепи и кольца (т. н. циклы) [3]-катенан ротоксан фулерен-С 60 16

Причины выделения органической химии в отдельную науку 3. Способность образовывать устойчивые или очень устойчивые связи с другими элементами 17
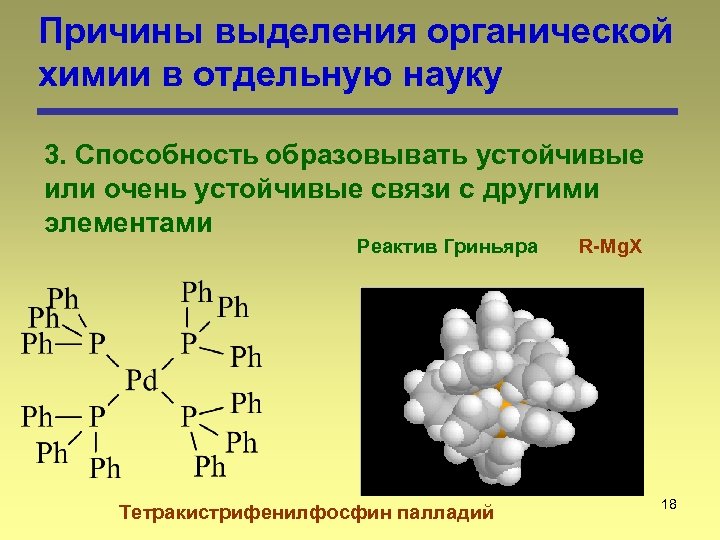
Причины выделения органической химии в отдельную науку 3. Способность образовывать устойчивые или очень устойчивые связи с другими элементами Реактив Гриньяра Тетракистрифенилфосфин палладий R-Mg. X 18

Причины выделения органической химии в отдельную науку 4. Из всех элементов периодической системы именно углерод играет главную и определяющую роль в биологическом мире 19
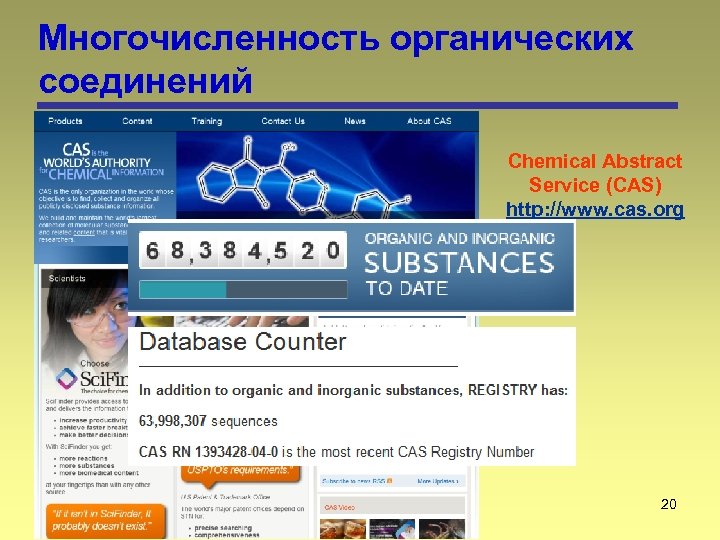
Многочисленность органических соединений Chemical Abstract Service (CAS) http: //www. cas. org 20

Многочисленность органических соединений Палитоксин 10 -7 г 21
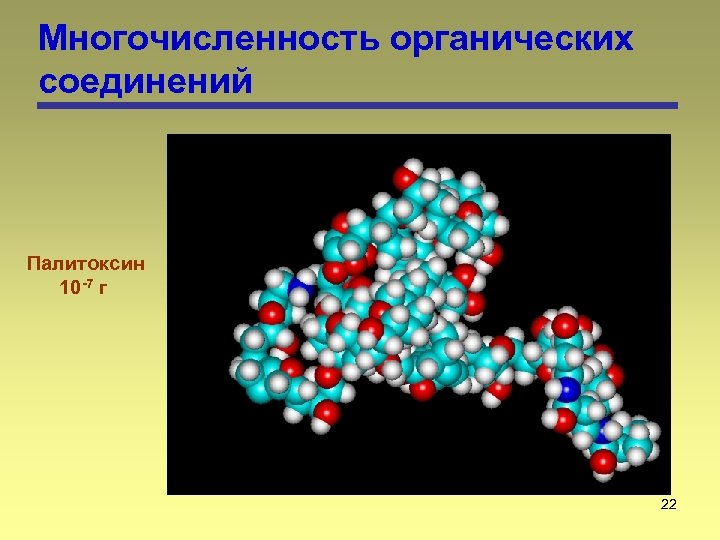
Многочисленность органических соединений Палитоксин 10 -7 г 22
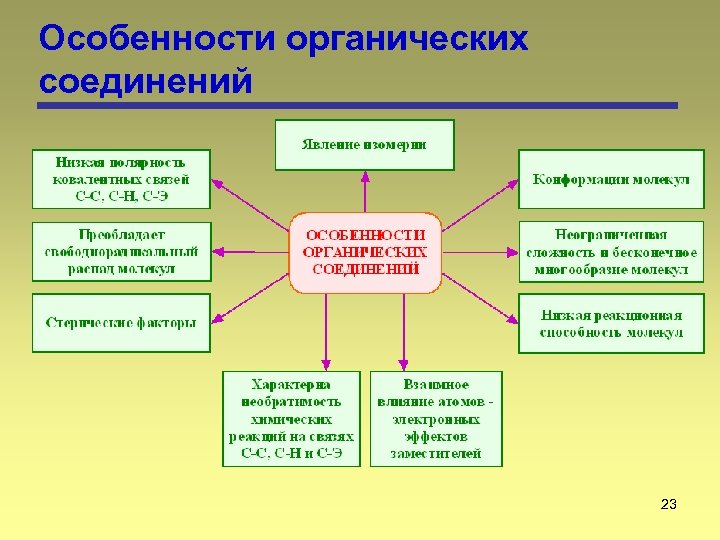
Особенности органических соединений 23
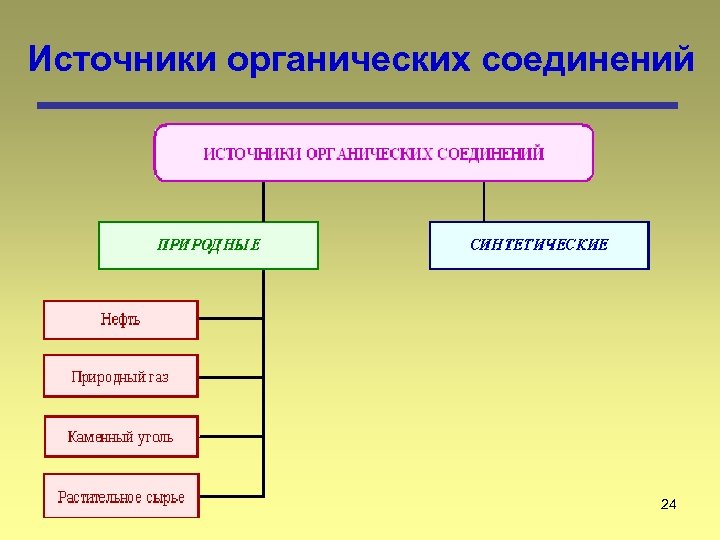
Источники органических соединений 24

Предельные углеводороды. Алканы 25
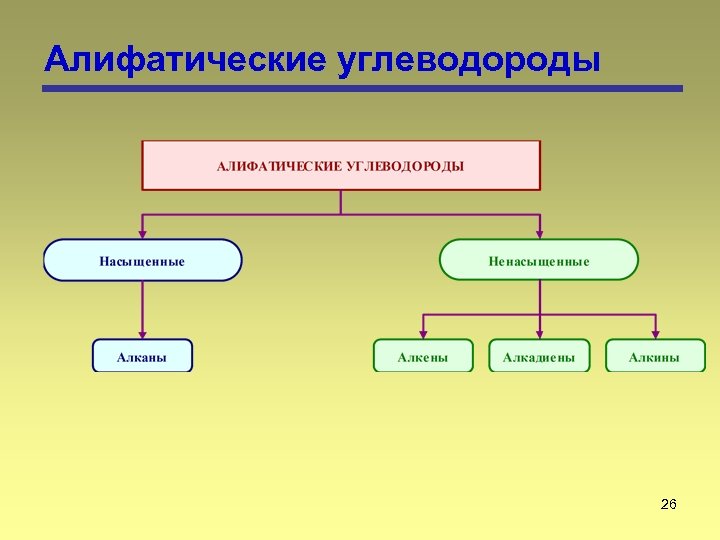
Алифатические углеводороды 26

Алканы Алканами называются насыщенные углеводороды, молекулы которых состоят из атомов углерода и водорода, связанных между собой только -связями. 27
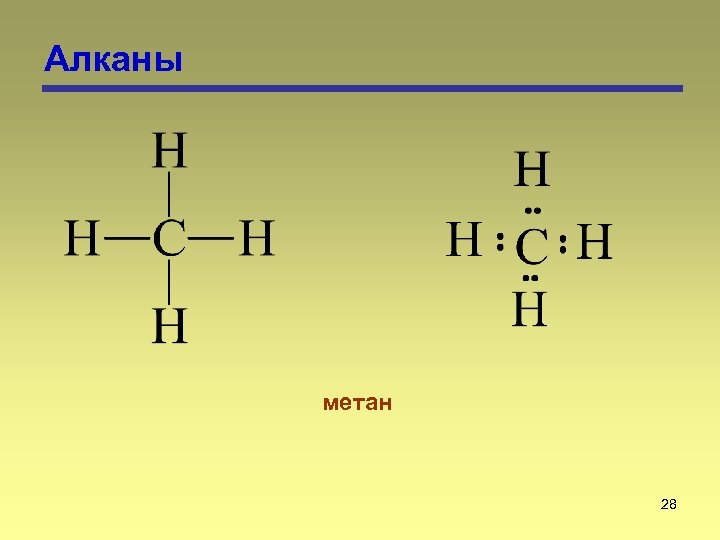
Алканы метан 28
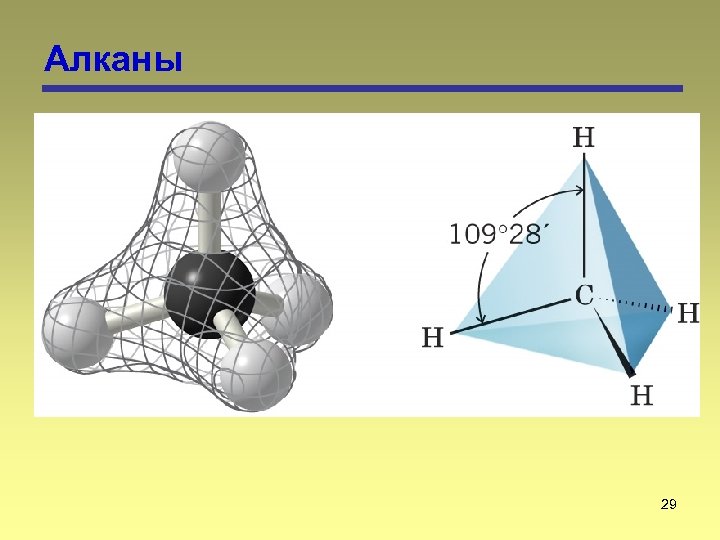
Алканы 29
Электронная структура атома углерода в органических соединениях 30
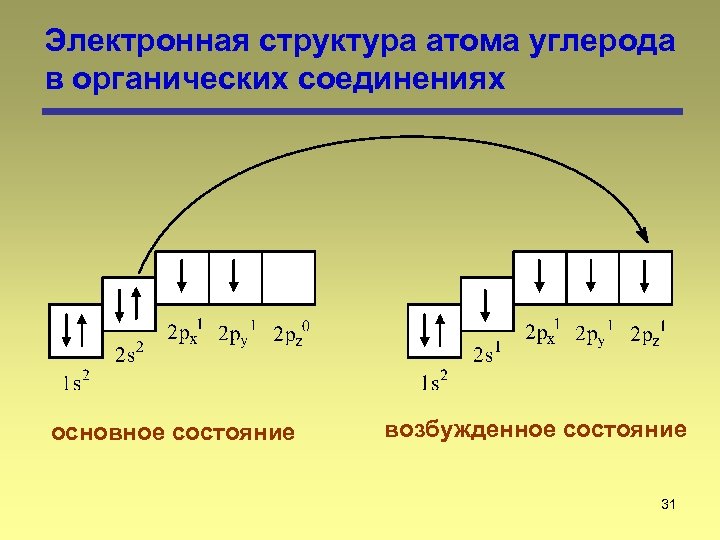
Электронная структура атома углерода в органических соединениях основное состояние возбужденное состояние 31
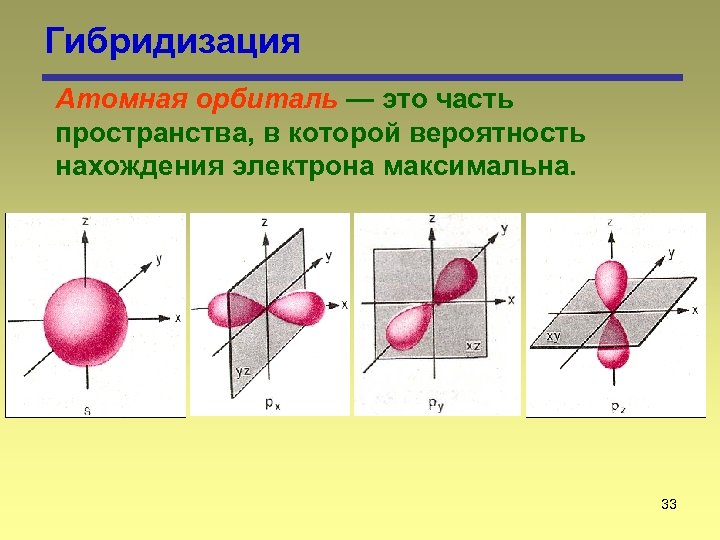
Гибридизация Атомная орбиталь — это часть пространства, в которой вероятность нахождения электрона максимальна. 33

Гибридизация 34

Алканы Группы органических соединений однотипной структуры с одинаковой функциональными группами, отличающиеся друг от друга по количеству групп CH 2 в углеродной цепи, составляют гомологический ряд. Гомологический ряд метана и т. д. 35
Алканы Гомологический ряд изобутана Сn. Н 2 n+2 36
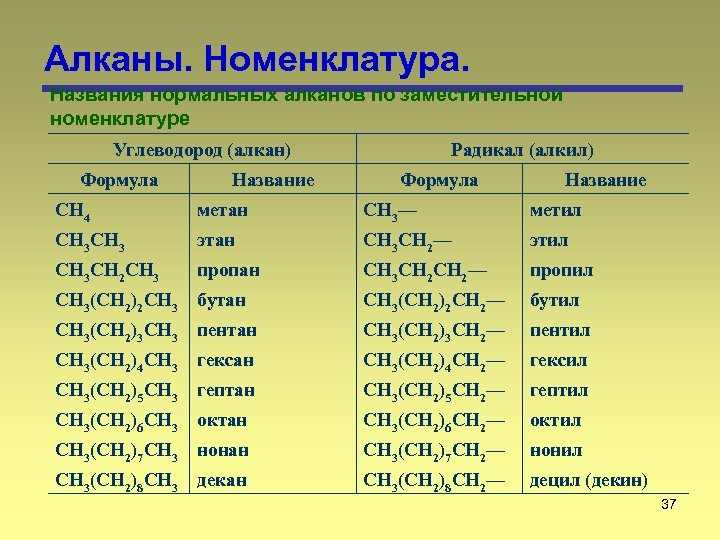
Алканы. Номенклатура. Названия нормальных алканов по заместительной номенклатуре Углеводород (алкан) Формула Название Радикал (алкил) Формула Название CH 4 метан CH 3— метил CH 3 этан CH 3 CH 2— этил CH 3 CH 2 CH 3 пропан CH 3 CH 2— пропил CH 3(CH 2)2 CH 3 бутан CH 3(CH 2)2 CH 2— бутил CH 3(CH 2)3 CH 3 пентан CH 3(CH 2)3 CH 2— пентил CH 3(CH 2)4 CH 3 гексан CH 3(CH 2)4 CH 2— гексил CH 3(CH 2)5 CH 3 гептан CH 3(CH 2)5 CH 2— гептил CH 3(CH 2)6 CH 3 октан CH 3(CH 2)6 CH 2— октил CH 3(CH 2)7 CH 3 нонан CH 3(CH 2)7 CH 2— нонил CH 3(CH 2)8 CH 3 декан CH 3(CH 2)8 CH 2— децил (декин) 37
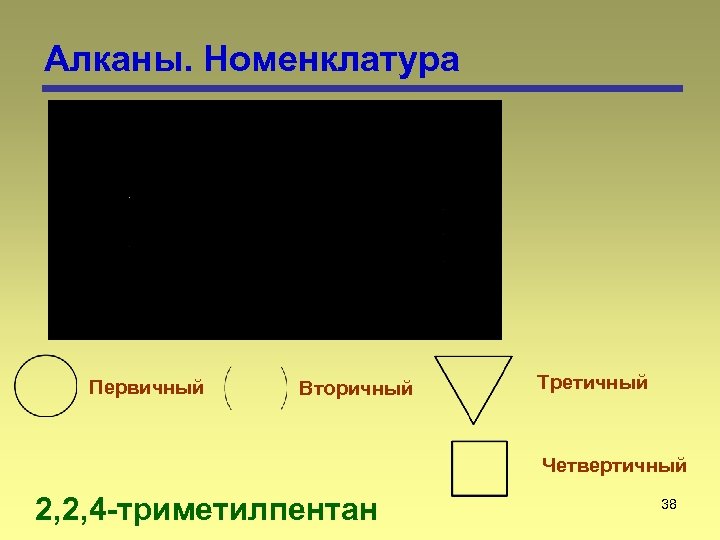
Алканы. Номенклатура Первичный Вторичный Третичный Четвертичный 2, 2, 4 -триметилпентан 38
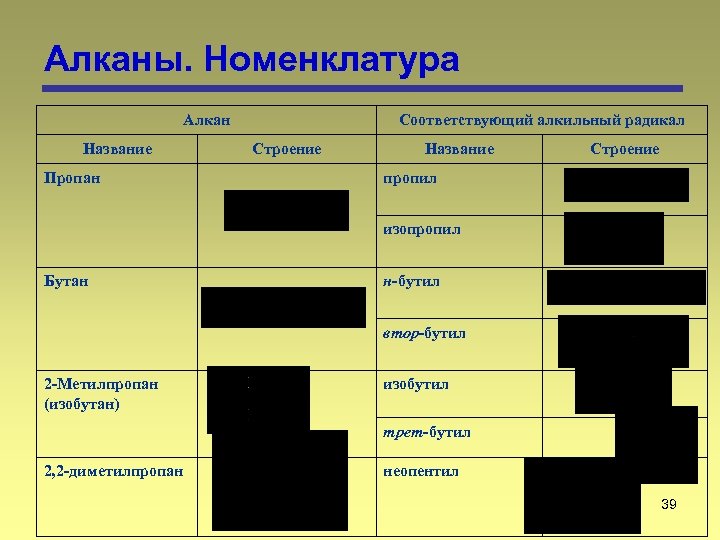
Алканы. Номенклатура Алкан Название Пропан Соответствующий алкильный радикал Строение Название Строение пропил изопропил Бутан н бутил втор-бутил 2 Метилпропан (изобутан) изобутил трет-бутил 2, 2 диметилпропан неопентил 39

Алканы. Номенклатура Систематическая номенклатура ИЮПАК 1) определяют самую длинную цепь атомов углерода. Число атомов углерода в этой цепи служит основой названия; 2) нумеруют главную цепь с того конца, ближе к которому находится заместитель (углеводородный радикал); 3) перед основой названия указывают цифровой номер того атома углерода в главной цепи, у которого находится заместитель, а затем в виде префикса называют этот заместитель; 40

Алканы. Номенклатура 4) при наличии двух и более заместителей нумерацию цепи производят так, чтобы заместители получили наименьшие номера. В названии алкана радикалы перечисляются в алфавитном порядке. Перед названием каждого радикала ставят цифру, обозначающую его положение в главной углеродной цепи. Если заместители одинаковые, то к их названию добавляют умножительные приставки ди-, три-, тетра-, пента- и т. д. 5) если в главной цепи на равном расстоянии от концов стоят одинаковые радикалы, то нумерацию производят таким образом, чтобы радикалы получили наименьшие номера. 41
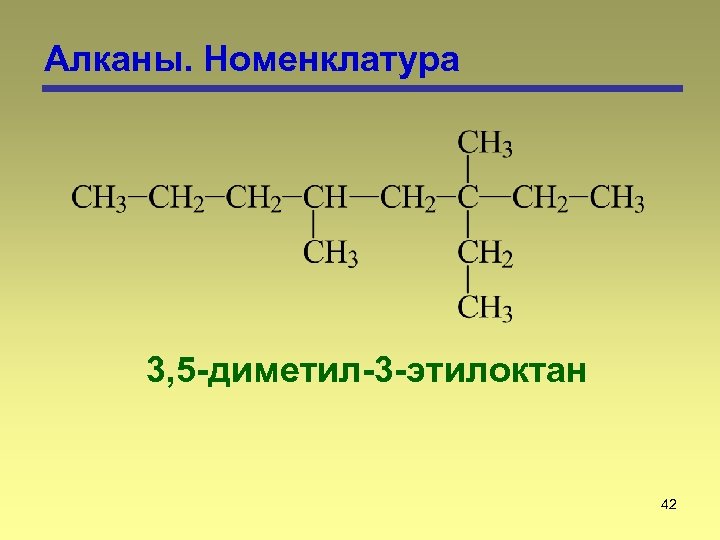
Алканы. Номенклатура 3, 5 -диметил-3 -этилоктан 42
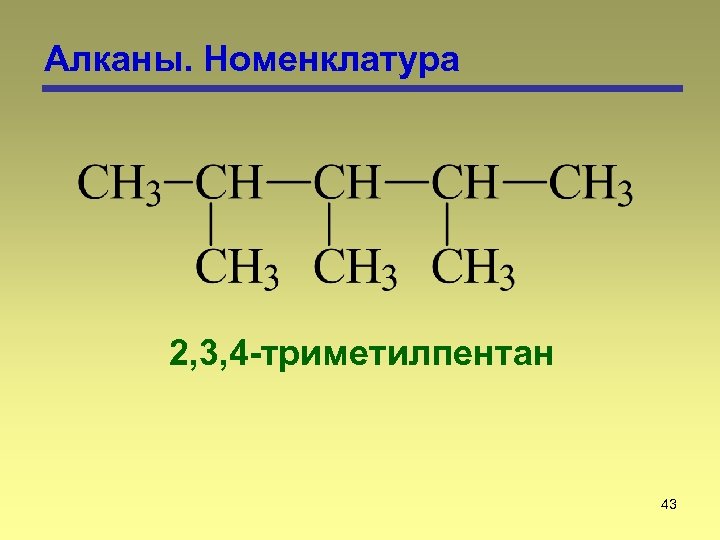
Алканы. Номенклатура 2, 3, 4 -триметилпентан 43
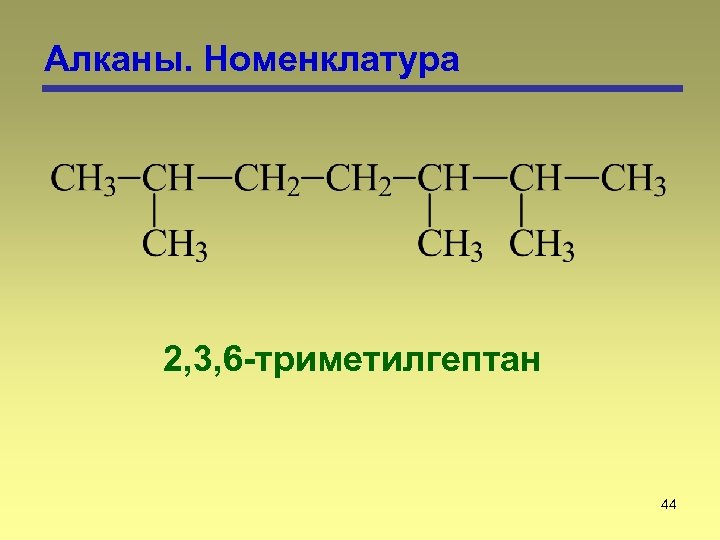
Алканы. Номенклатура 2, 3, 6 -триметилгептан 44
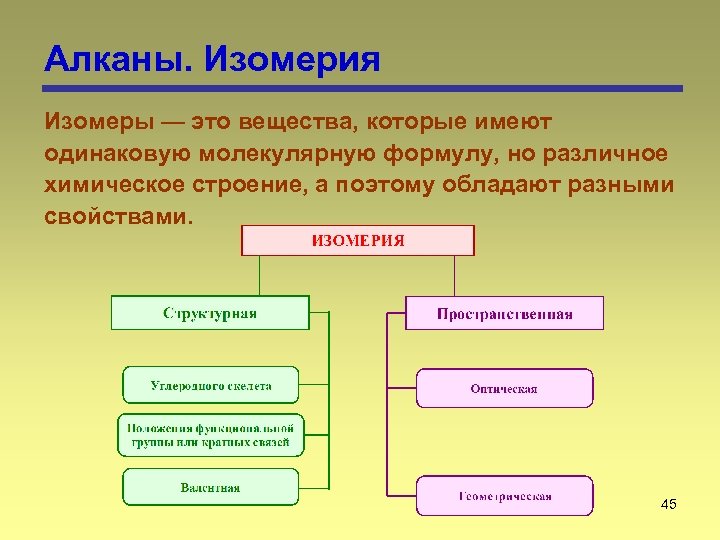
Алканы. Изомерия Изомеры — это вещества, которые имеют одинаковую молекулярную формулу, но различное химическое строение, а поэтому обладают разными свойствами. 45
Алканы. Номенклатура Структурная изомерия 46
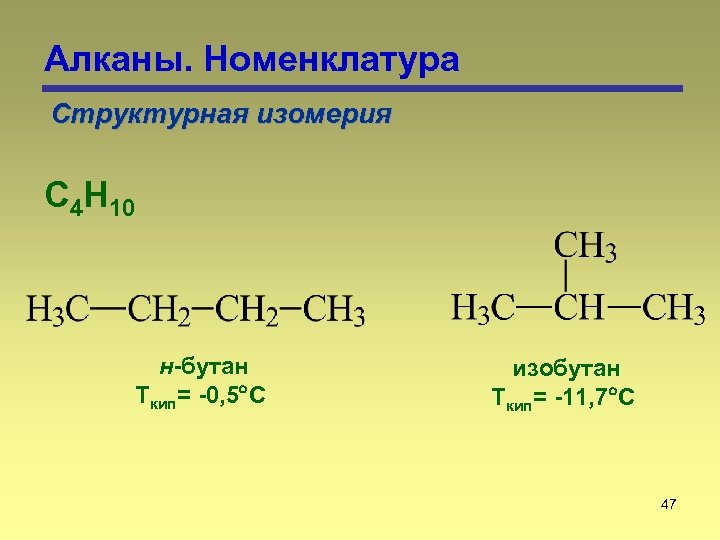
Алканы. Номенклатура Структурная изомерия С 4 Н 10 н-бутан Ткип= -0, 5 С изобутан Ткип= -11, 7 С 47
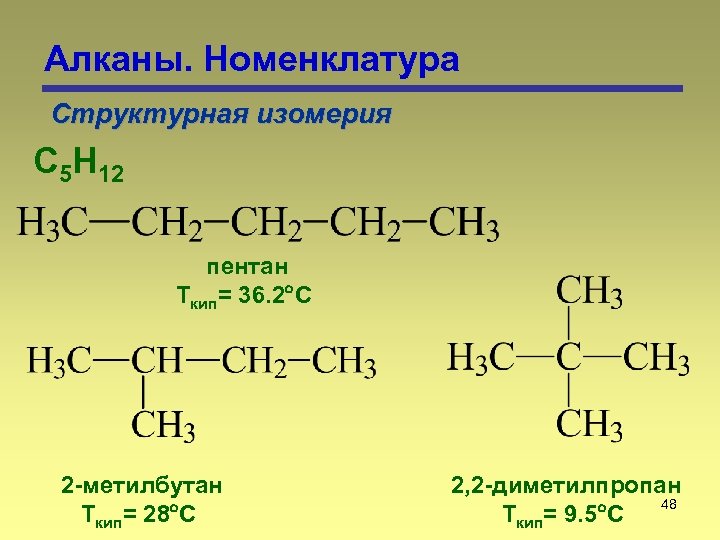
Алканы. Номенклатура Структурная изомерия С 5 Н 12 пентан Ткип= 36. 2 С 2 -метилбутан Ткип= 28 С 2, 2 -диметилпропан 48 Ткип= 9. 5 С
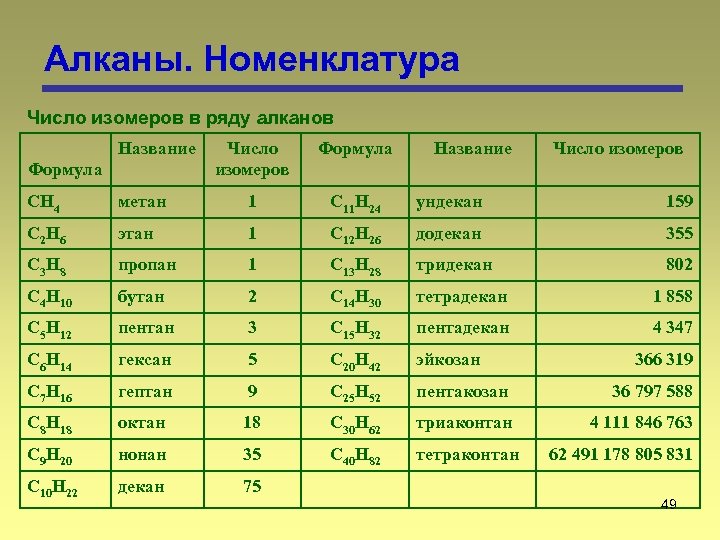
Алканы. Номенклатура Число изомеров в ряду алканов Название Формула Число изомеров Формула Название Число изомеров CH 4 метан 1 C 11 H 24 ундекан 159 C 2 H 6 этан 1 C 12 H 26 додекан 355 C 3 H 8 пропан 1 C 13 H 28 тридекан 802 C 4 H 10 бутан 2 C 14 H 30 тетрадекан 1 858 C 5 H 12 пентан 3 C 15 H 32 пентадекан 4 347 C 6 H 14 гексан 5 C 20 H 42 эйкозан C 7 H 16 гептан 9 C 25 H 52 пентакозан 36 797 588 C 8 H 18 октан 18 C 30 H 62 триаконтан 4 111 846 763 C 9 H 20 нонан 35 C 40 H 82 тетраконтан C 10 H 22 декан 75 366 319 62 491 178 805 831 49
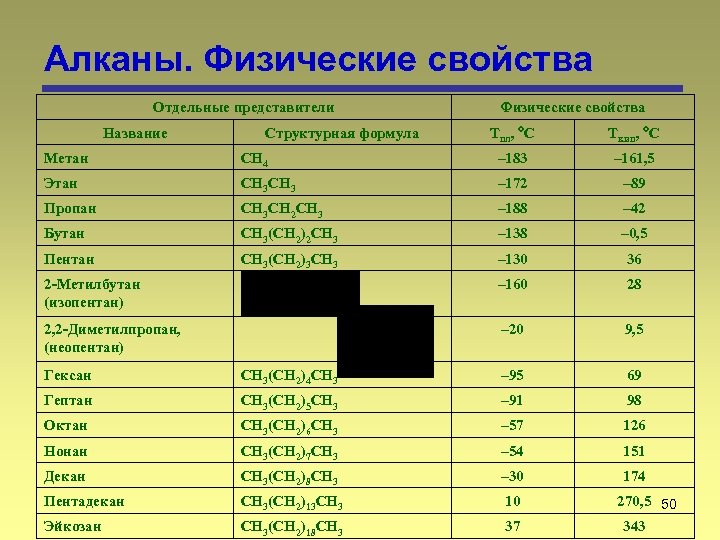
Алканы. Физические свойства Отдельные представители Название Структурная формула Физические свойства Tпл, С Tкип, С Метан CH 4 – 183 – 161, 5 Этан CH 3 – 172 – 89 Пропан CH 3 CH 2 CH 3 – 188 – 42 Бутан CH 3(CH 2)2 CH 3 – 138 – 0, 5 Пентан CH 3(CH 2)3 CH 3 – 130 36 2 Метилбутан (изопентан) – 160 28 2, 2 Диметилпропан, (неопентан) – 20 9, 5 Гексан CH 3(CH 2)4 CH 3 – 95 69 Гептан CH 3(CH 2)5 CH 3 – 91 98 Октан CH 3(CH 2)6 CH 3 – 57 126 Нонан CH 3(CH 2)7 CH 3 – 54 151 Декан CH 3(CH 2)8 CH 3 – 30 174 Пентадекан CH 3(CH 2)13 CH 3 10 Эйкозан CH 3(CH 2)18 CH 3 37 270, 5 50 343
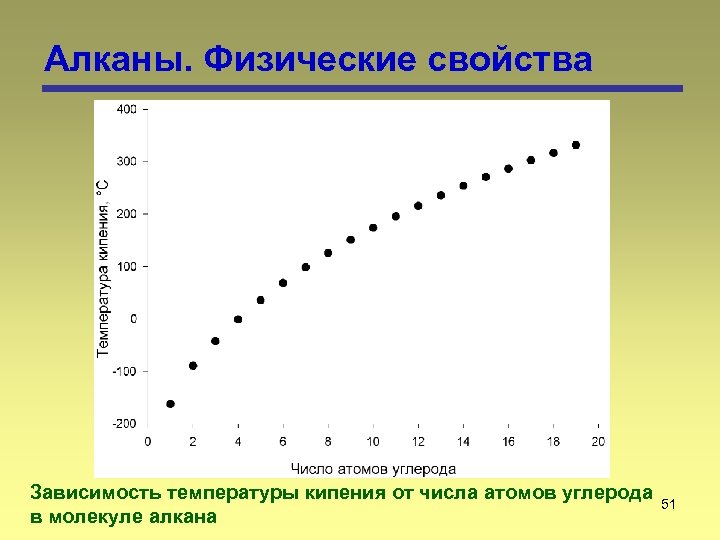
Алканы. Физические свойства Зависимость температуры кипения от числа атомов углерода 51 в молекуле алкана
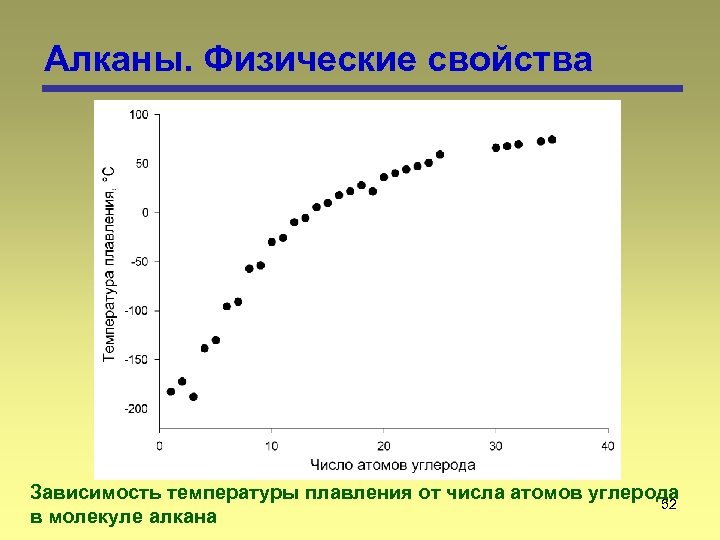
Алканы. Физические свойства Зависимость температуры плавления от числа атомов углерода 52 в молекуле алкана

Алканы. Физические свойства Изменение температуры кипения в изомерах гексана 53
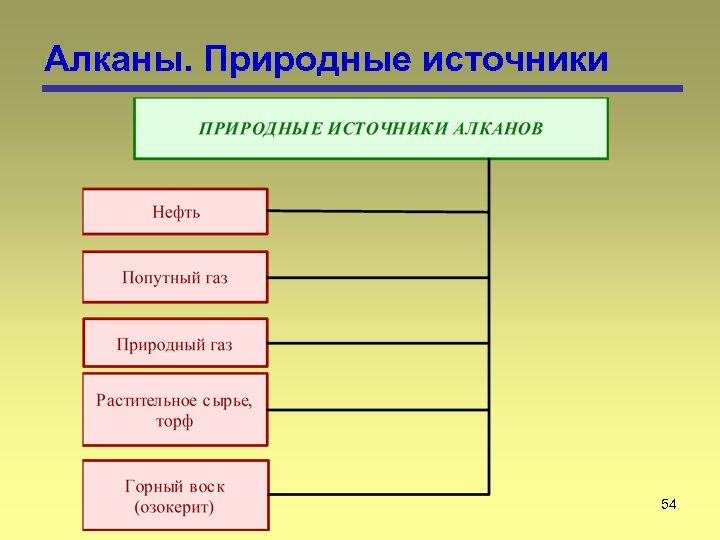
Алканы. Природные источники 54

Алканы. Способы получения Газофикация угля (Бертло, 1869) Сжижение угля Метод Фишера-Тропша Синтетический бензин — «синтин» 55
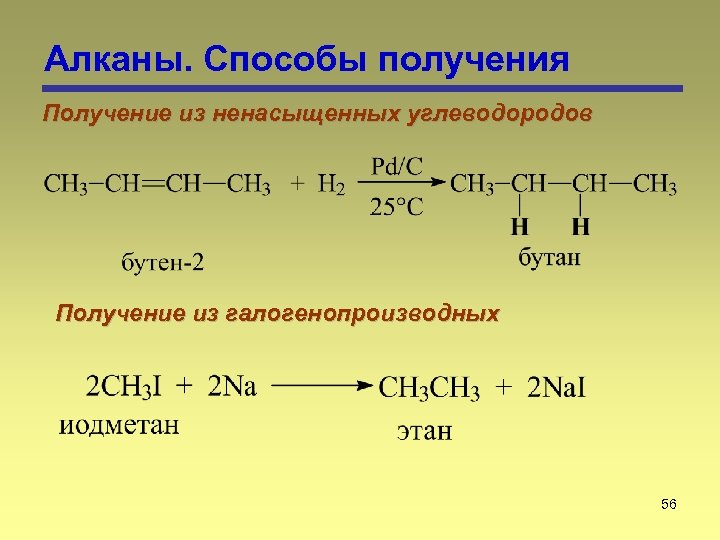
Алканы. Способы получения Получение из ненасыщенных углеводородов Получение из галогенопроизводных 56
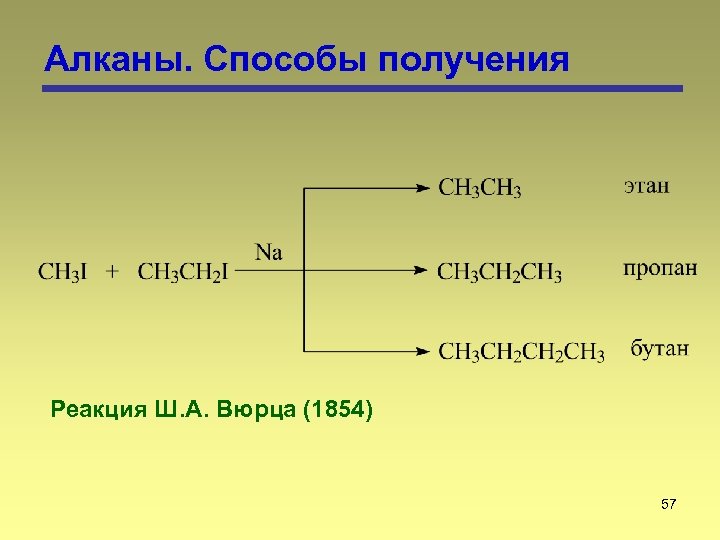
Алканы. Способы получения Реакция Ш. А. Вюрца (1854) 57

Алканы. Способы получения Восстановление галогеналканов 58
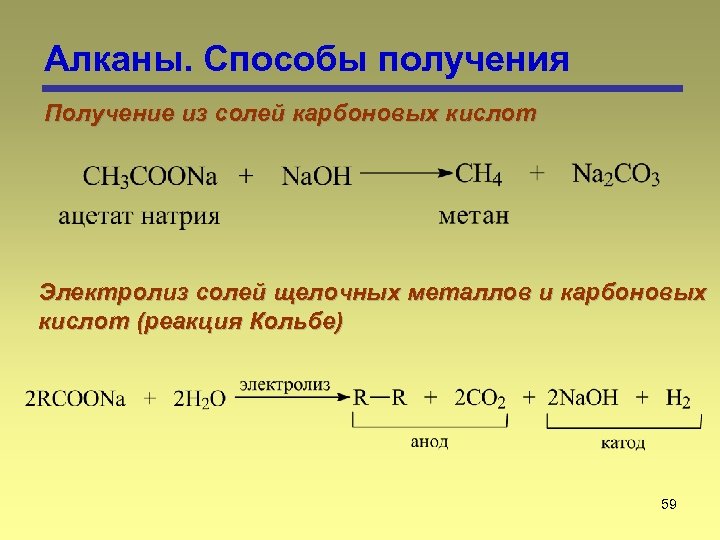
Алканы. Способы получения Получение из солей карбоновых кислот Электролиз солей щелочных металлов и карбоновых кислот (реакция Кольбе) 59

Алканы. Способы получения Гидролиз карбидов металлов 1) Карбиды, при гидролизе, которых образуется метан. (Карбиды алюминия и берилия Al 4 C 3, Be 2 C) Al 4 C 3 + 12 H 2 O = 3 CH 4 + 4 Al(OH)3 2) Карбиды при гидролизе, которых образуется ацетилен. (Na 2 C 2, K 2 C 2, Ca. C 2, Ba. C 2, Cu 2 C 2, Ag 2 C 2) 3) Карбиды при гидролизе, которых образуется смесь углеводородов (карбиды переходных металлов) Переработка отходов биологического происхождения 60

Алканы. Химические свойства Галогенирование 61
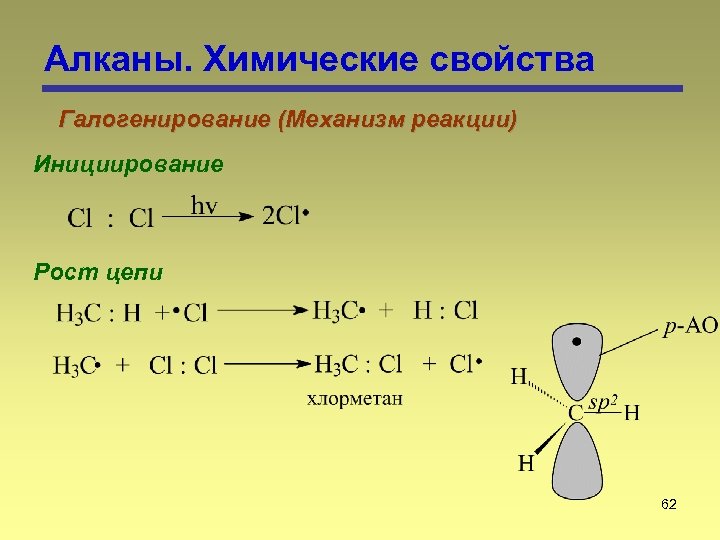
Алканы. Химические свойства Галогенирование (Механизм реакции) Инициирование Рост цепи 62

Алканы. Химические свойства Галогенирование (Механизм реакции) Обрыв цепи 63

Алканы. Химические свойства Галогенирование (Механизм реакции) 1. Галогенирование начинается только под действием инициатора радикальных реакций (УФсвет, радикальные реагенты, нагревание). 2. Реакционная способность в ряду галогенов уменьшается в ряду: F 2 > Cl 2 > Br 2 > I 2 3. Галогенирование под действием фтора и хлора может выйти из под контроля и приобрести взрывной характер. 64

Алканы. Химические свойства Галогенирование (Механизм реакции) 4. Реакционная способность водорода у третичного атома углерода выше, чем у вторичного, а вторичного выше, чем у первичного. 376 к. Дж/моль 390 к. Дж/моль 415 к. Дж/моль 65

Алканы. Химические свойства Галогенирование (Механизм реакции) 66
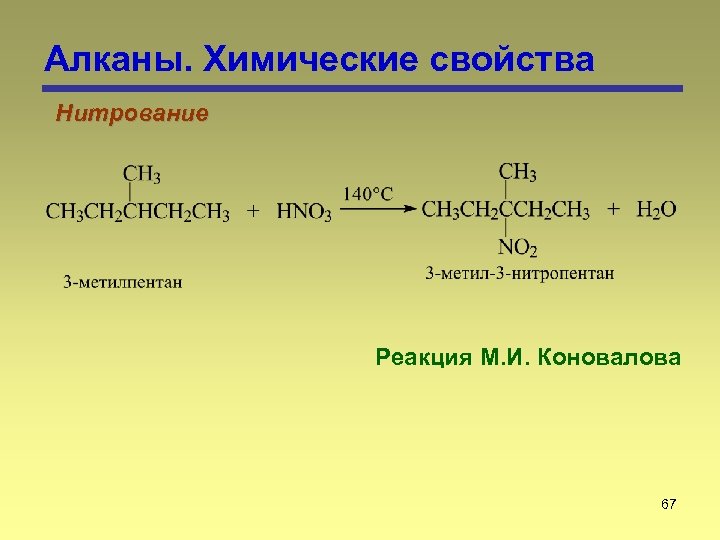
Алканы. Химические свойства Нитрование Реакция М. И. Коновалова 67
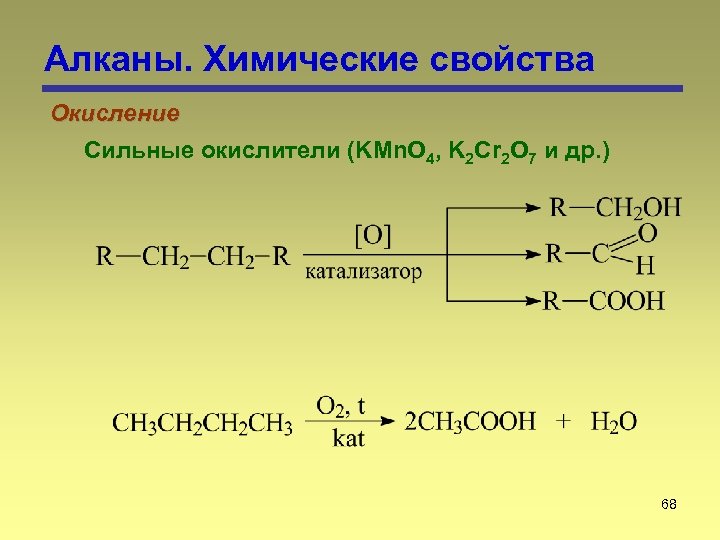
Алканы. Химические свойства Окисление Сильные окислители (KMn. O 4, K 2 Cr 2 O 7 и др. ) 68
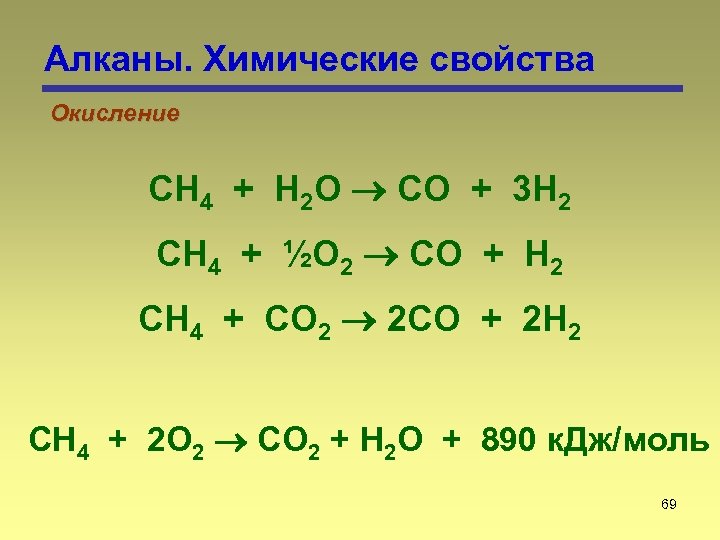
Алканы. Химические свойства Окисление CH 4 + H 2 O CO + 3 H 2 CH 4 + ½O 2 CO + H 2 CH 4 + CO 2 2 CO + 2 H 2 CH 4 + 2 O 2 CO 2 + H 2 O + 890 к. Дж/моль 69
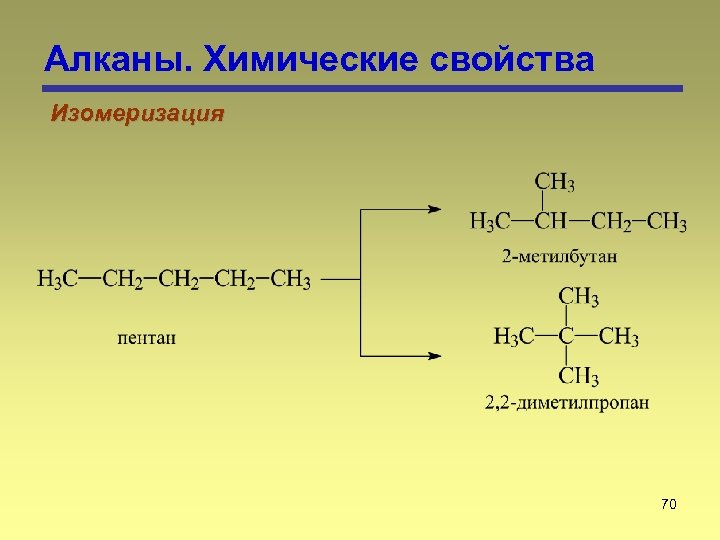
Алканы. Химические свойства Изомеризация 70

Алканы. Химические свойства Термическое разложение (Крекинг) Температура – 470— 650°С; В. Г. Шухов (1891) Давление – 7 МПа 71

Алканы. Химические свойства Каталитический крекинг Катализаторы – Аl. Сl 3, Сr 2 О 3, алюмосиликаты; Температура – 470— 500°С; Давление 0, 01— 0, 1 МПа Пиролиз и риформинг 72
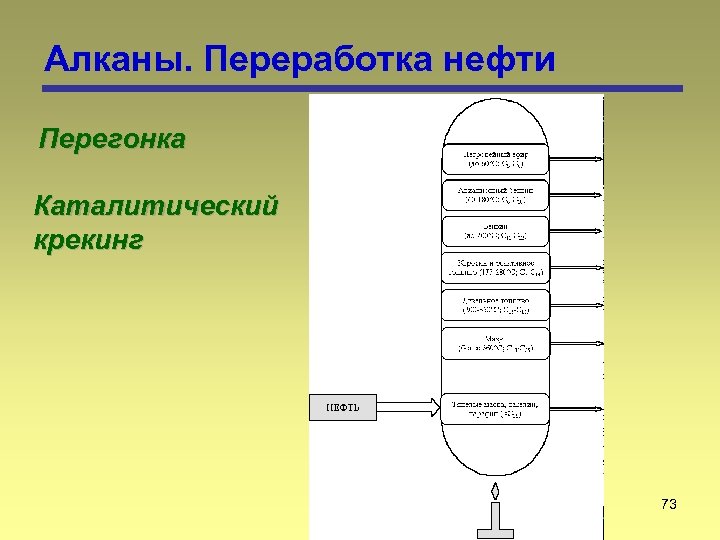
Алканы. Переработка нефти Перегонка Каталитический крекинг 73
74
4aff6d9b3185fed3e7516fb2ee5451b5.ppt