LECTURE 2.pptx
- Количество слайдов: 22

ОРГАНИЧЕСКАЯ ХИМИЯ ЭПИЗОД ВТОРОЙ: ГЛУБЖЕ О СТРУКТУРЕ

ПОВТОРИМ • СОВРЕМЕННАЯ МОДЕЛЬ АТОМА. ЗАПОЛНЕНИЕ ЭЛЕКТРОННЫХ ОБОЛОЧЕК – H, C, O, N, S – С-H, N-H, O-H – ТРИ ОСНОВНЫХ ПРАВИЛА – СТРУКТУРЫ ЛЬЮИСА • ТЕОРИЯ ОТТАЛКИВАНИЯ ЭЛЕКТРОННЫХ ПАР ВАЛЕНТНЫХ ОРБИТАЛЕЙ (ОЭПВО) – СТРУКТУРЫ С 2, 3, 4 ЭЛЕКТРОННЫМИ
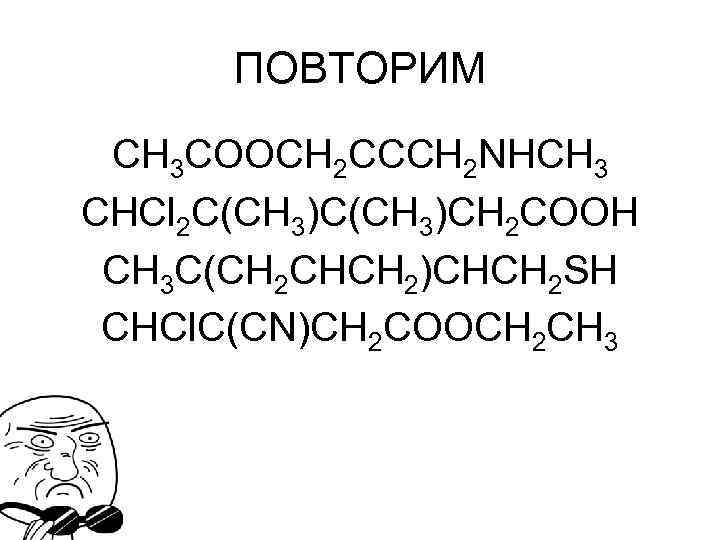
ПОВТОРИМ СH 3 COOCH 2 CCCH 2 NHCH 3 CHCl 2 C(CH 3)CH 2 COOH CH 3 C(CH 2 CHCH 2)CHCH 2 SH CHCl. C(CN)CH 2 COOCH 2 CH 3
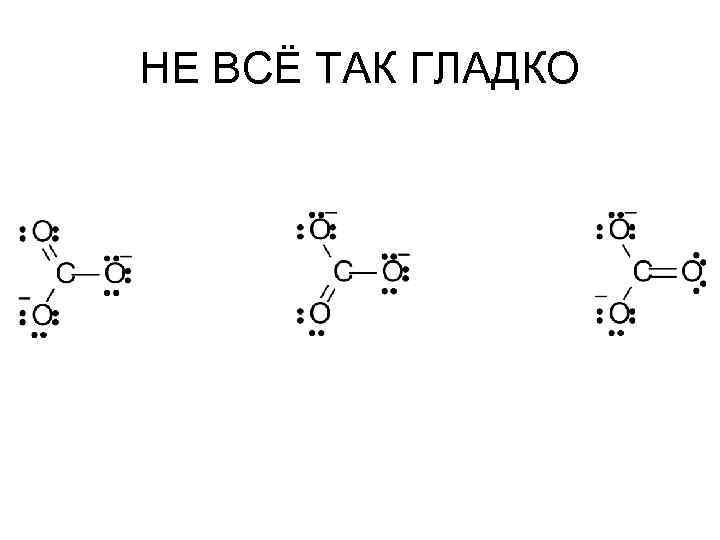
НЕ ВСЁ ТАК ГЛАДКО

ЛАЙНУС КАРЛ ПОЛИНГ
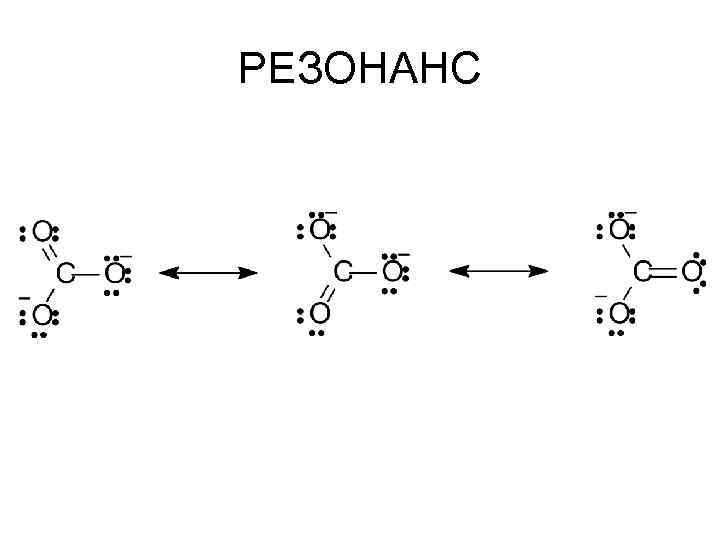
РЕЗОНАНС
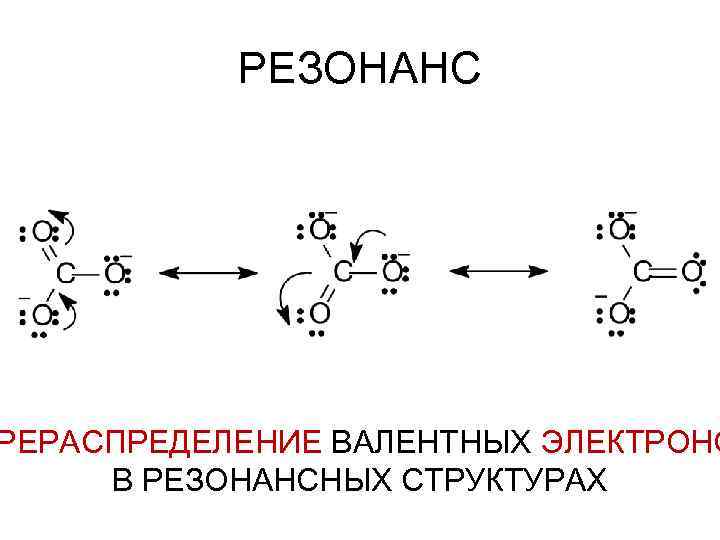
РЕЗОНАНС РЕРАСПРЕДЕЛЕНИЕ ВАЛЕНТНЫХ ЭЛЕКТРОНО В РЕЗОНАНСНЫХ СТРУКТУРАХ

РЕЗОНАНС

ПРАВИЛА ДЛЯ САМОПРОВЕРКИ • У ВСЕХ РЕЗОНАНСНЫХ СТРУКТУР ОДИНАКОВОЕ КОЛИЧЕСТВО ВАЛЕНТНЫХ ЭЛЕКТРОНОВ • В РЕЗОНАНСНЫХ СТРУКТУРАХ РАБОТАЮТ ПРАВИЛА ЗАПОЛНЕНИЯ ОБОЛОЧЕК • АТОМЫ ОСТАЮТСЯ НА СВОИХ МЕСТАХ • В СТРУКТУРАХ НЕ ИЗМЕНЯЕТСЯ
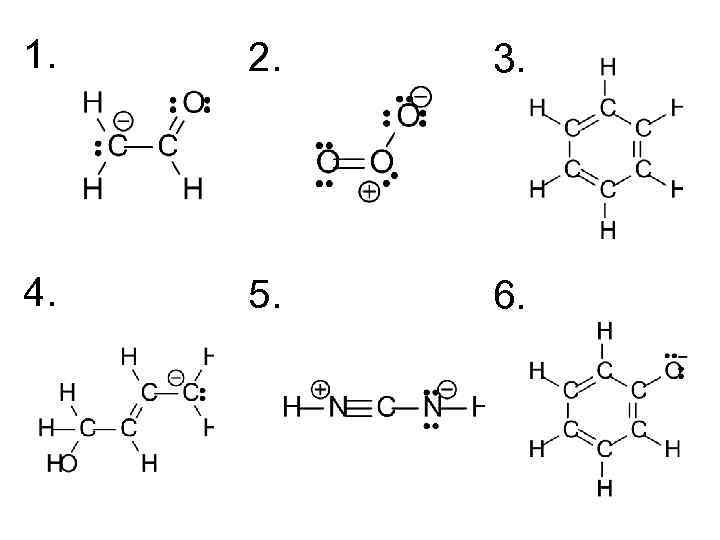
1. 2. 3. 4. 5. 6.

МОДЕЛЬ ПЕРЕКРЫВАНИЯ ОРБИТАЛЕЙ КЕЙ, ГУГЛ, С ЛЬЮИСОМ ВСЁ ПОНЯТН ЧТО ДАЛЬШЕ?
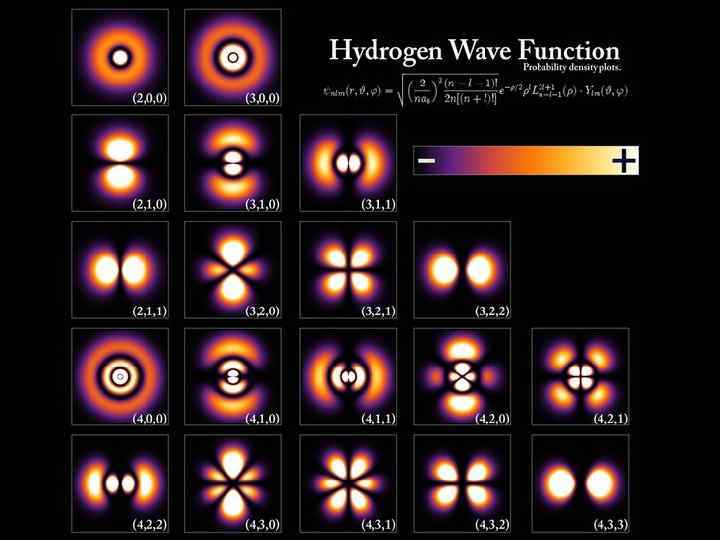
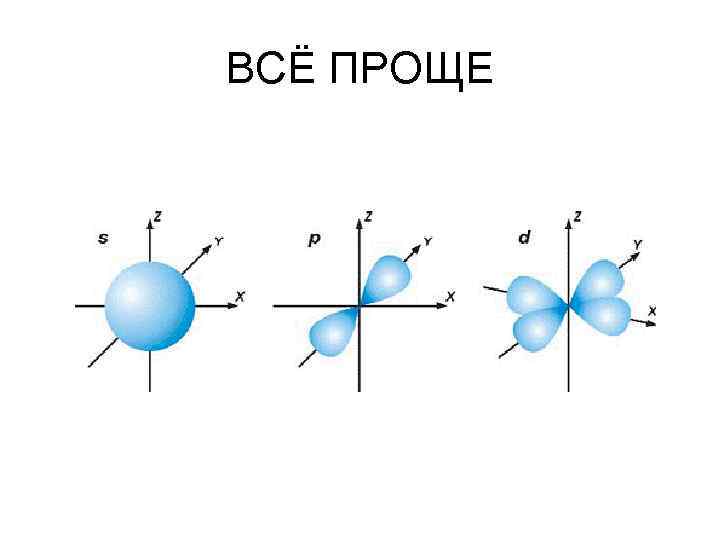
ВСЁ ПРОЩЕ
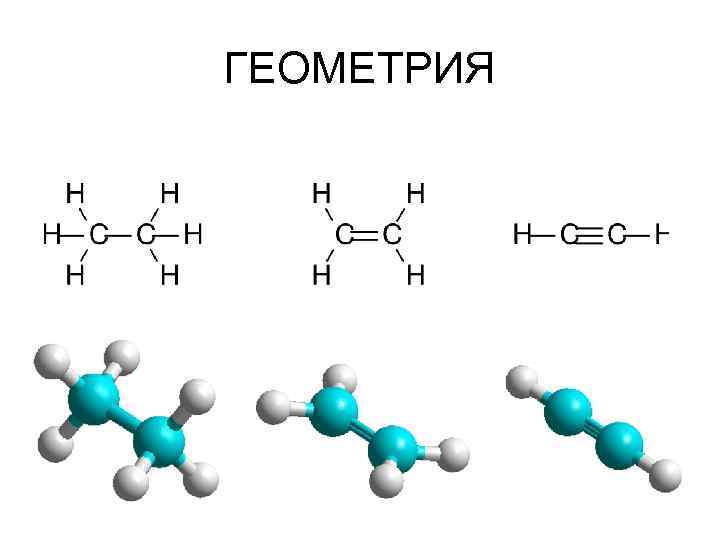
ГЕОМЕТРИЯ
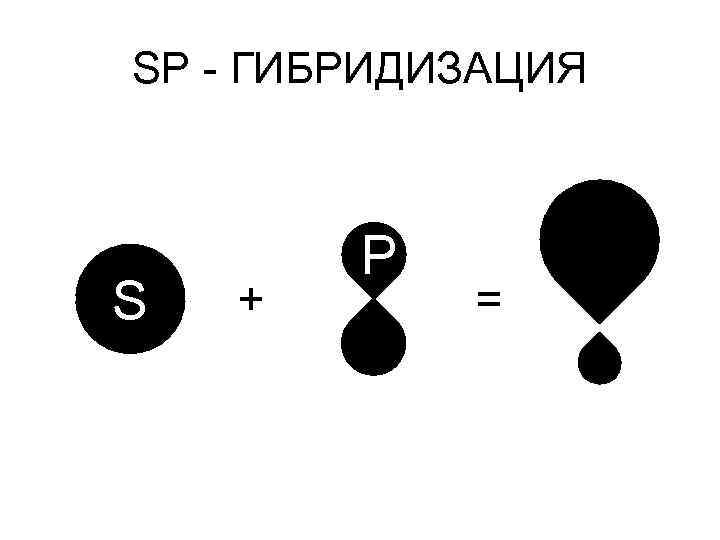
SP - ГИБРИДИЗАЦИЯ S + P =
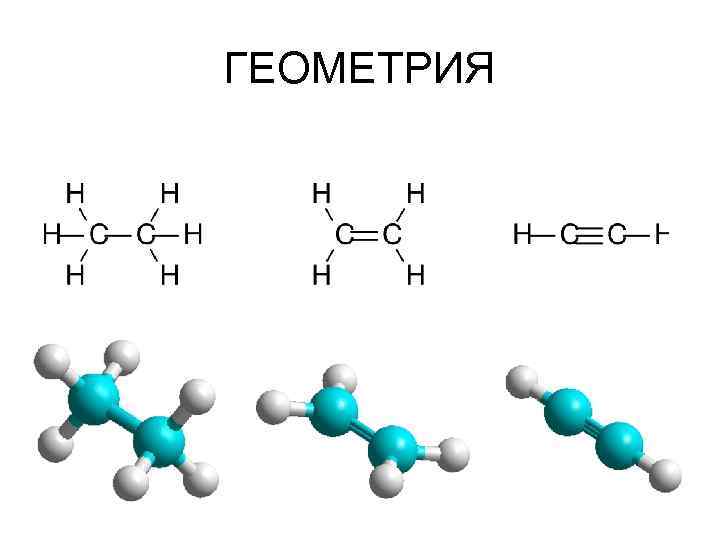
ГЕОМЕТРИЯ
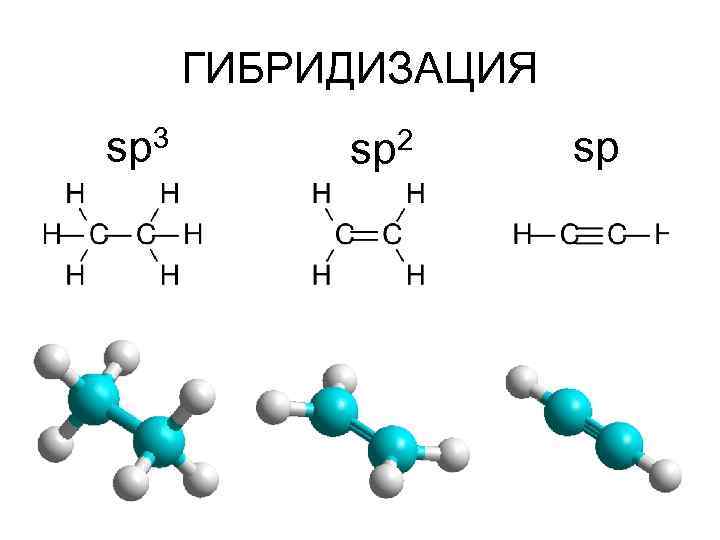
ГИБРИДИЗАЦИЯ sp 3 sp 2 sp

ИТОГО sp 3 – 109, 5 – ТЕТРАЭДР sp 2 – 120 – РАВНОСТОРОННИЙ ТРЕУГОЛЬНИК sp – 180 – ПРЯМАЯ σ-СВЯЗЬ – СВЯЗЬ С ПЕРЕКРЫВАНИЕМ НА ОСИ, СОЕДИНЯЮЩЕЙ АТОМЫ π-СВЯЗЬ – БОЛЕЕ СЛАБАЯ ВВИДУ МЕНЬШЕГО ПЕРЕКРЫВАНИЯ ВНЕ ОСИ
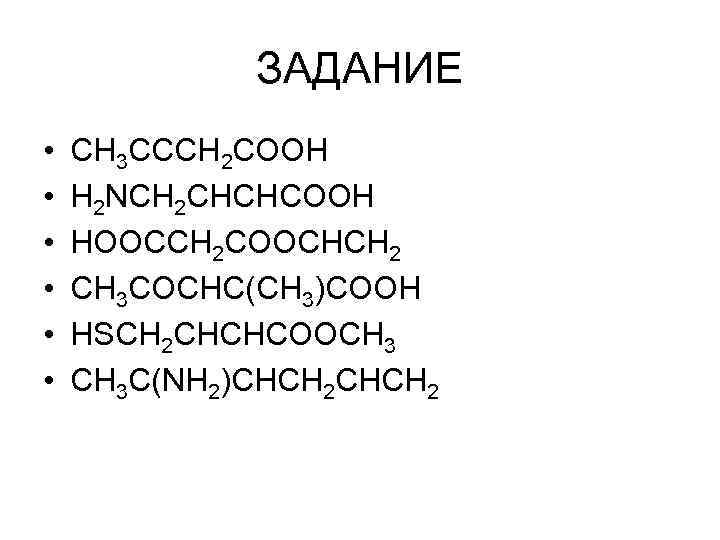
ЗАДАНИЕ • • • CH 3 CCCH 2 COOH H 2 NCH 2 CHCHCOOH HOOCCH 2 COOCHCH 2 CH 3 COCHC(CH 3)COOH HSCH 2 CHCHCOOCH 3 C(NH 2)CHCH 2

ЗАДАНИЕ 2 – УБИРАЕМ ПРОТОН
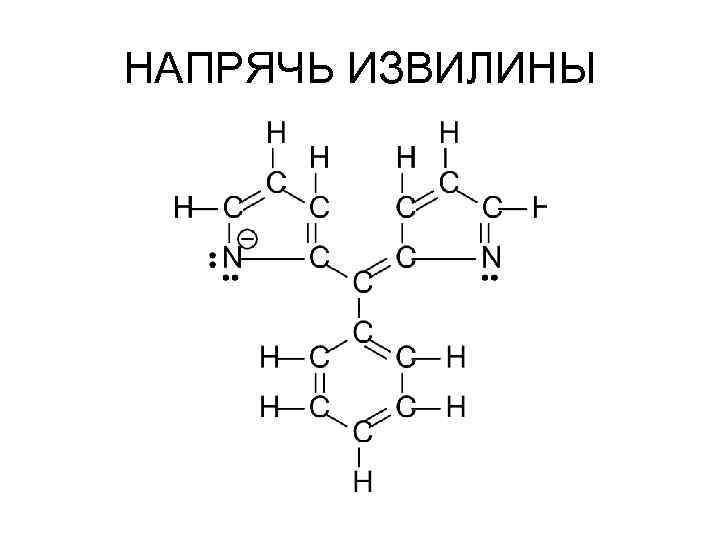
НАПРЯЧЬ ИЗВИЛИНЫ
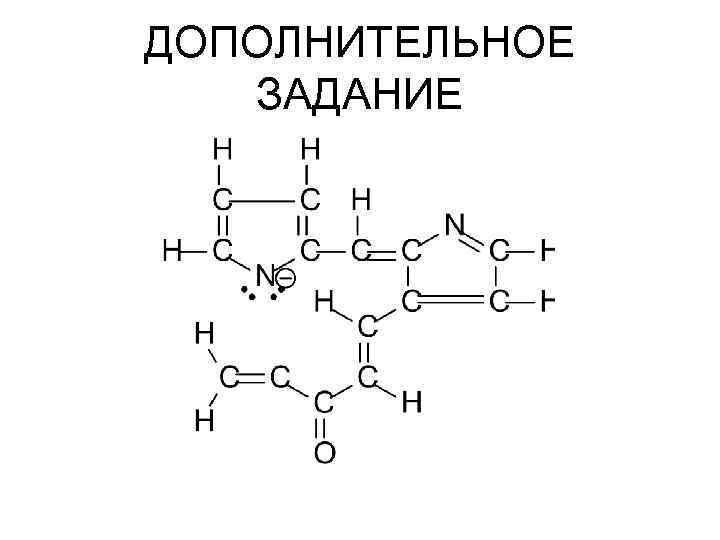
ДОПОЛНИТЕЛЬНОЕ ЗАДАНИЕ
LECTURE 2.pptx