LECTURE 1.pptx
- Количество слайдов: 48
 ОРГАНИЧЕСКАЯ ХИМИЯ ЭПИЗОД ПЕРВЫЙ: СТРОЕНИЕ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
ОРГАНИЧЕСКАЯ ХИМИЯ ЭПИЗОД ПЕРВЫЙ: СТРОЕНИЕ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ



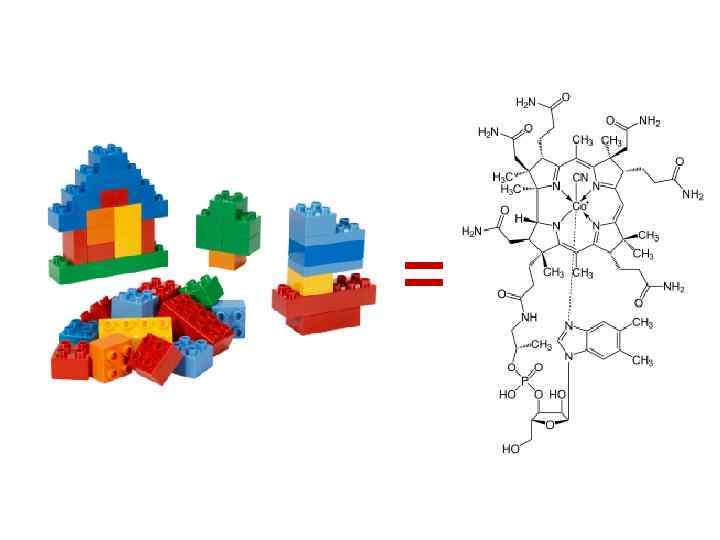 =
=

 ПРИНЦИПЫ МНОГООБРАЗИ
ПРИНЦИПЫ МНОГООБРАЗИ
 ПРИНЦИПЫ МНОГООБРАЗИЕ
ПРИНЦИПЫ МНОГООБРАЗИЕ
 ЭЛЕКТРОННАЯ СТРУКТУРА АТОМА ~10 -10 m ~10 -15 m 2 n 2 e 32 e 18 e 2 e
ЭЛЕКТРОННАЯ СТРУКТУРА АТОМА ~10 -10 m ~10 -15 m 2 n 2 e 32 e 18 e 2 e
 ПОЧЕМУ ИМЕННО ТАК? ЭВОЛЮЦИЯ УЧЕНИЙ ОБ АТОМЕ • ДЕМОКРИТ, ЭПИКУР, ЛУКРЕЦИЙ ШАНСЫ СБОРНОЙ РОССИИ ПОБЕДИТЬ В ЕВРО АТОМ(НЕДЕЛИМЫЙ) .
ПОЧЕМУ ИМЕННО ТАК? ЭВОЛЮЦИЯ УЧЕНИЙ ОБ АТОМЕ • ДЕМОКРИТ, ЭПИКУР, ЛУКРЕЦИЙ ШАНСЫ СБОРНОЙ РОССИИ ПОБЕДИТЬ В ЕВРО АТОМ(НЕДЕЛИМЫЙ) .
 ПОЧЕМУ ИМЕННО ТАК? ЭВОЛЮЦИЯ УЧЕНИЙ ОБ АТОМЕ • ДЕМОКРИТ, ЭПИКУР, ЛУКРЕЦИЙ • …
ПОЧЕМУ ИМЕННО ТАК? ЭВОЛЮЦИЯ УЧЕНИЙ ОБ АТОМЕ • ДЕМОКРИТ, ЭПИКУР, ЛУКРЕЦИЙ • …
 ПОЧЕМУ ИМЕННО ТАК? ЭВОЛЮЦИЯ УЧЕНИЙ ОБ АТОМЕ • ДЕМОКРИТ, ЭПИКУР, ЛУКРЕЦИЙ • МОДЕЛЬ АТОМА ТОМСОНА - МОДЕЛЬ «ПУДИНГ С ИЗЮМОМ»
ПОЧЕМУ ИМЕННО ТАК? ЭВОЛЮЦИЯ УЧЕНИЙ ОБ АТОМЕ • ДЕМОКРИТ, ЭПИКУР, ЛУКРЕЦИЙ • МОДЕЛЬ АТОМА ТОМСОНА - МОДЕЛЬ «ПУДИНГ С ИЗЮМОМ»
 ПОЧЕМУ ИМЕННО ТАК? ЭВОЛЮЦИЯ УЧЕНИЙ ОБ АТОМЕ • ДЕМОКРИТ, ЭПИКУР, ЛУКРЕЦИЙ • МОДЕЛЬ АТОМА ТОМСОНА (МОДЕЛЬ «ПУДИНГ С ИЗЮМОМ» ) • РАННЯЯ ПЛАНЕТАРНАЯ МОДЕЛЬ АТОМА НАГАОКИ
ПОЧЕМУ ИМЕННО ТАК? ЭВОЛЮЦИЯ УЧЕНИЙ ОБ АТОМЕ • ДЕМОКРИТ, ЭПИКУР, ЛУКРЕЦИЙ • МОДЕЛЬ АТОМА ТОМСОНА (МОДЕЛЬ «ПУДИНГ С ИЗЮМОМ» ) • РАННЯЯ ПЛАНЕТАРНАЯ МОДЕЛЬ АТОМА НАГАОКИ
 ПОЧЕМУ ИМЕННО ТАК? ЭВОЛЮЦИЯ УЧЕНИЙ ОБ АТОМЕ • ДЕМОКРИТ, ЭПИКУР, ЛУКРЕЦИЙ • МОДЕЛЬ АТОМА ТОМСОНА (МОДЕЛЬ «ПУДИНГ С ИЗЮМОМ» ) • РАННЯЯ ПЛАНЕТАРНАЯ МОДЕЛЬ АТОМА НАГАОКИ
ПОЧЕМУ ИМЕННО ТАК? ЭВОЛЮЦИЯ УЧЕНИЙ ОБ АТОМЕ • ДЕМОКРИТ, ЭПИКУР, ЛУКРЕЦИЙ • МОДЕЛЬ АТОМА ТОМСОНА (МОДЕЛЬ «ПУДИНГ С ИЗЮМОМ» ) • РАННЯЯ ПЛАНЕТАРНАЯ МОДЕЛЬ АТОМА НАГАОКИ
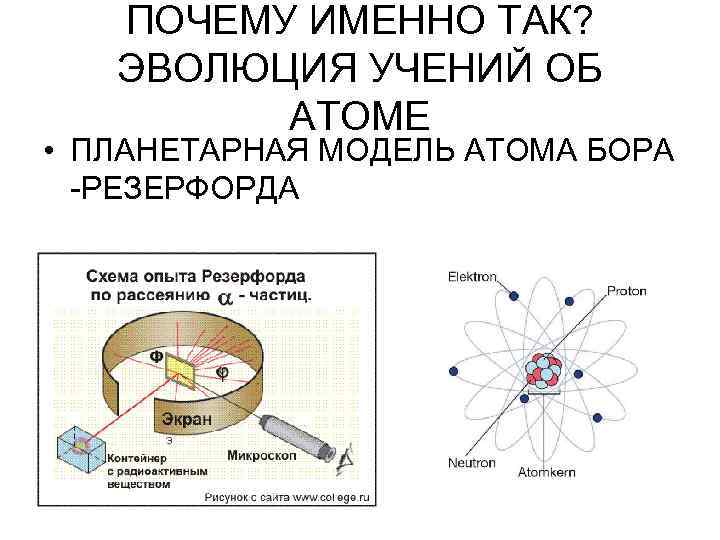 ПОЧЕМУ ИМЕННО ТАК? ЭВОЛЮЦИЯ УЧЕНИЙ ОБ АТОМЕ • ПЛАНЕТАРНАЯ МОДЕЛЬ АТОМА БОРА -РЕЗЕРФОРДА
ПОЧЕМУ ИМЕННО ТАК? ЭВОЛЮЦИЯ УЧЕНИЙ ОБ АТОМЕ • ПЛАНЕТАРНАЯ МОДЕЛЬ АТОМА БОРА -РЕЗЕРФОРДА
 ПОЧЕМУ ИМЕННО ТАК? ЭВОЛЮЦИЯ УЧЕНИЙ ОБ АТОМЕ • ДЕМОКРИТ, ЭПИКУР, ЛУКРЕЦИЙ • МОДЕЛЬ АТОМА ТОМСОНА (МОДЕЛЬ «ПУДИНГ С ИЗЮМОМ» ) • РАННЯЯ ПЛАНЕТАРНАЯ МОДЕЛЬ АТОМА НАГАОКИ • ПЛАНЕТАРНАЯ МОДЕЛЬ АТОМА БОРА -РЕЗЕРФОРДА • КВАНТОВАЯ МЕХАНИКА!
ПОЧЕМУ ИМЕННО ТАК? ЭВОЛЮЦИЯ УЧЕНИЙ ОБ АТОМЕ • ДЕМОКРИТ, ЭПИКУР, ЛУКРЕЦИЙ • МОДЕЛЬ АТОМА ТОМСОНА (МОДЕЛЬ «ПУДИНГ С ИЗЮМОМ» ) • РАННЯЯ ПЛАНЕТАРНАЯ МОДЕЛЬ АТОМА НАГАОКИ • ПЛАНЕТАРНАЯ МОДЕЛЬ АТОМА БОРА -РЕЗЕРФОРДА • КВАНТОВАЯ МЕХАНИКА!
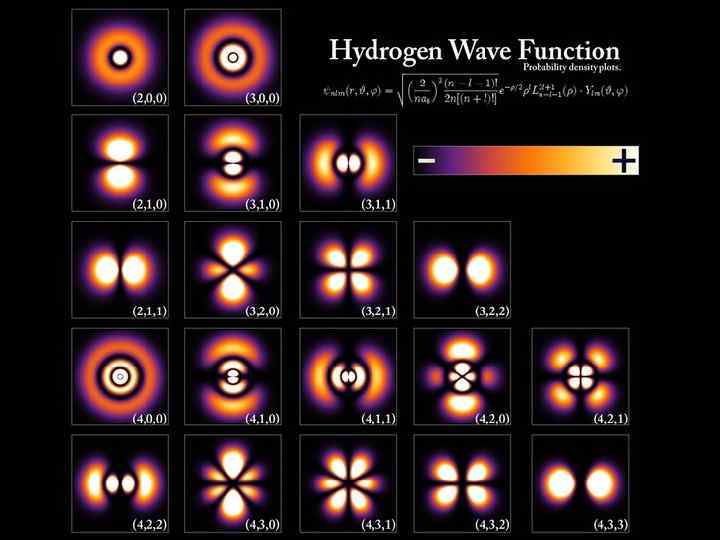
 ПОЧЕМУ ИМЕННО ТАК? ВЕРОЯТНОСТЬ И АТОМНАЯ ФИЗИКА ТОЯНИЕ ПОЛНОСТЬЮ ОПИСЫВАЕТСЯ НЕНИЕМ ШРЕДИНГЕРА НЕРГИЯ ЭЛЕКТРОНА И ВОЛНОВАЯ ФУНКЦИЯ – ИСЯТ ОТ НЕКОТОРЫХ МЕННЫХ, ВВЕДЁННЫХ ДЛЯ УДОБСТВА ФОРМА ОРБИТАЛИ ЛЕГКО ОПИСЫВАЕТСЯ ЭТИМИ E = f(n)
ПОЧЕМУ ИМЕННО ТАК? ВЕРОЯТНОСТЬ И АТОМНАЯ ФИЗИКА ТОЯНИЕ ПОЛНОСТЬЮ ОПИСЫВАЕТСЯ НЕНИЕМ ШРЕДИНГЕРА НЕРГИЯ ЭЛЕКТРОНА И ВОЛНОВАЯ ФУНКЦИЯ – ИСЯТ ОТ НЕКОТОРЫХ МЕННЫХ, ВВЕДЁННЫХ ДЛЯ УДОБСТВА ФОРМА ОРБИТАЛИ ЛЕГКО ОПИСЫВАЕТСЯ ЭТИМИ E = f(n)
 ПОЧЕМУ ИМЕННО ТАК? ВЕРОЯТНОСТЬ И АТОМНАЯ ФИЗИКА ТОЯНИЕ ПОЛНОСТЬЮ ОПИСЫВАЕТСЯ НЕНИЕМ ШРЕДИНГЕРА НЕРГИЯ ЭЛЕКТРОНА И ВОЛНОВАЯ ФУНКЦИЯ – ИСЯТ ОТ НЕКОТОРЫХ МЕННЫХ, ВВЕДЁННЫХ ДЛЯ УДОБСТВА ФОРМА ОРБИТАЛИ ЛЕГКО ОПИСЫВАЕТСЯ ЭТИМИ E = f(n)
ПОЧЕМУ ИМЕННО ТАК? ВЕРОЯТНОСТЬ И АТОМНАЯ ФИЗИКА ТОЯНИЕ ПОЛНОСТЬЮ ОПИСЫВАЕТСЯ НЕНИЕМ ШРЕДИНГЕРА НЕРГИЯ ЭЛЕКТРОНА И ВОЛНОВАЯ ФУНКЦИЯ – ИСЯТ ОТ НЕКОТОРЫХ МЕННЫХ, ВВЕДЁННЫХ ДЛЯ УДОБСТВА ФОРМА ОРБИТАЛИ ЛЕГКО ОПИСЫВАЕТСЯ ЭТИМИ E = f(n)
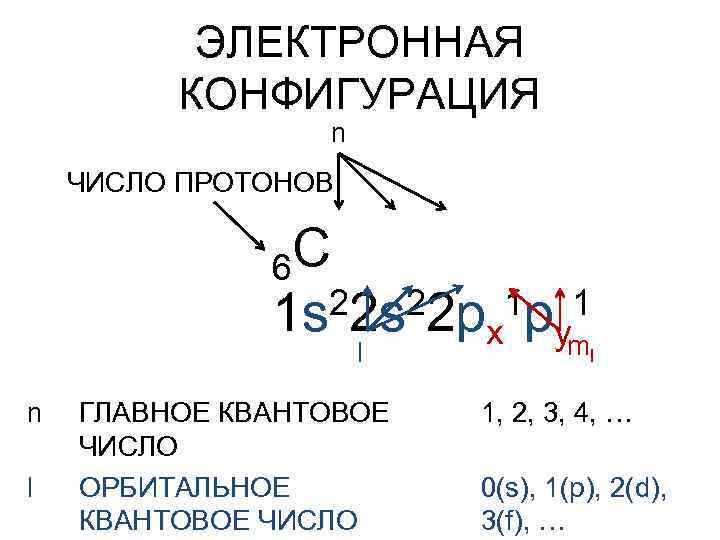 ЭЛЕКТРОННАЯ КОНФИГУРАЦИЯ n ЧИСЛО ПРОТОНОВ 6 C 22 s 22 p 1 p 1 1 s x yml l n l ГЛАВНОЕ КВАНТОВОЕ ЧИСЛО ОРБИТАЛЬНОЕ КВАНТОВОЕ ЧИСЛО 1, 2, 3, 4, … 0(s), 1(p), 2(d), 3(f), …
ЭЛЕКТРОННАЯ КОНФИГУРАЦИЯ n ЧИСЛО ПРОТОНОВ 6 C 22 s 22 p 1 p 1 1 s x yml l n l ГЛАВНОЕ КВАНТОВОЕ ЧИСЛО ОРБИТАЛЬНОЕ КВАНТОВОЕ ЧИСЛО 1, 2, 3, 4, … 0(s), 1(p), 2(d), 3(f), …
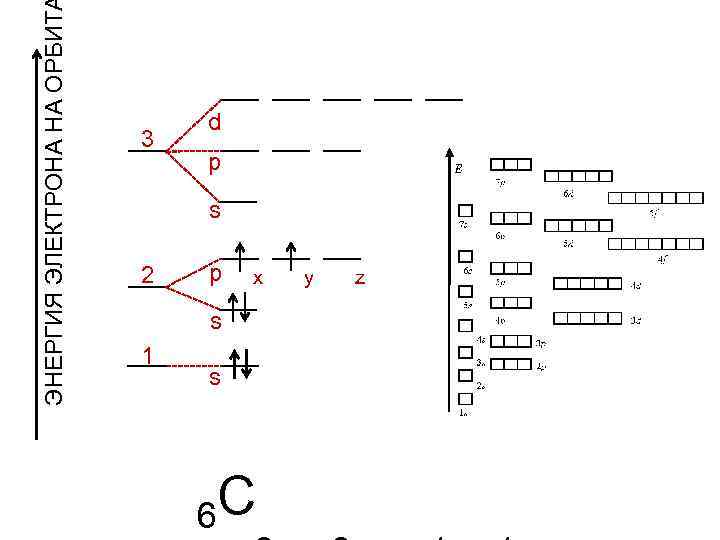 ЭНЕРГИЯ ЭЛЕКТРОНА НА ОРБИТ 3 2 1 d p s p x s s 6 C y z
ЭНЕРГИЯ ЭЛЕКТРОНА НА ОРБИТ 3 2 1 d p s p x s s 6 C y z
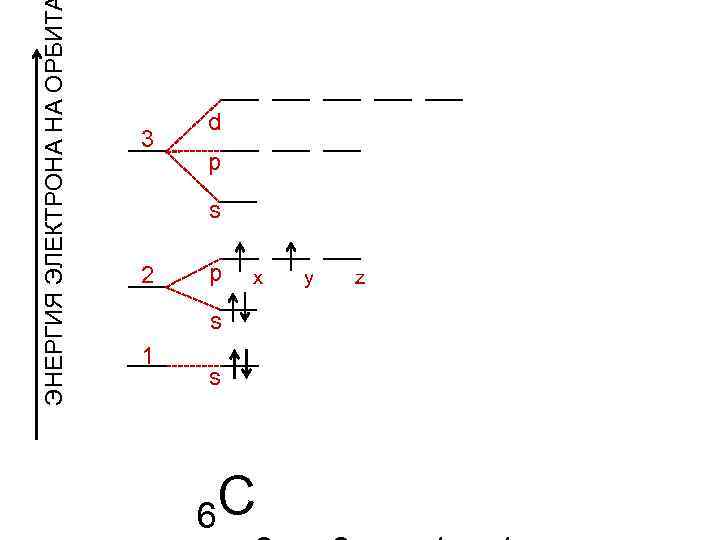 ЭНЕРГИЯ ЭЛЕКТРОНА НА ОРБИТ 3 2 1 d p s p x s s 6 C y z
ЭНЕРГИЯ ЭЛЕКТРОНА НА ОРБИТ 3 2 1 d p s p x s s 6 C y z
 ЭНЕРГЕТИЧЕСКИ ВЫГОДНО • ПРИНЦИП ПАУЛИ - ОДНУ ОРБИТАЛЬ ЗАНИМАЮТ МАКСИМУМ ДВА ЭЛЕКТРОНА С ПРОТИВОПОЛОЖНЫМ СПИНОМ • ПРАВИЛО КЛЕЧКОВСКОГО – ЗАПОЛНЕНИЕ ПРОИСХОДИТ ПО МЕРЕ ВОЗРАСТАНИЯ СУММЫ [n+l] • ЗАПРЕТ ХУНДА – СУММАРНЫЙ СПИН ДОЛЖЕН БЫТЬ МАКСИМАЛЬНЫМ
ЭНЕРГЕТИЧЕСКИ ВЫГОДНО • ПРИНЦИП ПАУЛИ - ОДНУ ОРБИТАЛЬ ЗАНИМАЮТ МАКСИМУМ ДВА ЭЛЕКТРОНА С ПРОТИВОПОЛОЖНЫМ СПИНОМ • ПРАВИЛО КЛЕЧКОВСКОГО – ЗАПОЛНЕНИЕ ПРОИСХОДИТ ПО МЕРЕ ВОЗРАСТАНИЯ СУММЫ [n+l] • ЗАПРЕТ ХУНДА – СУММАРНЫЙ СПИН ДОЛЖЕН БЫТЬ МАКСИМАЛЬНЫМ
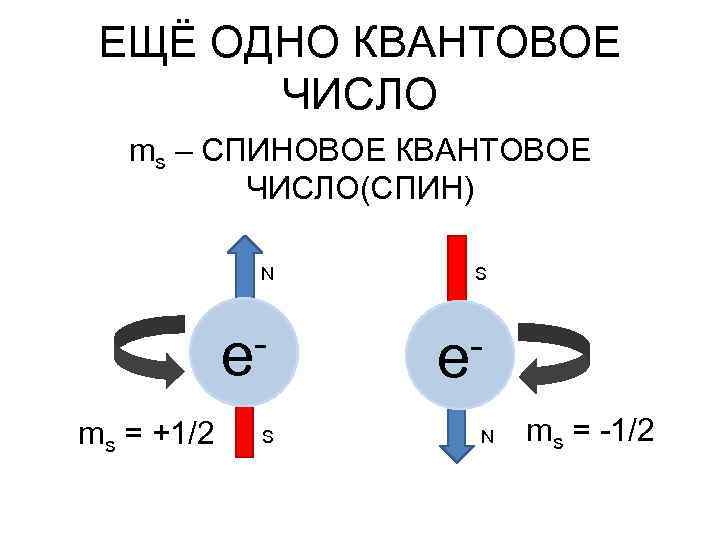 ЕЩЁ ОДНО КВАНТОВОЕ ЧИСЛО ms – СПИНОВОЕ КВАНТОВОЕ ЧИСЛО(СПИН) N e ms = +1/2 S S e N ms = -1/2
ЕЩЁ ОДНО КВАНТОВОЕ ЧИСЛО ms – СПИНОВОЕ КВАНТОВОЕ ЧИСЛО(СПИН) N e ms = +1/2 S S e N ms = -1/2
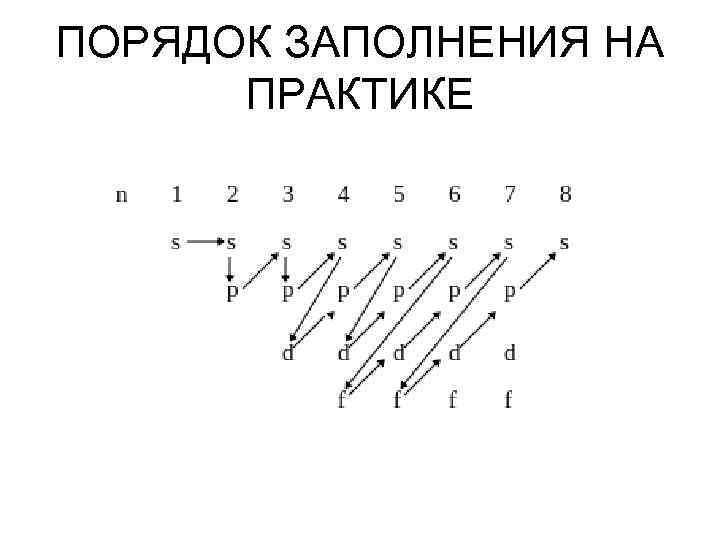 ПОРЯДОК ЗАПОЛНЕНИЯ НА ПРАКТИКЕ
ПОРЯДОК ЗАПОЛНЕНИЯ НА ПРАКТИКЕ
 ЭНЕРГИЯ ЭЛЕКТРОНА НА ОРБИТ НЕ ВСЁ ТАК СЛОЖНО 3 d p s 2 p x s 1 s 6 C y z
ЭНЕРГИЯ ЭЛЕКТРОНА НА ОРБИТ НЕ ВСЁ ТАК СЛОЖНО 3 d p s 2 p x s 1 s 6 C y z
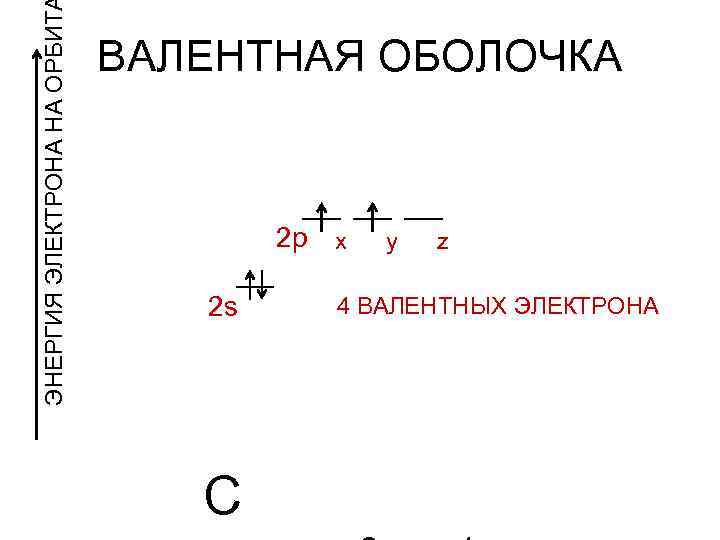 ЭНЕРГИЯ ЭЛЕКТРОНА НА ОРБИТ ВАЛЕНТНАЯ ОБОЛОЧКА 2 p x 2 s C y z 4 ВАЛЕНТНЫХ ЭЛЕКТРОНА
ЭНЕРГИЯ ЭЛЕКТРОНА НА ОРБИТ ВАЛЕНТНАЯ ОБОЛОЧКА 2 p x 2 s C y z 4 ВАЛЕНТНЫХ ЭЛЕКТРОНА
 ГИЛБЕРТ НЬЮТОН ЛЬЮИС 1. ЭЛЕКТРОНЫ ОБОЗНАЧАЮТСЯ ТОЧКАМИ У СИМВОЛА ЭЛЕМЕНТА 2. ЗАВЕРШЕННЫЙ ЭЛЕКТРОННЫЙ СЛОЙ СОДЕРЖИТ 8 ЭЛЕКТРОНОВ – ПРАВИЛО 2 p x ОКТЕТА y z 2 s 4 ВАЛЕНТНЫХ ЭЛЕКТРОНА
ГИЛБЕРТ НЬЮТОН ЛЬЮИС 1. ЭЛЕКТРОНЫ ОБОЗНАЧАЮТСЯ ТОЧКАМИ У СИМВОЛА ЭЛЕМЕНТА 2. ЗАВЕРШЕННЫЙ ЭЛЕКТРОННЫЙ СЛОЙ СОДЕРЖИТ 8 ЭЛЕКТРОНОВ – ПРАВИЛО 2 p x ОКТЕТА y z 2 s 4 ВАЛЕНТНЫХ ЭЛЕКТРОНА
 ГИЛБЕРТ НЬЮТОН ЛЬЮИС 1. ЭЛЕКТРОНЫ ОБОЗНАЧАЮТСЯ ТОЧКАМИ У СИМВОЛА ЭЛЕМЕНТА 2. ЗАВЕРШЕННЫЙ ЭЛЕКТРОННЫЙ СЛОЙ СОДЕРЖИТ 8 ЭЛЕКТРОНОВ – ПРАВИЛО 2 p x ОКТЕТА y z 2 s 4 ВАЛЕНТНЫХ ЭЛЕКТРОНА
ГИЛБЕРТ НЬЮТОН ЛЬЮИС 1. ЭЛЕКТРОНЫ ОБОЗНАЧАЮТСЯ ТОЧКАМИ У СИМВОЛА ЭЛЕМЕНТА 2. ЗАВЕРШЕННЫЙ ЭЛЕКТРОННЫЙ СЛОЙ СОДЕРЖИТ 8 ЭЛЕКТРОНОВ – ПРАВИЛО 2 p x ОКТЕТА y z 2 s 4 ВАЛЕНТНЫХ ЭЛЕКТРОНА
 МОДЕЛЬ СВЯЗИ ВСЁ ПРОСТО, НЕОБХОДИМО ЗАВЕРШИТЬ ОБОЛОЧКУ ПЕРЕДАЧЕЙ ЭЛЕКТРОНА (ИОННАЯ СВЯЗЬ): ЛИБО ОБРАЗОВАНИЕМ ПАРЫ (КОВАЛЕНТНАЯ СВЯЗЬ):
МОДЕЛЬ СВЯЗИ ВСЁ ПРОСТО, НЕОБХОДИМО ЗАВЕРШИТЬ ОБОЛОЧКУ ПЕРЕДАЧЕЙ ЭЛЕКТРОНА (ИОННАЯ СВЯЗЬ): ЛИБО ОБРАЗОВАНИЕМ ПАРЫ (КОВАЛЕНТНАЯ СВЯЗЬ):
 ЭЛЕКТРООТРИЦАТЕЛЬНОСТ Ь
ЭЛЕКТРООТРИЦАТЕЛЬНОСТ Ь
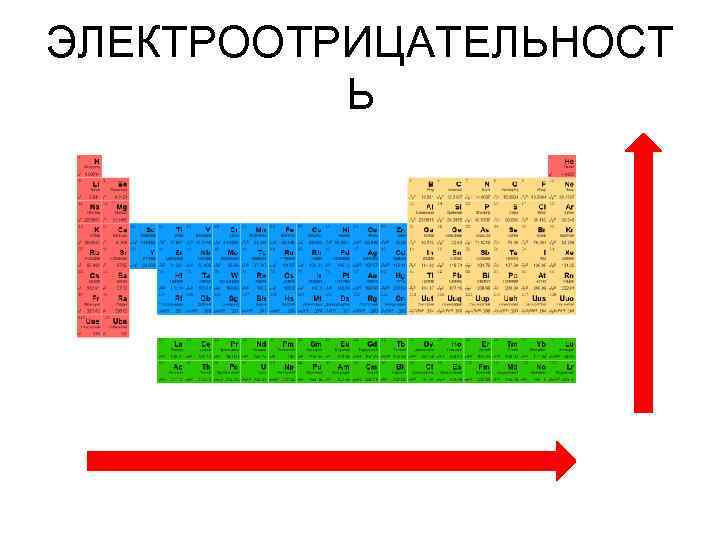 ЭЛЕКТРООТРИЦАТЕЛЬНОСТ Ь
ЭЛЕКТРООТРИЦАТЕЛЬНОСТ Ь
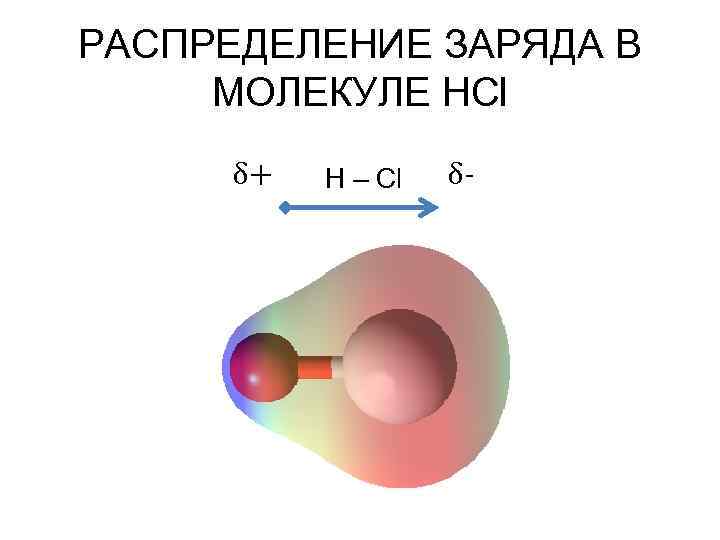 РАСПРЕДЕЛЕНИЕ ЗАРЯДА В МОЛЕКУЛЕ HCl δ+ H – Cl δ-
РАСПРЕДЕЛЕНИЕ ЗАРЯДА В МОЛЕКУЛЕ HCl δ+ H – Cl δ-
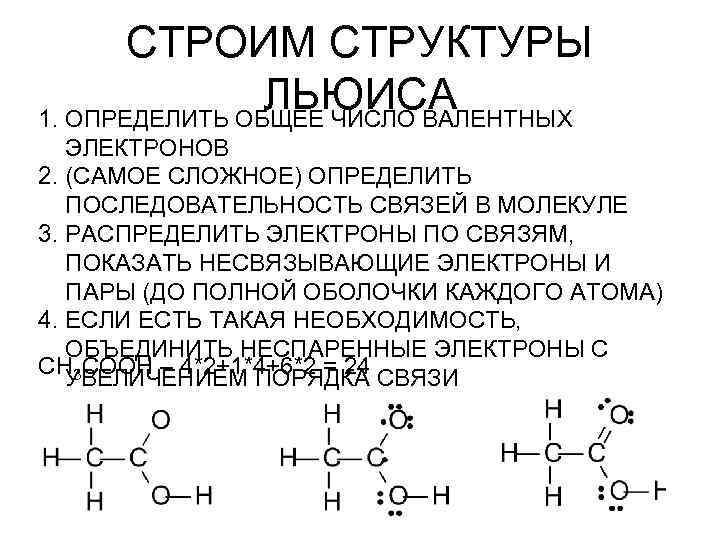 СТРОИМ СТРУКТУРЫ ЛЬЮИСА 1. ОПРЕДЕЛИТЬ ОБЩЕЕ ЧИСЛО ВАЛЕНТНЫХ ЭЛЕКТРОНОВ 2. (САМОЕ СЛОЖНОЕ) ОПРЕДЕЛИТЬ ПОСЛЕДОВАТЕЛЬНОСТЬ СВЯЗЕЙ В МОЛЕКУЛЕ 3. РАСПРЕДЕЛИТЬ ЭЛЕКТРОНЫ ПО СВЯЗЯМ, ПОКАЗАТЬ НЕСВЯЗЫВАЮЩИЕ ЭЛЕКТРОНЫ И ПАРЫ (ДО ПОЛНОЙ ОБОЛОЧКИ КАЖДОГО АТОМА) 4. ЕСЛИ ЕСТЬ ТАКАЯ НЕОБХОДИМОСТЬ, ОБЪЕДИНИТЬ НЕСПАРЕННЫЕ ЭЛЕКТРОНЫ С CH 3 COOH – 4*2+1*4+6*2 = 24 УВЕЛИЧЕНИЕМ ПОРЯДКА СВЯЗИ
СТРОИМ СТРУКТУРЫ ЛЬЮИСА 1. ОПРЕДЕЛИТЬ ОБЩЕЕ ЧИСЛО ВАЛЕНТНЫХ ЭЛЕКТРОНОВ 2. (САМОЕ СЛОЖНОЕ) ОПРЕДЕЛИТЬ ПОСЛЕДОВАТЕЛЬНОСТЬ СВЯЗЕЙ В МОЛЕКУЛЕ 3. РАСПРЕДЕЛИТЬ ЭЛЕКТРОНЫ ПО СВЯЗЯМ, ПОКАЗАТЬ НЕСВЯЗЫВАЮЩИЕ ЭЛЕКТРОНЫ И ПАРЫ (ДО ПОЛНОЙ ОБОЛОЧКИ КАЖДОГО АТОМА) 4. ЕСЛИ ЕСТЬ ТАКАЯ НЕОБХОДИМОСТЬ, ОБЪЕДИНИТЬ НЕСПАРЕННЫЕ ЭЛЕКТРОНЫ С CH 3 COOH – 4*2+1*4+6*2 = 24 УВЕЛИЧЕНИЕМ ПОРЯДКА СВЯЗИ
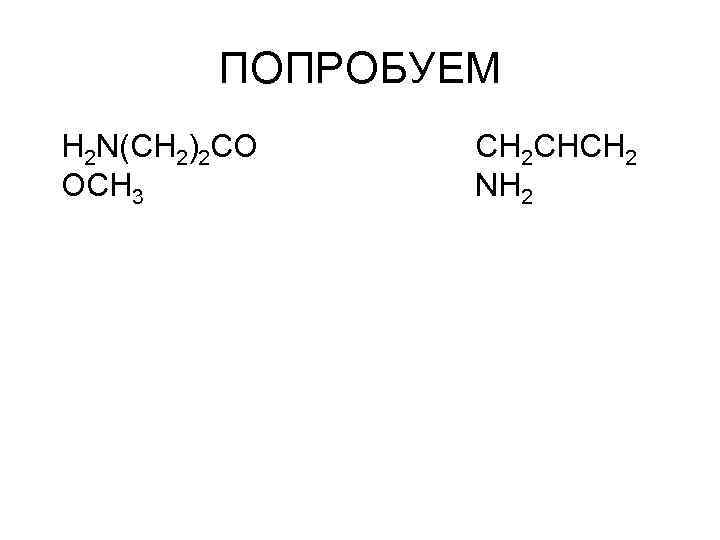 ПОПРОБУЕМ H 2 N(CH 2)2 CO OCH 3 CH 2 CHCH 2 NH 2
ПОПРОБУЕМ H 2 N(CH 2)2 CO OCH 3 CH 2 CHCH 2 NH 2
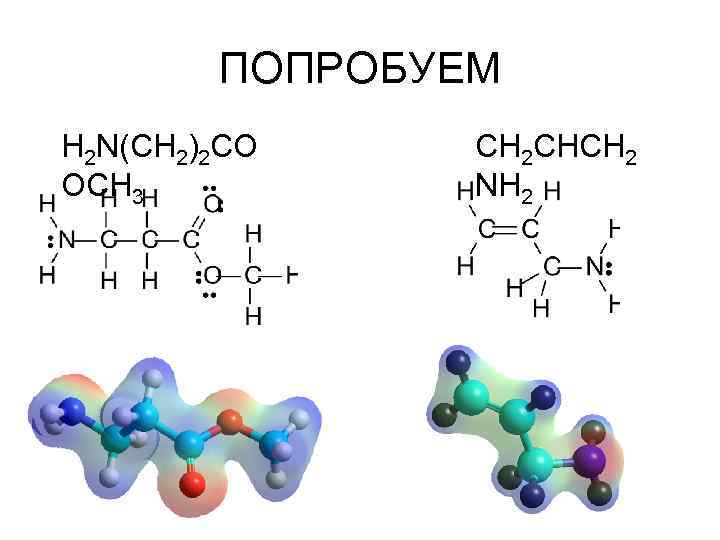 ПОПРОБУЕМ H 2 N(CH 2)2 CO OCH 3 CH 2 CHCH 2 NH 2
ПОПРОБУЕМ H 2 N(CH 2)2 CO OCH 3 CH 2 CHCH 2 NH 2
 ГЕОМЕТРИЯ МОЛЕКУЛ ТЕОРИЯ ОТТАЛКИВАНИЯ ЭЛЕКТРОННЫХ ПАР ВАЛЕНТНЫХ ОРБИТАЛЕЙ (ОЭПВО/VSEPR) СТРАШНО? И ПРАВИЛЬНО
ГЕОМЕТРИЯ МОЛЕКУЛ ТЕОРИЯ ОТТАЛКИВАНИЯ ЭЛЕКТРОННЫХ ПАР ВАЛЕНТНЫХ ОРБИТАЛЕЙ (ОЭПВО/VSEPR) СТРАШНО? И ПРАВИЛЬНО
 ГЕОМЕТРИЯ МОЛЕКУЛ ТЕОРИЯ ОТТАЛКИВАНИЯ ЭЛЕКТРОННЫХ ПАР ВАЛЕНТНЫХ ОРБИТАЛЕЙ (ОЭПВО/VSEPR) МОЛЕКУЛА ВСЕГДА БУДЕТ ПРИНИМАТЬ ФОРМУ, ПРИ КОТОРОЙ ОТТАЛКИВАНИЕ ВНЕШНИХ ЭЛЕКТРОННЫХ ПАР МИНИМАЛЬНО
ГЕОМЕТРИЯ МОЛЕКУЛ ТЕОРИЯ ОТТАЛКИВАНИЯ ЭЛЕКТРОННЫХ ПАР ВАЛЕНТНЫХ ОРБИТАЛЕЙ (ОЭПВО/VSEPR) МОЛЕКУЛА ВСЕГДА БУДЕТ ПРИНИМАТЬ ФОРМУ, ПРИ КОТОРОЙ ОТТАЛКИВАНИЕ ВНЕШНИХ ЭЛЕКТРОННЫХ ПАР МИНИМАЛЬНО
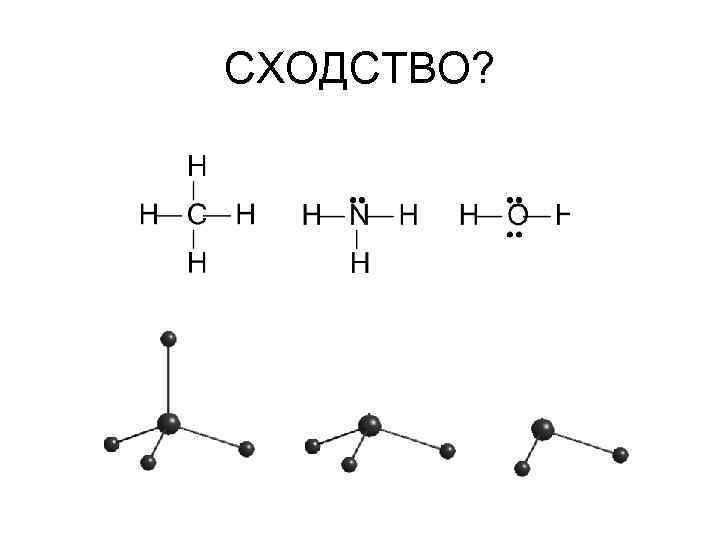 СХОДСТВО?
СХОДСТВО?
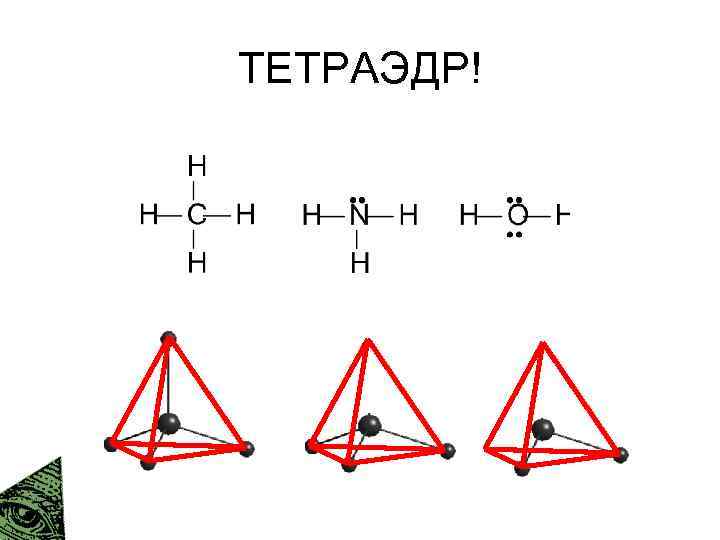 ТЕТРАЭДР!
ТЕТРАЭДР!
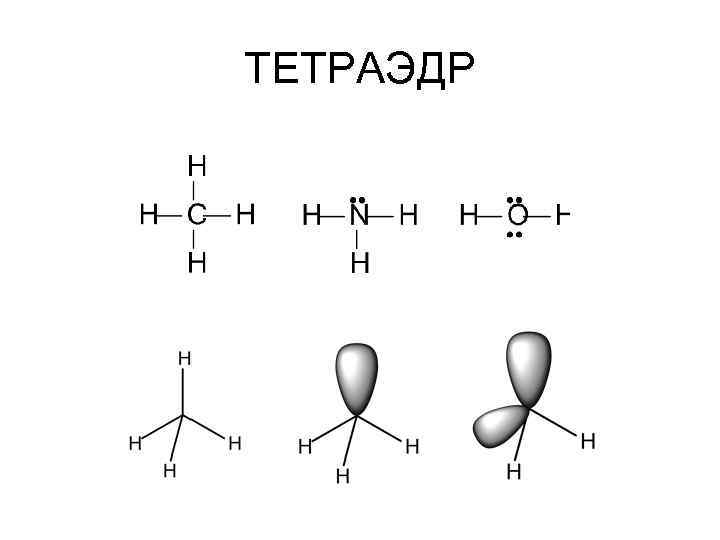 ТЕТРАЭДР
ТЕТРАЭДР
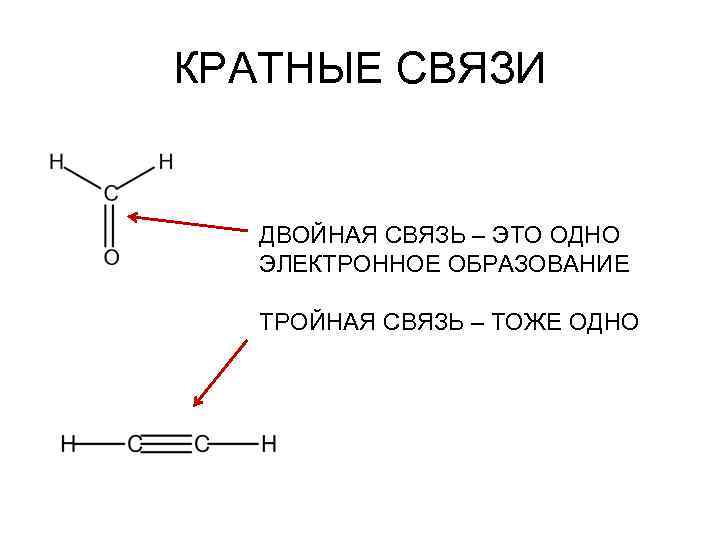 КРАТНЫЕ СВЯЗИ ДВОЙНАЯ СВЯЗЬ – ЭТО ОДНО ЭЛЕКТРОННОЕ ОБРАЗОВАНИЕ ТРОЙНАЯ СВЯЗЬ – ТОЖЕ ОДНО
КРАТНЫЕ СВЯЗИ ДВОЙНАЯ СВЯЗЬ – ЭТО ОДНО ЭЛЕКТРОННОЕ ОБРАЗОВАНИЕ ТРОЙНАЯ СВЯЗЬ – ТОЖЕ ОДНО
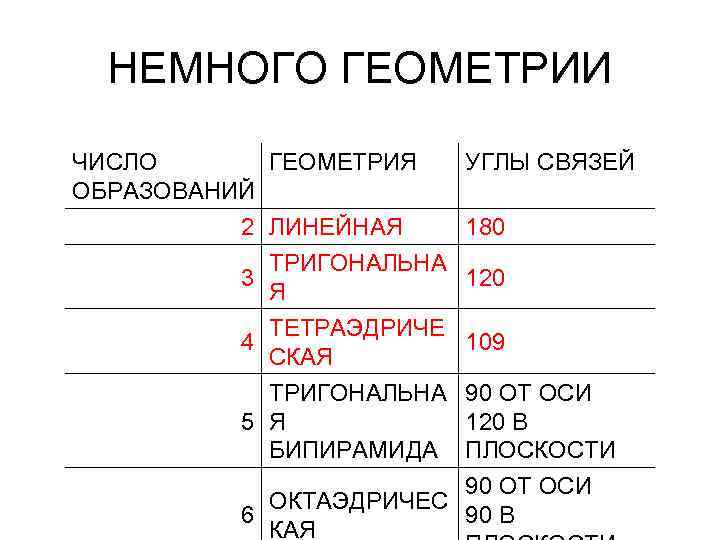 НЕМНОГО ГЕОМЕТРИИ ЧИСЛО ГЕОМЕТРИЯ ОБРАЗОВАНИЙ УГЛЫ СВЯЗЕЙ 2 ЛИНЕЙНАЯ 180 ТРИГОНАЛЬНА 3 120 Я ТЕТРАЭДРИЧЕ 4 109 СКАЯ ТРИГОНАЛЬНА 90 ОТ ОСИ 5 Я 120 В БИПИРАМИДА ПЛОСКОСТИ 90 ОТ ОСИ ОКТАЭДРИЧЕС 6 90 В КАЯ
НЕМНОГО ГЕОМЕТРИИ ЧИСЛО ГЕОМЕТРИЯ ОБРАЗОВАНИЙ УГЛЫ СВЯЗЕЙ 2 ЛИНЕЙНАЯ 180 ТРИГОНАЛЬНА 3 120 Я ТЕТРАЭДРИЧЕ 4 109 СКАЯ ТРИГОНАЛЬНА 90 ОТ ОСИ 5 Я 120 В БИПИРАМИДА ПЛОСКОСТИ 90 ОТ ОСИ ОКТАЭДРИЧЕС 6 90 В КАЯ
 ПОСЛЕДОВАТЕЛЬНОСТЬ ДЕЙСТВИЙ 1. НАРИСОВАТЬ СТРУКТУРУ ЛЬЮИСА (С УКАЗАНИЕМ НЕПОДЕЛЁННЫХ ПАР) 2. ОПРЕДЕЛИТЬ ЧИСЛО ЭЛЕКТРОННЫХ ОБРАЗОВАНИЙ В ОКРУЖЕНИИ КАЖДОГО АТОМА 3. НАРИСОВАТЬ ПРОСТРАНСТВЕННУЮ СТРУКТУРУ
ПОСЛЕДОВАТЕЛЬНОСТЬ ДЕЙСТВИЙ 1. НАРИСОВАТЬ СТРУКТУРУ ЛЬЮИСА (С УКАЗАНИЕМ НЕПОДЕЛЁННЫХ ПАР) 2. ОПРЕДЕЛИТЬ ЧИСЛО ЭЛЕКТРОННЫХ ОБРАЗОВАНИЙ В ОКРУЖЕНИИ КАЖДОГО АТОМА 3. НАРИСОВАТЬ ПРОСТРАНСТВЕННУЮ СТРУКТУРУ
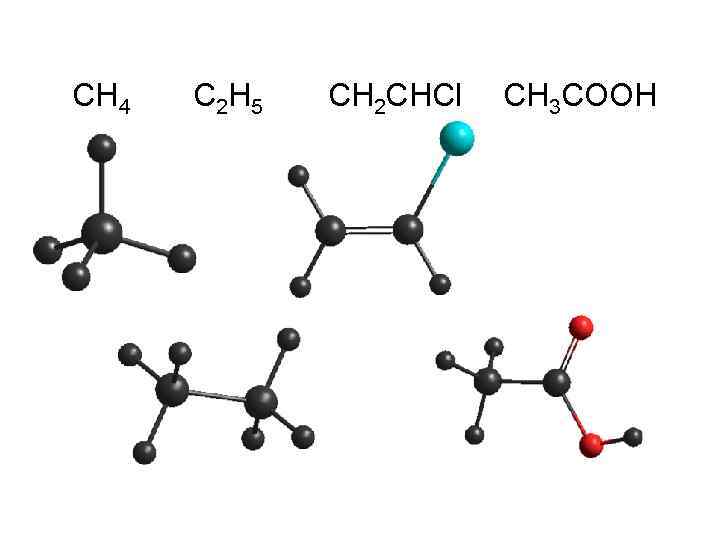 CH 4 C 2 H 5 CH 2 CHCl CH 3 COOH
CH 4 C 2 H 5 CH 2 CHCl CH 3 COOH
 ЗАЧЕМ ЭТО ЗНАТЬ СТРОЕНИЕ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ – ФУНДАМЕНТ ЗНАЯ СТРОЕНИЕ СОЕДИНЕНИЯ, МОЖНО ПРЕДСКАЗАТЬ ЕГО ПОВЕДЕНИЕ ЗНАЯ СТРОЕНИЕ СОЕДИНЕНИЯ, МОЖНО НАЙТИ СПОСОБ ЕГО ПОЛУЧЕНИЯ ДА ЭТО ПРОСТО КРУТО, МОЖНО ДРУЗЬЯМ
ЗАЧЕМ ЭТО ЗНАТЬ СТРОЕНИЕ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ – ФУНДАМЕНТ ЗНАЯ СТРОЕНИЕ СОЕДИНЕНИЯ, МОЖНО ПРЕДСКАЗАТЬ ЕГО ПОВЕДЕНИЕ ЗНАЯ СТРОЕНИЕ СОЕДИНЕНИЯ, МОЖНО НАЙТИ СПОСОБ ЕГО ПОЛУЧЕНИЯ ДА ЭТО ПРОСТО КРУТО, МОЖНО ДРУЗЬЯМ
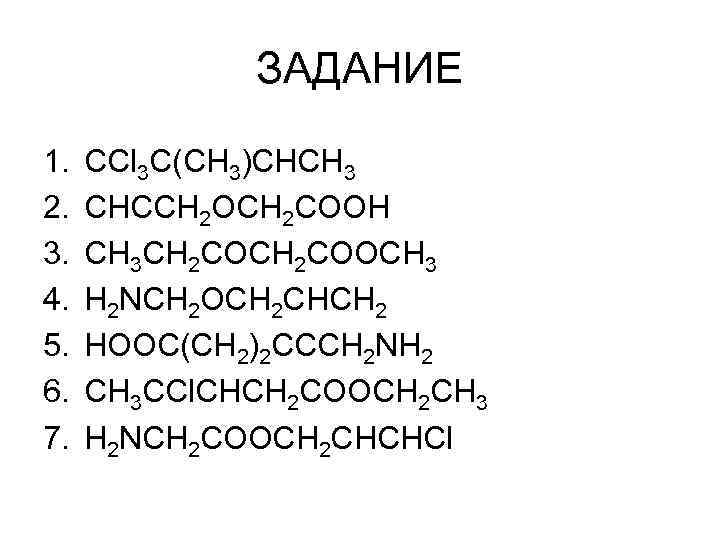 ЗАДАНИЕ 1. 2. 3. 4. 5. 6. 7. CCl 3 C(CH 3)CHCH 3 CHCCH 2 OCH 2 COOH CH 3 CH 2 COOCH 3 H 2 NCH 2 OCH 2 CHCH 2 HOOC(CH 2)2 CCCH 2 NH 2 CH 3 CCl. CHCH 2 СOOCH 2 CH 3 H 2 NCH 2 COOCH 2 CHCHCl
ЗАДАНИЕ 1. 2. 3. 4. 5. 6. 7. CCl 3 C(CH 3)CHCH 3 CHCCH 2 OCH 2 COOH CH 3 CH 2 COOCH 3 H 2 NCH 2 OCH 2 CHCH 2 HOOC(CH 2)2 CCCH 2 NH 2 CH 3 CCl. CHCH 2 СOOCH 2 CH 3 H 2 NCH 2 COOCH 2 CHCHCl
 ДОПОЛНИТЕЛЬНОЕ ЗАДАНИЕ • • СH 3 COOCH 2 CCCH 2 NHCH 3 CHCl 2 CCH 3 C(CH 3)CH 2 COOCH 3 C(CH 2 CHCH 2)CHCH 2 SH CHCl. C(CN)CH 2 COOCH 2 CH 3
ДОПОЛНИТЕЛЬНОЕ ЗАДАНИЕ • • СH 3 COOCH 2 CCCH 2 NHCH 3 CHCl 2 CCH 3 C(CH 3)CH 2 COOCH 3 C(CH 2 CHCH 2)CHCH 2 SH CHCl. C(CN)CH 2 COOCH 2 CH 3


