Опухоли печени и желчных протоков-1.pptx
- Количество слайдов: 156
 Опухоли печени. Диагностика и лечение 5 -й курс. Мед. факультет МГУ
Опухоли печени. Диагностика и лечение 5 -й курс. Мед. факультет МГУ
 Общая оболочка сосудистобилиарных структур печени впервые описана голландским врачом Johannis Walaeus в 1640 г. (Walaeus’ tunic), затем в 1654 г. – английским анатомом и физиологом Francis Glisson. Внутрипеченочные сосуды From Glisson, F. : Anatomia Hepatis. London, 1654. Исключительную важность сосудисто-билиарных футляров для хирургической анатомии печени впервые показал в своих работах Claude Couinaud (1957, 1989), который считал их с «хирургической точки зрения … важнейшей структурой в анатомии печени»
Общая оболочка сосудистобилиарных структур печени впервые описана голландским врачом Johannis Walaeus в 1640 г. (Walaeus’ tunic), затем в 1654 г. – английским анатомом и физиологом Francis Glisson. Внутрипеченочные сосуды From Glisson, F. : Anatomia Hepatis. London, 1654. Исключительную важность сосудисто-билиарных футляров для хирургической анатомии печени впервые показал в своих работах Claude Couinaud (1957, 1989), который считал их с «хирургической точки зрения … важнейшей структурой в анатомии печени»
 Описание первой успешной резекции печени по поводу очагового образования, выполненной в 1887 г. , принадлежит K. Langenbuch, хотя несколько наблюдений резекции печени по поводу крупных очаговых образований немногим ранее опубликовали J. W. Cousins в 1874, A. Lius в 1886 и Escher в 1886. Тем не менее, ни одна из этих резекций не привела к выздоровлению больного. Три успешных резекции печени по поводу очаговых образований выполнил за период с 1891 по 1899 гг. американский хирург W. W. Keen, которому также принадлежит приоритет впервые выполненной резекции печени в США. Carl Langenbuch (1846 – 1881)
Описание первой успешной резекции печени по поводу очагового образования, выполненной в 1887 г. , принадлежит K. Langenbuch, хотя несколько наблюдений резекции печени по поводу крупных очаговых образований немногим ранее опубликовали J. W. Cousins в 1874, A. Lius в 1886 и Escher в 1886. Тем не менее, ни одна из этих резекций не привела к выздоровлению больного. Три успешных резекции печени по поводу очаговых образований выполнил за период с 1891 по 1899 гг. американский хирург W. W. Keen, которому также принадлежит приоритет впервые выполненной резекции печени в США. Carl Langenbuch (1846 – 1881)
 В 1951 г. выходит работа C. H. Hjortsjo, впервые показавшего, что распределение желчных протоков и артерий в печени носит сегментарный характер. Его результаты подтверждаются в 1952 г. публикацией H. Elias и D. Petty, а годом позднее работой J. E. Healy a nd P. C. Schroy. Фундаментальные работы, касающиеся сегментарной анатомии воротной вены, были опубликованы в 1954 г. C. Couinaud, а в 1957 г - N. A. Goldsmith и R. T. Woodburne Claude Couinaud
В 1951 г. выходит работа C. H. Hjortsjo, впервые показавшего, что распределение желчных протоков и артерий в печени носит сегментарный характер. Его результаты подтверждаются в 1952 г. публикацией H. Elias и D. Petty, а годом позднее работой J. E. Healy a nd P. C. Schroy. Фундаментальные работы, касающиеся сегментарной анатомии воротной вены, были опубликованы в 1954 г. C. Couinaud, а в 1957 г - N. A. Goldsmith и R. T. Woodburne Claude Couinaud
 В. С. Шапкин (1918 – 1998) В 1964 г. защита докторской диссертации «Анатомические резекции печени (клинико-экспериментальное исследование)» . К моменту защиты докторской диссертации В. С. Шапкиным в центральной печати были опубликованы 17 работ, посвященных хирургической анатомии, технике анатомических резекций при очаговых заболеваниях и травме печени, а также послеоперационным осложнениям. В 1967 г. опубликован первый в отечественной литературе капитальный труд "Резекция печени (хирургическая анатомия и техника операций)" (Москва). На основе долевого и сегментарного строения печени подробно изучена и разработана техника разного рода анатомических резекций и других вмешательств на печени.
В. С. Шапкин (1918 – 1998) В 1964 г. защита докторской диссертации «Анатомические резекции печени (клинико-экспериментальное исследование)» . К моменту защиты докторской диссертации В. С. Шапкиным в центральной печати были опубликованы 17 работ, посвященных хирургической анатомии, технике анатомических резекций при очаговых заболеваниях и травме печени, а также послеоперационным осложнениям. В 1967 г. опубликован первый в отечественной литературе капитальный труд "Резекция печени (хирургическая анатомия и техника операций)" (Москва). На основе долевого и сегментарного строения печени подробно изучена и разработана техника разного рода анатомических резекций и других вмешательств на печени.
 Подчеркивая исключительную важность изучения сегментарной анатомии печени J. E. Healey в 1954 г. писал: «Хотя первая радикальная операция на печени была выполнена в 1886 г. , техника резекций печени с тех пор претерпела мало изменений. Основной причиной тому является полная неосведомленность как хирургов, так и анатомов, о внутрипеченочном расположении и распределении крупных сосудов и желчных протоков… В связи с этим неудивительно, что на сегодняшний день летальность при парциальных резекциях мало отличается от уровня смертности при аналогичных операциях в 1897 г. » . В результате внедрения принципов анатомической хирургии печени летальность снизилась с 15% в 1960 -х гг. до 2 -3% к началу 1990 гг.
Подчеркивая исключительную важность изучения сегментарной анатомии печени J. E. Healey в 1954 г. писал: «Хотя первая радикальная операция на печени была выполнена в 1886 г. , техника резекций печени с тех пор претерпела мало изменений. Основной причиной тому является полная неосведомленность как хирургов, так и анатомов, о внутрипеченочном расположении и распределении крупных сосудов и желчных протоков… В связи с этим неудивительно, что на сегодняшний день летальность при парциальных резекциях мало отличается от уровня смертности при аналогичных операциях в 1897 г. » . В результате внедрения принципов анатомической хирургии печени летальность снизилась с 15% в 1960 -х гг. до 2 -3% к началу 1990 гг.
 Классификация опухолей печени А. Первичные I. Рак печени: 1. Гепатоцеллюярный рак 2. Холангиоцеллюлярный рак 3. Злокачественная гепатохолангиома – рак смешанного строения II. Злокачественные опухоли печени, не содержащие специфических печеночных элементов 1. Саркома печени. 2. Злокачественная гемангиоэндотелиома (ангиоскаркома) 3. Гипернефрома печени (первичная) 4. Хорионэпителиома 5. Меланома (первичная) 6. Смешанные опухоли (тератомы) и опухоли неясного генеза. Б. Вторичные, или метастатические 1. 2. 3. Рак Саркома Меланома (В. С. Шапкин, 1970)
Классификация опухолей печени А. Первичные I. Рак печени: 1. Гепатоцеллюярный рак 2. Холангиоцеллюлярный рак 3. Злокачественная гепатохолангиома – рак смешанного строения II. Злокачественные опухоли печени, не содержащие специфических печеночных элементов 1. Саркома печени. 2. Злокачественная гемангиоэндотелиома (ангиоскаркома) 3. Гипернефрома печени (первичная) 4. Хорионэпителиома 5. Меланома (первичная) 6. Смешанные опухоли (тератомы) и опухоли неясного генеза. Б. Вторичные, или метастатические 1. 2. 3. Рак Саркома Меланома (В. С. Шапкин, 1970)
 Гистологическая классификация опухолей печени (ВОЗ) Эпителиальные опухоли I. Доброкачественные 1. Гепатоцеллюлярная аденома (печеночно-клеточная аденома) 2. Внутрипеченочная протоковая аденома (Intrahepatic bile duct adenoma) 3. Внутрипеченочная протоковая цистаденома (Intrahepatic bile duct cystadenoma) 4. Папилломатоз желчных протоков (Biliary papillomatosis) II. Злокачественные 1. Гепатоцеллюлярная карцинома (печеночноклеточная карцинома). 2. Внутрипеченончая холангиокарцинома (периферическая протоковая карцинома) 3. Протоковая цистаденокарцинома (Bile duct cystadenocarcinoma) 4. Комбинированная гепатоцеллюлярная и холангиокарцинома 5. Гепатобластома 6. Недифференцированная карцинома (Ishak K. G. et al. , Histological Typing of Tumours of the Liver, 1994)
Гистологическая классификация опухолей печени (ВОЗ) Эпителиальные опухоли I. Доброкачественные 1. Гепатоцеллюлярная аденома (печеночно-клеточная аденома) 2. Внутрипеченочная протоковая аденома (Intrahepatic bile duct adenoma) 3. Внутрипеченочная протоковая цистаденома (Intrahepatic bile duct cystadenoma) 4. Папилломатоз желчных протоков (Biliary papillomatosis) II. Злокачественные 1. Гепатоцеллюлярная карцинома (печеночноклеточная карцинома). 2. Внутрипеченончая холангиокарцинома (периферическая протоковая карцинома) 3. Протоковая цистаденокарцинома (Bile duct cystadenocarcinoma) 4. Комбинированная гепатоцеллюлярная и холангиокарцинома 5. Гепатобластома 6. Недифференцированная карцинома (Ishak K. G. et al. , Histological Typing of Tumours of the Liver, 1994)
 Неэпителиальные опухоли I. Доброкачественные 1. Ангиомиолипома 2. Лимфангиома и лимфангиоматоз 3. Гемангиома 4. Инфантильная гемангиоэндотелиома II. Злокачественные 1. Эпителиоидная гемангиоэндотелиома. 2. Ангиосаркома 3. Недифференцированная саркома (эмбриональная саркома) 4. Рабдомиосаркома 5. Другие Смешанные опухоли 1. Локальная фиброзная опухоль (локальная фиброзная мезотелиома, фиброма) 2. Тератома 3. Опухоль желточного мешка 4. Карциносаркома 5. Саркома Капоши 6. Рабдоидная опухоль 7. Другие (Ishak K. G. et al. , Histological Typing of Tumours of the Liver, 1994)
Неэпителиальные опухоли I. Доброкачественные 1. Ангиомиолипома 2. Лимфангиома и лимфангиоматоз 3. Гемангиома 4. Инфантильная гемангиоэндотелиома II. Злокачественные 1. Эпителиоидная гемангиоэндотелиома. 2. Ангиосаркома 3. Недифференцированная саркома (эмбриональная саркома) 4. Рабдомиосаркома 5. Другие Смешанные опухоли 1. Локальная фиброзная опухоль (локальная фиброзная мезотелиома, фиброма) 2. Тератома 3. Опухоль желточного мешка 4. Карциносаркома 5. Саркома Капоши 6. Рабдоидная опухоль 7. Другие (Ishak K. G. et al. , Histological Typing of Tumours of the Liver, 1994)
 Неклассифицируемые опухоли Опухоли гемопоетической и лимфоидной ткани Метастатические опухоли Эпителиальные аномалии 1. Печеночноклеточная дисплазия 2. Протоковые аномалии Опухолеподобные образования 1. Гамартомы i. Мезенхимальная гамартома ii. Билиартная гамартома 2. Врожденные билиарные кисты 3. Фокальная нодулярная гиперплазия 4. Компенсаторная лобарная гиперплазия 5. Печеночный пелиоз 6. Гетеротопия 7. Узловая трансформация (узловая регенаторная гиперплазия) 8. Аденоматозная гиперплазия 9. Очаговые жировые изменения 10. Воспалительные псевдоопухоли 11. Панкреатические псевдокисты 12. Другие (Ishak K. G. et al. , Histological Typing of Tumours of the Liver, 1994)
Неклассифицируемые опухоли Опухоли гемопоетической и лимфоидной ткани Метастатические опухоли Эпителиальные аномалии 1. Печеночноклеточная дисплазия 2. Протоковые аномалии Опухолеподобные образования 1. Гамартомы i. Мезенхимальная гамартома ii. Билиартная гамартома 2. Врожденные билиарные кисты 3. Фокальная нодулярная гиперплазия 4. Компенсаторная лобарная гиперплазия 5. Печеночный пелиоз 6. Гетеротопия 7. Узловая трансформация (узловая регенаторная гиперплазия) 8. Аденоматозная гиперплазия 9. Очаговые жировые изменения 10. Воспалительные псевдоопухоли 11. Панкреатические псевдокисты 12. Другие (Ishak K. G. et al. , Histological Typing of Tumours of the Liver, 1994)
 Какой диагноз, или с чего начинать? Ø Абсолютное большинство опухолей печени длительное время протекают бессимптомно Ø При появлении клинической симптоматики злокачественные опухоли нередко оказываются нерезектабельными (за исключением опухолей желчных протоков), а большинство доброкачественных опухолей и опухолеподобных образований подлежат удалению независимо от их гистологического строения. В связи с этим практическую значимость приобретают методы лучевой диагностики, которые позволяют определить лечебную тактику на доклинической стадии
Какой диагноз, или с чего начинать? Ø Абсолютное большинство опухолей печени длительное время протекают бессимптомно Ø При появлении клинической симптоматики злокачественные опухоли нередко оказываются нерезектабельными (за исключением опухолей желчных протоков), а большинство доброкачественных опухолей и опухолеподобных образований подлежат удалению независимо от их гистологического строения. В связи с этим практическую значимость приобретают методы лучевой диагностики, которые позволяют определить лечебную тактику на доклинической стадии
 Какой диагноз, или с чего начинать? На доклинических стадиях заболевания диагноз, и, соответственно, тактика лечения основываются на совокупности данных анамнеза и лучевых методов диагностики: 1. Длительность заболевания. 2. Данные МСКТ с внутривенным контрастированием (основной метод диагностики) 3. Данные МРТ (дополнительная информация при неясной картине МСКТ). 4. Данные УЗИ (скрининговая методика). 5. Онкомаркеры (α-фетопротеин, СЕА, СА 19 -9 и др. ). 6. Биопсия.
Какой диагноз, или с чего начинать? На доклинических стадиях заболевания диагноз, и, соответственно, тактика лечения основываются на совокупности данных анамнеза и лучевых методов диагностики: 1. Длительность заболевания. 2. Данные МСКТ с внутривенным контрастированием (основной метод диагностики) 3. Данные МРТ (дополнительная информация при неясной картине МСКТ). 4. Данные УЗИ (скрининговая методика). 5. Онкомаркеры (α-фетопротеин, СЕА, СА 19 -9 и др. ). 6. Биопсия.
 Какой диагноз, или с чего начинать? Биопсия – метод ИНВАЗИВНОЙ диагностики. Основная задача врача при обследовании хирургического больного – определить тактику лечения. Для этого не всегда нужен точный диагноз! Биопсия не нужна, если оперативное лечение показано в связи с: 1. Обоснованным подозрением на наличие злокачественной опухоли 2. Большими размерами доброкачественного образования Биопсия нужна, если все неинвазивные методы диагностики не позволяют ответить на вопрос: «Надо оперировать больного или нет? »
Какой диагноз, или с чего начинать? Биопсия – метод ИНВАЗИВНОЙ диагностики. Основная задача врача при обследовании хирургического больного – определить тактику лечения. Для этого не всегда нужен точный диагноз! Биопсия не нужна, если оперативное лечение показано в связи с: 1. Обоснованным подозрением на наличие злокачественной опухоли 2. Большими размерами доброкачественного образования Биопсия нужна, если все неинвазивные методы диагностики не позволяют ответить на вопрос: «Надо оперировать больного или нет? »
 Какой диагноз, или с чего начинать? Объективный осмотр больного с очаговым образованием печени - дань традиции или обоснованная необходимость?
Какой диагноз, или с чего начинать? Объективный осмотр больного с очаговым образованием печени - дань традиции или обоснованная необходимость?
 Какой диагноз, или с чего начинать? Объективный осмотр решает немногие, но очень важные задачи: 1. Есть ли клинические проявления заболевания? a) У больного со злокачественной опухолью печени: i. пальпируемые лимфоузлы, притупление в отлогих местах живота и ундуляция (асцит) являются косвенными признаками неоперабельности; ii. Существенное снижение веса, бледность (анемия), увеличение печени требуют тщательного обследования на предмет резектабельности опухоли и предоперационной коррекции нарушений гомеостаза iii. Наличие механической желтухи требует декомпрессии протоков
Какой диагноз, или с чего начинать? Объективный осмотр решает немногие, но очень важные задачи: 1. Есть ли клинические проявления заболевания? a) У больного со злокачественной опухолью печени: i. пальпируемые лимфоузлы, притупление в отлогих местах живота и ундуляция (асцит) являются косвенными признаками неоперабельности; ii. Существенное снижение веса, бледность (анемия), увеличение печени требуют тщательного обследования на предмет резектабельности опухоли и предоперационной коррекции нарушений гомеостаза iii. Наличие механической желтухи требует декомпрессии протоков
 Какой диагноз, или с чего начинать? Объективный осмотр решает немногие, но очень важные задачи: 1. Есть ли клинические проявления заболевания? б) У больного с доброкачественной опухолью печени: i. наличие боли при физических нагрузках, дискомфорта в верхних отделах живота, дефигурация живота свидетельствуют о необходимости удаления крупной опухоли; ii. Отсутствие клинических проявлений заболевания ставит под сомнение целесообразность операции, даже при относительно больших размерах образования
Какой диагноз, или с чего начинать? Объективный осмотр решает немногие, но очень важные задачи: 1. Есть ли клинические проявления заболевания? б) У больного с доброкачественной опухолью печени: i. наличие боли при физических нагрузках, дискомфорта в верхних отделах живота, дефигурация живота свидетельствуют о необходимости удаления крупной опухоли; ii. Отсутствие клинических проявлений заболевания ставит под сомнение целесообразность операции, даже при относительно больших размерах образования
 Какой диагноз, или с чего начинать? Объективный осмотр решает немногие, но очень важные задачи: 2. Есть ли проявления других заболеваний, которые могут повысить риск оперативного вмешательства? a. b. c. d. e. f. Сердечно-сосудистой системы Органов дыхания Почек Эндокринной системы ЖКТ Центральной и периферической нервной системы
Какой диагноз, или с чего начинать? Объективный осмотр решает немногие, но очень важные задачи: 2. Есть ли проявления других заболеваний, которые могут повысить риск оперативного вмешательства? a. b. c. d. e. f. Сердечно-сосудистой системы Органов дыхания Почек Эндокринной системы ЖКТ Центральной и периферической нервной системы
 Какой диагноз, или с чего начинать? Очаговые образования печени Жидкостные Доброкачественные очаговые образования (ДОО) Первичные Злокачественные очаговые образования (ЗОО) Метастатические Простые кисты – множественные, тонкостенные Эхинококк – эпид. анамнез, серология, толстая стенка, дочерние кисты Цистаденомы – солитарные, 4 -й сегмент, толстая стенка, женщины Солидные ФНГ, гемангиомы – длительный анамнез, характерные изменения на КТ, частые солидные ДОО Аденомы – длительный анамнез, нехарактерные изменения на КТ, встречаются крайне редко Цистаденокарциномы – солитарные, толстая стенка, крайне редки ГЦР – короткий анамнез, гепатит, цирроз, онкомаркеры, характерные изменения на КТ ХЦР – короткий анамнез, желтуха, онкомаркеры, нехарактерные изменения на КТ Рак яичников – множественные, толстая стенка, анамнез, онкомаркеры Колоректальный и другие раки – анамнез, онкомаркеры, нехарактерные изменения на КТ,
Какой диагноз, или с чего начинать? Очаговые образования печени Жидкостные Доброкачественные очаговые образования (ДОО) Первичные Злокачественные очаговые образования (ЗОО) Метастатические Простые кисты – множественные, тонкостенные Эхинококк – эпид. анамнез, серология, толстая стенка, дочерние кисты Цистаденомы – солитарные, 4 -й сегмент, толстая стенка, женщины Солидные ФНГ, гемангиомы – длительный анамнез, характерные изменения на КТ, частые солидные ДОО Аденомы – длительный анамнез, нехарактерные изменения на КТ, встречаются крайне редко Цистаденокарциномы – солитарные, толстая стенка, крайне редки ГЦР – короткий анамнез, гепатит, цирроз, онкомаркеры, характерные изменения на КТ ХЦР – короткий анамнез, желтуха, онкомаркеры, нехарактерные изменения на КТ Рак яичников – множественные, толстая стенка, анамнез, онкомаркеры Колоректальный и другие раки – анамнез, онкомаркеры, нехарактерные изменения на КТ,
 Гепатоцеллюлярный рак (ГЦР) Эпидемиология: Наиболее частая первичная злокачественная опухоль , которая составляет 8085% от всех злокачественных эпителиальных опухолей печени. По частоте среди всех злокачественных опухолей в мире ГЦР занимает 5 -е место. Ежегодно от ГЦР умирает 500, 000 человек. Этиология ГЦР продолжает изучаться, но очевидно, что первичный печеночноклеточный рак почти никогда не развивается в неповрежденной печеночной ткани. Наиболее частой причиной ГЦР в мире является цирроз печени – в исходе вирусного или алкогольного гепатита. Вирусный гепатит В является наиболее частой причиной развития ГЦР в странах Африки и Азии, вирусный гепатит С – в Японии, Европе и США. Заболевание чаще встречается у мужчин. Соотношение заболевших мужчин и женщин в среднем в мире составляет 2: 1; в развивающихся странах - 2. 4: 1; в Швейцарии – 4: 1, в Италии 5: 1.
Гепатоцеллюлярный рак (ГЦР) Эпидемиология: Наиболее частая первичная злокачественная опухоль , которая составляет 8085% от всех злокачественных эпителиальных опухолей печени. По частоте среди всех злокачественных опухолей в мире ГЦР занимает 5 -е место. Ежегодно от ГЦР умирает 500, 000 человек. Этиология ГЦР продолжает изучаться, но очевидно, что первичный печеночноклеточный рак почти никогда не развивается в неповрежденной печеночной ткани. Наиболее частой причиной ГЦР в мире является цирроз печени – в исходе вирусного или алкогольного гепатита. Вирусный гепатит В является наиболее частой причиной развития ГЦР в странах Африки и Азии, вирусный гепатит С – в Японии, Европе и США. Заболевание чаще встречается у мужчин. Соотношение заболевших мужчин и женщин в среднем в мире составляет 2: 1; в развивающихся странах - 2. 4: 1; в Швейцарии – 4: 1, в Италии 5: 1.
 Гепатоцеллюлярный рак (ГЦР) Эпидемиология: Частота ГЦР на 100. 000 населения среди мужчин
Гепатоцеллюлярный рак (ГЦР) Эпидемиология: Частота ГЦР на 100. 000 населения среди мужчин
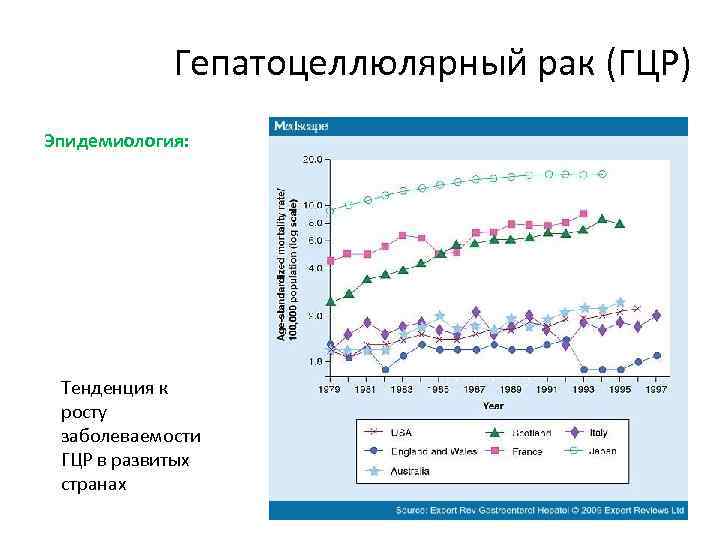 Гепатоцеллюлярный рак (ГЦР) Эпидемиология: Тенденция к росту заболеваемости ГЦР в развитых странах
Гепатоцеллюлярный рак (ГЦР) Эпидемиология: Тенденция к росту заболеваемости ГЦР в развитых странах
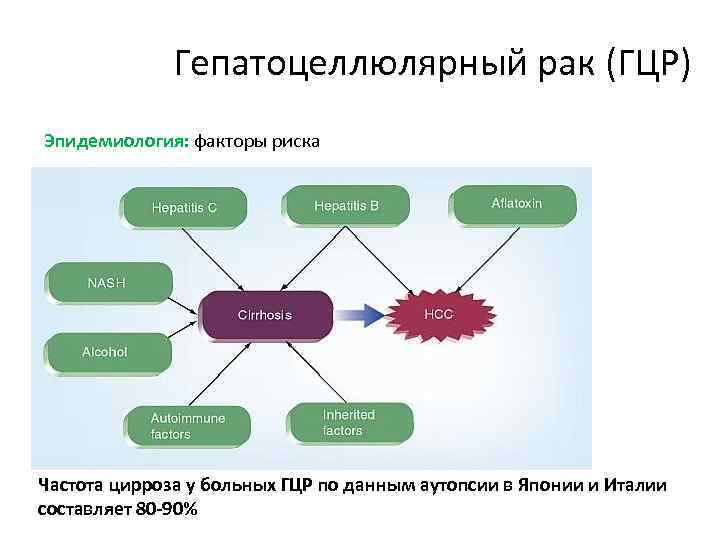 Гепатоцеллюлярный рак (ГЦР) Эпидемиология: факторы риска Частота цирроза у больных ГЦР по данным аутопсии в Японии и Италии составляет 80 -90%
Гепатоцеллюлярный рак (ГЦР) Эпидемиология: факторы риска Частота цирроза у больных ГЦР по данным аутопсии в Японии и Италии составляет 80 -90%
 Гепатоцеллюлярный рак (ГЦР) Эпидемиология: Частота развития ГЦР мало зависит от этиологии цирроза, но, тем не менее, прослеживается относительно более высокая частота возникновения ГЦР на фоне цирроза в исходе гепатита С. Кумулятивная 5 -летняя заболеваемость ГЦР при НСVассоциированном циррозе составляет 17% в Европе и США и 30% в Японии. Для гепатита В этот показатель составляет 15% в эндемичных регионах и 10% в развитых странах. Кроме того, гепатит В может приводить к развитию ГЦР без цирроза, что повышает риск возникновения ГЦР в популяции больных гепатитом В до 25%. Fattovich G, Stroffolini T, Zagni I, Donato F. Hepatocellular carcinoma in cirrhosis: incidence and risk factors. Gastroenterology 127(5 Suppl. 1), S 35– S 50 (2004).
Гепатоцеллюлярный рак (ГЦР) Эпидемиология: Частота развития ГЦР мало зависит от этиологии цирроза, но, тем не менее, прослеживается относительно более высокая частота возникновения ГЦР на фоне цирроза в исходе гепатита С. Кумулятивная 5 -летняя заболеваемость ГЦР при НСVассоциированном циррозе составляет 17% в Европе и США и 30% в Японии. Для гепатита В этот показатель составляет 15% в эндемичных регионах и 10% в развитых странах. Кроме того, гепатит В может приводить к развитию ГЦР без цирроза, что повышает риск возникновения ГЦР в популяции больных гепатитом В до 25%. Fattovich G, Stroffolini T, Zagni I, Donato F. Hepatocellular carcinoma in cirrhosis: incidence and risk factors. Gastroenterology 127(5 Suppl. 1), S 35– S 50 (2004).
 Гепатоцеллюлярный рак (ГЦР) Патогенез: Традиционно механизм канцерогенеза при развитии ГЦР на фоне вирусного гепатита B объясняли хроническим воспалением, фиброзом стромы и пролиферацией гепатоцитов. Тем не менее, доказано влияние на риск развития ГЦР воздействия собственно вируса, а именно следующих связанных с ним факторов: 1. Вирусных белков, в особенности HBx, влияющих на транскрипцию, деградацию белков, апоптоз, сигнальные пути. 2. Вирусная нагрузка. 3. Генотип вируса В: больший риск в странах Европы и США связан с генотипом D по сравнению с А, в странах Азии – С по сравнению с В. Liu CJ, Kao JH. Hepatitis B virus-related hepatocellular carcinoma: epidemiology and pathogenic role of viral factors. J. Chin Med. Assoc. 70(4), 141– 145 (2007). Wu BK, Li CC, Chen HJ et al. Blocking of G 1/S transition and cell death in the regenerating liver of hepatitis B virus X protein transgenic mice. Biochem. Biophys. Res. Commun. 340(3), 916– 928 (2006). Yuen MF, Tanaka Y, Fong DY et al. Independent risk factors and predictive score for the development of hepatocellular Carcinoma in chronic hepatitis B. J. Hepatol. 50(1), 80– 88 (2009).
Гепатоцеллюлярный рак (ГЦР) Патогенез: Традиционно механизм канцерогенеза при развитии ГЦР на фоне вирусного гепатита B объясняли хроническим воспалением, фиброзом стромы и пролиферацией гепатоцитов. Тем не менее, доказано влияние на риск развития ГЦР воздействия собственно вируса, а именно следующих связанных с ним факторов: 1. Вирусных белков, в особенности HBx, влияющих на транскрипцию, деградацию белков, апоптоз, сигнальные пути. 2. Вирусная нагрузка. 3. Генотип вируса В: больший риск в странах Европы и США связан с генотипом D по сравнению с А, в странах Азии – С по сравнению с В. Liu CJ, Kao JH. Hepatitis B virus-related hepatocellular carcinoma: epidemiology and pathogenic role of viral factors. J. Chin Med. Assoc. 70(4), 141– 145 (2007). Wu BK, Li CC, Chen HJ et al. Blocking of G 1/S transition and cell death in the regenerating liver of hepatitis B virus X protein transgenic mice. Biochem. Biophys. Res. Commun. 340(3), 916– 928 (2006). Yuen MF, Tanaka Y, Fong DY et al. Independent risk factors and predictive score for the development of hepatocellular Carcinoma in chronic hepatitis B. J. Hepatol. 50(1), 80– 88 (2009).
 Гепатоцеллюлярный рак (ГЦР) Патогенез: Гепатит С – развитие ГЦР, как правило, происходит на фоне НСVассоциированного цирроза. Годичный риск развития ГЦР у носителей HCV мал и составляет 1. 2%, в то время как при циррозе – 2. 5%. Ввиду отсутствия тяжелых воспалительных изменений патогенез ГЦР связывают с вирусными белками. Механизм изучается. NASH/NAFLD (nonalcoholic steatohepatitis and nonalcoholic fatty liver disease) считается исходным состоянием для т. н. криптогенных циррозов, служащих, в свою очередь, фоном для развития ГЦР. В Японии 5 -летняя заболеваемость ГЦР среди больных с NASH составила 7. 6%. В США риск развития ГЦР был в 4 -5 раз выше у пациентов с BMI 35 -40 кг/м², в Швеции и в Дании – в 2 -3 раза. El-Serag HB, Rudolph KL. Hepatocellular carcinoma: epidemiology and molecular carcinogenesis. Gastroenterology 132(7), 2557– 2576 (2007). Calle EE, Rodriguez C, Walker-Thurmond K, Thun MJ. Overweight, obesity, and mortality from cancer in a prospectively studied cohort of U. S. adults. N. Engl. J. Med. 348(17), 1625– 1638 (2003). Moller H, Mellemgaard A, Lindvig K, Olsen JH. Obesity and cancer risk: a Danish record-linkage study. Eur. J. Cancer 30 A(3), 344– 350 (1994).
Гепатоцеллюлярный рак (ГЦР) Патогенез: Гепатит С – развитие ГЦР, как правило, происходит на фоне НСVассоциированного цирроза. Годичный риск развития ГЦР у носителей HCV мал и составляет 1. 2%, в то время как при циррозе – 2. 5%. Ввиду отсутствия тяжелых воспалительных изменений патогенез ГЦР связывают с вирусными белками. Механизм изучается. NASH/NAFLD (nonalcoholic steatohepatitis and nonalcoholic fatty liver disease) считается исходным состоянием для т. н. криптогенных циррозов, служащих, в свою очередь, фоном для развития ГЦР. В Японии 5 -летняя заболеваемость ГЦР среди больных с NASH составила 7. 6%. В США риск развития ГЦР был в 4 -5 раз выше у пациентов с BMI 35 -40 кг/м², в Швеции и в Дании – в 2 -3 раза. El-Serag HB, Rudolph KL. Hepatocellular carcinoma: epidemiology and molecular carcinogenesis. Gastroenterology 132(7), 2557– 2576 (2007). Calle EE, Rodriguez C, Walker-Thurmond K, Thun MJ. Overweight, obesity, and mortality from cancer in a prospectively studied cohort of U. S. adults. N. Engl. J. Med. 348(17), 1625– 1638 (2003). Moller H, Mellemgaard A, Lindvig K, Olsen JH. Obesity and cancer risk: a Danish record-linkage study. Eur. J. Cancer 30 A(3), 344– 350 (1994).
 Гепатоцеллюлярный рак (ГЦР) Диагностика и наблюдение: Очаги 1 -2 см у больных в группе риска подлежат динамическому наблюдению. Диагноз ГЦР считается подтвержденным при размерах очага >2 см, типичной картине КТ, или повышении уровня АФП > 200 нг/мл. В сомнительных случаях показана биопсия образования с риском имплантационного обсеменения пункционного канала 1 -3%. Уровень α-фетопротеина (АФП) превышает 100 нг/мл только у 30% больных ГЦР. Диагностическим считается уровень 200 нг/мл с чувствительностью 64% и специфичностью 91%. Gomaa AI, Khan SA, Leen EL, Waked I, Taylor-Robinson SD. Diagnosis of hepatocellular carcinoma. World J. Gastroenterol. 15(11), 1301– 1314 (2009). Daniele B, Bencivenga A, Megna AS, Tinessa V. α-fetoprotein and ultrasonography screening for hepatocellular carcinoma. Gastroenterology 127(5 Suppl. 1), S 108–S 112 (2004). Sherman M, Peltekian KM, Lee C. Screening for hepatocellular carcinoma in chronic carriers of hepatitis B virus: incidence and prevalence of hepatocellular carcinoma in a North American urban population. Hepatology 22(2), 432– 438 (1995).
Гепатоцеллюлярный рак (ГЦР) Диагностика и наблюдение: Очаги 1 -2 см у больных в группе риска подлежат динамическому наблюдению. Диагноз ГЦР считается подтвержденным при размерах очага >2 см, типичной картине КТ, или повышении уровня АФП > 200 нг/мл. В сомнительных случаях показана биопсия образования с риском имплантационного обсеменения пункционного канала 1 -3%. Уровень α-фетопротеина (АФП) превышает 100 нг/мл только у 30% больных ГЦР. Диагностическим считается уровень 200 нг/мл с чувствительностью 64% и специфичностью 91%. Gomaa AI, Khan SA, Leen EL, Waked I, Taylor-Robinson SD. Diagnosis of hepatocellular carcinoma. World J. Gastroenterol. 15(11), 1301– 1314 (2009). Daniele B, Bencivenga A, Megna AS, Tinessa V. α-fetoprotein and ultrasonography screening for hepatocellular carcinoma. Gastroenterology 127(5 Suppl. 1), S 108–S 112 (2004). Sherman M, Peltekian KM, Lee C. Screening for hepatocellular carcinoma in chronic carriers of hepatitis B virus: incidence and prevalence of hepatocellular carcinoma in a North American urban population. Hepatology 22(2), 432– 438 (1995).
 Гепатоцеллюлярный рак (ГЦР) Диагностика (современные тенденции): Применение протеомного анализа, в частности protein-chip технологий (SELDITOF и i. TRAQ) позволило повысить чувствительность серологической диагностики ГЦР до 92%, специфичность – до 100%. Для этого используется целый спектр новых белков (galanin-related peptide, pro-neuregulin-4 protein, small inducible cytokine A 15 precursor, 9 -k. Da protein, CSL-zincfinger protein 1, mitochondrial hinge protein and actin-related protein). Применение методов метабономики с использованием протонной магнитнорезонансной спектроскопии (1 H MRS) позволило установить, что в ткани опухоли снижено содержание глюкозы, гликогена и триглицеридов наряду с повышением уровня других метаболитов, что позволяет дифференцировать in vitro ткань опухоли от нормальной и цирротически измененной ткани печени с точностью 92% и 90%. Geng X, Wang F, Li YG, Zhu GP, Zhang WM. SELDI-TOF MS proteinchip technology for screening of serum markers of HBV-induced hepatocellular carcinoma. J. Exp. Clin. Cancer Res. 26(4), 505– 508 (2007). Chaerkady R, Harsha HC, Nalli A et al. A quantitative proteomic approach for identification of potential biomarkers in hepatocellular carcinoma. J. Proteome Res. 7(10), 4289– 4298 (2008). Yang Y, Li C, Nie X et al. Metabonomic studies of human hepatocellular carcinoma using high-resolution magic-angle spinning 1 H NMR spectroscopy in conjunction with multivariate data analysis. J. Proteome Res. 6(7), 2605– 2614 (2007). Soper R, Himmelreich U, Painter D et al. Pathology of hepatocellular carcinoma and its precursors using proton Magnetic resonance spectroscopy and a statistical classification strategy. Pathology 34(5), 417– 422 (2002).
Гепатоцеллюлярный рак (ГЦР) Диагностика (современные тенденции): Применение протеомного анализа, в частности protein-chip технологий (SELDITOF и i. TRAQ) позволило повысить чувствительность серологической диагностики ГЦР до 92%, специфичность – до 100%. Для этого используется целый спектр новых белков (galanin-related peptide, pro-neuregulin-4 protein, small inducible cytokine A 15 precursor, 9 -k. Da protein, CSL-zincfinger protein 1, mitochondrial hinge protein and actin-related protein). Применение методов метабономики с использованием протонной магнитнорезонансной спектроскопии (1 H MRS) позволило установить, что в ткани опухоли снижено содержание глюкозы, гликогена и триглицеридов наряду с повышением уровня других метаболитов, что позволяет дифференцировать in vitro ткань опухоли от нормальной и цирротически измененной ткани печени с точностью 92% и 90%. Geng X, Wang F, Li YG, Zhu GP, Zhang WM. SELDI-TOF MS proteinchip technology for screening of serum markers of HBV-induced hepatocellular carcinoma. J. Exp. Clin. Cancer Res. 26(4), 505– 508 (2007). Chaerkady R, Harsha HC, Nalli A et al. A quantitative proteomic approach for identification of potential biomarkers in hepatocellular carcinoma. J. Proteome Res. 7(10), 4289– 4298 (2008). Yang Y, Li C, Nie X et al. Metabonomic studies of human hepatocellular carcinoma using high-resolution magic-angle spinning 1 H NMR spectroscopy in conjunction with multivariate data analysis. J. Proteome Res. 6(7), 2605– 2614 (2007). Soper R, Himmelreich U, Painter D et al. Pathology of hepatocellular carcinoma and its precursors using proton Magnetic resonance spectroscopy and a statistical classification strategy. Pathology 34(5), 417– 422 (2002).
 Гепатоцеллюлярный рак (ГЦР) Лучевая диагностика: Все методы лучевой диагностики имеют ограниченную точность в выявлении ГЦР при размерах узлов менее 2 см Способы повышения точности исследования: УЗИ с контрастированием – используются микропузырьки (перфторуглероды). Исследование позволяет дифференцировать опухоль размерами менее 2 см и предположительно судить о степени дифференцировки опухоли (чувствительность для малых узлов 87%, УЗИ без контраста – 13 -50%).
Гепатоцеллюлярный рак (ГЦР) Лучевая диагностика: Все методы лучевой диагностики имеют ограниченную точность в выявлении ГЦР при размерах узлов менее 2 см Способы повышения точности исследования: УЗИ с контрастированием – используются микропузырьки (перфторуглероды). Исследование позволяет дифференцировать опухоль размерами менее 2 см и предположительно судить о степени дифференцировки опухоли (чувствительность для малых узлов 87%, УЗИ без контраста – 13 -50%).
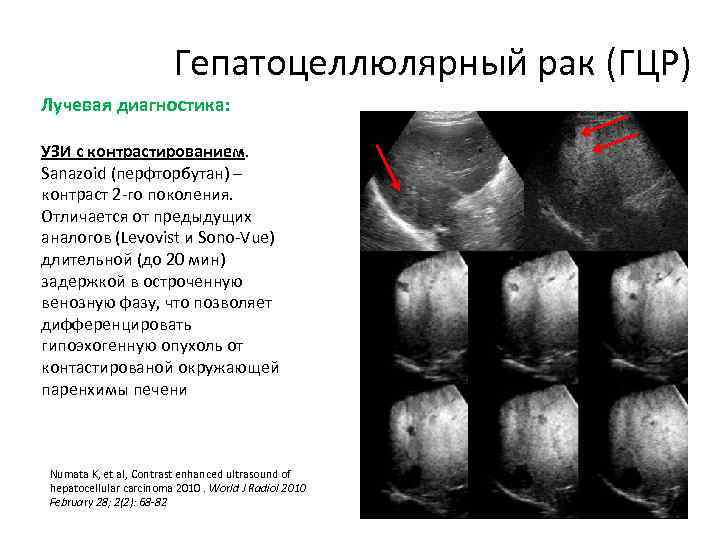 Гепатоцеллюлярный рак (ГЦР) Лучевая диагностика: УЗИ с контрастированием. Sanazoid (перфторбутан) – контраст 2 -го поколения. Отличается от предыдущих аналогов (Levovist и Sono-Vue) длительной (до 20 мин) задержкой в остроченную венозную фазу, что позволяет дифференцировать гипоэхогенную опухоль от контастированой окружающей паренхимы печени Numata K, et al, Contrast enhanced ultrasound of hepatocellular carcinoma 2010. World J Radiol 2010 February 28; 2(2): 68 -82
Гепатоцеллюлярный рак (ГЦР) Лучевая диагностика: УЗИ с контрастированием. Sanazoid (перфторбутан) – контраст 2 -го поколения. Отличается от предыдущих аналогов (Levovist и Sono-Vue) длительной (до 20 мин) задержкой в остроченную венозную фазу, что позволяет дифференцировать гипоэхогенную опухоль от контастированой окружающей паренхимы печени Numata K, et al, Contrast enhanced ultrasound of hepatocellular carcinoma 2010. World J Radiol 2010 February 28; 2(2): 68 -82
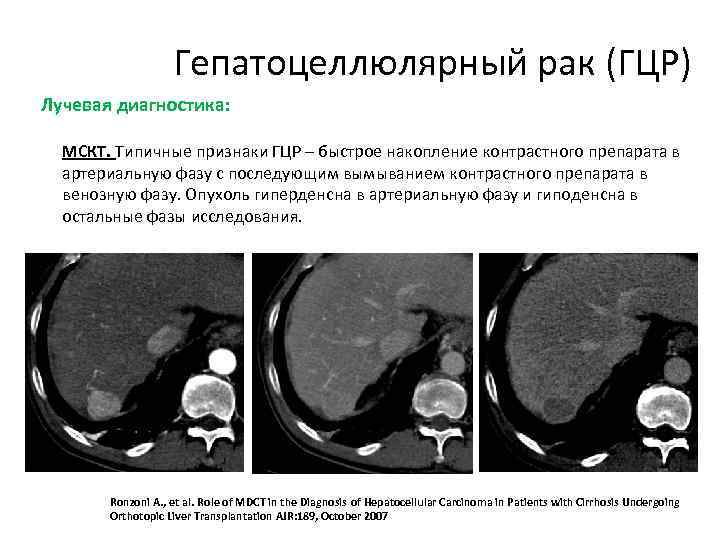 Гепатоцеллюлярный рак (ГЦР) Лучевая диагностика: МСКТ. Типичные признаки ГЦР – быстрое накопление контрастного препарата в артериальную фазу с последующим вымыванием контрастного препарата в венозную фазу. Опухоль гиперденсна в артериальную фазу и гиподенсна в остальные фазы исследования. Ronzoni A. , et al. Role of MDCT in the Diagnosis of Hepatocellular Carcinoma in Patients with Cirrhosis Undergoing Orthotopic Liver Transplantation AJR: 189, October 2007
Гепатоцеллюлярный рак (ГЦР) Лучевая диагностика: МСКТ. Типичные признаки ГЦР – быстрое накопление контрастного препарата в артериальную фазу с последующим вымыванием контрастного препарата в венозную фазу. Опухоль гиперденсна в артериальную фазу и гиподенсна в остальные фазы исследования. Ronzoni A. , et al. Role of MDCT in the Diagnosis of Hepatocellular Carcinoma in Patients with Cirrhosis Undergoing Orthotopic Liver Transplantation AJR: 189, October 2007
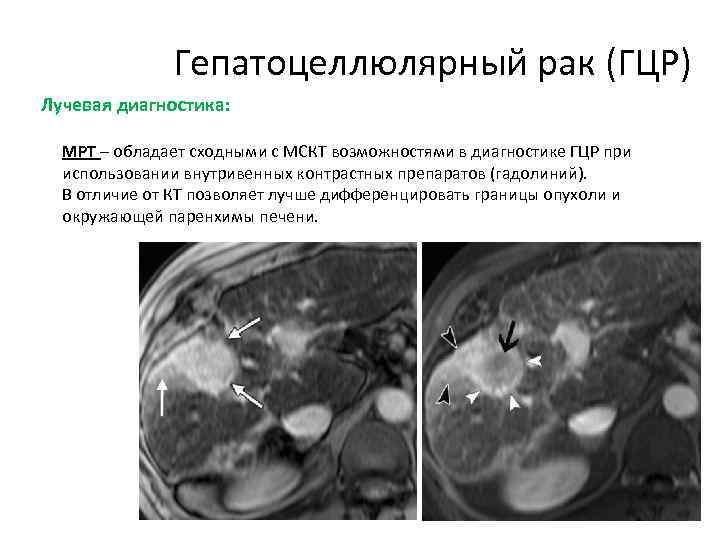 Гепатоцеллюлярный рак (ГЦР) Лучевая диагностика: МРТ – обладает сходными с МСКТ возможностями в диагностике ГЦР при использовании внутривенных контрастных препаратов (гадолиний). В отличие от КТ позволяет лучше дифференцировать границы опухоли и окружающей паренхимы печени.
Гепатоцеллюлярный рак (ГЦР) Лучевая диагностика: МРТ – обладает сходными с МСКТ возможностями в диагностике ГЦР при использовании внутривенных контрастных препаратов (гадолиний). В отличие от КТ позволяет лучше дифференцировать границы опухоли и окружающей паренхимы печени.
 Гепатоцеллюлярный рак (ГЦР) Лучевая диагностика: МРТ с гепатотропными контрастными препаратами (Примовист - гадоксетат динатрия, Gd. EOBDTPA, Bayer Schering Pharma) показала преимущества перед МСКТ: 1. В выявлении ГЦР малых размеров (чувствительность МРТ/МСКТ 83%/68%, специфичность 80%/80%) 2. В дифференциальной диагностике с другими солидными образованиями печени
Гепатоцеллюлярный рак (ГЦР) Лучевая диагностика: МРТ с гепатотропными контрастными препаратами (Примовист - гадоксетат динатрия, Gd. EOBDTPA, Bayer Schering Pharma) показала преимущества перед МСКТ: 1. В выявлении ГЦР малых размеров (чувствительность МРТ/МСКТ 83%/68%, специфичность 80%/80%) 2. В дифференциальной диагностике с другими солидными образованиями печени
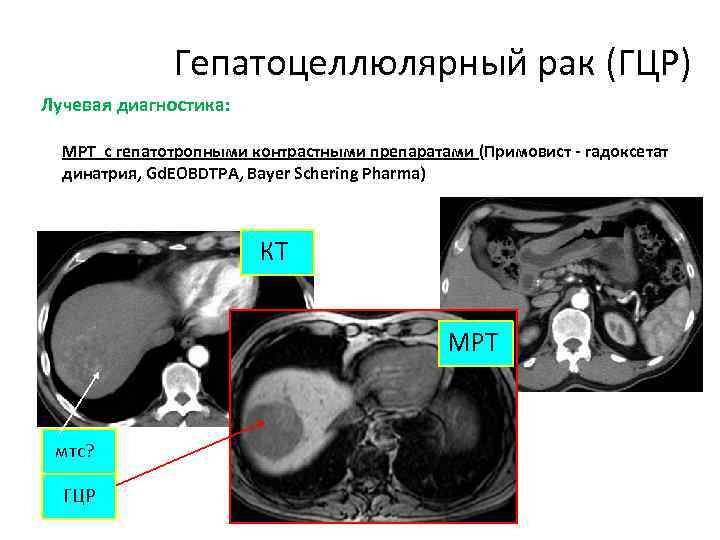 Гепатоцеллюлярный рак (ГЦР) Лучевая диагностика: МРТ с гепатотропными контрастными препаратами (Примовист - гадоксетат динатрия, Gd. EOBDTPA, Bayer Schering Pharma) КТ МРT мтс? ГЦР
Гепатоцеллюлярный рак (ГЦР) Лучевая диагностика: МРТ с гепатотропными контрастными препаратами (Примовист - гадоксетат динатрия, Gd. EOBDTPA, Bayer Schering Pharma) КТ МРT мтс? ГЦР
 Гепатоцеллюлярный рак (ГЦР) Лечение: I. Хирургическое: 1. 2. 3. 4. Резекция печени Локальная деструкция (РЧА, инъекции этанола) Артериальная химиоэмболизация Трансплантация II. Лекарственное (химиотерапия)
Гепатоцеллюлярный рак (ГЦР) Лечение: I. Хирургическое: 1. 2. 3. 4. Резекция печени Локальная деструкция (РЧА, инъекции этанола) Артериальная химиоэмболизация Трансплантация II. Лекарственное (химиотерапия)
 Гепатоцеллюлярный рак (ГЦР) Лечение: I. Хирургическое: Выбор способа хирургического лечения при ГЦР учитывает не только характеристики опухоли (размер, число, локализация), но и заболевание, послужившее фоном для развития опухоли (цирроз печени, гепатит). Эти факторы учитывают различные шкалы прогнозирования, основной задачей которых является выбор наиболее адекватного метода лечения с учетом стадии ГЦР и стадии фонового заболевания печени Стадирование TNM (UICC, AJCC) (2002) Child-Pugh (1983) Классификация Okuda (1985) Классификация BCLC Group (1999, Испания) Классификация Chevret (1999, Франция) CLIP-Score (2000, Италия ) Стадирование JIS (2000, Япония) CUPI-Score (2002, КНР) Шкала LCSGJ (2003, Япония)
Гепатоцеллюлярный рак (ГЦР) Лечение: I. Хирургическое: Выбор способа хирургического лечения при ГЦР учитывает не только характеристики опухоли (размер, число, локализация), но и заболевание, послужившее фоном для развития опухоли (цирроз печени, гепатит). Эти факторы учитывают различные шкалы прогнозирования, основной задачей которых является выбор наиболее адекватного метода лечения с учетом стадии ГЦР и стадии фонового заболевания печени Стадирование TNM (UICC, AJCC) (2002) Child-Pugh (1983) Классификация Okuda (1985) Классификация BCLC Group (1999, Испания) Классификация Chevret (1999, Франция) CLIP-Score (2000, Италия ) Стадирование JIS (2000, Япония) CUPI-Score (2002, КНР) Шкала LCSGJ (2003, Япония)
 Гепатоцеллюлярный рак (ГЦР) Лечение: Предоперацонное обследование: 1. 2. 3. 4. 5. 6. 7. 8. 9. Анамнез и физикальное обследование Обследование на вирусные гепатиты Билирубин, трансаминазы, щелочная фосфатаза, ЛДГ Протромбиновое времени или МНО, альбумин, общий белок Азот мочевины крови, креатинин Общий анализ крови, тромбоциты АФП Исследование грудной клетки методами визуализации Сканирование костей при наличии показаний либо при планировании трансплантации
Гепатоцеллюлярный рак (ГЦР) Лечение: Предоперацонное обследование: 1. 2. 3. 4. 5. 6. 7. 8. 9. Анамнез и физикальное обследование Обследование на вирусные гепатиты Билирубин, трансаминазы, щелочная фосфатаза, ЛДГ Протромбиновое времени или МНО, альбумин, общий белок Азот мочевины крови, креатинин Общий анализ крови, тромбоциты АФП Исследование грудной клетки методами визуализации Сканирование костей при наличии показаний либо при планировании трансплантации
 Гепатоцеллюлярный рак (ГЦР) Лечение: Условия для резекции печени: 1. 2. 3. 4. А, В по шкале Child-Pugh Отсутствие портальной гипертензии Доступная локализация опухоли Достаточный функциональный резерв печени (минимум 20% при отсутствии цирроза и минимум 30 -40% при наличии цирроза Child-Pugh А) 5. Достаточный объем печени, который предполагается оставить в ходе резекции
Гепатоцеллюлярный рак (ГЦР) Лечение: Условия для резекции печени: 1. 2. 3. 4. А, В по шкале Child-Pugh Отсутствие портальной гипертензии Доступная локализация опухоли Достаточный функциональный резерв печени (минимум 20% при отсутствии цирроза и минимум 30 -40% при наличии цирроза Child-Pugh А) 5. Достаточный объем печени, который предполагается оставить в ходе резекции
 Гепатоцеллюлярный рак (ГЦР) Лечение: Критерии UNOS для трансплантации печени: 1. Диаметр опухоли ≤ 5 см, либо 2 -3 опухоли диаметром ≤ 3 см каждая 2. Опухоль не прорастает крупные сосуды 3. Очаги внепеченочного поражения отсутствуют Если трансплантация невыполнима, возможна резекция Нет единого мнения о том, с чего начинать лечение больных с резектабельной опухолью, функцией печени Класс А по Child-Pugh и соответствующих критериям UNOS
Гепатоцеллюлярный рак (ГЦР) Лечение: Критерии UNOS для трансплантации печени: 1. Диаметр опухоли ≤ 5 см, либо 2 -3 опухоли диаметром ≤ 3 см каждая 2. Опухоль не прорастает крупные сосуды 3. Очаги внепеченочного поражения отсутствуют Если трансплантация невыполнима, возможна резекция Нет единого мнения о том, с чего начинать лечение больных с резектабельной опухолью, функцией печени Класс А по Child-Pugh и соответствующих критериям UNOS
 Гепатоцеллюлярный рак (ГЦР) Лечение больных, которым невозможно выполнение резекции или трансплантации: Абляционная терапия 1. Удобное для абляции расположение опухоли 2. Размер до 3 см. Опкхоли 3 -5 см подлежат комьбинирвоанному лечение: абляция + эмболизация 3. Осторожность при абляции вблизи крупных сосоудов и желчных протоков Эмболизация 1. Все опухоли подлежат эмболизации (ХЭ, простой эмболизации, лучевой эмболизации) 2. Противопоказана больным с тромбозом воротной вены и классом С по шкале Child-Pugh
Гепатоцеллюлярный рак (ГЦР) Лечение больных, которым невозможно выполнение резекции или трансплантации: Абляционная терапия 1. Удобное для абляции расположение опухоли 2. Размер до 3 см. Опкхоли 3 -5 см подлежат комьбинирвоанному лечение: абляция + эмболизация 3. Осторожность при абляции вблизи крупных сосоудов и желчных протоков Эмболизация 1. Все опухоли подлежат эмболизации (ХЭ, простой эмболизации, лучевой эмболизации) 2. Противопоказана больным с тромбозом воротной вены и классом С по шкале Child-Pugh
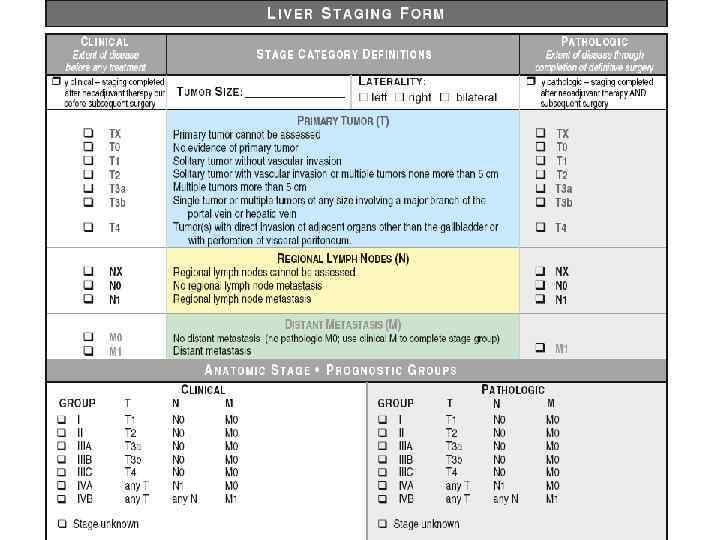
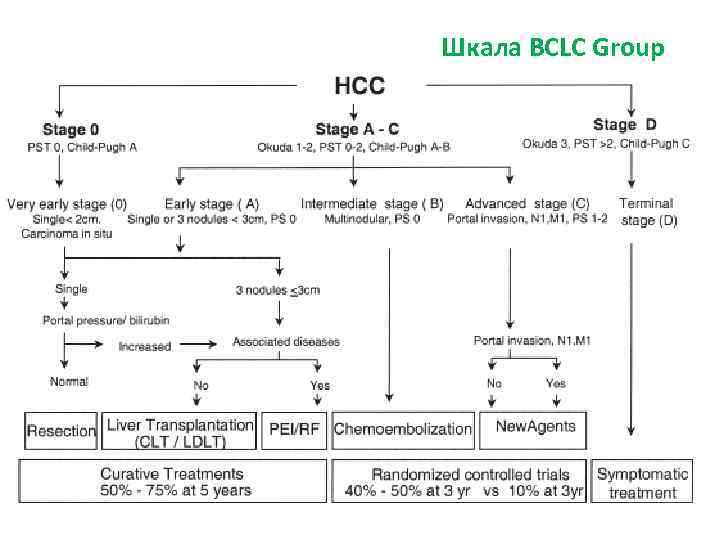 Шкала BCLC Group
Шкала BCLC Group
 Гепатоцеллюлярный рак (ГЦР) Лечение: II. Лекарственное (химиотерапия) Sorafenib представляет собой таблетированный мультикиназный ингибитор, который тормозит пролиферацию опухолевых клеток и ангионеогенез у широкого спектра опухолей. Действие основано на связывании VEGF рецепторов (Vascular Endothelial Growth Factor), PDGF рецепторов (Platelet- Derived Growth Factor) и Rafкиназ. Первые результаты рандомизироваого контролируемого исследования были опубликованы в 2008 г. Сорафениб увеличил медиану выживаемости нерезектабнльных больных до 10. 7 мес. , по сравнению с 7. 9 мес. в плацебогруппе (hazard ratio : 0. 69; 95% CI: 0. 55– 0. 87; p < 0. 001). Llovet JM, Ricci S, Mazzaferro V et al. Sorafenib in advanced hepatocellular carcinoma. N. Engl. J. Med. 359(4), 378– 390 (2008).
Гепатоцеллюлярный рак (ГЦР) Лечение: II. Лекарственное (химиотерапия) Sorafenib представляет собой таблетированный мультикиназный ингибитор, который тормозит пролиферацию опухолевых клеток и ангионеогенез у широкого спектра опухолей. Действие основано на связывании VEGF рецепторов (Vascular Endothelial Growth Factor), PDGF рецепторов (Platelet- Derived Growth Factor) и Rafкиназ. Первые результаты рандомизироваого контролируемого исследования были опубликованы в 2008 г. Сорафениб увеличил медиану выживаемости нерезектабнльных больных до 10. 7 мес. , по сравнению с 7. 9 мес. в плацебогруппе (hazard ratio : 0. 69; 95% CI: 0. 55– 0. 87; p < 0. 001). Llovet JM, Ricci S, Mazzaferro V et al. Sorafenib in advanced hepatocellular carcinoma. N. Engl. J. Med. 359(4), 378– 390 (2008).
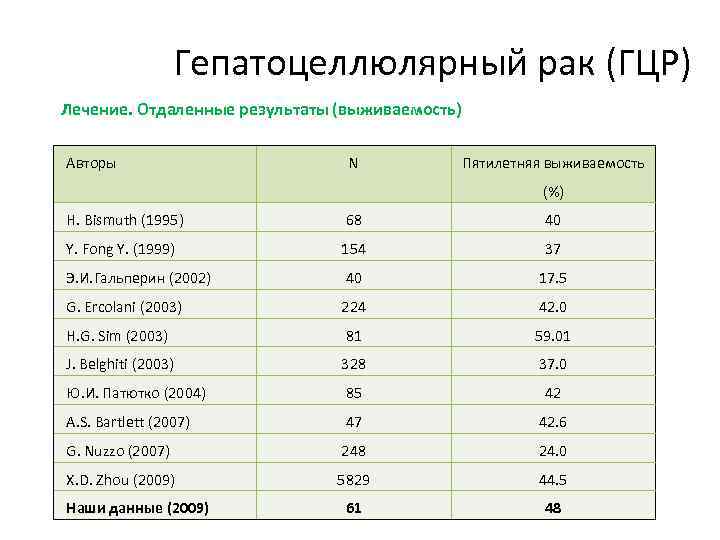 Гепатоцеллюлярный рак (ГЦР) Лечение. Отдаленные результаты (выживаемость) Авторы N Пятилетняя выживаемость (%) H. Bismuth (1995) 68 40 Y. Fong Y. (1999) 154 37 Э. И. Гальперин (2002) 40 17. 5 G. Ercolani (2003) 224 42. 0 H. G. Sim (2003) 81 59. 01 J. Belghiti (2003) 328 37. 0 Ю. И. Патютко (2004) 85 42 A. S. Bartlett (2007) 47 42. 6 G. Nuzzo (2007) 248 24. 0 X. D. Zhou (2009) 5829 44. 5 61 48 Наши данные (2009)
Гепатоцеллюлярный рак (ГЦР) Лечение. Отдаленные результаты (выживаемость) Авторы N Пятилетняя выживаемость (%) H. Bismuth (1995) 68 40 Y. Fong Y. (1999) 154 37 Э. И. Гальперин (2002) 40 17. 5 G. Ercolani (2003) 224 42. 0 H. G. Sim (2003) 81 59. 01 J. Belghiti (2003) 328 37. 0 Ю. И. Патютко (2004) 85 42 A. S. Bartlett (2007) 47 42. 6 G. Nuzzo (2007) 248 24. 0 X. D. Zhou (2009) 5829 44. 5 61 48 Наши данные (2009)
 Больной Б. , 58 лет Жалобы: на чувство тяжести в правом подреберье. Анамнез заболевания: считает себя больным в течение года, когда впервые появились вышеуказанные жалобы. При амбулаторной КТ брюшной полости в 6 сегменте печени определяется образование пониженной плотности, с нечеткими контурами, неравномерно накапливающее контрастный препарат, размерами 36 х50 мм.
Больной Б. , 58 лет Жалобы: на чувство тяжести в правом подреберье. Анамнез заболевания: считает себя больным в течение года, когда впервые появились вышеуказанные жалобы. При амбулаторной КТ брюшной полости в 6 сегменте печени определяется образование пониженной плотности, с нечеткими контурами, неравномерно накапливающее контрастный препарат, размерами 36 х50 мм.
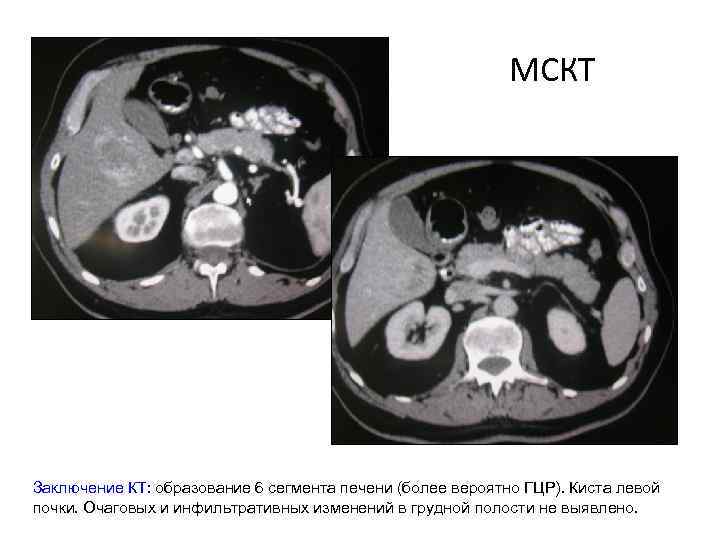 МСКТ Заключение КТ: образование 6 сегмента печени (более вероятно ГЦР). Киста левой почки. Очаговых и инфильтративных изменений в грудной полости не выявлено.
МСКТ Заключение КТ: образование 6 сегмента печени (более вероятно ГЦР). Киста левой почки. Очаговых и инфильтративных изменений в грудной полости не выявлено.
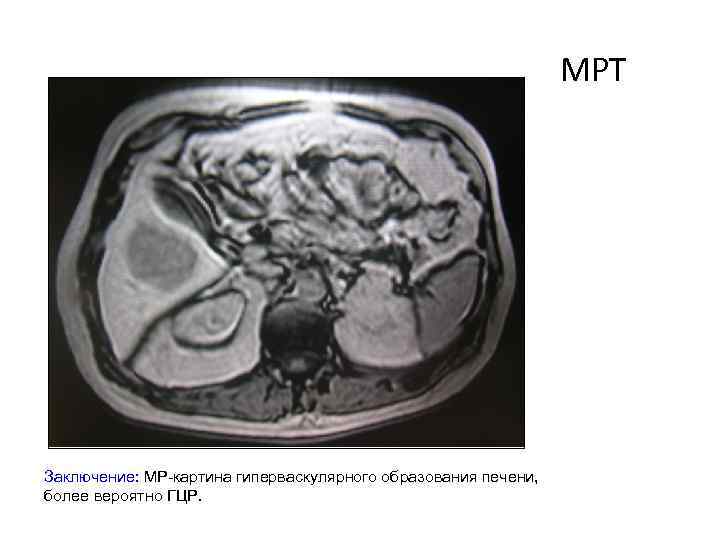 МРТ Заключение: МР-картина гиперваскулярного образования печени, более вероятно ГЦР.
МРТ Заключение: МР-картина гиперваскулярного образования печени, более вероятно ГЦР.
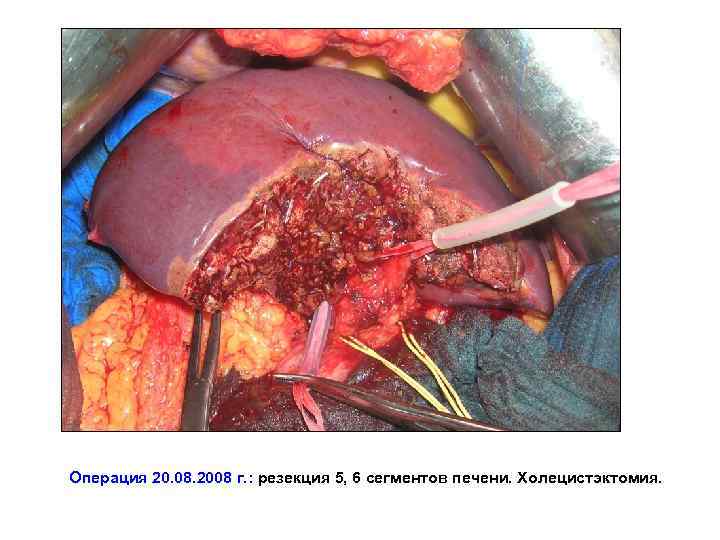 Операция 20. 08. 2008 г. : резекция 5, 6 сегментов печени. Холецистэктомия.
Операция 20. 08. 2008 г. : резекция 5, 6 сегментов печени. Холецистэктомия.
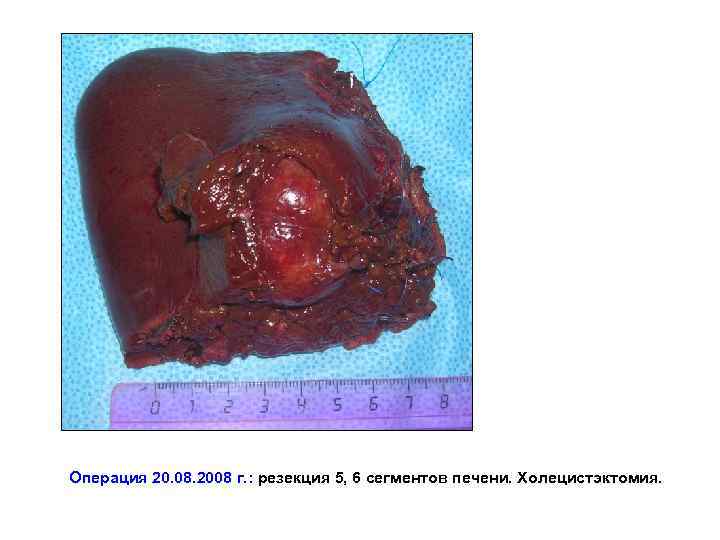 Операция 20. 08. 2008 г. : резекция 5, 6 сегментов печени. Холецистэктомия.
Операция 20. 08. 2008 г. : резекция 5, 6 сегментов печени. Холецистэктомия.
 Больной В. , 50 лет Диагноз: первичный рак правой доли печени (холангиоцеллюлярный? ) с метастазами в левую долю T 3 N 0 -1 M 1. Состояние после портоэмболизации правой доли печени 26. 01. 2011. МКБ Хронический пиелонефрит. Микролиты обеих почек.
Больной В. , 50 лет Диагноз: первичный рак правой доли печени (холангиоцеллюлярный? ) с метастазами в левую долю T 3 N 0 -1 M 1. Состояние после портоэмболизации правой доли печени 26. 01. 2011. МКБ Хронический пиелонефрит. Микролиты обеих почек.
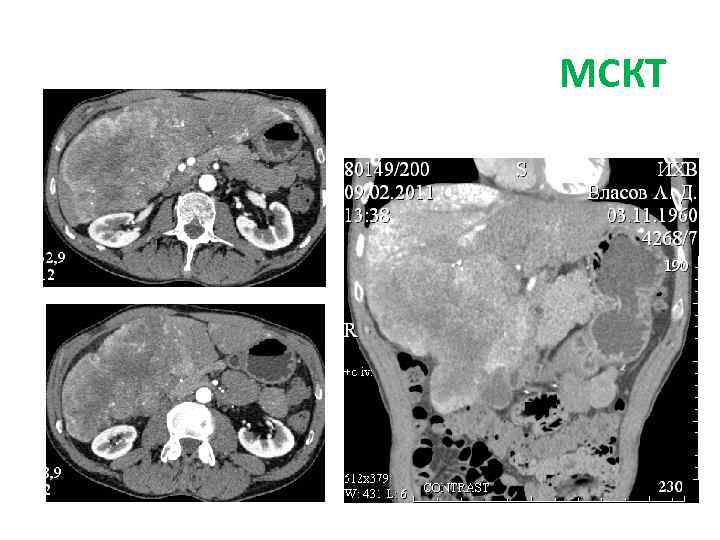 МСКТ
МСКТ
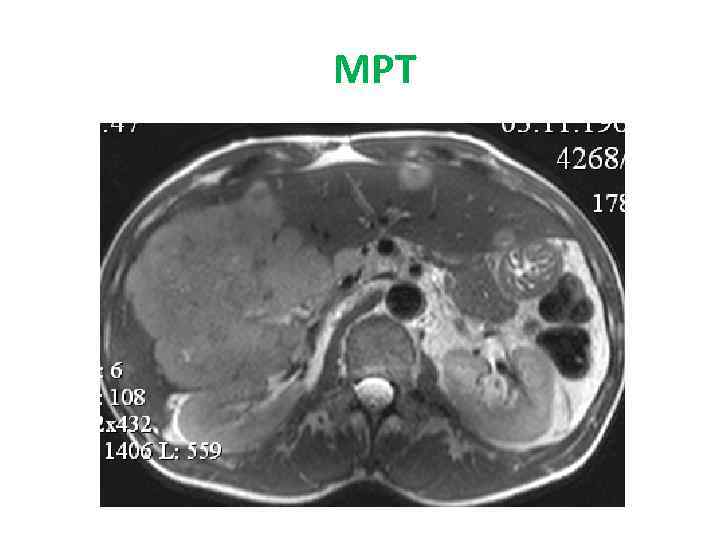 МРТ
МРТ
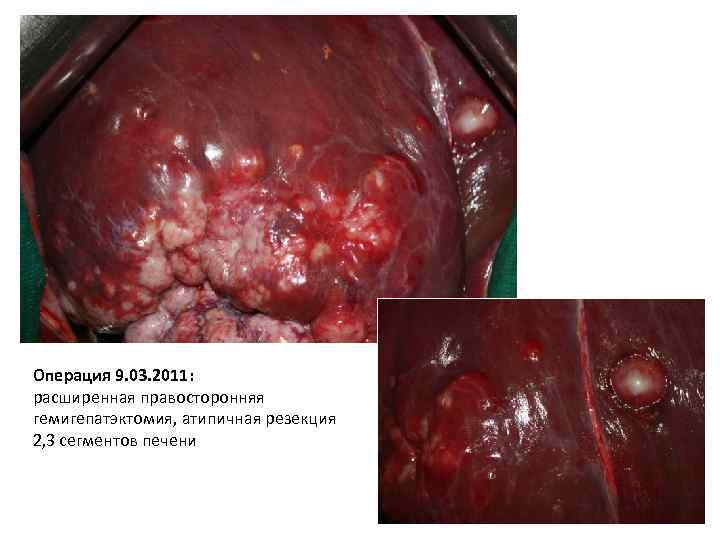 Операция 9. 03. 2011: расширенная правосторонняя гемигепатэктомия, атипичная резекция 2, 3 сегментов печени
Операция 9. 03. 2011: расширенная правосторонняя гемигепатэктомия, атипичная резекция 2, 3 сегментов печени
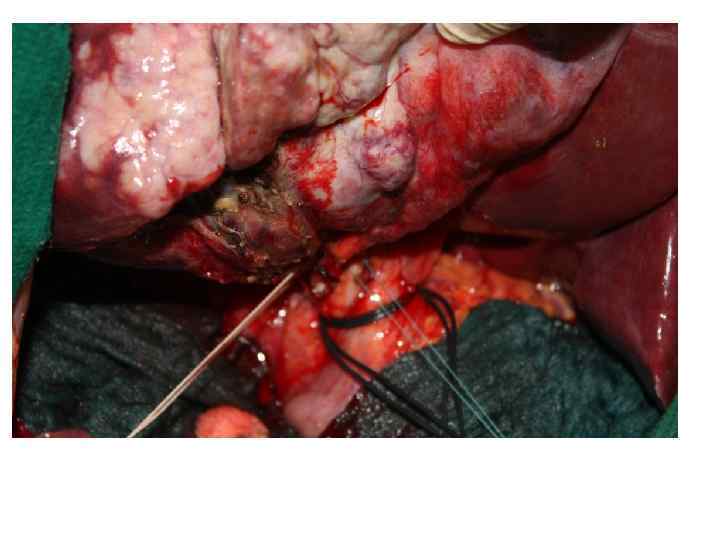
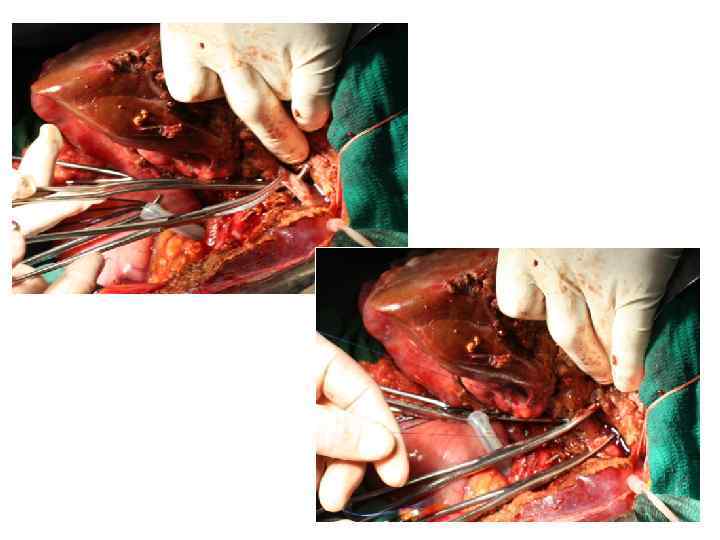
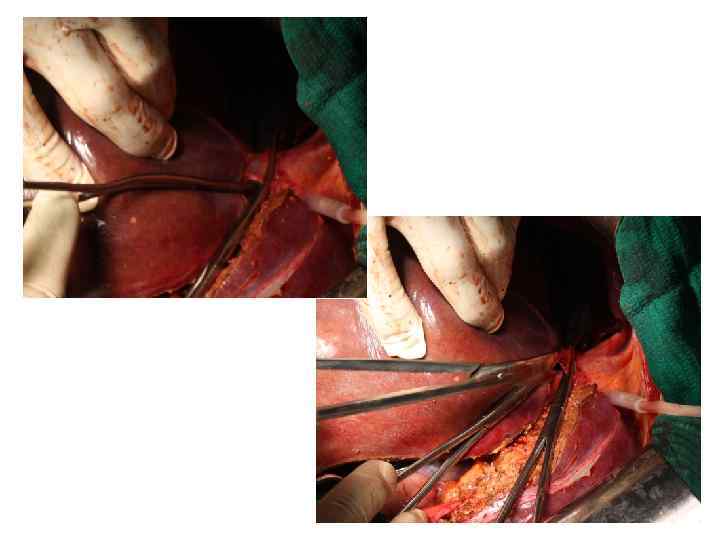
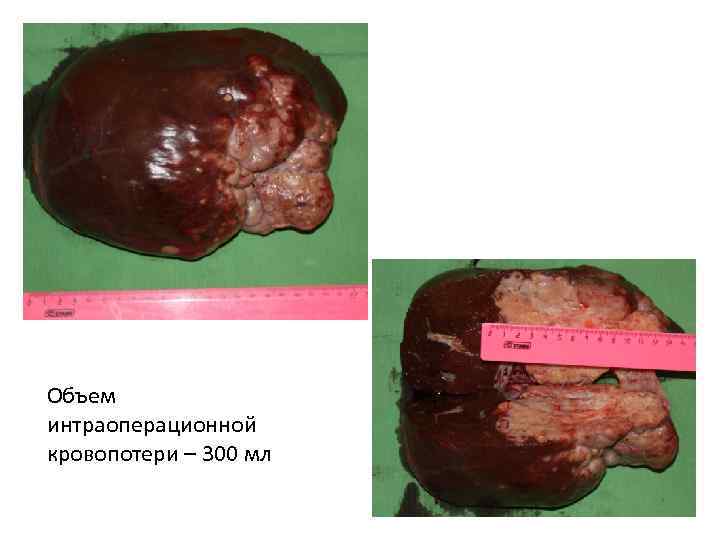 Объем интраоперационной кровопотери – 300 мл
Объем интраоперационной кровопотери – 300 мл
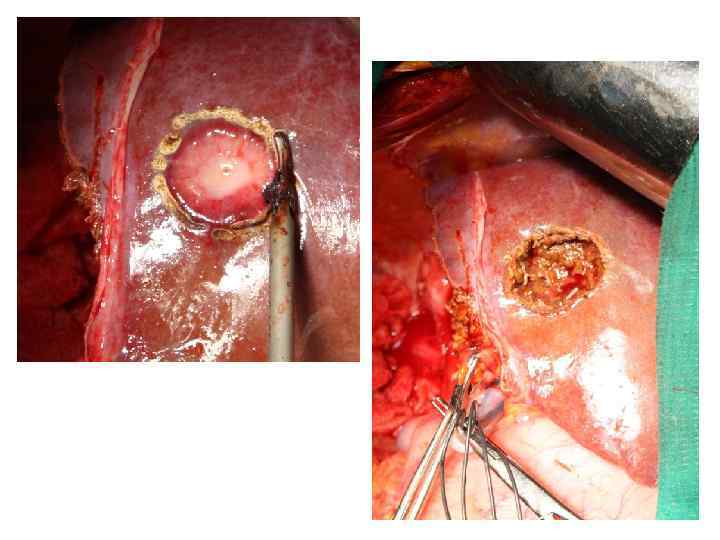
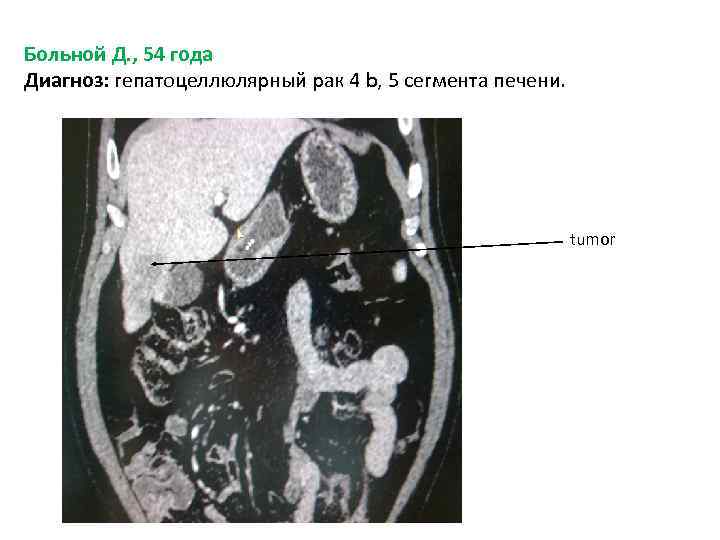 Больной Д. , 54 года Диагноз: гепатоцеллюлярный рак 4 b, 5 сегмента печени. tumor
Больной Д. , 54 года Диагноз: гепатоцеллюлярный рак 4 b, 5 сегмента печени. tumor
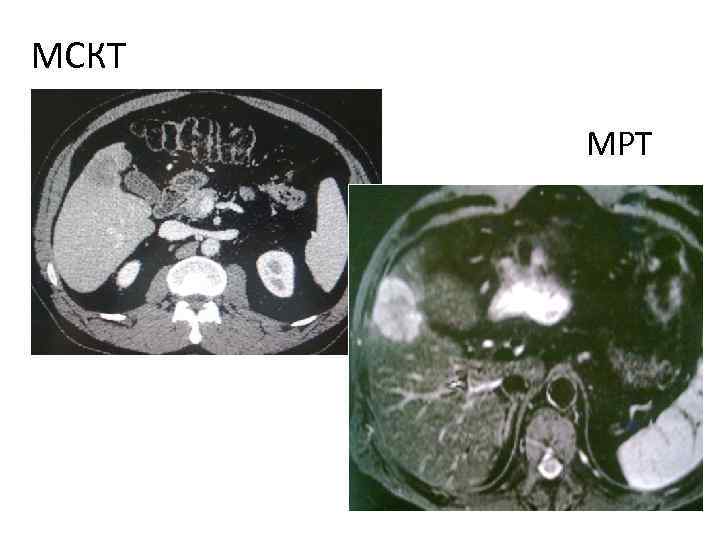 МСКТ МРТ
МСКТ МРТ
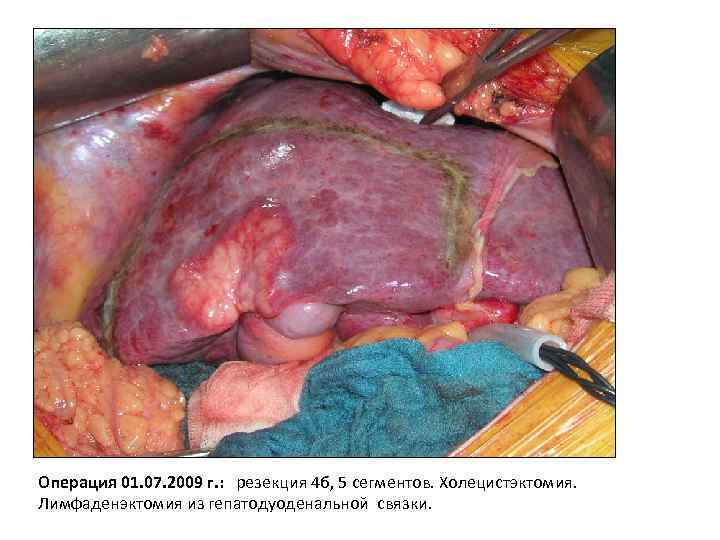 Операция 01. 07. 2009 г. : резекция 4 б, 5 сегментов. Холецистэктомия. Лимфаденэктомия из гепатодуоденальной связки.
Операция 01. 07. 2009 г. : резекция 4 б, 5 сегментов. Холецистэктомия. Лимфаденэктомия из гепатодуоденальной связки.
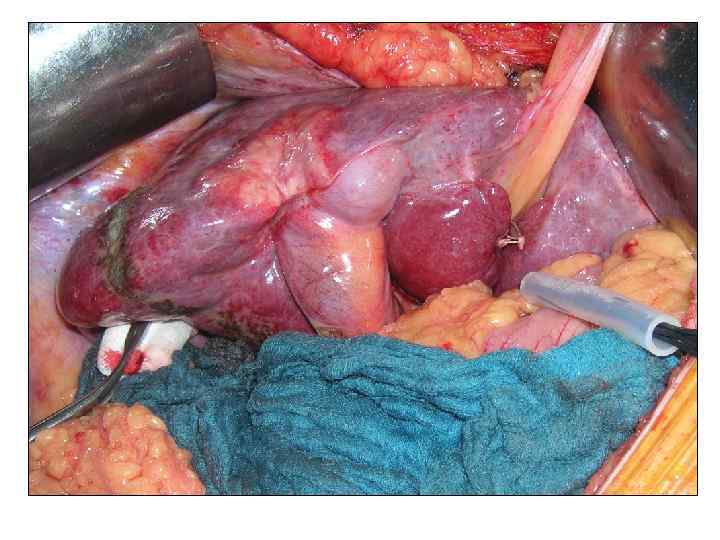
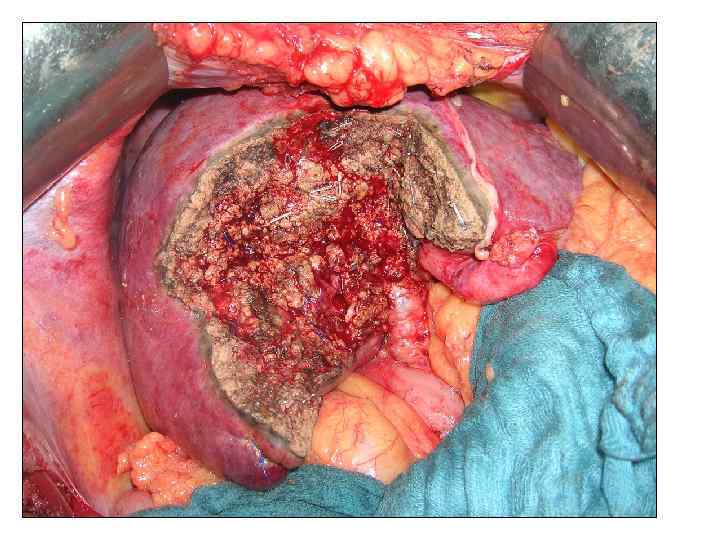
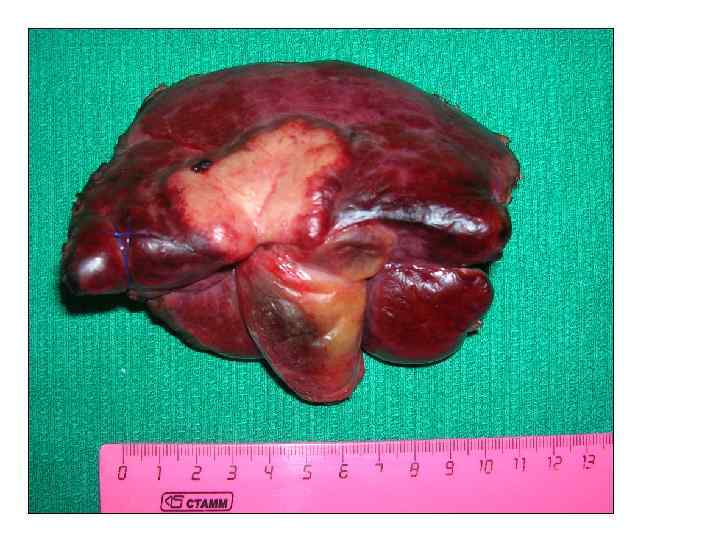
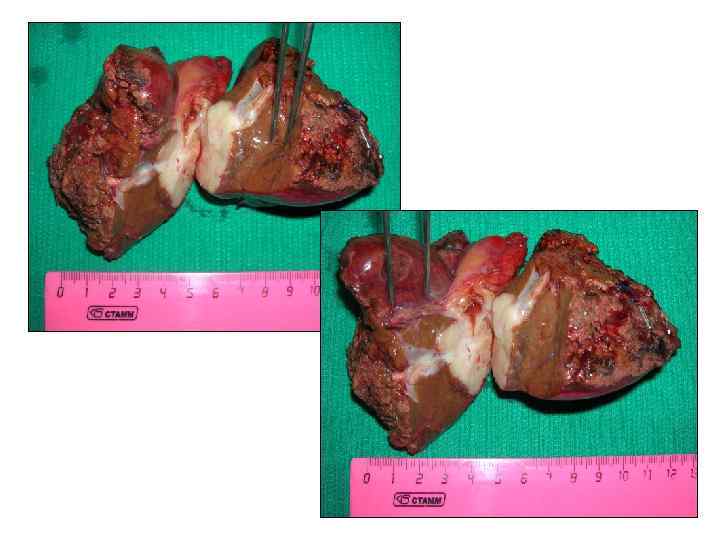
 Больной Н. , 61 г. . Жалобы: не предъявляет Анамнез заболевания: в течение 7 лет страдает хроническим вирусным гепатитом С. При плановом обследовании в сентябре 2010 г в 5 и 6 сегментах печени выявлено два очага 23 и 15 мм в диаметре, по данным КТ картина гепатцеллюлярного рака. При УЗИ в динамике отмечен рост образования в размерах до 35 и 30 мм. Диагноз: гепатоцеллюлярный рак 5 -6 сегментов печени. Хронический вирусный гепатит С. Цирроз печени HCV-этиологии, класс А по Child-Pugh. Портальная гипертензия. Варикозное расширен вен пищевода II степени. Спленомегалия. Иммунная лейкопения, тромбоцитопения.
Больной Н. , 61 г. . Жалобы: не предъявляет Анамнез заболевания: в течение 7 лет страдает хроническим вирусным гепатитом С. При плановом обследовании в сентябре 2010 г в 5 и 6 сегментах печени выявлено два очага 23 и 15 мм в диаметре, по данным КТ картина гепатцеллюлярного рака. При УЗИ в динамике отмечен рост образования в размерах до 35 и 30 мм. Диагноз: гепатоцеллюлярный рак 5 -6 сегментов печени. Хронический вирусный гепатит С. Цирроз печени HCV-этиологии, класс А по Child-Pugh. Портальная гипертензия. Варикозное расширен вен пищевода II степени. Спленомегалия. Иммунная лейкопения, тромбоцитопения.
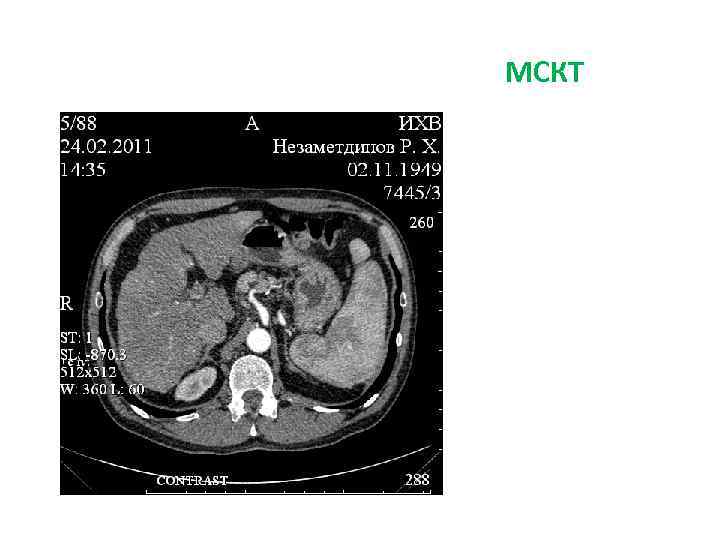 МСКТ
МСКТ
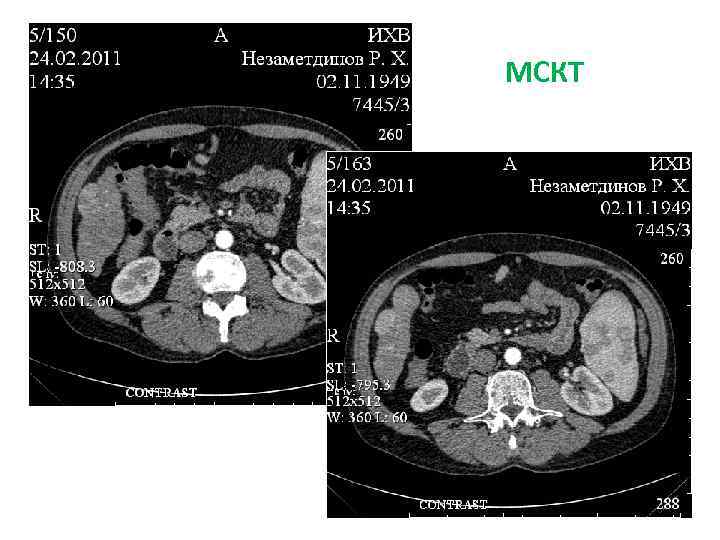 СКТ МСКТ
СКТ МСКТ
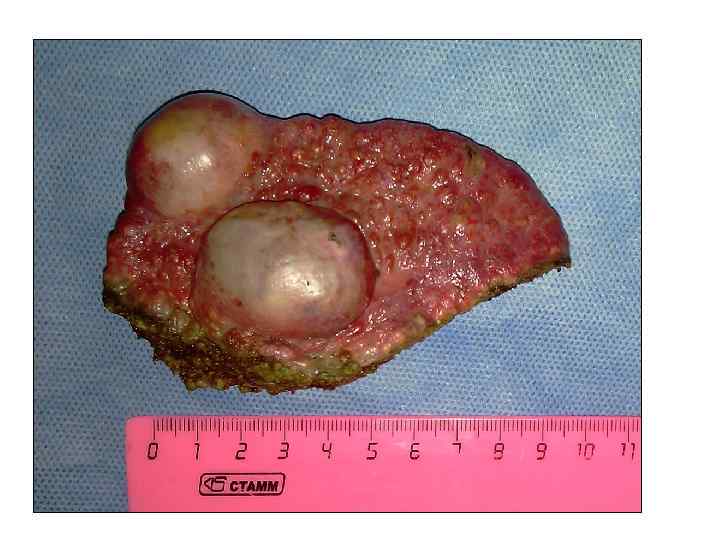
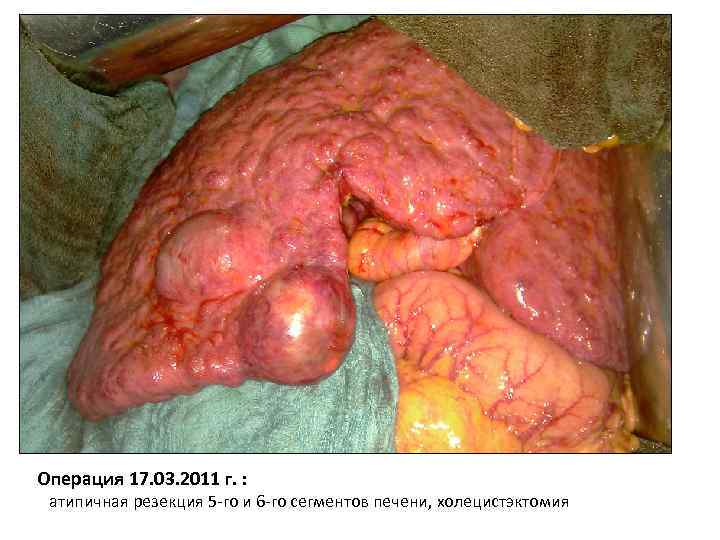 Операция 17. 03. 2011 г. : атипичная резекция 5 -го и 6 -го сегментов печени, холецистэктомия
Операция 17. 03. 2011 г. : атипичная резекция 5 -го и 6 -го сегментов печени, холецистэктомия
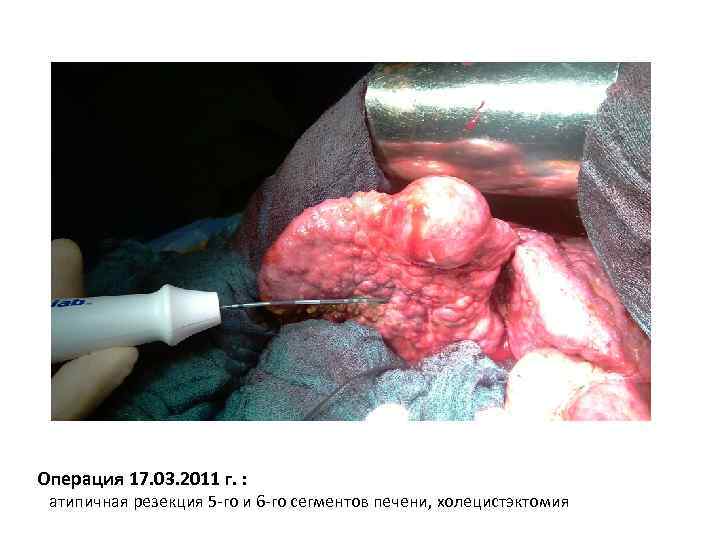 Операция 17. 03. 2011 г. : атипичная резекция 5 -го и 6 -го сегментов печени, холецистэктомия
Операция 17. 03. 2011 г. : атипичная резекция 5 -го и 6 -го сегментов печени, холецистэктомия
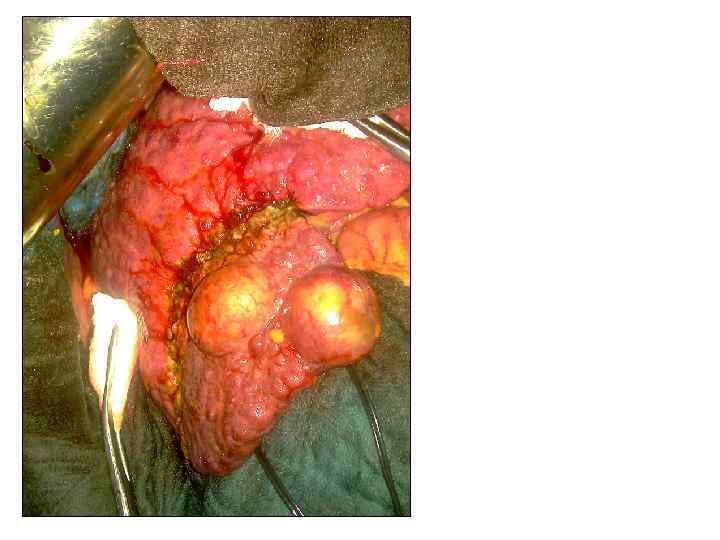
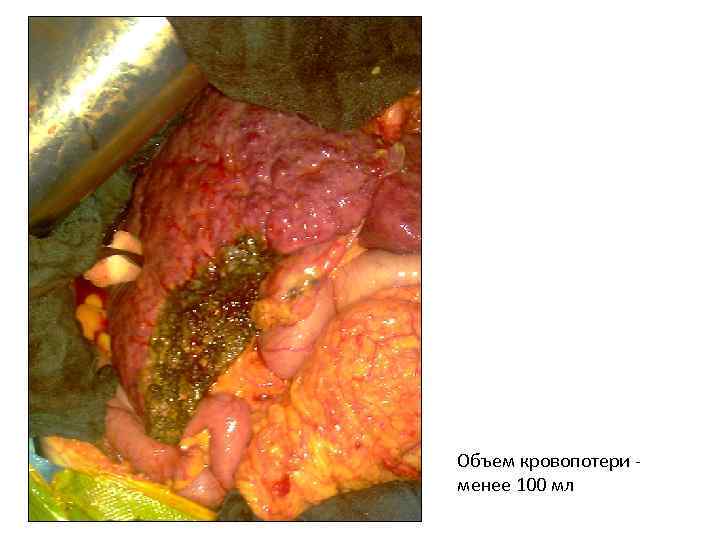 Объем кровопотери менее 100 мл
Объем кровопотери менее 100 мл
 Холангиоцеллюлярный рак (ХЦР) Холангиоцеллюлярный рак (холангиокарцинома) развивается на фоне хронического воспаления, билиарного стаза из клеток протокового эпителия мелких внутрипеченочных протоков (внутрипеченочный ХЦР) и внепеченочных желчных протоков (внепеченочный ХЦР – опухоль Клатскина, рак холедоха, рак желчного пузыря). Внутрипеченочный ХЦР - второй по частое первичный рак печени (15– 20%). В настоящее время отмечается медленный рост заболеваемости ХЦР в мире, что связано с увеличением заболеваемости вирусным гепатитом C. Заболевают в равной степени мужчины и женщины. Пик заболеваемости отмечает на 5 -й, 6 -й декаде жизни. В патогенезе важную роль играет вируса гепатита С. Риск развития ХЦР на фоне HCV-ассоциированного цирроза повышается в 1000 раз. Без лечения средняя продолжительность жизни составляет 6 мес. 5 -летняя выживаемость после резекции печени колеблется от 20% до 40%.
Холангиоцеллюлярный рак (ХЦР) Холангиоцеллюлярный рак (холангиокарцинома) развивается на фоне хронического воспаления, билиарного стаза из клеток протокового эпителия мелких внутрипеченочных протоков (внутрипеченочный ХЦР) и внепеченочных желчных протоков (внепеченочный ХЦР – опухоль Клатскина, рак холедоха, рак желчного пузыря). Внутрипеченочный ХЦР - второй по частое первичный рак печени (15– 20%). В настоящее время отмечается медленный рост заболеваемости ХЦР в мире, что связано с увеличением заболеваемости вирусным гепатитом C. Заболевают в равной степени мужчины и женщины. Пик заболеваемости отмечает на 5 -й, 6 -й декаде жизни. В патогенезе важную роль играет вируса гепатита С. Риск развития ХЦР на фоне HCV-ассоциированного цирроза повышается в 1000 раз. Без лечения средняя продолжительность жизни составляет 6 мес. 5 -летняя выживаемость после резекции печени колеблется от 20% до 40%.
 Холангиоцеллюлярный рак (ХЦР) Диагностика Специфических маркеров ХЦР в настоящее время не существует. Диагноз устанавливается на основании исключения ГЦР и метастатических опухолей (анамнез, данные лучевых методов обследования). В серологической диагностике на вероятный диагноз ХЦР указывает повышение СЕА и СА 19 -9. Окончательная диагностика гистологическая, как правило, с применением иммуногистохимии (ИГХ). Основная панель ИГХ-маркеров включает CK 7, CK 20, CDX-2, TTF-1, ER, PR, BRST-2 и PSA, которая позволяет исключить метастазы первичного рака толстой кишки, легких, молочных желез и простаты. Внутрипеченочный ХЦР проявляет наиболее сильное окрашивание на CK 7 и СK 19, отрицателен или слабо положителен на CK 20 и практически всегда отрицателен на другие маркеры.
Холангиоцеллюлярный рак (ХЦР) Диагностика Специфических маркеров ХЦР в настоящее время не существует. Диагноз устанавливается на основании исключения ГЦР и метастатических опухолей (анамнез, данные лучевых методов обследования). В серологической диагностике на вероятный диагноз ХЦР указывает повышение СЕА и СА 19 -9. Окончательная диагностика гистологическая, как правило, с применением иммуногистохимии (ИГХ). Основная панель ИГХ-маркеров включает CK 7, CK 20, CDX-2, TTF-1, ER, PR, BRST-2 и PSA, которая позволяет исключить метастазы первичного рака толстой кишки, легких, молочных желез и простаты. Внутрипеченочный ХЦР проявляет наиболее сильное окрашивание на CK 7 и СK 19, отрицателен или слабо положителен на CK 20 и практически всегда отрицателен на другие маркеры.
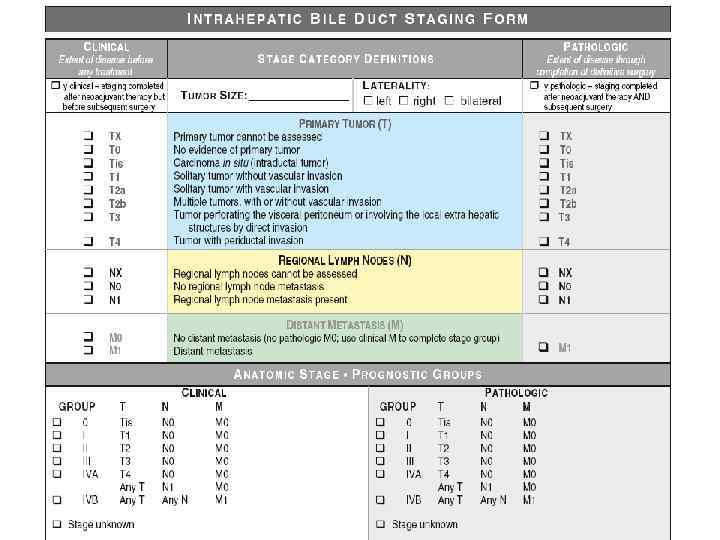
 Холангиоцеллюлярный рак (ХЦР) Стадирование TNM В 7 -ом пересмотре классификации TNM AJCC в 2010 г. введено отдельное от ГЦР стадирование для внутрипеченочного ХЦР. Впервые выделение стадирования внутрипеченочного ХЦР предложено в 2009 г. Необходимость раздельной классификации основана на различиях прогностических для выживаемости факторов. Различия в стадирующих классификациях TNM для ГЦР и внутрипеченочного ХЦР касаются характеристики фактора T. При ХЦР не учитываются размеры опухоли. Не проводится различия в инвазии крупных и мелких сосудов.
Холангиоцеллюлярный рак (ХЦР) Стадирование TNM В 7 -ом пересмотре классификации TNM AJCC в 2010 г. введено отдельное от ГЦР стадирование для внутрипеченочного ХЦР. Впервые выделение стадирования внутрипеченочного ХЦР предложено в 2009 г. Необходимость раздельной классификации основана на различиях прогностических для выживаемости факторов. Различия в стадирующих классификациях TNM для ГЦР и внутрипеченочного ХЦР касаются характеристики фактора T. При ХЦР не учитываются размеры опухоли. Не проводится различия в инвазии крупных и мелких сосудов.
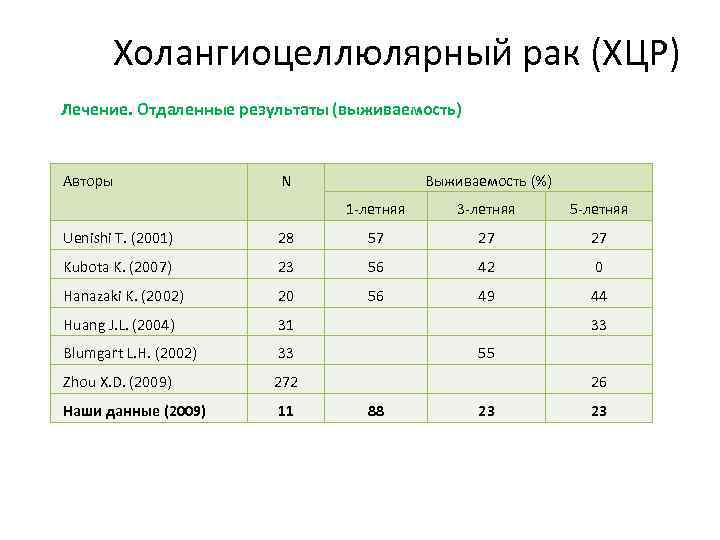 Холангиоцеллюлярный рак (ХЦР) Лечение. Отдаленные результаты (выживаемость) Авторы N Выживаемость (%) 1 -летняя 3 -летняя 5 -летняя Uenishi T. (2001) 28 57 27 27 Kubota K. (2007) 23 56 42 0 Hanazaki K. (2002) 20 56 49 44 Huang J. L. (2004) 31 Blumgart L. H. (2002) 33 Zhou X. D. (2009) 272 Наши данные (2009) 11 33 55 26 88 23 23
Холангиоцеллюлярный рак (ХЦР) Лечение. Отдаленные результаты (выживаемость) Авторы N Выживаемость (%) 1 -летняя 3 -летняя 5 -летняя Uenishi T. (2001) 28 57 27 27 Kubota K. (2007) 23 56 42 0 Hanazaki K. (2002) 20 56 49 44 Huang J. L. (2004) 31 Blumgart L. H. (2002) 33 Zhou X. D. (2009) 272 Наши данные (2009) 11 33 55 26 88 23 23
 Больной Х. , 47 лет Жалобы: снижение массы тела на 8 -10 кг за последние 2 месяца Анамнез заболевания: Июнь 2008 – механическая желтуха (общ. билирубин 580 мкмоль/л). Госпитализирован в Институт хирургии 04. 07. 08 с диагнозом: «Опухоль внутрипеченочных желчных протоков (ХЦР? ) с метастазами в 4, 6, 8 S печени» . 07. 08 – ЧЧХС печеночных желчных протоков Диагноз: ХЦР правой доли Т 4 N 1 Mo (метастазы в 4 сегмент печени), с прорастанием в конфлюенс печеночных протоков. Состояние после ЧЧХС обеих долей печени от 07. 08
Больной Х. , 47 лет Жалобы: снижение массы тела на 8 -10 кг за последние 2 месяца Анамнез заболевания: Июнь 2008 – механическая желтуха (общ. билирубин 580 мкмоль/л). Госпитализирован в Институт хирургии 04. 07. 08 с диагнозом: «Опухоль внутрипеченочных желчных протоков (ХЦР? ) с метастазами в 4, 6, 8 S печени» . 07. 08 – ЧЧХС печеночных желчных протоков Диагноз: ХЦР правой доли Т 4 N 1 Mo (метастазы в 4 сегмент печени), с прорастанием в конфлюенс печеночных протоков. Состояние после ЧЧХС обеих долей печени от 07. 08
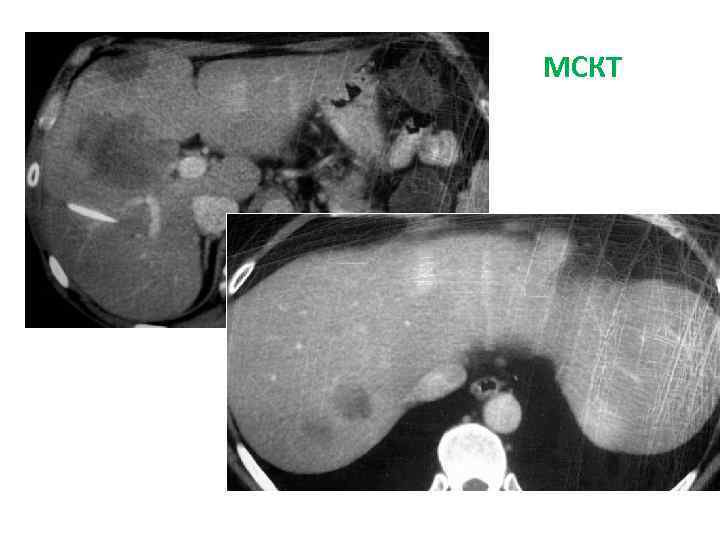 МСКТ
МСКТ
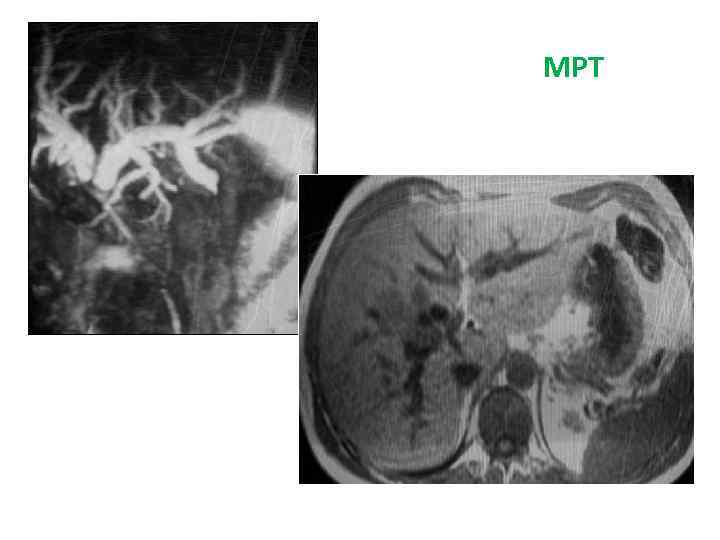 МРТ
МРТ
 Функциональный резерв печени Ш объем 2, 3 сегментов – 29% от общего объема печени за вычетом объема опухоли Ш псевдохолинэстераза 8457 ед/л (N: 4500 -12000) Ш альбумин - 47, 3 г/л (N: 39 -49) Ш протеин С - 91% (N: 80 -120%) Ш протромбиновый индекс - 78% (N: 80 -100%) Ш общ. билирубин - 38 мкмоль/л (N > 20, 5)
Функциональный резерв печени Ш объем 2, 3 сегментов – 29% от общего объема печени за вычетом объема опухоли Ш псевдохолинэстераза 8457 ед/л (N: 4500 -12000) Ш альбумин - 47, 3 г/л (N: 39 -49) Ш протеин С - 91% (N: 80 -120%) Ш протромбиновый индекс - 78% (N: 80 -100%) Ш общ. билирубин - 38 мкмоль/л (N > 20, 5)
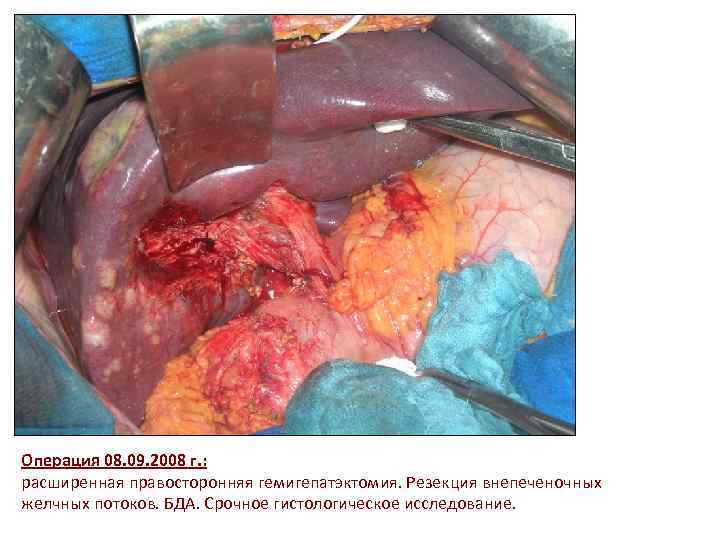 Операция 08. 09. 2008 г. : расширенная правосторонняя гемигепатэктомия. Резекция внепеченочных желчных потоков. БДА. Срочное гистологическое исследование.
Операция 08. 09. 2008 г. : расширенная правосторонняя гемигепатэктомия. Резекция внепеченочных желчных потоков. БДА. Срочное гистологическое исследование.
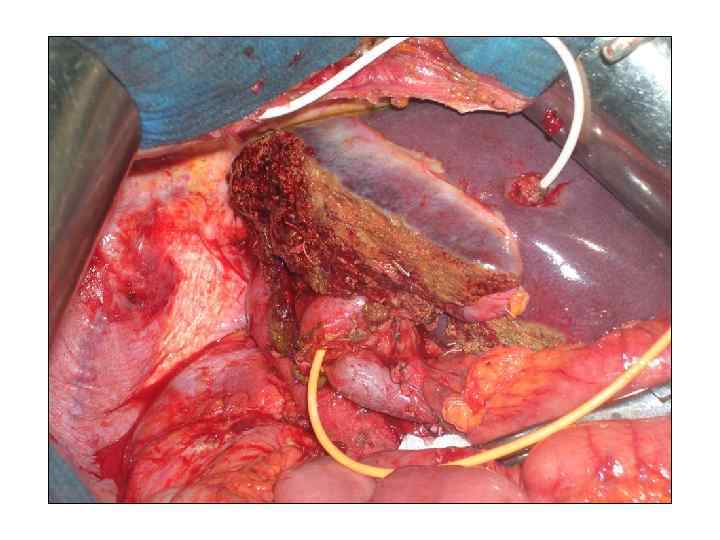
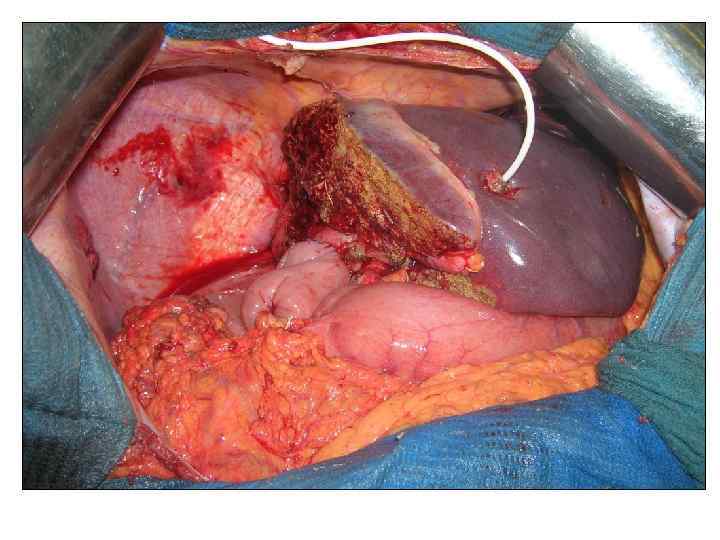
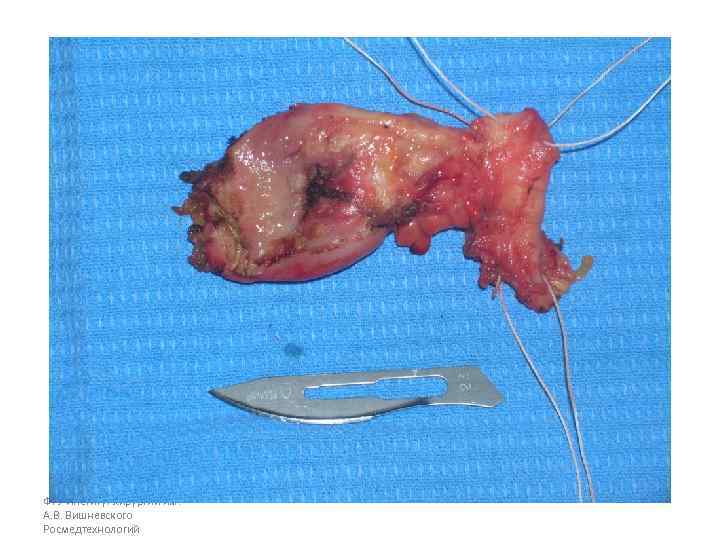 ФГУ Институт хирургии им. А. В. Вишневского Росмедтехнологий
ФГУ Институт хирургии им. А. В. Вишневского Росмедтехнологий
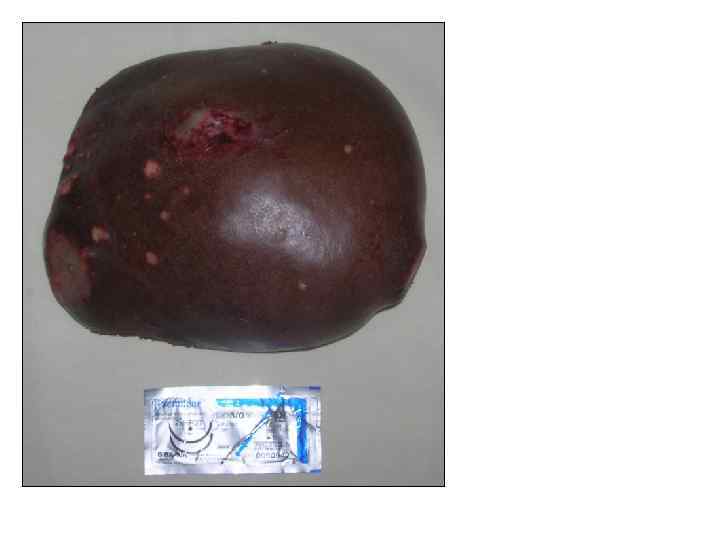
 Метастатический (вторичный) рак печени Среди метастатического злокачественных опухолей печени наиболее распространенными являются метастазы колоректального рака (КРР). Отмечается непрерывный рост заболеваемости КРР в мире. На момент первичной диагностики КРР 35 -55% больных уже имеют метастазы в печень. В течение 5 лет 65% больных имеют рецидив заболевания. Диагностика Основные задачи диагностики: 1. 2. 3. 4. Определение числа метастазов Определение их локализации Диагностика вовлечения в опухоль сосудов Выявление внпеченочных очагов опухоли МСКТ и МРТ являются основными методами диагностики метастазов КРР.
Метастатический (вторичный) рак печени Среди метастатического злокачественных опухолей печени наиболее распространенными являются метастазы колоректального рака (КРР). Отмечается непрерывный рост заболеваемости КРР в мире. На момент первичной диагностики КРР 35 -55% больных уже имеют метастазы в печень. В течение 5 лет 65% больных имеют рецидив заболевания. Диагностика Основные задачи диагностики: 1. 2. 3. 4. Определение числа метастазов Определение их локализации Диагностика вовлечения в опухоль сосудов Выявление внпеченочных очагов опухоли МСКТ и МРТ являются основными методами диагностики метастазов КРР.
 Метастатический (вторичный) рак печени Диагностика На МСКТ метастазы КРР выявляются как гиподенсные образования, слабо накапливающие контрастный препарат с гиперденсным ободком. Лучше всего метастазы визуализируются в венозную фазу исследования. Ограничения МСКТ касаются метастазов размером менее 1 см, подкапсульных метастазов, а также внепеченочных рецидивов заболевания (поражения париетальной брюшины). С внедрением мультиспиральных КТ чувствительность методики в обнаружении возросла в течение последних двух десятилетий с 52 -63% до 95%.
Метастатический (вторичный) рак печени Диагностика На МСКТ метастазы КРР выявляются как гиподенсные образования, слабо накапливающие контрастный препарат с гиперденсным ободком. Лучше всего метастазы визуализируются в венозную фазу исследования. Ограничения МСКТ касаются метастазов размером менее 1 см, подкапсульных метастазов, а также внепеченочных рецидивов заболевания (поражения париетальной брюшины). С внедрением мультиспиральных КТ чувствительность методики в обнаружении возросла в течение последних двух десятилетий с 52 -63% до 95%.
 Метастатический (вторичный) рак печени Диагностика МРТ с внутривенным контрастным усилением (гадолиний и его хелаты) позволяет более четко визуализировать метастазы небольших размеров. Чувствительность МРТ составляет 80 -90%. Дальнейший прогресс в МР-визуализации метастазов КРР связывают с внедрением новых контрастных препаратов: - контрастных агентов на основе окиси железа (superparamagnetic iron oxide (SPIO), - гепатотропных контрастных агентов.
Метастатический (вторичный) рак печени Диагностика МРТ с внутривенным контрастным усилением (гадолиний и его хелаты) позволяет более четко визуализировать метастазы небольших размеров. Чувствительность МРТ составляет 80 -90%. Дальнейший прогресс в МР-визуализации метастазов КРР связывают с внедрением новых контрастных препаратов: - контрастных агентов на основе окиси железа (superparamagnetic iron oxide (SPIO), - гепатотропных контрастных агентов.
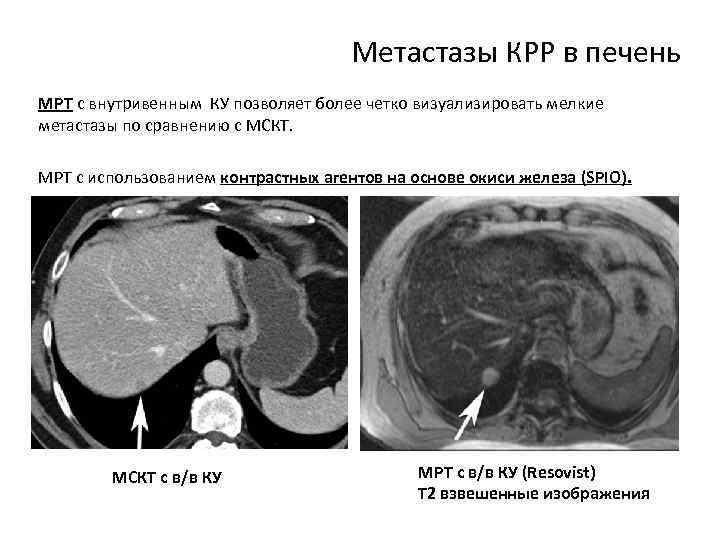 Метастазы КРР в печень МРТ с внутривенным КУ позволяет более четко визуализировать мелкие метастазы по сравнению с МСКТ. МРТ с использованием контрастных агентов на основе окиси железа (SPIO). МСКТ с в/в КУ МРТ с в/в КУ (Resovist) Т 2 взвешенные изображения
Метастазы КРР в печень МРТ с внутривенным КУ позволяет более четко визуализировать мелкие метастазы по сравнению с МСКТ. МРТ с использованием контрастных агентов на основе окиси железа (SPIO). МСКТ с в/в КУ МРТ с в/в КУ (Resovist) Т 2 взвешенные изображения
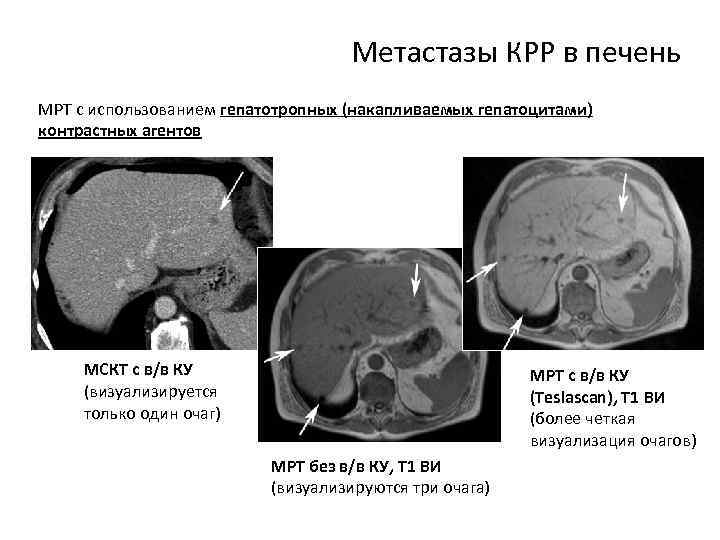 Метастазы КРР в печень МРТ с использованием гепатотропных (накапливаемых гепатоцитами) контрастных агентов МСКТ с в/в КУ (визуализируется только один очаг) МРТ с в/в КУ (Teslascan), Т 1 ВИ (более четкая визуализация очагов) МРТ без в/в КУ, Т 1 ВИ (визуализируются три очага)
Метастазы КРР в печень МРТ с использованием гепатотропных (накапливаемых гепатоцитами) контрастных агентов МСКТ с в/в КУ (визуализируется только один очаг) МРТ с в/в КУ (Teslascan), Т 1 ВИ (более четкая визуализация очагов) МРТ без в/в КУ, Т 1 ВИ (визуализируются три очага)
 Метастазы КРР в печень Лечение комбинированное: хирургическое + химиотерапия. Современные принципы лечения метастазов КРР в печень предполагают приоритет хирургической эрадикации опухоли с последующим назначением химиотерапии I. Хирургическое 1. Резекция печени 2. РЧА II. Химиотерапия 1. Системная 2. Региональная (химиоэмболизация, химиоинфузия)
Метастазы КРР в печень Лечение комбинированное: хирургическое + химиотерапия. Современные принципы лечения метастазов КРР в печень предполагают приоритет хирургической эрадикации опухоли с последующим назначением химиотерапии I. Хирургическое 1. Резекция печени 2. РЧА II. Химиотерапия 1. Системная 2. Региональная (химиоэмболизация, химиоинфузия)
 Метастазы КРР в печень Лечение Основным принципом резекционной хирургии при метастазах КРР является выполнение резекции печени в объеме R 0. Ширина отступа плоскости резекции не имеет принципиального значения, если операция выполнена в объеме R 0. В связи с этим при метастазах КРР целесообразно выполнять органосберегающие резекции печени, т. е. сегментарные и субсегментарные резекции, если размеры и число метастазов позволяет избежать обширной резекции печени (гемигепатэктомии).
Метастазы КРР в печень Лечение Основным принципом резекционной хирургии при метастазах КРР является выполнение резекции печени в объеме R 0. Ширина отступа плоскости резекции не имеет принципиального значения, если операция выполнена в объеме R 0. В связи с этим при метастазах КРР целесообразно выполнять органосберегающие резекции печени, т. е. сегментарные и субсегментарные резекции, если размеры и число метастазов позволяет избежать обширной резекции печени (гемигепатэктомии).
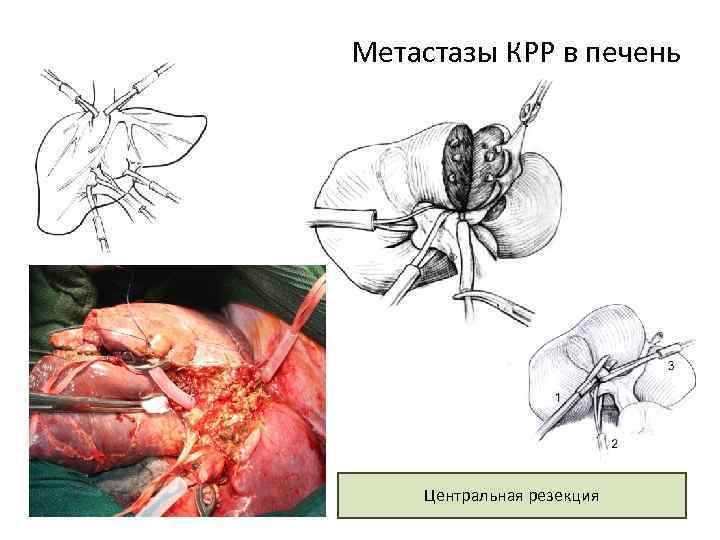 Метастазы КРР в печень Центральная резекция
Метастазы КРР в печень Центральная резекция
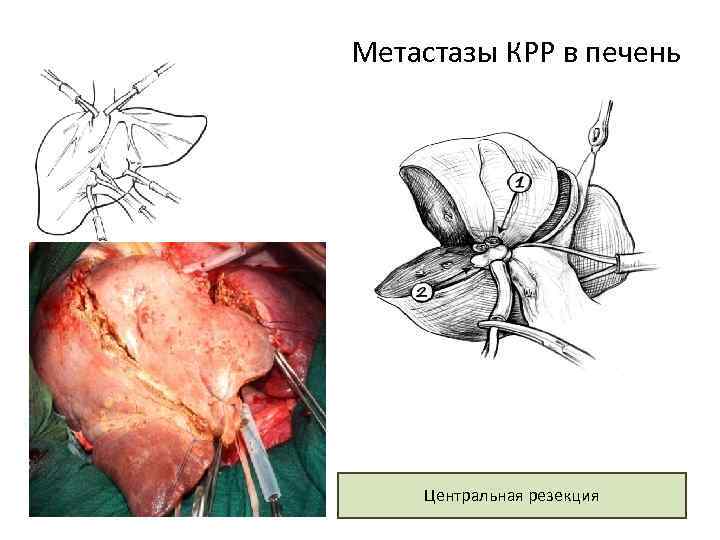 Метастазы КРР в печень Центральная резекция
Метастазы КРР в печень Центральная резекция
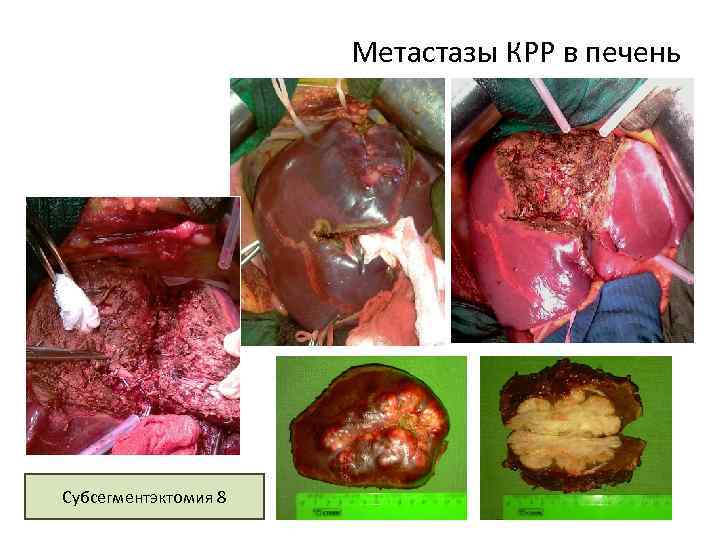 Метастазы КРР в печень Субсегментэктомия 8
Метастазы КРР в печень Субсегментэктомия 8
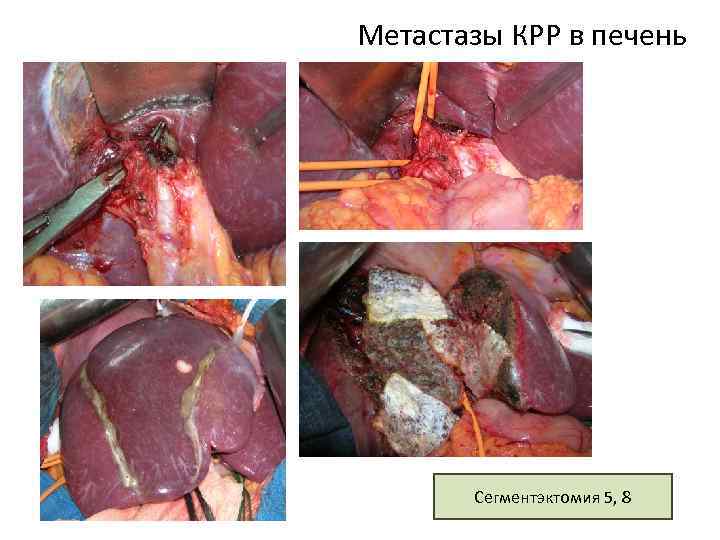 Метастазы КРР в печень Сегментэктомия 5, 8
Метастазы КРР в печень Сегментэктомия 5, 8
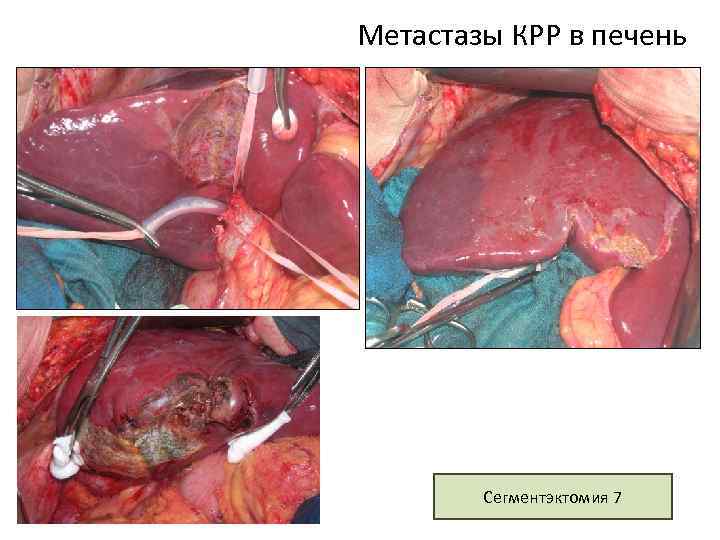 Метастазы КРР в печень Сегментэктомия 7
Метастазы КРР в печень Сегментэктомия 7
 Метастазы КРР в печень Отдаленные результаты резекций печени из 363 центров мира (декабрь 2010)
Метастазы КРР в печень Отдаленные результаты резекций печени из 363 центров мира (декабрь 2010)
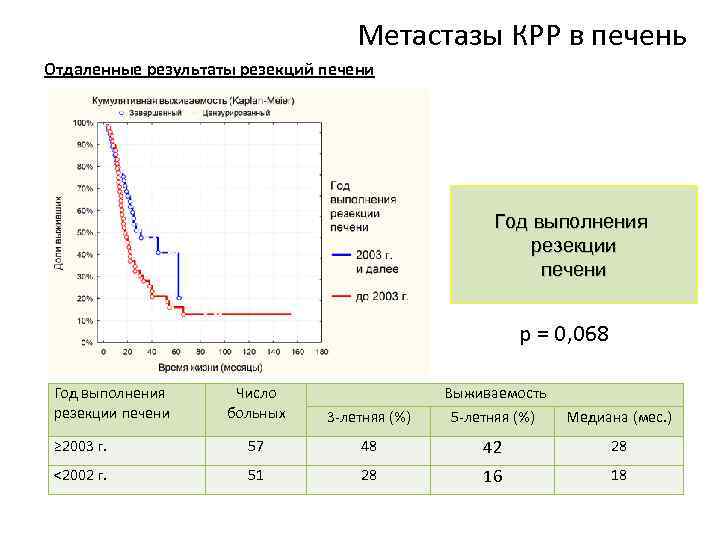 Метастазы КРР в печень Отдаленные результаты резекций печени Год выполнения резекции печени p = 0, 068 Год выполнения резекции печени Число больных 3 -летняя (%) Выживаемость 5 -летняя (%) Медиана (мес. ) ≥ 2003 г. 57 48 42 28 <2002 г. 51 28 16 18
Метастазы КРР в печень Отдаленные результаты резекций печени Год выполнения резекции печени p = 0, 068 Год выполнения резекции печени Число больных 3 -летняя (%) Выживаемость 5 -летняя (%) Медиана (мес. ) ≥ 2003 г. 57 48 42 28 <2002 г. 51 28 16 18
 Метастазы КРР в печень Химиотерапия (современные принципы) Препаратами 1 -й линии являются современные цитостатики (оксалиплатин, иринотекан) в комбинации с традиционными цитостатиками (5 -фторурацил+лейковарин): 1. 2. 3. 4. 5. FOLFOX FOLFIRI XELOX FOLFOXIRI и др. … 5 -ФТУ + ЛВ + оксалиплатин 5 -ФТУ + ЛВ + иринотекан кселода + ЛВ + оксалиплатин 5 -ФТУ + ЛВ + оксалиплатин + иринотекан Во 2 -й линии производится смена вышеперечисленных комбинаций цистостатиков. В 3 -й и 4 -й линиях к цитостатикам добавляются биопрепараты (таргетные препараты) – моноклональные антитела: ингибиторы рецепторов эпидермального фактора роста (цетуксимаб, гефитиниб, эрлотиниб и др. ) и ингибиторы сосудистого эндотелиального фактора роста (бевацизумаб).
Метастазы КРР в печень Химиотерапия (современные принципы) Препаратами 1 -й линии являются современные цитостатики (оксалиплатин, иринотекан) в комбинации с традиционными цитостатиками (5 -фторурацил+лейковарин): 1. 2. 3. 4. 5. FOLFOX FOLFIRI XELOX FOLFOXIRI и др. … 5 -ФТУ + ЛВ + оксалиплатин 5 -ФТУ + ЛВ + иринотекан кселода + ЛВ + оксалиплатин 5 -ФТУ + ЛВ + оксалиплатин + иринотекан Во 2 -й линии производится смена вышеперечисленных комбинаций цистостатиков. В 3 -й и 4 -й линиях к цитостатикам добавляются биопрепараты (таргетные препараты) – моноклональные антитела: ингибиторы рецепторов эпидермального фактора роста (цетуксимаб, гефитиниб, эрлотиниб и др. ) и ингибиторы сосудистого эндотелиального фактора роста (бевацизумаб).
 Метастазы КРР в печень Химиотерапия Number of resected metastases Median follow-up (months) Lorenz M (1998) ≤ 6 liver metastases ≥ 18 108 vs 111 Kemeny N (1999) Any number of liver metastases 62· 7 1– 3 liver metastases Mitry E (2006) Portier G (2006) Kemeny M (2002) Number of patients Randomised postoperative treatments Median TTP/PFS (months) Median overall survival (months) HAI FU/FA vs surgery alone 14· 2 vs 13· 7 (NS) 34· 5 vs 40· 8 (p=0· 15) 74 vs 82 Systemic FU/FA +HAI FUDR vs systemic FU/FA 37· 4 vs 17· 2 (p=0· 06) 72· 2 vs 59· 3 (p=0· 21) 51 30 vs 45 HAI FUDR +systemic FU vs surgery alone 45· 7%*vs 25· 2%* (p=0· 04) 63· 7 vs 49· 0 (p=0· 60) ≤ 4 liver or lung metastases NR 138 vs 140 Systemic FU/FA vs surgery alone 26· 4 vs 18· 6 (p=0· 059) 61· 1 vs 46· 9 (p=0· 125) Any number of liver metastases 87 86 vs 87 Systemic FU/FA vs surgery alone 24· 4 vs 17· 6 (p=0· 028) 62· 1 vs 46· 4 (p=0· 13) TTP=time to progression. PFS=progression-free survival. HAI=hepatic arterial infusion. FUDR=floxuridine. FU=fluorouracil. FA=folinic acid. NS=not significant. NR=not reported. * - 4 -year progression-free survival rates. Perioperative chemotherapy with FOLFOX 4 and surgery versus surgery alone for resectable liver metastases from colorectal cancer (EORTC Intergroup trial 40983): a randomised controlled Trial. Lancet. 2008 March 22; 371(9617): 1007– 1016.
Метастазы КРР в печень Химиотерапия Number of resected metastases Median follow-up (months) Lorenz M (1998) ≤ 6 liver metastases ≥ 18 108 vs 111 Kemeny N (1999) Any number of liver metastases 62· 7 1– 3 liver metastases Mitry E (2006) Portier G (2006) Kemeny M (2002) Number of patients Randomised postoperative treatments Median TTP/PFS (months) Median overall survival (months) HAI FU/FA vs surgery alone 14· 2 vs 13· 7 (NS) 34· 5 vs 40· 8 (p=0· 15) 74 vs 82 Systemic FU/FA +HAI FUDR vs systemic FU/FA 37· 4 vs 17· 2 (p=0· 06) 72· 2 vs 59· 3 (p=0· 21) 51 30 vs 45 HAI FUDR +systemic FU vs surgery alone 45· 7%*vs 25· 2%* (p=0· 04) 63· 7 vs 49· 0 (p=0· 60) ≤ 4 liver or lung metastases NR 138 vs 140 Systemic FU/FA vs surgery alone 26· 4 vs 18· 6 (p=0· 059) 61· 1 vs 46· 9 (p=0· 125) Any number of liver metastases 87 86 vs 87 Systemic FU/FA vs surgery alone 24· 4 vs 17· 6 (p=0· 028) 62· 1 vs 46· 4 (p=0· 13) TTP=time to progression. PFS=progression-free survival. HAI=hepatic arterial infusion. FUDR=floxuridine. FU=fluorouracil. FA=folinic acid. NS=not significant. NR=not reported. * - 4 -year progression-free survival rates. Perioperative chemotherapy with FOLFOX 4 and surgery versus surgery alone for resectable liver metastases from colorectal cancer (EORTC Intergroup trial 40983): a randomised controlled Trial. Lancet. 2008 March 22; 371(9617): 1007– 1016.
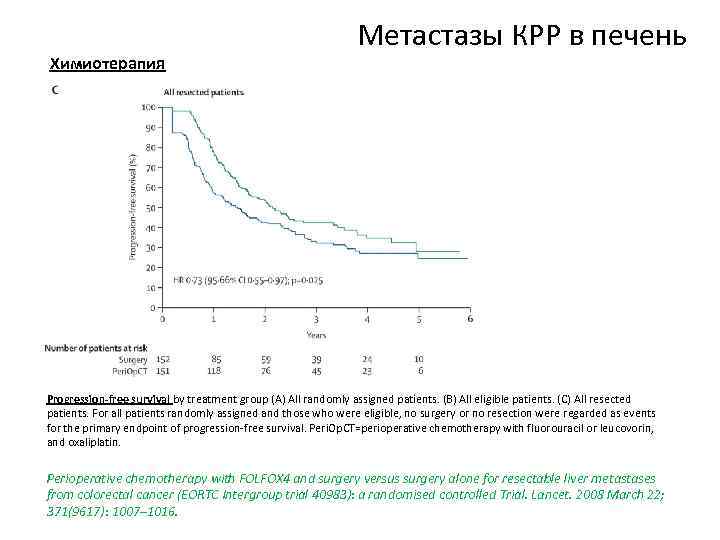 Химиотерапия Метастазы КРР в печень Progression-free survival by treatment group (A) All randomly assigned patients. (B) All eligible patients. (C) All resected patients. For all patients randomly assigned and those who were eligible, no surgery or no resection were regarded as events for the primary endpoint of progression-free survival. Peri. Op. CT=perioperative chemotherapy with fluorouracil or leucovorin, and oxaliplatin. Perioperative chemotherapy with FOLFOX 4 and surgery versus surgery alone for resectable liver metastases from colorectal cancer (EORTC Intergroup trial 40983): a randomised controlled Trial. Lancet. 2008 March 22; 371(9617): 1007– 1016.
Химиотерапия Метастазы КРР в печень Progression-free survival by treatment group (A) All randomly assigned patients. (B) All eligible patients. (C) All resected patients. For all patients randomly assigned and those who were eligible, no surgery or no resection were regarded as events for the primary endpoint of progression-free survival. Peri. Op. CT=perioperative chemotherapy with fluorouracil or leucovorin, and oxaliplatin. Perioperative chemotherapy with FOLFOX 4 and surgery versus surgery alone for resectable liver metastases from colorectal cancer (EORTC Intergroup trial 40983): a randomised controlled Trial. Lancet. 2008 March 22; 371(9617): 1007– 1016.
 Доброкачественные опухоли и опухолеподобные образования Фокальная нодулярная гиперплазия (ФНГ) является вторым по частоте после гемангиомы доброкачественным солидным очаговым образованием печени, выявляемым приблизительно у 3% взрослых людей ФНГ впервые была описана в 1958 г. Edmondson. Развитие ФНГ связывают с локальной гиперперфузией печеночной паренхимы на фоне микроскопической артериальной мальформации (Wanlesset al. 1985). ФНГ чаще всего развивается у женщин (в 8 раз чаще) в возрасте 20 -50 лет. Обсуждается роль в развитии ФНГ гормональных контрацептивов, что до сих пор не доказано, хотя подтверждено, что прием этих препаратов вызывает рост ФНГ, как правило, является случайной находкой при обследовании , выполняемым по различным другим поводам. ФНГ имеет типичные УЗ и МСКТ характеристики, но в ряде случаев требует морфологического подтверждения. Подтвердить или отвергнуть диагноз ФНГ или опухоли печени (аденома, ГЦР) по результатам пункционной биопсии не всегда возможно. Тем не менее, сама ФНГ никогда не малигнизируется. Также казуистикой является разрыв ФНГ с кровотечением. Edmondson HA. Tumors of the liver and intrahepatic bile ducts. In: Atlas of tumor pathology. In: Washington, DC: Armed Forces Institute of Pathology; 1958. Wanless IR, Mawdsley C, Adams R. On the pathogenesis of focal nodular hyperplasia of the liver. Hepatology 1985; 5: 1194 -200.
Доброкачественные опухоли и опухолеподобные образования Фокальная нодулярная гиперплазия (ФНГ) является вторым по частоте после гемангиомы доброкачественным солидным очаговым образованием печени, выявляемым приблизительно у 3% взрослых людей ФНГ впервые была описана в 1958 г. Edmondson. Развитие ФНГ связывают с локальной гиперперфузией печеночной паренхимы на фоне микроскопической артериальной мальформации (Wanlesset al. 1985). ФНГ чаще всего развивается у женщин (в 8 раз чаще) в возрасте 20 -50 лет. Обсуждается роль в развитии ФНГ гормональных контрацептивов, что до сих пор не доказано, хотя подтверждено, что прием этих препаратов вызывает рост ФНГ, как правило, является случайной находкой при обследовании , выполняемым по различным другим поводам. ФНГ имеет типичные УЗ и МСКТ характеристики, но в ряде случаев требует морфологического подтверждения. Подтвердить или отвергнуть диагноз ФНГ или опухоли печени (аденома, ГЦР) по результатам пункционной биопсии не всегда возможно. Тем не менее, сама ФНГ никогда не малигнизируется. Также казуистикой является разрыв ФНГ с кровотечением. Edmondson HA. Tumors of the liver and intrahepatic bile ducts. In: Atlas of tumor pathology. In: Washington, DC: Armed Forces Institute of Pathology; 1958. Wanless IR, Mawdsley C, Adams R. On the pathogenesis of focal nodular hyperplasia of the liver. Hepatology 1985; 5: 1194 -200.
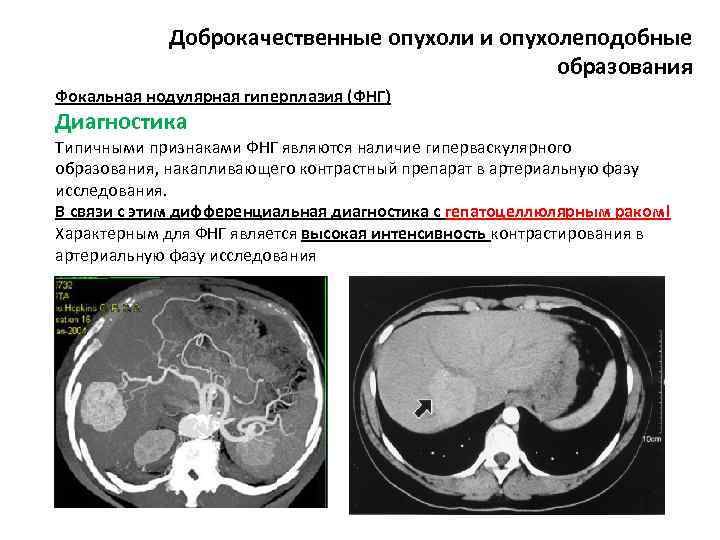 Доброкачественные опухоли и опухолеподобные образования Фокальная нодулярная гиперплазия (ФНГ) Диагностика Типичными признаками ФНГ являются наличие гиперваскулярного образования, накапливающего контрастный препарат в артериальную фазу исследования. В связи с этим дифференциальная диагностика с гепатоцеллюлярным раком! Характерным для ФНГ является высокая интенсивность контрастирования в артериальную фазу исследования
Доброкачественные опухоли и опухолеподобные образования Фокальная нодулярная гиперплазия (ФНГ) Диагностика Типичными признаками ФНГ являются наличие гиперваскулярного образования, накапливающего контрастный препарат в артериальную фазу исследования. В связи с этим дифференциальная диагностика с гепатоцеллюлярным раком! Характерным для ФНГ является высокая интенсивность контрастирования в артериальную фазу исследования
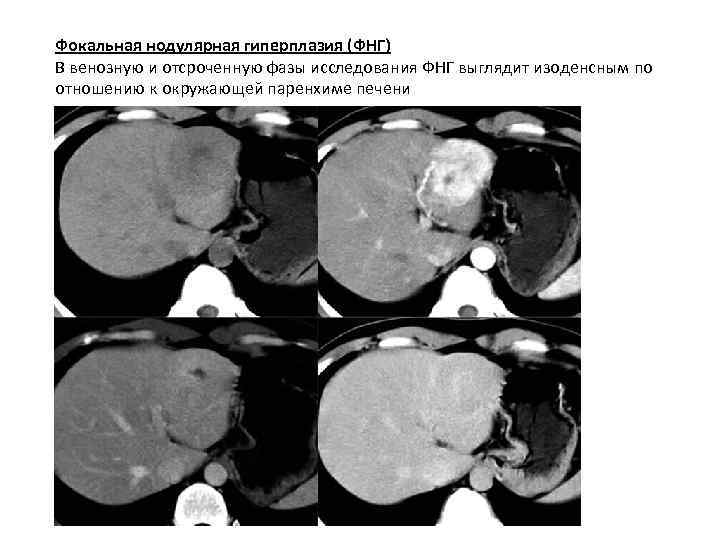 Фокальная нодулярная гиперплазия (ФНГ) В венозную и отсроченную фазы исследования ФНГ выглядит изоденсным по отношению к окружающей паренхиме печени
Фокальная нодулярная гиперплазия (ФНГ) В венозную и отсроченную фазы исследования ФНГ выглядит изоденсным по отношению к окружающей паренхиме печени
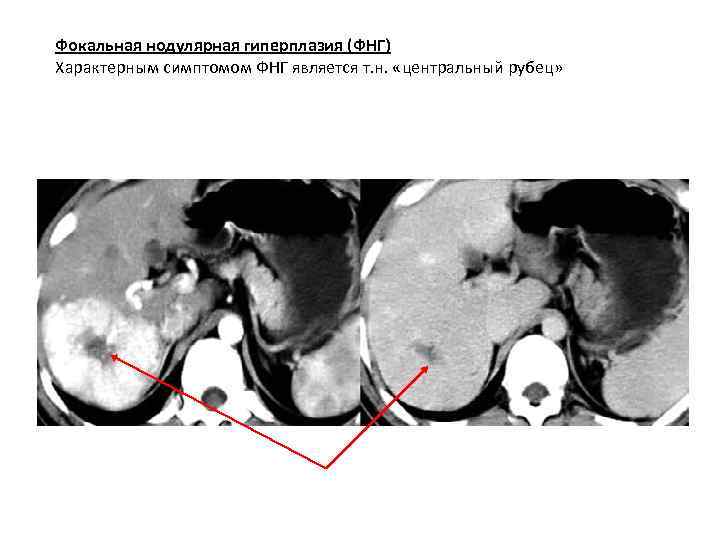 Фокальная нодулярная гиперплазия (ФНГ) Характерным симптомом ФНГ является т. н. «центральный рубец»
Фокальная нодулярная гиперплазия (ФНГ) Характерным симптомом ФНГ является т. н. «центральный рубец»
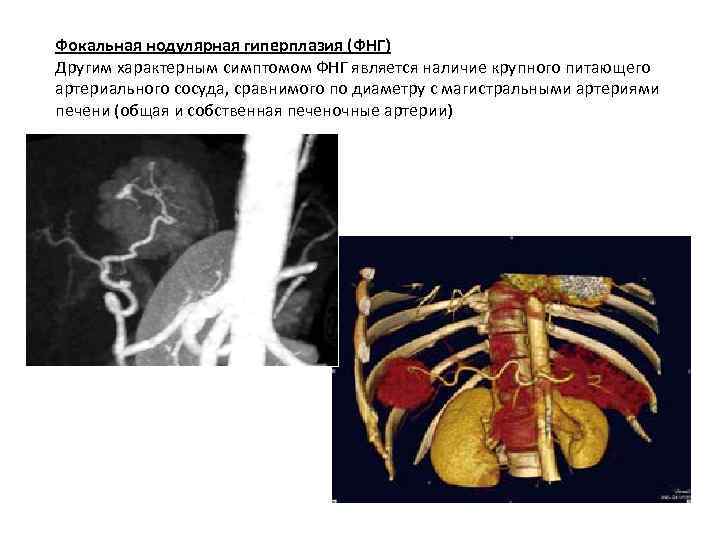 Фокальная нодулярная гиперплазия (ФНГ) Другим характерным симптомом ФНГ является наличие крупного питающего артериального сосуда, сравнимого по диаметру с магистральными артериями печени (общая и собственная печеночные артерии)
Фокальная нодулярная гиперплазия (ФНГ) Другим характерным симптомом ФНГ является наличие крупного питающего артериального сосуда, сравнимого по диаметру с магистральными артериями печени (общая и собственная печеночные артерии)
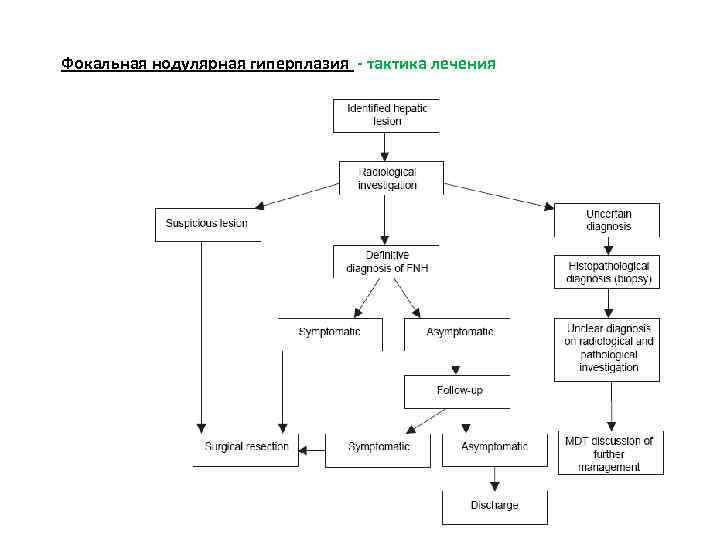 Фокальная нодулярная гиперплазия - тактика лечения
Фокальная нодулярная гиперплазия - тактика лечения
 Больная Б. , 27 л. Жалобы: на боли периодические боли в эпигастрии, тошноту, изжогу Анамнез заболевания: • Впервые образование левой доли печени (гемангиома) выявлено при УЗИ в 2009 г. • Рекомендовано динамическое наблюдение. В конце 2010 г появились вышеуказанные жалобы. При обследовании отмечается увеличение образование в размерах, смещение желудка влево. Диагноз: фокальная нодулярная гиперплазия левой доли печени
Больная Б. , 27 л. Жалобы: на боли периодические боли в эпигастрии, тошноту, изжогу Анамнез заболевания: • Впервые образование левой доли печени (гемангиома) выявлено при УЗИ в 2009 г. • Рекомендовано динамическое наблюдение. В конце 2010 г появились вышеуказанные жалобы. При обследовании отмечается увеличение образование в размерах, смещение желудка влево. Диагноз: фокальная нодулярная гиперплазия левой доли печени
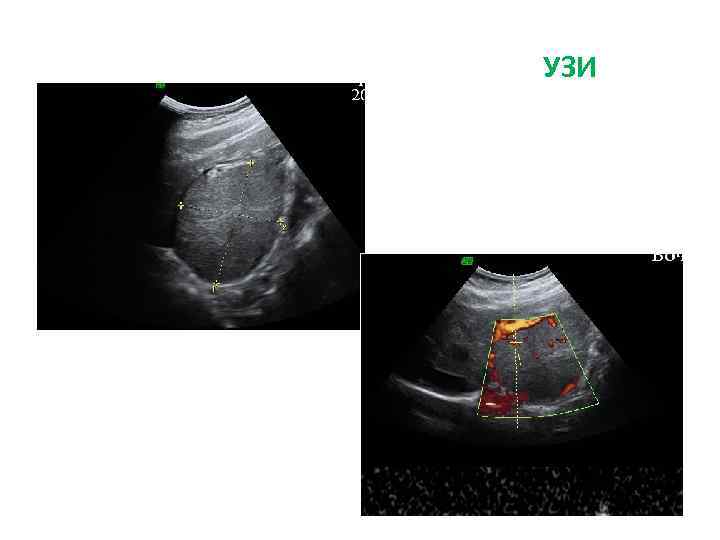 УЗИ
УЗИ
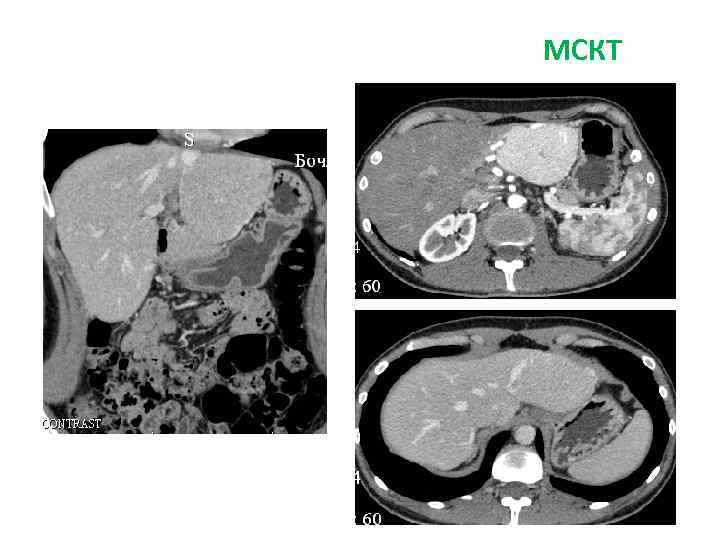 СКТ МСКТ
СКТ МСКТ
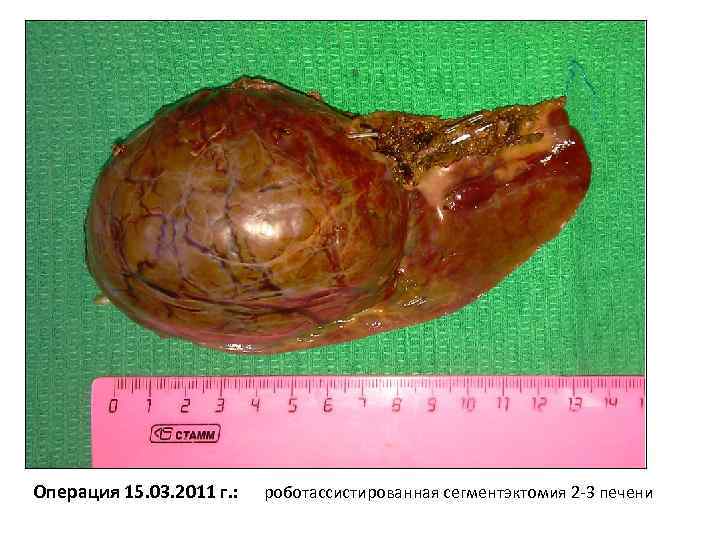 Операция 15. 03. 2011 г. : роботассистированная сегментэктомия 2 -3 печени
Операция 15. 03. 2011 г. : роботассистированная сегментэктомия 2 -3 печени
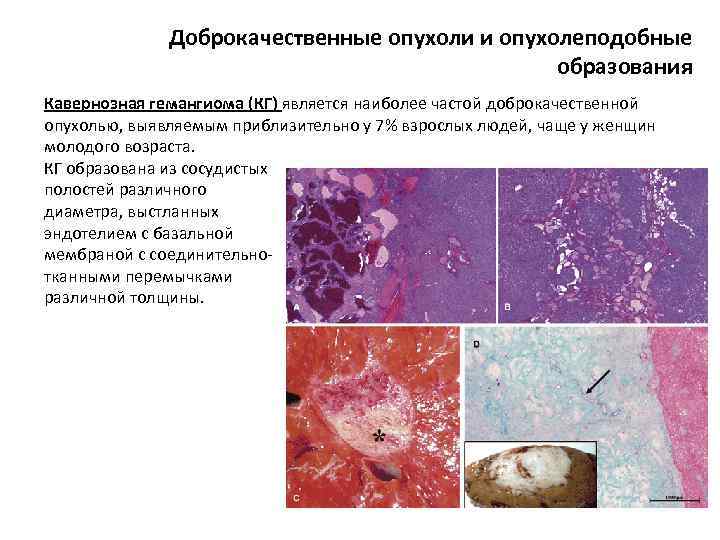 Доброкачественные опухоли и опухолеподобные образования Кавернозная гемангиома (КГ) является наиболее частой доброкачественной опухолью, выявляемым приблизительно у 7% взрослых людей, чаще у женщин молодого возраста. КГ образована из сосудистых полостей различного диаметра, выстланных эндотелием с базальной мембраной с соединительнотканными перемычками различной толщины.
Доброкачественные опухоли и опухолеподобные образования Кавернозная гемангиома (КГ) является наиболее частой доброкачественной опухолью, выявляемым приблизительно у 7% взрослых людей, чаще у женщин молодого возраста. КГ образована из сосудистых полостей различного диаметра, выстланных эндотелием с базальной мембраной с соединительнотканными перемычками различной толщины.
 Доброкачественные опухоли и опухолеподобные образования Кавернозная гемангиома (КГ) Патогенез КГ не известен. Предположительно КГ развиваются в результате нарушения процесса ангиогенеза. Эндотелиальные клетки КГ имеют большую склонность к избыточному ангиогенезу по сравнению с эндотелиальными клетками синусоидов печени. Диагностика УЗИ. КГ небольших размеров визуализируются как гиперэхогенные образования с четкими ровными контурами.
Доброкачественные опухоли и опухолеподобные образования Кавернозная гемангиома (КГ) Патогенез КГ не известен. Предположительно КГ развиваются в результате нарушения процесса ангиогенеза. Эндотелиальные клетки КГ имеют большую склонность к избыточному ангиогенезу по сравнению с эндотелиальными клетками синусоидов печени. Диагностика УЗИ. КГ небольших размеров визуализируются как гиперэхогенные образования с четкими ровными контурами.
 Доброкачественные опухоли и опухолеподобные образования Кавернозная гемангиома (КГ) Патогенез КГ не известен. Предположительно КГ развиваются в результате нарушения процесса ангиогенеза. Эндотелиальные клетки КГ имеют большую склонность к избыточному ангиогенезу по сравнению с эндотелиальными клетками синусоидов печени. Диагностика УЗИ. КГ небольших размеров визуализируются как гиперэхогенные образования с четкими ровными контурами.
Доброкачественные опухоли и опухолеподобные образования Кавернозная гемангиома (КГ) Патогенез КГ не известен. Предположительно КГ развиваются в результате нарушения процесса ангиогенеза. Эндотелиальные клетки КГ имеют большую склонность к избыточному ангиогенезу по сравнению с эндотелиальными клетками синусоидов печени. Диагностика УЗИ. КГ небольших размеров визуализируются как гиперэхогенные образования с четкими ровными контурами.
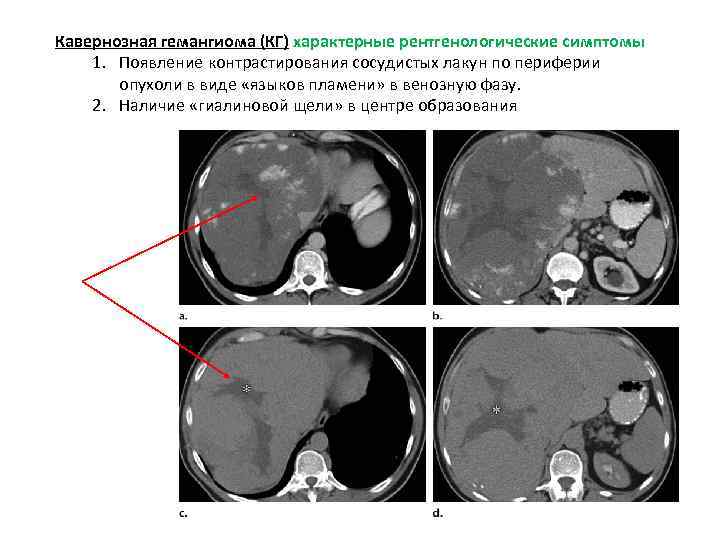 Кавернозная гемангиома (КГ) характерные рентгенологические симптомы 1. Появление контрастирования сосудистых лакун по периферии опухоли в виде «языков пламени» в венозную фазу. 2. Наличие «гиалиновой щели» в центре образования
Кавернозная гемангиома (КГ) характерные рентгенологические симптомы 1. Появление контрастирования сосудистых лакун по периферии опухоли в виде «языков пламени» в венозную фазу. 2. Наличие «гиалиновой щели» в центре образования
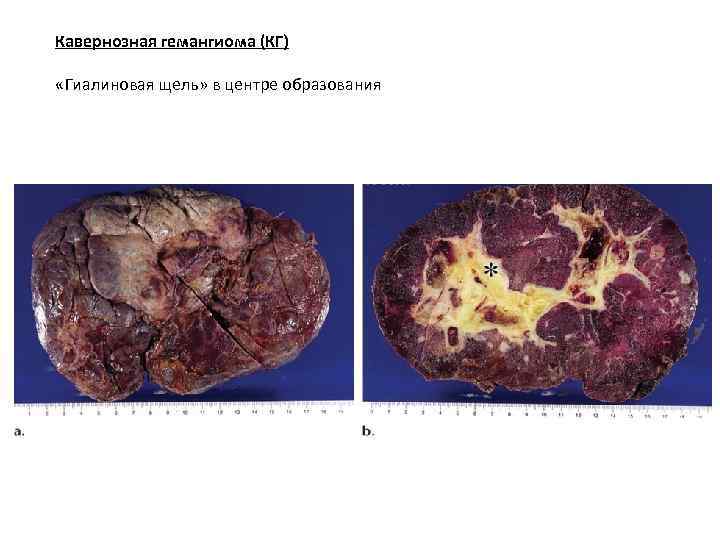 Кавернозная гемангиома (КГ) «Гиалиновая щель» в центре образования
Кавернозная гемангиома (КГ) «Гиалиновая щель» в центре образования
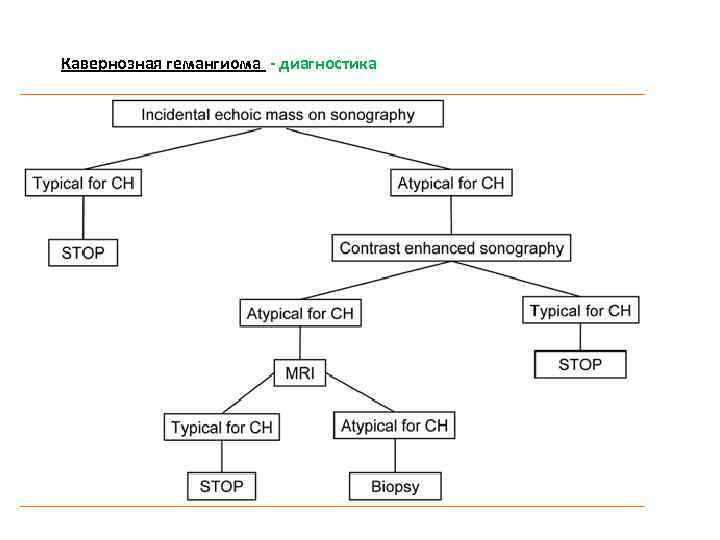 Кавернозная гемангиома - диагностика
Кавернозная гемангиома - диагностика
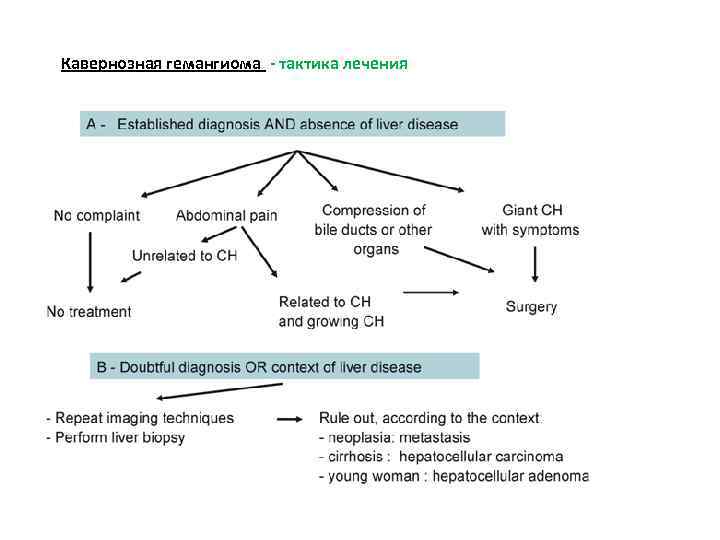 Кавернозная гемангиома - тактика лечения
Кавернозная гемангиома - тактика лечения
 Больная М. , 45 л. Диагноз до операции: «Опухоль правой доли печени (гемангиома? гепатоцеллюлярный рак? )» Жалобы: на периодические умеренной интенсивности боли и чувство дискомфорта в правой половине живота, провоцируемых физической нагрузкой. Анамнез заболевания: болеет с августа 2006 г. , когда впервые выявлена опухоль печени при обследовании по поводу болевого синдрома в верхних отделах живота при физической нагрузке.
Больная М. , 45 л. Диагноз до операции: «Опухоль правой доли печени (гемангиома? гепатоцеллюлярный рак? )» Жалобы: на периодические умеренной интенсивности боли и чувство дискомфорта в правой половине живота, провоцируемых физической нагрузкой. Анамнез заболевания: болеет с августа 2006 г. , когда впервые выявлена опухоль печени при обследовании по поводу болевого синдрома в верхних отделах живота при физической нагрузке.
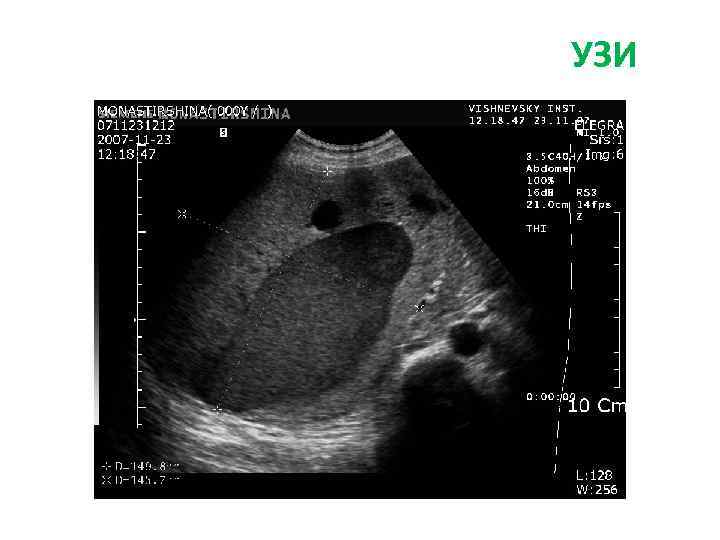 УЗИ
УЗИ
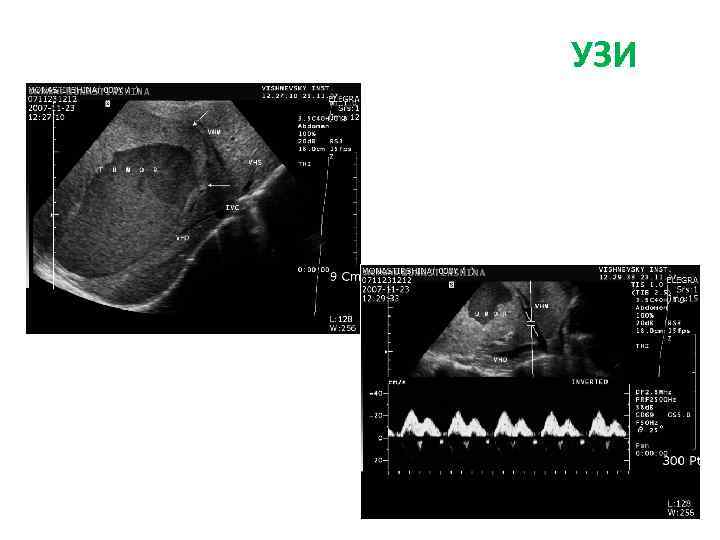 УЗИ + ДС сосудов брюшной полости УЗИ
УЗИ + ДС сосудов брюшной полости УЗИ
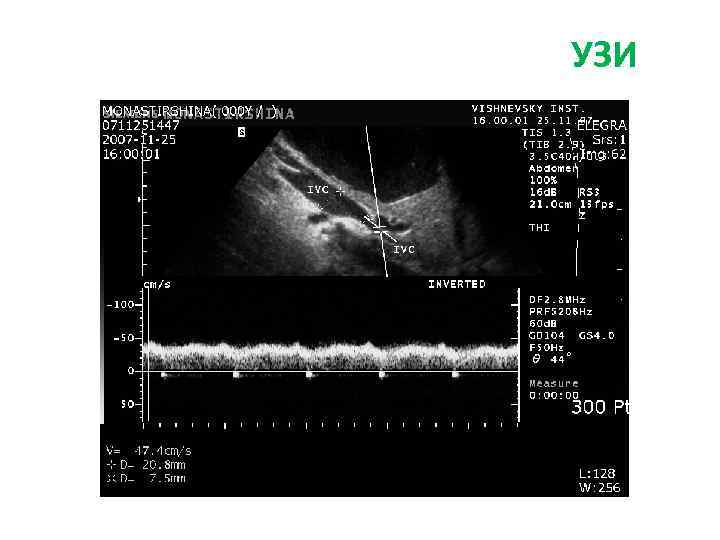 УЗИ + ДС сосудов брюшной полости УЗИ
УЗИ + ДС сосудов брюшной полости УЗИ
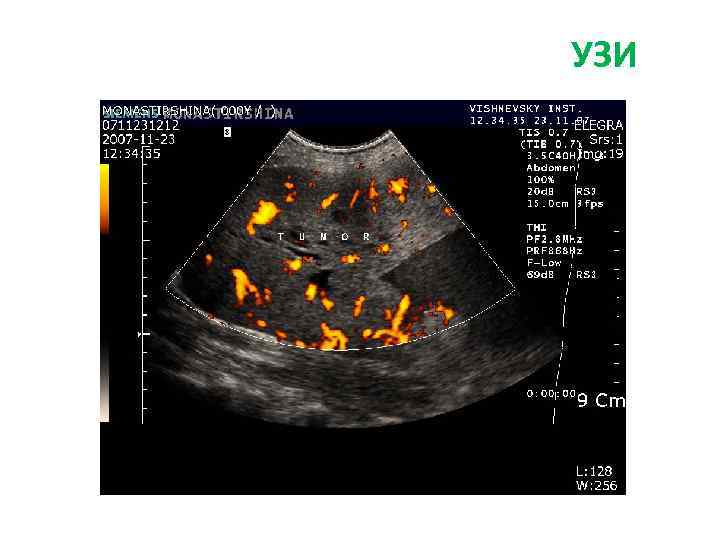 УЗИ + ДС сосудов брюшной полости УЗИ
УЗИ + ДС сосудов брюшной полости УЗИ
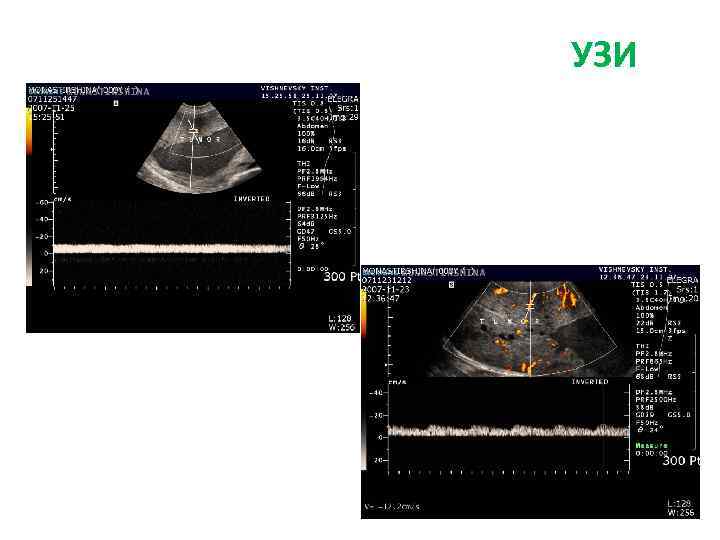 УЗИ + ДС сосудов брюшной полости УЗИ
УЗИ + ДС сосудов брюшной полости УЗИ
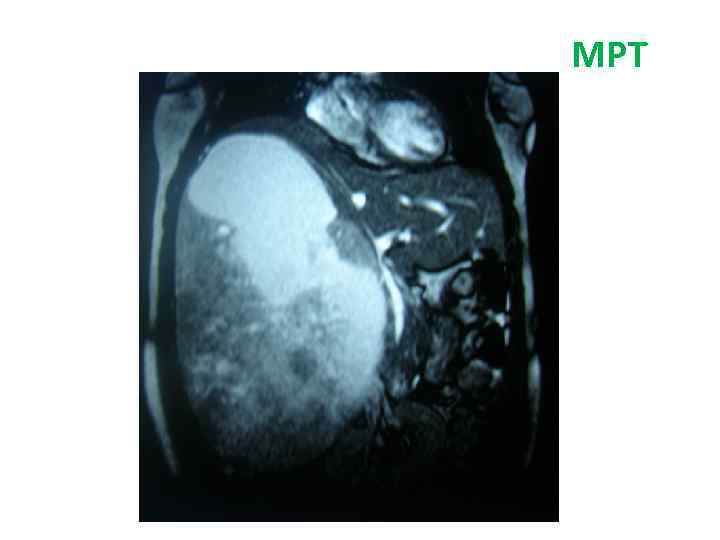 МРТ брюшной полости МРТ
МРТ брюшной полости МРТ
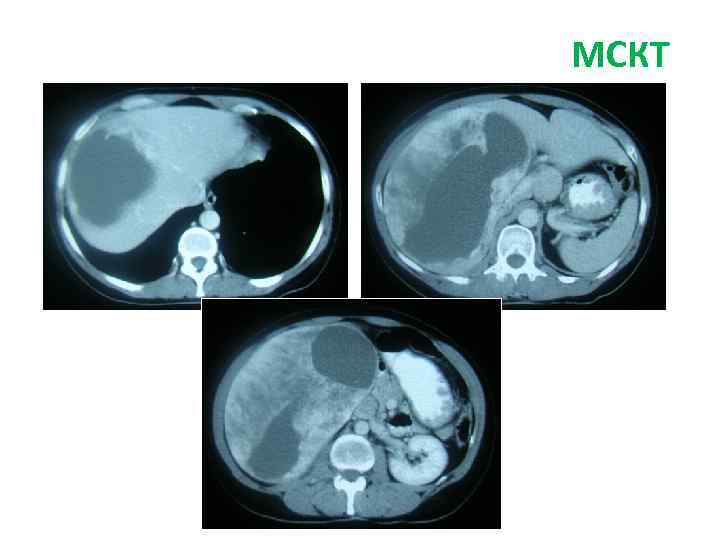 СКТ брюшной полости МСКТ
СКТ брюшной полости МСКТ
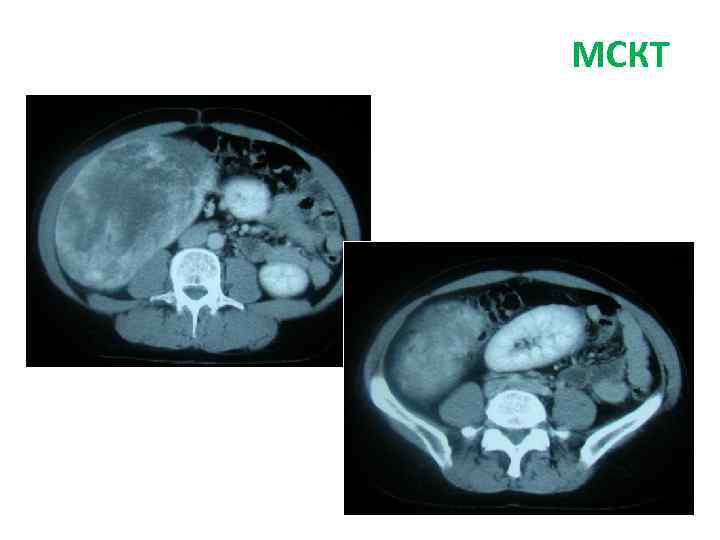 СКТ брюшной полости МСКТ
СКТ брюшной полости МСКТ
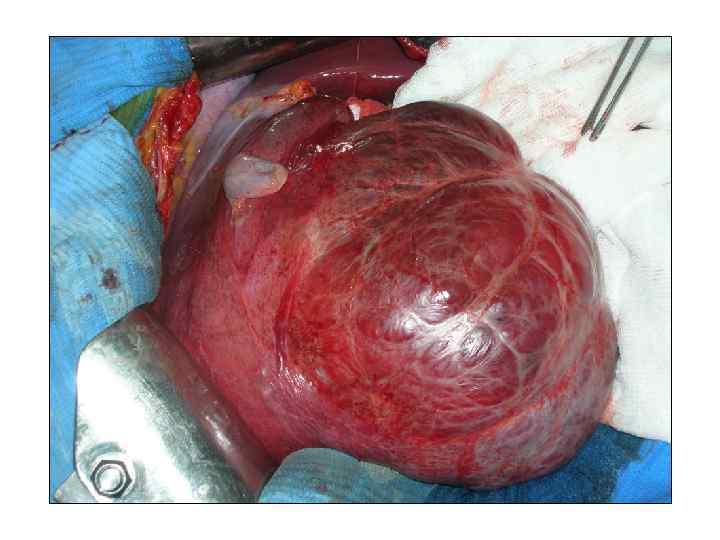
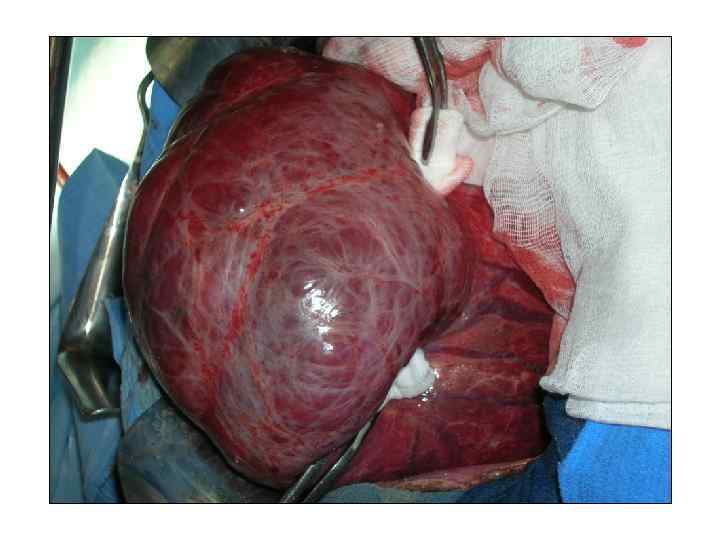
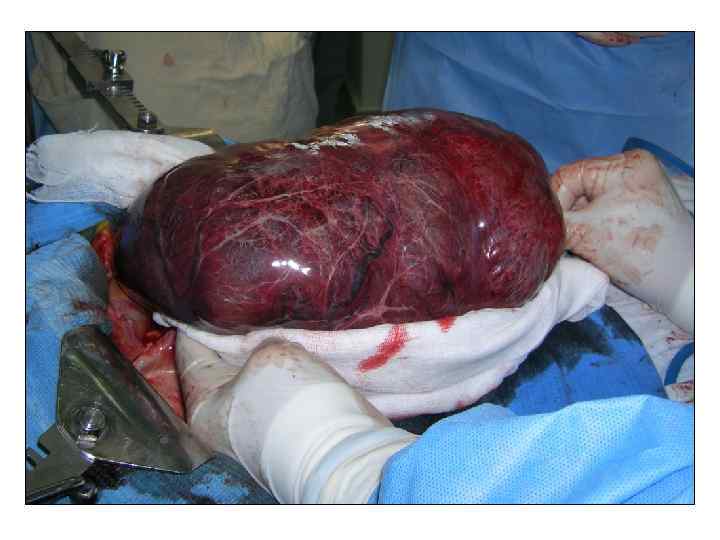
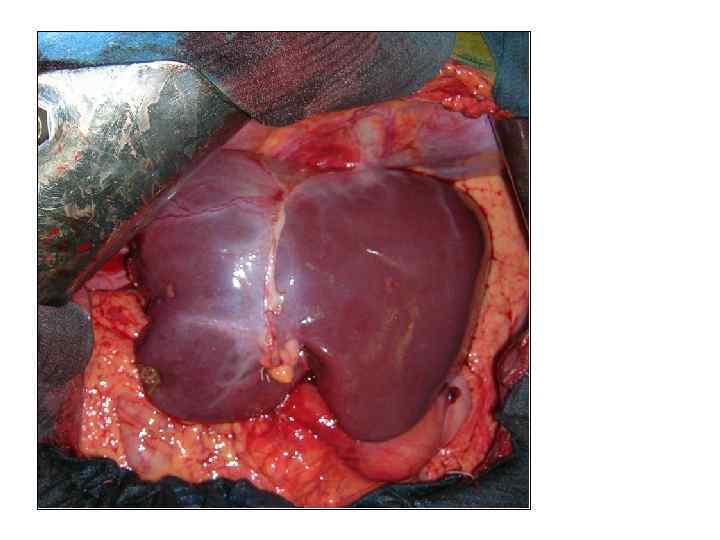
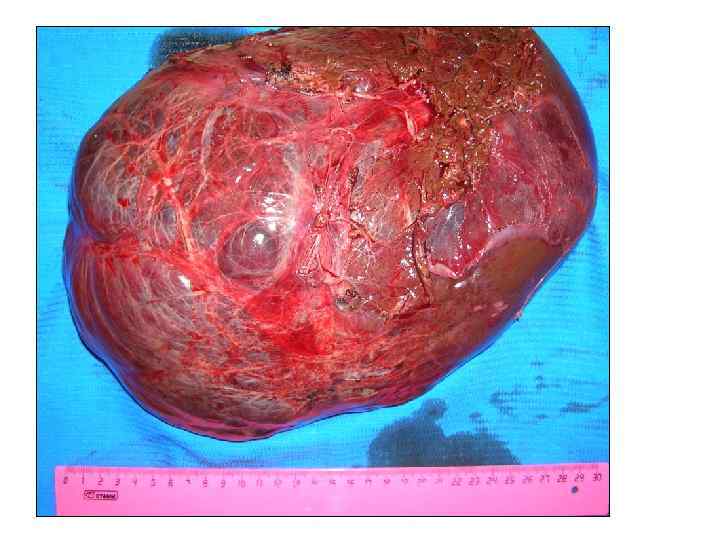
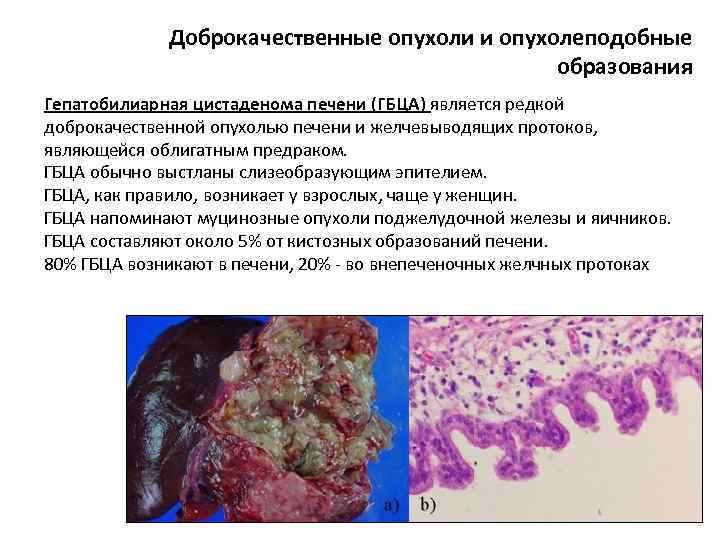 Доброкачественные опухоли и опухолеподобные образования Гепатобилиарная цистаденома печени (ГБЦА) является редкой доброкачественной опухолью печени и желчевыводящих протоков, являющейся облигатным предраком. ГБЦА обычно выстланы слизеобразующим эпителием. ГБЦА, как правило, возникает у взрослых, чаще у женщин. ГБЦА напоминают муцинозные опухоли поджелудочной железы и яичников. ГБЦА составляют около 5% от кистозных образований печени. 80% ГБЦА возникают в печени, 20% - во внепеченочных желчных протоках
Доброкачественные опухоли и опухолеподобные образования Гепатобилиарная цистаденома печени (ГБЦА) является редкой доброкачественной опухолью печени и желчевыводящих протоков, являющейся облигатным предраком. ГБЦА обычно выстланы слизеобразующим эпителием. ГБЦА, как правило, возникает у взрослых, чаще у женщин. ГБЦА напоминают муцинозные опухоли поджелудочной железы и яичников. ГБЦА составляют около 5% от кистозных образований печени. 80% ГБЦА возникают в печени, 20% - во внепеченочных желчных протоках
 Больная П. , 60 л. Диагноз: цистаденома левой доли печени. Эхинококковые кисты печени и брюшной полости? Состояние после дренирования кисты 06. 2011. ЖКБ. Хронический калькулезный холецистит. Гипертоническая болезнь II стадии. Варикозное расширение вен обеих нижних конечностей, 3 ст CEAP.
Больная П. , 60 л. Диагноз: цистаденома левой доли печени. Эхинококковые кисты печени и брюшной полости? Состояние после дренирования кисты 06. 2011. ЖКБ. Хронический калькулезный холецистит. Гипертоническая болезнь II стадии. Варикозное расширение вен обеих нижних конечностей, 3 ст CEAP.
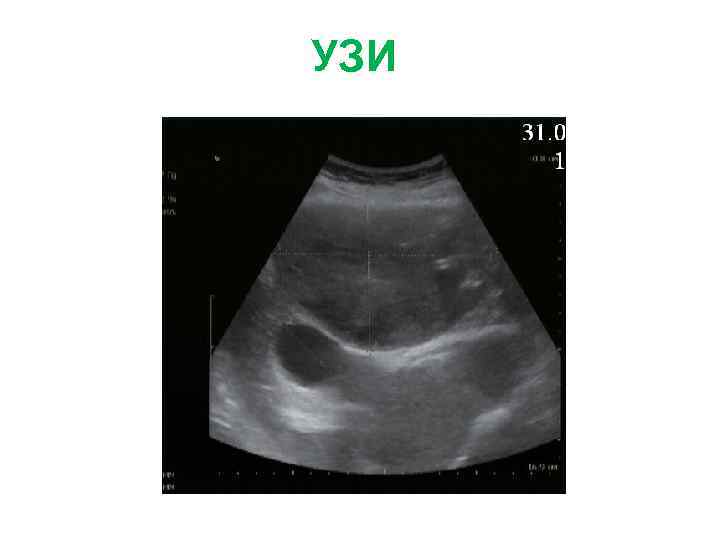 УЗИ
УЗИ
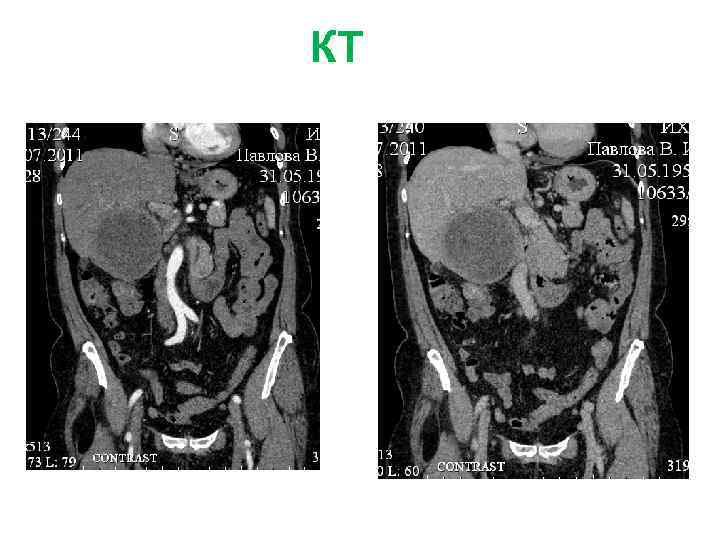 КТ
КТ
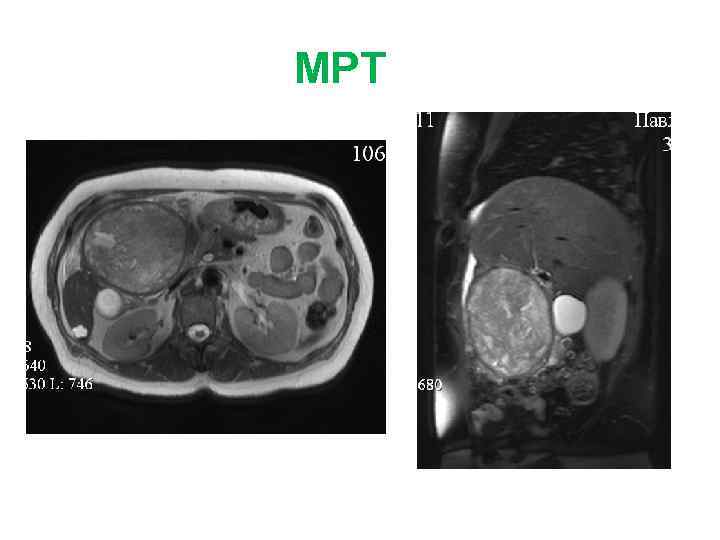 МРТ
МРТ
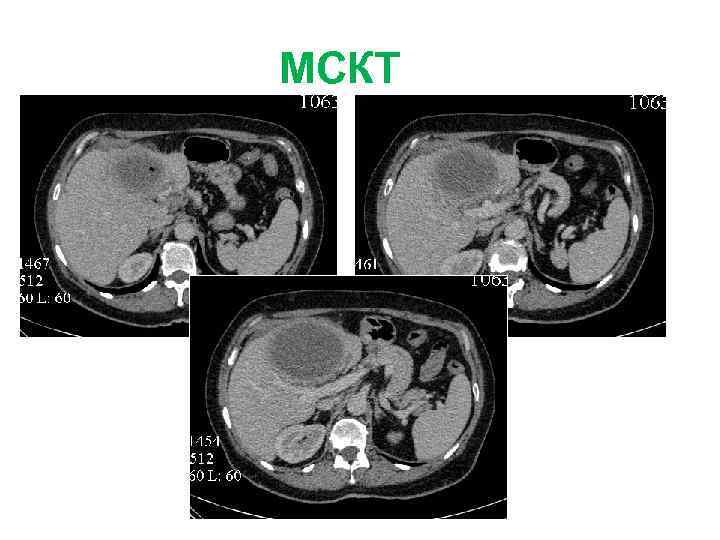 МСКТ
МСКТ
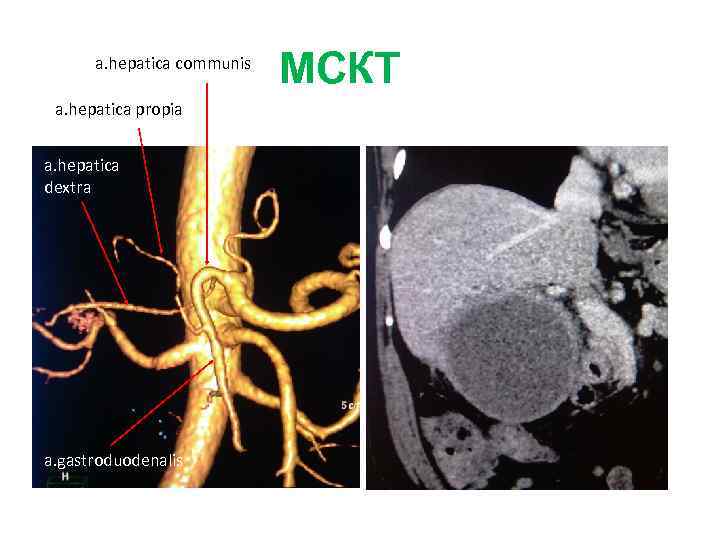 a. hepatica communis a. hepatica propia a. hepatica dextra a. gastroduodenalis МСКТ
a. hepatica communis a. hepatica propia a. hepatica dextra a. gastroduodenalis МСКТ
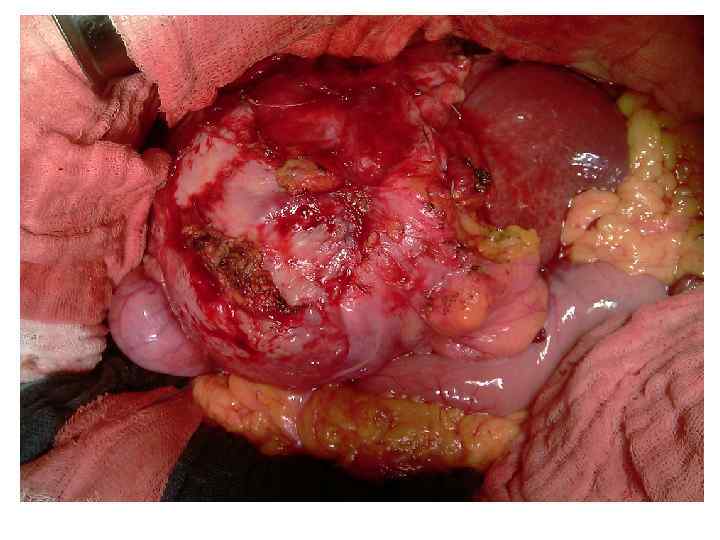
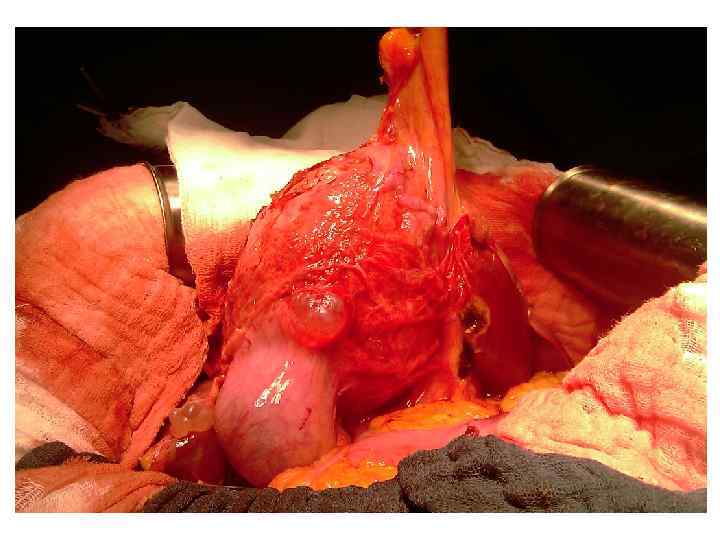
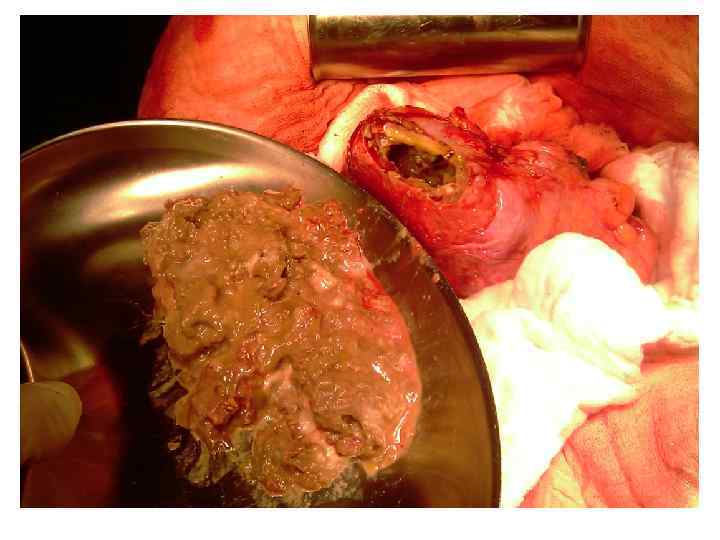
 Срочное гистологическое исследование: стенка кисты представлена фиброзной тканью, содержащей участки некрозов. Хроническая воспалительная инфильтрация. Клеточная выстилка отсутствует. Уровень онкомаркеров в содержимом кисты: СЕА – 27 ед/мл, СА 19 -9 - > 5 000 ед/мл Интраоперационный диагноз: киста 4 -го сегмента печени (цистаденома? цистаденокарцинома? нагноившаяся непаразитарная киста? ) Операция: левосторонняя гемигепатэктомия
Срочное гистологическое исследование: стенка кисты представлена фиброзной тканью, содержащей участки некрозов. Хроническая воспалительная инфильтрация. Клеточная выстилка отсутствует. Уровень онкомаркеров в содержимом кисты: СЕА – 27 ед/мл, СА 19 -9 - > 5 000 ед/мл Интраоперационный диагноз: киста 4 -го сегмента печени (цистаденома? цистаденокарцинома? нагноившаяся непаразитарная киста? ) Операция: левосторонняя гемигепатэктомия
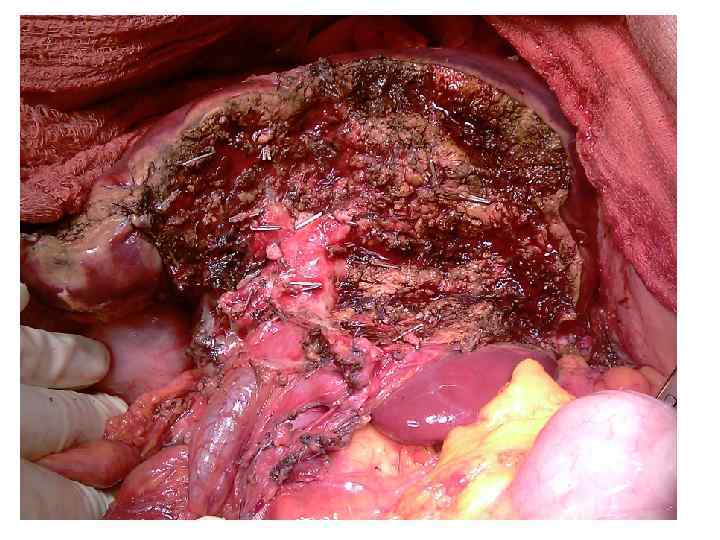
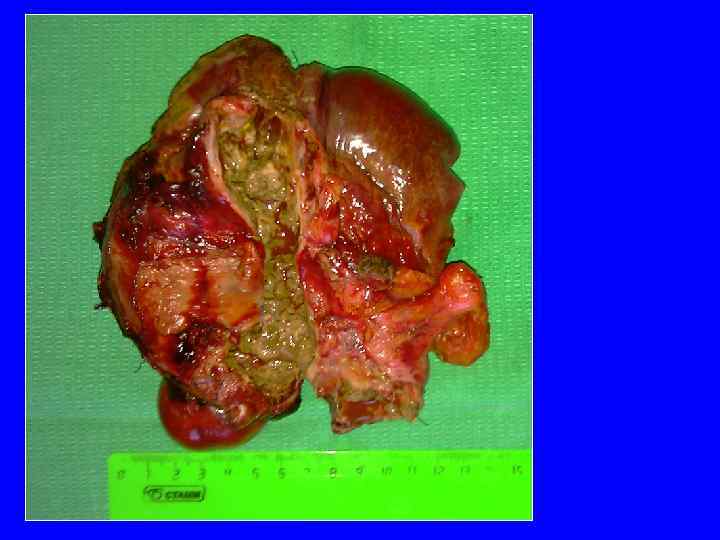
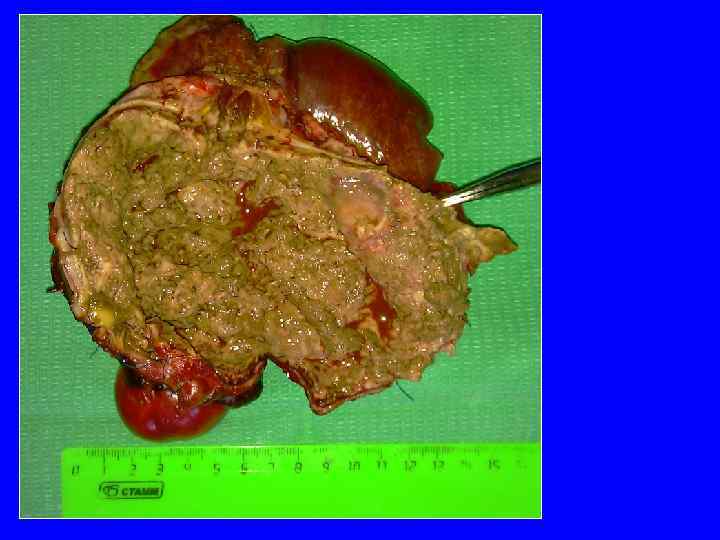
 Vol. 44, No. 5, October 2001
Vol. 44, No. 5, October 2001

 Hepatobiliary cystadenomas and cystadenocarcinomas: a report of 33 cases. Sang X, Sun Y, Mao Y, Yang Z, Lu X, Yang H, Xu H, Zhong S, Huang J. Source Department of Liver Surgery, Peking Union Medical College (PUMC) Hospital, Chinese Academy of Medical Sciences & PUMC, Beijing, China Department of Hepatobiliary Surgery, China-Japan Friendship Hospital, Beijing, China. Abstract Background: Hepatobiliary cystadenomas and cystadenocarcinomas are rare and often misdiagnosed. Aims: We report our experience with 33 cases over 20 years to discuss an algorithm for these diseases. Methods: Patients presenting with a diagnosis of hepatobiliary cystadenomas and cystadenocarcinomas were retrospectively reviewed from January 1991 to October 2010. Clinical data were collected by examining hospital records and by follow-up questionnaire interviews. Results: Thirty-three patients had pathologically diagnosed hepatobiliary cystadenomas (19/33, 17 females and two males) or cystadenocarcinomas (14/33, five females and nine males). Symptoms of cystadenomas at hospitalization were abdominal bloating or pain (9/19). Nine patients had an elevated level of carbohydrate antigen (CA) 19 -9. The surgical procedures, i. e. cyst enucleation, segmentectomy, sectionectomy and hemihepatectomy, were performed with satisfactory outcomes. Symptoms of cystadenocarcinomas included abdominal bloating or pain (8/14) and fever (3/14). Seven patients had elevated CA 19 -9. The imaging characteristics of cystadenocarcinomas were similar to those of cystadenomas. The clinical outcomes for cystadenocarcinomas were mostly poor after either surgical or conservative treatment. Conclusions: Clinical symptoms are unreliable for these diagnoses and their differential diagnosis. Imaging evaluations and CA 19 -9 are of value for the recognition of cystadenoma and cystadenocarcinoma, but not for their differential diagnosis. Any recurrence of liver cyst after surgery or other treatments should lead one to suspect one of these diseases. Invasive examination and percutaneous fine-needle aspiration cytology are not recommended. Complete excision or careful enucleation should be the first treatment choice for a better prognosis. © 2011 John Wiley & Sons A/S.
Hepatobiliary cystadenomas and cystadenocarcinomas: a report of 33 cases. Sang X, Sun Y, Mao Y, Yang Z, Lu X, Yang H, Xu H, Zhong S, Huang J. Source Department of Liver Surgery, Peking Union Medical College (PUMC) Hospital, Chinese Academy of Medical Sciences & PUMC, Beijing, China Department of Hepatobiliary Surgery, China-Japan Friendship Hospital, Beijing, China. Abstract Background: Hepatobiliary cystadenomas and cystadenocarcinomas are rare and often misdiagnosed. Aims: We report our experience with 33 cases over 20 years to discuss an algorithm for these diseases. Methods: Patients presenting with a diagnosis of hepatobiliary cystadenomas and cystadenocarcinomas were retrospectively reviewed from January 1991 to October 2010. Clinical data were collected by examining hospital records and by follow-up questionnaire interviews. Results: Thirty-three patients had pathologically diagnosed hepatobiliary cystadenomas (19/33, 17 females and two males) or cystadenocarcinomas (14/33, five females and nine males). Symptoms of cystadenomas at hospitalization were abdominal bloating or pain (9/19). Nine patients had an elevated level of carbohydrate antigen (CA) 19 -9. The surgical procedures, i. e. cyst enucleation, segmentectomy, sectionectomy and hemihepatectomy, were performed with satisfactory outcomes. Symptoms of cystadenocarcinomas included abdominal bloating or pain (8/14) and fever (3/14). Seven patients had elevated CA 19 -9. The imaging characteristics of cystadenocarcinomas were similar to those of cystadenomas. The clinical outcomes for cystadenocarcinomas were mostly poor after either surgical or conservative treatment. Conclusions: Clinical symptoms are unreliable for these diagnoses and their differential diagnosis. Imaging evaluations and CA 19 -9 are of value for the recognition of cystadenoma and cystadenocarcinoma, but not for their differential diagnosis. Any recurrence of liver cyst after surgery or other treatments should lead one to suspect one of these diseases. Invasive examination and percutaneous fine-needle aspiration cytology are not recommended. Complete excision or careful enucleation should be the first treatment choice for a better prognosis. © 2011 John Wiley & Sons A/S.
 Цистаденому печени необходимо предполагать при наличии следующих составляющих: 1) наличие перегородок в кисте 2) наличие кровотока в стенках и перегородках кисты по данным УЗИ и КТ 3) высокий уровень в содержимом онкомаркеров СЕА и СА 19 -9 4) женский пол; 5) крупная солитарная киста; 6) поражение 4 -го сегмента
Цистаденому печени необходимо предполагать при наличии следующих составляющих: 1) наличие перегородок в кисте 2) наличие кровотока в стенках и перегородках кисты по данным УЗИ и КТ 3) высокий уровень в содержимом онкомаркеров СЕА и СА 19 -9 4) женский пол; 5) крупная солитарная киста; 6) поражение 4 -го сегмента
 МСКТ пациентов с цистаденомами печени из различных публикаций
МСКТ пациентов с цистаденомами печени из различных публикаций
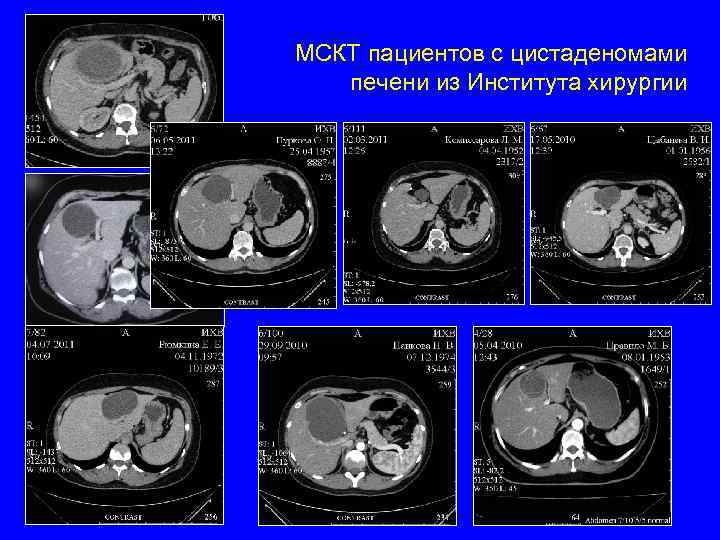 МСКТ пациентов с цистаденомами печени из Института хирургии
МСКТ пациентов с цистаденомами печени из Института хирургии
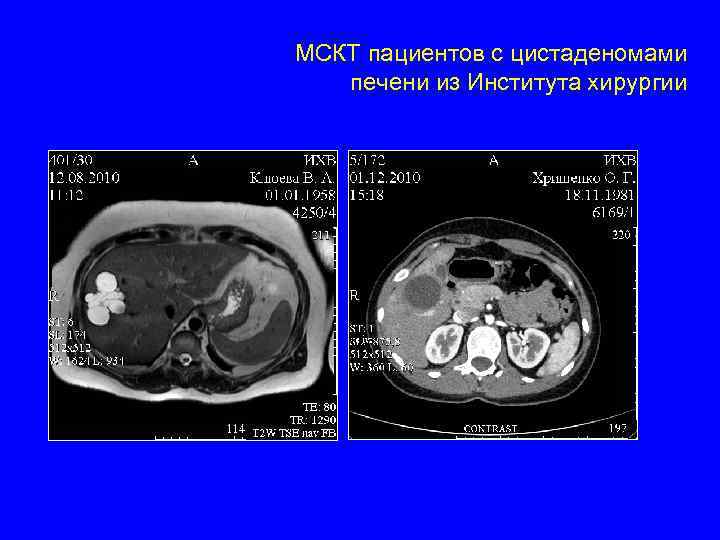 МСКТ пациентов с цистаденомами печени из Института хирургии
МСКТ пациентов с цистаденомами печени из Института хирургии
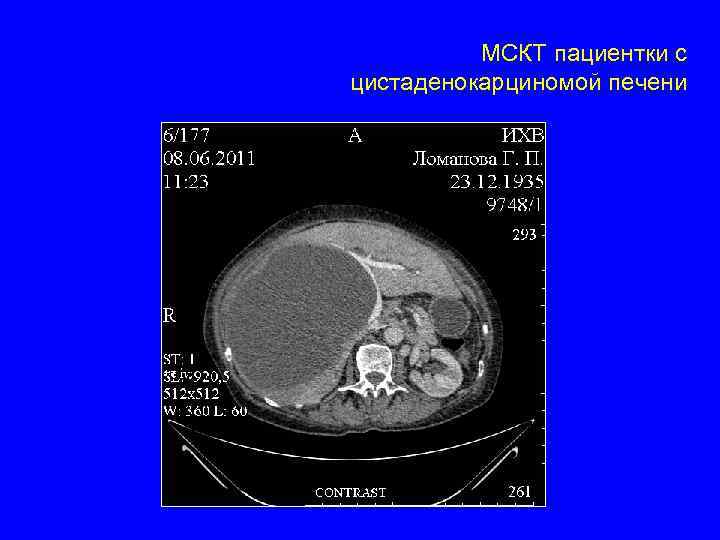 МСКТ пациентки с цистаденокарциномой печени
МСКТ пациентки с цистаденокарциномой печени


