Опухоли ЦНС. Внутричерепные образования. СПб МАПО


Опухоли ЦНС. Внутричерепные образования. СПб МАПО 2013 г.

Эпидемиология. n В мире ежегодно регистрируется от 2, 5 до 16, 5 случаев опухолей ЦНС на 100000 населения, что составляет 1, 8 - 2, 3% от общего количества онкологических больных. n В США в 2008 году выявлено 21810 новых случаев опухолей ЦНС– 1, 3% от общего числа онкологических больных n 13070 смертей от опухолей ЦНС – 2, 3% онкологической смертности n В России в 2009 году выявлено 6969 первичных случаев опухолей ЦНС, в С-Петербурге и Лен. области 387; смертность за тот же период 6558 и 385 случаев, соответственно.

Эпидемиология. Первый пик заболеваемости приходится на возраст от 0 -4 лет. С возрастом частота возникновения глиом увеличивается приблизительно на 1, 2% в год Второй пик заболеваемости - старше 60 лет, достигая 70 случаев на 100 тыс. после 70 лет.

Частота встречаемости: менингиомы 30 -35%; глиобластомы – 20%; анапластические глиомы – 10%; высокодифференцированные глиомы 10%; невриномы 10%; аденомы -10%; лимфомы 5%. Распределение опухолей по локализации: лобные доли -18, 6%, височные – 12, 8% теменные 8, 6%, затылочные – 2% сочетание – 28, 4% ствол -5, 6% мозжечок – 4, 3% другие структуры – 20%

Этиология. n 1 группа – генетически обусловленные факторы (5%): мутация ТР 53 –присутствует в 60% опухолей глиальной природы; нейрофиброматоз 1 тип, мутация 17 хромосомы (глиальные н/о, астроцитомы оптических путей); нейрофиброматоз 2 тип, делеция 22 хромосомы (менингиомы, шванномы корешков нервов, в том числе акустические); с-м Тюрко (медуллобластомы); синдром Ли-Фраумени (глиомы), делеция 1 p/19 q хромосом – (олигодендроглиомы) n 2 группа – связанные с внешним воздействием: электромагнитные поля, сельскохозяйственные удобрения (пестициды), нефтепродукты, соли тяжелых металлов (свинец), лучевая терапия в детском возрасте, иммунодефицитные состояния

Клинические проявления 1 группа – общемозговые: - гипертензионно-гидроцефальный с-м (эффект «массы» , нарушение гемо и ликвородинамики, раздражение оболочек головного мозга) 2 группа – очаговая неврологическая симптоматика

По частоте встречаемости симптомов: головная боль (утренняя) -33, 4%, сочетается с тошнотой, рвотой. судорожные приступы – 19, 4% (при ГНЗ первый признак более чем у 50% - поэтому больных эпилепсией, впервые проявившейся после 35 -летнего возраста, необходимо обследовать на наличие опухоли мозга) парезы -5, 2% нарушение когнитивных функций -3 -30%

Диагностика n 1. Сбор жалоб и анамнеза. n 2. Физический осмотр (оценка). n 3. Неврологический осмотр +ментальный статус. n 4. Осмотр окулиста. n 5. Компьютерная томография с контрастным усилением. n 6. МРТ+ МРТ спектрография. n 7. Сцинтиграфия головного мозга (технеций 99 ДТПА). n 8. ПЭТ (бутират натрия, меченная глюкоза, метионин). n 9. Церебральная ангиография.

Диагностика n 10. Люмбальная пункция. n 11. Стереотаксическая биопсия (при невозможности выполнения операции или при подозрении на лимфому ЦНС) n 12. Гистологическая верификация опухоли +ИГХ (Ki-67(8%), гиперэкспрессия VEGFR, антиапоптического белка bcl-2)+ генетический анализ ( точечная мутация p 53 и связанная с ней суперэкспрессия белка MDM-2 (активация ангиогенеза), аномалии 17, 19 и 22 хромосом.
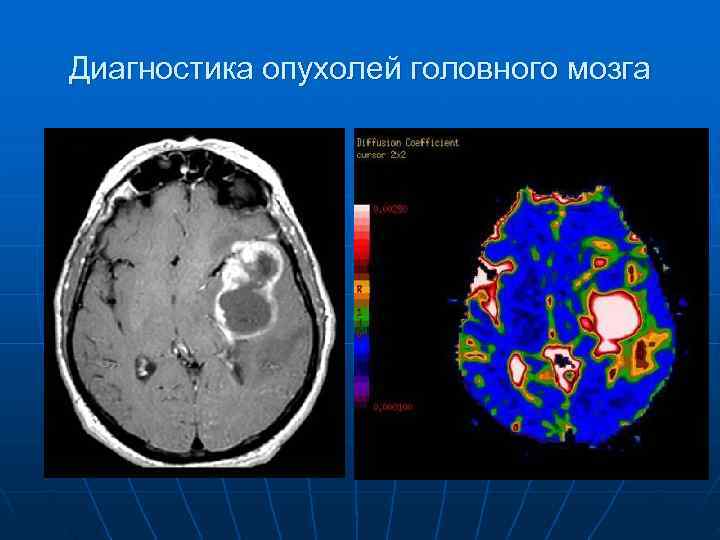
Диагностика опухолей головного мозга

Признаки злокачественности, лежащие в основе классификации: клеточный и ядерный полиморфизм, пролиферация эндотелия сосудов опухоли, наличие в опухоли митозов и некрозов. Gr. I- доброкачественное образование Gr. II- имеет место умеренная атипия клеток опухоли Gr. III- атипия + митотическая активность Gr. IV- выраженная атипия, большое количество митозов и некрозов в опухоли, пролиферация эндотелия сосудов.
Классификация опухолей ЦНС (ВОЗ 2000 г)

Основная цель лучевой терапии – создание высокой и гомогенной дозы в облучаемом объеме и максимальное щажение окружающей опухоль нормальной ткани головного мозга.

Выбор объемов облучения при лечении опухолей ЦНС n А-Объем опухоли n В – А+ субклиническое распространение опухоли n С –В + окружающие ткани с поправкой на вариации в размере и форме n Д – поля облучения + отступ с учетом технических особенностей аппарата

Определяющие факторы для проведения лучевой терапии: толерантность нормальных тканей, возраст пациента, его соматический статус, (индекс Карновского более 50 -60 или градация по ВОЗ 1 -2), гистологический тип опухоли, ее локализация.

Опухоли центральной нервной системы: n I группа первичные – 1) высокодифференцированные или низкозлокачественные (Gr. I-II); 2) низкодифференцированные или высокозлокачественные (Gr. III-IV), отдельная группа – с потенцией к метастазированию по ликворным путям; II группа вторичные (метастатические).
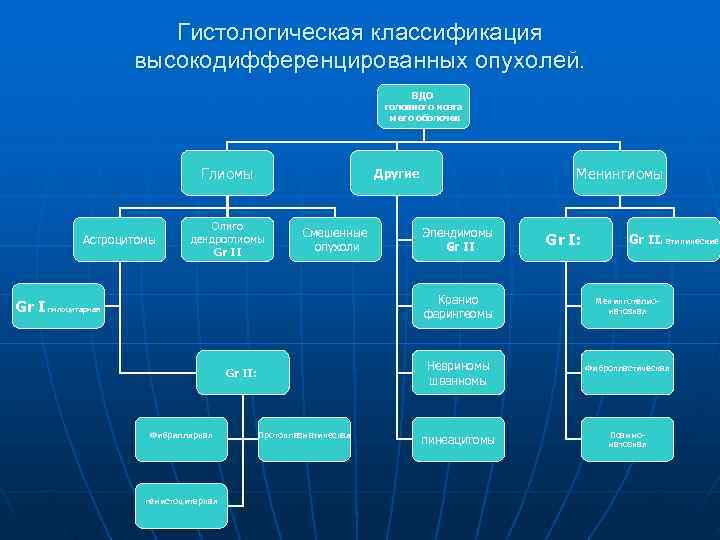
Гистологическая классификация высокодифференцированных опухолей. ВДО головного мозга и его оболочек Глиомы Другие Менингиомы Олиго Смешенные Эпендимомы Астроцитомы дендроглиомы опухоли Gr II Gr I: Gr II: атипические Gr II Кранио Менинготелио- Gr I пилоцитарная фарингеомы матозная Невриномы Фибропластическая Gr II: шванномы Фибриллярная Протоплазматическая Псаммо- пинеацитомы матозная гемистоцитарная

Эпидемиология. АНЗ 1, 5 на 100000 Наибольшая частота возникновения высокодифференцированных глиом головного мозга приходится на период с 20 до 40 лет, т. е. на возраст максимальной социальной и профессиональной активности человека. Менингиомы 2, 8 на 100000 Менингиомы Gr. I-II встречаются во все возрастные периоды, достигая максимума после 60 лет.
Методы диагностики n МРТ, КТ, ПЭТ способствуют более раннему выявлению новообразований головного мозга, когда у больного имеет место минимальная неврологическая симптоматика.
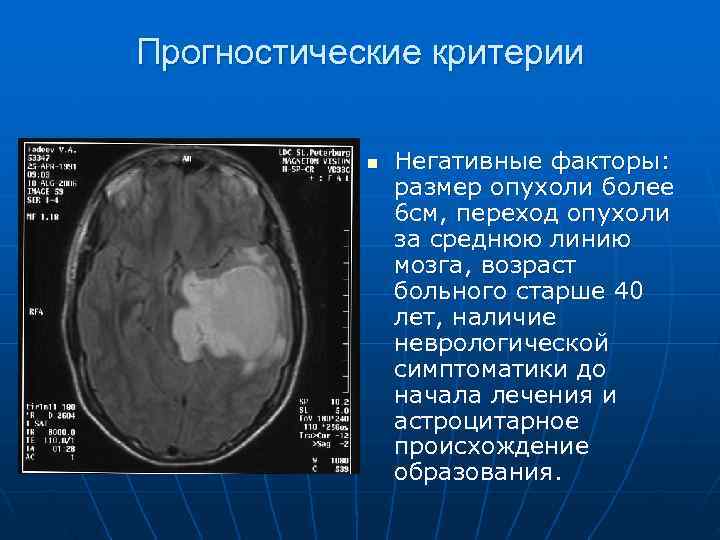
Прогностические критерии n Негативные факторы: размер опухоли более 6 см, переход опухоли за среднюю линию мозга, возраст больного старше 40 лет, наличие неврологической симптоматики до начала лечения и астроцитарное происхождение образования.
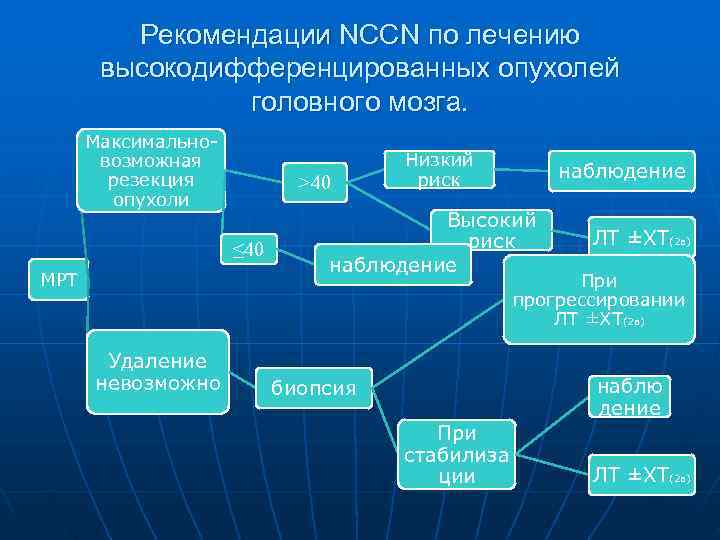
Рекомендации NCCN по лечению высокодифференцированных опухолей головного мозга. Максимально- возможная Низкий резекция риск наблюдение >40 опухоли Высокий риск ЛТ ±ХТ(2 в) ≤ 40 наблюдение МРТ При прогрессировании ЛТ ±ХТ(2 в) Удаление невозможно биопсия наблю дение При стабилиза ции ЛТ ±ХТ(2 в)

Основные принципы лечения первичных опухолей ЦНС Gr I-II n 1. При тотальном удалении опухоли Gr I– только наблюдение n 2. В случае проведения курса лучевой терапии необходимо использование щадящих методик лучевой терапии (многопольная статика, подвижное облучение). n 3. Ограничение объема облучения (опухоль + 1 -2 см от края). n 4. Оптимизация дозного распределения (посредством конформной лучевой терапии с использованием мегавольтных источников, оснащенных многолепестковыми коллиматорами. n 5. Применение стереотаксического наведения пучка излучения. n 6. Использование радиохирургических подходов. n 7. Высокий уровень подготовки к облучению, надежная фиксация. n 8. Стандартный режим фракционирования дозы 1, 8 - 2, 0 Гр, до СОД=50 -56, 0 Гр
Локальное облучение головного мозга

Конформное облучение

Выбор дозы облучения в зависимости от объема облучения при радиохирургическом лечении в соответствии с рекомендациями ВОЗ n Менее 20 мм – 24 Гр n 21 -30 мм – 18 Гр n 31 -40 мм – 15 Гр n При локализации в стволе – 14 Гр
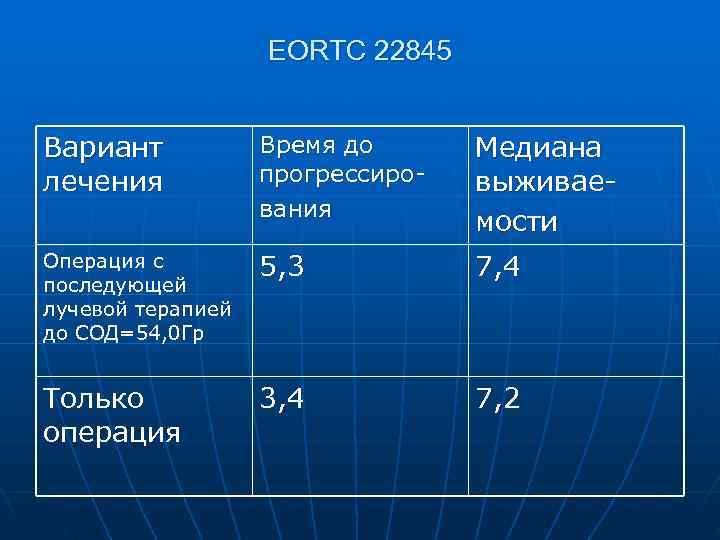
EORTC 22845 Вариант Время до Медиана лечения прогрессиро- выживае- вания мости Операция с 5, 3 7, 4 последующей лучевой терапией до СОД=54, 0 Гр Только 3, 4 7, 2 операция
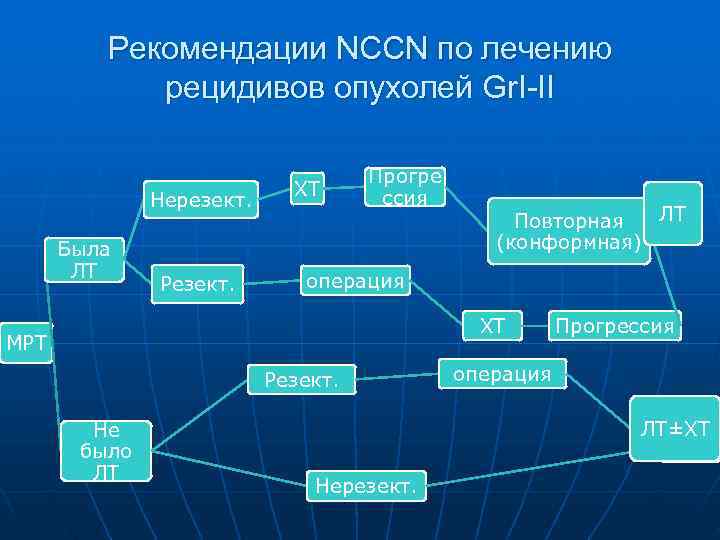
Рекомендации NCCN по лечению рецидивов опухолей Gr. I-II Прогре ХТ ссия Нерезект. Повторная ЛТ Была (конформная) ЛТ операция Резект. ХТ Прогрессия МРТ Резект. операция Не ЛТ±ХТ было ЛТ Нерезект.
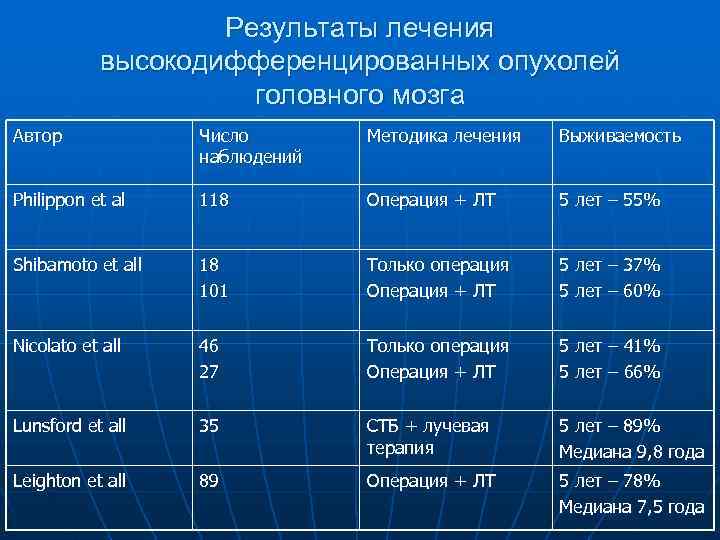
Результаты лечения высокодифференцированных опухолей головного мозга Автор Число Методика лечения Выживаемость наблюдений Philippon et al 118 Операция + ЛТ 5 лет – 55% Shibamoto et all 18 Только операция 5 лет – 37% 101 Операция + ЛТ 5 лет – 60% Nicolato et all 46 Только операция 5 лет – 41% 27 Операция + ЛТ 5 лет – 66% Lunsford et all 35 СТБ + лучевая 5 лет – 89% терапия Медиана 9, 8 года Leighton et all 89 Операция + ЛТ 5 лет – 78% Медиана 7, 5 года

Основные принципы лечения первичных опухолей ЦНС Gr III-IV n 1. Обязательно комбинированное лечение n 2. Увеличение объемов облучение (включение в объем облучения первичного опухолевого очага, зоны окружающего отека +2 -3 см окружающих нормальных тканей). n 3. Использование нестандартных режимов фракционирования (СОД эквивалентна 60 -66, 0 Гр обычного фракционирования). n 4. Дополнение локального воздействия одновременно или последовательно системным лечением. n 5. Использование современных методик лучевой терапии с одновременной или последовательной добавкой на опухолевый остаток (увеличение СОД).
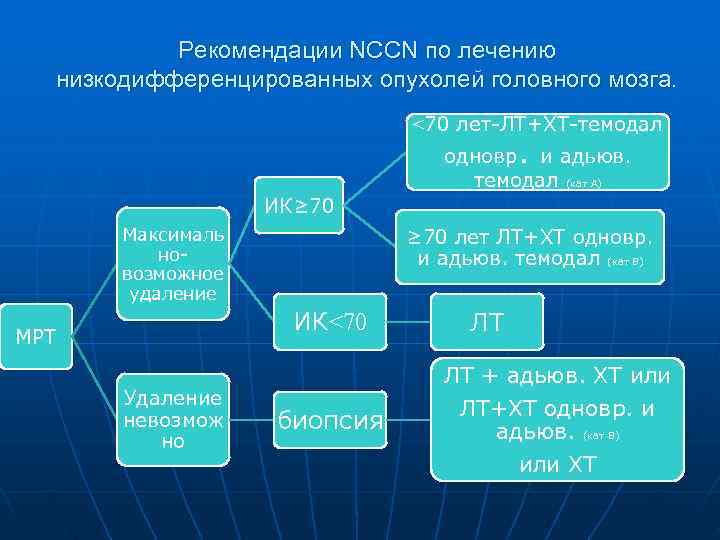
Рекомендации NCCN по лечению низкодифференцированных опухолей головного мозга. <70 лет-ЛТ+ХТ-темодал одновр. и адьюв. темодал (кат А) ИК≥ 70 Максималь ≥ 70 лет ЛТ+ХТ одновр. но- и адьюв. темодал (кат В) возможное удаление ИК<70 ЛТ МРТ ЛТ + адьюв. ХТ или Удаление ЛТ+ХТ одновр. и невозмож биопсия адьюв. (кат В) но или ХТ
Лучевая терапия глиобластом на ЛУЭ

Факторы, влияющие на прогноз выживаемости больных. n Гистологический вариант n Возраст (до 40 лет – 31, 9 мес; старше 40 лет – 20, 5 мес) n Соматическое состояние (более 80 – 60, 2 мес; 60 -70 – 30, 2 мес; менее 50 – 17, 3 мес) n Объем операции (тотальное удаление – 30, 2 мес; субтотальное – 24, 2 мес; частичное 12 мес) n Повторные операции (однократное – 18, 6 мес; повторные – 36, 5 мес) n Ментальный статус
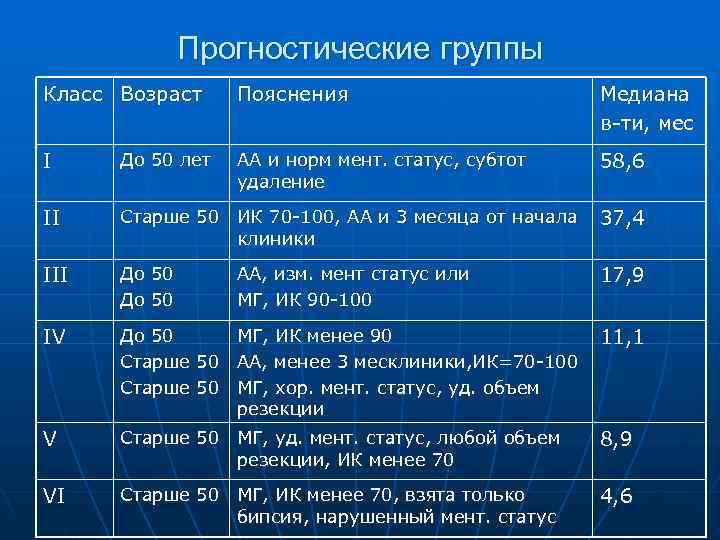
Прогностические группы Класс Возраст Пояснения Медиана в-ти, мес I До 50 лет АА и норм мент. статус, субтот 58, 6 удаление II Старше 50 ИК 70 -100, АА и 3 месяца от начала 37, 4 клиники III До 50 АА, изм. мент статус или 17, 9 До 50 МГ, ИК 90 -100 IV До 50 МГ, ИК менее 90 11, 1 Старше 50 АА, менее 3 месклиники, ИК=70 -100 Старше 50 МГ, хор. мент. статус, уд. объем резекции V Старше 50 МГ, уд. мент. статус, любой объем 8, 9 резекции, ИК менее 70 VI Старше 50 МГ, ИК менее 70, взята только 4, 6 бипсия, нарушенный мент. статус

Варианты химиотерапии, используемые при лечении первичных опухолей ЦНС n Обычная системная химиотерапия. n Местная химиотерапия- используются высокие дозы химиопрепаратов, которые в составе полимеров вводятся в ложе опухоли после хирургического вмешательства (препараты платины). n Регионарная (мюстофоран, кармустин) n Внутриартериальная химиотерапия n Интратекальная химиотерапия (метотрексат). n Высокодозная химиотерапия с последующей пересадкой костного мозга.

Спектр химиопрепаратов, используемых при лечении первичных опухолей ЦНС. n 1. Производные нитрозомочевины: ломустин, кармустин (39 - 50%), нимустин, фотемустин (22, 2% лечебных ответов, 44, 4% стабилизаций при рецидивах анапластических астроцитом, медиана выживаемости 40 недель, при рецидивах глиобластом 24 недели, одновременно с лучевой терапией 27% ответов и 44% стабилизаций) n 2. Имидазотетразины: темодал (11 -47% лечебных ответов, при рецидивах анапластической астроцитомы 11 -35%, глиобластомы – 21%, выживаемость 6 мес – более 60%, 12 месяцев – 24%) n 3. Винкалколоиды: винкристин. n 4. Иринотекан- ингибитор топоизомеразы ( в сочетании с кармустином в качестве 2 линии ХТ при рецидивах – 21% ответов; с темодалом 28% ответов и выживаемость 6 месяцев -39%) n 5. Липосомальный доксорубицин (келикс или доксил) n 6. При нарушении проницаемости гематоэнцефалического барьера: производные платины, циклофосфамид, доксорубицин и т. д. n Полихимиотерапия: PCV (CCNU, прокарбазин, винкристин)

Интенсивная методика химиоиммунолучевой терапии больных глиомами высокой степени злокачественности n Начало – октябрь 2002 года n Лучевая терапия: РОД= 3, 0 Гр до СОД=51, 0 Гр на ЛУЭ с Е=6 Мэ. В n ПХТ: при СОД=18, 0; 33, 0; 48, 0 Гр в/в введение 1, 0 мг винкристина; при СОД=21, 0; 36, 0; 51, 0 Гр 80 мг ломустина р. о. n Иммунотерапия: после завершения облучения на фоне одновременной ПХТ курс ронколейкина 1 -3 млн в/в до общей дозы 10 - 20 млн МЕ n Далее еще 3 цикла химиоиммунотерапии с двухнедельными перерывами n Результаты: выживаемость 12 месяцев – 34%; средняя продолжительность жизни 14 месяцев.
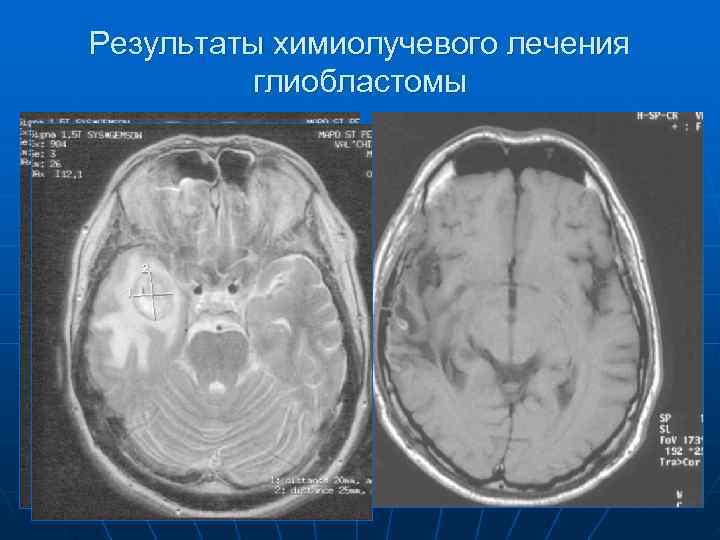
Результаты химиолучевого лечения глиобластомы

Современные методы лечения n 1. Антиангиогенная терапия n 2. Генная терапия n 3. Иммунотерапия n 4. Фотодинамическая терапия n 5. Интрастициальная брахитерапия n 6. Таргентная терапия (гефитиниб, бевацизумаб).
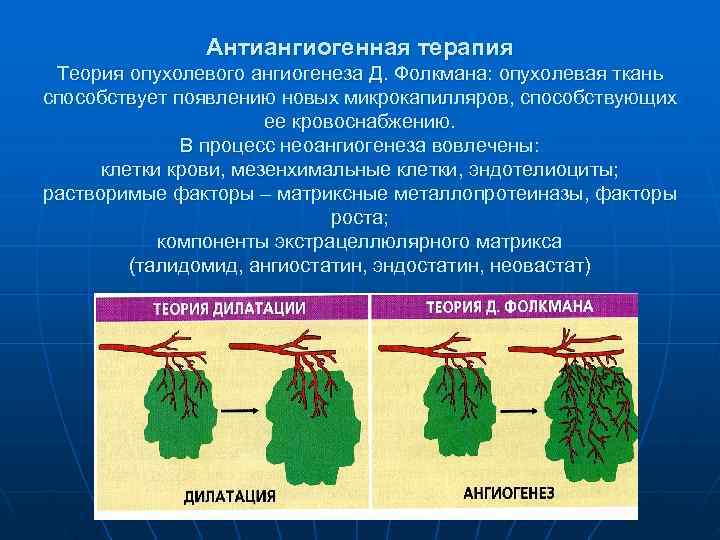
Антиангиогенная терапия Теория опухолевого ангиогенеза Д. Фолкмана: опухолевая ткань способствует появлению новых микрокапилляров, способствующих ее кровоснабжению. В процесс неоангиогенеза вовлечены: клетки крови, мезенхимальные клетки, эндотелиоциты; растворимые факторы – матриксные металлопротеиназы, факторы роста; компоненты экстрацеллюлярного матрикса (талидомид, ангиостатин, эндостатин, неовастат)

Генная терапия (введение с помощью векторов-ретровирусов в опухолевые клетки конструкции ДНК, кодирующей ген- супрессор опухолевого роста р53, ответственный за синтез нормального белка р53, что приводит к гибели клетки посредством апоптоза).

Вакцинотерапия ГНЗ n 1. Создание противоопухолевых вакцин и цитокинотерапия (интерферон-альфа, интерлейкин-2) n 2. Методика разработана РНХИ им. А. Л. Поленова совместно с ПИЯФ. n Во время операции забирают 1 см 3 опухолевой ткани из которой в последующим готовят экстракт белков, используемый в качестве антигена для представления дендритным клеткам n Из крови больного (60 мл) выделяют моноциты и культивируют с ростовыми факторами, затем соединяют с белковым экстрактом и вводят больному с помощью электропорации n Кроме того из крови больного выделяют мононуклеарные лейкоциты, активируют их и вводят подкожно с целью стимуляции Т-клеточного звена иммунитета n Результаты: средняя продолжительность жизни больных с рецидивными глиобластмами составила 10, 2 месяца

ФДТ n В основе ФДТ лежит взаимодействие фотосенсибилизатора, который избирательно накапливается опухолью с определенной длинной световой волны, что приводит к деструкции опухолевых клеток n РНХИ им. А. Л. Поленова совместно с институтом онкологии им. Н. Н. Петрова начали совместную работу по использованию сенсибилизатора – фотодиазин. Препарат вводится пациенту в/в непосредственно перед операцией. Его максимальная концентрация в опухоли создается через 3 -4 часа + эффект флюорисценции.

Интрастициальная брахитерапия: непосредственно во время операции, после удаления основного опухолевого объема, в образовавшуюся полость вводят интростат с Ir 192 Результаты: выживаемость 12 месяцев при анапластических астроцитомах составила 66%, глиобластомах 60%; средняя продолжительность жизни 11, 5 месяца

Использование радиохирургии при облучении ГНЗ n Boost – методика представляет собой дополнительное локальное облучение опухолевого остатка n Объем облучения 14 -22, 5 см 3, средняя РОД=12, 5 Гр n Результаты: 24 месяца – 35, 9%, средняя продолжительность жизни – 19, 9 мес.
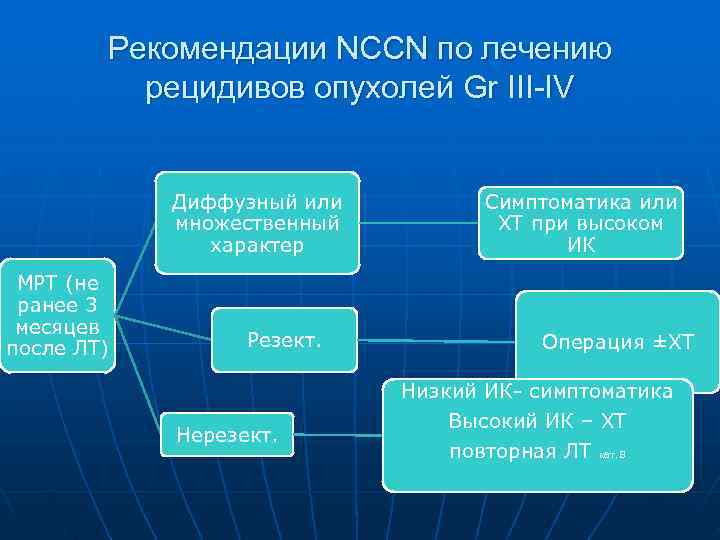
Рекомендации NCCN по лечению рецидивов опухолей Gr III-IV Диффузный или Симптоматика или множественный ХТ при высоком характер ИК МРТ (не ранее 3 месяцев после ЛТ) Резект. Операция ±ХТ Низкий ИК- симптоматика Высокий ИК – ХТ Нерезект. повторная ЛТ кат. В

Основные принципы лечения первичных опухолей ЦНС с потенцией к метастазированию по ликворным путям n Обязательно комбинированное лечение n Тотальное краниальное или краниоспинальное облучение (СОД на весь объем головного и спинного мозга = 30 -36 ГР и далее локально на клинически определяемые опухолевые очаги 20 -24 Гр) n Дополнение лучевой терапии системным воздействием
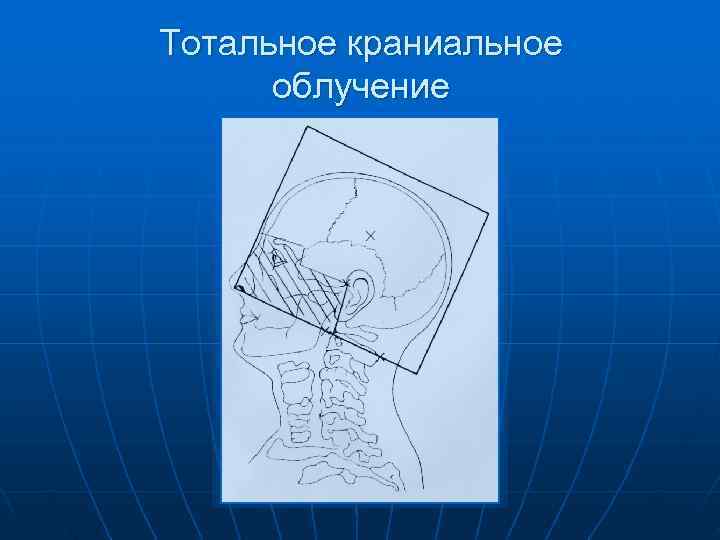
Тотальное краниальное облучение
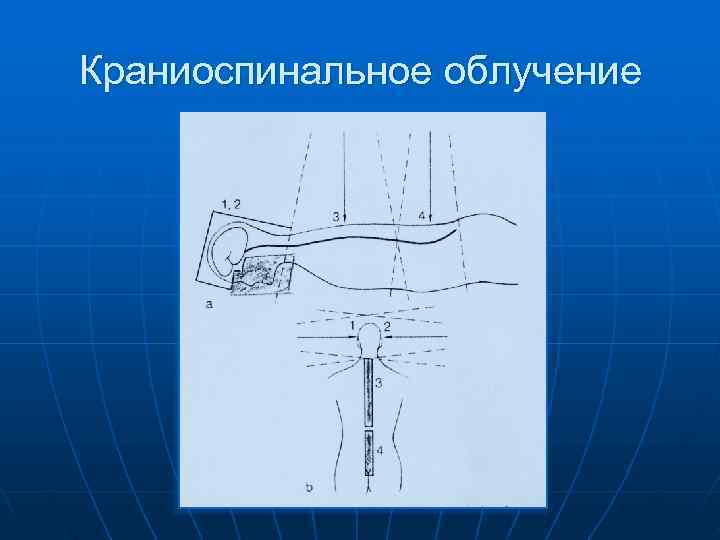
Краниоспинальное облучение

Облучение всего объема головного мозга
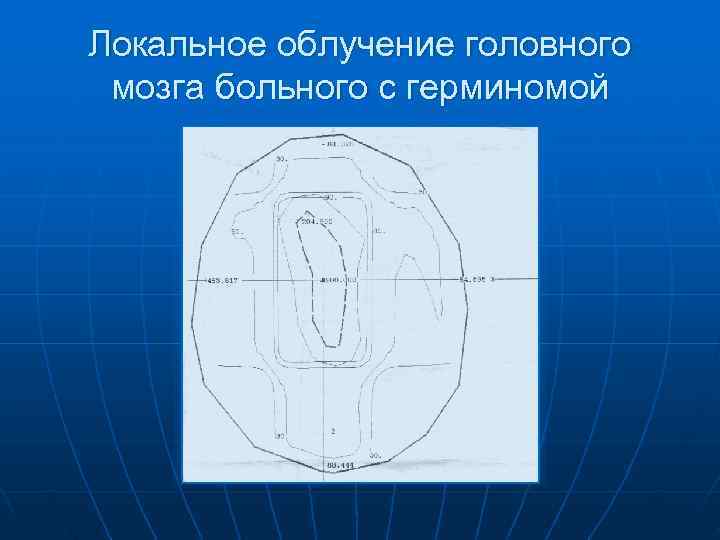
Локальное облучение головного мозга больного с герминомой
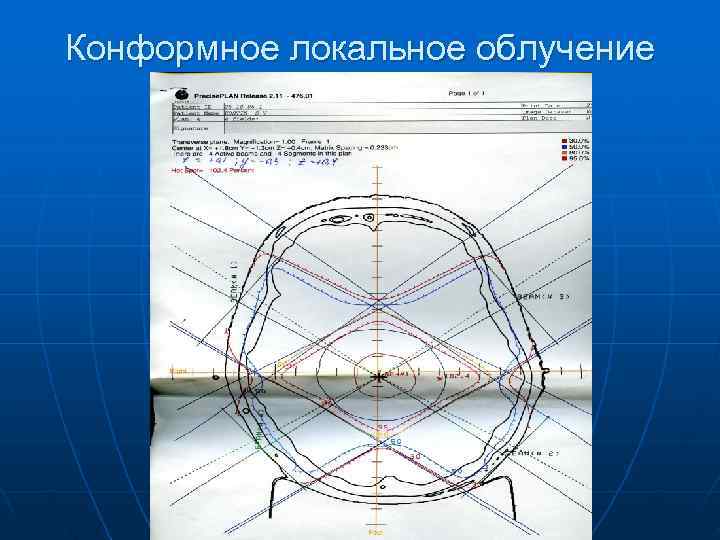
Конформное локальное облучение
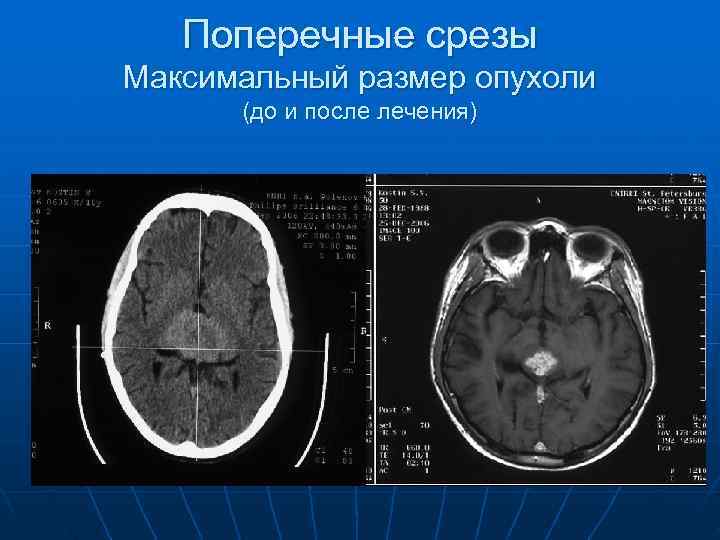
Поперечные срезы Максимальный размер опухоли (до и после лечения)
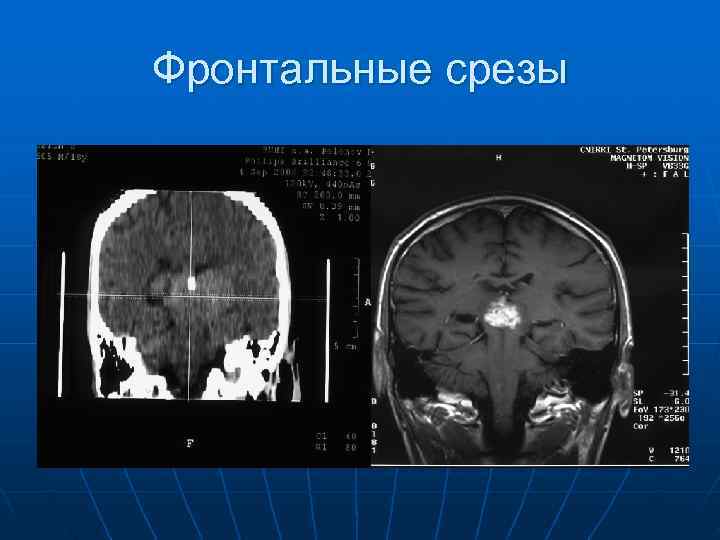
Фронтальные срезы
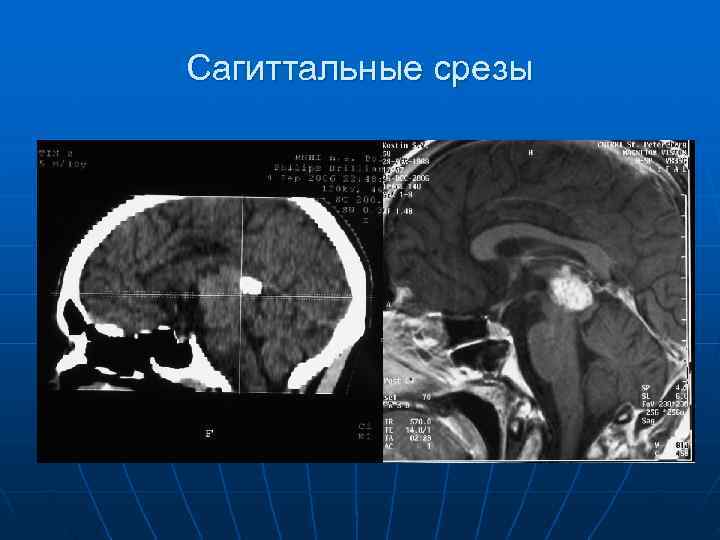
Сагиттальные срезы
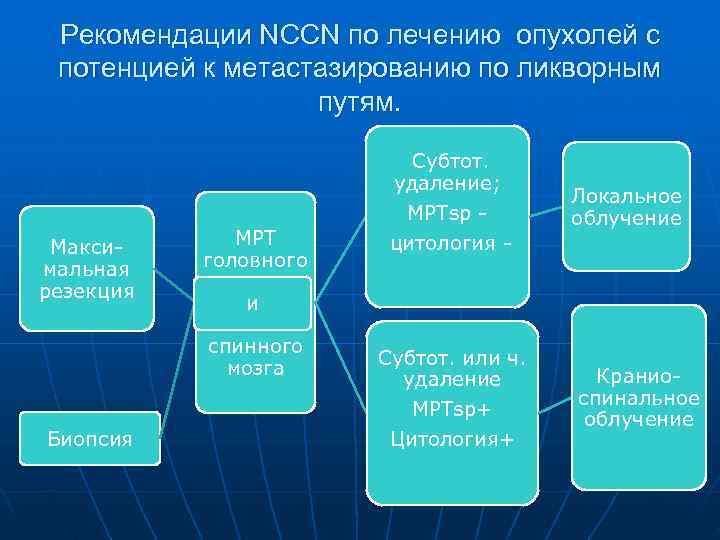
Рекомендации NCCN по лечению опухолей с потенцией к метастазированию по ликворным путям. Субтот. удаление; Локальное МРТsp - облучение Макси- МРТ цитология - мальная головного резекция и спинного мозга Субтот. или ч. удаление Кранио- спинальное МРТsp+ облучение Биопсия Цитология+

Лечение первичной лимфомы ЦНС n Лимфома ЦНС характеризуется быстрым ростом и плохим прогнозом для жизни (медиана выживаемости 4 месяца) n Оперативное вмешательство не показано (биопсия) n Облучение всего объема головного мозга, РОД=2, 0 Гр до СОД=36 -40 Гр позволяет увеличить выживаемость до 18 месяцев. Возможна локальная добавка на опухолевый остаток (10 - 20 Гр). n Обязательно проведение ПХТ
Конформное облучение всего объема головного мозга.

Тактика лечения больных с метастатическим поражением головного мозга n При наличии одиночных метастазов – комбинированное лечение: операция с последующей лучевой терапией и химиотерапией n При множественном характере поражения: облучение всего объема головного мозга, с последующим решением о локальной добавке на отдельные крупные очаги и химиотерапией

Тотальное облучение головного мозга у больных с множественными метастазами

Опухоли спинного мозга Интрамедуллярные (5%): астроцитомы (75%), эпендимомы (пояснично- крестцовый отдел) и др. Интрадуральные (под твердой мозговой оболочкой, 40%): менингиомы (80% локализуются в грудном отделе), нейрофибромы, невриномы, шванномы и др Экстрадуральные (в телах позвонков, 55%): метастатической природы

Лучевые реакции при облучении опухолей ЦНС n Острые – связаны с отеком ткани головного мозга (5 степеней градации)-до 100 дней. Реакции имеют преходящий характер и могут быть купированы с помощью препаратов симптоматической терапии (глюкокортикоиды, мочегонные средства). n Со стороны спинного мозга характеризуются синдромом Лермита. n Поздние – необратимы; полная оценка при сроках наблюдения до 10 лет.

Поздние осложнения. n Степень выраженности лучевых повреждений варьирует от умеренных нейрокогнитивных расстройств (ухудшение внимания, снижение уровня оперативной памяти и способности к обучению, особенно у молодых пациентов) до развития деменции, летаргии и локальных постлучевых некрозов ткани мозга (до 15%), требующих оперативного лечения и приводящих к глубокой инвалидизации больного. n Со стороны спинного мозга – два пика частоты: 13 месяцев – прямая демиелинизация, 29 месяцев преобладание сосудистого компонента)

Поздние осложнения. n Гистопатологические изменения при поздних лучевых осложнениях включают в себя: сосудистые реакции (телеангиоэктазии, расширение капилляров, гиалинизацию стенок сосудов и утолщение их за счет отложения фибрина); атрофию глии, демиелинизацию нервых волокон и формирование очагов некроза в ткани мозга. Большинство современных исследователей считает ключевым моментом в развитии лучевых повреждений гибель клеток эндотелия, что приводит, как к острому, так и хроническому нарушению проницаемости гематоэнцефалического барьера. Далее возникает отек ткани, запускается каскад иммунных реакций по типу нейровоспаления, что приводит к ишемии и, соответственно, гипоксии нервных клеток с последующей их гибелью.

Профилактика возникновения лучевых осложнений включает в себя: n Оптимизацию дозиметрического планирования лучевой терапии n Оптимизацию дозно-временных соотношений n Контроль качества лучевой терапии n Контроль радиологического оборудования

Выживаемость больных с опухолями ЦНС n Олигодендроглиомы высокодифференцированные ( медиана - 120 месяцев) > олигоастроцитомы > астроцитомы высокодифференцированные (медиана 60 -80 месяцев) > олигодендроглиомы анапластические (медиана 60 месяцев) > астроцитомы анапластические ( медиана 40 месяцев) > глиобластомы ( медиана 12 месяцев). Менингиомы (5 лет): высокодифференцированные > 85%; анапластические 50 -60%. Герминомы (5 лет) 80%, но при наличии отсевов в спиномозговой канал – 10 -20%. Медуллоблластомы (5 лет): низкий риск 85%; высокий риск 50%.

Особенности течения и тактики лечения опухолей ЦНС у детей n Наиболее часто встречающимися опухолями ЦНС у детей являются астроцитомы(35%) и медуллобластомы(20%) n Опухоли ЦНС у детей склонны к кистообразованию, часто встречаются отложения извести в ткани опухоли, редки кровоизлияния и некрозы n Не всегда имеет место соответствие гистотипа и биологического «поведения» опухоли n Сравнительно малый объем черепа и тесное расположение жизненно-важных структур приводят к быстрому развитию тяжелой клинической картины n Проведение лучевой терапии до завершения миелинизации нервных волокон может привести к недоразвитию и дисфункции нервной системы n При проведении лучевой терапии у детей необходима коррекция РОД и СОД

Классификация аденом гипофиза. (В. М. Дильман) n Аденомы составляют 18% от всех новообразований головного мозга n Из аденогипофиза развиваются аденомы, и крайне редко – рак; из нейрогипофиза _ глиомы, гранулезоклеточная опухоль. n 1. Эозинофильные аденомы (СТГ-продуцирующие). n 2. Пролактинома n 3. Базофильные аденомы (АКТГ-продуцирующие) n 4. Тиреотропиномы. n 5. Гормональнонеактивные (40%), хромофобные аденомы.

По характеру роста аденомы делятся n Эндоселлярные (внутри турецкого седла). n Эндосупраселлярные (выходит вверх за пределы турецкого седла). n Эндоинфраселлярные (опухоль выходит вниз из турецкого седла). n Эндолатероселлярные (опухоль разрушает боковую стенку турецкого седла и прорастает в кавернозный синус). n Очень часто направление роста аденомы гипофиза бывает различным – вверх, в сторону, вниз и т. д. , и тогда опухоль называют эндо-супра-инфра-латероселлярной. n Микроаденомы – до 1, 0 см, макроаденомы – более 1, 0 см

Диагностика аденом гипофиза 1. Осмотр нейрохирурга, эндокринолога. 2. Рентгенография черепа. 3. Гормональное исследование крови. 4. Компьютерная томография головного мозга. 5. Магнитно-резонансная томография.

Тактика лечения при аденомах, расположенных в пределах турецкого седла n Нейрохирургическое удаление n Лучевая терапия (узким пучком фотонов, протонная терапия РОД=60 -80 Гр, гамма-нож) n Медикаментозная терапия (агонисты дофамина, аналоги соматостатина и т. д. )

Зал проведения протонной стереотаксической терапии
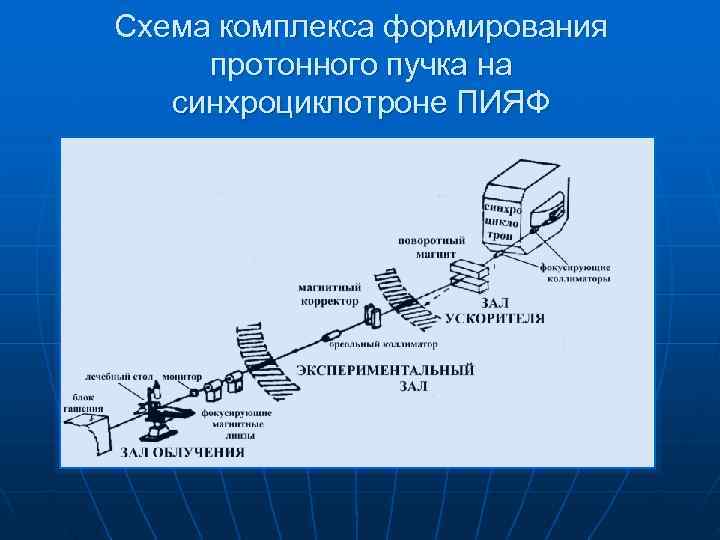
Схема комплекса формирования протонного пучка на синхроциклотроне ПИЯФ
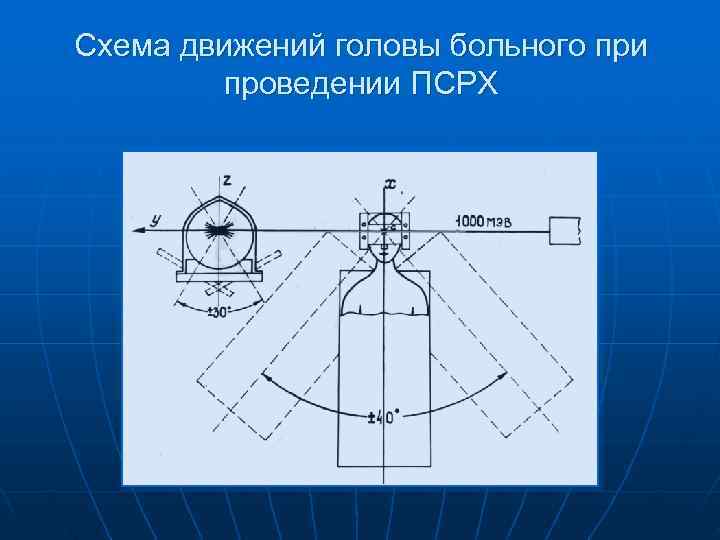
Схема движений головы больного при проведении ПСРХ

Основные технические параметры метода ПСРХ

Тактика лечения больных с аденомами гипофиза при выходе за пределы турецкого седла 1 этапом выполняется оперативное вмешательство, 2 этапом послеоперационный курс лучевой терапии с использованием мегавольтных источников излучения, в стандартном режиме фракционирования до СОД=50 - 56, 0 Гр

Локальное облучение головного мозга больной с аденомой гипофиза

Сосудистые пороки развития головного мозга n Артериовенозные мальформации (частота встречаемости АВМ составляет 19 на 100000 населения) n Кавернозные ангиомы n Капиллярные телеангиоэктазии n Венозные пороки развития
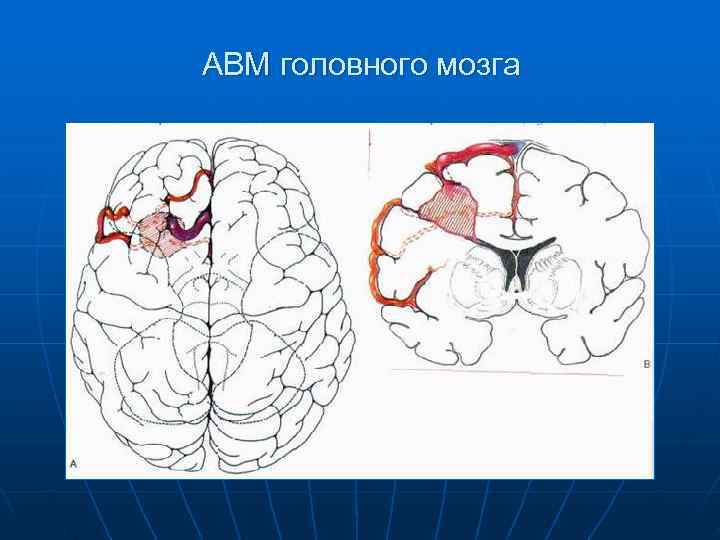
АВМ головного мозга

Характеристика АВМ n АВМ в 5 -10% случаев является причиной САК n Наиболее часто САК происходят в возрасте 20 -40 лет и служат причиной инвалидизации больного n Различают два клинических типа АВМ 1. Геморрагический тип течения заболевания – в 50 – 70 % случаев. Для этого типа течения характерно наличие у больного артериальной гипертензии, небольшого размера узла мальформации, дренажа ее в глубокие вены, а так же локализация в задней черепной ямке. 2. Торпидный тип течения, характерен для больных с АВМ больших размеров, локализацией ее в коре, кровоснабжение ветвями средней мозговой артерии.

Основные механизмы патологического влияния артерио-венозной мальформации на ткань головного мозга: - Разрыв патологически измененных сосудов клубка или аневризм артерий, питающих АВМ. - Хроническая недостаточность кровообращения, вызванная артериовенозным шунтированием.

Классификация АВМ (по Spetzler-Martin, 1986) n По размеру: Менее 3 см – 1 балл 3 – 6 см – 2 балла Более 6 см – 3 балла По локализации: Вне функционально значимой зоны – 0 баллов В пределах функционально значимой зоны – 1 балл Подразделение АВМ по характеру дренирования: Отсутствие глубоких дренирующих вен – 0 баллов Наличие глубоких дренирующих вен – 1 балл n По этой классификации большинством нейрохирургов определяется степень операбельности мальформации. Существует 5 градаций мальформации: при I (1 балл) градации риск оперативного вмешательства незначительный, при V градации (5 баллов) – возникают большие технические сложности, высок риск глубокой инвалидизации и летального исхода.

Методы лечения артериовенозных мальформаций. n 1. Хирургические: открытые операции, эндоваскуляные вмешательства 2. Консервативное 3. Радиохирургическое

Показания к радиохирургии: n 1. Мальформации диаметром менее 3 см, недоступные для прямого хирургического удаления. 2. Остатки АВМ того же размера после прямых или эндовазальных операций. n Результаты лечения: полная облитерация через два года АВМ до 3, 0 см – 85%

Подставка для стереотаксической разметки внутричерепных мишеней
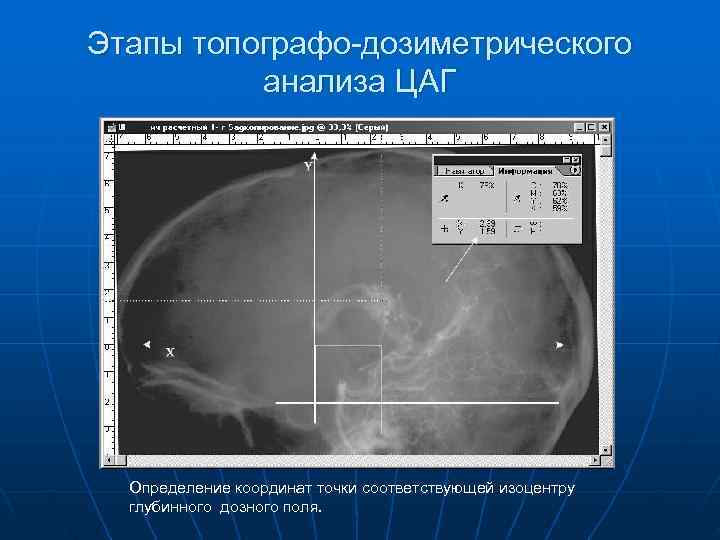
Этапы топографо-дозиметрического анализа ЦАГ Определение координат точки соответствующей изоцентру глубинного дозного поля.
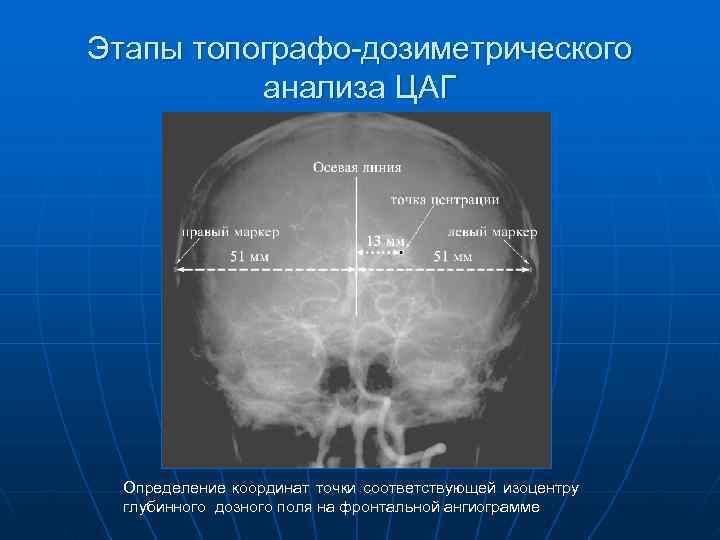
Этапы топографо-дозиметрического анализа ЦАГ Определение координат точки соответствующей изоцентру глубинного дозного поля на фронтальной ангиограмме
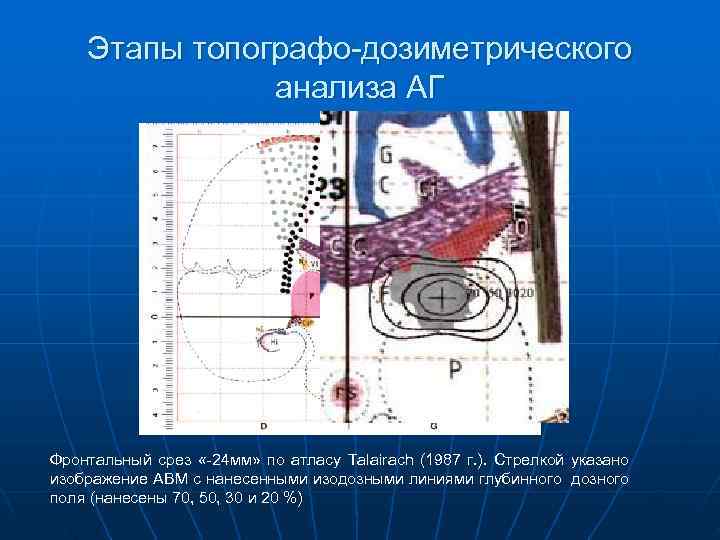
Этапы топографо-дозиметрического анализа АГ Фронтальный срез «-24 мм» по атласу Talairach (1987 г. ). Стрелкой указано изображение АВМ с нанесенными изодозными линиями глубинного дозного поля (нанесены 70, 50, 30 и 20 %)
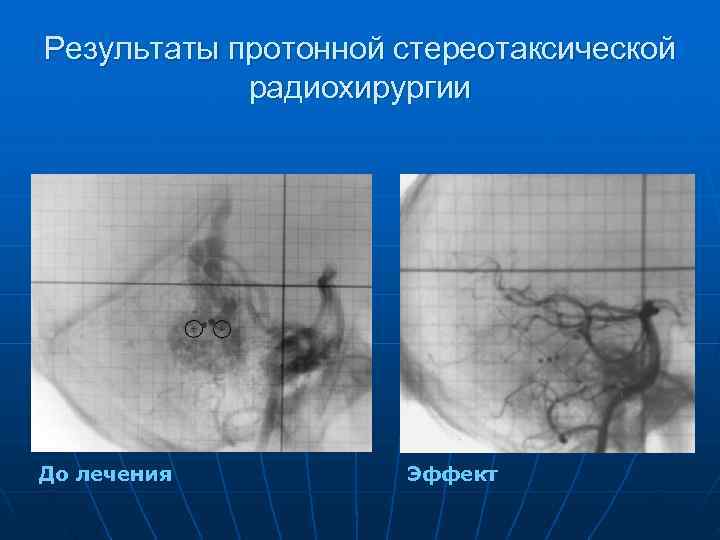
Результаты протонной стереотаксической радиохирургии До лечения Эффект
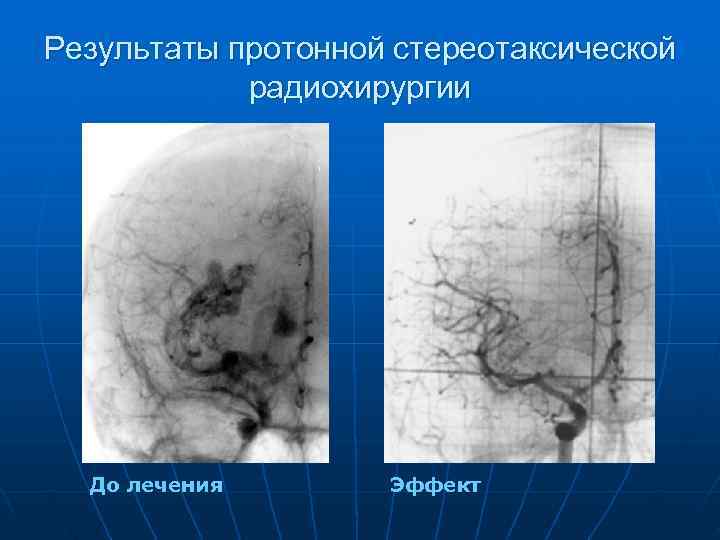
Результаты протонной стереотаксической радиохирургии До лечения Эффект

Стереотаксическая лучевая терапия узкими фотонными пучками n Больная с кавернозной ангиомой головного мозга, подготовленная к стереотаксической лучевой терапии узким пучком фотонов по неинвазивной методике (МРТ-контрастные метки на индивидуальной фиксирующей маске, отражающие реперные, исходные координаты и координаты мишени).

Лечение больного с АВМ головного мозга на линейном ускорителе (ЛУЭР 20 М)
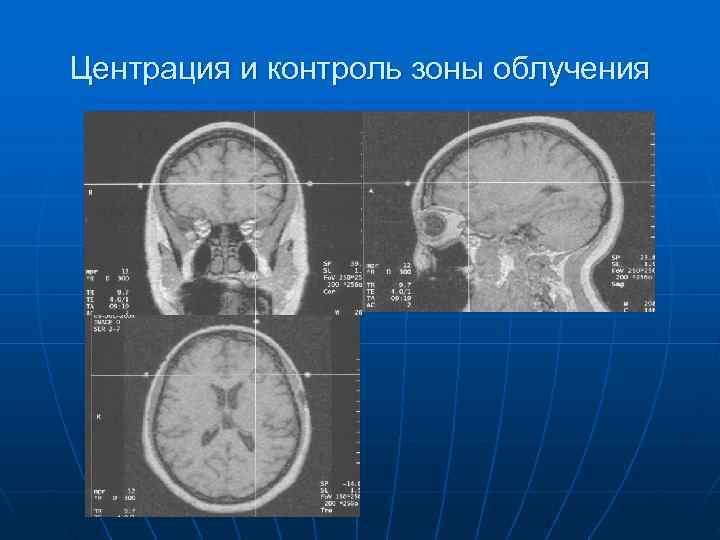
Центрация и контроль зоны облучения

Спасибо за внимание
ЛЕКЦИЯ цнс, полностью - копия, врачи - копия.PPT
- Количество слайдов: 93

