Оптимизация лечения РС.ppt
- Количество слайдов: 66

Оптимизaция лечения РС: смена иммуномодуляторов и комбинированная терапия Howard Zwibel, M. D. Baptist Health Doctors Hospital MS Center Coral Gables, Florida USA 1

Почему нужно переключаться и комбинировать? • В настоящий момент доступные виды терапии эффективны только частично • Контроль заболевания может быть неполным у большого числа больных • Выработка нейтрализующих антител требует изменения терапии • Субоптимальный ответ на лечение может потребовать альтернативного подхода • Переключение с одного иммуномодулятора на другой и комбинированная терапия рутинно практикуются, хотя данные спланированных клинических исследований по этому вопросу не многочисленны 2
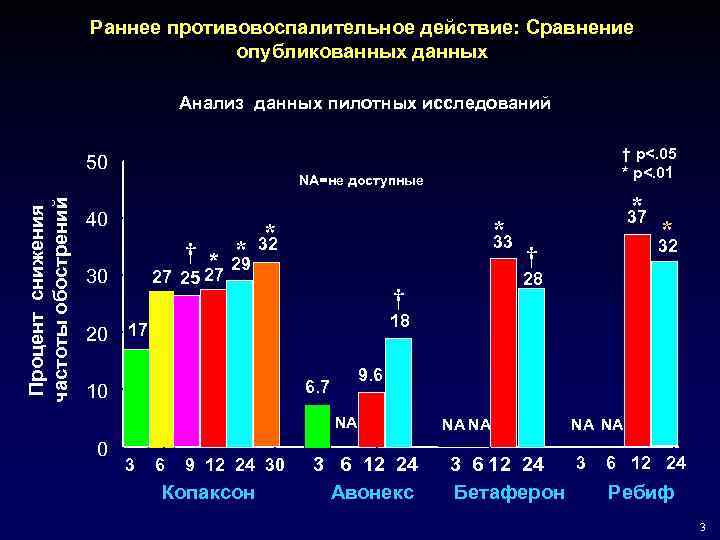
Раннее противовоспалительное действие: Сравнение опубликованных данных Анализ данных пилотных исследований Процент снижения частоты обострений 50 NA=не доступные 40 * † * 29 27 30 20 * * 33 * 32 27 25 * 32 † 18 9. 6 6. 7 NA 3 * 37 28 † 17 10 0 † p<. 05 * p<. 01 6 9 12 24 30 Копаксон 3 6 12 24 Авонекс NA NA 3 3 6 12 24 Бетаферон 6 12 24 Ребиф 3

Нейтрализующие антитела к интерферонам - использование в практике результатов определения НАТ 4

Выявление и лечение пациентов с субоптимальным ответом на иммуномодуляторы 5

Руководство по определению антител к интерферонам бета: отчет рабочей группы EFNS 6

Данные по переключению на другую ИМТ 7

Клиническое течение РРС после изменения иммуномодулирующей терапии C. Caon, M. Din, W. Ching, A. Tselis, R. Lisak and O. Khan European J Neurol 2006 13: 471 -474 8

Цели и дизайн исследования • Проспективное открытое исследование, продолжительностью 36 -42 мес. для определения эффективности терапии при переключении на ГА у больных РРС, после неудачного применения IFN -1 a вм 1 раз в неделю • Больные РРС (N=85) получали IFN -1 a в течение 18 месяцев и прекратили иньекции вследствие: – Отсутствия эффективности • Одно обострение за последний год – Токсичности и побочных эффектов определяемой клинически и/или лабораторно после титрования дозы интерферона • Гепатотоксичность ( повышение ферментов печени в два раза выше верхней границы нормы) • Лейкопения < 2500 клеток • Усталость, постинъекционная лихорадка, слабость • Оценка по шкале EDSS проводилась каждые 6 месяцев Caon C. et al. Eur J Neurol 2006 13: 471 -74 9
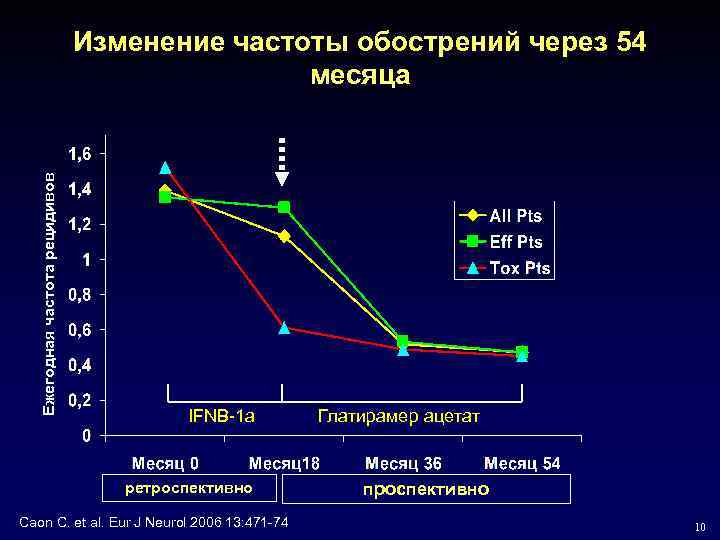
Ежегодная частота рецидивов Изменение частоты обострений через 54 месяца IFNB-1 a ретроспективно Caon C. et al. Eur J Neurol 2006 13: 471 -74 Глатирамер ацетат проспективно 10
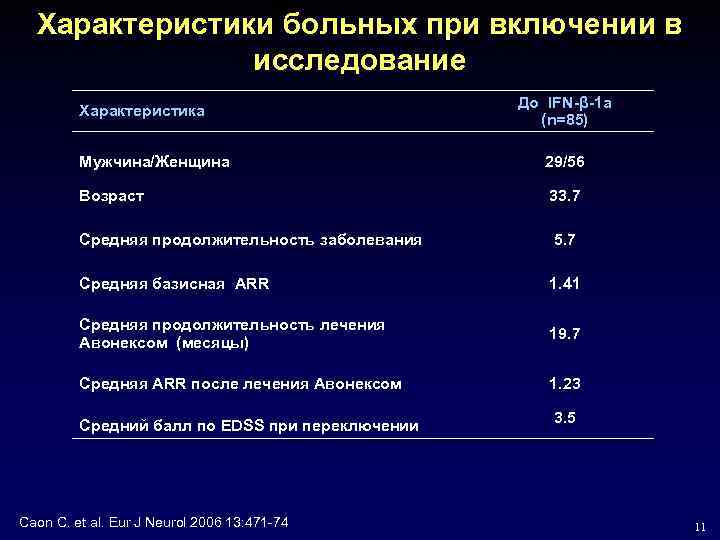
Характеристики больных при включении в исследование Характеристика До IFN-β-1 a (n=85) Мужчина/Женщина 29/56 Возраст 33. 7 Средняя продолжительность заболевания 5. 7 Средняя базисная ARR 1. 41 Средняя продолжительность лечения Авонексом (месяцы) 19. 7 Средняя ARR после лечения Авонексом 1. 23 Средний балл по EDSS при переключении Caon C. et al. Eur J Neurol 2006 13: 471 -74 3. 5 11
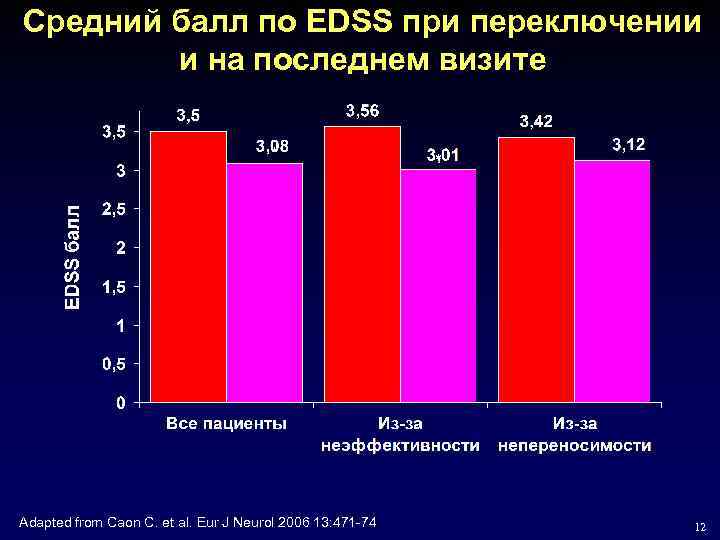
Средний балл по EDSS при переключении и на последнем визите * Adapted from Caon C. et al. Eur J Neurol 2006 13: 471 -74 * 12

Влияние изменения ИМТ на частоту обострений • Снижение среднегодовой частоты обострений на 57% после переключения на Копаксон: – На 61% в подгруппе из 62 больных, переключившихся из-за не эффективности – На 23% дополнительное снижение среднегодовой частоты в группе из 23 больных, переключившихся из-за токсичности и побочных эффектов Caon C. et al. Eur J Neurol 2006 13: 471 -74 13

Переносимость ГА • У всех больныx, прекратившиx прием IFNB-1 a вследствие побочных эффектов и токсичности, показатели лабораторных анализов вернулись к нормальному статусу при лечении ГА. • Ни один больной не прекратил терапию ГА в течение >3 лет • 6 больных прекратили участие в исследовании по несвязанным с терапией причинами (например, переезд); все 6 продолжали лечение ГА и после выхода из исследования Caon et al. Eur J Neurol 2006: 13: 471 -4. 14
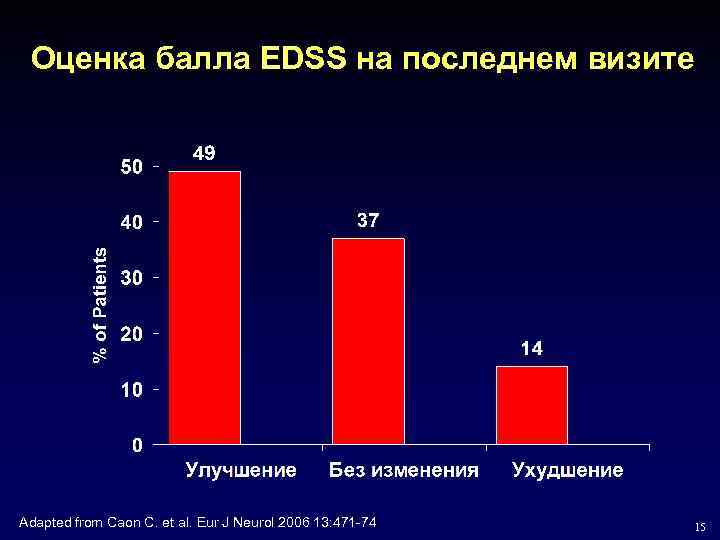
Оценка балла EDSS на последнем визите Adapted from Caon C. et al. Eur J Neurol 2006 13: 471 -74 15

Выводы • Больные с активным течением РРС и неэффективностью терапии IFN beta-1 a 30 мкг в/м 1 раз в неделю могут получить положительные результаты при переводе на Копаксон • Частота обострений снизилась на 58% после перевода с IFN beta-1 a в/м еженедельно на ГА • Балл по шкале EDSS не увеличивался во время исследования, напротив, наблюдалось снижение балла EDSS с 3. 5 до 3. 08 • Больные лучше переносили ГА ежедневно п/к, чем IFN beta 1 a в/м 1 раз в неделю Caon C. et al. Eur J Neurol 2006 13: 471 -74 17

ГА в лечении РРС у ранее не лечившихся больных и у больных, получавших интерферон бета-1 b H. L. Zwibel for the Copolymer-1 Treatment Study Principal Investigators Acta Neurol Scan 2006 113: 378 -86 18

Причины отказа от терапии IFN β-1 b до включения в исследование отчеты (n)* % больные (n=247) Гриппоподобный синдром 92 37. 2 Отсутствие эффекта 90 36. 4 Реакция в месте инъекции 72 29. 2 Депрессия 54 21. 9 Другие побочные реакции 53 21. 5 Повышение печеночных ферментов 21 8. 5 Нарушение менструального цикла 6 2. 4 Респираторные нарушения 4 1. 6 Сердечно-сосудистые нарушения 2 0. 8 Другие причины# 110 44. 5 Неизвестно 35 14. 2 Причина * Patients may have reported more than one reason for discontinuation # Of 110 patients, 100 (91%) gave the reason “felt better after discontinuation” Zwibel H. et al Acta Neuro Scan 2006 113: 378 -386 19

Исследование Zwibel Перевод с Бетаферона на Копаксон • Проспективное открытое исследование эффективности и безопасности Копаксона у не получавших ИМТ больных РРС и больных, ранее получавших IFNß-1 b • Проводилось в 48 центрах в США в течение более 3. 5 лет • 247 больных ранее получавших IFNß-1 b, 558 больных ранее не получавших ИМТ • Продолжительность приема ГА ~20 месяцев для группы не получавших ранее ИМТ больных и ~15 месяцев для группы переведенных пациентов Zwibel H. et al Acta Neuro Scan 2006 113: 378 -386 20
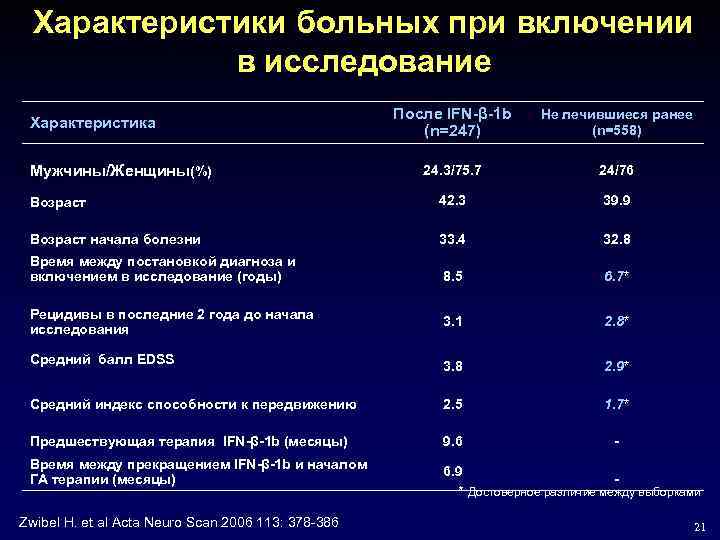
Характеристики больных при включении в исследование После IFN-β-1 b (n=247) Не лечившиеся ранее (n=558) 24. 3/75. 7 24/76 Возраст 42. 3 39. 9 Возраст начала болезни 33. 4 32. 8 Время между постановкой диагноза и включением в исследование (годы) 8. 5 6. 7* 3. 1 2. 8* 3. 8 2. 9* Средний индекс способности к передвижению 2. 5 1. 7* Предшествующая терапия IFN-β-1 b (месяцы) 9. 6 - Характеристика Мужчины/Женщины(%) Рецидивы в последние 2 года до начала исследования Средний балл EDSS Время между прекращением IFN-β-1 b и началом ГА терапии (месяцы) Zwibel H. et al Acta Neuro Scan 2006 113: 378 -386 6. 9 * Достоверное различие между выборками 21
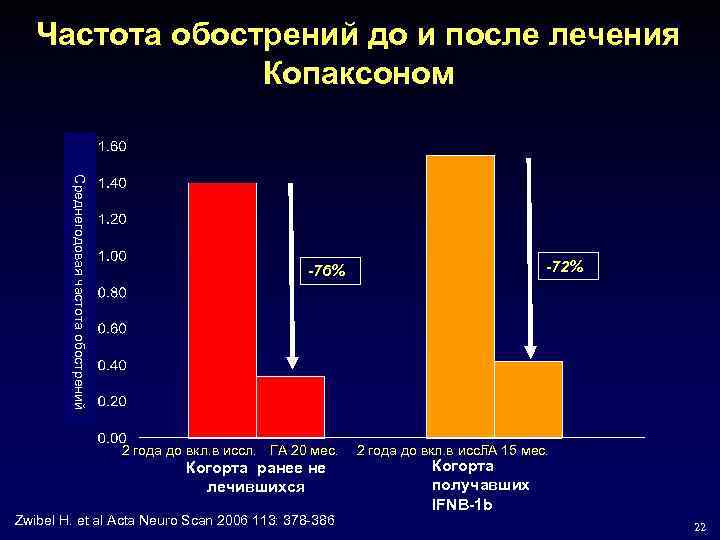
Частота обострений до и после лечения Копаксоном Среднегодовая частота обострений -72% -76% 2 года до вкл. в иссл. ГА 20 мес. Когорта ранее не лечившихся Zwibel H. et al Acta Neuro Scan 2006 113: 378 -386 2 года до вкл. в иссл. 15 мес. ГА Когорта получавших IFNB-1 b 22

Влияние на частоту обострений Больные без обострений • 68. 4% больных, ранее получавших IFNß-1 b • 69. 5% нелеченных больных Время до наступления первого обострения • среднее: – 1391 дней для не получавших ИМТ больных – Не определялось у больных, лечившихся ранее IFNß-1 b т. к. у 50% из них не было обострений до конца исследования. • У 25% больных: – 328 дней для не получавших ИМТ больных (по сравнению с 287 днями в базовых исследованиях) – 245 дней для больных, лечившихся ранее IFNß-1 b Zwibel H. et al Acta Neuro Scan 2006 113: 378 -386 23
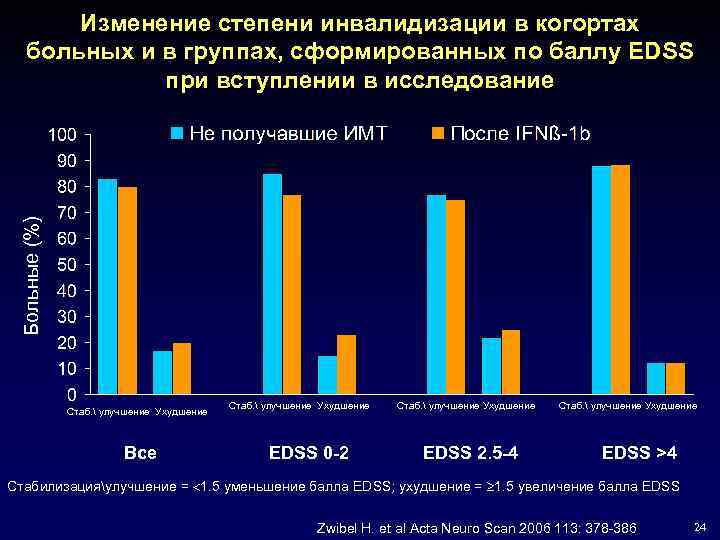
Больные (%) Изменение степени инвалидизации в когортах больных и в группах, сформированных по баллу EDSS при вступлении в исследование Стаб. улучшение Ухудшение Все Стаб. улучшение Ухудшение EDSS 0 -2 Стаб. улучшение Ухудшение EDSS 2. 5 -4 Стаб. улучшение Ухудшение EDSS >4 Стабилизацияулучшение = 1. 5 уменьшение балла EDSS; ухудшение = 1. 5 увеличение балла EDSS Zwibel H. et al Acta Neuro Scan 2006 113: 378 -386 24

Причины прерывания терапии Копаксоном Не получавшие ИМТ (n) Больные после лечения IFN -1 b (n) Побочные реакции 61 27 Смерть (не связанная с лечением) (не лечением) 1 0 Конец запланированного исследования 311 140 Вышедшие из под наблюдения 67 24 Другое 16 7 Решение пациента о выходе из исследования 99 48 Серьезная побочная реакция 3 1 Причина Zwibel H. et al Acta Neuro Scan 2006 113: 378 -386 27

Выводы • Копаксон эффективно снижал частоту обострений в обеих группах пациентов – Предшествующая иммуномодулирующая терапия не оказывала влияния на эффективность Копаксона у больных • Копаксон эффективно предотвращал развитие стойкой инвалидизации – Самые инвалидизированные больные на момент включения в исследование (EDSS >4) в обеих группах почувствовали улучшение после перевода на ГА • Копаксон был безопасен и хорошо переносился Zwibel H. et al Acta Neuro Scan 2006 113: 378 -386 28

Индукция ремиссии и комбинированная терапия, последние данные 29

Комбинации должны быть… • Рациональными – – • Ни один препарат не может обеспечить контроль заболевания у всех пациентов Ни один препарат не обеспечивает полного контроля заболевания у отдельно взятого больного Прeдставлять разумное сочетание – эффективности • • – безопасности • • – Комбинировать препараты с синергестическим механизмом действия Препарат A + Препарат B > A или B отдельно Учитывать возможность появления новых побочных эффектов при комбинировании Влияние метаболизма одного препарата на метаболизм другого в комбинации может вести к снижению эффективности комбинации Эффективности затрат на комбинацию препаратов 30

Комбинированная терапия других заболеваний • • Сердечно-сосудистые заболевания – Аспирин + холестерин-снижающие препараты + ACE-Is + β-блокаторы + др. Эпилепсия – Монотерапия, двойная и тройная комбинированная терапия • Онкология – Сочетанная химиотерапия ! • Ревматоидный артрит – Нестероидные противовспалительные средства+ стероиды + иммуномодуляторы(метотрексан/голд/pпеницилламин) + анти-ФНО α 31

Подходы к комбинированной терапии • Эскалационный подход – Последовательное усиление терапии для контроля заболевания (например, эпилепсия) • Подход фиксированной политерапии – Сочетания препаратов для контроля различных проявлений заболевания • Индукция ремиссии + поддерживающая терапия – Использование агрессивных препаратов для подавления активности заболевания – Поддержания контроля заболевания базисными препаратами для длительного лечения • Например, онкологические заболевания, ревматоидный артрит 32

Рациональное обоснование комбинированной терапии при РРС • Ремиттирующий характер воспалительного процесса • • Все виды лечения являются только отчасти эффективными Неспецифические и селективные иммуносупрессоры эффективны при РС: – Эффективность пропорциональна уровню иммуносупрессии – Риск осложнений пропорционален продолжительности иммуносупрессии • Различные механизмы действия влияют на различные направления патогенеза заболевания • Опыт лечения других воспалительных заболеваний подтверждает целесообразность индукционной/ комбинированной терапии 33

Гипотезы • Митоксантрон разрушает пул аутоагрессивных Т-клеток, а Копаксон усиливает выработку T- клеток с противовоспалительными свойствами • Если это так, тогда краткосрочная иммуносупрессия, в комбинации с долгосрочной терапией ГА может обеспечить надежную и эффективную долгосрочную терапию РС 34

Исследования индукции ремиссии РРС Митоксантроном • исследование Ramathal/Boggild США • исследование Vollmer NC-100 США • исследование Tellez Испания 35

Ramtahal et al. J Neurol. 2006; 253: 1160 -4. 36

Последовательный курс Митоксантрон + Копаксон (81) Ramtahal et al. J Neurol. 2006; 253: 1160 -4. 37
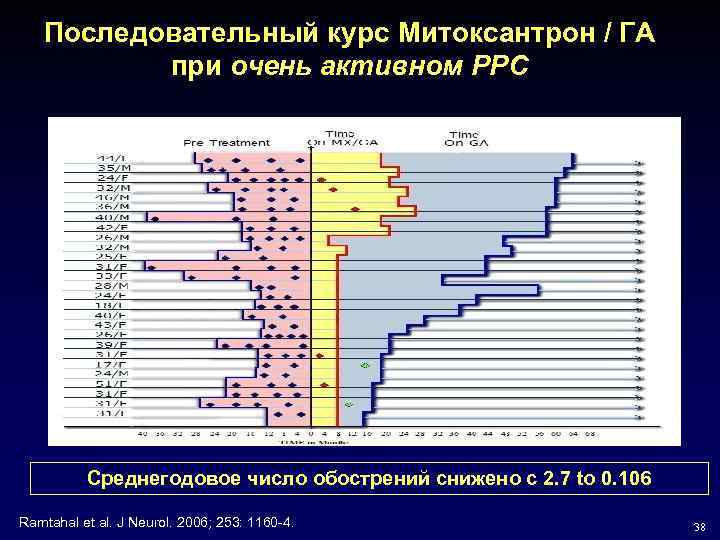
Последовательный курс Митоксантрон / ГА при очень активном РРС Среднегодовое число обострений снижено с 2. 7 to 0. 106 Ramtahal et al. J Neurol. 2006; 253: 1160 -4. 38

Индукция ремиссии коротким курсом митоксантрона обеспечивает ранний и выраженный эффект на МРТ активность заболевания у больных с активными формами РРС (Протокол по Копаксону МC 100) T. Vollmer, D. Campagnolo, H. Panitch, M. S. Freedman, S. K. Gazda, A. Bar-Or, D. L. Arnold (Phoenix, Burlington, San Antonio USA; Ottawa, Montreal CA) Vollmer T et al. Mult Scler. 2006; 12: S 11 39

Цели исследования Определить, обеспечивает ли краткосрочная индукция иммуносупрессии Митоксантроном у больных РРС большую эффективность лечения ГА в первый год терапии • Определить приводит ли краткосрочная индукция иммуносупрессии митоксантроном к усилению долгосрочного эффекта ГА (36 месяцев) • Vollmer T et al. Mult Scler. 2006; 12: S 11 40

Дизайн исследования • Четыре центра • Рандомизированное • Две терапевитческие группы • Ослепленное (исследователь получает EDSS и МРT п-та) • Одинаковая длительность терапии в группах • Ключевой критерий включения: по крайней мере один активный очаг на МРТ • Первая фаза исследования 15 месяцев факультативное продление фазы наблюдения до 36 месяцев Vollmer T et al. Mult Scler. 2006; 12: S 11 41

Дизайн исследования Месяцы Неврологическое обследование 0 2. 5 6 9 12 15 24 36 M-ГА 20 mg пк qd Двойное-слепое, В параллельных группах II фаза исследований Открытая обсервационная фаза M-ГА 20 mg – Открытая индукция тремя в/в инфузиями Mitox 12 mg/m 2 в месяцы 0, 1 и 2 до кумулятивной дозы 36 mg/m 2 – 2 недельный период отмывки – Ежедневная терапия ГА 20 mg пк в течение 12. 5 месяцев + продленная открытая фаза Только 20 mg ГА – Ежедневная терапия ГА 20 mg пк в течение 15 месяцев+ продленная открытая фаза Vollmer T et al. Mult Scler. 2006; 12: S 11 43

Первичные показатели безопасности • Иммуносупрессия и токсичность препарата – Оценка в начале исследования, на 14 ± 2 день после каждого введения митоксантрона, далее каждые 3 месяца – Анализ лейкоцитарной формулы с дифференцированным подсчетом тромбоцитов; ACT, AЛT, щелочной фосфотазы, общего билирубина; мочевины крови Кардиотоксичность – Оценка в начале исследования, на 14 ± 2 день после каждого введения митоксантрона, далее каждые 15 месяцев – ЭКГ и Multiple gated acquisition (MUGA) тест для LVEF Vollmer T et al. Mult Scler. 2006; 12: S 11 44

Критерии оценки эффективности • Первичные критерии: – Число очагов, накапливающих Gd на МРТ • Вторичные критерии: – Частота обострений – – • Число пациентов без обострений Время до наступления первого обострения Дополнительные критерии: – Изменения EDSS на 3, 6, 9, 12 and 15 месяце набл. – – Подтвержденное прогрессирование заболевания МРТ: общее количество очагов, степень атрофии мозга, Gd накапливающие очаги – Утомляемость Vollmer T et al. Mult Scler. 2006; 12: S 11 45
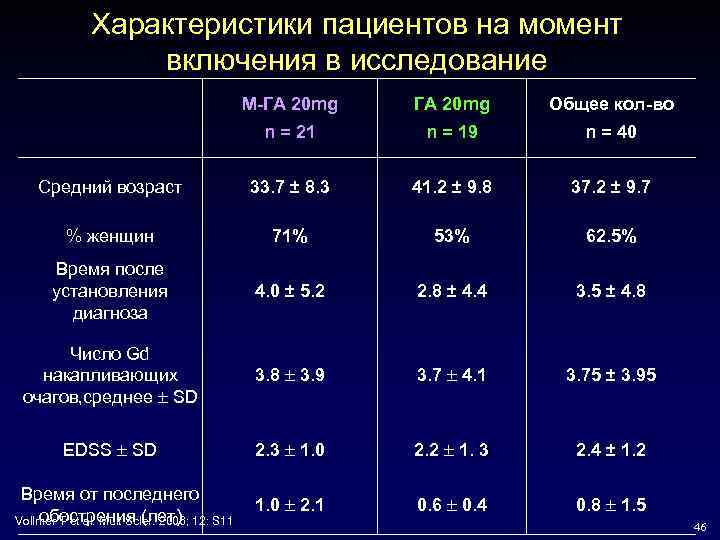
Характеристики пациентов на момент включения в исследование M-ГА 20 mg Общее кол-во n = 21 n = 19 n = 40 Средний возраст 33. 7 ± 8. 3 41. 2 ± 9. 8 37. 2 ± 9. 7 % женщин 71% 53% 62. 5% Время после установления диагноза 4. 0 ± 5. 2 2. 8 ± 4. 4 3. 5 ± 4. 8 Число Gd накапливающих очагов, среднее SD 3. 8 3. 9 3. 7 4. 1 3. 75 ± 3. 95 EDSS SD 2. 3 1. 0 2. 2 1. 3 2. 4 ± 1. 2 1. 0 2. 1 0. 6 0. 4 0. 8 1. 5 Время от последнего обострения (лет) Vollmer T et al. Mult Scler. 2006; 12: S 11 46
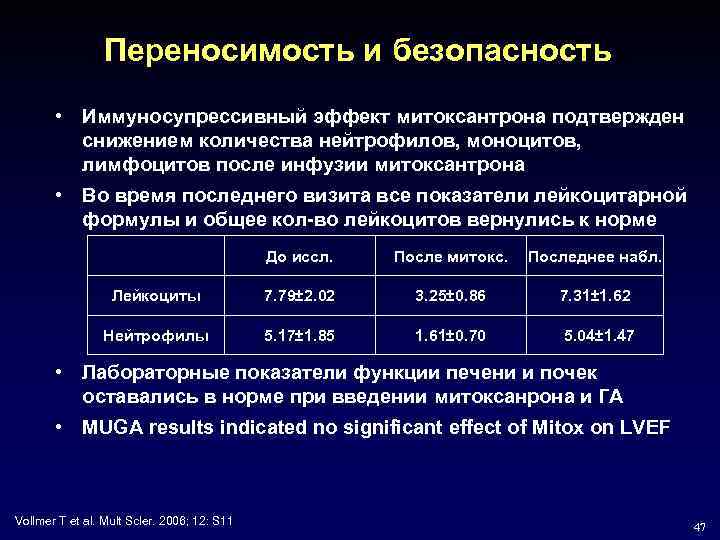
Переносимость и безопасность • Иммуносупрессивный эффект митоксантрона подтвержден снижением количества нейтрофилов, моноцитов, лимфоцитов после инфузии митоксантрона • Во время последнего визита все показатели лейкоцитарной формулы и общее кол-во лейкоцитов вернулись к норме До иссл. После митокс. Последнее набл. Лейкоциты 7. 79± 2. 02 3. 25± 0. 86 7. 31± 1. 62 Нейтрофилы 5. 17± 1. 85 1. 61± 0. 70 5. 04± 1. 47 • Лабораторные показатели функции печени и почек оставались в норме при введении митоксанрона и ГА • MUGA results indicated no significant effect of Mitox on LVEF Vollmer T et al. Mult Scler. 2006; 12: S 11 47
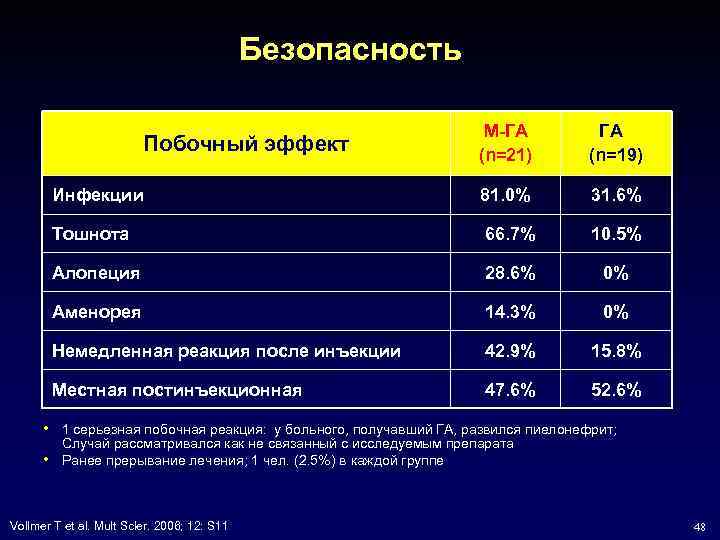
Безопасность M-ГА (n=21) ГА (n=19) Инфекции 81. 0% 31. 6% Тошнота 66. 7% 10. 5% Алопеция 28. 6% 0% Аменорея 14. 3% 0% Немедленная реакция после инъекции 42. 9% 15. 8% Местная постинъекционная 47. 6% 52. 6% Побочный эффект • • 1 серьезная побочная реакция: у больного, получавший ГА, развился пиелонефрит; Случай рассматривался как не связанный с исследуемым препарата Ранее прерывание лечения; 1 чел. (2. 5%) в каждой группе Vollmer T et al. Mult Scler. 2006; 12: S 11 48
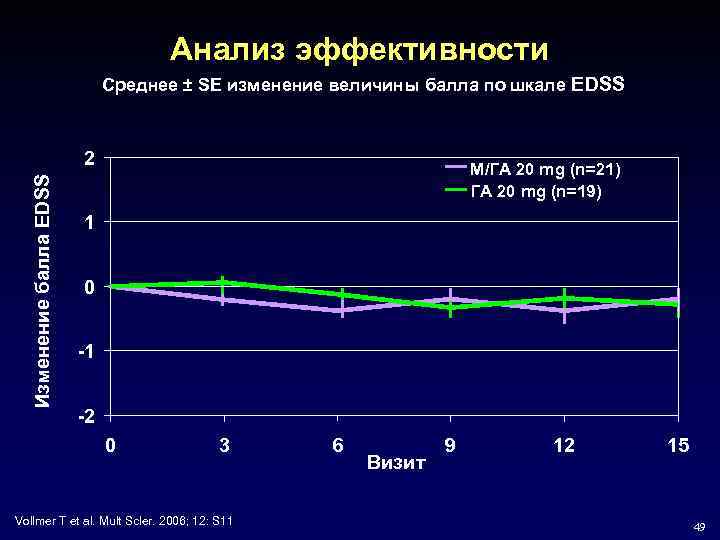
Анализ эффективности Среднее ± SE изменение величины балла по шкале EDSS Изменение балла EDSS 2 M/ГА 20 mg (n=21) ГА 20 mg (n=19) 1 0 -1 -2 0 3 Vollmer T et al. Mult Scler. 2006; 12: S 11 6 Визит 9 12 15 49

Анализ эффективности Общее число очагов в T 1 - режиме (среднее зн. (±SE)) Общее количество Т 1 взвешенныных очагов 5 M-GA 20 mg (n=21) GA 20 mg (n=19) 4 3 P=0. 0001 2 1 0 0 3 6 9 12 15 Визит Vollmer T et al. Mult Scler. 2006; 12: S 11 50

Анализ эффективности Снижение частоты обострений Среднегодовая частота обостренй • • 46% снижение Коэф. относительного риска = 0. 54 95% доверительный интервал [0. 16 - 1. 84] Регрессия Пуассона; p=0. 31 0. 4 • % без обострений 0. 3 M-ГА = 81% ГА = 79% • Число рецидивов 0. 2 M-ГА = 4 0. 1 ГА = 7 0 M-ГА Vollmer T et al. Mult Scler. 2006; 12: S 11 ГА 51

MC-100 продленное исследование • Открытая продленная фаза MC-100 • Оценки состояния на визитах 24 и 36 месяцев • Неврологическое обследование, оценка по шкале EDSS, анамнестическая оценка количества обострений, общий анализ крови, биохимия и МРТ • Участие 3 из 4 центров 30 из 40 больных приняли участие Vollmer T et al. Mult Scler. 2006; 12: S 11 52
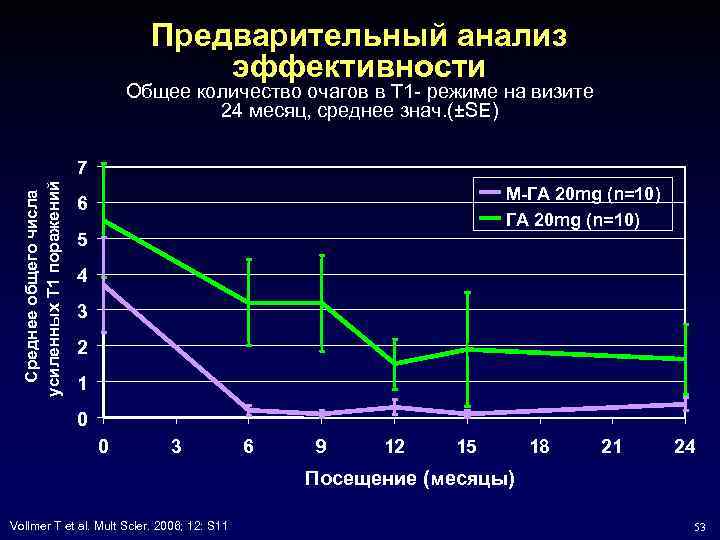
Предварительный анализ эффективности Общее количество очагов в T 1 - режиме на визите 24 месяц, среднее знач. (±SE) Среднее общего числа усиленных T 1 поражений 7 M-ГА 20 mg (n=10) 6 5 4 3 2 1 0 0 3 6 9 12 15 18 21 24 Посещение (месяцы) Vollmer T et al. Mult Scler. 2006; 12: S 11 53
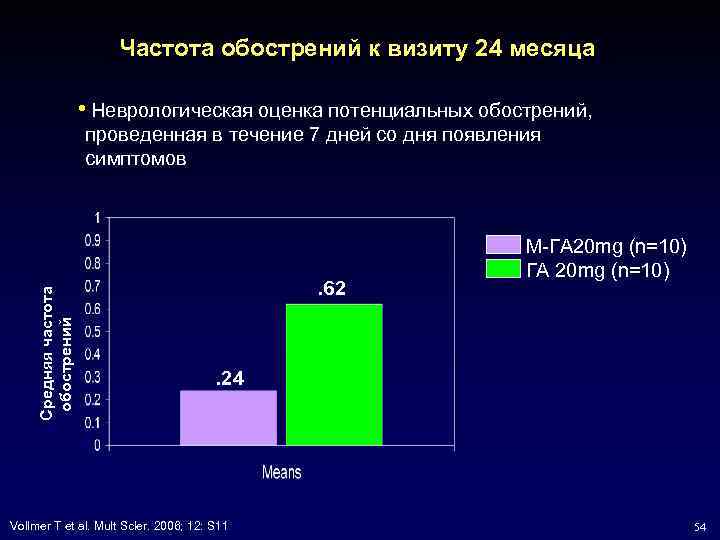
Частота обострений к визиту 24 месяца • Неврологическая оценка потенциальных обострений, Средняя частота обострений проведенная в течение 7 дней со дня появления симптомов . 62 M-ГА 20 mg (n=10) . 24 Vollmer T et al. Mult Scler. 2006; 12: S 11 54

выводы • Индукция ремиссии коротким инфузионным курсом митоксантрона с последующим длительным пк введением ГА 20 мг/ в течение 15 месяцев является – Безопасной и хорошо переносимой терапией – Более эффективной в отношении снижения активности заболевания (снижение на 89% по результатам МРТ), чем один ГА • Первичные результаты предполагают, что снижение активности заболевания (результаты МРТ) сохраняется по крайней мере последующие 24 месяца • Имеется тенденция относительного снижения частоты обострений в течение 24 месяцев в после индукции ремиссии митоксантроном с последующим ежедневным приемом ГА по сравнению с монотерапией • Результаты данного исследования доказательно обоснованы Vollmer T et al. Mult Scler. 2006; 12: S 11 55

Терапия Глатирамера ацетатом после курса митоксантрона у не ответивших на лечение интерфероном бета пациентов N. Téllez, J. Río, M. Tintoré, Á. Rovira, C. Nos, I. Galán, R. Pelayo, H. Perkal, X. Montalban (Barcelona, Spain) Mult Scler. 2006; 12: S 216 56
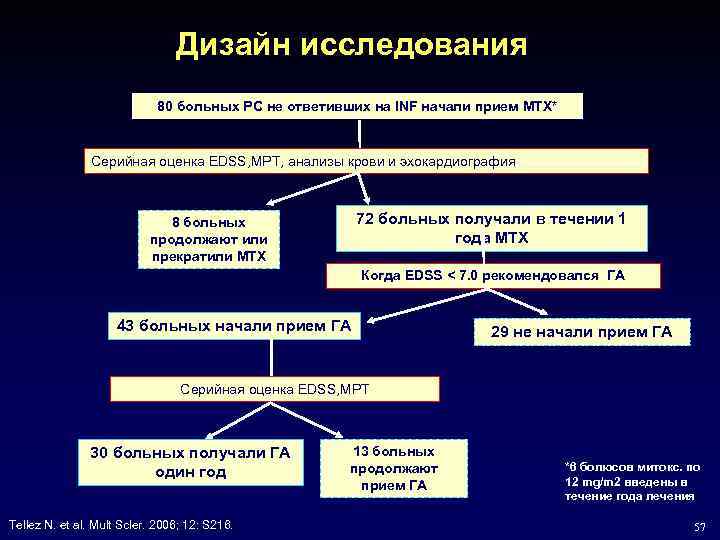
Дизайн исследования 80 больных РС не ответивших на INF начали прием MTХ* Серийная оценка EDSS, МРТ, анализы крови и эхокардиография 72 больных получали в течении 1 года MTХ 8 больных продолжают или прекратили MTХ Когда EDSS < 7. 0 рекомендовался ГА 43 больных начали прием ГА 29 не начали прием ГА Серийная оценка EDSS, МРТ 30 больных получали ГА один год Tellez N. et al. Mult Scler. 2006; 12: S 216. Scler. 12: S 216. 13 больных продолжают прием ГА *6 болюсов митокс. по 12 mg/m 2 введены в течение года лечения 57
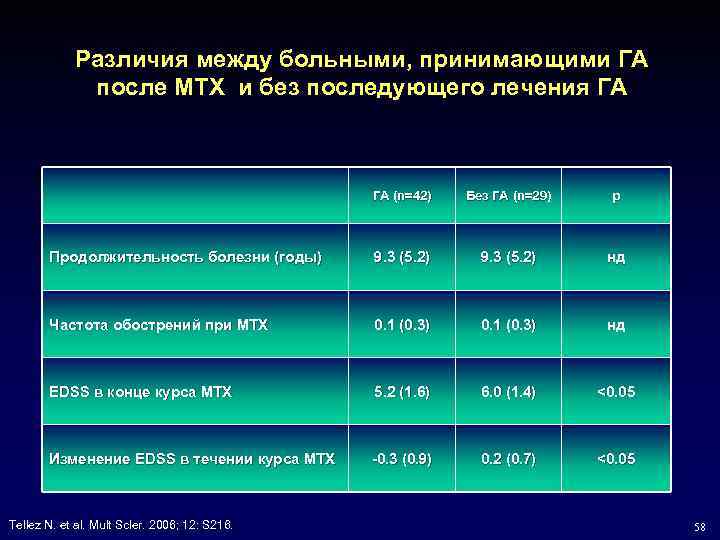
Различия между больными, принимающими ГА после MTX и без последующего лечения ГА ГА (n=42) Без ГА (n=29) p Продолжительность болезни (годы) 9. 3 (5. 2) нд Частота обострений при MTX 0. 1 (0. 3) нд EDSS в конце курса MTX 5. 2 (1. 6) 6. 0 (1. 4) <0. 05 Изменение ЕDSS в течении курса MTX -0. 3 (0. 9) 0. 2 (0. 7) <0. 05 Tellez N. et al. Mult Scler. 2006; 12: S 216. Scler. 12: S 216. 58
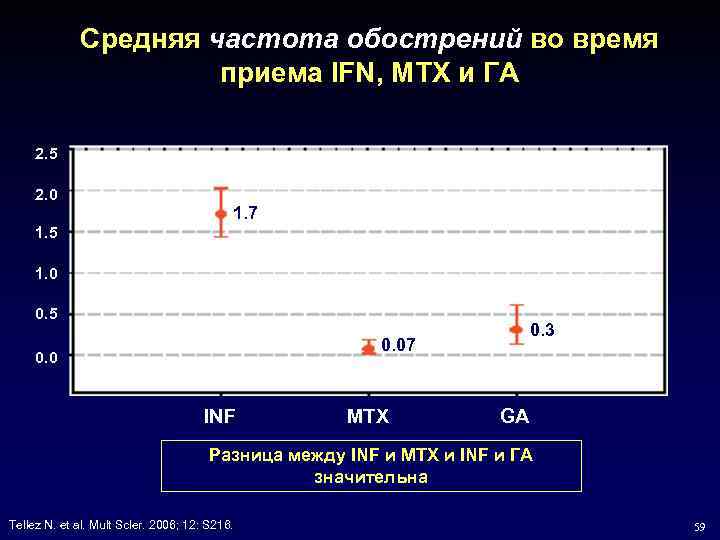
Средняя частота обострений во время приема IFN, MTX и ГА 2. 5 2. 0 1. 7 1. 5 1. 0 0. 5 0. 3 0. 07 0. 0 INF MTX GA Разница между INF и MTX и INF и ГА значительна Tellez N. et al. Mult Scler. 2006; 12: S 216. Scler. 12: S 216. 59
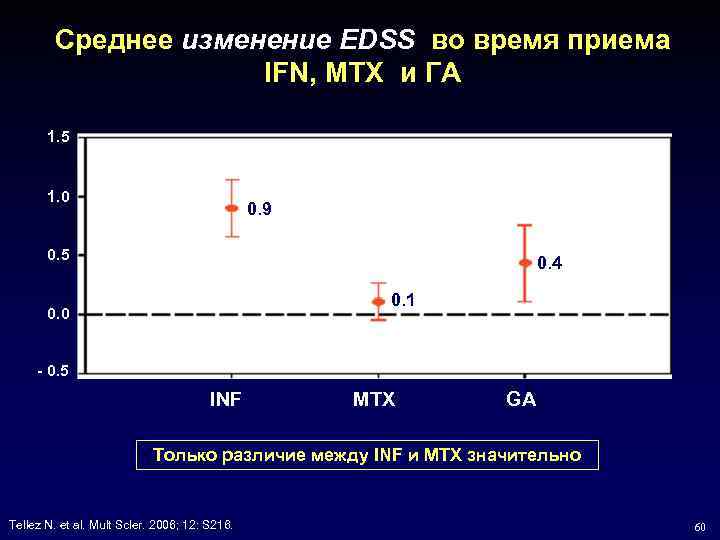
Среднее изменение EDSS во время приема IFN, MTX и ГА 1. 5 1. 0 0. 9 0. 5 0. 4 0. 1 0. 0 - 0. 5 INF MTX GA Только различие между INF и MTX значительно Tellez N. et al. Mult Scler. 2006; 12: S 216. Scler. 12: S 216. 60

Среднее количество активных очагов приеме IFN, MTX и ГА 5 4 3 2 1 1 0 0 INF MTX 0 GA Разница между INF и MTX и INF и ГА значительна Tellez N. et al. Mult Scler. 2006; 12: S 216. Scler. 12: S 216. 61

Кратковременная комбинация лечения ГА и вв стероидами, предшествующая лечению ГА, предлагают раннее начало и длительное действие на активность заболевания (результаты МРT) у больных РРС Clive Hawkins FRCP, Massimo Fillipi MD, Nicola De. Stefano MD, Ph. D UK/Italy Presented at ECTRIMS 2006, Madrid, Late Breaking News Session 62

Дизайн исследования • 89 больных принимали ГА в комбинации с ежемесячным курсом стероидов в течение 6 месяцев. Все больные получали только ГА еще 6 месяцев дополнительно • МРT мозга проводились при скрининге, вступлении в исследование и на 5, 6, 11 и 12 месяцах • Неврологическую оценку производили при скрининге, вступлении в исследовании, 3 месяце и далее через каждые 3 месяца • Лабораторные тесты проводились при скрининге, вступлении в исследование, 1, 6 месяцах и при завершении исследования Hawkins C. et al, presented at ECTRIMS 2006 Late breaking News Session 63

Дизайн исследования Первичный критерий оценки: • Изменение количества Gd накапливающих очагов в Т 1 -режиме к 6 месяцу и 12 месяцу исследования • Разница между изменением количества Gd накапливающих очагов в Т 1 -режиме в первые 6 месяцев исследования и в первые 12 месяцев исследования Hawkins C. et al, presented at ECTRIMS 2006 Late breaking News Session 64
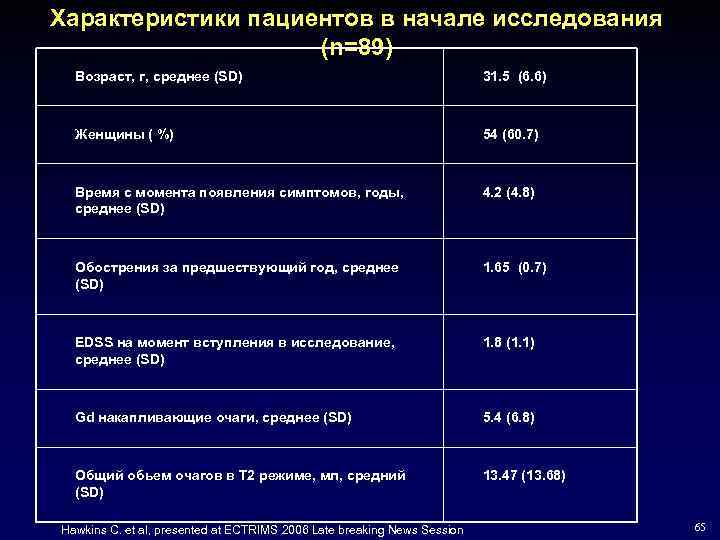
Характеристики пациентов в начале исследования (n=89) Возраст, г, среднее (SD) 31. 5 (6. 6) Женщины ( %) 54 (60. 7) Время с момента появления симптомов, годы, среднее (SD) 4. 2 (4. 8) Обострения за предшествующий год, среднее (SD) 1. 65 (0. 7) EDSS на момент вступления в исследование, среднее (SD) 1. 8 (1. 1) Gd накапливающие очаги, среднее (SD) 5. 4 (6. 8) Общий обьем очагов в Т 2 режиме, мл, средний (SD) 13. 47 (13. 68) Hawkins C. et al, presented at ECTRIMS 2006 Late breaking News Session 65
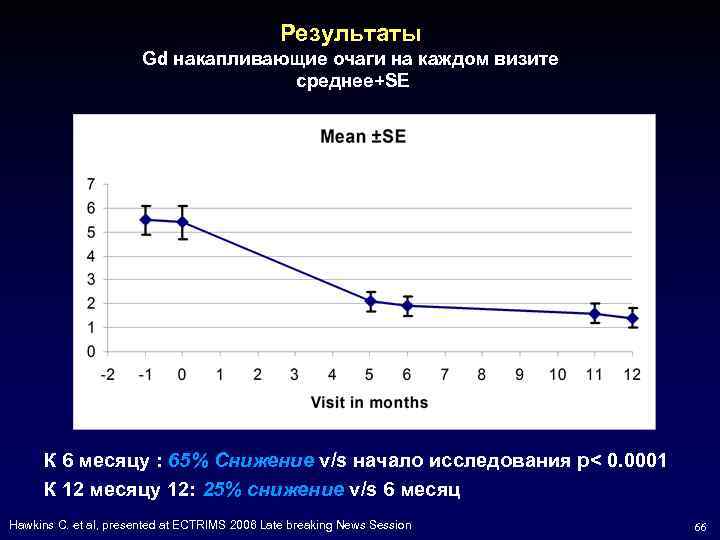
Результаты Gd накапливающие очаги на каждом визите среднее+SE • К 6 месяцу : 65% Снижение v/s начало исследования p< 0. 0001 • К 12 месяцу 12: 25% снижение v/s 6 месяц Hawkins C. et al, presented at ECTRIMS 2006 Late breaking News Session 66

Результаты Ежегодная частота обострений Частота обострений 1. 65 66% 0. 55 Hawkins C. et al, presented at ECTRIMS 2006 Late breaking News Session 73% 0. 45 67
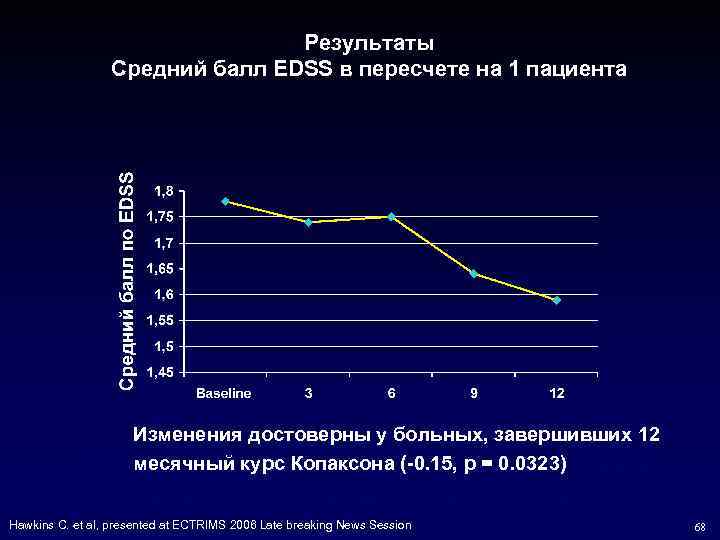
Результаты Средний балл EDSS в пересчете на 1 пациента Изменения достоверны у больных, завершивших 12 месячный курс Копаксона (-0. 15, p = 0. 0323) Change from baseline reached significance for patients completing 12 months treatment (-0. 15, p = 0. 0323) Hawkins C. et al, presented at ECTRIMS 2006 Late breaking News Session 68

Выводы • При использовании ГА в комбинации с ежемесячным курсом в/в стероидов в течение 6 месяцев возникает 65% снижение Gd накапливающих очагов, данное снижение поддерживается в течение еще 6 месяцев приеме одного ГА • По сравнению со среднегодовой частотой обострений до исследования, частота обострений в исследовании снизилась до 0. 55 ( на 66%) в первые 6 месяцев терапии ГА в комбинации со стероидами и до 0. 45 (на 73%) в последующие 6 месяцев монотерапии ГА • Средняя величина изменений по шкале EDSS достигла достоверных значений у больных в конце 12 месяца лечения (-0. 15, 95% CI: -0. 29, -0. 13, p = 0. 0323) • Побочные реакций в течение года терапии соответствовали профилю безопасности ГА Hawkins C. et al, presented at ECTRIMS 2006 Late breaking News Session 69

Резюме и выводы • Помните о том, что РС является болезнью длиною в жизнь, то есть 30 -40 лет, поэтому нашими главными целями является оптимизация лечения и обеспечение минимального нарастания инвалидизации • Это достигается путем: – Переключения на альтернативные виды терапии – Сочетанием разных видов лечения • Имеющиеся в настоящее время и появляющиеся новые виды лечения несут в себе значительный потенциал для изучения возможностей комбинированной терапии при РРС • Комбинированная терапия активно изучается в 95 -ти различных исследованиях • Индукция ремиссии и последующая терапия ГА многообещающи, что и далее будет подтверждаться крупномасштабными клиническими исследованиями 70
Оптимизация лечения РС.ppt