 Определите степень окисления атомов химических элементов по формулам их соединений: 1 вариант H 2 S, O 2, NH 3, HNO 3, Cu. Cl 2, K 2 Cr 2 O 7 2 вариант – H 3 P, H 2, Na. H, HNO 2, Fe 2 O 3, Na 2 Cr. O 4
Определите степень окисления атомов химических элементов по формулам их соединений: 1 вариант H 2 S, O 2, NH 3, HNO 3, Cu. Cl 2, K 2 Cr 2 O 7 2 вариант – H 3 P, H 2, Na. H, HNO 2, Fe 2 O 3, Na 2 Cr. O 4
 Составьте уравнения полуреакций окисления и восстановления, определите окислитель и восстановитель в реакции: 1 вариант – взаимодействия хлорида никеля (II) с алюминием 2 вариант – взаимодействия бромида железа (II) с магнием
Составьте уравнения полуреакций окисления и восстановления, определите окислитель и восстановитель в реакции: 1 вариант – взаимодействия хлорида никеля (II) с алюминием 2 вариант – взаимодействия бромида железа (II) с магнием
 Методом электронного баланса расставьте коэффициенты в схеме реакции: 1 вариант – Ba. SO 4 + C → Ba. S + CO 2 вариант – KCl. O 3+P→KCl+P 2 O 5
Методом электронного баланса расставьте коэффициенты в схеме реакции: 1 вариант – Ba. SO 4 + C → Ba. S + CO 2 вариант – KCl. O 3+P→KCl+P 2 O 5
 ЧТО ОБЪЕДИНЯЕТ ? Нанесение металлических покрытий на различные поверхности
ЧТО ОБЪЕДИНЯЕТ ? Нанесение металлических покрытий на различные поверхности
 Как это происходит? Какой химический процесс лежит в основе? ЭЛЕКТРОЛИЗ
Как это происходит? Какой химический процесс лежит в основе? ЭЛЕКТРОЛИЗ
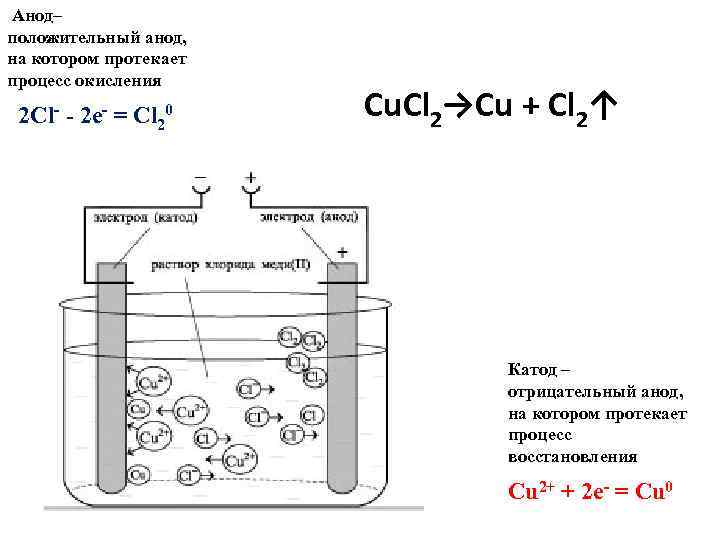 Анод– положительный анод, на котором протекает процесс окисления 2 Cl- - 2 e- = Cl 20 Cu. Cl 2→Cu + Cl 2↑ Катод – отрицательный анод, на котором протекает процесс восстановления Cu 2+ + 2 e- = Cu 0
Анод– положительный анод, на котором протекает процесс окисления 2 Cl- - 2 e- = Cl 20 Cu. Cl 2→Cu + Cl 2↑ Катод – отрицательный анод, на котором протекает процесс восстановления Cu 2+ + 2 e- = Cu 0
 Используя метод электронного баланса, расставьте коэффициенты в схемах электролиза расплавов: Al 2 O 3 →Al + O 2 KBr →K + Br 2 KOH → K + O 2 + H 2 O
Используя метод электронного баланса, расставьте коэффициенты в схемах электролиза расплавов: Al 2 O 3 →Al + O 2 KBr →K + Br 2 KOH → K + O 2 + H 2 O