ОЛ новое.ppt
- Количество слайдов: 62

определение Лейкоз- это клоновое заболевание гематопоэтической системы, возникающее в результате мутации стволовой кроветворной клетки крови.

определение Гемобластозы – это опухолевые заболевания, возникшие из кроветворных клеток (haemoblastosis; греч. haima кровь + blastos росток, зародыш + -osis). По морфологии субстрата все лейкозы делятся на 2 большие группы: • Острые лейкозы- субстрат опухоли представляют молодые (бластные) клетки; • Хронические лейкозы – субстрат опухоли представляют морфологические зрелые клетки.

эпидемиология По данным мировой статистики острые лейкозы у детей занимают первое место в структуре заболеваемости злокачественными новообразованиями. На их долю приходится 25 -30% случаев (Desanders E. Clavel J. et al. Pediatric Blood Cancer, 2004; Ph. Lanzkowsky, 2005).

эпидемиология В Республике Беларусь за период 1990 -2004 гг. общее количество лейкозов (de novo) зарегистрированных у детей (0 -14 лет)составило 1 117 случаев: ОЛЛ -878 случаев; ОМЛ -170 случаев; ОЛ (БДУ) и хронические лейкозы -69 случаев.

этиология и патогенез Источники повреждения клетки Внешний: • • • ионизирующая радиация; радиоактивные вещества химические факторы; лекарственные препараты вирусы Внутренний: генетические факторы повреждение ДНК клетки (мутации)

этиология и патогенез повреждение ДНК клетки (мутации) Репарация клетки Могут включиться механизмы апоптоза Клетка продолжает жить, производя себе подобных (клон)

роль апоптоза в лейкозогенезе Термин «апоптоз” (от греческого “опадание листьев”) был веден в 1972 г. Kerr для обозначения своеобразного механизма гибели клетки, отличного от некроза. При некрозе клетка разбухает, ее мембрана разрушается, лизосомальные ферменты выходят наружу, развивается воспаление. При апоптозе клетка сморщивается, хроматин конденсируется и фрагментируются, образуя апоптотические тельца и без воспалительной реакции остатки клетки фагоцитируются.

Downloaded from: Robbins & Cotran Pathologic Basis of Disease (on 3 March 2006 10: 35 PM) © 2005 Elsevier

Выявление апоптотических клеток Морфологическое исследование Флуоресцентная микроскопия Ж Ак Афр Ак – апоптотические клетки с конденсированным хроматином; Афр – фрагментированным хроматином; Ж – живые неапоптотические клетки.

биохимические основы апоптоза Существует система генов, «отправляющих» клетку в апоптоз и система генов, препятствующих этому процессу. Ген р53 - обеспечивает апоптоз клеток, подвергшихся действию радиации, цитостатиков и др. В злокачественных опухолях много клеток, с мутантным геном р53. Останавливает апоптоз ген Bcl-2 - он обеспечивает выживание клеток в отсутствии ростовых факторов.

биохимические основы апоптоза Участие механизма апоптоза в онкогенезе может реализоваться как по линии блокады клеточной гибели и предания мутировавшим клеткам «бессмертия» , так и по линии нарастания злокачественности за счет новых субклонов. Первый вариант – может быть реализован геном Bcl-2. Второй – геном р53.

К генетическим детерминантам клетки, вовлеченным в канцерогенез, можно отнести 1) протоонкогены — нормальные клеточные гены, участвующие в ключевых процессах жизнедеятельности клетки - регуляции транскрипции, роста, клеточного цикла, передаче сигнала и т. д. В случае структурных изменений или повышении уровня экспрессии этих генов нарушается контроль нормального клеточного роста и дифферцировки, что приводит к трансформации клетки. Такие активированные протоонкогены принято: называть онкогенами:

Известны три основных механизма активации протоонкогенов, которые обнаруживаются в опухолях человека: 1) мутации в первичной структуре протоонкогена; 2) амплификация (увеличение числа копий гена в ДНК клетки); 3) перестройка ДНК клетки, затрагивающая структуру протоонкогена. • В результате мутаций в структуре гена изменяется кодирующий белок, что отражается на его свойствах. • В результате амплификации наблюдается аномально высокая продукция кодируемого белка в клетках. • Превращение протоонкогена в активированный онкоген может быть следствием структурных перестроек клеточного генома.

Химерные гены и хромосомные перестройки BCR-ABL t(9; 22) (q 34; q 11) CML, B-lineage ALL TEL-AML 1 t(12; 21) (p 13; q 22) B-lineage ALL MLL-AF 4 t(4; 11) (q 21: q 23) Pro B-ALL PML-RARa t(15; 17) (q 21; q 22) AML M 3 CBFb-MYH 11 inv 16 (p 13; q 22) AML M 4 AML 1 -ETO t(8; 22) (q 24; q 11) AML M 2

патогенез • концепция онкогена, т. е. дискретного носителя генетической информации, который при определенных условиях способен вызывать трансформацию нормальной клетки, впервые в истории онкологии позволила объединить основные направления исследований канцерогенеза. • Практически все канцерогенные факторы (химические, физические, наследственные и т. д. ) в конечном итоге приводят к повреждению онкогенов (онкогенных генетических детерминант) и их функций.

патогенез • В основе патогенеза острых лейкозов лежит мутация стволовой клетки крови, что влечет за собой практически полную потерю потомками мутировавшей клетки способности к созреванию. • Мутантный клон автономен от каких-либо регулирующих воздействий организма и довольно быстро вытесняет нормальные гемопоэтические клетки, замещая собой весь гемопоэз.

Злокачественные свойства опухолевых клеток • Самодостаточность ростовых сигналов; • Не чувствительность к другим сигналам, ингибирующим рост (например: апоптоз); • Неограниченный пролиферативный потенциал (иммортальность); • Способность к ангиогенезу; • Инвазивный рост и метастазирование.

Законы опухолевой прогрессии • Бластные клетки при остром лейкозе теряют ферментную специфичность. • Клетки становятся морфологически и цитохимически недифференцируемыми. Они характеризуются: Ø Изменением ядра и цитоплазмы (вместо крупных появляются клетки неправильной формы с увеличением площади ядра и цитоплазмы; Ø Обладают способностью расти вне органов гемопоэза (пролифераты из лейкозных клеток находят в коже, почках, головном мозге и в мозговых оболочках), они неравноценны и представляют разные этапы прогрессии;

Классификация Острый лейкоз классифицируют на основании: Øморфологических; Øцитохимических; Øиммунологических; Ø цитогенетических; Ø молекулярных характеристик.

Классификация Франко-американо-британская (ФАБ) классификация 1. Острый лимфобластный лейкоз – L 1; L 2; L 3 2. Острый миелобластный лейкоз (М 0 - М 7): § § § § тип М 0 - острый миелобластный недифференцированный лейкоз; тип М 1 - острый миелобластный лейкоз без созревания; тип М 2 - острый миелобластный лейкоз с созреванием; тип М 3; М 3 v - острый промиелоцитарный лейкоз; тип М 4 ео; – острый миеломонобластный лейкоз; тип М 5 – острый монобластный лейкоз; тип М 6 – острый эритробластный лейкоз; тип М 7 – острый мегакариобластный лейкоз.

Морфологические характеристики лимфобластов и миелобластов Характеристики Размер Ядро Форма Хроматин Ядрышки Ядерная мембрана Соотношение ядро/цитоплазма Цитоплазма Цвет Количество Гранулы Палочки Ауэра Лимфобласты 10 -20 мкм круглая или овальная гладкий, гомогенный 0 -2, слабо выраженные гладкая, ровная высокое голубой тонкий ободок вокруг ядра отсутствуют Миелобласты 14 -20 мкм круглая или овальная губчатая, неплотная, тонкоорганизованн ая сетчатая структура 2 -5, отчетливые неровная невысокое сине-серый большое количество присутствуют

Цитологические признаки острого лимфобластного лейкоза Цитологические признаки Размер клеток Ядерный хроматин Форма ядра Ядрышки Количество цитоплазмы Базофилия цитоплазмы Количество вакуолей в L 1 L 2 L 3 Преобладают мелкие клетки Гомогенный почти во всех случаях Правильная, иногда зазубренной ядро Невидимые или мелкие и невыраженные Скудное Слабая или умеренная, редко- интенсивная Крупные клетки неодинакового размера В основном гетерогенный Неправильное, часто зазубренное ядро Одно или несколько часто больших размеров Разное, часто достаточно большое Различная, в отдельных случаях может быть интенсивной Различное Крупные клетки неодинакового размера Мелкозернистый, гомогенный Правильная округлая или овальная Выраженные, одна или несколько вакуолей Различное Умеренное Интенсивная Часто очень много

Иммунологическая характеристика острых лейкозов 1. Острые лимфобластные лейкозы (ОЛЛ) В-линейные: • В-I (про-В) ОЛЛ • B-II (сommon) ОЛЛ • B-III (пре-В) ОЛЛ • B-IV (зрелый В) ОЛЛ Т-линейные: • T-I (про-Т) ОЛЛ • T-II (пре-Т) ОЛЛ • T-III (кортикальный- Т) ОЛЛ • T-IV (зрелый –Т) ОЛЛ • T- и 2. Острые миелоидные лейкозы (ОМЛ) • • • Миеломоноцитарный Эритроидный (раннийнезрелый и зрелый) Мегакариоцитарный Низкодифференцированный миелоидный Tdt+ОМЛ с экспрессией одного или двух лимфоидных маркеров (лимфо+ОМЛ) 3. Бифенотипические ОЛ 4. Недифференцированные ОЛ

Клиника острого лейкоза Симптоматика ОЛ может быть различной, но основная клиническая картина складывается из 4 -х основных синдромов: ØГиперпластический; ØАнемический; ØГеморрагический; ØИнтоксикационный.

Клиника острого лейкоза I. Гиперпластический синдром. Обусловлен инфильтрацией бластными клетками ЛУ, печени, селезенки, почек, миокарда, легких и т. д. 1) ЛАП – может быть регионарной или генерализованной. • увеличенный ЛУ плотные, безболезненные, при пальпации, не спаяны между собой и окружающими тканями; • чаще увеличиваются задне- и переднешейные и подчелюстные ЛУ, реже - паховые, подмышечные. Могут увеличиваться ЛУ средостения. 2) гиперплазия миндалин, десен, язвенно-некротические изменения в полости рта (характерно для ОМЛ) – обусловлена инфильтрацией бластными клетками подслизистого слоя. 3) лейкемиды –инфильтраты бластных клеток в дерме в виде красновато - синеватых папулообразных бляшек.

Клиника острого лейкоза

Клиника острого лейкоза

Клиника острого лейкоза

Клиника острого лейкоза 4) гепатомегалия; 5) спленомегалия; 6) поражение почек (гематурия, гипертензия, почечная недостаточность; 7) поражение сердца (менее 5% лейкемическими бластами или кровоизлияниями в миокард, перикард); 8) поражение легких; 9)поражение яичек и яичников; 10)боли в костях (оссалгии) –обусловлено прорастанием бластных клеток в поднадкостницу и костно-мозговые полости с разрушением компактного вещества кости: Øостеопороз кортикальных и мозговых отделов; Øпатологические переломы; Øсубпериостальные костные образования.

Клиника острого лейкоза 11) поражение ЦНС- синдром нейролейкоза (у 5% больных) – обусловлен диффузной инфильтрацией бластными клетками вещества мозга и оболочек мозга (занос через ГЭБ). Клинически проявляется: Ø Ø Ø Ø головной болью; тошнотой; рвотой; повышением АД; головокружением; нарушением походки; зрения В зависимости от локализации и характера лейкозного поражения ЦНС различают: 1. 2. 3. 4. менингоэнцефалический синдром; (69%) расстройство функции черепно-мозговых нервов (22%); локальное поражение в-ва головного мозга (4, 5%); поражение периферических нервов – полирадикулопатия (4, 5%)

Клиника острого лейкоза II. Анемический синдром. Лейкозная гиперплазия и инфильтрация костного мозга приводит к угнетению нормального кроветворения. В клинической картине –бледность кожи и слизистых, систолический шум на верхушке, тахикардия. В ОАК – анемия, нормохромная, нормоцитарная. Уровень гемоглобина- различный (у 20% детей с ОЛЛ гемоглобин менее 60 г/л). III. Геморрагический синдром. В клинической картине: Øпетехеально-пятнистый тип кровоточивости (экхимозы, петехии); Øкровотечения (носовые, десневые, маточные, почечные). В ОАК- тромбоцитопения. IV. Интоксикационный синдром. Обусловлен лизисом бластных клеток. В клинической картине: ØПовышение температуры тела (у 60% больных); ØВялость (у 50% больных); ØСнижение аппетита

Клиника острого лейкоза

Стадии острого лейкоза 1. Начальная стадия (латентный период) – идет нарастание опухолевой • • • массы, а явной клинической картины нет. Этот период занимает от 3 до 6 мес. могут появиться изменения в ПК: анемия; лейкопения (лейкоцитоз); нейтропения. 2. Стадия развернутых клинических проявлений. 3. Стадия ремиссии. Полная клинико-гематологическая ремиссия: • полная нормализация клинической симптоматики (нет ЛАП, гепатоспленомегалии и т. д. ); • отсутствие симптомов нейролейкоза (нет симптомов поражения ЦНС и бластов в ликворе); • нормализация анализов ПК (отсутствие бластных клеток, гранулоциты более 500 в мкм 3 , тромбоциты более 75 х109л, Ни более 110 г/л; • костный мозг: количество бластов менее 5%, клеточность норма или снижена, восстановление 3 -х ростков кроветворения.

Стадии острого лейкоза 4. Стадия выздоровления - это состояние полной клинико-гематологической ремиссии на протяжении 5 лет и отсутствие признаков минимальной резидуальной болезни. 5. Рецидив заболевания – обусловлен возвратом опухолевого процесса к прежним показателям в результате выхода остаточной лейкозной популяции в митотический цикл. Различают рецидивы: а) изолированные Øкостно-мозговой; Øнейролейкоз; Øтестикулярный. б) комбинированные Øкостно-мозговой + нейролейкоз; Øкостно-мозговой + тестикулярный; Øкостно-мозговой + нейролейкоз +тестикулярный. Ранние рецидивы –до 6 мес. от начала терапии и поздние рецидивы – свыше 6 мес. от начала терапии.

Стадии острого лейкоза 6. Терминальная стадия - это некурабельный этап лейкоза. Он характеризуется: Øнеэффективностью ПХТ; Øпрогрессированием лейкоза; Øистощением нормального кроветворения.

Диагностика ОЛ основывается на: • • • данных анамнеза; данных клинического обследования; результатов лабораторно- инструментального обследования. I. 1. 2. ОАК: анемия, нормохромная , нормоцитарная, у 85% детей уровень Нв ниже 100 гл, количество Rt снижено; лейкопения менее 4 х10 9/л - у 20%, а лейкоцитоз более 10 х109/л - у 50% детей. Может быть наличие бластных клеток (лейкемический вариант), или их отсутствие (алейкемический вариант). Однако необходимо отметить, что гематологические характеристики при ОЛЛ могут быть крайне разнообразны. 3. тромбоцитопения. II. Миелограмма: • наличие бластов более 25%; • количество миелокариоцитов повышено. • соотношение лейкоэритро- 10: 1 • угнетение нормальных ростков гемопоэза.

Острый лимфобластный лейкоз
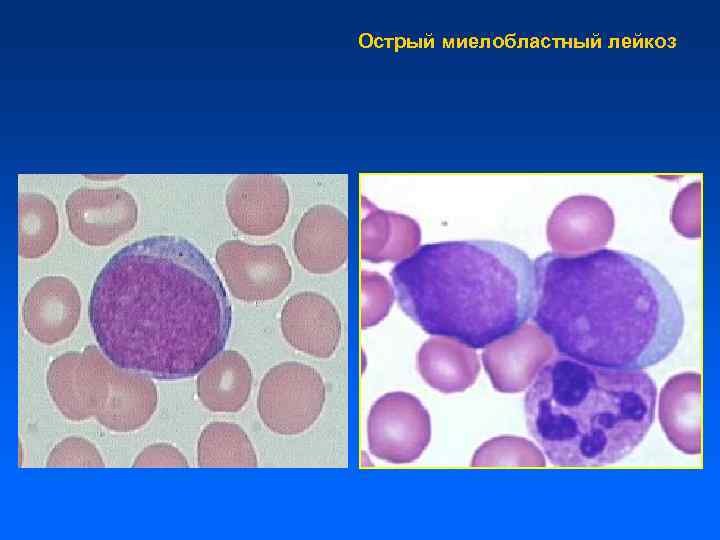
Острый миелобластный лейкоз

Диагностика ОЛ ОМЛ –палочки Ауэра
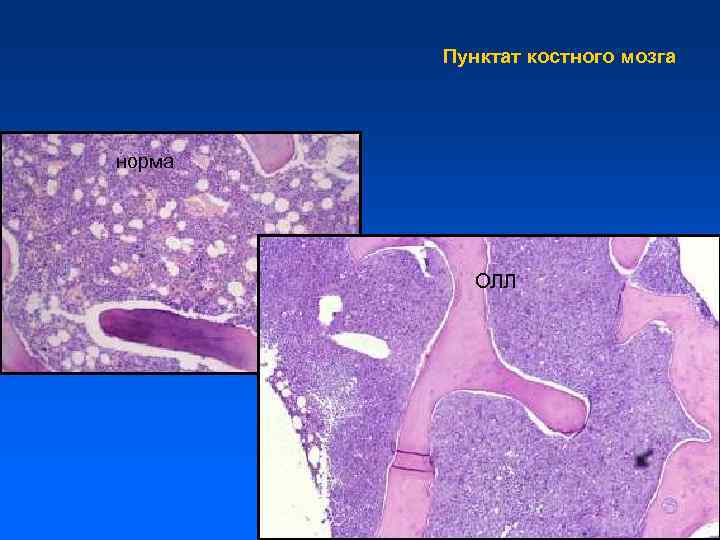
Пунктат костного мозга норма ОЛЛ

Диагностика ОЛ III. Цитохимические исследования – метод основан на химическом анализе лейкозных клеток, отражающий особенности их метаболизма и выявляющий определенные субстанции в различных клеточных элементах

Цитохимические признаки острых лейкозов Методы окраски Неферментн ые Крупные гранулы или скопления гранул Судан черный (на липиды) α- нафтилацет атэстераза кислая фофатаза ОМЛ (М 6) ОМЛ (М 7) Грануляция отсутствует или диффузно Отсутствие грануляции или мелкие гранулы Резко положитель ная зернистая грануляция положительн ая Ферментны е Окраска на пероксидаз у ОМЛ (М 4) PAS (реакция на гликоген) ОМЛ ОЛЛ + при ТОЛЛ + + - + Сильно + - +/ +- +

Реакция на гликоген в лимфобластах

Реакция на гликоген в миелобластах

Реакция на липиды в миелобластах

Реакция на миелопероксидазу

Неспецифическая эстераза без ингибирования фторидом натрия

Неспецифическая эстераза с ингибированием фторидом натрия

Диагностика ОЛ IV. Иммунофенотипирование- метод иммунологического фенотипирования позволяет по поверхностным дифференцировочным антигенам и по внутриклеточным маркерам уточнить тип лейкозной клетки и определить стадию дифференцировки, на которой произошло развитие лейкоза. Иммунофенотипы ОЛ Миелоидные- CD 13, CD 33, CD 117 • B-линейные CD 10, CD 19, CD 20, CD 22, иммуноглобулины • T линейные- CD 1, CD 2, CD 3, CD 4, CD 5, CD 7, CD 8 • Ранние предшественники- CD 34, Td. T

Диагностика ОЛ V. Цитогенетические исследования. VI. Молекулярно-биологическое исследование.

Диагностика ОЛ Общие цитогенетические нарушения при ОЛЛ t(1; 19) E 2 A-PBX 1 Pre-B t (4; 11) AF 4 -MLL CD 10 отр. B cell t(8; 14) MYC-Ig genes B-cell, L 3 (100%) t(9; 22) BCR-ABL mixed lineage t(12; 21) TEL-AML 1 pre-B +4, +10* Unknown pre-B, гиперплоидность t(1; 14) TAL 1 -T cell receptor T-cell

Диагностика ОЛ VII. Биохимический анализ крови (уровень мочевой кислоты, Са, К, фосфаты, мочевина, АСТ, АЛТ и маркеры опухолевого процесса -ЛДГ, ЩФ). VIII. Исследование ликвора – (норма : цитоз менее 5 мм 3 , нет бластов). IX. Исследование свертывающей система крови (при ОМЛ часто возникает гипофибриногенемия и снижение уровня факторов V, IX, X. Рентгенография органов грудной клетки. XI. УЗИ органов брюшной полости. XII. Исследование функции сердца (ЭКГ и УЗИ сердца). XIII. Вирусологическое исследование крови (титр антител к ЦМВ, вирус простого герпеса, вирусам гепатита). XIV. ОАМ. XV. Бак. посевы с кожи и слизистых оболочек.

Лечение острых лейкозов • В истории лечения ОЛ выделен 1948 год, когда S. Farber впервые применив антагонист фолиевой кислоты аметоптерин (метотрексат) добился ремиссии у ребенка, страдающего ОЛ. До этого времени основным в лечении ОЛ была симптоматическая терапия, при которой продолжительность жизни составляла 4 -6 мес. • Введение в клиническую практику цитостатических средств положило начало активной химиотерапии ОЛ. • Точка приложения цитостатического действия химиопрепаратов- внутриклеточный обмен лейкозной клетки, а также нарушение или прекращение синтеза важных субстанций.

Лечение острых лейкозов • С позиций клеточной кинетики все химиотерапевтические препараты делятся на 2 группы. • 1 группа - это химические агенты, специфически действующие на клеточный цикл (циклоспецифичные). Они могут действовать на одну или несколько фаз. На фазу S действуют, т. е активны в отношении пролиферирующих клеток: цитозар, 6 -МР, винкристин и др. • 2 группа – это химические вещества, действие которых проявляется независимо от клеточного цикла (нециклоспецифичные). Это противоопухолевые антибиотики, алкилирующие соединения. Эти препараты вызывают гибель опухолевых клеток в фазе покоя G 0. • При ПХТ комбинируют циклоспецифичные нециклоспецифичные препараты, чтобы охватить лейкозные клетки во всех фазах клеточного цикла и в состоянии покоя.

Противолейкозные препараты. Применяемые противолейкозые препараты делят на 6 групп: 1. Антиметаболиты – нарушают синтез предшественников нуклеиновых 2. 3. 4. 5. 6. кислот, путем конкуренции с последними в лейкозной клетке (метотрексат, тиогуанин, 6 -меркаптопурин, цитозар); Алкилирующие соединения- подавляют синтез ДНК и в меньшей степени РНК лейкозной клетки (циклофосфан) Алкалоиды растений – винкристин действует на все фазы покоящейся клетки; этопозид (VP-16) из растений мандрагоры, предотвращает вхождение клетки в митоз. Ферментные препараты- аспаргиназа разлагает аспаргин, необходимый для синтеза протеина на аспаргиновую кислоту и аммоний в лейкозной клетке, которая не способна к самостоятельному синтезу аспаргина и поэтому погибает от его эндогенного дефицита. Противоопухолевые антибиотики - адриамицин, рубомицин – обладают цитостатическим действием, подавляет синтез нуклеиновых кислот путем взаимодействия с ДНК и РНК – полимеразами. Гормональные препараты. Преднизолон – обладает цитолитическим действием на лейкозные клетки (лимфобласты и недифференцируемые бласты) и не вызывает разрушения нормальных лимфоцитов.

Современная терапия острого лейкоза состоит из нескольких этапов: 1. Этап – индукция ремиссии – период от разгара до полной клиникогематологической ремиссии. 2. Этап – консолидация ремиссии (укрепление) – дополнительный курс ПХТ, направленный на уничтожение внекостно-мозговых инфильтратов. 3. Этап –поддерживающая терапия. Наиболее стабильными в течении последних 20 лет являются программы лечения (протоколы), включающие ПХТ, лучевую терапию и ТКМ (при ОМЛ).


Диагноз ОМЛ Промежуточный риск t(9; 11) Inv 16 ADE+HDAra. C+VP Capizzi Высокий риск ADE-HAM CLAE HDAra. C 4+Ida 3 Capizzi+VP t(8; 21) без а/м, донора нет AME-H (4 дн) Capizzi Донор есть Алло ТГСК

Стратификация пациентов на группы риска Стандартный риск • Inv 16 • t(9; 11) Промежуточный риск • t(8; 21) без активирующей мутации c-kit с бластозом < 15% на 15 -й день • Нормальный кариотип без flt-3 ITD • отсутствие кариотипических и молекулярно-биологических критериев высокого риска Высокий риск • Нормальный кариотип с flt-3 ITD и без NРМ(+) • 11 q 23 аномалии (особенно t(6; 11) и t(10; 11) • inv 3, t(3; 3), сложные аномалии (>3 аномалий) • t(8; 21) с активирующей мутацией c-kit • моносомия 7 • моносомия 5 • ОМЛ с мультилинейной дисплазией • М 7


p<0. 01

ОЛ новое.ppt