Аминокислоты.pptx
- Количество слайдов: 34


Определение Аминокислоты – бифункциональные соединения, которые обязательно содержат две функциональные группы: аминогруппу – NH 2 и карбоксильную группу – COOH, связанные с углеводородным радикалом Аминокислоты – производные кислот, которые можно рассматривать как продукты замещения одного или более атомов водорода в их радикалах на одну или более аминогрупп
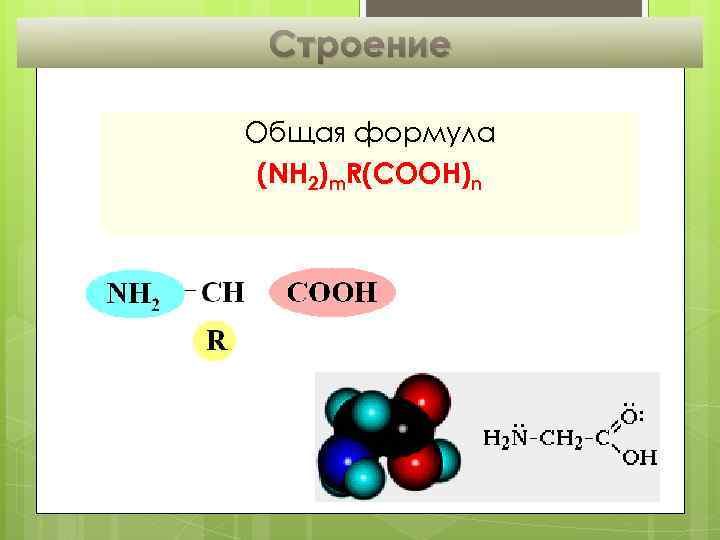
Строение Общая формула (NH 2)m. R(COOH)n
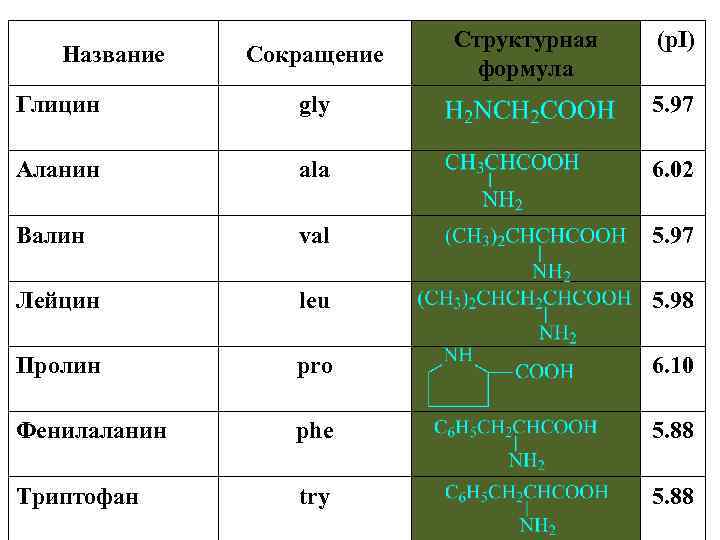
Название Сокращение Структурная формула (p. I) Глицин gly 5. 97 Аланин ala 6. 02 Валин val 5. 97 Лейцин leu 5. 98 Пролин pro 6. 10 Фенилаланин phe 5. 88 Триптофан try 5. 88 4
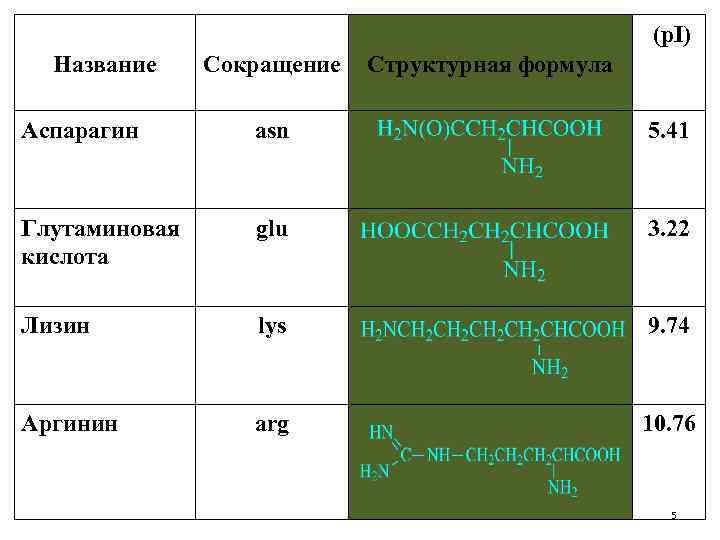
(p. I) Название Сокращение Структурная формула Аспарагин asn 5. 41 Глутаминовая кислота glu 3. 22 Лизин lys 9. 74 Аргинин arg 10. 76 5
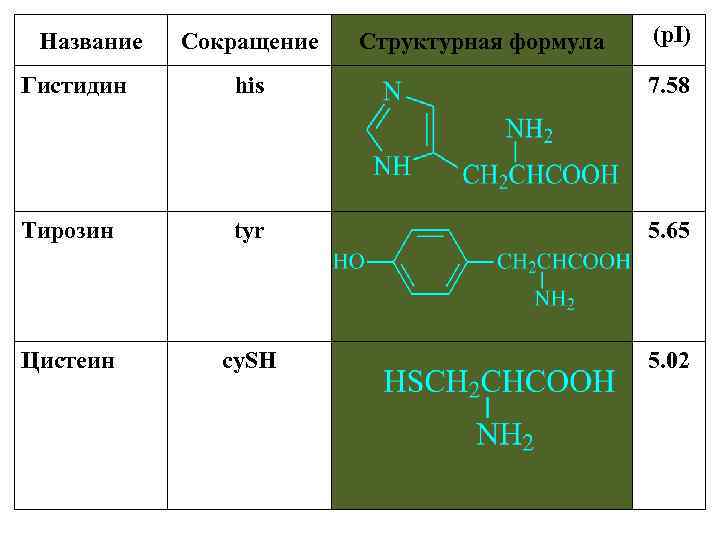
Название Сокращение Структурная формула (p. I) Гистидин his 7. 58 Тирозин tyr 5. 65 Цистеин cy. SH 5. 02 6

Классификация Классификация АК по природе радикала: 1). алифатические (гли, ала, вал, лей, иле и. т. д. ); 2). ароматические (фен, тир, три, гис); 3). гетероциклические (про, оксипро). Классификация АК по количеству карбоксильных и аминогрупп: 1). нейтральные; 2). кислые (глу, асп); 3) основные (арг, лиз). Классификация АК по функциональным группам в радикале: 1). содержащие –ОН (сер, тре); 2). содержащие –SH (цис, мет); 3). содержащие –СОNH 2 (глн, асн); Классификация АК по способности к синтезу: 1. АК, которые синтезируются в организме, называют заменимыми (глицин, аспарагиновая кислота, аспарагин, глутаминовая кислота, глутамин, серин, пролин, аланин). 2. АК, которые не синтезируются в организме, но для него необходимы, называются незаменимыми (фенилаланин, метионин, треонин, триптофан, валин, лизин, лейцин, изолейцин). 3. Аргинин и гистидин частично заменимые АК, у взрослых они образуются в достаточных количе ствах, а у детей нет. Поэтому, необходимо дополнительное поступление этих АК с пищей. 4. Тирозин и цистеин — условно заме нимые так как для их синтеза , необходимы незаменимые АК (фенилаланин и метионин).

По взаимному расположению карбоксильной и аминогруппы α –аминокислоты, β – аминокислоты, γаминокислоты, δ – аминокислоты, ε – аминокислоты и т. д.
По строению углеводородного радикала Предельные Непредельные Циклические Ароматические

Аминокислоты делят на: Природные Их около 150, они были обнаружены в живых организмах, около 20 из них входят в состав белков. Половина этих аминокислот – незаменимые (не синтезируются в организме человека), они поступают с пищей. Синтетические Получают кислотным гидролизом белков, либо из карбоновых кислот, воздействуя на них галогенном и, далее, аммиаком.

Систематическая номенклатура выбрать самую длинную цепь содержащую карбоксильную группу и аминогруппу; 2. пронумеровать начиная с углерода карбоксильной группы; 3. Место (NH 2) – амино – что – овая кислота Например: 2 аминопропановая кислота 1.

Рациональная номенклатура По рациональной номенклатуре положение аминогруппы указывается буквами греческого алфавита, начиная со второго атома углерода от СООН: α, β, γ, δ, ε и т. д. Например: α – аминопропионовая кислота

Тривиальные названия Многие аминокислоты имеют тривиальные названия, например: Аланин

Физические свойства Аминокислоты – бесцветные кристаллические вещества с высокими температурами плавления. Плавятся с разложением, нелетучие. Хорошо растворимы в воде и плохо растворимы во многих органических растворителях. Водные растворы электропроводны В большинстве аминокислоты D ряда сладкие на вкус, L ряда горькие или безвкусные.
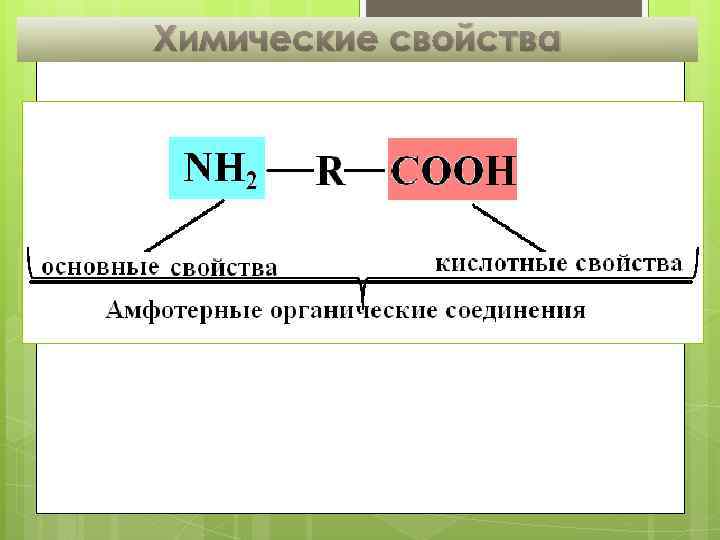
Химические свойства

Амфотерность Все аминокислоты — амфотерные соединения, они могут проявлять как кислотные свойства, обусловленные наличием в их молекулах карбоксильной группы —COOH, так и основные свойства, обусловленные наличием аминогруппы —NH 2. Аминокислоты реагируют как с кислотами, так и с основаниями: H 2 N–CH 2–COOH + HCl → [H 3 N+–CH 2–COOH] Cl (хлороводородная соль глицина) NH 2 —COOH + Na. OH → H 2 O + NH 2 —CH 2 — COONa (натриевая соль глицина)

Цвиттер ион При растворении аминокислот в воде карбоксильная группа отщепляет ион водорода, который может присоединиться к аминогруппе. Благодаря этому растворы аминокислот в воде обладают свойствами буферных растворов, то есть образуется внутренняя соль, молекула которой представляет собой биполярный ион (цвиттер ион):

Реакции аминогруппы Подобно первичным аминам, аминокислоты реагируют с азо тистойкислотой (дезаминирование), при этом аминогруппа превращается в гидроксогруппу, а аминокислота — в гидроксикислоту: Измерение объема выделившегося азота позволяет определить количество аминокислоты (метод Ван Слайка).

Реакции карбоксильной группы Аминокислоты могут реагировать со спиртами в присутствии газообразного хлороводорода, превращаясь в сложный эфир (точнее, в хлороводородную соль эфира):

Реакции карбоксильной группы Реакция с активными металлами Mg + 2 NH 2 – COOH → (NH 2 – COO)2 Mg + H 2 Глицинат магния 2 Na + 2 NH 2 – COOH → 2 NH 2 – COONa + H 2 Глицинат натрия
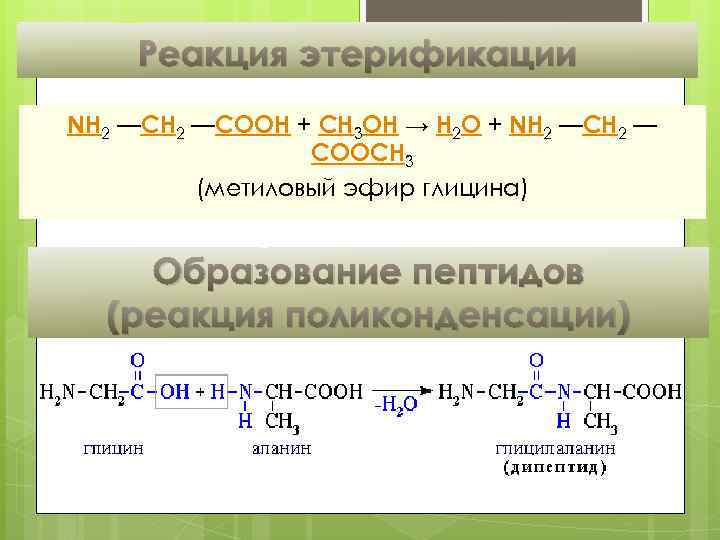
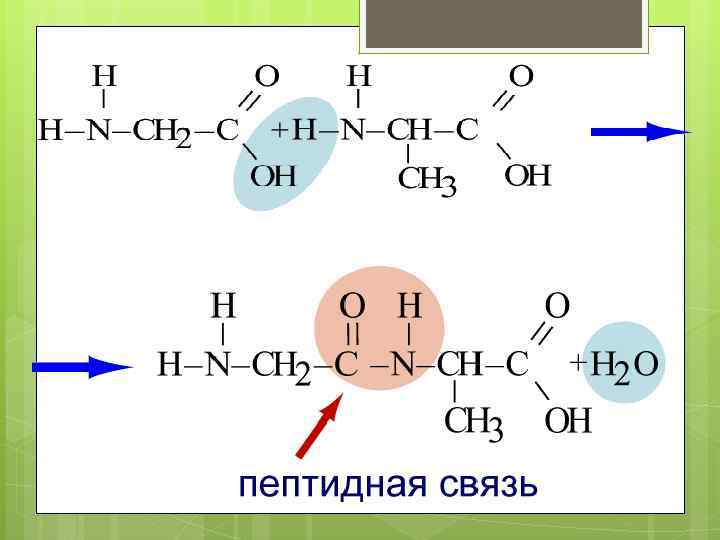
Реакция этерификации NH 2 —COOH + CH 3 OH → H 2 O + NH 2 —CH 2 — COOCH 3 (метиловый эфир глицина) Образование пептидов (реакция поликонденсации)
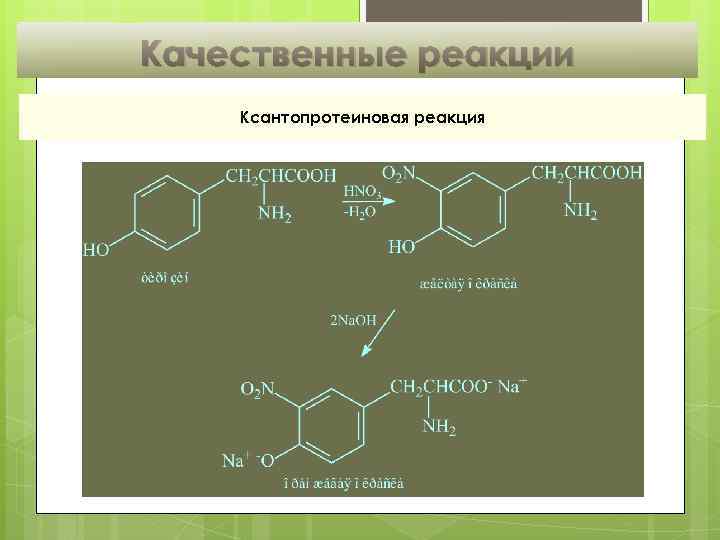
Качественные реакции Ксантопротеиновая реакция
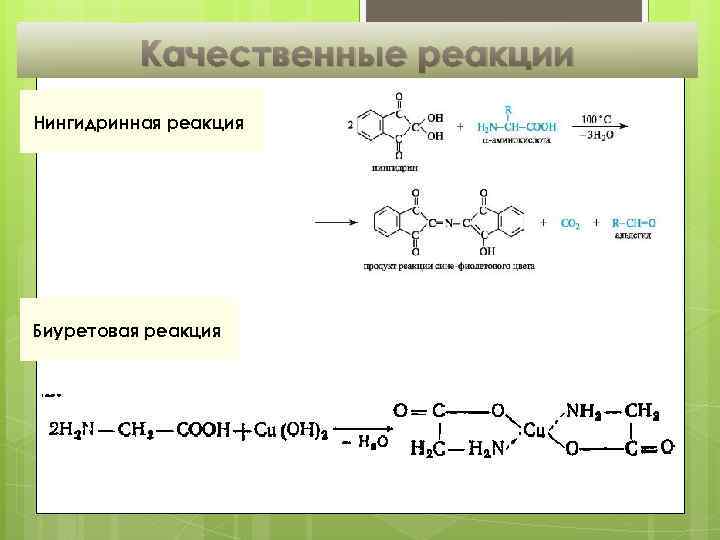
Качественные реакции Нингидринная реакция Биуретовая реакция
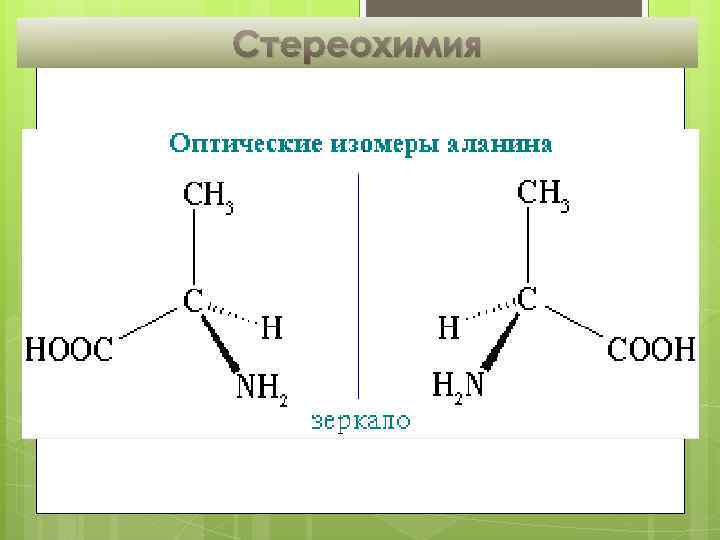
Стереохимия
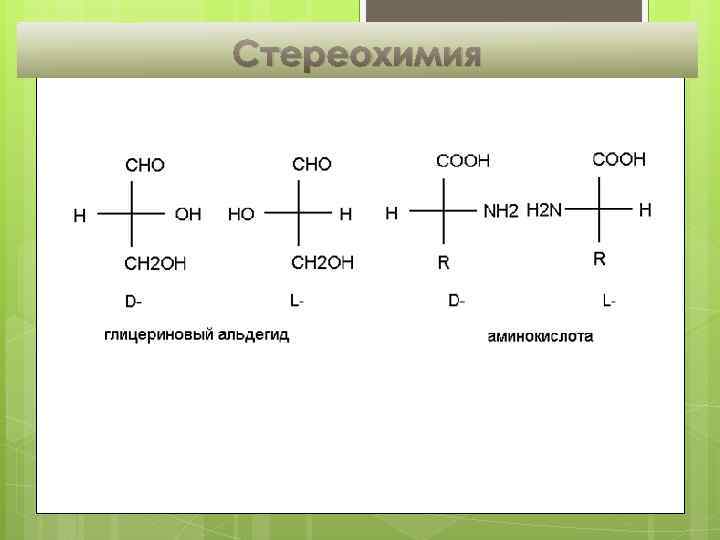
Стереохимия
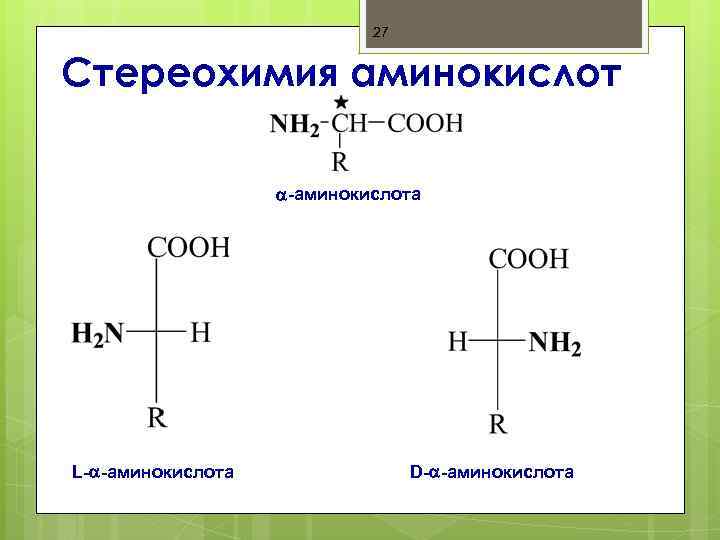
27 Стереохимия аминокислот -аминокислота L- -аминокислота D- -аминокислота
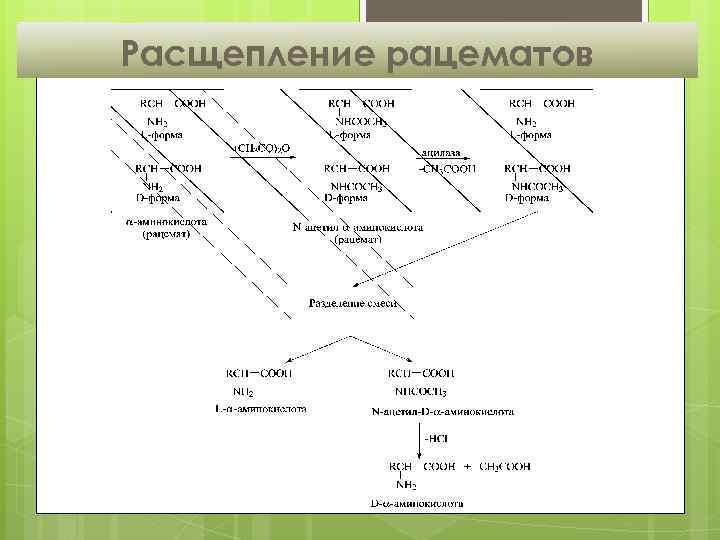
Расщепление рацематов
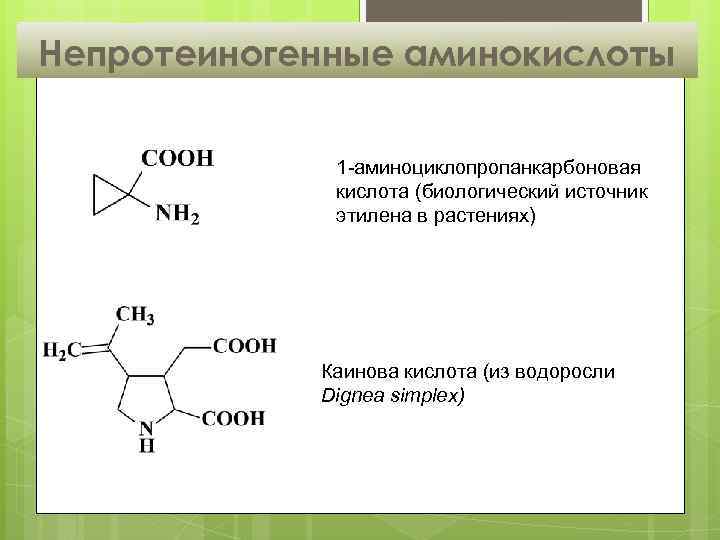
Непротеиногенные аминокислоты 1 -аминоциклопропанкарбоновая кислота (биологический источник этилена в растениях) Каинова кислота (из водоросли Dignea simplex)
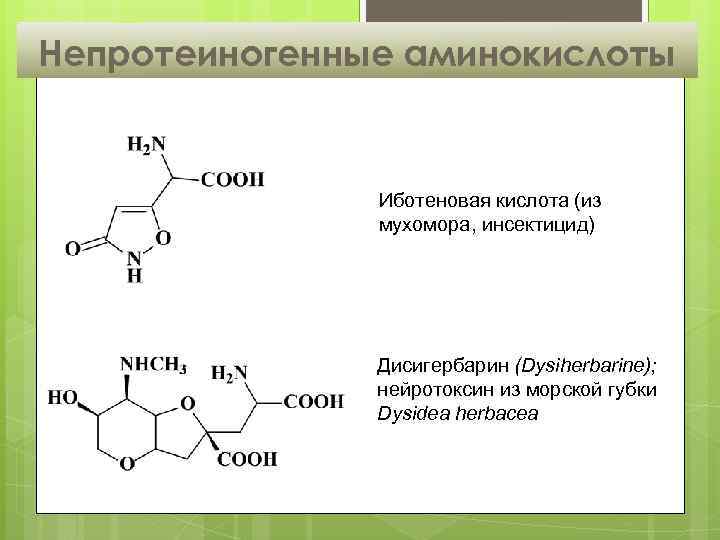
Непротеиногенные аминокислоты Иботеновая кислота (из мухомора, инсектицид) Дисигербарин (Dysiherbarine); нейротоксин из морской губки Dysidea herbacea

Аминокислоты Классификация АК по способности к синтезу: 1. АК, которые синтезируются в организме, называют заменимыми (глицин, аспарагиновая кислота, аспарагин, глутаминовая кислота, глутамин, серин, пролин, аланин). 2. АК, которые не синтезируются в организме, но для него необходимы, называются незаменимыми (фенилаланин, метионин, треонин, триптофан, валин, лизин, лейцин, изолейцин). 3. Аргинин и гистидин частично заменимые АК, у взрослых они образуются в достаточных количе ствах, а у детей нет. Поэтому, необходимо дополнительное поступление этих АК с пищей. 4. Тирозин и цистеин — условно заме нимые так как для их , синтеза необходимы незаменимые АК (фенилаланин и метионин).
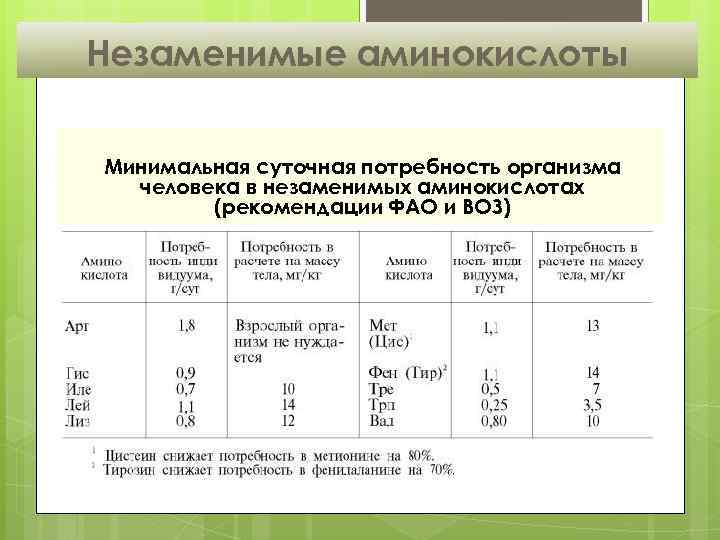
Незаменимые аминокислоты Минимальная суточная потребность организма человека в незаменимых аминокислотах (рекомендации ФАО и ВОЗ)

Спасибо за внимание!
Аминокислоты.pptx