ЭУ Гальванический элемент.ppt
- Количество слайдов: 26

Омский государственный технический университет Кафедра «Химия» Шубенкова Е. Г. Общая химия Химические источники тока. Гальванический элемент. Мультимедийная слайд-лекция ©Ом. ГТУ, 2014

Химические источники тока. Гальванический элемент.

Электрохимические процессы Процессы взаимного превращения химической и электрической форм энергии в системах, состоящих из электродов и электролитов. o Процессы превращения химической энергии в электрическую Гальванический элемент o Процессы превращения электрической энергии в химическую Электролизеры
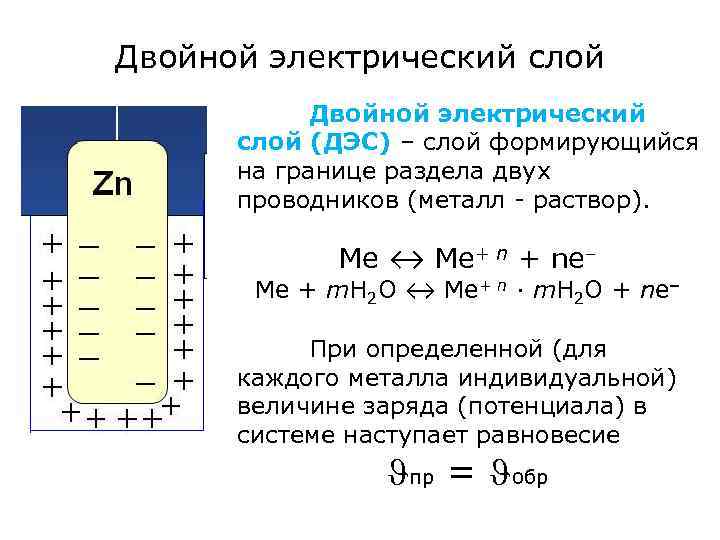
Двойной электрический слой (ДЭС) – слой формирующийся на границе раздела двух проводников (металл - раствор). Me ↔ Me+ n + ne– Me + m. H 2 O ↔ Me+ n ∙ m. H 2 O + ne– При определенной (для каждого металла индивидуальной) величине заряда (потенциала) в системе наступает равновесие пр = обр
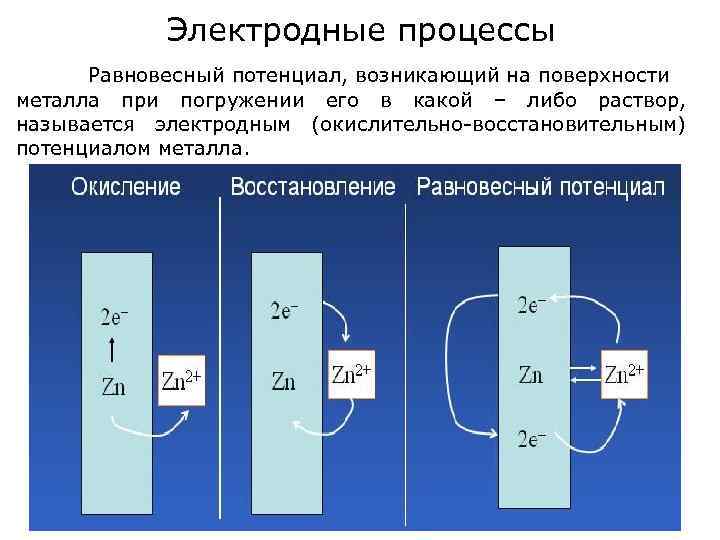
Электродные процессы Равновесный потенциал, возникающий на поверхности металла при погружении его в какой – либо раствор, называется электродным (окислительно-восстановительным) потенциалом металла.
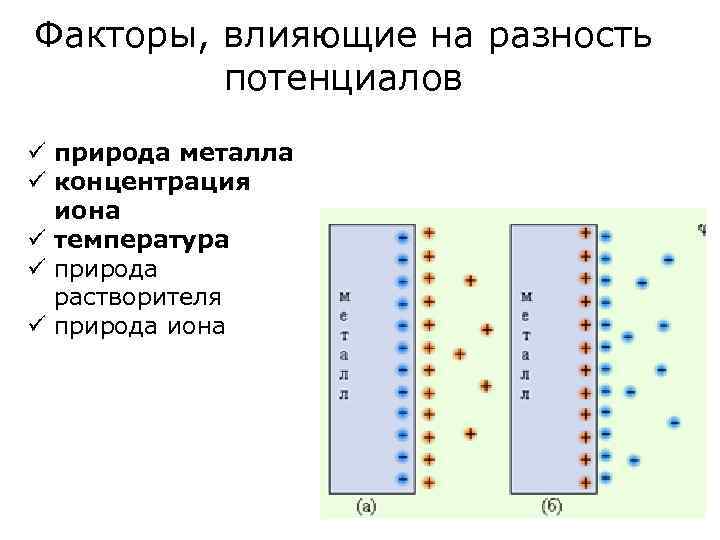
Факторы, влияющие на разность потенциалов ü природа металла ü концентрация иона ü температура ü природа растворителя ü природа иона
![Стандартный водородный электрод Водородный электрод, находящийся при стандартных условиях ([Н+] = 1 моль/л, Р Стандартный водородный электрод Водородный электрод, находящийся при стандартных условиях ([Н+] = 1 моль/л, Р](https://present5.com/presentation/3/257308262_335581466.pdf-img/257308262_335581466.pdf-7.jpg)
Стандартный водородный электрод Водородный электрод, находящийся при стандартных условиях ([Н+] = 1 моль/л, Р 0 H 2 = 101, 3 к. Па), называют стандартным водородным электродом, а потенциал такого электрода условно принят за ноль при любой температуре. Запись водородного электрода: Pt, H 2/H 2 SO 4. Равновесный потенциал электрода при стандартных условиях, измеренный относительно стандартного водородного электрода, носит название стандартного электродного потенциала и обозначается Е 0.
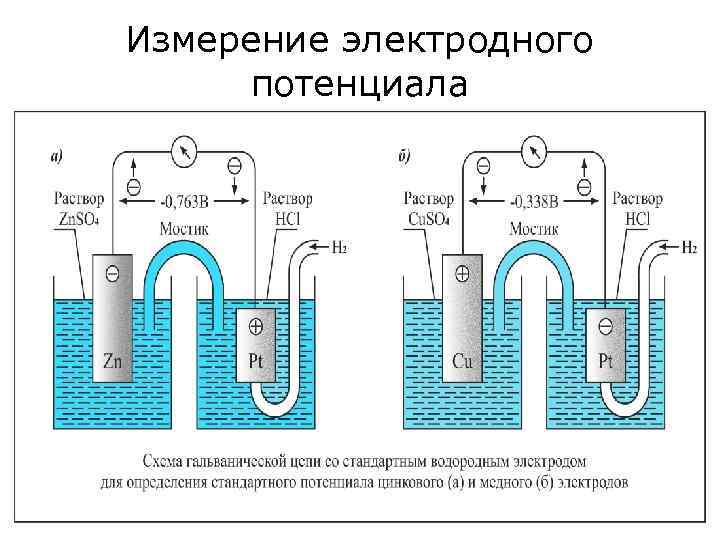
Измерение электродного потенциала

Стандартный электродный потенциал Стандартный электродный (окислительновосстановительный) потенциал – это разность потенциалов в гальваническом элементе, образованном металлом, погруженным в раствор соли с концентрацией ионов этого металла 1 моль/л и водородным электродом в стандартных условиях (Т = 298 К, Р = 105 Па, Ссоли = 1 моль/л). Стандартный электродный потенциал металла – справочная величина
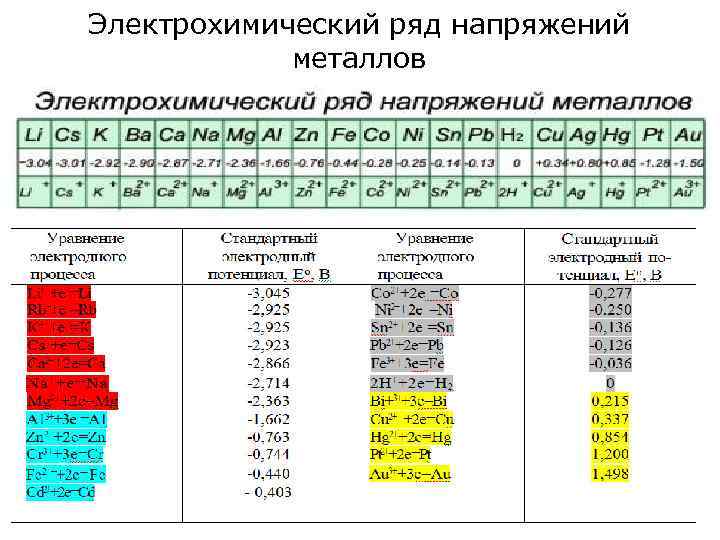
Электрохимический ряд напряжений металлов

Закономерности ряда напряжений металлов Металлы, стоящие в ряду напряжений условно делят на три группы: Активные металлы – от Li до Al включительно; Металлы средней активности – от Al до Н; Малоактивные металлы – после Н. Чем левее расположен металл, тем он активнее, легче окисляется, обладает большей восстановительной способностью (и наоборот). ü Металлы расположенные в ряду левее водорода, вытесняют водород из разбавленных кислот. ü Металлы, расположенные в ряду напряжений левее, вытесняют последующие металлы из растворов их солей. ü

Уравнение Нернста Для вычисления электродных потенциалов в условиях, отличных от стандартных, используют уравнение Нернста: Е — электродный потенциал металла, В; Е 0— стандартный электродный потенциал металла, В; R— универсальная газовая постоянная, равная 8, 31 Дж/(моль·K); T — абсолютная температура, К; F — постоянная Фарадея, равная 96485, 35 Кл/моль; n — число электронов, участвующих в процессе; [Ox] и [Red] — молярные концентрации окисленной и восстановленной форм металла, моль/л.

Уравнение Нернста в практических расчетах Реакция: Me ↔ Me+ n + ne– Me+ n - окисленная форма, Me – восстановленная форма. Т. к. металлы – твердые вещества, то концентрация восстановленной формы в уравнении Нернста равна 1 ([Red] = 1). Уравнение Нернста принимает вид: ЕMеn+/Mе = Е 0 Mеn+/Mе + (RT/n∙F)lg[Men+] или, после объединения и вычисления всех констант (RT/F): ЕMеn+/Mе = Е 0 Mеn+/Mе + (0, 059/n)lg[Men+] В стандартных условиях, когда [Men+]=1 (следовательно lg[Men+]=0) ЕMеn+/Mе = Е 0 Mеn+/Mе

Гальванический элемент – это устройство в котором за счет протекания электрохимических (окислительно-восстановительных) реакций возникает электрический ток. Устройство в котором химическая энергия окислительно-восстановительной реакции превращается в электрическую за счет пространственного разделения процессов окисления и восстановления.

История гальванического элемента
Электрический ток – упорядоченное движение заряженных частиц.
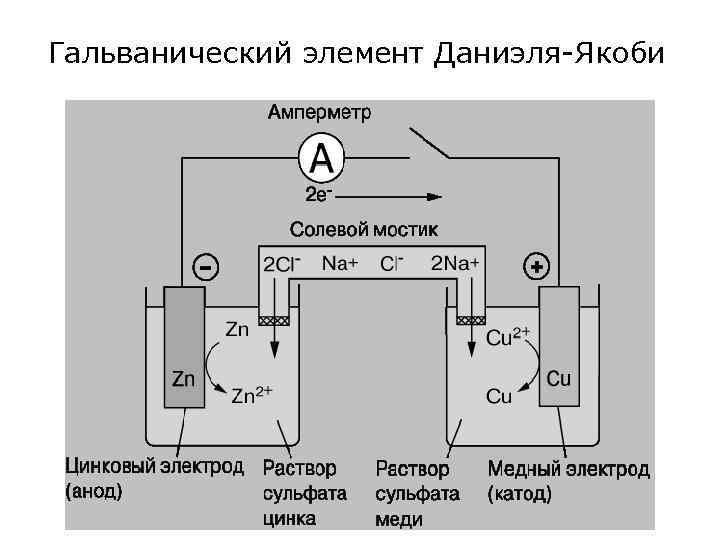
Гальванический элемент Даниэля-Якоби
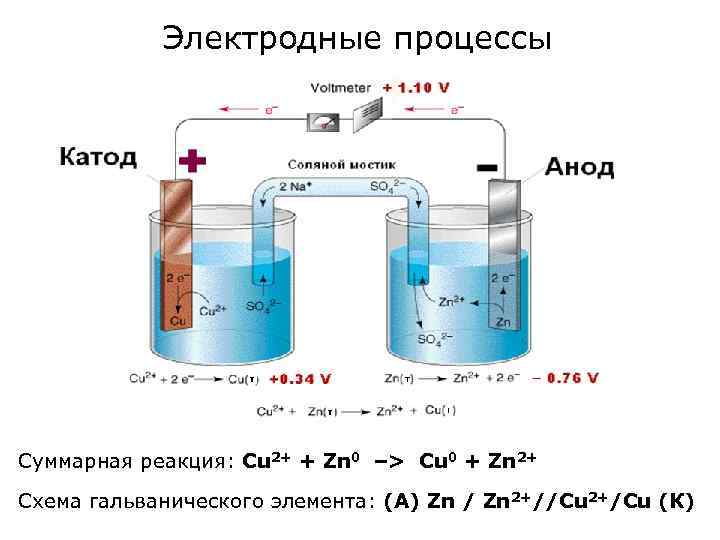
Электродные процессы Суммарная реакция: Сu 2+ + Zn 0 –> Сu 0 + Zn 2+ Схема гальванического элемента: (А) Zn / Zn 2+//Cu 2+/Cu (К)

ЭДС гальванического элемента Максимальная разность потенциалов, возникающая при обратимой работе гальванического элемента, есть электродвижущая сила (ЭДС) гальванического элемента. ЭДС = Екатода – Еанода > 0! Для элемента Даниэля–Якоби (СMen+ = 1 моль/л, стандартные условия): ЕZn 2+/Zn = Е 0 Zn 2+/Zn + (0, 059/n) lg 1 = Е 0 Zn 2+/Zn = - 0, 76 В (Анод) ЕCu 2+/Cu =Е 0 Cu 2+/Cu + (0, 059/n) lg 1 = Е 0 Cu 2+/Cu = + 0, 34 В (Катод) ЭДС = Е 0 Cu 2+/Cu - Е 0 Zn 2+/Zn = 0, 34 – (- 0, 76) = 1, 1 В
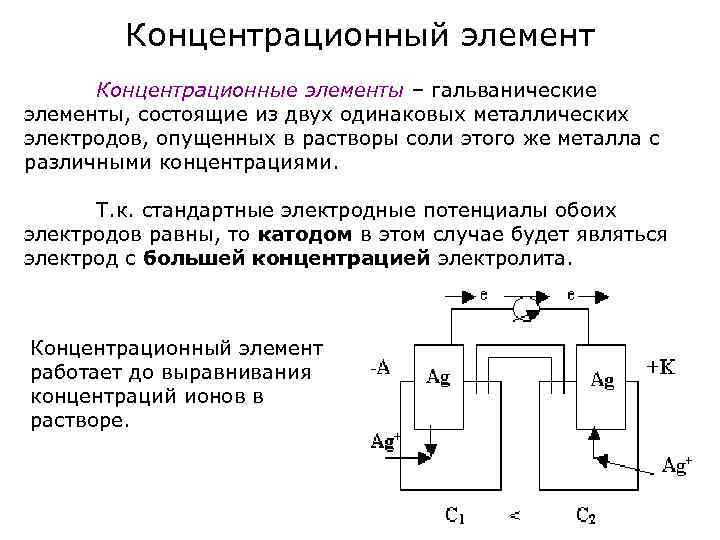
Концентрационный элемент Концентрационные элементы – гальванические элементы, состоящие из двух одинаковых металлических электродов, опущенных в растворы соли этого же металла с различными концентрациями. Т. к. стандартные электродные потенциалы обоих электродов равны, то катодом в этом случае будет являться электрод с большей концентрацией электролита. Концентрационный элемент работает до выравнивания концентраций ионов в растворе.

Источники автономного питания Представляют собой одиночный гальванический элемент, несколько гальванических элементов объединенных между собой в батарею, аккумулятор.

Аккумуляторы Аккумулятор (от лат. accumulator - собиратель) - устройство для накопления энергии с целью ее последующего использования. Аккумуляторы – обратимые гальванические элементы многоразового действия (пропускание через аккумулятор электрического тока – зарядка, работа в режиме гальванического элемента - разрядка). Электродные процессы: Схема аккумулятора: (-)Pb/Pb. SO 4//H 2 SO 4 /Pb. O 2 (+)

Топливный элемент Топливные элементы – это устройства непрерывного действия, в которых энергия сгорания топлива непосредственно превращается в электрическую энергию. Окисление топлива происходит на поверхности электродов, материалом которых являются графит, либо платина, серебро, никель. В качестве топлива (восстановителя) используется водород, гидразин, уголь, оксид углерода, различные углеводороды. Окислителем в топливных элементах обычно является кислород или воздух.

Водородно-кислородный топливный элемент Уравнения электродных процессов: (-) A: 2 H 2 + 4 OH- → 4 H 2 O + 4 e- (+) K: O 2 + 2 H 2 O +4 e- → 4 OH- Суммарная токобразующая реакция имеет вид 2 Н 2 + О 2 → 2 Н 2 О Обычное значение ЭДС топливных элементов составляет 1, 0 – 1, 5 В.

В подготовке учебных материалов использовались следующие электронные ресурсы: - himhelp. ru - alhimik. ru - http: //www. energy-units. ru/en_units. php

Контактная информация Разработчик: доцент, к. х. н. , Шубенкова Е. Г. Кафедра «Химия» пр. Мира, 11 главный корпус кабинет 422 А т. 65 -98 -11 phiscem@omgtu. ru http: //www. omgtu. ru/
ЭУ Гальванический элемент.ppt