3 2-й закон термодинамики.ppt
- Количество слайдов: 30
 ОМСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КАФЕДРА ХИМИИ Лекция 3. Второй закон термодинамики 1. Самопроизвольные и несамопроизвольные процессы. Второй закон термодинамики. 2. Энтропия как критерий самопроизвольности процесса в изолированной системе. 3. Энергия Гиббса и Гельмгольца как критерий самопроизвольности в закрытых и открытых системах. 4. Критерии направленности процессов в системах переменного состава. Химический потенциал. Лектор: доцент кафедры химии Григорьева Марина Викторовна
ОМСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КАФЕДРА ХИМИИ Лекция 3. Второй закон термодинамики 1. Самопроизвольные и несамопроизвольные процессы. Второй закон термодинамики. 2. Энтропия как критерий самопроизвольности процесса в изолированной системе. 3. Энергия Гиббса и Гельмгольца как критерий самопроизвольности в закрытых и открытых системах. 4. Критерии направленности процессов в системах переменного состава. Химический потенциал. Лектор: доцент кафедры химии Григорьева Марина Викторовна
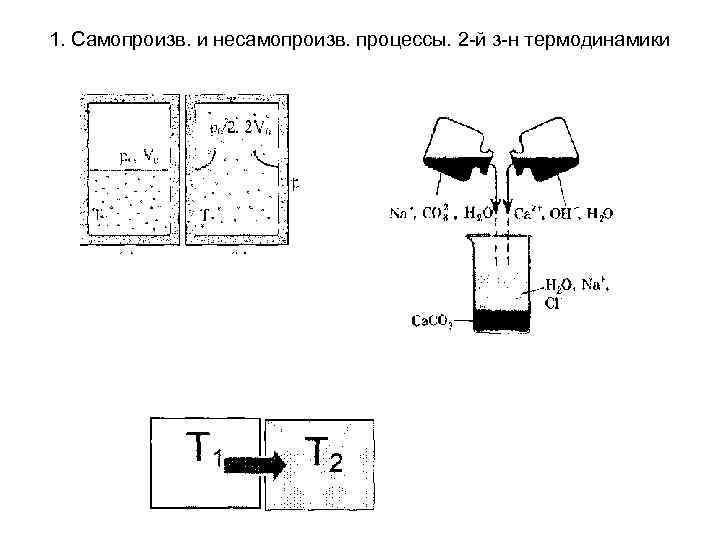
 1. Самопроизв. и несамопроизв. процессы. 2 -й з-н термодинамики Процессы подразделяются на самопроизвольные и не самопроизвольные. Самопроизвольные процессы - процессы протекающие без сообщения энергии системе извне. Они протекают до установления равновесия в термодинамической системе. К ним относят переход теплоты от горячего тела к холодному, расширение газа при подвижных границах раздела система - среда, реакции протекающие с выпадением осадка, реакции протекающие с выделением газа и т. д. За счет самопроизвольных процессов может быть совершена работа: например, за счет разности давлений можно получить механическую работу; за счет разности температур может работать тепловой двигатель или термопара.
1. Самопроизв. и несамопроизв. процессы. 2 -й з-н термодинамики Процессы подразделяются на самопроизвольные и не самопроизвольные. Самопроизвольные процессы - процессы протекающие без сообщения энергии системе извне. Они протекают до установления равновесия в термодинамической системе. К ним относят переход теплоты от горячего тела к холодному, расширение газа при подвижных границах раздела система - среда, реакции протекающие с выпадением осадка, реакции протекающие с выделением газа и т. д. За счет самопроизвольных процессов может быть совершена работа: например, за счет разности давлений можно получить механическую работу; за счет разности температур может работать тепловой двигатель или термопара.
 1. Самопроизв. и несамопроизв. процессы. 2 -й з-н термодинамики
1. Самопроизв. и несамопроизв. процессы. 2 -й з-н термодинамики
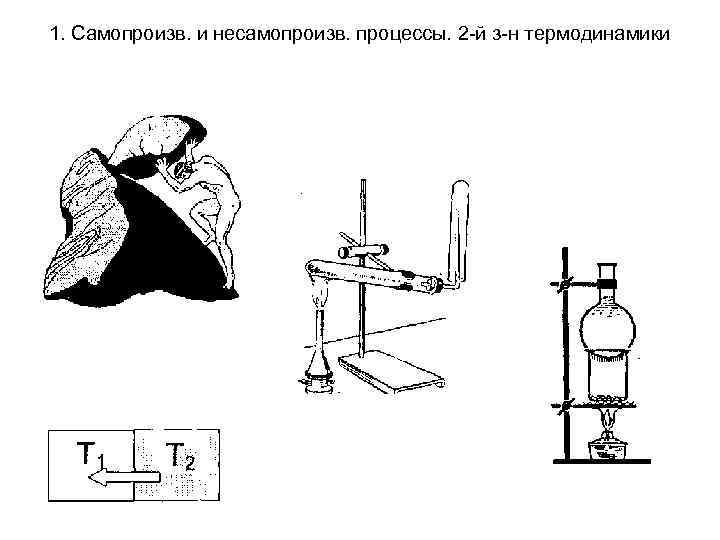
 1. Самопроизв. и несамопроизв. процессы. 2 -й з-н термодинамики Несамопроизвольные процессы - процессы протекающие при сообщении системе энергии извне. В результате таких процессов система удаляется от состояния равновесия. Примерами таких процессов служит подъем тела в гору ( «сизифов труд» ), переход теплоты от более холодного тела к более нагретому (в холодильных машинах), разложение воды на водород и кислород , разложение перманганата калия, возгонка нафталина и т. д.
1. Самопроизв. и несамопроизв. процессы. 2 -й з-н термодинамики Несамопроизвольные процессы - процессы протекающие при сообщении системе энергии извне. В результате таких процессов система удаляется от состояния равновесия. Примерами таких процессов служит подъем тела в гору ( «сизифов труд» ), переход теплоты от более холодного тела к более нагретому (в холодильных машинах), разложение воды на водород и кислород , разложение перманганата калия, возгонка нафталина и т. д.
 1. Самопроизв. и несамопроизв. процессы. 2 -й з-н термодинамики
1. Самопроизв. и несамопроизв. процессы. 2 -й з-н термодинамики
 1. Самопроизв. и несамопроизв. процессы. 2 -й з-н термодинамики Первый закон термодинамики не дает ответа на вопрос «Что является критерием самопроизвольности процесса? » Данные критерии определяются 2 -м законом термодинамики. 2 -й закон термодинамики как и 1 -й, является постулатом. Его справедливость подтверждается опытами. Основоположниками закона являются С. Карно, Р. Клаузис, У. Томсон, Дж. Максвелл и др. Сначала закон был сформулирован как основной закон действия тепловых машин, затем его границы расширились до объяснения физико-химических процессов.
1. Самопроизв. и несамопроизв. процессы. 2 -й з-н термодинамики Первый закон термодинамики не дает ответа на вопрос «Что является критерием самопроизвольности процесса? » Данные критерии определяются 2 -м законом термодинамики. 2 -й закон термодинамики как и 1 -й, является постулатом. Его справедливость подтверждается опытами. Основоположниками закона являются С. Карно, Р. Клаузис, У. Томсон, Дж. Максвелл и др. Сначала закон был сформулирован как основной закон действия тепловых машин, затем его границы расширились до объяснения физико-химических процессов.
 1. Самопроизв. и несамопроизв. процессы. 2 -й з-н термодинамики Предложено много разнообразных качественных формулировок 2 -го начала термодинамики: • теплота не может переходить сама собой от менее нагретого тела к более нагретому. (Р. Клаузиус, 1850) • невозможно превратить в механическую работу теплоту какого-либо тела, не произведя никакого другого действия, кроме охлаждения этого тела (Кельвин, 1854) • невозможен вечный двигатель второго рода, т. е. невозможно полное превращение теплоты в работу (В. Освальд, 1888).
1. Самопроизв. и несамопроизв. процессы. 2 -й з-н термодинамики Предложено много разнообразных качественных формулировок 2 -го начала термодинамики: • теплота не может переходить сама собой от менее нагретого тела к более нагретому. (Р. Клаузиус, 1850) • невозможно превратить в механическую работу теплоту какого-либо тела, не произведя никакого другого действия, кроме охлаждения этого тела (Кельвин, 1854) • невозможен вечный двигатель второго рода, т. е. невозможно полное превращение теплоты в работу (В. Освальд, 1888).
 1. Самопроизв. и несамопроизв. процессы. 2 -й з-н термодинамики Количественно второй закон термодинамики можно сформулировать так: существуют некие функции состояния системы - термодинамические потенциалы, по значению изменения которых можно определить возможность, направление и предел протекания самопроизвольного процесса.
1. Самопроизв. и несамопроизв. процессы. 2 -й з-н термодинамики Количественно второй закон термодинамики можно сформулировать так: существуют некие функции состояния системы - термодинамические потенциалы, по значению изменения которых можно определить возможность, направление и предел протекания самопроизвольного процесса.
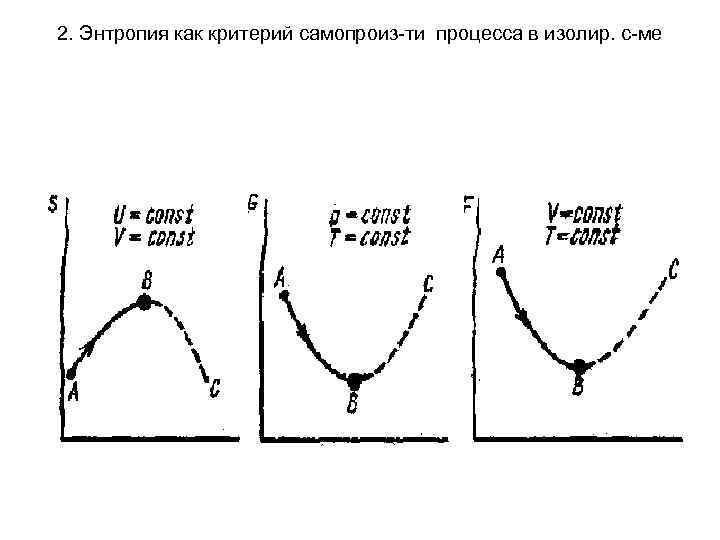
 2. Энтропия как критерий самопроиз-ти процесса в изолир. с-ме Термодинамическими потенциалами являются различные функции состояния в зависимости от вида термодинамической системы: • для изолированной системы (при U=const, V= const) критерием самопроизвольности процесса является энтропия (S). Процесс протекает самопроизвольно, если ΔS> 0, будет протекать не самопроизвольно, если ΔS< 0, в момент равновесия ΔS = 0. В неизолированной системе энтропия может уменьшаться но при этом должен происходить рост энтропии в окружающей среде.
2. Энтропия как критерий самопроиз-ти процесса в изолир. с-ме Термодинамическими потенциалами являются различные функции состояния в зависимости от вида термодинамической системы: • для изолированной системы (при U=const, V= const) критерием самопроизвольности процесса является энтропия (S). Процесс протекает самопроизвольно, если ΔS> 0, будет протекать не самопроизвольно, если ΔS< 0, в момент равновесия ΔS = 0. В неизолированной системе энтропия может уменьшаться но при этом должен происходить рост энтропии в окружающей среде.
 2. Энтропия как критерий самопроиз-ти процесса в изолир. с-ме • для закрытой системы (при T=const, V= const) критерием самопроизвольности процесса является энергия Гельмгольца (F). ΔF=0 - равновесие; ΔF< 0 - самопроизвольный процесс; ΔF>0 – не самопроизвольный процесс. • для открытой системы (при T=const, р= const) критерием самопроизвольности процесса является энергия Гиббса (G). ΔG=0 - равновесие; ΔG< 0 - самопроизвольный процесс; ΔG >0 - не самопроизвольный процесс.
2. Энтропия как критерий самопроиз-ти процесса в изолир. с-ме • для закрытой системы (при T=const, V= const) критерием самопроизвольности процесса является энергия Гельмгольца (F). ΔF=0 - равновесие; ΔF< 0 - самопроизвольный процесс; ΔF>0 – не самопроизвольный процесс. • для открытой системы (при T=const, р= const) критерием самопроизвольности процесса является энергия Гиббса (G). ΔG=0 - равновесие; ΔG< 0 - самопроизвольный процесс; ΔG >0 - не самопроизвольный процесс.
 2. Энтропия как критерий самопроиз-ти процесса в изолир. с-ме
2. Энтропия как критерий самопроиз-ти процесса в изолир. с-ме
 2. Энтропия как критерий самопроизвольности процесса в изолированной системе • Термодинамическое определение энтропии введено Р. Клаузиусом в 1865 г. На основе изучения процессов превращения теплоты в работу, происходящих в тепловой машине (нагреватель - рабочее тело - холодильник), он вывел, что существует некоторое экстенсивное свойство системы S, называемое энтропией, которое может служить мерой рассеивания энергии при переходе теплоты в работу.
2. Энтропия как критерий самопроизвольности процесса в изолированной системе • Термодинамическое определение энтропии введено Р. Клаузиусом в 1865 г. На основе изучения процессов превращения теплоты в работу, происходящих в тепловой машине (нагреватель - рабочее тело - холодильник), он вывел, что существует некоторое экстенсивное свойство системы S, называемое энтропией, которое может служить мерой рассеивания энергии при переходе теплоты в работу.
 2. Энтропия как критерий самопроиз-ти процесса в изолир. с-ме Приращение энтропии в равновесном процессе равно приведенной теплоте – отношению элементарного количества теплоты к температуре. Энтропия является функцией состояния системы, следовательно изменение энтропии зависит от начального и конечного состояния системы и не зависит от пути процесса: ΔS = S 2 -S 1
2. Энтропия как критерий самопроиз-ти процесса в изолир. с-ме Приращение энтропии в равновесном процессе равно приведенной теплоте – отношению элементарного количества теплоты к температуре. Энтропия является функцией состояния системы, следовательно изменение энтропии зависит от начального и конечного состояния системы и не зависит от пути процесса: ΔS = S 2 -S 1
 2. Энтропия как критерий самопроиз-ти процесса в изолир. с-ме • Статистическое определение энтропии в 1896 г дает Л. Больцман. В связи с тем, что теплота, связана с идеей хаотического движения молекул, следовательно можно определить физический смысл энтропии на основе представлений молекулярной статистики.
2. Энтропия как критерий самопроиз-ти процесса в изолир. с-ме • Статистическое определение энтропии в 1896 г дает Л. Больцман. В связи с тем, что теплота, связана с идеей хаотического движения молекул, следовательно можно определить физический смысл энтропии на основе представлений молекулярной статистики.
 2. Энтропия как критерий самопроиз-ти процесса в изолир. с-ме • Макросостояние системы характеризуется определенными термодинамическими параметрами , в т. ч. и энтропией. Микросостояние системы определяется энергией и положением каждой частицы. Макросостояние системы может существовать при различном расположении и разной энергии частиц определяющих микросостояние. Число микросостояний, которое соответствует данному макросостоянию вещества, называется термодинамической вероятностью W. Например, для системы состоящей из 10 частиц W=12600.
2. Энтропия как критерий самопроиз-ти процесса в изолир. с-ме • Макросостояние системы характеризуется определенными термодинамическими параметрами , в т. ч. и энтропией. Микросостояние системы определяется энергией и положением каждой частицы. Макросостояние системы может существовать при различном расположении и разной энергии частиц определяющих микросостояние. Число микросостояний, которое соответствует данному макросостоянию вещества, называется термодинамической вероятностью W. Например, для системы состоящей из 10 частиц W=12600.
 2. Энтропия как критерий самопроиз-ти процесса в изолир. с-ме Больцман установил взаимосвязь энтропии с термодинамической вероятностью: S= КБ In W , где КБ - постоянная Больцмана (КБ = R/NA= 1, 38 · 10 -23 Дж/ моль), Энтропия - мера наиболее вероятностного состояния системы, а следовательно и мера беспорядка (хаотичности) системы.
2. Энтропия как критерий самопроиз-ти процесса в изолир. с-ме Больцман установил взаимосвязь энтропии с термодинамической вероятностью: S= КБ In W , где КБ - постоянная Больцмана (КБ = R/NA= 1, 38 · 10 -23 Дж/ моль), Энтропия - мера наиболее вероятностного состояния системы, а следовательно и мера беспорядка (хаотичности) системы.
 2. Энтропия как критерий самопроиз-ти процесса в изолир. с-ме При абсолютном нуле прекращаются колебательные движения частиц, образующих кристаллическую решетку. Такое микросостояние достигается лишь при одном варианте расположения микрочастиц (W) и в соответствии с формулой Больцмана: S = КБ In 1 = 0 Эта закономерность известна как третий закон термодинамики (постулат Планка): при абсолютном нуле энтропия чистого вещества равна нулю.
2. Энтропия как критерий самопроиз-ти процесса в изолир. с-ме При абсолютном нуле прекращаются колебательные движения частиц, образующих кристаллическую решетку. Такое микросостояние достигается лишь при одном варианте расположения микрочастиц (W) и в соответствии с формулой Больцмана: S = КБ In 1 = 0 Эта закономерность известна как третий закон термодинамики (постулат Планка): при абсолютном нуле энтропия чистого вещества равна нулю.
 2. Энтропия как критерий самопроиз-ти процесса в изолир. с-ме Расчет абсолютного значения энтропии Для многих практических целей, особенно для расчета химических равновесий, надо знать стандартные энтропии веществ S°. Для их вычисления используют табличные данные теплоемкости, определенные при возможно низких температурах и теплоты фазовых переходов. Значение теплоемкости вблизи абсолютного нуля находят путём экстраполяции. Если в интервале температур от 0 до Т вещество претерпевает ф. п. , то они должны быть учтены.
2. Энтропия как критерий самопроиз-ти процесса в изолир. с-ме Расчет абсолютного значения энтропии Для многих практических целей, особенно для расчета химических равновесий, надо знать стандартные энтропии веществ S°. Для их вычисления используют табличные данные теплоемкости, определенные при возможно низких температурах и теплоты фазовых переходов. Значение теплоемкости вблизи абсолютного нуля находят путём экстраполяции. Если в интервале температур от 0 до Т вещество претерпевает ф. п. , то они должны быть учтены.
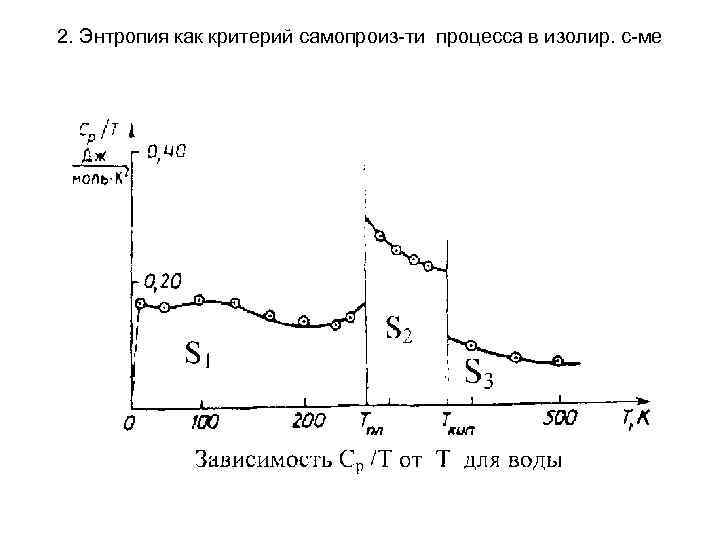
 2. Энтропия как критерий самопроиз-ти процесса в изолир. с-ме Где S 0 ид - поправка на неидеальность газа (пара) при данной температуре. Расчет энтропии осуществляется графически: каждый интеграл равен соответствующей площади.
2. Энтропия как критерий самопроиз-ти процесса в изолир. с-ме Где S 0 ид - поправка на неидеальность газа (пара) при данной температуре. Расчет энтропии осуществляется графически: каждый интеграл равен соответствующей площади.
 2. Энтропия как критерий самопроиз-ти процесса в изолир. с-ме
2. Энтропия как критерий самопроиз-ти процесса в изолир. с-ме
 2. Энтропия как критерий самопроиз-ти процесса в изолир. с-ме Сложив сумму этих интегральных членов с изменениями энтропии при всех фазовых переходах в исследуемом интервале температур (от О К до Т К) и с поправкой на неидеальность, находят значение абсолютной энтропии данного вещества при температуре Т.
2. Энтропия как критерий самопроиз-ти процесса в изолир. с-ме Сложив сумму этих интегральных членов с изменениями энтропии при всех фазовых переходах в исследуемом интервале температур (от О К до Т К) и с поправкой на неидеальность, находят значение абсолютной энтропии данного вещества при температуре Т.
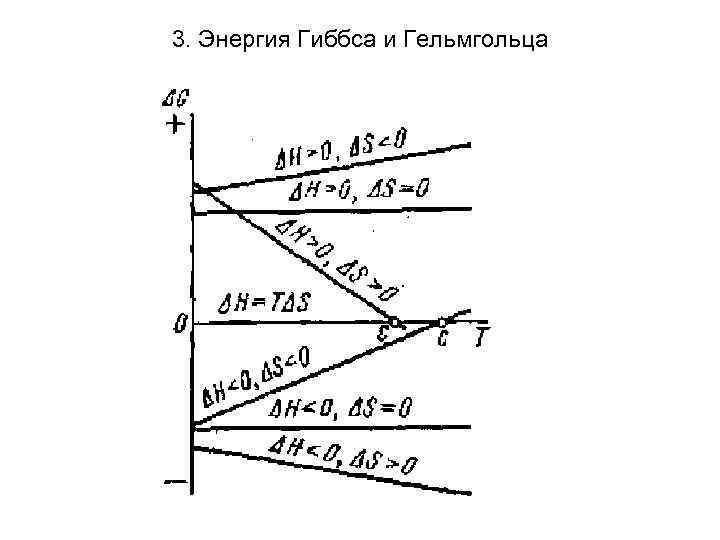
 3. Энергия Гиббса и Гельмгольца При Т, р =const (изохорно-изотермические условия) критерием самопроизвольности является изобарно-изотермический потенциал (энергия Гиббса) G = Н - TS (ΔG = ΔН -TΔS). При ΔG=0 -равновесие; ΔG<0 самопроизвольный процесс; ΔG>0 – не самопроизвольный процесс. Знак и величина ΔG определяется энтальпий- ным ΔН и энтропийным факторами TΔS. Возможные случаи зависимости энтальпийного и энтропийного фактора:
3. Энергия Гиббса и Гельмгольца При Т, р =const (изохорно-изотермические условия) критерием самопроизвольности является изобарно-изотермический потенциал (энергия Гиббса) G = Н - TS (ΔG = ΔН -TΔS). При ΔG=0 -равновесие; ΔG<0 самопроизвольный процесс; ΔG>0 – не самопроизвольный процесс. Знак и величина ΔG определяется энтальпий- ным ΔН и энтропийным факторами TΔS. Возможные случаи зависимости энтальпийного и энтропийного фактора:
 3. Энергия Гиббса и Гельмгольца
3. Энергия Гиббса и Гельмгольца
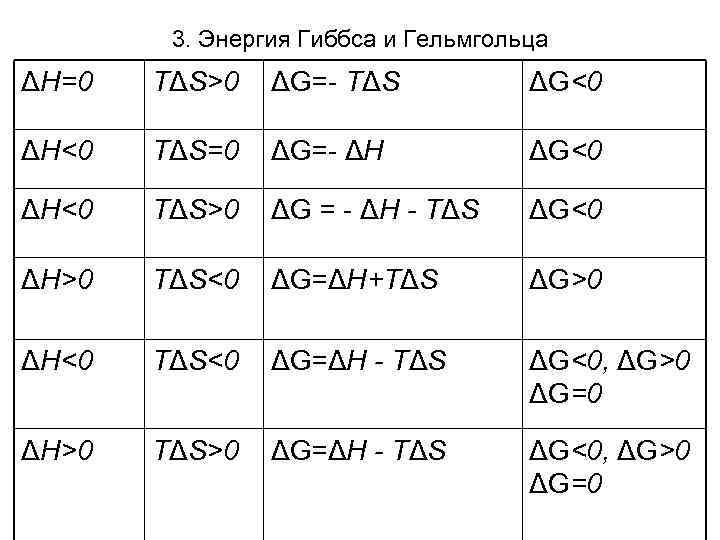 3. Энергия Гиббса и Гельмгольца ΔН=0 TΔS>0 ΔG=- TΔS ΔG<0 ΔН<0 TΔS=0 ΔG=- ΔН ΔG<0 ΔН<0 TΔS>0 ΔG = - ΔН - TΔS ΔG<0 ΔН>0 TΔS<0 ΔG=ΔН+TΔS ΔG>0 ΔН<0 TΔS<0 ΔG=ΔН - TΔS ΔG<0, ΔG>0 ΔG=0 ΔН>0 TΔS>0 ΔG=ΔН - TΔS ΔG<0, ΔG>0 ΔG=0
3. Энергия Гиббса и Гельмгольца ΔН=0 TΔS>0 ΔG=- TΔS ΔG<0 ΔН<0 TΔS=0 ΔG=- ΔН ΔG<0 ΔН<0 TΔS>0 ΔG = - ΔН - TΔS ΔG<0 ΔН>0 TΔS<0 ΔG=ΔН+TΔS ΔG>0 ΔН<0 TΔS<0 ΔG=ΔН - TΔS ΔG<0, ΔG>0 ΔG=0 ΔН>0 TΔS>0 ΔG=ΔН - TΔS ΔG<0, ΔG>0 ΔG=0
 3. Энергия Гиббса и Гельмгольца При T, V = const, критерием самопроизвольности является изохорно -изотермический потенциал (энергия Гельмгольца) F = U -TS (ΔF = ΔU -TΔS).
3. Энергия Гиббса и Гельмгольца При T, V = const, критерием самопроизвольности является изохорно -изотермический потенциал (энергия Гельмгольца) F = U -TS (ΔF = ΔU -TΔS).
 3. Энергия Гиббса и Гельмгольца Характеристические функции - функции, частные производные которых по какому-либо из параметров (естественной переменной) равны другому параметру. Энергия Гиббса относится к характеристическим функциям.
3. Энергия Гиббса и Гельмгольца Характеристические функции - функции, частные производные которых по какому-либо из параметров (естественной переменной) равны другому параметру. Энергия Гиббса относится к характеристическим функциям.
 4. Химический потенциал μ – термодинамическая функция состояния, определяющая изменение термодинамических потенциалов при изменении числа частиц в системе и необходимая для описания свойств открытых систем (с переменным числом частиц).
4. Химический потенциал μ – термодинамическая функция состояния, определяющая изменение термодинамических потенциалов при изменении числа частиц в системе и необходимая для описания свойств открытых систем (с переменным числом частиц).
 4. Химический потенциал Наиболее просто химический потенциал связан с термодинамическим потенциалом G: G=∑μi Ni. Для однокомпонентной системы μ = G/N, т. е. представляет собой энергию Гиббса, отнесённую к одной частице.
4. Химический потенциал Наиболее просто химический потенциал связан с термодинамическим потенциалом G: G=∑μi Ni. Для однокомпонентной системы μ = G/N, т. е. представляет собой энергию Гиббса, отнесённую к одной частице.
 4. Химический потенциал В простейшем случае идеальных газов зависит только от концентрации i -го компонента: μi = μi 0+ k. T ln С
4. Химический потенциал В простейшем случае идеальных газов зависит только от концентрации i -го компонента: μi = μi 0+ k. T ln С
 Спасибо за внимание!
Спасибо за внимание!


