БАКТЕРИОФАГИ НТВ.pptx
- Количество слайдов: 30

Омский государственный медицинский университет, кафедра микробиологии, вирусологии и иммунологии Бактериофаги Лектор: К. М. Н. , доцент Темникова Наталья Владимировна 2017 г.

«Без согласованных действий всех стран многие великие открытия, сделанные учеными-медиками за последние 50 лет, могут утратить свое значение из-за распространения антибиотикорезистентности» (ВОЗ Глобальная стратегия по сдерживанию устойчивости к противомикробным препаратам, 2002 г. )

Фаги — облигатные внутриклеточные паразиты, так как у них нет механизмов для выработки энергии и рибосом для синтеза белка. Размножение фага происходит только внутри бактерии-хозяина.

Для справки……… • Бактериофаги — незримо присутствуют повсюду в нашем мире — в океане, почве, глубоководных источниках, питьевой воде и пище. Они — наиболее представленная форма жизни на Земле — от 1030 до 1032 фаговых частиц в биосфере, — и играют ключевую роль в поддержании баланса всех исследованных экосистем. • Бактериофаги являются естественными регуляторами бактерий и обеспечивают динамическое равновесие в природе, сохраняя относительное постоянство микробного пейзажа в природе и ограничивая рост популяции бактерий.

История открытия БФ • В 1896 году английский бактериолог Э. Ханкин, исследуя антибактериальное действие воды индийских рек, пришел к выводу о существовании агента, проходящего через бактериальные фильтры и вызывающего лизис холерных вибрионов. • Российский микробиолог Н. Ф. Гамалея в 1897 году наблюдал лизис бацилл сибирской язвы. • Однако первая научная публикация о фагах — статья 1915 года английского микробиолога Ф. Туорта, в которой он описал инфекционное поражение стафилококков, значительно изменявшее морфологию колоний. • Инфекционный агент свободно проходил через бактериальные фильтры, и его можно было переносить из одной колонии в другую. Туорт выдвинул несколько гипотез, объясняющих это явление, в частности — гипотезу о фильтрующемся вирусе, подобном вирусам растений и животных. Однако его работа не привлекла внимания ученых, а Туорт забросил ее из-за службы в армии: началась Первая мировая.

• В 1917 году канадский бактериолог Ф. Д’Эрелль независимо от Туорта сообщил об открытии вируса, «пожирающего» бактерий, — бактериофага. • Микробиологи того времени считали, что чума свиней вызывается совместным действием микроба и вируса. • Д’Эрелль предположил, что схожая этиология и у дизентерии(шигеллез). С помощью Бактериальных фильтров он отфильтровал фекалии больных дизентерией и добавил их в пробирки с культурами шигелл, намереваясь ввести смесь бактерий и предполагаемого вируса экспериментальным животным. • Однако на следующие сутки он обнаружил, что бульон, в котором росли шигеллы, стал прозрачным, что свидетельствовало о гибели бактерий. Профильтровав бульон из этих пробирок, он снова заразил полученными фильтратами культуры шигелл. И вновь на следующие сутки он обнаружил, что бульон стал прозрачным. Полученное «литическое начало» можно было бесконечно пассировать от одной культуры к другой, что привело Д’Эрелля к мысли о существовании вируса, разрушающего бактерии. • Учитывая эффективность фагов против патогенных микроорганизмов и их широкое распространение в природе, Д’Эрелль предположил, что они играют определенную роль в развитии иммунитета к инфекционным заболеваниям и выздоровлении. • В СССР в ранние годы бактериофагам уделяли достаточно внимания. В 1923 грузинский микробиолог Г. Г. Элиава, ученик Д’Эрелля, основал в Тбилиси Институт бактериофагов, ставший впоследствии Всесоюзным центром фаготерапии, коллекция которого на сегодняшний день составляет около 3000 фаговых штаммов.

• На протяжении почти 70 лет бактериофаги, как и другие вирусы, были для биологов такими же невидимыми, как атомы для физиков, в силу их субмикроскопических размеров.
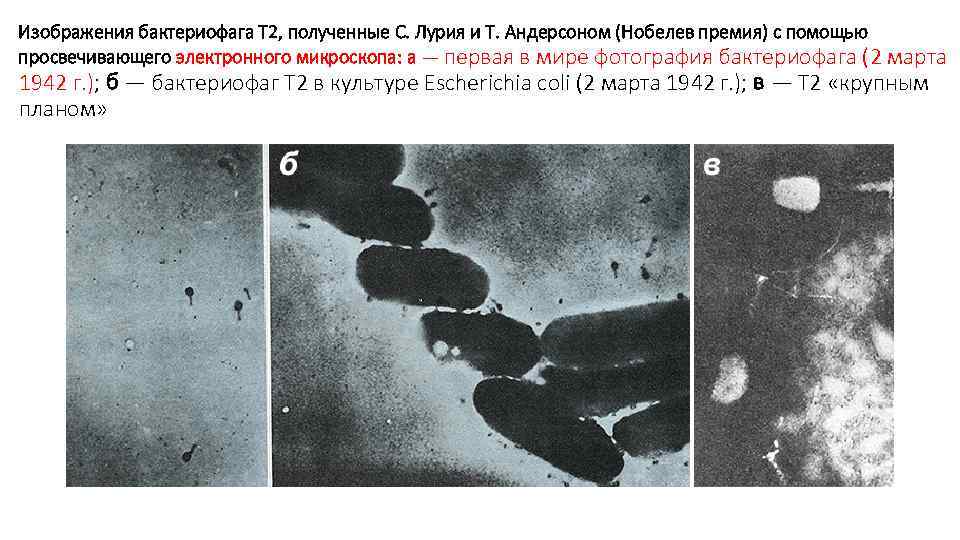
Изображения бактериофага Т 2, полученные С. Лурия и Т. Андерсоном (Нобелев премия) с помощью просвечивающего электронного микроскопа: а — первая в мире фотография бактериофага (2 марта 1942 г. ); б — бактериофаг Т 2 в культуре Escherichia coli (2 марта 1942 г. ); в — Т 2 «крупным планом»

• В тридцатых годах прошлого века крупный американский концерн основал даже клинику, где начали лечить фагами. Пропагандисты нового метода сулили исцеление от всех болезней. • Однако действительность оставляла желать лучшего: научные основы такой терапии были ещё так скудны, что новое средство применяли практически вслепую. Считалось, что все фаги одинаковы и побеждают любую бактерию. Одним и тем же бактериофагом начинали лечить разные заболевания, а болезнь всё не уходила — так метод был серьёзно скомпрометирован. • Однако успешное применение антибиотиков в 1960– 1970 -е годы практически похоронило идеи фаготерапии. Так, например, в Большой советской энциклопедии указано: «Антибиотики и другие химиотерапевтические средства оказались эффективнее фагов, в связи с чем их применение с лечебной целью сузилось» .

Номенклатура и биологические особенности Номенклатура основана на видовом наименовании хозяина. Например, фаги, лизирующие дизентерийные бактерии, получили название дизентерийных бактериофагов. ● Структура. Имеют сперматозоидную форму. Состоят из головки, которая содержит нуклеиновую кислоту и отростка. У некоторых фагов отросток очень короткий или вовсе отсутствует. Размеры фаговой частицы колеблются от 20 до 200 нм.

● Наиболее изучены Т фаги (англ. type типовые). Они со ставляют Т группу коли дизентерийных фагов: 4 нечетных (Т 1, ТЗ, Т 5, Т 7) и 3 четных (Т 2, Т 4, Т 6). ● Наиболее сложной структура Т четных фагов (Т 2). Он состоит из головки гексагональной формы и отростка, который образован полым стержнем. Снаружи стержень окружен чехлом, способным к сокращению. На дистальном конце отростка имеется шестиугольная базальная пластинка, в углах которой распола гаются короткие зубцы. От каждого зубца отходит по одной нити длиной 150 нм. Базальная пластинка и нити осуществляют процесс адсорбции фага на бактериальной клетке.
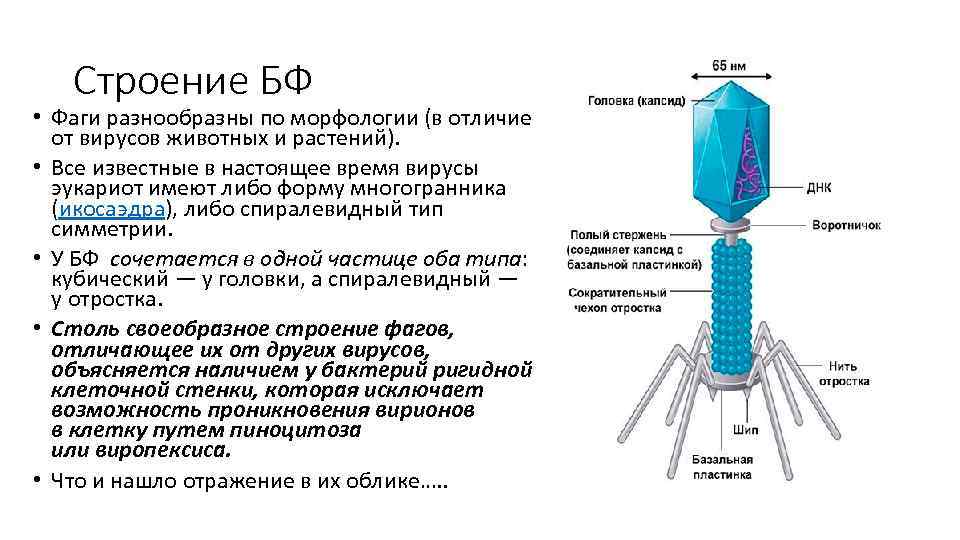
Строение БФ • Фаги разнообразны по морфологии (в отличие от вирусов животных и растений). • Все известные в настоящее время вирусы эукариот имеют либо форму многогранника (икосаэдра), либо спиралевидный тип симметрии. • У БФ сочетается в одной частице оба типа: кубический — у головки, а спиралевидный — у отростка. • Столь своеобразное строение фагов, отличающее их от других вирусов, объясняется наличием у бактерий ригидной клеточной стенки, которая исключает возможность проникновения вирионов в клетку путем пиноцитоза или виропексиса. • Что и нашло отражение в их облике…. .
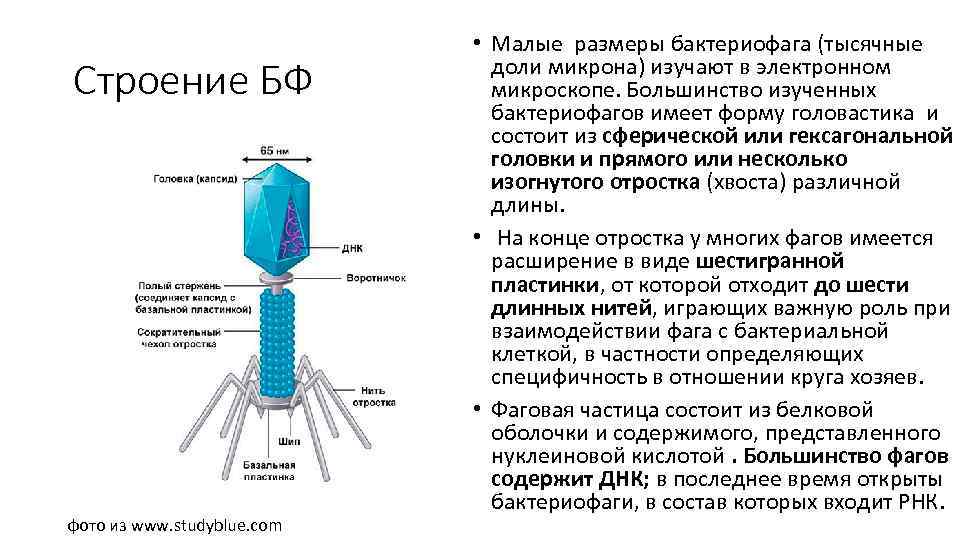
Строение БФ фото из www. studyblue. com • Малые размеры бактериофага (тысячные доли микрона) изучают в электронном микроскопе. Большинство изученных бактериофагов имеет форму головастика и состоит из сферической или гексагональной головки и прямого или несколько изогнутого отростка (хвоста) различной длины. • На конце отростка у многих фагов имеется расширение в виде шестигранной пластинки, от которой отходит до шести длинных нитей, играющих важную роль при взаимодействии фага с бактериальной клеткой, в частности определяющих специфичность в отношении круга хозяев. • Фаговая частица состоит из белковой оболочки и содержимого, представленного нуклеиновой кислотой. Большинство фагов содержит ДНК; в последнее время открыты бактериофаги, в состав которых входит РНК.

Взаимодействие БФ и клетки-хозяина • Важным свойством бактериофагов является их специфичность: фаги могут поражать определенный вид бактерий (моновалентные фаги) или же только избранные штаммы/варианты внутри вида (типовые фаги, например, фаги V. cholerae classica и El Tor), но некоторые не столь разборчивы и поражают бактерий разных видов и даже родов (поливалентные фаги).
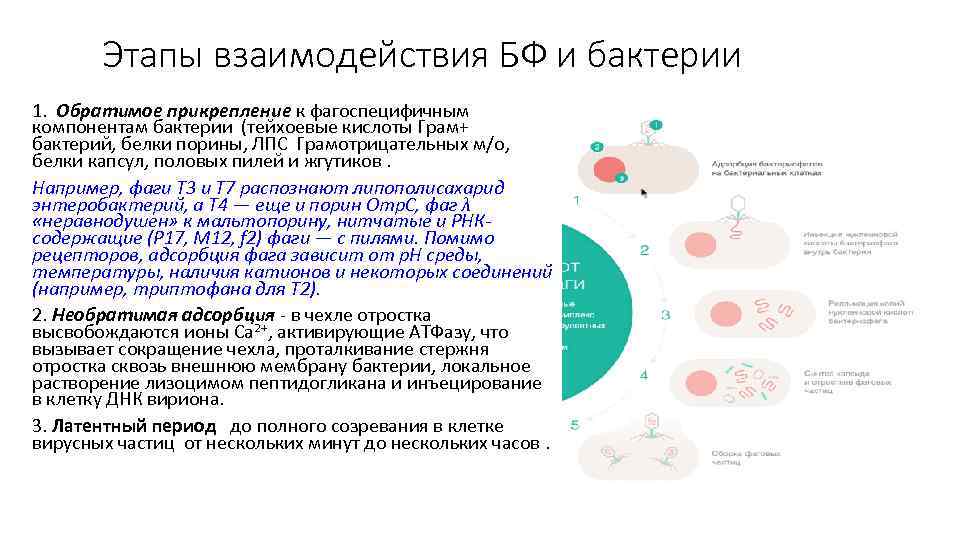
Этапы взаимодействия БФ и бактерии 1. Обратимое прикрепление к фагоспецифичным компонентам бактерии (тейхоевые кислоты Грам+ бактерий, белки порины, ЛПС Грамотрицательных м/о, белки капсул, половых пилей и жгутиков. Например, фаги Т 3 и Т 7 распознают липополисахарид энтеробактерий, а Т 4 — еще и порин Omp. C, фаг λ «неравнодушен» к мальтопорину, нитчатые и РНКсодержащие (P 17, M 12, f 2) фаги — с пилями. Помимо рецепторов, адсорбция фага зависит от р. Н среды, температуры, наличия катионов и некоторых соединений (например, триптофана для Т 2). 2. Необратимая адсорбция - в чехле отростка высвобождаются ионы Са 2+, активирующие АТФазу, что вызывает сокращение чехла, проталкивание стержня отростка сквозь внешнюю мембрану бактерии, локальное растворение лизоцимом пептидогликана и инъецирование в клетку ДНК вириона. 3. Латентный период до полного созревания в клетке вирусных частиц от нескольких минут до нескольких часов.

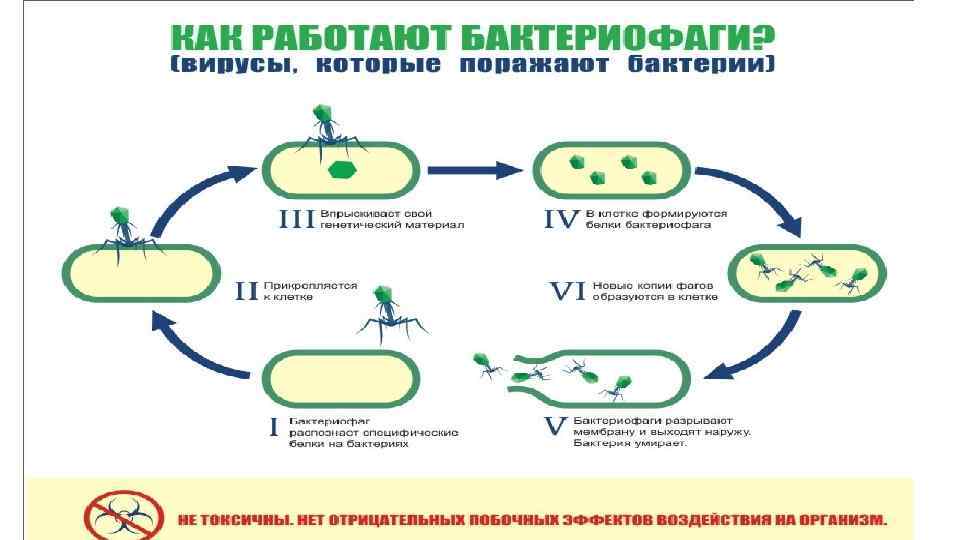
Этапы взаимодействия БФ и бактерии 4. Перестройка метаболизма бактерии: прекращается синтез ее собственных ДНК, РНК и белков. ДНК бактериофага может начинать транскрибироваться его же РНК-полимеразой — например, фаг Т 4 впрыскивает этот фермент вместе с ДНК. Или же, как в случае Т 4, фаг впрыскивает фермент АДФ-рибозилтрансферазу (продукт гена alt), модифицирующий хозяйскую РНК-полимеразу так, что та переключается на транскрипцию исключительно фаговых генов. 5. Синтезирующиеся м. РНК поступают на рибосомы бактерии, которые послушно производят белки бактериофага: ранние (ДНК-полимеразу, нуклеазы) и поздние (белки капсида, отростка, базальной пластинки и др. ). 6. Репликация ДНК бактериофага осуществляется его собственной ДНК-полимеразой. 7. Образование зрелых инфекционных фаговых частиц. Поздние белки и копии фаговой ДНК объединяются. 8. Выход вирионов. Фаговые лизины (гидролазы) и холины изнутри пробивают отверстия в бактериальной мембране и пептидогликане, и в клетку начинает поступать вода. В итоге бактерия лопается с выходом зрелых бактериофагов. При этом в зависимости от типа фага количество образовавшихся вирионов будет различным — от единичных частиц до нескольких тысяч. •
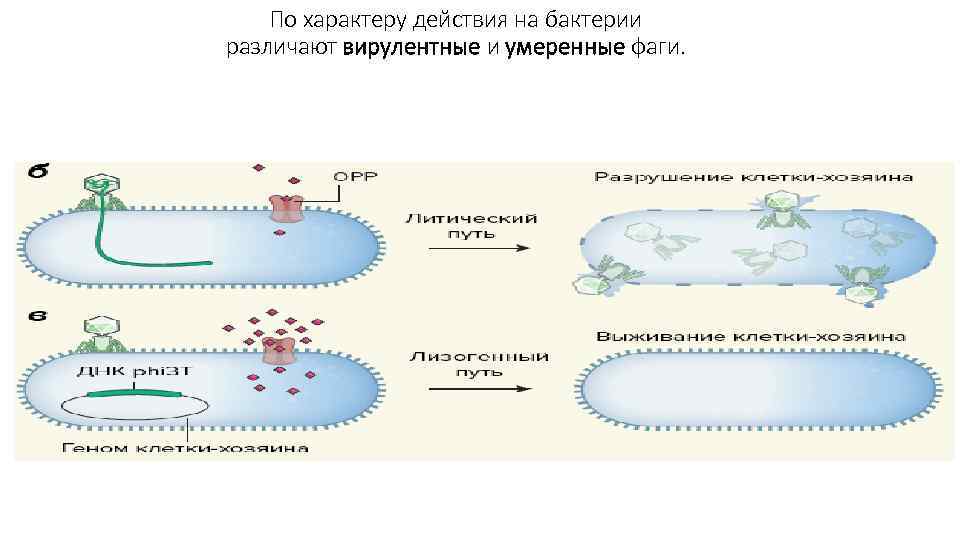
По характеру действия на бактерии различают вирулентные и умеренные фаги.

Умеренные фаги (профаги) • Умеренный фаг инициирует лизогенный цикл, при котором он вместо репликации обратимо взаимодействует с геномом бактерии-хозяина, интегрируясь в хромосому (фаг λ), либо поддерживается в клетке в виде плазмиды. • При делении бактерии фаговый геном передается дочерним клеткам. Бактерия, содержащая профаг, лизогенна до тех пор, пока при определенных условиях профаг не активируется и не вступит в литический цикл. • Переход от лизогении к лизису называется лизогенной индукцией, или индукцией профага. На индукцию фага оказывают влияние условия внешней среды, состояние клетки хозяина, наличие питательных веществ и т. д. • Лизогенизация лежит в основе фаговой или лизогенной конверсии. Она заключается в изменении свойств у лизогенных бактерий, например приобретении способности продуцировать токсин, изменять морфологию, антигенные свойства и другие признаки. Механизм этого явления связан с внесением новой информации в бактериальную клетку (КОРИНЕФАГИ) • Умеренные фаги могут быть дефективными, т. е. неспособными образовывать фаговое потомство, например, трансдуцирующие фаги. Их используют в качестве векторов в генной инженерии.

Изучение бактериофагов • Для выделения бактериофага исследуемый материал (воду, испражнения, почву и др. ) засевают в жидкую питательную среду, инкубируют в термостате, и через сутки помутневшую жидкость пропускают через бумажный, а затем через бактериальный фильтры, асбестовые пластины, керамические свечи. • Полученный фильтрат исследуют на наличие бактериофага путем совместного посева с подходящей микробной культурой на плотные или в жидкие питательные среды. • Если бактериофаг выделился, то после 18 часовой инкубации на поверхности агара вырастает сплошной газон культуры с прозрачными бляшками — зонами лизиса (на рисунке). В бульоне бактериофаг обусловливает просветление среды.

Применение БФ • Метод фаготипирования, основанный на исключительной специфичности определенных фаговых штаммов, позволил распределить на фаготипы ряд штаммов бактерий, неотличимых друг от друга по другим признакам. Фаготипирование с успехом применяют для идентификации типов кишечной палочки, сальмонелл (включая возбудителя брюшного тифа), стафилококков и др. Этот метод дает эпидемиологам возможность отследить цепочку случаев заболевания и определить источник инфекции. • Бактериофаги- маркеры прекрасно подходят для быстрого обнаружения небольших количеств патогенных бактерий во внешней среде: появляются и множатся хозяева — нарастает титр специфического бактериофага. Определение колифагов стало одним из ключевых мероприятий в санитарном контроле вод, поскольку позволяет выявить фекальное загрязнение даже при малом количестве кишечной палочки, не определяемом бактериологическими методами. • Лечение БФ (свободно проникают в кровь и лимфу и выводятся через почки с мочой. ; не вызывают побочных эффектов и аллергии. Не подавляют рост нормофлоры, не ослабляют иммунитет; подходят для пациентов любого возраста, нет противопоказаний. ) • Фаги применяются и в борьбе с бактериальными вредителями различных технических брожений, и в производстве ферментов с помощью бактериальных культур.

Современные лечебные цели назначения БФ • Элиминация бактериальных инфекций без риска развития осложнений на печень, почки и другие жизненно важные органы, подвергающиеся повреждающему действию обычных антибактериальных средств. • Локальность цели - уничтожают только определенные бактерии, не вызывая дисбактериоз. • При отсутствии эффекта от применения антибиотиков (при устойчивости бактерий к антибиотикам) и наличии хронической, рецидивирующей инфекции, бактериофаги являются отличным выбором в качестве препаратов антибактериальной терапии.

Причины не эффективности БФ • Каждый бактериофаг инфицирует только строго определенный вид бактерий или даже определенный штамм, что требует проведения бактериологического исследования биологического материала больного с целью фаготипирования, а следовательно, отсрочивает начало фаготерапии; • Для поддержания активности бактериофаги требуют особых условий хранения и транспортировки. • Бактериофаги не действуют на внутриклеточных микроорганизмов. • Многие бактериофаги инактивируются в условиях низкого р. Н желудка при пероральном применении препаратов, а также ингибируются неспецифическим действием различных факторов в жидкостях организма.

Почему они до сих пор не уничтожили всех бактерий? Если бактериофаги атакуют любых бактерий и их численность настолько велика (фаги — самые многочисленные вирусные формы в биосфере Земли, их общее количество — 1030– 1032 фаговых частиц , что примерно равно количеству бактерий, 4– 6× 1030)? ? ? ? Почему они до сих пор не уничтожили всех бактерий? Ответ: в процессе эволюционного соразвития бактерии выработали «иммунитет» против фагов. Во-первых, бактерия может быть изначально лишена рецепторов к тому или иному фагу или лишиться их посредством мутаций. Во-вторых, бактерия может быть иммунизирована уже «прописавшимися» в ней профагами, которые с помощью специфических репрессоров просто не дадут вновь прибывшим сородичам размножиться. В-третьих, бактерия (или ее мобильные генетические элементы) кодирует рестрикционно-модификационные системы, которые просто рубят на кусочки нуклеиновые кислоты, не содержащие особых метильных меток — подписей «я свой» .

• А в-четвертых. . . В 2005 году стало известно, что функциональной основой бактериального иммунитета является система CRISPR( clustered regularly interspaced short palindromic repeats/CRISPR-associated genes (proteins). По русски- сгруппированные регулярно перемежающиеся короткие палиндромные повторы и ассоциированные с ними гены (белки)и белок Cas, а в 2012 -м уже появилась возможность создания инженерных систем на основе CRISPR-Cas 9* Streptococcus pyogenes. • Работа системы CRISPR-Cas основана на том, что На основе спейсеров синтезируются молекулы РНК, комплементарные соответствующему участку фагового (или плазмидного) генома. Эти РНК в комплексе с белками Cas затем опознают и обезвреживают мишень — чужеродную ДНК с комплементарной последовательностью нуклеотидов. Таким образом, если в клетку однажды проникла фаговая ДНК, но клетка выжила и встроила фрагмент чужеродного генома в свой нуклеоид, то последующие попытки таких же фагов эксплуатировать клетку или ее потомков будут неэффективны [24].

• CRISPR-кассета и прилегающий к ней кластер генов cas. • Кассета — это блок прямых «зеркальных» , взаимокомплементарных последовательностей, способных складываться в шпильки повторов размером 24– 48 пар нуклеотидов. • Эти повторы перемежаются спейсерами — уникальными вставками примерно такой же длины. Спейсеры идентичны различным участкам фагов и других мобильных элементов, когда-либо проникавших в эту клетку или ее предков. • Таким образом, CRISPR можно считать коллекцией разделенных повторами «фотографий» нарушителей клеточных границ. • ЕШЕ РАЗ!!!! небольшой фрагмент, вырезанный из проникшей в бактериальную клетку фаговой ДНК, вставляется в специальный участок (локус CRISPR) генома бактерии. Каждый локус CRISPR содержит множество таких вставок (спейсеров, разделенных особыми короткими нуклеотидными повторами), представляющих собой фрагменты ДНК встреченных когда-либо фагов и плазмид. • Составляется эта коллекция простым заимствованием их кусочков, а чтобы противостоять новой инвазии этих же

• Гены cas кодируют белки, берущие на себя всю тяжесть работы по встраиванию спейсеров и уничтожению агентов с идентичными последовательностями (протоспейсерами) и помогающие процессировать CRISPRтранскрипт: разделять фото-гирлянду на отдельные портреты. • Функцию уничтожения выполняют эффекторные Cas-белки. • При обнаружении комплементарной cr. РНК последовательности, то есть протоспейсера, модуль «слипается» с ней и определяет, не помечена ли она как «своя» , клеточная. Если нет, и если к ней прилегает тот самый PAM, то эффекторный белок, который представляет собой эндонуклеазу и разрезает цепи ДНК. • Ну и появляется лишняя возможность «получит » новые спейсеры. !!!!!

Зачем это МНЕ? ? ? ? Можно применять у эукариот!!!!!? Будем все здоровы, генетический подход к терапии рака и «врожденныхнаследуемых» заболеваний • Всё, что требовалось для ИСПОЛЬЗОВАНИЯ новой технологии, — это разместить на векторах ген белка Cas и CRISPR-кассету, где спейсеры сделать идентичными местам генома, которые нужно изменить. • Меняя число и тип спейсеров, можно модифицировать сразу несколько разных участков генома. • Ну и еще потребовалось оптимизировать систему для эукариотических клеток: подправить кодонный состав и добавить ядерный «адрес» , чтобы она четко следовала к месту работы — хромосомам. • Когда СИСТЕМА находит комплементарный участок в геноме организма, Cas разрезает «натупо» обе цепи ДНК. Всё, работа CRISPR-системы на этом окончена. • Теперь эстафета передается репарационным системам самогό организма. Они решают, как лучше залатать разрез: то ли просто сшить куски (это будет негомологичное соединение концов, NHEJ), то ли, если есть подходящая матрица с флангами, комплементарными участкам ДНК с двух сторон от разрыва, поставить «заплатку» (это будет гомологичная рекомбинация). • Первый вариант выгоден, если нужно что-то вырезать, второй — если нужно что-то вставить или заменить дефектный участок ДНК на нормальный, который просто вводят на подходящем векторе.

Примеры • для улучшения свойств сельскохозяйственных животных и растений. Уже создали и протестировали CRISPR-системы для риса, пшеницы, кукурузы, сорго и многих других культур. • Помимо улучшения пищевых качеств, такими инструментами легко наделять культуры устойчивостью к вредителям и химикалиям, а животных — избавлять от нежелательных генов • для контроля распространения инфекций, переносимых животными. Например, уже всерьез размышляют о «заносе» в природные популяции малярийных комаров генов устойчивости к малярии. • «CRISPR — для терапии» . Здесь пределов для фантазии, кажется, и вовсе нет. Если говорить о наследственных заболеваниях, то CRISPR-Cas 9 в культурах клеток или животных моделях уже «примерили» для серповидноклеточной анемии, миодистрофии Дюшенна, муковисцидоза…. .

БАКТЕРИОФАГИ НТВ.pptx