testy_gidroliz.pptx
- Количество слайдов: 34
 ОМСКАЯ ГОСУДАРСТВЕННАЯ МЕДИЦИНСКАЯ АКАДЕМИЯ КАФЕДРА ХИМИИ Тесты «Гидролиз солей» Составитель: доктор биологических наук, профессор, зав. кафедрой химии Ирина Петровна Степанова
ОМСКАЯ ГОСУДАРСТВЕННАЯ МЕДИЦИНСКАЯ АКАДЕМИЯ КАФЕДРА ХИМИИ Тесты «Гидролиз солей» Составитель: доктор биологических наук, профессор, зав. кафедрой химии Ирина Петровна Степанова
 1. При сливании растворов хлорида алюминия и карбоната натрия: 1) образуется 3) выделяется газ, а только осадок, а газ не выделяется раствор остается прозрачным 2) образуется 4) ничего не осадок и выделяется происходит газ
1. При сливании растворов хлорида алюминия и карбоната натрия: 1) образуется 3) выделяется газ, а только осадок, а газ не выделяется раствор остается прозрачным 2) образуется 4) ничего не осадок и выделяется происходит газ
 2. В водных растворах не подвергается гидролизу: 1) сульфат натрия 2) сульфит натрия 3) сульфат алюминия 4) сульфат меди
2. В водных растворах не подвергается гидролизу: 1) сульфат натрия 2) сульфит натрия 3) сульфат алюминия 4) сульфат меди
 3. В водных растворах не подвергается гидролизу хлорид 1) меди 3) цинка 2) бария 4) бериллия
3. В водных растворах не подвергается гидролизу хлорид 1) меди 3) цинка 2) бария 4) бериллия
 4. В водных растворах необратимо гидролизуются 1) нитрат железа(III) 2) фосфат натрия 3) сульфид алюминия 4) карбонат аммония
4. В водных растворах необратимо гидролизуются 1) нитрат железа(III) 2) фосфат натрия 3) сульфид алюминия 4) карбонат аммония
 5. Гидролиз по аниону имеет место в водных растворах: 1) K 2 SO 4 3) CH 3 COONa 2) Fe. SO 4 4) KCl
5. Гидролиз по аниону имеет место в водных растворах: 1) K 2 SO 4 3) CH 3 COONa 2) Fe. SO 4 4) KCl
 6. Полному и необратимому гидролизу подвергается: 1) силикат натрия 3) сульфид калия 2) сульфид алюминия 4) хлорид бария
6. Полному и необратимому гидролизу подвергается: 1) силикат натрия 3) сульфид калия 2) сульфид алюминия 4) хлорид бария
 7. И анион, и катион гидролизуются в растворе соли 1) ацетат калия 2) хлорид меди(II) 3) силикат натрия 4) сульфид аммония
7. И анион, и катион гидролизуются в растворе соли 1) ацетат калия 2) хлорид меди(II) 3) силикат натрия 4) сульфид аммония
 8. Только анион гидролизуется в растворе соли: 1) ацетат аммония 2) иодид калия 3) бромид алюминия 4) фторид натрия
8. Только анион гидролизуется в растворе соли: 1) ацетат аммония 2) иодид калия 3) бромид алюминия 4) фторид натрия
 9. При растворении в воде хлорида цинка среда становится 1) нейтральной 2) кислой 3) щелочной 4) слабощелочной
9. При растворении в воде хлорида цинка среда становится 1) нейтральной 2) кислой 3) щелочной 4) слабощелочной
 10. При растворении в воде сульфида калия среда становится 1) кислой 2) щелочной 3) нейтральной 4) не изменяется
10. При растворении в воде сульфида калия среда становится 1) кислой 2) щелочной 3) нейтральной 4) не изменяется
 11. Щелочную среду имеет раствор 1) нитрата аммония 3) силиката натрия 2) хлорида цинка 4) сульфата калия
11. Щелочную среду имеет раствор 1) нитрата аммония 3) силиката натрия 2) хлорида цинка 4) сульфата калия
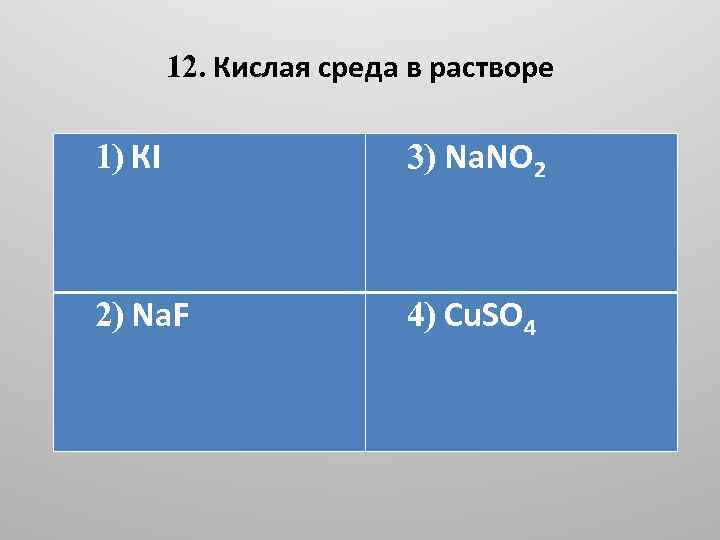 12. Кислая среда в растворе 1) КI 3) Na. NO 2 2) Na. F 4) Cu. SO 4
12. Кислая среда в растворе 1) КI 3) Na. NO 2 2) Na. F 4) Cu. SO 4
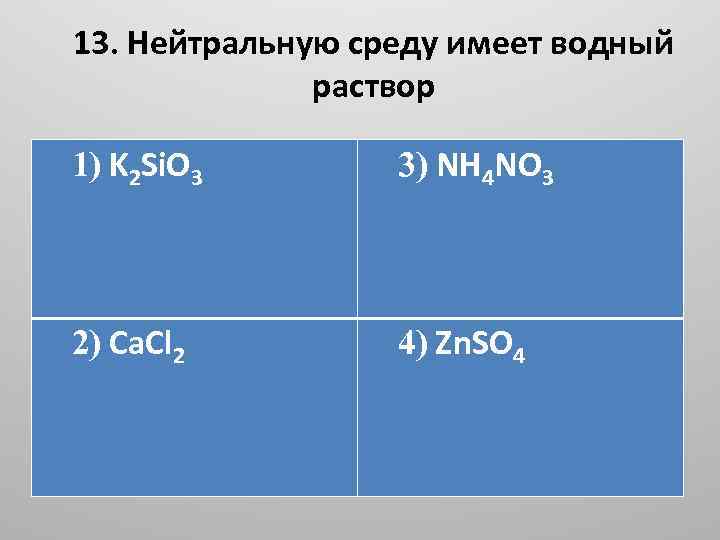 13. Нейтральную среду имеет водный раствор 1) K 2 Si. O 3 3) NH 4 NO 3 2) Ca. Cl 2 4) Zn. SO 4
13. Нейтральную среду имеет водный раствор 1) K 2 Si. O 3 3) NH 4 NO 3 2) Ca. Cl 2 4) Zn. SO 4
 14. Нейтральная среда в растворе 1) нитрата натрия а) +(0, 06– 1, 00); б) +(0, 8– 1, 40); 2) сульфита калия 3) фторида калия в) +(1, 02– 1, 30); г) +(0, 6– 0, 90). 4) ацетата натрия
14. Нейтральная среда в растворе 1) нитрата натрия а) +(0, 06– 1, 00); б) +(0, 8– 1, 40); 2) сульфита калия 3) фторида калия в) +(1, 02– 1, 30); г) +(0, 6– 0, 90). 4) ацетата натрия
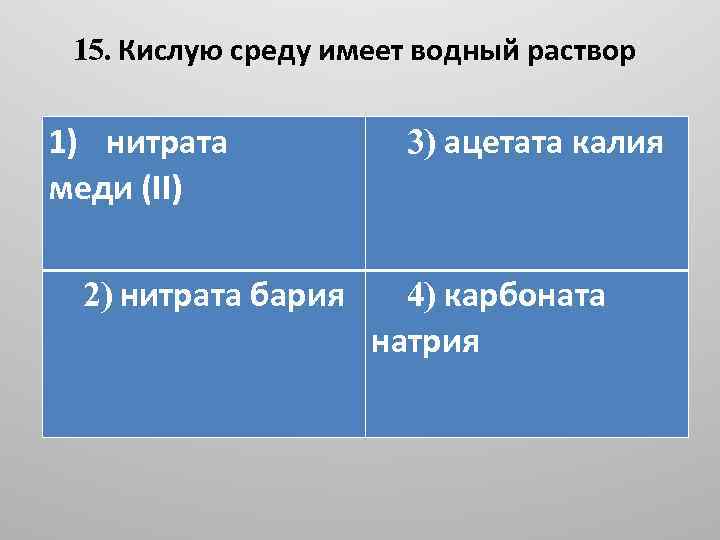 15. Кислую среду имеет водный раствор 1) нитрата меди (II) 2) нитрата бария 3) ацетата калия 4) карбоната натрия
15. Кислую среду имеет водный раствор 1) нитрата меди (II) 2) нитрата бария 3) ацетата калия 4) карбоната натрия
 16. Кислая среда в растворе 1) Fе. Сl 3 3) KCl 2) Na 3 PO 4 4) Nа. НСО 3
16. Кислая среда в растворе 1) Fе. Сl 3 3) KCl 2) Na 3 PO 4 4) Nа. НСО 3
 17. Щелочную среду имеет водный раствор: 1) хлорида цинка 3) бромида натрия 2) фторида 4) хлорида калия алюминия
17. Щелочную среду имеет водный раствор: 1) хлорида цинка 3) бромида натрия 2) фторида 4) хлорида калия алюминия
 18. Одинаковую реакцию среды имеют растворы хлорида меди (II) 1) хлорида натрия 2) хлорида калия 3) ацетата кальция 4) нитрата цинка
18. Одинаковую реакцию среды имеют растворы хлорида меди (II) 1) хлорида натрия 2) хлорида калия 3) ацетата кальция 4) нитрата цинка
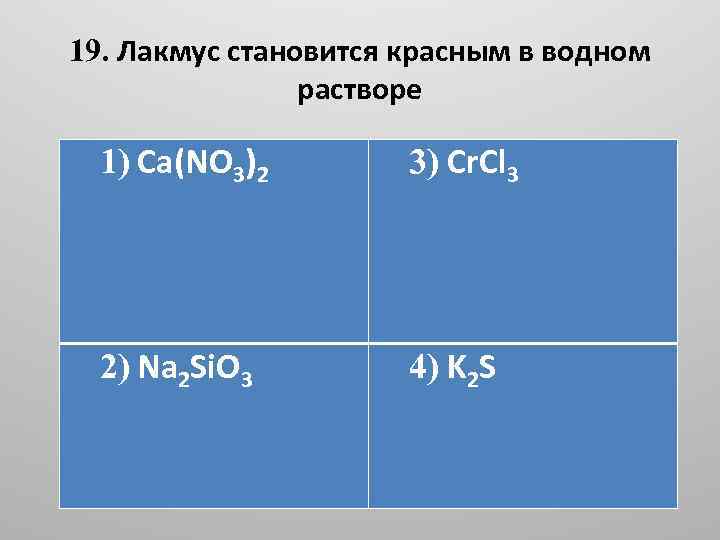 19. Лакмус становится красным в водном растворе 1) Ca(NO 3)2 3) Cr. Cl 3 2) Na 2 Si. O 3 4) K 2 S
19. Лакмус становится красным в водном растворе 1) Ca(NO 3)2 3) Cr. Cl 3 2) Na 2 Si. O 3 4) K 2 S
 20. В растворе йодида цинка лакмус имеет окраску 1) зелёную 2) красную 3) синюю 4) фиолетовую
20. В растворе йодида цинка лакмус имеет окраску 1) зелёную 2) красную 3) синюю 4) фиолетовую
 21. В растворе нитрата алюминия метилоранж имеет окраску 1) оранжевую 3) бесцветную 2) красную 4) жёлтую
21. В растворе нитрата алюминия метилоранж имеет окраску 1) оранжевую 3) бесцветную 2) красную 4) жёлтую
 22. Лакмус станет синим в растворе 1) сульфида калия 2) хлорида цинка 3) нитрата магния 4) сульфата натрия
22. Лакмус станет синим в растворе 1) сульфида калия 2) хлорида цинка 3) нитрата магния 4) сульфата натрия
 23. Фенолфталеин приобретёт малиновую окраску в растворе 1) карбоната натрия 3) нитрата бария 2) сульфата меди 4) хлорида калия
23. Фенолфталеин приобретёт малиновую окраску в растворе 1) карбоната натрия 3) нитрата бария 2) сульфата меди 4) хлорида калия
 24. Гидролиз какой соли описывается уравнением S 2 - + H 2 O ⇄ HS- + OH- 1) сульфида алюминия 3) сульфида аммония 2) ) 4) сульфида гидросульфида натрия
24. Гидролиз какой соли описывается уравнением S 2 - + H 2 O ⇄ HS- + OH- 1) сульфида алюминия 3) сульфида аммония 2) ) 4) сульфида гидросульфида натрия
 25. В результате гидролиза хлорида аммония: 3) уменьшается 1) увеличивается концентрация гидроксид-ионов в растворе 2) концентрация ионов водорода и гидроксид-ионов в растворе остается неизменной концентрация ионов водорода в растворе 4) увеличивается концентрация ионов водорода в растворе
25. В результате гидролиза хлорида аммония: 3) уменьшается 1) увеличивается концентрация гидроксид-ионов в растворе 2) концентрация ионов водорода и гидроксид-ионов в растворе остается неизменной концентрация ионов водорода в растворе 4) увеличивается концентрация ионов водорода в растворе
 26. В результате гидролиза ацетата натрия: 1) увеличивается концентрация гидроксид-ионов в растворе 2) концентрация ионов водорода и гидроксид-ионов в растворе остается неизменной 3) уменьшается концентрация ионов водорода в растворе 4) увеличивается концентрация ионов водорода в растворе
26. В результате гидролиза ацетата натрия: 1) увеличивается концентрация гидроксид-ионов в растворе 2) концентрация ионов водорода и гидроксид-ионов в растворе остается неизменной 3) уменьшается концентрация ионов водорода в растворе 4) увеличивается концентрация ионов водорода в растворе
 27. Раствор какой соли можно отличить от других с помощью лакмуса? . 1) К 2 SO 3 3) Рb(NO 3)2 2) Аl. Br 3 4) Zn. SО 4
27. Раствор какой соли можно отличить от других с помощью лакмуса? . 1) К 2 SO 3 3) Рb(NO 3)2 2) Аl. Br 3 4) Zn. SО 4
 28. Раствор какой соли можно отличить от других с помощью фенолфталеина? 1) Sr(NO 3)2 3) КСl. O 4 2) Li. I 4) Na. Cl. O
28. Раствор какой соли можно отличить от других с помощью фенолфталеина? 1) Sr(NO 3)2 3) КСl. O 4 2) Li. I 4) Na. Cl. O
 29. Какие ионы присутствуют в водном растворе фосфата натрия? 1) Na+, PO 43–, 3) Na+, PO 43–, OH– H 2 PO 4–, HPO 42–, OH– , H+ 2) Na+, PO 43– 4) Na+, PO 43–, OH–
29. Какие ионы присутствуют в водном растворе фосфата натрия? 1) Na+, PO 43–, 3) Na+, PO 43–, OH– H 2 PO 4–, HPO 42–, OH– , H+ 2) Na+, PO 43– 4) Na+, PO 43–, OH–
 30. Установите соответствие между формулой соли и средой ее водного раствора (формула соли --- среда раствора) a) K 2 SO 4 1) нейтральная b) Cr. Cl 3 в) Li 2 CO 3 г) NH 4 Br 2) кислая 3) щелочная 4) слабощелочная
30. Установите соответствие между формулой соли и средой ее водного раствора (формула соли --- среда раствора) a) K 2 SO 4 1) нейтральная b) Cr. Cl 3 в) Li 2 CO 3 г) NH 4 Br 2) кислая 3) щелочная 4) слабощелочная
 31. Установите соответствие между формулой соли и средой ее водного раствора (формула соли --- тип гидролиза) a) K 2 SO 4 b) NH 4 F в) СН 3 СООNa г) NH 4 Br 1) по катиону 2) по аниону 3) по катиону и аниону 4) гидролизу не подвергается
31. Установите соответствие между формулой соли и средой ее водного раствора (формула соли --- тип гидролиза) a) K 2 SO 4 b) NH 4 F в) СН 3 СООNa г) NH 4 Br 1) по катиону 2) по аниону 3) по катиону и аниону 4) гидролизу не подвергается
 32. Установите соответствие между формулой соли и окраской лакмуса в ее водном растворе (формула соли --- окраска раствора) a) нитрат лития b) силикат кальция в) роданид натрия г) ацетат калия 1) фиолетовая 2) красная 3) синяя 4) малиновая
32. Установите соответствие между формулой соли и окраской лакмуса в ее водном растворе (формула соли --- окраска раствора) a) нитрат лития b) силикат кальция в) роданид натрия г) ацетат калия 1) фиолетовая 2) красная 3) синяя 4) малиновая
 33. Чтобы ослабить или прекратить гидролиз в растворе хлоридa алюминия необходимо: 1) добавить воду 3) добавить серную кислоту 2) добавить 4) охладить гидроксид натрия раствор
33. Чтобы ослабить или прекратить гидролиз в растворе хлоридa алюминия необходимо: 1) добавить воду 3) добавить серную кислоту 2) добавить 4) охладить гидроксид натрия раствор


