СтереоизомерияОВ.ppt
- Количество слайдов: 32
 ОМСКАЯ ГОСУДАРСТВЕННАЯ МЕДИЦИНСКАЯ АКАДЕМИЯ КАФЕДРА ХИМИИ ОРГАНИЧЕСКАЯ ХИМИЯ Пространственное строение органических соединений 1. Энантиомерия. 2. Ϭ-диастереомерия. 3. π-диастереомерия. Лектор: кандидат биологических наук, доцент Атавина Ольга Васильевна
ОМСКАЯ ГОСУДАРСТВЕННАЯ МЕДИЦИНСКАЯ АКАДЕМИЯ КАФЕДРА ХИМИИ ОРГАНИЧЕСКАЯ ХИМИЯ Пространственное строение органических соединений 1. Энантиомерия. 2. Ϭ-диастереомерия. 3. π-диастереомерия. Лектор: кандидат биологических наук, доцент Атавина Ольга Васильевна
 Цели лекции: 1. Обучающая - Сформировать знания о конфигурационных видах стереоизомерии. 2. Развивающая – Расширить кругозор обучающихся на основе интеграции знаний; развивать логическое мышление. 3. Воспитательная – Содействовать формированию у обучающихся устойчивого интереса к изучению дисциплины «Органическая химия»
Цели лекции: 1. Обучающая - Сформировать знания о конфигурационных видах стереоизомерии. 2. Развивающая – Расширить кругозор обучающихся на основе интеграции знаний; развивать логическое мышление. 3. Воспитательная – Содействовать формированию у обучающихся устойчивого интереса к изучению дисциплины «Органическая химия»
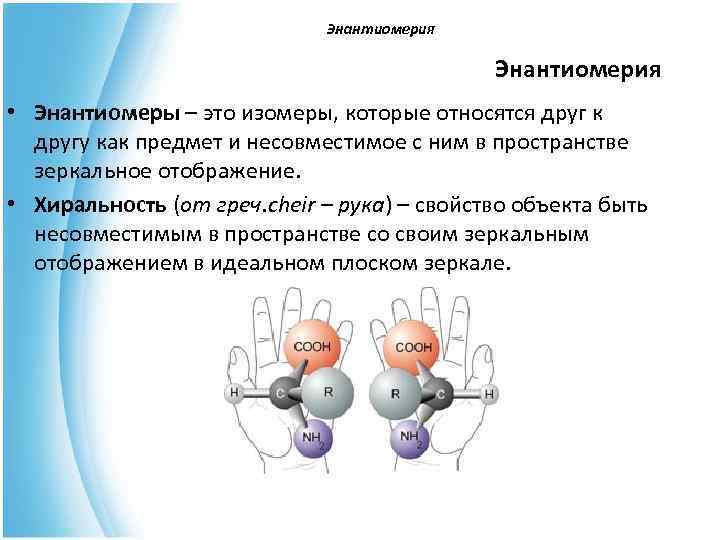 Энантиомерия • Энантиомеры – это изомеры, которые относятся друг к другу как предмет и несовместимое с ним в пространстве зеркальное отображение. • Хиральность (от греч. cheir – рука) – свойство объекта быть несовместимым в пространстве со своим зеркальным отображением в идеальном плоском зеркале.
Энантиомерия • Энантиомеры – это изомеры, которые относятся друг к другу как предмет и несовместимое с ним в пространстве зеркальное отображение. • Хиральность (от греч. cheir – рука) – свойство объекта быть несовместимым в пространстве со своим зеркальным отображением в идеальном плоском зеркале.
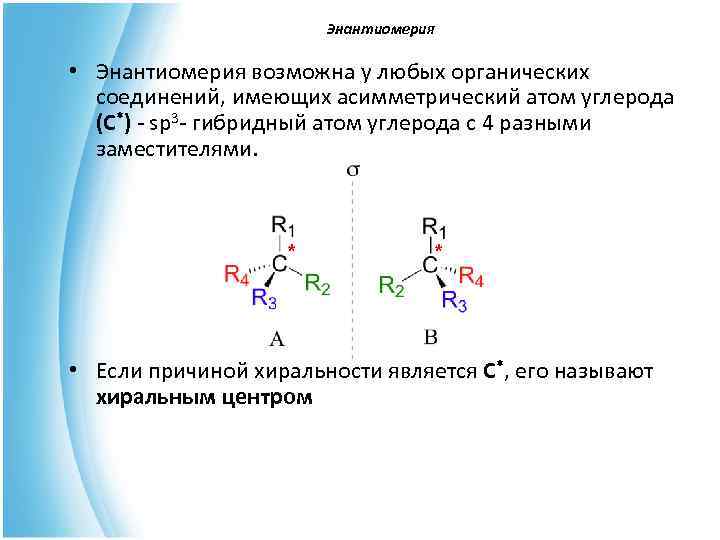 Энантиомерия • Энантиомерия возможна у любых органических соединений, имеющих асимметрический атом углерода (C*) - sp 3 - гибридный атом углерода с 4 разными заместителями. * • Если причиной хиральности является C*, его называют хиральным центром
Энантиомерия • Энантиомерия возможна у любых органических соединений, имеющих асимметрический атом углерода (C*) - sp 3 - гибридный атом углерода с 4 разными заместителями. * • Если причиной хиральности является C*, его называют хиральным центром
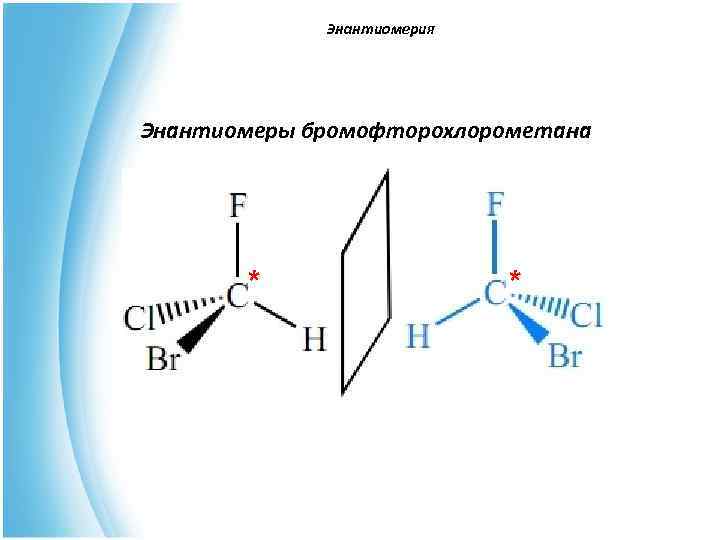 Энантиомерия Энантиомеры бромофторохлорометана *
Энантиомерия Энантиомеры бромофторохлорометана *
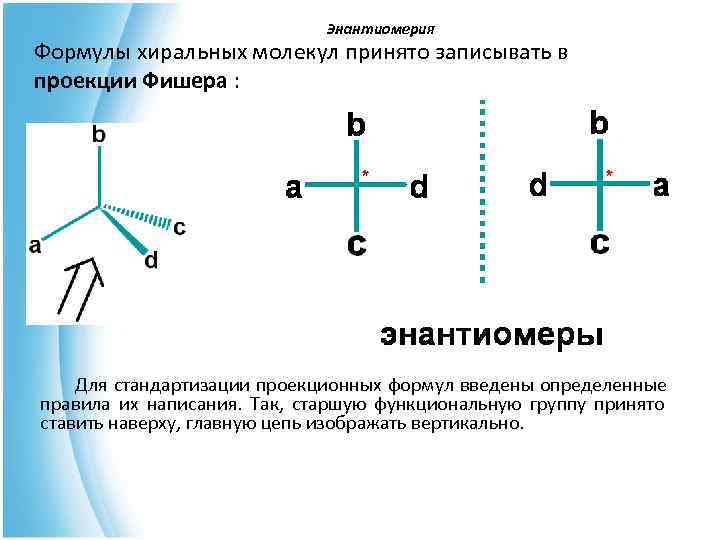 Энантиомерия Формулы хиральных молекул принято записывать в проекции Фишера : * Для стандартизации проекционных формул введены определенные правила их написания. Так, старшую функциональную группу принято ставить наверху, главную цепь изображать вертикально.
Энантиомерия Формулы хиральных молекул принято записывать в проекции Фишера : * Для стандартизации проекционных формул введены определенные правила их написания. Так, старшую функциональную группу принято ставить наверху, главную цепь изображать вертикально.
 Энантиомерия Для того, чтобы сопоставить «нестандартно» написанные проекционные формулы не меняя их стереохимического смысла, существуют правила их преобразования: 1) формулы можно вращать в плоскости чертежа на 180°, не меняя их стереохимического смысла. 2) можно производить две (или любое четное число) перестановок заместителей у одного асимметрического атома, не меняя их стереохимического смысла. A B 1 2 C D C B C A B D 3) поворот на 90° или любое нечетное число перестановок приводит к формуле с противоположной конфигурацией.
Энантиомерия Для того, чтобы сопоставить «нестандартно» написанные проекционные формулы не меняя их стереохимического смысла, существуют правила их преобразования: 1) формулы можно вращать в плоскости чертежа на 180°, не меняя их стереохимического смысла. 2) можно производить две (или любое четное число) перестановок заместителей у одного асимметрического атома, не меняя их стереохимического смысла. A B 1 2 C D C B C A B D 3) поворот на 90° или любое нечетное число перестановок приводит к формуле с противоположной конфигурацией.
 Энантиомерия • Энантиомеры имеют одинаковые физические и химические свойства. • Различаются энантиомеры знаком оптической активности, измерение которой проводят экспериментально с помощью поляриметра. Проходя через специальную призму Николя свет становится плоскополяризованным. Энантиомер, который отклоняет плоскость поляризации влево, называется левовращающим и обозначается знаком (-); вправо – правовращающим (+). • Смесь энантиомеров называется рацематом (оптически не активна).
Энантиомерия • Энантиомеры имеют одинаковые физические и химические свойства. • Различаются энантиомеры знаком оптической активности, измерение которой проводят экспериментально с помощью поляриметра. Проходя через специальную призму Николя свет становится плоскополяризованным. Энантиомер, который отклоняет плоскость поляризации влево, называется левовращающим и обозначается знаком (-); вправо – правовращающим (+). • Смесь энантиомеров называется рацематом (оптически не активна).
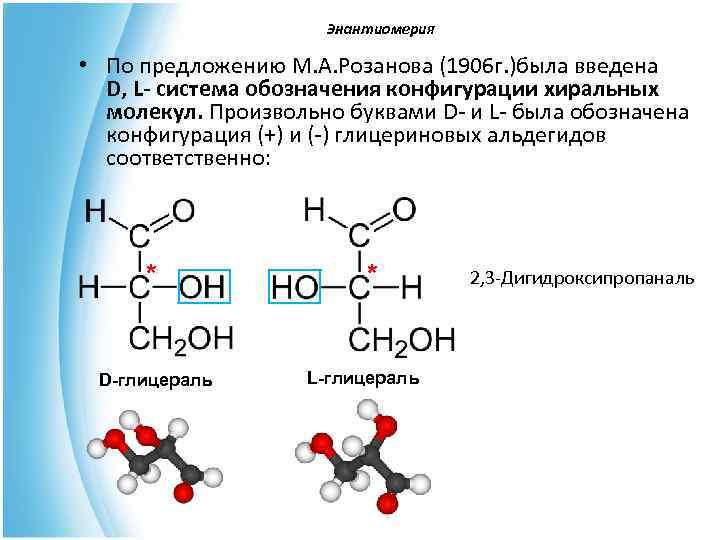 Энантиомерия • По предложению M. А. Розанова (1906 г. )была введена D, L- система обозначения конфигурации хиральных молекул. Произвольно буквами D- и L- была обозначена конфигурация (+) и (-) глицериновых альдегидов соответственно: * 2, 3 -Дигидроксипропаналь D-глицераль L-глицераль
Энантиомерия • По предложению M. А. Розанова (1906 г. )была введена D, L- система обозначения конфигурации хиральных молекул. Произвольно буквами D- и L- была обозначена конфигурация (+) и (-) глицериновых альдегидов соответственно: * 2, 3 -Дигидроксипропаналь D-глицераль L-глицераль
 Энантиомерия • Хиральные молекулы, имеющие такую же конфигурацию хирального атома углерода, как D-(+)-глицериновый альдегид, относятся к D-стереохимическому ряду и, соответственно, к L-ряду, при совпадении конфигурации с L-(-)-глицериновым альдегидом.
Энантиомерия • Хиральные молекулы, имеющие такую же конфигурацию хирального атома углерода, как D-(+)-глицериновый альдегид, относятся к D-стереохимическому ряду и, соответственно, к L-ряду, при совпадении конфигурации с L-(-)-глицериновым альдегидом.
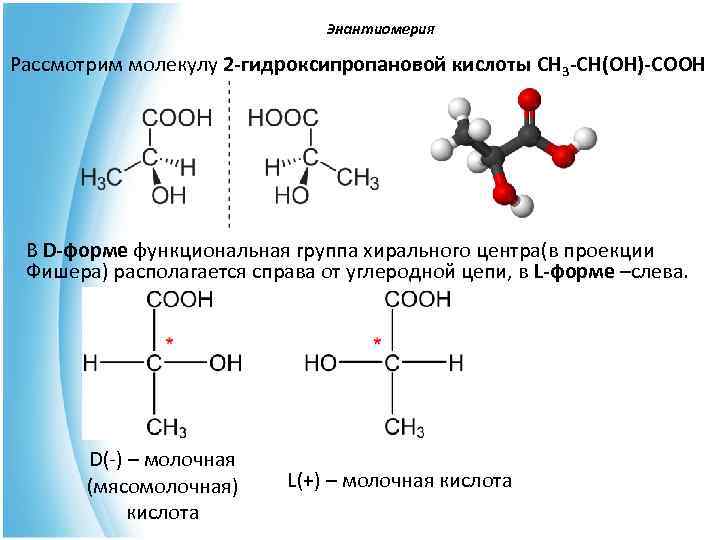 Энантиомерия Рассмотрим молекулу 2 -гидроксипропановой кислоты CH 3 -CH(OH)-COOH В D-форме функциональная группа хирального центра(в проекции Фишера) располагается справа от углеродной цепи, в L-форме –слева. D(-) – молочная (мясомолочная) L(+) – молочная кислота
Энантиомерия Рассмотрим молекулу 2 -гидроксипропановой кислоты CH 3 -CH(OH)-COOH В D-форме функциональная группа хирального центра(в проекции Фишера) располагается справа от углеродной цепи, в L-форме –слева. D(-) – молочная (мясомолочная) L(+) – молочная кислота
 Энантиомерия • В настоящее время D, L -система находит применение в основном в химии углеводов, аминокислот и родственных с ними соединений. • Более современной номенклатурой энантиомеров является R, S-система обозначений (Кан, Ингольд и Прелог), которая отражает абсолютную конфигурацию хиральных атомов углерода в молекуле. • R, S-номенклатура основана на правилах последовательного старшинства. Объективным критерием старшинства является величина атомного номера : старшим считается атом с большим атомным номером I(53) > Br(35) > Cl(17) > S(16) > P(15) > F(9) > N(7) > C(6) > H(1)
Энантиомерия • В настоящее время D, L -система находит применение в основном в химии углеводов, аминокислот и родственных с ними соединений. • Более современной номенклатурой энантиомеров является R, S-система обозначений (Кан, Ингольд и Прелог), которая отражает абсолютную конфигурацию хиральных атомов углерода в молекуле. • R, S-номенклатура основана на правилах последовательного старшинства. Объективным критерием старшинства является величина атомного номера : старшим считается атом с большим атомным номером I(53) > Br(35) > Cl(17) > S(16) > P(15) > F(9) > N(7) > C(6) > H(1)
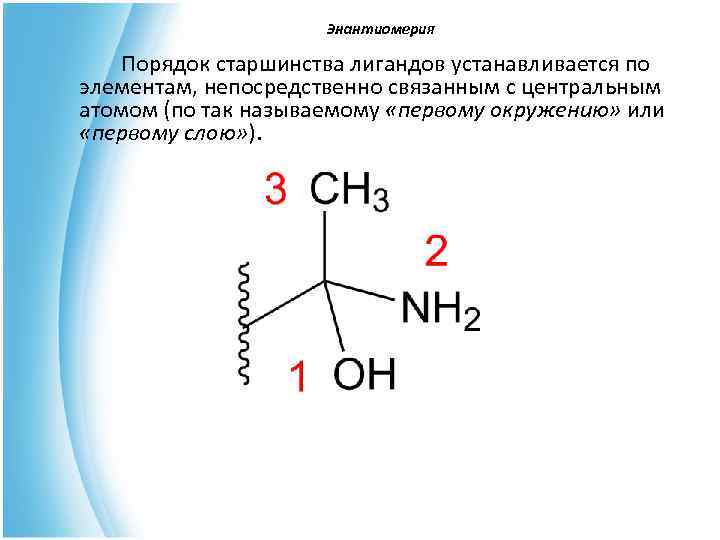 Энантиомерия Порядок старшинства лигандов устанавливается по элементам, непосредственно связанным с центральным атомом (по так называемому «первому окружению» или «первому слою» ).
Энантиомерия Порядок старшинства лигандов устанавливается по элементам, непосредственно связанным с центральным атомом (по так называемому «первому окружению» или «первому слою» ).
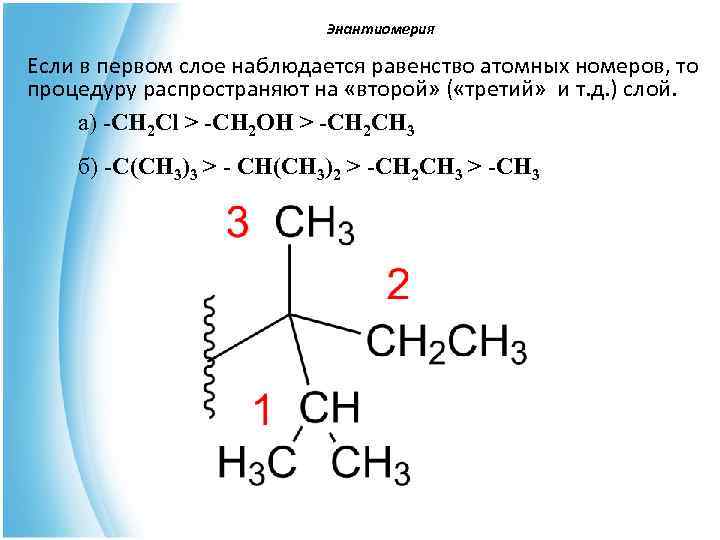 Энантиомерия Если в первом слое наблюдается равенство атомных номеров, то процедуру распространяют на «второй» ( «третий» и т. д. ) слой. а) -CH 2 Cl > -CH 2 OH > -CH 2 CH 3 б) -C(CH 3)3 > - CH(CH 3)2 > -CH 2 CH 3 > -CH 3
Энантиомерия Если в первом слое наблюдается равенство атомных номеров, то процедуру распространяют на «второй» ( «третий» и т. д. ) слой. а) -CH 2 Cl > -CH 2 OH > -CH 2 CH 3 б) -C(CH 3)3 > - CH(CH 3)2 > -CH 2 CH 3 > -CH 3
 Энантиомерия Если группа содержит двойную (тройную) связь, то её атомы следует удвоить (утроить). а) -COOCH 3 > -COOH > -CONH 2 > -CHO б)
Энантиомерия Если группа содержит двойную (тройную) связь, то её атомы следует удвоить (утроить). а) -COOCH 3 > -COOH > -CONH 2 > -CHO б)
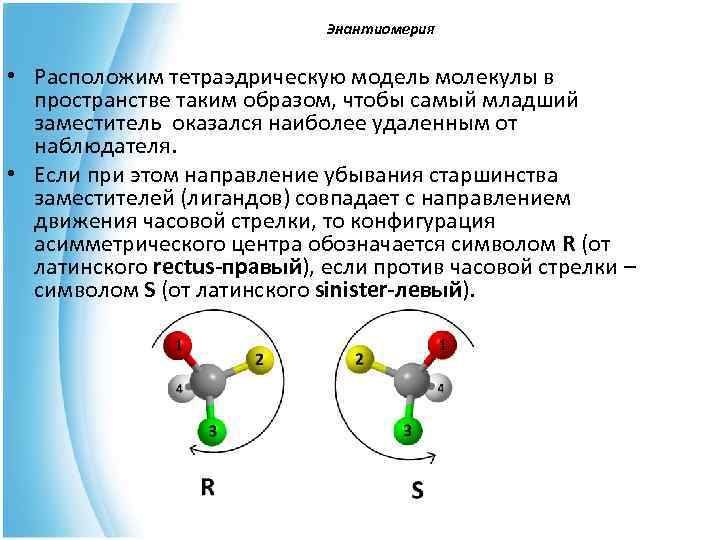 Энантиомерия • Расположим тетраэдрическую модель молекулы в пространстве таким образом, чтобы самый младший заместитель оказался наиболее удаленным от наблюдателя. • Если при этом направление убывания старшинства заместителей (лигандов) совпадает с направлением движения часовой стрелки, то конфигурация асимметрического центра обозначается символом R (от латинского rectus-правый), если против часовой стрелки – символом S (от латинского sinister-левый).
Энантиомерия • Расположим тетраэдрическую модель молекулы в пространстве таким образом, чтобы самый младший заместитель оказался наиболее удаленным от наблюдателя. • Если при этом направление убывания старшинства заместителей (лигандов) совпадает с направлением движения часовой стрелки, то конфигурация асимметрического центра обозначается символом R (от латинского rectus-правый), если против часовой стрелки – символом S (от латинского sinister-левый).
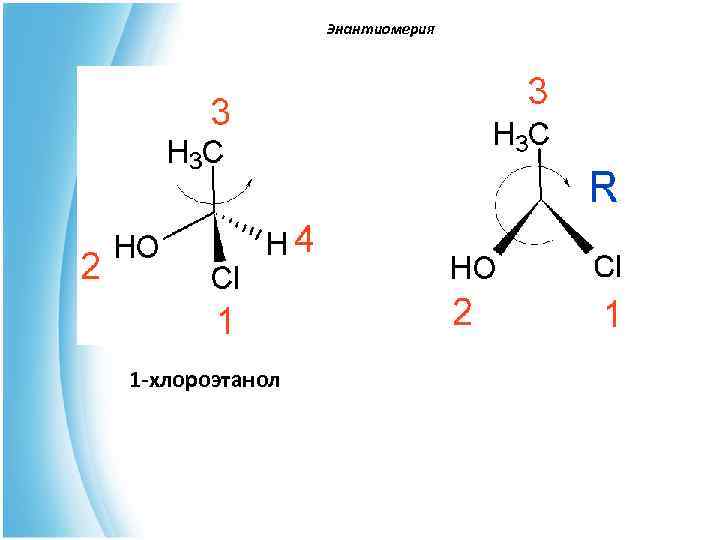 Энантиомерия 1 -хлороэтанол
Энантиомерия 1 -хлороэтанол
 Энантиомерия Обозначение конфигурации хиральных центров можно провести с применением проекционных формул Фишера. Для этого проекцию преобразуют так, чтобы младший заместитель расположился на одной из вертикальных связей (соответствует положению заместителя за плоскостью чертежа). Если после преобразования проекции падение старшинства остальных трех группировок происходит против часовой стрелки, то асимметрическому атому приписывают S- конфигурацию, в противоположном случае – R-конфигурацию.
Энантиомерия Обозначение конфигурации хиральных центров можно провести с применением проекционных формул Фишера. Для этого проекцию преобразуют так, чтобы младший заместитель расположился на одной из вертикальных связей (соответствует положению заместителя за плоскостью чертежа). Если после преобразования проекции падение старшинства остальных трех группировок происходит против часовой стрелки, то асимметрическому атому приписывают S- конфигурацию, в противоположном случае – R-конфигурацию.
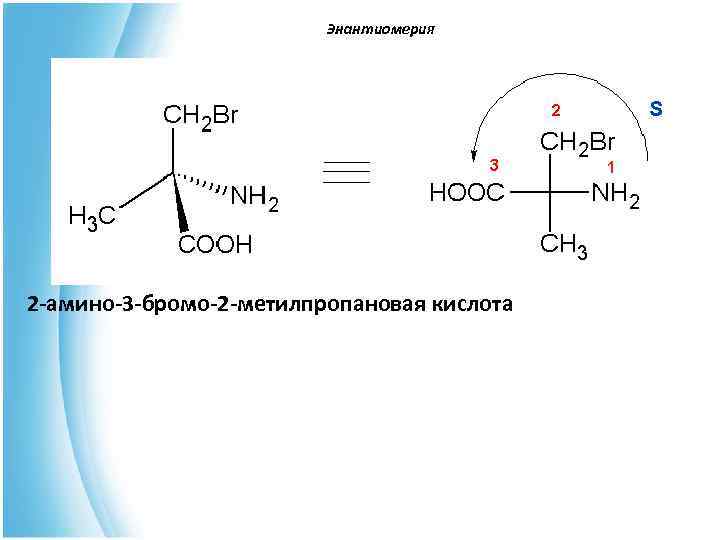 Энантиомерия 2 -амино-3 -бромо-2 -метилпропановая кислота
Энантиомерия 2 -амино-3 -бромо-2 -метилпропановая кислота
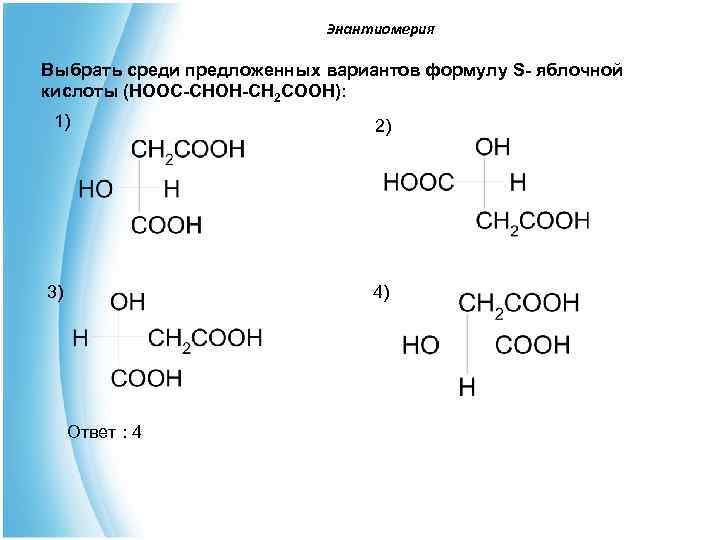 Энантиомерия Выбрать среди предложенных вариантов формулу S- яблочной кислоты (НООС-СНОН-СН 2 СООН): 1) 2) 3) 4) Ответ : 4
Энантиомерия Выбрать среди предложенных вариантов формулу S- яблочной кислоты (НООС-СНОН-СН 2 СООН): 1) 2) 3) 4) Ответ : 4
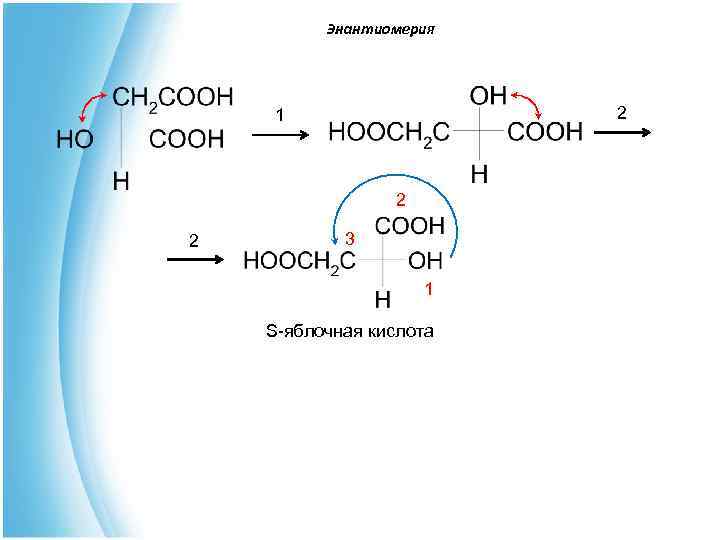 Энантиомерия 1 2 2 3 1 S-яблочная кислота
Энантиомерия 1 2 2 3 1 S-яблочная кислота
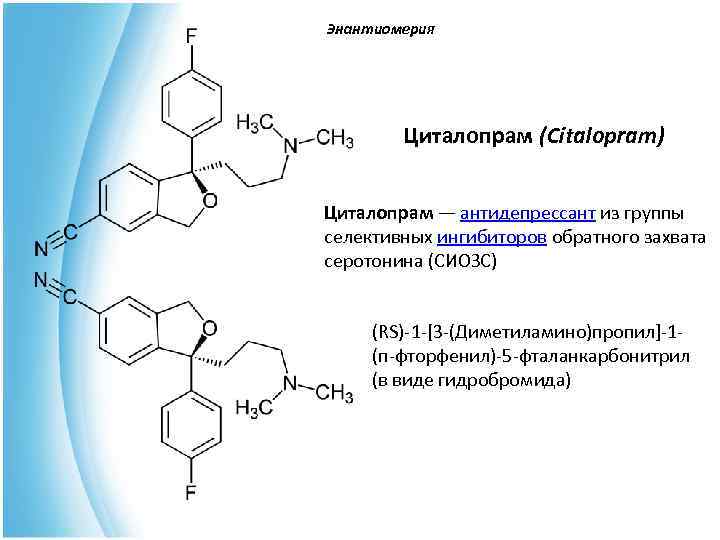 Энантиомерия Циталопрам (Citalopram) Циталопрам — антидепрессант из группы селективных ингибиторов обратного захвата серотонина (СИОЗС) (RS)-1 -[3 -(Диметиламино)пропил]-1 - (п-фторфенил)-5 -фталанкарбонитрил (в виде гидробромида)
Энантиомерия Циталопрам (Citalopram) Циталопрам — антидепрессант из группы селективных ингибиторов обратного захвата серотонина (СИОЗС) (RS)-1 -[3 -(Диметиламино)пропил]-1 - (п-фторфенил)-5 -фталанкарбонитрил (в виде гидробромида)
 Энантиомерия В отличие от рацемата циталопрама, эсциталопрам представлен только S -изомером (R-изомер не имеет терапевтического эффекта). Дозировка эсциталопрама составляет ½ от дозировки циталопрама.
Энантиомерия В отличие от рацемата циталопрама, эсциталопрам представлен только S -изомером (R-изомер не имеет терапевтического эффекта). Дозировка эсциталопрама составляет ½ от дозировки циталопрама.
 Диастереомерия • Различают σ- и π-диастереомерию. • σ-Диастереомерия возникает в молекулах с 2 и более центрами хиральности. • σ-Диастереомеры – оптические изомеры, не являющиеся зеркальным отображением друга. • Число стереоизомеров рассчитывают по формуле Фишера: Z =2 n, где Z – число стереоизомеров n – число C* (асимметрических атомов углерода)
Диастереомерия • Различают σ- и π-диастереомерию. • σ-Диастереомерия возникает в молекулах с 2 и более центрами хиральности. • σ-Диастереомеры – оптические изомеры, не являющиеся зеркальным отображением друга. • Число стереоизомеров рассчитывают по формуле Фишера: Z =2 n, где Z – число стереоизомеров n – число C* (асимметрических атомов углерода)
 Ϭ-Диастереомерия Ϭ- • D-, L-определяющим является гидроксил при нижнем асимметрическом атоме углерода (кроме гидроксикислот и аминокислот). • Если заместители находятся по одну сторону углеродной цепи, то такой изомер называется эритро-формой, по разные – трео-формой.
Ϭ-Диастереомерия Ϭ- • D-, L-определяющим является гидроксил при нижнем асимметрическом атоме углерода (кроме гидроксикислот и аминокислот). • Если заместители находятся по одну сторону углеродной цепи, то такой изомер называется эритро-формой, по разные – трео-формой.
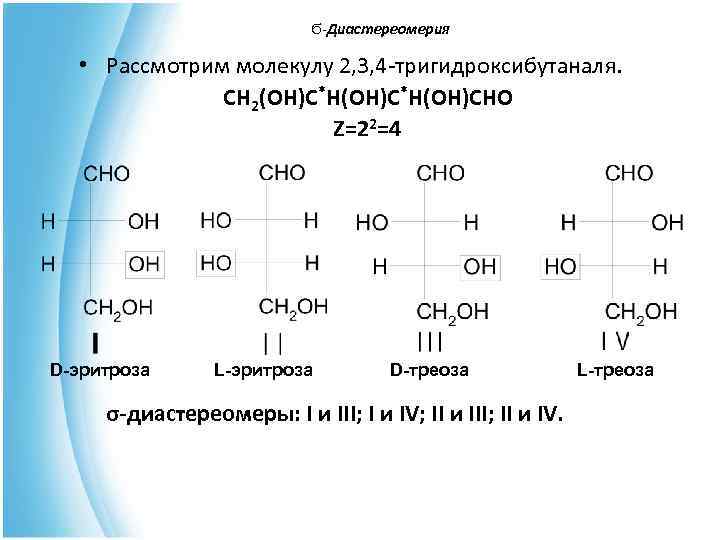 Ϭ-Диастереомерия Ϭ- • Рассмотрим молекулу 2, 3, 4 -тригидроксибутаналя. CH 2(OH)C*H(OH)CHO Z=22=4 D-эритроза L-эритроза D-треоза L-треоза σ-диастереомеры: I и III; I и IV; II и III; II и IV.
Ϭ-Диастереомерия Ϭ- • Рассмотрим молекулу 2, 3, 4 -тригидроксибутаналя. CH 2(OH)C*H(OH)CHO Z=22=4 D-эритроза L-эритроза D-треоза L-треоза σ-диастереомеры: I и III; I и IV; II и III; II и IV.
 Ϭ-Диастереомерия Ϭ- • Понятия энантиомерии и -диастереомерии взаимоисключающие. Если пара стереоизомеров не являются энантиомерами (зеркальные отображения), они будут -диастереомерами.
Ϭ-Диастереомерия Ϭ- • Понятия энантиомерии и -диастереомерии взаимоисключающие. Если пара стереоизомеров не являются энантиомерами (зеркальные отображения), они будут -диастереомерами.
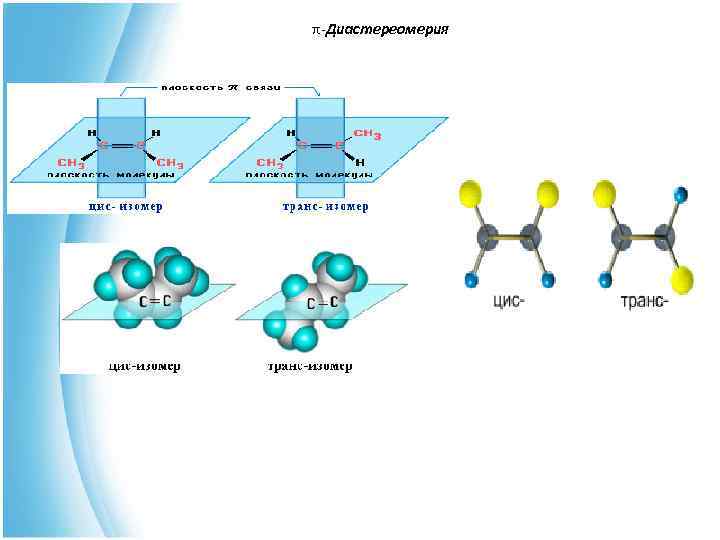
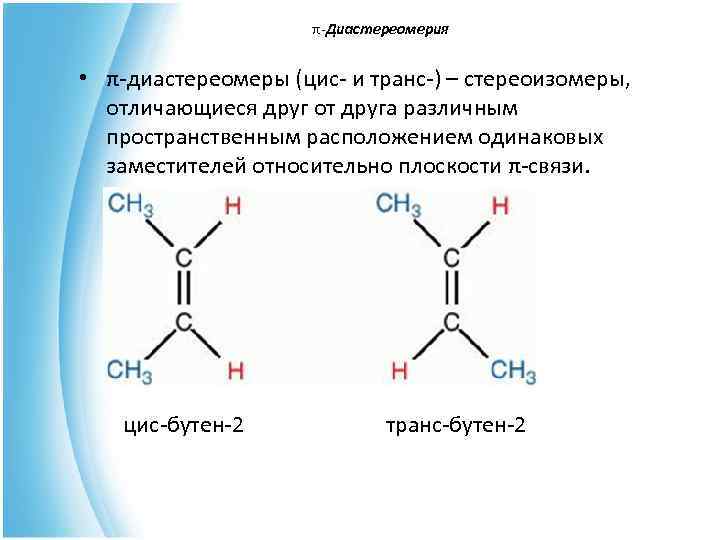 π-Диастереомерия π- • π-диастереомеры (цис- и транс-) – стереоизомеры, отличающиеся друг от друга различным пространственным расположением одинаковых заместителей относительно плоскости π-связи. цис-бутен-2 транс-бутен-2
π-Диастереомерия π- • π-диастереомеры (цис- и транс-) – стереоизомеры, отличающиеся друг от друга различным пространственным расположением одинаковых заместителей относительно плоскости π-связи. цис-бутен-2 транс-бутен-2
 π-Диастереомерия π-
π-Диастереомерия π-
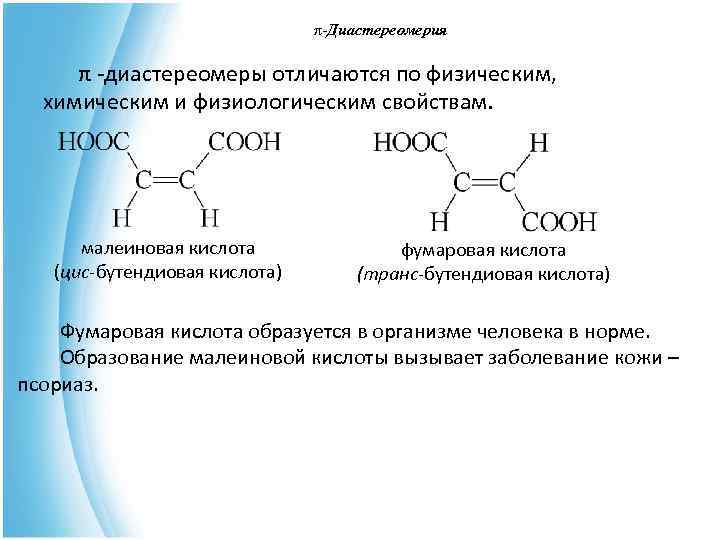 π-Диастереомерия π- π -диастереомеры отличаются по физическим, химическим и физиологическим свойствам. малеиновая кислота фумаровая кислота (цис-бутендиовая кислота) (транс-бутендиовая кислота) Фумаровая кислота образуется в организме человека в норме. Образование малеиновой кислоты вызывает заболевание кожи – псориаз.
π-Диастереомерия π- π -диастереомеры отличаются по физическим, химическим и физиологическим свойствам. малеиновая кислота фумаровая кислота (цис-бутендиовая кислота) (транс-бутендиовая кислота) Фумаровая кислота образуется в организме человека в норме. Образование малеиновой кислоты вызывает заболевание кожи – псориаз.
 π-Диастереомерия π- • В настоящее время для обозначения π- диастереомеров используется E, Z - система, основанная на старшинстве заместителей, определяемом атомным номером. π-диастереомер, у которого старшие заместители находятся по одну сторону плоскости π-связи, обозначаются Z (от нем. Zusammen-вместе), по разные стороны – E (от нем. Entgegen-напротив). 3 -бромо-2 -метил-3 -хлоропропен-2 -амин-1
π-Диастереомерия π- • В настоящее время для обозначения π- диастереомеров используется E, Z - система, основанная на старшинстве заместителей, определяемом атомным номером. π-диастереомер, у которого старшие заместители находятся по одну сторону плоскости π-связи, обозначаются Z (от нем. Zusammen-вместе), по разные стороны – E (от нем. Entgegen-напротив). 3 -бромо-2 -метил-3 -хлоропропен-2 -амин-1
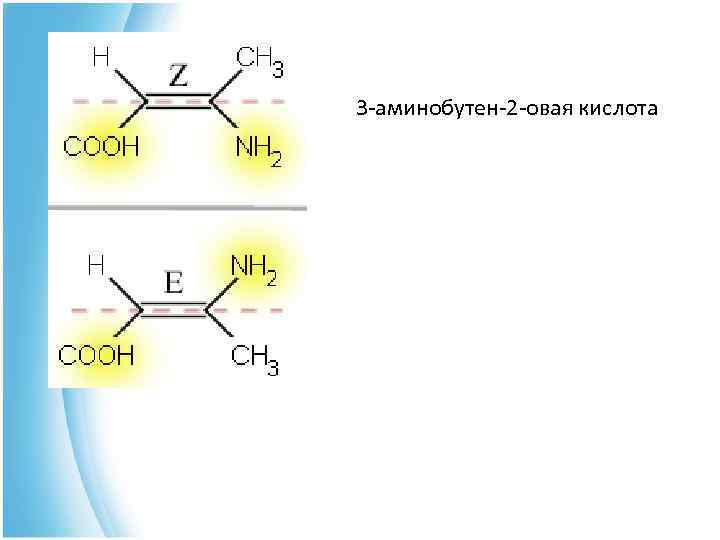 3 -аминобутен-2 -овая кислота
3 -аминобутен-2 -овая кислота


